Инфекционный полиневрит у детей
Обновлено: 12.05.2024
Хроническая воспалительная демиелинизирующая полинейропатия (ХВДП) – приобретенное заболевание периферических нервов аутоиммунной природы, характеризующееся рецидивирующим или прогрессирующим течением с преимущественно демиелинизирующим типом поражения.
Классификация
• Хроническая воспалительная демиелинизирующая полинейропатия, атипичная форма. Преимущественная проксимальная форма
• Хроническая воспалительная демиелинизирующая полинейропатия, атипичная форма. Асимметричная форма (синдром Льюиса-Самнера)
Типичная форма ХВДП (симметричная проксимальная и дистальная мышечная слабость, чувствительные нарушения в руках и ногах, развивающиеся в течение не менее 2-х месяцев).
Этиология и патогенез
Этиология ХВДП в настоящее время неизвестна. Начало ХВДП часто связывают с интеркуррентными инфекциями или с иммунизацией (профилактической вакцинацией), так у 33-57% детей развитие болезни отмечалось в течение 1 месяца после перенесенной инфекции или вакцинации.
Ранее считалось, что среди пациентов с ХВДП чаще встречаются определенные группы HLA (A1, B8, DRW3), предрасполагающие к заболеванию, но впоследствии это не было подтверждено. Тем не менее, предполагается, что наиболее вероятной является иммуноопосредованная природа болезни.
При ХВДП аутоиммунные воспалительные процессы опосредованы нарушениями как клеточного, так и гуморального звена иммунной системы. Проявления демиелинизации могут наблюдаться на любом отрезке периферического нерва от спинномозговых корешков до его дистальных участков. Помимо демиелинизации в биоптатах икроножного нерва были выявлены воспалительные инфильтраты и отек подоболочечного пространства нерва.
Эпидемиология
Распространенность ХВДП составляет у взрослых – 1,0-1,9 на 100 000 и у детей – 0,48 на 100 000. При этом у 20% больных, у которых диагноз ХВДП ставился во взрослом возрасте, первые симптомы болезни отмечались в возрасте до 20 лет. Анализ 27 случаев ХВДП у детей выявил, что дебют заболевания может наблюдаться в любом возрасте (от 1 до 18 лет), а максимум заболеваемости отмечался в 7-8 лет [8,10].
Диагностика
• постепенное развитие симптомов, но нарастание двигательных нарушений может быть быстрым у 16% пациентов [1,2,3,8,10]).
• При проведении клинического осмотра рекомендуется обращать особое внимание на наличие хронической прогрессирующей, ступенеобразной или рецидивирующей симметричной проксимальной и дистальной слабость мышц рук и ног, в сочетании с чувствительными нарушениями. Развитие слабости должно развиваться в течение не менее 2 мес. У части пациентов возможно поражение черепных нервов.
Обязательным условием является отсутствие или значимое снижение рефлексов во всех конечностях [1,2,8,10,12,17].
• При атипичных формах ХВДП двигательные нарушения всегда присутствуют, но могут локализоваться только в дистальных или только в проксимальных группах мышц, а также возможно преимущественная слабость на одной стороне. При этом сухожильные рефлексы могут быть нормальными в непораженных конечностях.
- другие причины демиелинизирующей невропатии, включая POEMS синдром, остеосклеротическую миелому, диабетическую и недиабетическую пояснично-
• Рекомендовано проведение люмбальной пункции с исследованием цереброспинальной жидкости [3,8,10,12].
Комментарии: Характерным является увеличение белка в цереброспинальной жидкости при числе лейкоцитов менее 10/мм 3 .
а) увеличение латентности М-ответа при стимуляции в дистальной точке на 50% и более от верхнего предела нормативных значений в двух нервах (но необходимо исключить нейропатию срединного нерва на запястье вследствие синдрома карпального канала);
б) снижение скорости распространения возбуждения по двигательным волокнам на 30% и более от нижнего предела нормативных значений в двух нервах;
в) увеличение латентности F-волны на 20% и более от верхнего предела нормативных значений в двух нервах (или на 50% и более от верхнего предела нормативных значений, если амплитуда негативного пика дистального М-ответа составляет менее 80% от нижнего предела нормативных значений);
д) локальный блок проведения двигательного нерва: снижение амплитуды негативного пика проксимального М-ответа относительно дистального на 50% и более, если негативный пик дистального М-ответа составляет 20% и более от нижнего предела нормативных значений в двух нервах или в одном нерве + один другой параметр демиелинизации (в любом нерве, удовлетворяющий любому из критериев а-ж) в одном или более других нервах;
ж) увеличение длительности дистального М-ответа (интервал между началом первого негативного пика и возвращением к изолинии последнего негативного пика) в одном и более нервах (срединном ≥ 6,6 мс; локтевом ≥ 6,7 мс; малоберцовом ≥ 7,6 мс; большеберцовом ≥ 8,8 мс) + один другой параметр демиелинизации (в любом нерве, удовлетворяющий любому из критериев а-ж) в одном или более других нервах.
(2) Вероятный диагноз соответствует следующим характеристикам: уменьшение амплитуды негативного пика проксимального М-ответа относительно дистального на 30% и более, за исключением большеберцового нерва, если негативный пик дистального М-ответа составляет 20% и более от нижнего предела нормативных значений, в двух нервах или в одном нерве + один другой параметр демиелинизации (в любом нерве, удовлетворяющий любому из критериев а-ж) в одном или более других нервах (3) Возможный диагноз соответствует любой из характеристик (а-ж) достоверного диагноза, но обнаруженной только в одном нерве
• Рекомендовано проведение магнитно-резонансной томографии (МРТ) шейного и поясничного отделов позвоночника и спинного мозга
Комментарии: показывает накопление гадолиния и/или гипертрофию конского хвоста, пояснично-крестцовых или шейных корешков спинного мозга, или плечевого или пояснично-крестцового сплетений [3,7,14,17].
Комментарии: выявляются признаки демиелинизации и/или ремиелинизации при электронной микроскопии или при использовании анализа расчесанных нервных волокон (teased fiber analysis) [7,8,10].
Если у вас совпадает больше 80% перечисленных симптомов, то настоятельно рекомендуем вам обратиться к врачу за консультацией.
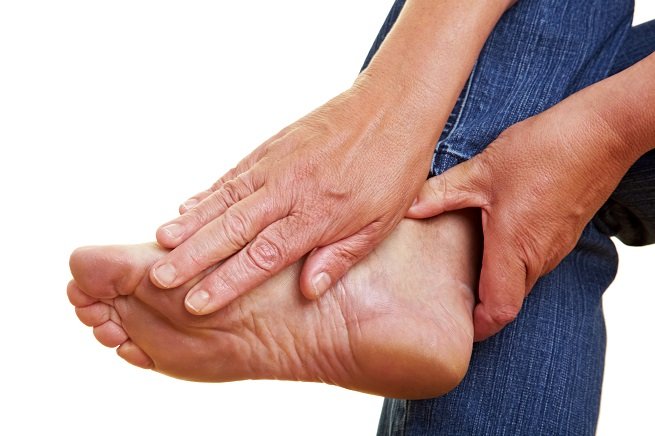
Полиневрит – это тяжелое и опасное заболевание, связанное с поражением периферической нервной системы. Патология носит множественный и обширный характер. Полиневрит сопровождается множественными парезами, мышечной слабостью, снижением функционала и чувствительности конечностей. При остром характере течения болезни полиневриты могут осложняться. Воспалительные процессы, распространившиеся на центральную нервную систему, существенно ухудшают самочувствие пациента.
Причины возникновения болезни
Диагностика полиневрита начинается с определения и выявления причин, вызвавших заболевание. Чаще всего инфекционный полиневрит вызван внешним механическим или токсическим воздействием. Особое внимание при сборе анамнеза и определения клинической картины стоит уделить взаимодействию с ядами – полиневрит часто вызывается при отравлении организма ртутью или свинцом. Однако это не главная причина развития патологии – сильнодействующие антибиотики, злоупотребление наркотическими или алкогольными веществами тоже может нанести ущерб периферической нервной системе и вызвать неконтролируемое распространение болезни.
Также вызывают распространение полиневрита тяжелые бактериальные или онкологические заболевания, при которых периферическая нервная система теряет способность к нормальному функционированию. Принимая собственные нервные волокна за опасные инородные тела, организм может начать атаковать сам себя – так проявляется аутоимунный характер полиневрита.
Классификация полиневритов
Перед началом лечения необходимо выявить не только форму (хроническую или острую) заболевания, но и его тип. В зависимости от причин, повлекших за собой распространение полиневрита, назначается разное лечение. Полиневрит делят на две обширные категории – аксонопатический (погибает аксон нерва) и демиелинизационный (разрушается оболочка нерва). Дальнейшая классификация говорит об источнике заболевания:
Инфекционный полиневрит. Возникает при воспалительных процессах в периферической нервной системе. Один из самых опасных видов патологии, поскольку характеризуется обширной зоной поражения и гибелью множества нервных волокон.
Дифтерийный полиневрит. Возникает у 10-20% детей, перенесших дифтерию, при несвоевременном диагностировании и лечении болезни.
Алкогольный полиневрит. Воспалительный процесс форсируется за счет неумеренного потребления алкогольных токсичных веществ. Ускоряет развитие алкогольного полиневрита постоянное поступление токсинов и отравляющих веществ.
Мышьяковый полиневрит. Следствие отравления организма мышьяком. Не имеет хронической формы, так как болезнь сразу же переходит в острую форму.
Диабетический полиневрит. Повреждаются периферические нервы лица или конечностей.
Классификация не ограничивается причиной происхождения заболевания. Как мы упоминали ранее, выделяют острую и хроническую форму полиневрита. Острая форма – одно из наиболее опасных проявлений полиневрита, она развивается в считанные часы или дни. Чаще всего острая форма заболевания возникает на фоне ослабления иммунитета и перенесенного инфекционного заболевания. Хроническая же форма заболевания прогрессирует медленно и может быть с легкостью упущена как пациентом, так и лечащим врачом. Заболевание растет с каждым днем на фоне постоянного воздействия провоцирующего фактора – алкоголя, отравления ядами, инфекции.
Симптомы полиневрита
Полиневрит – чрезвычайно опасное заболевание, грозящее не только возможными проблемами со здоровьем, но и инвалидизацией пациента. Для того, чтобы своевременно диагностировать заболевание, определить его классификацию и причины, нужно знать симптомы полиневрита:
Мышечная слабость, постоянное чувство усталости и разбитости.
Пониженная чувствительность нервных окончаний конечностей. В частности, пациент ощущает утрату природной чувствительности подушечек пальцев.
Истончение кожного покрова на руках и ногах. Изменение цвета кожи с природного до мраморно-белого или синюшного.
Повреждение периферических нервов в области лица. Пониженная чувствительность органов восприятия – глаз, ушей, носа.
Симптомы полиневрита становятся тем заметнее, чем больше прогрессирует заболевание. На более поздних этапах периферическая нервная система поражена настолько, что человеку становится трудно управляться с конечностями – ослабленные мышцы практически не подчиняются воле пациента. Затрудняется ходьба, стопа начинает отвисать. При ходьбе пациент с запущенным полиневритом выглядит неуверенно и неловко, высоко поднимает ноги и с трудом их переставляет. Нарушается координация и равновесие – возможны частые падения.
Диагностика полиневрита
Определить наличие или отсутствие столь тяжелого заболевания на ранних этапах развития полиневрита может специализированный врач. Опытный невролог без труда определит не только наличие или отсутствие болезни, но и ее характер и классификацию. Для этого проводится ряд клинических анализов и медицинских исследований:
Сбор анамнеза и опрос пациента. Зачастую на этом этапе невролог уже имеет четкое представление о болезни пациента – характерные жалобы и видимые признаки позволяют определить наличие или отсутствие болезни.
Для подтверждения результатов первичного опроса и осмотра проводятся биохимические анализы крови и мочи. Лаборант проверит жидкости на наличие токсических веществ.
Завершающий этап сбора информации – диагностика эндокринной и поджелудочной желез, печени и почек.
Для того, чтобы определить степень поражения периферической нервной системы и определить стадию полиневрита, используется электромиография – инструмент для определения электрической проводимости мышц.
Также в диагностике принимает участие и специалист-онколог. С его помощью невролог может дифференцировать полиневрит и не перепутать его с онкологическими заболеваниями.
Лечение полиневрита
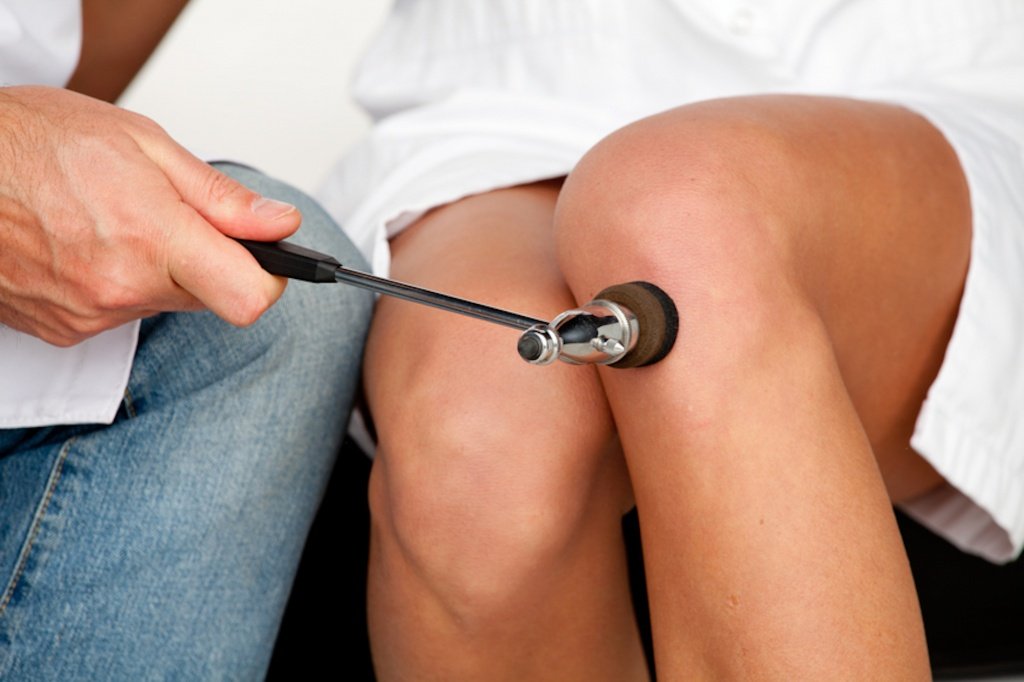
Полиневрит – опасное заболевание, но на данном этапе развития медицины при грамотном подходе он поддается лечению. Общее время восстановления организма и реабилитации нервов составляет около 3-х месяцев, а негативное воздействие болезни на организм пациента прекращается на 10 день после начала лечения.
Общие рекомендации носят следующий характер:
Пациенту необходимо соблюдать постельный режим и двигаться как можно меньше вне зависимости от характера полиневрита и тяжести заболевания. Это обусловлено необходимостью обездвижить поврежденные сегменты тела.
Токсины, провоцирующие развитие патологии, устраняются при помощи антидотов. Пациент избавляется от негативных факторов, влияющих на развитие болезни, после чего полиневрит прекращает свое развитие.
При инфекционном полиневрите лечение происходит за счет медицинских препаратов. Дифтерийный тип болезни лечится сывороткой против дифтерии.
Независимо от классификации полиневрита начальная стадия включает в себя медицинскую терапию – средства для обезболивания, ускорения метаболизма, витаминотерапию и многое другое.
После окончания постельного режима и перехода на домашнее восстановление полиневрит лечится при помощи соблюдения особого режима реабилитации. Он включает в себя регулярные занятия физкультурой, стимулирующие поврежденные нервные волокна конечностей, специальную диету, регулярный массаж.
Несмотря на то, что полиневриты и полинейропатии являются достаточно опасными заболеваниями, их можно вылечить при своевременном обращении к врачу. При возникновении первых симптомов развития болезни следует немедленно посетить невролога, чтобы избежать возможных осложнений, а также исключить провокационные факторы – алкоголь, курение, наркотические вещества, токсины вроде мышьяка, свинца или ртути. Промедление грозит не только возможной инвалидностью, но и летальным исходом – опасность полиневрита для нормальной жизнедеятельности и жизни человека нельзя недооценивать.
Процедуры
Приемы и консультации
- Прием врача-невролога лечебно-диагностический, первичный 2 360 руб.
- Прием врача-невролога лечебно-диагностический, повторный 2 230 руб.
- Прием врача-невролога к.м.н., первичный 2 970 руб.
- Прием врача-невролога к.м.н., повторный 2 620 руб.
- Прием врача-невролога д.м.н., первичный 3 570 руб.
- Прием врача-невролога д.м.н., повторный 3 210 руб.
- Прием врача-гирудотерапевта 2 360 руб.
Манипуляции
- Гирудотерапия до 5 пиявок 3 080 руб.
- Гирудотерапия за 1 дополнительную пиявку 320 руб.
- Кинезиотейпирование – 1 зона 1 310 руб.
Пиелонефрит у детей – неспецифическое микробно-воспалительное поражение почечной паренхимы и чашечно-лоханочной системы. Пиелонефрит у детей протекает с болевым синдромом в поясничной области, дизурическими расстройствами (частыми позывами к мочеиспусканию, болезненностью, неудержанием мочи), повышением температуры тела, интоксикацией. Диагностика пиелонефрита у детей включает исследование крови (клинический, биохимический анализ) и мочи (общий анализ, бакпосев), УЗИ мочевой системы, оценку уродинамики, внутривенную урографию и др. В лечении пиелонефрита у детей используется антибактериальная, противовоспалительная, антиоксидантная терапия, фитотерапия.

Общие сведения
Пиелонефрит у детей – воспалительный процесс, захватывающий чашечно-лоханочную систему, канальца и интерстицию почек. По распространенности пиелонефрит стоит на втором месте после ОРВИ у детей, и между этими заболеваниями существует тесная взаимосвязь. Так, в детской урологии каждый 4-ый случай пиелонефрита у ребенка раннего возраста является осложнением острой респираторной инфекции. Наибольшее число случаев пиелонефрита у детей регистрируется в дошкольном возрасте. Острый пиелонефрит в 3 раза чаще диагностируется у девочек, что обусловлено особенностью женской анатомии нижних отделов мочевых путей (более широким и коротким мочеиспускательным каналом).

Причины пиелонефрита у детей
Самым распространенным этиологическим агентом, вызывающим пиелонефрит у детей, является кишечная палочка; также при бактериологическом посеве мочи обнаруживаются протей, синегнойная палочка, золотистый стафилококк, энтерококки, внутриклеточные микроорганизмы (микоплазмы, хламидии) и др.
Попадание инфекционных агентов в почки может происходить гематогенным, лимфогенным, уриногенным (восходящим) путем. Гематогенный занос возбудителей наиболее часто встречается у детей первого года жизни (при гнойном омфалите у новорожденных, пневмонии, ангинах, гнойничковых заболеваниях кожи и т. д.). У более старших детей преобладает восходящее инфицирование (при дисбактериозе, колитах, кишечных инфекциях, вульвитах, вульвовагинитах, баланопоститах, циститах и пр.). Большую роль в развитии пиелонефрита у детей играет неправильный или недостаточный гигиенический уход за ребенком.
Условиями, предрасполагающими к возникновению пиелонефрита у детей, могут выступать структурные или функциональные аномалии, нарушающие пассаж мочи: врожденные пороки развития почек, пузырно-мочеточниковый рефлюкс, нейрогенный мочевой пузырь, мочекаменная болезнь. Риску развития пиелонефрита более подвержены дети с гипотрофией, рахитом, гипервитаминозом D; ферментопатиями, дисметаболической нефропатией, глистными инвазиями и пр. Манифестация или обострение пиелонефрита у детей, как правило, случается после интеркуррентных инфекций (ОРВИ, ветряной оспы, кори, скарлатины, эпидемического паротита и др.), вызывающих снижение общей сопротивляемости организма.
Классификация
В педиатрии выделяют 2 основные формы пиелонефрита у детей – первичный (микробно-воспалительный процесс изначально развивается в почках) и вторичный (обусловлен другими факторами). Вторичный пиелонефрит у детей, в свою очередь, может быть обструктивным и необструктивным (дисметаболическим).
В зависимости от давности и особенностей проявлений патологического процесса выделяют острый и хронический пиелонефрит у детей. Признаком хронического пиелонефрита у детей служит сохранение симптомов инфекции мочевыводящих путей более 6 месяцев либо возникновением за этот период не менее 2-х обострений. Характер течения хронический пиелонефрита у детей бывает рецидивирующим (с периодами обострений и ремиссий) и латентным (только с мочевым синдромом).
В течении острого пиелонефрита у детей выделяют активный период, период обратного развития симптомов и полную клинико-лабораторную ремиссию; в течении хронического пиелонефрита – активный период, частичную и полную клинико-лабораторную ремиссию. Пиелонефритический процесс имеет две стадии – инфильтративную и склеротическую.
Симптомы пиелонефрита у детей
Ведущими проявлениями острого и активного периода хронического пиелонефрита у детей служат болевой, дизурический и интоксикационный синдромы.
Пиелонефрит у детей обычно манифестирует с лихорадки ремиттирующего типа, ознобов, потливости, слабости, головной боли, анорексии, адинамии. У грудных детей возможны упорные срыгивания, рвота, жидкий стул, снижение массы тела.
Дизурический синдром развивается при вовлечении в микробно-воспалительный процесс нижних отделов мочевого тракта. Он характеризуется беспокойством ребенка перед или во время мочеиспускания, частыми позывами к опорожнению мочевого пузыря, болезненностью, чувством жжения при мочеиспускании, неудержанием мочи.
Болевой синдром при пиелонефрите у детей может проявляться либо абдоминальными болями без четкой локализации, либо болями в поясничной области, усиливающимися при поколачивании (положительный с-м Пастернацкого), физической нагрузке.
Вне обострения симптомы хронического пиелонефрита у детей скудные; отмечается утомляемость, бледность кожных покровов, астенизация. При латентной форме хронического пиелонефрита клинические проявления вовсе отсутствуют, однако заподозрить заболевание у детей позволяют характерные изменения в общем анализе мочи (лейкоцитурия, бактериурия, умеренная протеинурия).
Течение острого пиелонефрита у детей может осложниться апостематозным интерстициальным нефритом, паранефритом, карбункулом почки, пионефрозом, сепсисом. Хронический пиелонефрит, развившийся в детском возрасте, с годами может привести к нефросклерозу, гидронефрозу, артериальной гипертензии и хронической почечной недостаточности.
Диагностика
Если пиелонефрит у ребенка впервые выявлен педиатром, необходима обязательная консультация детского нефролога или детского уролога. Комплекс лабораторной диагностики при пиелонефрите у детей включает исследование клинического анализа крови, биохимического анализа крови (мочевины, общего белка, белковых фракций, фибриногена, СРБ), общего анализа мочи, рН мочи, количественных проб (по Нечипоренко, Аддис–Каковскому, Амбурже, Зимницкому), посева мочи на флору с антибиотикограммой, биохимического анализа мочи. При необходимости для выявления возбудителей инфекции проводятся исследования методами ПЦР, ИФА. Важное значение при пиелонефрите у детей имеет оценка ритма и объема спонтанных мочеиспусканий, контроль диуреза.
Обязательное инструментальное обследование детей, больных пиелонефритом, предусматривает проведение УЗИ почек (при необходимости УЗИ мочевого пузыря), УЗДГ почечного кровотока. Для исключения обструктивных уропатий, часто выступающих причиной пиелонефрита у детей, может потребоваться выполнение экскреторной урографии, уродинамических исследований, динамической сцинтиграфии почек, почечной ангиографии, КТ почек и других дополнительных исследований.
Дифференциальную диагностику пиелонефрита у детей необходимо проводить с гломерулонефритом, аппендицитом, циститом, аднекситом, в связи с чем дети могут нуждаться в консультации детского хирурга, детского гинеколога; проведении ректального обследования, УЗИ органов малого таза.
Лечение пиелонефрита у детей
Комплексная терапия пиелонефрита предусматривает проведение медикаментозной терапии, организацию правильного питьевого режима и питания детей.
В остром периоде назначается постельный режим, растительно-белковая диета, увеличение водной нагрузки на 50% по сравнению с возрастной нормой. Основу лечение пиелонефрита у детей составляет антибиотикотерапия, для которой используются цефалоспорины (цефуроксим, цефотаксим, цефпиром др.), β-лактамы (амоксициллин), аминогликозиды (гентамицин, амикацин). После завершения антибактериального курса назначаются уроантисептики: производные нитрофурана (нитрофурантоин) и хинолина (налидиксовая кислота).
Для усиления почечного кровотока, элиминации продуктов воспаления и микроорганизмов показан прием быстродействующих диуретиков (фуросемида, спиронолактон). При пиелонефрите детям рекомендуется прием НПВС, антигистаминные препараты, антиоксиданты, иммунокорректоры.
Длительность курса лечения острого пиелонефрита у детей (или обострения хронического процесса) - 1-3 месяца. Критерием ликвидации воспаления является нормализация клинико-лабораторных показателей. Вне обострения пиелонефрита у детей необходима фитотерапия антисептическими и мочегонными сборами, прием щелочной минеральной воды, массаж, ЛФК, санаторное лечение.
Прогноз и профилактика
Острый пиелонефрит у детей заканчивается полным выздоровлением в 80% случаев. Осложнения и летальные исходы возможны в редких случаях, главным образом, у ослабленных детей с сопутствующей патологией. Исходом хронического пиелонефрита у 67-75% детей служит прогрессирование патологического процесса в почках, нарастание нефросклеротических изменений, развитие ХПН. Дети, перенесшие острый пиелонефрит, наблюдаются нефрологом в течение 3-х лет с ежемесячным контролем общего анализа мочи. Осмотры детского отоларинголога и стоматолога обязательны 1 раз в 6 месяцев.
Предупреждение пиелонефрита у детей связано с соблюдением мер гигиены, профилактикой дисбактериоза и ОКИ, ликвидацией хронических воспалительных очагов и укреплением сопротивляемости организма. Сроки проведения профилактической вакцинации устанавливаются в индивидуальном порядке. После любой перенесенной инфекции у детей необходимо исследовать анализ мочи. Для профилактики развития хронического пиелонефрита у детей следует адекватно лечить острые мочевые инфекции.
Пиелонефрит – это неспецифическое инфекционное заболевание почек, вызываемое различными бактериями. Острая форма заболевания проявляется повышением температуры, симптомами интоксикации и болями в поясничной области. Хронический пиелонефрит может протекать бессимптомно или сопровождаться слабостью, нарушением аппетита, учащением мочеиспускания и неинтенсивными болями в пояснице. Диагноз выставляется на основании результатов лабораторных анализов (общий и биохимический анализы мочи, бакпосев), урографии и УЗИ почек. Лечение - антибактериальная терапия, иммуностимуляторы.
МКБ-10

Общие сведения
Пиелонефрит – широко распространенная патология. Пациенты, страдающие острым и хроническим пиелонефритом, составляют около 2/3 всех урологических больных. Болезнь может протекать в острой или хронической форме, поражать одну или обе почки. Диагностику и лечение осуществляет специалист в сфере клинической урологии и нефрологии. В случае отсутствия своевременной терапии пиелонефрит может привести к таким тяжелым осложнениям как почечная недостаточность, карбункулу или абсцессу почки, сепсису и бактериальному шоку.

Причины пиелонефрита
Заболевание может возникнуть в любом возрасте. Чаще пиелонефрит развивается:
Любые органические или функциональные причины, препятствующие нормальному оттоку мочи, увеличивают вероятность развития патологии. Нередко пиелонефрит появляется у больных мочекаменной болезнью. К неблагоприятным факторам, способствующим возникновению пиелонефрита, относится сахарный диабет, иммунные нарушения, хронические воспалительные болезни и частые переохлаждения. В ряде случаев (обычно у женщин) пиелонефрит развивается после перенесенного острого цистита.
Бессимптомное течение нередко является причиной несвоевременной диагностики хронического пиелонефрита. Больные начинают получать лечение, когда функция почек уже нарушена. Поскольку патология очень часто возникает у пациентов, страдающих мочекаменной болезнью, таким больным необходимо специальная терапия даже при отсутствии симптоматики пиелонефрита.
Симптомы пиелонефрита
Острый пиелонефрит
Для острого процесса характерно внезапное начало с резким повышением температуры до 39-40°С. Гипертермия сопровождается обильным потоотделением, потерей аппетита, выраженной слабостью, головной болью, иногда – тошнотой и рвотой. Тупые боли в поясничной области различной интенсивности, чаще односторонние, появляются одновременно с повышением температуры. Физикальное обследование выявляет болезненность при поколачивании в области поясницы (положительный симптом Пастернацкого).
Неосложненная форма острого пиелонефрита не вызывает нарушений мочеиспускания. Моча становится мутной или приобретает красноватый оттенок. При лабораторном исследовании мочи выявляется бактериурия, незначительная протеинурия и микрогематурия. Для общего анализа крови характерен лейкоцитоз и повышение СОЭ. Примерно в 30% случаев в биохимическом анализе крови отмечается повышение азотистых шлаков.
Хронический пиелонефрит
Хронический пиелонефрит нередко становится исходом недолеченной острой формы. Возможно развитие первичного хронического процесса. Иногда патология обнаруживается случайно при исследовании мочи. Больные предъявляют жалобы на слабость, снижение аппетита, головные боли и учащенное мочеиспускание. Некоторых пациентов беспокоят тупые ноющие боли в поясничной области, усиливающиеся в холодную сырую погоду. Симптомы, свидетельствующие об обострении, совпадают с клинической картиной острого процесса.
Осложнения
Двухсторонний острый пиелонефрит может стать причиной острой почечной недостаточности. К числу наиболее грозных осложнений следует отнести сепсис и бактериальный шок. В некоторых случаях острая форма заболевания осложняется паранефритом. Возможно развитие апостеноматозного пиелонефрита (формирование множественных мелких гнойничков на поверхности почки и в ее корковом веществе), карбункула почки (нередко возникает вследствие слияния гнойничков, характеризуется наличием гнойно-воспалительного, некротического и ишемического процессов) абсцесса почки (расплавление почечной паренхимы) и некроза почечных сосочков.
Если лечение не проводится, наступает терминальная стадия гнойно-деструктивного острого процесса. Развивается пионефроз, при котором почка полностью подвергается гнойному расплавлению и представляет собой очаг, состоящий из полостей, заполненных мочой, гноем и продуктами тканевого распада. При прогрессировании хронического двухстороннего пиелонефрита функция почек постепенно нарушается, что приводит к снижению удельного веса мочи, артериальной гипертензии и развитию хронической почечной недостаточности.
Диагностика
Постановка диагноза обычно не представляет затруднений для врача-уролога из-за наличия ярко выраженных клинических симптомов. В анамнезе часто отмечается наличие хронических заболеваний или недавно перенесенные острые гнойные процессы. Клиническую картину формирует характерное сочетание выраженной гипертермии с болью в пояснице (чаще односторонней), болезненными мочеиспусканиями и изменениями мочи. Моча мутная или с красноватым оттенком, имеет выраженный зловонный запах. В рамках диагностических мероприятий выполняются:
- Лабораторные исследования. Лабораторным подтверждением диагноза служит обнаружение в моче бактерий и небольших количеств белка. Для определения возбудителя проводят бакпосев мочи. О наличии острого воспаления свидетельствует лейкоцитоз и увеличение СОЭ в общем анализе крови. При помощи специальных тест-наборов проводится идентификация вызвавшей воспаление микрофлоры. Концентрационную способность почек оценивают при помощи пробы Зимницкого.
- Лучевая диагностика. В ходе обзорной урографии выявляется увеличение объема одной почки. Экскреторная урография свидетельствует о резком ограничении подвижности почки при проведении ортопробы. При апостематозном пиелонефрите отмечается снижение выделительной функции на стороне поражения (тень мочевыводящих путей появляется с запозданием или отсутствует). При карбункуле или абсцессе на экскреторной урограмме определяется выбухание контура почки, сдавление и деформация чашечек и лоханки. Диагностику структурных изменений почечной ткани при пиелонефрите проводят при помощи УЗИ почек. Для исключения мочекаменной болезни и анатомических аномалий выполняют КТ почек.

Лечение пиелонефрита
Лечение острого пиелонефрита
Неосложненный острый процесс лечится консервативно в условиях стационара. Проводится антибактериальная терапия. Медикаменты подбираются с учетом чувствительности обнаруженных в моче бактерий. Для того, чтобы максимально быстро ликвидировать воспалительные явления, не допустив перехода пиелонефрита в гнойно-деструктивную форму, лечение начинают с самого эффективного препарата.
Проводится дезинтоксикационная терапия, коррекция иммунитета. При лихорадке назначается диета с пониженным содержанием белков, после нормализации температуры пациента переводят на полноценное питание с повышенным содержанием жидкости. На первом этапе терапии вторичного острого пиелонефрита следует устранить препятствия, затрудняющие нормальный отток мочи: как правило, для этого производится установка мочеточникового катетера-стента. Назначение антибактериальных препаратов при нарушенном пассаже мочи не дает желаемого эффекта и может привести к развитию серьезных осложнений.
Лечение хронического пиелонефрита
Осуществляется по тем же принципам, что и терапия острого процесса, но отличается большей длительностью и трудоемкостью. Терапевтическая программа предусматривает устранение причин, которые привели к затруднению оттока мочи или вызвали нарушения почечного кровообращения, антибактериальную терапию и нормализацию общего иммунитета.
При наличии препятствий необходимо восстановить нормальный пассаж мочи. Восстановление оттока мочи производится оперативно (нефропексия при нефроптозе, удаление камней из почек и мочевыводящих путей, удаление аденомы предстательной железы и т. д.). Устранение препятствий, мешающих пассажу мочи, во многих случаях позволяет достичь стойкой длительной ремиссии. Антибактериальные препараты назначаются с учетом данных антибиотикограммы. До определения чувствительности микроорганизмов проводится терапия антибактериальными препаратами широкого спектра действия.
Пациентам с хроническим пиелонефритом требуется длительная систематическая терапия сроком не менее года. Лечение начинают с непрерывного курса антибактериальной терапии продолжительностью 6-8 недель. Такая методика позволяет устранить гнойный процесс в почке без развития осложнений и образования рубцовой ткани. Если функция почек нарушена, требуется постоянный контроль фармакокинетики нефротоксичных антибактериальных препаратов. Для коррекции иммунитета при необходимости применяют иммуностимуляторы и иммуномодуляторы. После достижения ремиссии назначают прерывистые курсы антибактериальной терапии.
В период ремиссии больным показано санаторно-курортное лечение (Джермук, Железноводск, Трускавец и др.). Следует помнить об обязательной преемственности терапии. Начатое в стационаре антибактериальное лечение необходимо продолжать амбулаторно. Назначаемая врачом санатория схема лечения должна включать в себя прием антибактериальных препаратов, рекомендуемых врачом, постоянно наблюдающим пациента. В качестве дополнительного метода лечения применяется фитотерапия.
Инфекционный мононуклеоз – это острое вирусное заболевание (преимущественно вирус Эпштейна-Барр), которое характеризуется лихорадкой, поражением ротоглотки, лимфатических узлов, печени, селезенки и своеобразными изменениями состава крови (лимфомоноцитоз, атипичные мононуклеары).
Код(ы) МКБ-10:
| Коды МКБ-10 | |
| B27 | Инфекционный мононуклеоз |
| B27.0 | Мононуклеоз, вызванный гамма-герпетическим вирусом Мононуклеоз, вызванный вирусом Эпштейна-Барр |
| B27.1 | Цитомегаловирусный мононуклеоз |
| B27.8 | Другой инфекционный мононуклеоз |
| B27.9 | Инфекционный мононуклеоз неуточнённый |
| D82.3 | Иммунодефицит вследствие наследственного дефекта, вызванного вирусом Эпштейна-Барр |
Дата разработки/пересмотра протокола: 2017 год.
Сокращения, используемые в протоколе:
| EA | – | ранний антиген ВЭБ вируса Эпштейна-Барр |
| EBNA | – | ядерный антиген вируса Эпштейна-Барр |
| IgG | – | иммуноглобулины класса G |
| IgM | – | иммуноглобулины класса М |
| VCA | – | капсульный антиген вируса Эпштейна-Барр |
| ВИЧ | – | вирус иммунодефицита человека |
| ВОП | – | врач общей практики |
| ВЭБ | – | вирус Эпштейна-Барр |
| ДНК | – | дезоксирибонуклеиновая кислота |
| ЖКТ | – | желудочно-кишечный тракт |
| ИФА | – | иммуноферментный анализ |
| МКБ | – | международная классификация болезней |
| НПВС | – | нестероидные противовоспалительные средства |
| ОАК | – | общий анализ крови |
| ОАМ | – | общий анализ мочи |
| ПЦР | – | полимеразная цепная реакция |
| СОЭ | – | скорость оседания эритроцитов |
Пользователи протокола: врачи скорой неотложной помощи, фельдшеры, врачи общей практики, педиатры, детские инфекционисты, детские хирурги.
Категория пациентов: дети.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
| GPP | Наилучшая клиническая практика. |
Классификация
| По типу: • типичный; • атипичный (бессимптомный, стертый, висцеральный). | По тяжести: • легкая форма; • среднетяжелая форма; • тяжелая форма. | По течению: • острое (до 3 мес.); • затяжное (3-6 мес.); • хроническое (более 6 мес.); • рецидивирующее (возврат клинических симптомов болезни через 1 месяц и более после перенесенного заболевания). |
Осложнения:
· ранние осложнения (1-3 недели болезни): разрыв селезенки, асфиксия, (вследствие фаринготонзиллярного отека), миокардит, интерстициальная пневмония, энцефалит, паралич черепных нервов, в том числе паралич Белла, менингоэнцефалит, полиневрит, синдром Гийена-Барре;
· поздние осложнения (позже 3 недели болезни): гемолитическая анемия, тромбоцитопеническая пурпура, апластическая анемия, гепатит, синдром мальабсорбции и др., как следствие аутоиммунного процесса.
Типичная форма характеризуется лихорадкой, поражением ротоглотки, лимфатических узлов, печени, селезенки и своеобразными изменениями состава крови (лимфомоноцитоз на фоне лейкоцитоза и атипичные мононуклеары в количестве 10% и более).
Атипичные формы инфекционного мононуклеоза:
· стертая форма: протекает со слабо выраженными и быстро проходящими формами, симптомами или под маской острых респираторных заболеваний, диагностируется преимущественно в эпидемических очагах;
· бессимптомная форма: протекает с отсутствием клинических симптомов, диагностируется на основании обследования гематологическими, серологическими методами и методом эпидемиологического анализа;
· висцеральная форма: отличается тяжелым течением с полиорганным поражением, с вовлечением сердечно-сосудистой, центральной и периферической нервной систем, почек, надпочечников и других жизненно важных органов.
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Диагностические критерии [1-5,9,12,15,16]:
| Признак | Характеристика |
| Лихорадка | Высокая, длительная |
| Синдром поражения рото-и носоглотки | Синдром тонзиллита с налетами или без, аденоидит, фарингит |
| Синдром поражения лимфатических узлов | Преимущественно увеличение передне- и/или заднешейных групп лимфоузлов, внутрибрюшных лимфоузлов, наиболее часто у ворот печени и селезенки, гипертрофия небных и глоточной миндалин |
| Синдром гепатоспленомегалии | Увеличение размеров печени и селезенки |
| Синдром цитолиза печеночных клеток и нарушения пигментного (билирубинового) обмена Печени | Повышение аланинаминотрансминазы, аспартатаминотрансминазы. Нарушение пигментного обмена печени, проявляющееся желтухой и повышением билирубина |
| Синдром экзантемы | Сыпь пятнисто-папулезная, реже геморрагическая с локализацией на лице, туловище, конечностях, чаще проксимальных отделов, яркая, обильная, местами сливная. Возможен кожный зуд, отечность лица. Появляется на 5-10 день болезни. |
Критерии оценки степени тяжести инфекционного мононуклеоза по клиническим признакам [1-5,9,12,15,16]:
| Признак | Характеристика признака | |||
| Легкая степень тяжести | Средняя степень тяжести | Тяжелая степень тяжести | ||
| Выраженность и длительность интоксикации | Отсутствует или легкая выраженность, 1-5 дней | Умеренной выраженности, 6-7 дней | Ярко выражена, более 8 дней | |
| выраженность и продолжительность лихорадки | повышение температуры до 38 ° С, длительность 1-5 дней | повышение температуры от 38,1 до 39 ° С, длительность 6-8 дней | повышение температуры более 39,0 ° С, длительность более 9 дней | |
| Характер воспалительных изменений в рото- и носоглотке | Воспалительные изменения катарального характера или с островчатыми, тонкими налетами, продолжительностью 1-3 дня; затруднение носового дыхания 1-4 дня | Воспалительные изменения с лакунарными налетами, продолжительностью 4-6 дней; затруднение носового дыхания 5-8 дней | ||
| ОАК | лейкопения/умеренный лейкоцитоз (12-25х109/л); лимфомоноцитоз до 70-80%; нейтропения; увеличение СОЭ до 20-30 мм/ч; атипичные мононуклеары (отсутствие или увеличение от 10 до 50%). | |
| Серологический (ИФА с определением показателя индекса авидности) | обнаружение специфических антител IgM VCA к ВЭБ и IgG VCA, IgG EA, IgG-EBNA к ВЭБ с определением показателя индекса авидности | |
Дополнительные лабораторные исследования: | ||
| Молекулярно-генетический метод (ПЦР) | обнаружение в крови ДНК вируса Эпштейна-Барр. | |
| Биохимический анализ крови (при гепатомегалии и желтухе) | определение концентрации билирубина и АЛАТ в крови: умеренная гиперферментемия, гипербилирубинемия. | |
| Бактериологическое исследование слизи с миндалин и задней стенки глотки на аэробные и факультативно-анаэробные микроорганизмы | для идентификации бактериальной этиологии острого тонзиллита. | |
| Признак | Критерии |
| Атипичные мононуклеары | Выявление атипичных мононуклеаров в периферической крови более10% (со 2-3 недели болезни) |
| Лимфомоноцитоз | Выявление лимфомоноцитоза в периферической крови |
| IgM VCA VCA, IgG-EBNA вируса Эпштейна- Барр | В острый период: IgM VCA с момента развития клинических признаков болезни и следующие 4-6 недель присутствуют и снижаются, IgG EA с первой недели болезни нарастают до нескольких лет после нее, персистируют на невысоком уровне, IgG VCA обнаруживаются через несколько недель после появления IgM VCA, нарастают, персистируют пожизненно на высоком уровне, IgG-EBNA-1, 2- отсутствуют или имеются в небольшом количестве. В период реконвалесценции: IgM VCA отсутствуют или имеются в малом количестве, IgG EA персистируют пожизненно на невысоком уровне, IgG VCA персистируют пожизненно IgG EBNA несколько недель после появления клинических признаков и персистируют обнаруживаются через пожизненно на невысоком уровне |
| Определение показателя индекса авидности | Обнаружение IgG с низкой авидностью при наличии или отсутствии IgM свидетельствует о первичной (недавней) инфекции. Присутствие высокоавидных антител IgG указывает на период реконвалесценции |
| ДНК вируса Эпштейна-Барр в крови и слюне | Выявление ДНК вируса методом ПЦР в крови (через 1-2 недели после появления клинических симптомов), слюне. |
Инструментальные исследования: нет.
Показания для консультации специалистов:
· консультация оториноларинголога: при аденоидите, формировании паратонзиллярного абсцесса, воспалительных процессах со стороны придаточных пазух носа;
· консультация гематолога: при прогрессировании гематологических сдвигов;
· консультация хирурга: при выраженном абдоминальном болевом синдроме.

Диагностический алгоритм: (схема)
Читайте также:

