Инфекция на сердце у плода
Обновлено: 19.04.2024
Если в семье уже рождались дети с ВПС, или возраст женщины более 35 лет, следует особенно тщательно планировать беременность. Нужно вести здоровый образ жизни, убедиться в отсутствии инфекций или излечить имеющиеся отклонения.
Конечно, полностью минимизировать риски заболевания не удастся. Здесь совет только один: вовремя проходить все обязательные скрининги и другие обследования, показанные при беременности.
Причины и механизм развития пороков сердца

Сердце формируется одним из первых из всех органов эмбриона. Уже в первом триместре оно начинает свою работу. Порок сердца при беременности у плода является чаще всего результатом наследственных факторов, болезней женщины, расплатой за вредный образ жизни будущей матери. Реже формирование ВПС связано с другими аномалиями развития эмбриона, например, с синдромом Дауна.
Женщины с высоким риском: кто подвержен опасности?
- перенесших выкидыши, мертворождения;
- возрастом старше 35 лет;
- куривших во время беременности;
- живущих в районах с неблагополучной экологией;
- переболевших на ранних сроках беременности краснухой;
- употреблявших во время беременности аспирин, сульфаниламидные препараты, антибиотики;
- имеющих тяжелый семейный анамнез по порокам сердца.
Врожденный порок сердца – дефект, находящийся в структуре сердца. По статистике, десять детей из тысячи будут иметь диагноз ВПС в своих медицинских картах. И число их будет расти, в основном по причине повышения доступности и эффективности диагностических методик. Сейчас диагноз можно поставить не дожидаясь рождения малыша, с помощью стандартных аналитических систем на различных сроках внутриутробного развития.
К комбинированным принято относить патологии клапанов сердца. Они вызываются недоразвитием створок, а также их склеиванием, как правило, из-за перенесенной матерью при беременности вирусной инфекции.
Самый важный период в развитии сердца — с четырнадцатого по шестидесятый день от зачатия. Именно тогда сердце разделится перегородками и станет четырехкамерным, из общего артериального ствола выделится аорта и легочная артерия, образуется желудочек, сформируются клапаны.
Если в любой из этих важных для развития эмбриона дней беременный организм столкнется с угрозой, вполне возможны последствия в виде формирования дефекта в сердечно-сосудистой системе.
Как правило, о многих пороках сердца будущие родители узнают на первом скрининге, то есть, начиная с 12 недели беременности. Если аномалия слишком тяжела, после ряда уточняющих обследований матери будет предложено прервать беременность. Если ВПС будущего ребенка совместим с жизнью, у родителей будет время подготовиться к неизбежной после его рождения операции на сердце.
В некоторых регионах России уже сейчас проводятся внутриутробные операции на сердце, позволяющие малышу родиться полностью здоровым.
Клинические проявления во время беременности

Как правило, беременность плодом с ВПС для женщины мало чем отличается от типичного варианта. Диагноз становится очевидным лишь при проведении УЗИ плода и его сердца, допплерографии или КТГ.
Плод, как правило, страдает от гипоксии и отличается отставанием в развитии. Возможно назначение беременной лекарственных средств, облегчающих работу сердца плода. Но о полной компенсации состояния речь, как правило, речь не идет.
Главная задача матери, вынашивающей ребенка с дефектом развития сердца, — максимально продлить срок беременности в динамике состояния плода.
Диагностика и детализация состояния плода
Основной показатель нормального развития плода – его сердечный ритм.
- 110-130 ударов до восьмой недели беременности;
- 175-185 до конца первого триместра;
- 145-160 до родов.
На пороки развития сердечно-сосудистой системы плода указывают:
- брадикардия или тахикардия;
- различные временные интервалы между ударами;
- приглушенные звуки сердцебиения – признак кислородного голодания плода.

Порок сердца у плода на УЗИ становится очевидным в случае визуализации дефекта камер органа. ЧСС будущего ребенка можно посчитать уже в первом триместре беременности на рутинном обследовании при помощи акушерского стетоскопа. Более полную информацию о работе сердца плода даст КТГ, которое назначается после 32 недели беременности. Оценив его результаты, акушеры определяют параметры состояния малыша.
Основные заключения анализа показателей состояния плода:
Это доступные и для пациентки, и для врача методики обследования. Они не требуют особой подготовки и не занимают много времени.
Но лидером в исследованиях гемодинамических процессов в сердце и сосудах плода считается доплер-эхокардиография.Этот метод оценивает три основных показателя –направление, скорость и характер кровотока. Процедура такова:на животе беременной устанавливается датчик УЗИ. На экран передается цветное изображение. Красным обозначается течение крови, которая двигается в сторону датчика.Синий цвет указывает на объем крови, идущий в обратном направлении. Максимальная интенсивность того или иного цвета обозначает повышенную гемодинамику.
Чрезвычайно ценную информацию о сердце и самом плоде дает ЭХО-КГ. Исследование может назначаться на любом сроке беременности, но, как правило, выполняется начиная с 12 недели после получения настораживающих показаний первого скрининга.
Это исследование определит:
- направление и скорость кровотока в сосудах;
- проходимость кровяного русла;
- соотношение объемов входящей и выходящей из сердца плода крови;
- ЧСС.
Лучше всего проводить процедуру на сроке от 18 до 24 недели, так как именно в этот срок обеспечивается максимальный визуальный эффект.
Исследования, проведенные ранее этого времени, не будут достаточно объективными из-за малых размеров сердца. К концу беременности ЭХО-КГ плода редко используется из-за большого объема живота, затрудняющего визуализацию органа.
К решению вопросов, касающихся результатов исследования плода с ВПС, привлекается детский кардиолог и кардиохирург.
Тактика ведения беременной

Акушерская тактика ведения беременной, которая вынашивает плод с ВПС представляет собой постановку вопроса об амнио- или кордоцентезе после тщательного эхокардиографического исследования. Их цель — получить материал для проведения хромосомного анализа. Если дефект выявится у нежизнеспособного эмбриона, беременной будет предложен аборт. Срок при этом не имеет никакого значения, особенно если порок сердца будет сочетаться с генетическими аномалиями.
Если ВПС совместим с жизнью, беременная будет до конца срока находится под усиленным наблюдением акушеров. По истечению сорока недель ей будет предложено госпитализироваться для родов в специализированный перинатальный центр. Как правило, у подобного плода показано родоразрешение при помощи кесарева сечения.
После родов малыш будет переведен для обследования, лечения и возможной хирургической операции в кардиологическое отделение детской больницы.
Выводы
Любой порок развития плода, выявленный при беременности, — это всегда сложная проблема и для будущей матери и для обеспечивающих ее течение врачей. Аномалия сердца — не исключение. Сейчас существует множество достоверных методик, позволяющих на ранних сроках опровергнуть или подтвердить диагноз ВПС, оценить состояние, сделать предположение о его жизнеспособности. Почти все они широко применяются и доступны пациенткам.
Для подготовки материала использовались следующие источники информации.
Врожденные пороки сердца – группа заболеваний, объединенных наличием анатомических дефектов сердца, его клапанного аппарата или сосудов, возникших во внутриутробном периоде, приводящих к изменению внутрисердечной и системной гемодинамики. Проявления врожденного порока сердца зависят от его вида; к наиболее характерным симптомам относятся бледность или синюшность кожных покровов, шумы в сердце, отставание в физическом развитии, признаки дыхательной и сердечной недостаточности. При подозрении на врожденный порок сердца выполняется ЭКГ, ФКГ, рентгенография, ЭхоКГ, катетеризация сердца и аортография, кардиография, МРТ сердца и т. д. Чаще всего при врожденных пороках сердца прибегают к кардиохирургической операции – оперативной коррекции выявленной аномалии.
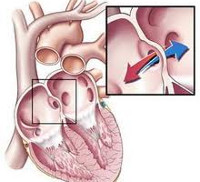
Общие сведения
Врожденные пороки сердца - весьма обширная и разнородная группа заболеваний сердца и крупных сосудов, сопровождающихся изменением кровотока, перегрузкой и недостаточностью сердца. Частота встречаемости врожденных пороков сердца высока и, по оценке различных авторов, колеблется от 0,8 до 1,2% среди всех новорожденных. Врожденные пороки сердца составляют 10-30% всех врожденных аномалий. В группу врожденных пороков сердца входят как относительно легкие нарушения развития сердца и сосудов, так и тяжелые формы патологии сердца, несовместимые с жизнью.
Многие виды врожденных пороков сердца встречаются не только изолированно, но и в различных сочетаниях друг с другом, что значительно утяжеляет структуру дефекта. Примерно в трети случаев аномалии сердца сочетаются с внесердечными врожденными пороками ЦНС, опорно-двигательного аппарата, ЖКТ, мочеполовой системы и пр.
К наиболее частым вариантам врожденных пороков сердца, встречающимся в кардиологии, относятся дефекты межжелудочковой перегородки (ДМЖП – 20%), дефекты межпредсердной перегородки (ДМПП), стеноз аорты, коарктация аорты, открытый артериальный проток (ОАП), транспозиция крупных магистральных сосудов (ТКС), стеноз легочной артерии (10-15% каждый).

Причины врожденных пороков сердца
Этиология врожденных пороков сердца может быть обусловлена хромосомными нарушениями (5%), генной мутацией (2-3%), влиянием факторов среды (1-2%), полигенно-мультифакториальной предрасположенностью (90%).
Различного рода хромосомные аберрации приводят к количественным и структурным изменениям хромосом. При хромосомных перестройках отмечаются множественные полисистемные аномалии развития, включая врожденные пороки сердца. В случае трисомии аутосом наиболее частыми пороками сердца оказываются дефекты межпредсердной или межжелудочковой перегородок, а также их сочетание; при аномалиях половых хромосом врожденные пороки сердца встречаются реже и представлены, главным образом, коарктацией аорты или дефектом межжелудочковой перегородки.
Врожденные пороки сердца, обусловленные мутациями единичных генов, также в большинстве случаев сочетаются с аномалиями других внутренних органов. В этих случаях сердечные пороки являются частью аутосомно-доминантных (синдромы Марфана, Холта-Орама, Крузона, Нунана и др.), аутосомно-рецессивных синдромов (синдром Картагенера, Карпентера, Робертса, Гурлер и др.) или синдромов, сцепленных с Х-хромосомой (синдромы Гольтца, Аазе, Гунтера и др.).
Среди повреждающих факторов внешней среды к развитию врожденных пороков сердца приводят вирусные заболевания беременной, ионизирующая радиация, некоторые лекарственные препараты, пагубные привычки матери, производственные вредности. Критическим периодом неблагоприятного воздействия на плод являются первые 3 месяца беременности, когда происходит фетальный органогенез.
Внутриутробное поражение плода вирусом краснухи наиболее часто вызывает триаду аномалий – глаукому или катаракту, глухоту, врожденные пороки сердца (тетраду Фалло, транспозицию магистральных сосудов, открытый артериальный проток, общий артериальный ствол, клапанные пороки, стеноз легочной артерии, ДМЖП и др.). Также обычно имеют место микроцефалия, нарушение развития костей черепа и скелета, отставание в умственном и физическом развитии.
В структуру эмбриофетального алкогольного синдрома обычно входят дефекты межжелудочковой и межпредсердной перегородки, открытый артериальный проток. Доказано, что тератогенное действие на сердечно-сосудистую систему плода оказывает прием амфетаминов, приводящий к транспозиции магистральных сосудов и ДМЖП; противосудорожных средств, обусловливающих развитие стеноза аорты и легочной артерии, коарктации аорты, открытого артериального протока, тетрады Фалло, гипоплазии левых отделов сердца; препаратов лития, приводящих к атрезии трехстворчатого клапана, аномалии Эбштейна, ДМПП; прогестагенов, вызывающих тетраду Фалло, другие сложные врожденные пороки сердца.
У женщин, страдающих преддиабетом или диабетом, дети с врожденными пороками сердца рождаются чаще, чем у здоровых матерей. В этом случае у плода обычно формируются ДМЖП или транспозиция крупных сосудов. Вероятность рождения ребенка с врожденным пороком сердца у женщины с ревматизмом составляет 25 %.
Кроме непосредственных причин, выделяют факторы риска формирования аномалий сердца у плода. К ним относят возраст беременной младше 15-17 лет и старше 40 лет, токсикозы I триместра, угрозу самопроизвольного прерывания беременности, эндокринные нарушения у матери, случаи мертворождения в анамнезе, наличие в семье других детей и близких родственников с врожденными пороками сердца.
Классификация врожденных пороков сердца
Существует несколько вариантов классификаций врожденных пороков сердца, в основу которых положен принцип изменения гемодинамики. С учетом влияния порока на легочный кровоток выделяют:
- врожденные пороки сердца с неизмененным (либо незначительно измененным) кровотоком в малом круге кровообращения: атрезия аортального клапана, стеноз аорты, недостаточность легочного клапана, митральные пороки (недостаточность и стеноз клапана), коарктация аорты взрослого типа, трехпредсердное сердце и др.
- врожденные пороки сердца с увеличенным кровотоком в легких: не приводящие к развитию раннего цианоза (открытый артериальный проток, ДМПП, ДМЖП, аортолегочный свищ, коарктация аорты детского типа, синдром Лютамбаше), приводящие к развитию цианоза (атрезия трехстворчатого клапана с большим ДМЖП, открытый артериальный проток с легочной гипертензией)
- врожденные пороки сердца с обедненным кровотоком в легких: не приводящие к развитию цианоза (изолированный стеноз легочной артерии), приводящие к развитию цианоза (сложные пороки сердца – болезнь Фалло, гипоплазия правого желудочка, аномалия Эбштейна)
- комбинированные врожденные пороки сердца, при которых нарушаются анатомические взаимоотношения между крупными сосудами и различными отделами сердца: транспозиция магистральных артерий, общий артериальный ствол, аномалия Тауссиг-Бинга, отхождение аорты и легочного ствола из одного желудочка и пр.
Нарушения гемодинамики при врожденных пороках сердца
В результате выше названных причин у развивающего плода может нарушаться правильное формирование структур сердца, что выражается в неполном или несвоевременном закрытии перепонок между желудочками и предсердиями, неправильном образовании клапанов, недостаточном повороте первичной сердечной трубки и недоразвитии желудочков, аномальном расположении сосудов и т. д. После рождения у части детей остаются открытыми артериальный проток и овальное окно, которые во внутриутробном периоде функционируют в физиологическом порядке.
При врожденных пороках сердца бледного типа с артериовенозным сбросом вследствие гиперволемии развивается гипертензия малого круга кровообращения; при пороках синего типа с веноартериальным шунтом у больных имеет место гипоксемия.
Около 50% детей с большим сбросом крови в малый круг кровообращения погибают без кардиохирургической помощи на первом году жизни от явлений сердечной недостаточности. У детей, перешагнувших этот критический рубеж, сброс крови в малый круг уменьшается, самочувствие стабилизируется, однако постепенно прогрессируют склеротические процессы в сосудах легких, обусловливая легочную гипертензию.
При цианотических врожденных пороках сердца венозный сброс крови или ее смешение приводит к перегрузке большого и гиповолемии малого круга кровообращения, вызывая снижение насыщения крови кислородом (гипоксемию) и появление синюшности кожи и слизистых. Для улучшения вентиляции и перфузии органов развивается коллатеральная сеть кровообращения, поэтому, несмотря на выраженные нарушения гемодинамики, состояние больного может длительное время оставаться удовлетворительным. По мере истощения компенсаторных механизмов, вследствие длительной гиперфункции миокарда, развиваются тяжелые необратимые дистрофические изменения в сердечной мышце. При цианотических врожденных пороках сердца оперативное вмешательство показано уже в раннем детском возрасте.
Симптомы врожденных пороков сердца
Клинические проявления и течение врожденных пороков сердца определяется видом аномалии, характером нарушений гемодинамики и сроками развития декомпенсации кровообращения.
У новорожденных с цианотическими врожденными пороками сердца отмечается цианоз (синюшность) кожных покровов и слизистых оболочек. Синюшность усиливается при малейшем напряжении: сосании, плаче ребенка. Белые пороки сердца проявляются побледнением кожи, похолоданием конечностей.
Дети с врожденными пороками сердца обычно беспокойные, отказываются от груди, быстро устают в процессе кормления. У них появляется потливость, тахикардия, аритмии, одышка, набухание и пульсация сосудов шеи. При хроническом нарушении кровообращения дети отстают в прибавлении веса, росте и физическом развитии. При врожденных пороках сердца обычно сразу поле рождения выслушиваются сердечные шумы. В дальнейшем обнаруживаются признаки сердечной недостаточности (отеки, кардиомегалия, кардиогенная гипотрофия, гепатомегалия и др.).
Осложнениями врожденных пороков сердца могут стать бактериальный эндокардит, полицитемия, тромбозы периферических сосудов и тромбоэмболии сосудов головного мозга, застойные пневмонии, синкопальные состояния, одышечно-цианотические приступы, стенокардитический синдром или инфаркт миокарда.
Диагностика врожденных пороков сердца
Выявление врожденных пороков сердца осуществляется путем комплексного обследования. При осмотре ребенка отмечают окраску кожных покровов: наличие или отсутствие цианоза, его характер (периферический, генерализованный). При аускультации сердца нередко выявляется изменение (ослабление, усиление или расщепление) сердечных тонов, наличие шумов и пр. Физикальное обследование при подозрении на врожденный порок сердца дополняется инструментальной диагностикой - электрокардиографией (ЭКГ), фонокардиографией (ФКГ), рентгенографией органов грудной клетки, эхокардиографией (ЭхоКГ).
ЭКГ позволяет выявить гипертрофию различных отделов сердца, патологическое отклонение ЭОС, наличие аритмий и нарушений проводимости, что в совокупности с данными других методов клинического обследования позволяет судить о тяжести врожденного порока сердца. С помощью суточного холтеровского ЭКГ-мониторирования обнаруживаются скрытые нарушения ритма и проводимости. Посредством ФКГ более тщательно и детально оценивается характер, длительность и локализация сердечных тонов и шумов. Данные рентгенографии органов грудной клетки дополняют предыдущие методы за счет оценки состояния малого круга кровообращения, расположения, формы и размеров сердца, изменений со стороны других органов (легких, плевры, позвоночника). При проведении ЭхоКГ визуализируются анатомические дефекты перегородок и клапанов сердца, расположение магистральных сосудов, оценивается сократительная способность миокарда.
При сложных врожденных пороках сердца, а также сопутствующей легочной гипертензии, с целью точной анатомической и гемодинамической диагностики, возникает необходимость в выполнении зондирования полостей сердца и ангиокардиографии.
Лечение врожденных пороков сердца
Наиболее сложной проблемой в детской кардиологии является хирургическое лечение врожденных пороков сердца у детей первого года жизни. Большинство операций в раннем детском возрасте выполняется по поводу цианотических врожденных пороков сердца. При отсутствии у новорожденного признаков сердечной недостаточности, умеренной выраженности цианоза операция может быть отложена. Наблюдение за детьми с врожденными пороками сердца осуществляют кардиолог и кардиохирург.
Специфическое лечение в каждом конкретном случае зависит от разновидности и степени тяжести врожденного порока сердца. Операции при врожденных дефектах перегородок сердца (ДМЖП, ДМПП) могут включать пластику или ушивание перегородки, рентгенэндоваскулярную окклюзию дефекта. При наличии выраженной гипоксемии детям с врожденными пороками сердца первым этапом выполняется паллиативное вмешательство, предполагающее наложение различного рода межсистемных анастомозов. Подобная тактика улучшает оксигенацию крови, уменьшает риск осложнений, позволяет провести радикальную коррекцию в более благоприятных условиях. При аортальных пороках выполняется резекция или баллонная дилатация коарктации аорты, пластика аортального стеноза и др. При ОАП производится его перевязка. Лечение стеноза легочной артерии заключается в проведении открытой или эндоваскулярной вальвулопластики и т. д.
Анатомически сложные врожденные пороки сердца, при которых радикальная операция не представляется возможной, требуют выполнения гемодинамической коррекции, т. е. разделения артериального и венозного потоков крови без устранения анатомического дефекта. В этих случаях могут проводиться операции Фонтена, Сеннинга, Мастарда и др. Серьезные пороки, не поддающиеся оперативному лечению, требуют проведения пересадки сердца.
Консервативное лечение врожденных пороков сердца может включать в себя симптоматическую терапию одышечно-цианотических приступов, острой левожелудочковой недостаточности (сердечной астмы, отека легких), хронической сердечной недостаточности, ишемии миокарда, аритмий.
Прогноз и профилактика врожденных пороков сердца
В структуре смертности новорожденных врожденные пороки сердца занимают первое место. Без оказания квалифицированной кардиохирургической помощи в течение первого года жизни погибает 50-75% детей. В периоде компенсации (2-3 года) смертность снижается до 5%. Ранее выявление и коррекция врожденного порока сердца позволяет существенно улучшить прогноз.
Профилактика врожденных пороков сердца требует тщательного планирования беременности, исключения воздействия неблагоприятных факторов на плод, проведения медико-генетического консультирования и разъяснительной работы среди женщин групп риска по рождению детей с сердечной патологией, решения вопроса о пренатальной диагностике порока (УЗИ, биопсия хориона, амниоцентез) и показаниях к прерыванию беременности. Ведение беременности у женщин с врожденными пороками сердца требует повышенного внимания со стороны акушера-гинеколога и кардиолога.
Пороки сердца у беременных — это врожденные или приобретенные анатомические аномалии сердечных клапанов, отверстий, внутрикардиальных перегородок, аорты и легочной артерии, течение которых может осложниться при гестации или ухудшить ее прогноз. Проявляются слабостью, утомляемостью, сонливостью, тяжестью в ногах, одышкой, сердцебиениями, периферическими отеками, сухим кашлем. Диагностируются при помощи эхокардиографии, ЭКГ, фонокардиографии. Для лечения используют антибиотики, гликозиды, диуретики, периферические вазодилалаторы, β-адреноблокаторы, антитромботические средства. Операции выполняют в исключительных случаях по показаниям.
МКБ-10

Общие сведения

Причины
Аномалии строения клапанного аппарата, перегородок, отверстий и отходящих магистральных сосудов обычно возникают задолго до начала гестации. Однако изменения гемодинамики, характерные для периода беременности, могут проявить кардиологическое заболевание или усугубить его клиническую картину. Наиболее распространенными причинами пороков сердца, обнаруживаемых у беременных, являются:
- Воспаление эндокарда и миокарда. В 80-85% случаев аномалии строения сердца развиваются вследствие ревматического поражения. Реже они становятся результатом инфекционного эндокардита другого генеза, сифилиса, специфических воспалительных изменений при диффузных заболеваниях соединительной ткани (склеродермии, системной красной волчанке, ревматоидном артрите).
- Врожденные дефекты. До 7,3-8,0% кардиальных пороков являются дизэмбриогенетическими либо наследуемыми по аутосомно-рецессивному, аутосомно-доминантному типам. Чаще других у беременных наблюдаются признаки открытого аортального протока, дефектов межпредсердной и межжелудочковой перегородок, стеноза легочной артерии, коарктации аорты, транспозиции магистральных сосудов.
У некоторых пациенток вторичная функциональная недостаточность клапанов возникает на фоне кардиологических заболеваний, которые сопровождаются перегрузкой желудочков или расширением фиброзного кольца клапанных структур (гипертонической болезнью, симптоматической артериальной гипертензией, дилатационной кардиомиопатией, кардиосклерозом, инфарктом миокарда).
Патогенез
Механизм развития патологических проявлений при пороках сердцах у беременных зависит от особенностей конкретной аномалии, однако в гестационном периоде возникает ряд общих нагрузочных и адаптационных гемодинамических факторов, влияющих на течение сердечно-сосудистого заболевания. С 10 по 32 неделю объем крови, циркулирующей в сосудистом русле, увеличивается на 30-35%, что в сочетании с повышением гидростатического капиллярного давления приводит к возрастанию количества внеклеточной жидкости на 5-6 л. Одновременно с этим усиливается работа левого желудочка, что сопровождается увеличением ударного и минутного объемов на 35-50%, ростом систолического и пульсового давления, снижением диастолического давления на руках. В конце второго-третьем триместрах возникает физиологическая тахикардия до 85-90 сокращений сердца в минуту.
Классификация
В зависимости от происхождения пороки сердца, выявляемые у беременных, бывают врожденными и приобретенными. С учетом локализации различают изолированные митральные, аортальные, трикуспидальные аномалии, повреждения клапанов легочной артерии, дефекты внутрисердечных перегородок, комбинированные и сочетанные поражения. По характеру патологических изменений выделяют стеноз (сужение), недостаточность (расширение), аномальные отверстия, транспозиции сосудов.
Большое прогностическое значение в систематизации пороков имеет выраженность сердечной недостаточности: при I (скрытой) стадии ее признаки появляются только при физических нагрузках, при IIА отмечаются умеренно выраженные симптомы в покое, усиливающиеся при движении, при IIБ — в покое определяются значительные нарушения гемодинамики, для III (дистрофической) характерны органные метаболические расстройства. На основании этого критерия различают четыре степени риска осложнений у беременных, страдающих пороками сердца:
- Iстепень. Риск отсутствует. Признаков сердечной недостаточности нет, давление в легочной артерии нормальное, ревматический процесс неактивен. Отделы сердца и толщина миокарда не изменены. Вероятность осложненного течения гестации не отличается от показателей в общей популяции. Беременность не противопоказана.
- IIстепень. Умеренно повышенный риск. Отмечаются скрытая сердечная недостаточность и I степень активности ревматизма, умеренное увеличение давления в системе легочной артерии. Отделы сердца незначительно или умеренно утолщены и дилатированы. Беременность допускается, но возможно ухудшение состояния пациентки.
- IIIстепень. Высокий риск акушерских и кардиологических осложнений. Определяются сердечная недостаточность IIА ст., ревматизм II-III степени активности, легочная гипертензия, нарушения ритма. Отделы сердца гипертрофированы и расширены. Большинству пациенток гестацию рекомендуется прервать до 12 недели.
- IVстепень. Крайне высокий риск материнской летальности из-за кардиологических и акушерских осложнений. Диагностируется сердечная недостаточность IIБ-III ст., значительная легочная гипертензия, выраженная систолическая дисфункция левого желудочка, цианоз. Беременность обычно прерывают независимо от сроков.
Симптомы пороков сердца у беременных
Клинические признаки зависят от типа анатомических дефектов, длительности заболевания и функциональной состоятельности миокарда. Пациентки с кардиологическими пороками жалуются на повышенную утомляемость, сонливость, ощущение слабости в мышцах, тяжесть в ногах. При нагрузках наблюдаются одышка, перебои, сердцебиения. У больных с выраженной недостаточностью кровообращения перечисленные симптомы также отмечаются в покое. Возможно появление бледности или цианотичности кожных покровов, отеков в области стоп, голеностопных суставов, голеней, возникновение приступов сердечной астмы с сухим кашлем или откашливанием небольшого количества слизистой мокроты, иногда содержащей прожилки крови.
Осложнения
Пороки со значительной декомпенсацией работы сердца являются ведущей причиной материнской смертности, которая может достигать 150-200 случаев на 100 тыс. живорождений, занимают второе место по показателям перинатальной летальности (12-29%). Основные акушерские осложнения при аномалиях строения сердца — самопроизвольные аборты, преждевременные роды, ранний токсикоз, гестозы, HELLP-синдром, дискоординация и слабость родовой деятельности, коагулопатические кровотечения в послеродовом периоде. Практически у каждой пятой беременной несвоевременно изливаются околоплодные воды.
В каждом втором случае беременности (кроме пациенток с риском I степени) отмечаются признаки задержки развития и гипоксии плода, вызванные хронической плацентарной недостаточностью. У женщин, имеющих врожденные сердечные аномалии, чаще рождаются дети с такой же кардиологической патологией. При пороках сердца повышается вероятность развития клинически значимых нарушений ритма, требующих специальной терапии, сердечно-сосудистых осложнений (тромбоэмболии, инфаркта миокарда, инсульта), эндокардита.
Диагностика
Поскольку врожденные и приобретенные пороки сердца могут протекать субклинически, в 27% случаев они впервые диагностируются именно в период беременности. Кроме традиционных физикальных исследований (перкуссии и аускультации сердца) при постановке диагноза используют современные инструментальные методы, позволяющие визуализировать анатомические дефекты и оценить функциональные возможности сердечно-сосудистой системы. Наиболее информативными для диагностики пороков сердца у беременных считаются:
- Эхокардиография. Совокупное использование различных УЗИ-методик (одномерной и двухмерной ЭхоКГ), доплеровского сканирования дает возможность исследовать состояние клапанного аппарата, оценить толщину сердечных стенок и объем полостей, выполнить фазовый анализ и оценку сократимости. С помощью этого метода также определяются пороки крупных сосудов (грудной аорты и др.).
- Электрокардиография. ЭКГ применяют для скрининга нарушений частоты и регулярности сердечного ритма, изменений проводимости, выявления возможных острых и хронических повреждений миокарда, осложняющих клиническую картину и ухудшающих прогноз беременности при пороке сердца. По показаниям исследование дополняют суточным мониторированием ЭКГ и фонокардиографией.
Из-за возможных повреждающих воздействий на плод беременным с анатомическими пороками сердца не рекомендуется проводить рентгенологические исследования и МРТ. В порядке исключения при подготовке к кардиовмешательствам допустимо зондирование полостей сердца. Для оценки состояния электролитного баланса и свертывающей системы показано определение концентрации калия и натрия в сыворотке крови, коагулограмма. Дифференциальная диагностика проводится с функциональными шумами в сердце при анемии, вегетососудистой дистонии, ИБС с развитием аневризмы, гипертонической болезнью у беременных, миокардитом, токсическими кардиомиопатиями, миокардиодистрофией, кардиомегалией. Кроме акушера-гинеколога к сопровождению беременной привлекается кардиолог. При необходимости пациентку осматривают кардиохирург, ревматолог, инфекционист, невропатолог, гематолог.
Лечение пороков сердца у беременных
При кардиологических пороках существует три критических периода гестации, во время которых рекомендована плановая госпитализация. На 10-12 неделях возможно обострение ревматизма за счет физиологического снижения иммунитета и уменьшения секреции кортикостероидов. Именно на этом сроке принимается решение о возможности пролонгации беременности. На 26-32 неделях сердечно-сосудистая система пациентки испытывает наибольшие нагрузки, что требует дополнительной коррекции терапии. За 2-3 недели до родов возможно развитие или усугубление сердечной недостаточности под действием перегрузочных гемодинамических факторов, которые следует учитывать при выборе способа родоразрешения.
Основными терапевтическими задачами являются профилактика акушерских осложнений, купирование обострений и рецидивов у больных ревматизмом, предупреждение расстройств ритма и проводимости. Адекватное медикаментозное лечение является предпочтительным для ведения большинства беременных женщин с пороками сердца, включая пациенток с сердечной недостаточностью. Лекарственные средства для фармакотерапии подбираются кардиологом индивидуально. Обычно беременным назначаются:
- Антибактериальная терапия. 10-14-дневные профилактические курсы полусинтетических пенициллинов показаны женщинам с ревматическими пороками из I и II групп риска. Антибиотики применяют по показаниям с учетом активности ревматического процесса и при необходимости дополняют глюкокортикоидами.
- Тиазидные и петлевые диуретики. Обеспечивают уменьшение объема циркулирующей крови при недостаточной сократительной активности желудочков. При левожелудочковой недостаточности средства комбинируют с препаратами, которые уменьшают приток крови в камеры сердца, и периферическими вазодилататорами.
- Сердечные гликозиды. При отсутствии легочной гипертензии такие медикаменты поддерживают сердечный выброс и адекватную перфузию различных органов и систем, в том числе фетоплацентарного комплекса. С помощью гликозидов также можно купировать тахисистолическую фибрилляцию предсердий.
- Нитраты. Благодаря депонированию крови в венах большого круга кровообращения средства этой группы снижают преднагрузку на сердце, что позволяет уменьшить признаки венозной легочной гипертензии и застоя крови в малом круге. Недостатком применения нитратов является возможное уменьшение сердечного выброса.
- β-адреноблокаторы. Препараты, снижающие силу сокращений миокарда, рекомендованы беременным с синусовой тахикардией, при которой увеличивается давление в полости левого предсердия, возникает застой крови в легочном круге кровообращения. Могут применяться при тахисистолической фибрилляции предсердий.
- Антикоагулянты. С учетом срока беременности и результатов тромбоэластограммы женщинам с сердечными пороками назначают низкомолекулярные гепарины, антиагреганты в комбинации с периферическими вазодилататорами, улучшающими капиллярный кровоток. Во время родов введение гепарина прекращают.
При наличии показаний выполняются малоинвазивные операции (эндоваскулярная баллонная дилатация аортального стеноза и пр.) и закрытая митральная комиссуротомия. Открытые хирургические вмешательства по протезированию клапанов с выключением естественного кровообращения проводятся только при угрозе жизни женщины и невозможности чрескожной коррекции аномалии.
При наличии порока сердца предпочтительны программированные естественные роды в дневное время суток с введением гормонально-энергетического комплекса для профилактики аномальной родовой деятельности и максимальным нарастающим обезболиванием с использованием масочного наркоза и эпидуральной анальгезии. Для бережного родоускорения применяется амниотомия. В родах допустимо назначение утеротоников, спазмолитиков, антигипоксантов. Потуги в период изгнания выключаются при высокой активности ревматизма, комбинированных и сочетанных пороках, стенозах, нарушениях кровообращения.
При обнаружении активного ревматического процесса, признаков нарушения кровообращений, развитии поздних гестозов, плацентарной недостаточности с хронической гипоксией или задержкой развития плода родоразрешение выполняется досрочно на 34-37 неделях. Абсолютными показаниями к проведению кесарева сечения являются терапевтически резистентная прогрессирующая сердечная недостаточность, III степень активности ревмокардита, аневризма аорты, коарктация аорты с выраженной гипертензией, полное нарушение атриовентрикулярной проводимости, использование искусственного водителя ритма, подострое течение септического эндокардита, пороки с нагрузкой преимущественно на левые отделы сердца, сопутствующая акушерская патология (крупный плод, узкий таз, неправильное положение ребенка).
Прогноз и профилактика
Исход беременности и родов при пороках сердца зависит от варианта анатомического дефекта, наличия нарушений кровообращения, активности ревматизма (при аномалиях ревматического происхождения). Абсолютными противопоказаниями к вынашиванию ребенка считаются сочетанные и комбинированные виды пороков, единый желудочек, коарктация аорты, выраженный аортальный стеноз, сочетание анатомических аномалий с бактериальным эндокардитом, тахиаритмией, легочной гипертензией 2-3 степени, синдром Эйзенменгера, синдром Марфана с увеличением диаметра корня аорты более 4,5 см, предшествующая послеродовая кардиомиопатия. Прогноз также ухудшается при выраженных степенях сужения (недостаточности) сердечных клапанов и по мере увеличения возраста беременной – после 30 лет вероятность развития недостаточности кровообращения повышается вдвое.
В остальных случаях при планировании беременности необходимо учитывать рекомендации кардиолога, на прегравидарном этапе максимально компенсировать порок и купировать ревматическую лихорадку, по показаниям выполнить операцию по коррекции порока до зачатия. Беременным показана ранняя постановка на учет в женской консультации, диетотерапия с достаточным потреблением белка, микроэлементов и витаминов, ограничением количества жидкости и поваренной соли. Рекомендованы дозированные физические нагрузки, нормализация режима работы и отдыха, профилактическое использование растительных препаратов с седативным эффектом.
1. Ведение беременных с врожденными пороками сердца/ Волчкова Н.С., Субханкулова С.Ф., Субханкулова А.Ф.// Вестник современной клинической медицины. — 2016 — Т. 9, вып. 4.
3. Врожденные пороки сердца и беременность/ Дашкевич В.Е., Кирильчук М.Е.// Международный медицинский журнал. – 2011 - №1.
Внутриутробные инфекции – группа заболеваний плода и новорожденного, развивающихся вследствие заражения в дородовом периоде или в родах. Внутриутробные инфекции могут приводить к гибели плода, самопроизвольному аборту, задержке внутриутробного развития, преждевременным родам, формированию врожденных пороков, поражению внутренних органов и ЦНС. Методы диагностики внутриутробных инфекций включают микроскопические, культуральные, иммуноферментные, молекулярно-биологические исследования. Лечение внутриутробных инфекций проводится с использованием иммуноглобулинов, иммуномодуляторов, противовирусных, антибактериальных препаратов.

Общие сведения
Внутриутробные инфекции – патологические процессы и заболевания, обусловленные антенатальным и интранатальным инфицированием плода. Истинная распространенность внутриутробных инфекций не установлена, однако, согласно обобщенным данным, с врожденными инфекциями рождается не менее 10% новорожденных. Актуальность проблемы внутриутробных инфекций в педиатрии обусловлена высокими репродуктивными потерями, ранней неонатальной заболеваемостью, приводящей к инвалидизации и постнатальной гибели детей. Вопросы профилактики внутриутробных инфекций лежат в плоскости рассмотрения акушерства и гинекологии, неонатологии, педиатрии.

Причины внутриутробных инфекций
Внутриутробные инфекции развиваются в результате инфицирования плода в дородовом периоде или непосредственно во время родов. Обычно источником внутриутробной инфекции для ребенка выступает мать, т. е. имеет место вертикальный механизм передачи, который в антенатальном периоде реализуется трансплацентарным или восходящим (через инфицированные околоплодные воды) путями, а в интранатальном - аспирационным или контактным путями.
Реже происходит ятрогенное инфицирование плода в период беременности при проведении женщине инвазивной пренатальной диагностики (амниоцентеза, кордоцентеза, биопсии ворсин хориона), введении плоду препаратов крови через сосуды пуповины (плазмы, эритроцитарной массы, иммуноглобулинов) и т. д.
В антенатальном периоде инфицирование плода обычно связано с вирусными агентами (вирусами краснухи, герпеса, цитомегалии, гепатита В и С, Коксаки, ВИЧ) и внутриклеточными возбудителями (токсоплазмоза, микоплазмоза).
В интранатальном периоде чаще происходит микробная контаминация, характер и степень которой зависит от микробного пейзажа родовых путей матери. Среди бактериальных агентов наиболее распространены энтеробактерии, стрептококки группы В, гонококки, синегнойная палочки, протей, клебсиелла и др. Плацентарный барьер непроницаем для большинства бактерий и простейших, однако при повреждении плаценты и развитии фетоплацентарной недостаточности, может произойти антенатальное микробное инфицирование (например, возбудителем сифилиса). Кроме этого, не исключается и интранатальное вирусное заражение.
Факторами возникновения внутриутробных инфекций служат отягощенный акушерско-гинекологический анамнез матери (неспецифические кольпиты, эндоцервициты, ЗППП, сальпингофориты), неблагополучное течение беременности (угроза прерывания, гестозы, преждевременная отслойка плаценты) и инфекционная заболеваемость беременной. Риск развития манифестной формы внутриутробной инфекции существенно выше у недоношенных детей и в том случае, когда женщина инфицируется первично во время беременности.
Известно, что тяжесть проявлений инфекционного процесса у беременной и у плода может не совпадать. Бессимптомное или малосимптомное течение инфекции и у матери может вызвать тяжелые поражения плода, вплоть до его гибели. Это связано с повышенным тропизмом вирусных и микробных возбудителей к эмбриональным тканям, преимущественно ЦНС, сердца, органа зрения.
Классификация
Этиологическая структура внутриутробных инфекций предполагает их деление на:
- вирусные (вирусный гепатит, герпес, краснуха, ОРВИ, цитомегалия, эпидемический паротит, энтеровирусная инфекция)
- бактериальные (туберкулез, сифилис, листериоз, сепсис)
- паразитарные и грибковые (микоплазмоз, токсоплазмоз, хламидиоз, кандидоз и др.)
Для обозначения группы наиболее распространенных внутриутробных инфекций используется аббревиатура TORCH-синдром, объединяющий токсоплазмоз (toxoplasmosis), краснуху (rubella), цитомегалию (cytomegalovirus), герпес (herpes simplex). Буквой О (other) обозначаются другие инфекции, в числе которых - вирусные гепатиты, ВИЧ-инфекция, ветряная оспа, листериоз, микоплазмоз, сифилис, хламидиоз и др.).
Симптомы внутриутробных инфекций
Наличие внутриутробной инфекции у новорожденного может быть заподозрено уже во время родов. В пользу внутриутробного инфицирования может свидетельствовать излитие мутных околоплодных вод, загрязненных меконием и имеющих неприятный запах, состояние плаценты (полнокровие, микротробозы, микронекрозы). Дети с внутриутробной инфекцией часто рождаются в состоянии асфиксии, с пренатальной гипотрофией, увеличенной печенью, пороками развития или стигмами дисэмбриогенеза, микроцефалией, гидроцефалией. С первых дней жизни у них отмечается желтуха, элементы пиодермии, розеолезных или везикулезных высыпаний на коже, лихорадка, судорожный синдром, респиратрные и кардиоваскулярные расстройства.
Ранний неонатальный период при внутриутробных инфекциях нередко отягощается интерстициальной пневмонией, омфалитом, миокардитом или кардитом, анемией, кератоконъюнктивитом, хориоретинитом, геморрагическим синдромом и др. При инструментальном обследовании у новорожденных могут обнаруживаться врожденная катаракта, глаукома, врожденные пороки сердца, кисты и кальцификаты мозга.
В перинатальном периоде у ребенка отмечаются частые и обильные срыгивания, мышечная гипотония, синдром угнетения ЦНС, серый цвет кожных покровов. В поздние сроки при длительном инкубационном периоде внутриутробной инфекции возможно развитие поздних менингитов, энцефалитов, остеомиелита.
Рассмотрим проявления основных внутриутробных инфекций, составляющих TORCH-синдром.
Врождённый токсоплазмоз
Внутриутробное инфицирование одноклеточным протозойным паразитом Toxoplasma Gondii приводит к тяжелым поражениям плода – задержке развития, врожденным порокам развития мозга, глаз, сердца, скелета.
После рождения в остром периоде внутриутробная инфекция проявляется лихорадкой, желтухой, отечным синдромом, экзантемой, геморрагиями, диареей, судорогами, гепатоспленомегалией, миокардитом, нефритом, пневмонией. При подостром течении доминирую признаки менингита или энцефалита. При хронической персистенции развивается гидроцефалия с микроцефалией, иридоциклит, косоглазие, атрофия зрительных нервов. Иногда встречаются моносимптомные и латентные формы внутриутробной инфекции.
К числу поздних осложнений врожденного токсоплазмоза относятся олигофрения, эпилепсия, слепота.
Врождённая краснуха
Внутриутробная инфекция возникает из-за заболевания краснухой при беременности. Вероятность и последствия инфицирования плода зависят от гестационного срока: в первые 8 недель риск достигает 80%; последствиями внутриутробной инфекции могут служить самопроизвольное прерывание беременности, эмбрио- и фетопатии. Во II триместре риск внутриутробного инфицирования составляет 10-20%, в III – 3-8%.
Дети с внутриутробной инфекцией обычно рождаются недоношенными или с низкой массой тела. Для периода новорожденности характерна геморрагическая сыпь, длительная желтуха.
Классические проявления врожденной краснухи представлены триадой Грега: поражением глаз (микрофтальмией, катарактой, глаукомой, хориоретинитом), ВПС (открытым артериальным протоком, ДМПП, ДМЖП, стенозом легочной артерии), поражением слухового нерва (сенсоневральной глухотой). В случае развития внутриутробной инфекции во второй половине беременности у ребенка обычно имеется ретинопатия и глухота.
Кроме основных проявлений врожденной краснухи, у ребенка могут выявляться и другие аномалии: микроцефалия, гидроцефалия, расщелины нёба, гепатит, гепатоспленомегалия, пороки развития мочеполовой системы и скелета. В дальнейшем внутриутробная инфекция напоминает о себе отставанием ребенка в физическом развитии, ЗПР или умственной отсталостью.
Врождённая цитомегалия
Внутриутробное заражение цитомегаловирусной инфекцией может приводить к локальному или генерализованному поражению многих органов, иммунодефициту, гнойно-септическим осложнениям. Врожденные дефекты развития обычно включают микроцефалию, микрогирию, микрофтальмию, ретинопатию, катаракту, ВПС и др. Неонатальный период врожденной цитомегалии осложняется желтухой, геморрагическим синдромом, двусторонней пневмонией, интерстициальным нефритом, анемией.
К отдаленным последствиям внутриутробной инфекции относятся слепота, нейросенсорная глухота, энцефалопатия, цирроз печени, пневмосклероз.
Врождённая герпетическая инфекция
Внутриутробная герпес-инфекция может протекать в генерализованной (50%), неврологической (20%), слизисто-кожной форме (20%).
Генерализованная внутриутробная врожденная герпетическая инфекция протекает с выраженным токсикозом, респираторным дистресс-синдромом, гепатомегалией, желтухой, пневмонией, тромбоцитопенией, геморрагическим синдромом. Неврологическая форма врожденного герпеса клинически проявляется энцефалитом и менингоэнцефалитом. Внутриутробная герпес-инфекция с развитием кожного синдрома сопровождается появлением везикулярной сыпи на кожных покровах и слизистых оболочках, в т. ч. внутренних органов. При наслоении бактериальной инфекции развивается сепсис новорожденных.
Внутриутробная герпес-инфекция у ребенка может приводить к формированию пороков развития - микроцефалии, ретинопатии, гипоплазии конечностей (кортикальной карликовости). В числе поздних осложнений врожденного герпеса - энцефалопатия, глухота, слепота, задержка психомоторного развития.
Диагностика
В настоящее время актуальной задачей является пренатальная диагностика внутриутробных инфекций. С этой целью на ранних сроках беременности проводится микроскопия мазка, бактериологический посев из влагалища на флору, ПЦР-исследование соскоба, обследование на TORCH-комплекс. Беременным из группы высокого риска по развитию внутриутробной инфекции показана инвазивная пренатальная диагностика (аспирация ворсин хориона, амниоцентез с исследованием амниотической жидкости, кордоцентез с исследованием пуповинной крови).
Возможно выявление эхографических маркеров внутриутробных инфекций с помощью акушерского УЗИ. К косвенным эхографическим признакам внутриутробного инфицирования относятся маловодие или многоводие; наличие гиперэхогенной взвеси в околоплодных водах или амниотических тяжей; гипоплазия ворсин хориона, плацентит; преждевременное старение плаценты; отечный синдром плода (асцит, перикардит, плеврит), гепатоспленомегалия, кальцификаты и пороки развития внутренних органов и др. В процессе допплерографического исследования кровотока выявляются нарушения плодово-плацентарного кровотока. Кардиотокография обнаруживает признаки гипоксии плода.
После рождения ребенка с целью достоверной верификации этиологии внутриутробной инфекции используются микробиологические (вирусологические, бактериологические), молекулярно-биологические (ДНК-гибридизация, ПЦР), серологические (ИФА) методики обследования. Важное диагностическое значение имеет гистологическое исследование плаценты.
По показаниям новорожденные с внутриутробными инфекциями в первые сутки жизни должны быть осмотрены детским неврологом, детским кардиологом, детским офтальмологом и др. специалистами. Целесообразно провести ЭхоКГ, нейросонографию, офтальмоскопию, исследование слуха методом вызванной отоакустической эмиссии.
Лечение внутриутробных инфекций
Общие принципы лечения внутриутробных инфекций предполагают проведение иммунотерапии, противовирусной, антибактериальной и посиндромной терапии.
Иммунотерапия включает применение поливалентных и специфических иммуноглобулинов, иммуномодуляторов (интерферонов). Противовирусная терапия направленного действия осуществляется, главным образом, ацикловиром. Для противомикробной терапии бактериальных внутриутробных инфекций используются антибиотики широкого спектра действия (цефалоспорины, аминогликозиды, карбапенемы), при микоплазменной и хламидийной инфекциях – макролиды.
Посиндромная терапия внутриутробных инфекций направлена на купирование отдельных проявлений перинатального поражения ЦНС, геморрагического синдрома, гепатита, миокардита, пневмонии и т. д.
Прогноз и профилактика
При генерализованных формах внутриутробных инфекций летальность в неонатальном периоде достигает 80%. При локальных формах возникают серьезные поражения внутренних органов (кардиомиопатии, ХОБЛ, интерстициальный нефрит, хронический гепатит, цирроз и т. д.). Практически во всех случаях внутриутробные инфекции приводят к поражению ЦНС.
Профилактика внутриутробных инфекций заключается в проведении предгравидарной подготовки, лечении ЗППП до наступления беременности, исключении контактов беременной с инфекционными больными, коррекции программы ведения беременности у женщин групп риска. Женщины, ранее не болевшие краснухой и не получавшие прививки против краснухи, должны быть вакцинированы не позднее, чем за 3 месяца до предполагаемой беременности. В ряде случаев внутриутробные инфекции могут являться основанием для искусственного прерывания беременности.
Читайте также:

