Инфекция после операции на легком
Обновлено: 19.04.2024
Частота бронхиальных свищей. Эмпиема плевры после операции на легком
Бронхиальные свищи представляют собой частое осложнение после резекции легкого, заметно удлиняющее послеоперационный период и нередко оказывающее серьезное влияние на исход операции.
Ф. X. Кутушев из клиники П. А. Куприянова приводит данные, касающиеся бронхиальных свищей, наблюдаемых у больных после резекции легкого. После 230 радикальных операций, в том числе 190 пневмэктомий и 40 лобэктомий, у 38 больных были бронхиальные свищи (16,5%), в том числе при лобэктомиях 9(22%) и при пневмэктомиях 29 (15,2%). При нагноительных заболеваниях после 162 операций наблюдались бронхиальные свищи 34 раза (20,9%), из 68 больных раком после операции бронхиальные свищи встретились 4 раза.
Наши данные очень близки к данным Ф. X. Кутушева. На 170 операций резекции, проведенных нами, наблюдалось 24 больных с бронхиальными свищами, т. е. 14%. При этом с приобретением большего опыта количество бронхиальных свищей заметно уменьшается.
Так, если на 62 резекции, о которых говорилось в первом издании книги, мы наблюдали 14 больных с бронхиальными свищами, т. е. 22,5%, то на 108 операций, произведенных с 1950 г., было 10 больных с бронхиальными свищами, или 9,1%. На 109 резекций по поводу гнойных заболеваний встретилось 20 больных с бронхиальными свищами, или 18%, а при раках — 4 на 61 резекцию. При лобэктомиях бронхиальные свищи были в 24,3, а при пневмэктомиях — в 6%.
Бронхиальные свищи, образовавшиеся после лобэктомий, как правило, заживают самостоятельно и не требуют их оперативного закрытия. После пневмэктомий они редко закрываются самостоятельно и, как правило, требуют торакопластики с мышечной пластикой. Из 19 больных с бронхиальными свищами после лобэктомий только у 2 была произведена торакопластика с мышечной пластикой. При пневмэктомиях бронхиальные свищи у больных требуют для излечения, как правило, торакопластики.
Кроме того, у этих больных отмечается высокая смертность вскоре же после образования бронхиального свища: из 6 больных с бронхиальными свищами после пневмэктомий умерло 4, в том числе 3 в первые 6 недель после операции.
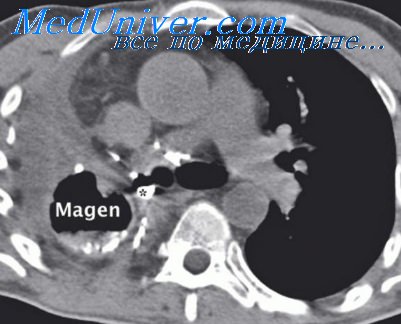
Эмпиема плевры после операции на легком
При резекции легких, как бы асептично она ни была сделана, имеются все предпосылки для развития инфекции в остаточной плевральной полости. Даже при всей осторожности оператора рассечение бронха приводит к тому, что инфекция в каком-то количестве попадает в плевральную полость. При лобэктомий во время рассечения междолевой плевры почти всегда ранят легочную паренхиму, которая часто бывает инфицирована, и инфекция легко может попасть в плевральную полость.
Во время пневмэктомий при рассечении спаек также можно легко поранить легочную паренхиму, где в случаях гнойных заболеваний легкого даже в поверхностных слоях гнездится инфекция в большом количестве. И, наконец, в самих спайках находится разнообразная инфекция. Посевы кусочков плевральных спаек на различных средах давали богатый рост разнообразной, типичной для легочной инфекции, флоры.
Все это создает благоприятные условия для послеоперационного развития эмпиемы. Плевра оказывает серьезное сопротивление развитию инфекции, и нагноение обычно наблюдается там, где грубо нарушена асептика, где имеется прямое инфицирование плевральной полости, а главное, где остается источник для продолжающегося инфицирования.
При турникетном способе резекции, когда все разрезы проходят через легочную ткань, инфицированную в послеоперационном периоде, развивается инфекция культи корня легкого с последующей эмпиемой. При раздельном лигировании элементов корня легкого удаляют всю пораженную легочную ткань и тем самым — источник инфекции. Но для борьбы с той инфекцией, которая уже попала в плевральную полость, необходимо создать максимум благоприятных условий.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Внутрибольничная пневмония – это легочная инфекция, развившаяся спустя двое и более суток после поступления больного в стационар, при отсутствии признаков заболевания на момент госпитализации. Проявления внутрибольничной пневмонии аналогичны таковым при других формах воспаления легких: лихорадка, кашель с мокротой, тахипноэ, лейкоцитоз, инфильтративные изменения в легких и т. п., однако могут быть слабо выраженными, стертыми. Диагноз основывается на клинических, физикальных, рентгенологических и лабораторных критериях. Лечение внутрибольничной пневмонии включает адекватную антибиотикотерапию, санацию дыхательных путей (лаваж, ингаляции, физиометоды), инфузионную терапию.
МКБ-10
Общие сведения
Внутрибольничная (нозокомиальная, госпитальная) пневмония – приобретенная в стационаре инфекция нижних дыхательных путей, признаки которой развиваются не ранее 48 часов после поступления больного в лечебное учреждение. Нозокомиальная пневмония входит в тройку самых распространенных внутрибольничных инфекций, уступая по распространенности лишь раневым инфекциям и инфекциям мочевыводящих путей. Внутрибольничная пневмония развивается у 0,5-1% больных, проходящих лечение в стационарах, а у пациентов отделений реанимации и интенсивной терапии встречается в 5-10 раз чаще. Летальность при внутрибольничной пневмонии чрезвычайно высока – от 10-20% до 70-80% (в зависимости от вида возбудителя и тяжести фонового состояния пациента).
Причины
Основная роль в этиологии внутрибольничной бактериальной пневмонии принадлежит грамотрицательной флоре (синегнойной палочке, клебсиелле, кишечной палочке, протею, серрациям и др.) – эти бактерии обнаруживаются в секрете дыхательных путей в 50-70% случаев. У 15-30% пациентов ведущим возбудителем выступает метициллинрезистентный золотистый стафилококк. За счет различных приспособительных механизмов названные бактерии вырабатывают устойчивость к большинству известных антибактериальных средств. Анаэробы (бактериоды, фузобактерии и др.) являются этиологическими агентами 10-30% внутрибольничных пневмоний. Примерно у 4% пациентов развивается легионеллезная пневмония – как правило, она протекает по типу массовых вспышек в стационарах, причиной которых служит контаминация легионеллами систем кондиционирования и водоснабжения.
Значительно реже, чем бактериальные пневмонии, диагностируются нозокомиальные инфекции нижних дыхательных путей, вызванные вирусами. Среди возбудителей внутрибольничных вирусных пневмоний ведущая роль принадлежит вирусам гриппа А и В, РС-вирусу, у больных с ослабленным иммунитетом – цитомегаловирусу.
Общими факторами риска инфекционных осложнений со стороны дыхательных путей служат длительная госпитализация, гипокинезия, бесконтрольная антибиотикотерапия, пожилой и старческий возраст. Существенное значение имеет тяжесть состояния больного, обусловленная сопутствующими ХНЗЛ, послеоперационным периодом, травмами, кровопотерей, шоком, иммуносупрессией, комой и пр. Способствовать колонизации нижних дыхательных путей микробной флорой могут медицинские манипуляции: эндотрахеальная интубация и реинтубация, трахеостомия, бронхоскопия, бронхография и пр. Основными путями попадания патогенной микрофлоры в дыхательные пути служат аспирация секрета ротоносоглотки или содержимого желудка, гематогенное распространение инфекции из отдаленных очагов.
Вентилятор-ассоциированная пневмония возникает у больных, находящихся на ИВЛ; при этом каждый день, проведенный на аппаратном дыхании, увеличивает риск развития внутрибольничной пневмонии на 1%. Послеоперационная, или застойная пневмония, развивается у обездвиженных больных, перенесших тяжелые оперативные вмешательства, главным образом, на грудной и брюшной полости. В этом случае фоном для развития легочной инфекции служит нарушение дренажной функции бронхов и гиповентиляция. Аспирационный механизм возникновения внутрибольничной пневмонии характерен для больных с цереброваскулярными расстройствами, у которых отмечаются нарушения кашлевого и глотательного рефлексов; в этом случае патогенное действие оказывают не только инфекционные агенты, но и агрессивный характер желудочного аспирата.
Классификация
По срокам возникновения госпитальная инфекция подразделяется на раннюю и позднюю. Ранней считается внутрибольничная пневмония, возникшая в первые 5 суток после поступления в стационар. Как правило, она вызывается возбудителями, присутствовавшими в организме пациента еще до госпитализации (St. аureus, St. pneumoniae, H. influenzae и др. представителями микрофлоры верхних дыхательных путей). Обычно эти возбудители проявляют чувствительность к традиционным антибиотикам, а сама пневмония протекает более благоприятно.
Поздняя внутрибольничная пневмония манифестирует через 5 и более дней стационарного лечения. Ее развитие обусловлено собственно госпитальными штаммами (метициллинрезистентным St. аureus, Acinetobacter spp., P. аeruginosa, Enterobacteriaceae и др.), проявляющими высоковирулентные свойства и полирезистентность к противомикробным препаратам. Течение и прогноз поздней внутрибольничной пневмонии весьма серьезны.
С учетом причинных факторов выделяют 3 формы нозокомиальной инфекции дыхательных путей:
При этом довольно часто различные формы наслаиваются друг на друга, еще в большей степени утяжеляя течение внутрибольничной пневмонии и увеличивая риск летального исхода.
Симптомы внутрибольничной пневмонии
Особенностью течения внутрибольничной пневмонии является стертость симптомов, из-за чего распознавание легочной инфекции бывает затруднительным. В первую очередь, это объясняется общей тяжестью состояния больных, связанной с основным заболеванием, хирургическим вмешательством, пожилым возрастом, коматозным состоянием и т. п.
Тем не менее, в ряде случаев заподозрить внутрибольничную пневмонию можно на основании клинических данных: нового эпизода лихорадки, увеличения количества мокроты/трахеального аспирата или изменение их характера (вязкости, цвета, запаха и пр.). Больные могут предъявлять жалобы на появление или усиление кашля, одышки, болей в грудной клетке. У пациентов, находящихся в тяжелом или бессознательном состоянии следует обратить внимание на гипертермию, увеличение ЧСС, тахикардию, признаки гипоксемии. Критериями тяжелого инфекционного процесса в легких служат признаки выраженной дыхательной (ЧД > 30/мин.) и сердечно-сосудистой недостаточности (ЧСС > 125/мин., АД < 100/60 мм рт. ст.), нарушение сознания, двустороннее или мультилобарное поражение легких и др. При этом необходимо исключить возможные неинфекционные причины кардиопульмональных расстройств: пневмоторакс, острый респираторный дистресс-синдром, отек легких, ТЭЛА, инфаркт легкого и др. Осложнениями внутрибольничной пневмонии чаще всего становятся абсцесс легкого, эмпиема плевры, сепсис.
Диагностика
Полное диагностическое обследование при подозрении на внутрибольничную пневмонию строится на сочетании клинических, физикальных, инструментальных (рентгенография легких, КТ грудной клетки), лабораторных методов (ОАК, биохимический и газовый состав крови, бакпосев мокроты).
Для выставления соответствующего диагноза пульмонологи руководствуются рекомендуемыми критериями, включающими в себя: лихорадку выше 38,3°С, усиление бронхиальной секреции, гнойный характер мокроты или бронхиального секрета, кашель, тахипноэ, бронхиальное дыхание, влажные хрипы, инспираторную крепитацию. Факт внутрибольничной пневмонии подтверждается рентгенологическими признаками (появлением свежих инфильтратов в легочной ткани) и лабораторными данными (лейкоцитозом >12,0х10 9 /л, палочкоядерным сдвигом >10%, артериальной гипоксемией Ра02< 60 мм рт. ст., Sa02 < 90%.).
С целью верификации вероятных возбудителей внутрибольничной пневмонии и определения антибиотикочувствительности производится микробиологическое исследование секрета трахеобронхиального дерева. Для этого используются не только образцы свободно откашливаемой мокроты, но и трахеальный аспират, промывные воды бронхов. Наряду с культуральным выделение возбудителя, широко применяется ПЦР-исследование.
Лечение внутрибольничной пневмонии
Сложность лечения внутрибольничной пневмонии заключается в полирезистентности возбудителей к противомикробным препаратам и тяжести общего состояния больных. Практически во всех случаях первоначальная антибиотикотерапия является эмпирической, т. е. начинается еще до микробиологической идентификации возбудителя. После установления этиологии внутрибольничной пневмонии может быть произведена замена препарата на более действенный в отношении выявленного микроорганизма.
Препаратами выбора при внутрибольничной пневмонии, вызванной E.Coli и K. pneumoniae, служат цефалоспорины III-IV поколения, ингибиторзащищенные пенициллины, фторхинолоны. Синегнойная палочка чувствительна к сочетанию цефалоспоринов III-IV поколения (или карбапенемов) с аминогликозидами. Если госпитальные штаммы представлены St. аureus, требуется назначение цефазолина, оксациллина, амоксициллина с клавулановой кислотой и т. д. Для терапии аспергиллеза легких используется вориконазол или каспофунгин.
В начальном периоде предпочтителен внутривенный путь введения препарата, в дальнейшем при положительной динамике возможен переход на внутримышечные инъекции либо пероральный прием. Продолжительность курса антибиотикотерапии у пациентов с нозокомиальной пневмонией составляет 14-21 день. Оценка эффективности этиотропной терапии проводится по динамике клинических, лабораторных и рентгенологических показателей.
Кроме системной антибиотикотерапии, при внутрибольничной пневмонии важное внимание уделяется санации дыхательных путей: проведению бронхоальвеолярного лаважа, ингаляционной терапии, трахеальной аспирации. Больным показан активный двигательный режим: частая смена положения и присаживание в постели, ЛФК, дыхательные упражнения и т. п. Дополнительно проводится дезинтоксикационная и симптоматическая терапия (инфузии растворов, введение и прием бронхолитиков, муколитиков, жаропонижающих препаратов). Для профилактики тромбозов глубоких вен назначается гепарин или ношение компрессионного трикотажа; с целью предупреждения стрессовых язв желудка используются Н2-блокаторы, ингибиторы протонной помпы. Пациентам с тяжелыми септическими проявлениями может быть показано введение внутривенных иммуноглобулинов.
Прогноз и профилактика
Клиническими исходами внутрибольничной пневмонии могут быть разрешение, улучшение, неэффективность терапии, рецидив и летальный исход. Внутрибольничная пневмония является главной причиной смертности в структуре внутрибольничных инфекций. Это объясняется сложностью ее своевременной диагностики, особенно у пожилых, ослабленных больных, пациентов, пребывающих в коматозном состоянии.
Профилактика внутрибольничной пневмонии базируется на комплексе медицинских и эпидемиологических мероприятий: лечении сопутствующих очагов инфекции, соблюдении санитарно-гигиенического режима и инфекционного контроля в ЛПУ, предупреждении переноса возбудителей медперсоналом при проведении эндоскопических манипуляций. Чрезвычайно важна ранняя послеоперационная активизация пациентов, стимуляция откашливания мокроты; тяжелые больные нуждаются в адекватном туалете ротоглотки, постоянной аспирации трахеального секрета.
1. Нозокомиальная пневмония у взрослых (Национальные рекомендации)/ под ред. Чучалина А.Г., Гельфанда Б.Р.//Клиническая микробиология и антимикробная химиотерапия. - 2009 - Т.11, №2.
Что такое аспирационная пневмония? Причины возникновения, диагностику и методы лечения разберем в статье доктора Яковлевой Марины Геннадьевны, пульмонолога со стажем в 22 года.
Над статьей доктора Яковлевой Марины Геннадьевны работали литературный редактор Елизавета Цыганок , научный редактор Елена Лобова и шеф-редактор Маргарита Тихонова

Определение болезни. Причины заболевания
Аспирационная пневмония (Aspiration pneumonia) — это воспаление лёгочной ткани, которое развивается после массивного проникновения в дыхательные пути посторонних веществ (аспирата). Сопровождается симптомами обычной пневмонии, а также выделением мокроты с неприятным запахом [4] .

Аспирационная пневмония возникает при 10 % внебольничной и 25 % внутрибольничной пневмонии. При этом смертность от аспирационной пневмонии выше, так как её возбудители (бактерии кишечной группы и анаэробы ротовой полости) вызывают более тяжёлое течение болезни, чем возбудители типичной пневмонии [2] [3] [8] [10] . При этом доказано, что аспирация происходит у 45–50 % здоровых людей и у 70 % пожилых пациентов старше 75 лет с нарушением сознания.
Причины и факторы риска аспирационной пневмонии
Аспиратом может выступать содержимое желудка и носоглотки, околоплодные воды у новорождённых, рвотные массы, зубы (чаще искусственные) и содержимое рта при стоматологических манипуляциях, жидкости, мелкие предметы и остатки пищи. Если в дыхательные пути проникают масла или нефтепродукты низкой вязкости, например технический вазелин, развивается липоидная аспирационная пневмония. В организм эти вещества попадают при вдохе, однако не каждая аспирация провоцирует пневмонию.
Аспирационная пневмония проявляется по-разному: она может пройти бессимптомно или вызывать острую дыхательную недостаточность вплоть до летального исхода [2] .
Чаще всего типичную пневмонию вызывает именно аспирация, однако помимо неё есть множество других факторов, например число бактерий, попавших в бронхи, и состояние защитных сил организма. Непосредственно аспирационную пневмонию диагностируют, когда аспирация сопровождается следующими факторами риска:
- неврологическими болезнями с нарушением сознания и судорожным синдромом, например эпилепсией и комой;
- черепно-мозговой травмой с потерей сознания;
- болезнями желудка, например г астроэзофагеальным рефлюксом и гастритом с пониженной кислотностью; ;
- любой операцией под общим наркозом;
- тяжёлой пневмонией и любыми другими патологическими состояниями с остановкой дыхания, которые требуют интубации трахеи и искусственной вентиляции лёгких.

Самая частая причина аспирации — это дисфагия (нарушение нормального глотания). Её могут вызвать кома, наркоз, судороги и инсульт. При дисфагии содержимое носоглотки и желудка затекает в дыхательные пути, то есть происходит аспирация. Если она массивная, то это приводит к быстрому развитию аспирационной пневмонии [3] .
Болезни желудочно-кишечного тракта, при которых плохо сокращаются мышцы (например, гастроэзофагеальный рефлюкс и болезни пищевода), также являются частыми причинами развития аспирационной пневмонии. При гастроэзофагеальном рефлюксе пищу и желудочный сок забрасывает в верхние отделы ЖКТ и далее в дыхательные пути, что приводит к аспирационной пневмонии. Риск увеличивается, когда человек лежит на спине [6] .

Такой же процесс, как и при рефлюксе, протекает при использовании назогастрального зонда. Его вводят людям, которые не могут самостоятельно принимать пищу, например после обширной операции или при кишечной непроходимости. Он не даёт нижнему сфинктеру пищевода закрыться, и пища попадает в дыхательные пути с последующим развитием аспирационной пневмонии.
В группе риска также находятся люди, злоупотребляющие алкоголем. Это связано с рвотой и тем, что они не могут контролировать себя при алкогольном опьянении.
Кроме того, спровоцировать аспирационную пневмонию могут кариес, плохая гигиена и сухая слизистая рта. Они меняют состав слюны, повышают концентрацию патологической микрофлоры во рту и способствуют развитию воспаления, которое может перейти в дыхательные пути [7] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы аспирационной пневмонии
Характерной особенностью такой пневмонии является постепенное начало: симптомы обычно проявляются через 8–14 дней после аспирации.
Важный отличительный признак — это появление мокроты с неприятным, гнилостным запахом и иногда с примесью крови.
Другие проявления похожи на симптомы обычной пневмонии: кашель, одышка, боли в грудной клетке, повышение температуры тела от 37,5 до 39–40 °С. При хронической аспирации кашель и одышка могут возникать только после еды.
Обычно самочувствие ухудшается постепенно в течение нескольких дней. Больной чувствует слабость и теряет аппетит, что приводит к снижению веса [6] .
Иногда аспирационная пневмония протекает почти бессимптомно с небольшим подъёмом температуры, хрипами и постепенной потерей веса. Её выявляют случайно, когда человек болеет хронической аспирацией из-за другой патологии [3] .
При липоидной аспирационной пневмонии больной может только храпеть, поэтому, чтобы определить болезнь, нужна рентгенограмма. В таком случае рентген показывает разные изменения, например медленно развивающиеся уплотнения, узловые скопления различных веществ или воспаление плевры.
Патогенез аспирационной пневмонии
Аспирационная пневмония — это инфекционно-токсическое воспаление лёгких, тяжесть которого зависит не только от количества и агрессивности вредных микроорганизмов, но и от защитных механизмов дыхательных путей и организма в целом.
Лёгкие — это парный орган, который обеспечивает обмен углекислого газа и кислорода в организме. В правом лёгком есть три доли, в левом – две. Эти доли делятся на сегменты. К каждому лёгкому подходят бронхи, которые на концах переходят в альвеолы. Именно в них происходит газообмен.
Каждое лёгкое защищает специальная оболочка — плевра. Она состоит из двух листков: один присоединяется к грудной клетке (париетальный), другой выстилает наружную часть лёгкого (висцеральный). Между ними есть полость, где содержится небольшое количество жидкости, которое предотвращает трение листков плевры при дыхании.
Все дыхательные пути также выстланы защитным эпителием, при этом большую часть занимает реснитчатый эпителий. В нижних отделах эпителий не содержит реснички, но в нём располагаются бокаловидные железы, которые производят защитную слизь. Клетки эпителия не дают раздражающим веществам оставаться на поверхности дыхательных путей.
Аспирация механически и химически воздействует на ткани, блокирует работу эпителия и повреждает защитные механизмы очищения дыхательных путей. Например, аспирация желудочного сока вызывает химический ожог дыхательных путей, что приводит к бронхоспазму, спаданию лёгочной ткани, отёку и альвеолярному кровотечению. Таким образом она создаёт благоприятные условия для размножения микроорганизмов и развития воспаления в лёгочной ткани (пневмонии).
Если аспирация привела к развитию воспаления в лёгочной ткани, организм запускает защитный механизм, который ограничивает очаг воспаления, поэтому в большинстве случаев пневмония является односторонней и не выходит за рамки одного сегмента. Однако при тяжёлой форме воспаление распространяется на другие сегменты или даже долю лёгкого.
Часто при аспирационной пневмонии в лёгком образуется полость со скоплением гноя — абсцесс. Это происходит, когда в развитии воспаления участвует особенная анаэробная микрофлора. Она формируется в распадающейся ткани и той части организма, где снижено содержание кислорода. Такая микрофлора способствует скоплению гноя.
Если в процесс вовлекается плевра, пневмония осложняется плевритом (воспалением плевры), а при накоплении гноя между листками может развиться эмпиема плевры (гнойный плеврит). В самых тяжёлых случаях инфекция проникает в кровь и начинается сепсис, так называемое заражение крови [4] .

Можно выделить несколько основных патогенетических механизмов, которые приводят к аспирационной пневмонии:
- механическая закупорка дыхательных путей;
- химическое повреждение;
- бактериальная пневмония [1] .
Микроаспирация слизи из носоглотки обычно не вызывает никаких осложнений и выводится с кашлем. Но это правило работает, если человек здоров: защитные механизмы организма работают нормально, слизистая хорошо очищает бронхи и нет никаких факторов риска для развития аспирации.
Если аспирата слишком много или в нём содержатся твёрдые частицы, организм не всегда может с ним справится, так как он перекрывает дыхательные пути. При этом аспират не откашливается, а проникает в нижние отделы дыхательных путей, закупоривает бронхи и бронхиолы, что приводит к застою бронхиального секрета и слизи. Так формируется благоприятная среда для активации и размножения микроорганизмов и развития воспаления.
Воспалительная реакция, возникшая в бронхах, постепенно распространяется в нижние отделы лёгких и достигает альвеол. В этом случае речь идёт об ограниченном воспалении — очаге (очаговой пневмонии). При неблагоприятном течении очаги могут сливаться, тогда воспаление поражает сегмент, долю или всё лёгкое.
Чем больше площадь поражения лёгкого, тем ярче выражены симптомы дыхательной недостаточности, которая развивается после того, как альвеолы больше не могут проводить газообмен. Пациенту с дыхательной недостаточностью тяжело дышать, у него появляется одышка и другие признаки болезни [1] [9] .
При аспирационной пневмонии место воспаления зависит от положения тела больного в момент аспирации. Если аспирация произошла, когда человек лежал, аспирационная пневмония с большей вероятностью проявится в задних сегментах верхних долей или верхних сегментах нижних долей. Если человек стоял, то болезнь обычно развивается в нижних долях.
Классификация и стадии развития аспирационной пневмонии
В зависимости от места возникновения аспирационную пневмонию делят на:
- внебольничную;
- внутрибольничную (госпитальную).
Можно выделить следующие этапы развития аспирационной пневмонии:
- Пневмония
- Некротизирующая пневмония (формирование очага разрушения) – повышается температура тела, появляется боль в грудной клетке и признаки отравления.
- Абсцесс лёгкого — добавляется сильный кашель с большим количеством гнойной мокроты.
- Эмпиема плевры — присоединяется резкая боль со стороны поражения [2][3] .
Осложнения аспирационной пневмонии
Появление стадии абсцесса лёгкого или эмпиемы плевры — это уже осложнённое течение болезни.
Самым грозным осложнением аспирационной пневмонии является сепсис — нарушение работы внутренних органов, которое вызвано снижением иммунитета на фоне тяжёлой болезни. При сепсисе нарушается деятельность сразу нескольких систем организма (в основном дыхательной и сердечно-сосудистой систем, а также печени и почек), что может привести к летальному исходу [1] .
Ещё одним тяжёлым осложнением аспирационной пневмонии является острый респираторный дистресс-синдром — тип дыхательной недостаточности, при котором пациента нужно срочно госпитализировать в реанимацию.
Диагностика аспирационной пневмонии
Алгоритм диагностики включает в себя сбор анамнеза, характерные жалобы, физикальный осмотр, дополнительные лабораторные и инструментальные обследования.
Диагностика аспирационной пневмонии в первую очередь основывается на самом факте аспирации или факторах риска, которые могли привести к аспирации дыхательных путей. Затем врач обращает внимание на типичные жалобы, включая кашель со зловонной гнойной мокротой, повышение температуры тела, одышку, слабость и снижение аппетита.
Пациент должен обязательно рассказать врачу о фоновых заболеваниях, например о болезнях периодонта, нарушениях глоточного рефлекса, алкоголизме и эпизодах нарушения сознания, в том числе коме, оглушении и т. д. [3]
При физическом обследовании врач измеряет частоту дыхания, насыщенность крови кислородом (сатурацию), частоту сердечных сокращений, артериальное давление, температуру тела, слушает лёгкие и сердце и простукивает грудную клетку. Если на осмотре врач обнаружил характерные признаки пневмонии, например учащённое дыхание, снижение сатурации крови ниже 96 % и крепитирующие, напоминающие хруст, хрипы в одном из лёгких, он отправляет пациента на дополнительное обследование, которое включает в себя лабораторную и инструментальную диагностику.
Лабораторная диагностика
В лабораторную диагностику входит:
- анализ крови с подсчётом лейкоцитарной формулы — наблюдается подъём лейкоцитов и ускорение скорости оседания эритроцитов;
- общий анализ мочи — может показать наличие лейкоцитов и белков;
- биохимический анализ крови — определяет общий белок и белковую фракцию, креатинин, мочевину, глюкозу, печёночные ферменты (АСТ и АЛТ) и СРБ (С-реактивный белок);
- тест на прокальцитонин (по возможности) — его повышение говорит о присоединении бактериальной инфекции.
При сопутствующей патологии сердечно-сосудистой системы могут назначить дополнительные исследования, которые определяют уровень электролитов и газов в крови.
Чтобы определить возбудителя пневмонии и правильно подобрать антибиотик, необходимо также провести микробиологическое исследование мокроты [2] .
Инструментальная диагностика
Среди методов инструментальной диагностики выделяют:
- Рентгенографию органов грудной клетки — выявляет скопление вредных элементов в задних или верхних сегментах нижней доли или заднем сегменте верхней доли, при абсцессе показывает полости.
- Компьютерную томографию органов грудной клетки, как правило, без контрастирования — при подозрении на осложнённое течение пневмонии. С контрастированием — показывает очаги скопления газа или жидкости.
- Пульсоксиметрию — измеряют насыщение крови кислородом.
- Ультразвуковое исследование грудной полости — при подозрении на развитие плеврита.
- Фибробронхоскопию (эндоскопическое исследование бронхов с помощью эндоскопа) — при выделении большого количества гнойной мокроты. С помощью бронхоскопии также проводят биопсию, чтобы точно определить возбудителя инфекции.
- ЭКГ (электрокардиографию) — в случае тяжёлого течения болезни с сопутствующей сердечнно-сосудистой патологией [3] .
- Рентгенографию с контрастированием пищевода жидким барием — чтобы уточнить расстройство глотания при скудной клинической картине болезни.
Дифференциальная диагностика
Прежде всего аспирационную пневмонию необходимо дифференцировать с внебольничной или внутрибольничной бактериальной пневмонией, развитие которой не связано с аспирацией. Дифференциальную диагностику также проводят, чтобы исключить туберкулёзное поражение лёгких.
На стадии образования абсцесса необходимо провести дифференциальную диагностику с периферической формой рака лёгкого, которая развивается в бронхах мелкого калибра. В большинстве случаев диагностика не представляет больших трудностей [1] .
Чтобы исключить тромбоэмболию лёгочной артерии, проводят УЗИ сердца.
Лечение аспирационной пневмонии
Антибактериальные препараты являются главной терапией при лечении аспирационной пневмонии. Выбор того или иного антибиотика зависит от тяжести пневмонии, наличия осложнений и сопутствующих факторов риска, например подключения пациента к искусственной вентиляции лёгких или пневмонии, которая развилась у больного в стационаре [1] .
Если пневмония протекает легко и нет факторов риска, способных ухудшить состояние пациента, возможно амбулаторное лечение под наблюдением участкового врача. В этом случае антибиотики назначают в таблетках.
Когда пневмония протекает тяжело и возникает риск развития осложнений (или они уже проявились), пациента лечат в специализированной больнице и также назначают антибиотики (Карбапенем или Пиперациллин+тазобактам) . Их нужно принимать в течение 2 – 8 недель [7] .
Чтобы вылечить липоидную аспирационную пневмонию, назначают малые дозы противовоспалительных препаратов.
При развитии осложнений, например абсцесса лёгкого, плеврита или эмпиемы плевры, помимо антибактериальной терапии может понадобиться хирургическое лечение, которое включает в себя:
- установку дренажа — для удаления воздуха и жидкости из грудной клетки и введения лекарств в плевральную полость;
- установку катетера — чтобы удалить слизь и облегчить дыхание;
- операции на плевре [2] .
Больным с тяжёлым течением аспирационной пневмонии может понадобиться искусственная вентиляция лёгких или поддержка кислородом.
Прогноз. Профилактика
Прогноз и исход аспирационной пневмонии зависит от тяжести болезни и наличия осложнений. При небольших объёмах аспирата, стабильном общем состоянии и своевременном грамотном лечении прогноз для аспирационной пневмонии чаще всего благоприятный, однако смертность составляет от 13 до 37 %.
Летальность при аспирационном абсцессе лёгких — около 20 %. Прогноз также связан с размером полости абсцесса и его местонахождением (более неблагоприятное — в нижней доле правого лёгкого) [8] [10] . Плохой прогноз может быть связан с неэффективной антибактериальной терапией, наличием бактерий в кровотоке, внутрибольничной инфекцией и сопутствующими болезнями.
Профилактика аспирационной пневмонии
Методы профилактики включают:
- устранение факторов, которые могут привести к аспирации, например лечение гастроэзофагеального рефлюкса;
- профилактику заброса содержимого желудка в дыхательные пути у пациентов с тяжёлой неврологической патологией;
- своевременное посещение стоматолога;
- гигиену полости рта и профилактику кариеса;
- отказ от злоупотребления алкоголем и курения.
Правильный подход к гигиене полости рта и регулярные осмотры у стоматолога могут помочь предотвратить развитие пневмонии или абсцесса у пациентов с рецидивирующей аспирацией.
Механизмы инфицирования плевральной полости. Антибиотикотерапия плевральных осложнений
Вопрос о возможности инфицирования плевральной полости во время операции из плевральных сращений и из поврежденной паренхимы здоровых участков легкого в литературе освещен по-разному. По данным ряда авторов плевральные спайки не содержат микробов и поэтому не могут явиться причиной инфицирования плевральной полости. По нашим данным спайки были инфицированы в 36,3% случаев.
Изучение характера микрофлоры, осуществленное на различных этапах операции показало, что строжайшими мерами соблюдения асептики удается значительно уменьшить обсемененность операционного поля микроорганизмами.
Большую роль в профилактике послеоперационных осложнений играет рациональное, обоснованное применение антибиотиков. В послеоперационном периоде имеются прямые показания для их применения. Исходя из того, что во время операции удаляется основной патологический очаг, содержащий патогенную микрофлору, следовательно количество микроорганизмов значительно уменьшается, основной задачей хирурга является помочь организму мобилизовать силы для борьбы с остающейся микрофлорой. Этому не содействует использование ударных доз любого антибиотика, а особенно антибиотиков широкого спектра действия. Тем более этого нет необходимости делать с целью профилактики инфекции, так как применение больших доз антибиотиков на фоне ослабленного операцией организма ведет к усилению дисбактериоза, развитию и генерализации грибковой инфекции и прямому токсическому влиянию на ткани и органы.
Анализ иммуногенеза у больных с хроническими нагноениями легких позволил нам разработать схему антибиотикотерапии в послеоперационном периоде следующим образом: исключив из применения антибиотики широкого спектра действия, мы назначаем больным пенициллин со стрептомицином или полусинтетические пенициллины, как наименее токсичные и, в применяемых дозах, не влияющие на иммунные реакции организма. Кроме того, за последнее время в связи с их редким использованием, а также иммунизацией и отменой антибиотиков перед операцией, чувствительность к ним возросла в 3—4 раза.
Полусинтетические пенициллины еще не вошли в широкую практику поликлиник и терапевтических отделений. Метициллин и оксациллин назначались не более 1,5—2 млн ЕД в сутки (0,5—1000000 ЕД внутриплеврально и 1000000—внутримышечно). Пенициллин назначался в той же дозировке, но со стрептомицином (1000000).
Антибиотикотерапия проводилась в течение 5—7 дней. Одновременно с этим больным давался сульфапиридазин по схеме и фурагин—К.
Подобная терапия сочеталась с продолжающейся иммунизацией, которая в послеоперационном периоде проводилась следующим образом: после операции мы продолжали введение анатоксина, начиная вновь с первой дозы (0,1) и увеличивали ее в той же последовательности, что и до операции.
Антибиотико- и иммунотерапия осуществлялась на фоне общеукрепляющего лечения, регулярных переливаний крови, плазмы, гамма-глобулина, витаминов.
Применяемые в клинике вышеуказанные методы предоперационной подготовки, операционного и послеоперационного ведения больных позволили значительно снизить число гнойно-воспалительных осложнений — эмпием до 1,2%, пневмоний— до 4%. Бронхиальных свищей и нагноений послеоперационных ран не наблюдалось. Летальных исходов в этой группе больных от гнойно-воспалительных осложнений не было.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

