Инфекция в околоплодных водах у беременных
Обновлено: 11.05.2024
Рассмотрена проблема внутриутробного инфицирования и внутриутробной инфекции (ВУИ) плода, факторы риска внутриутробных инфекций, патогенетические механизмы возникновения, развития и воздействия ВУИ, подходы к диагностике и лечению.
The issue of fetal intrauterine infecting and intrauterine infection (IUI) was considered, as well as the risk factors of intrauterine infections, pathogenic mechanisms of their occurrence, development and effect of IUI, and approaches to the diagnostics and treatment.
Проблема внутриутробной инфекции особо актуальна в современных условиях в связи с распространенностью и тяжестью воспалительных процессов. Проблема внутриутробного инфицирования и внутриутробной инфекции (ВУИ) плода является одной из ведущих в акушерской практике и в перинатологии в связи с высоким уровнем инфицирования беременных, рожениц и родильниц, опасностью нарушения развития плода и рождения больного ребенка. Наличие инфекции у матери является фактором риска ВУИ плода, но не всегда означает его заболевание [1, 5–7, 13].
Внутриутробная инфекция — группа инфекционно-воспалительных заболеваний плода и детей раннего возраста, которые вызываются различными возбудителями, но характеризуются сходными эпидемиологическими параметрами и нередко имеют однотипные клинические проявления. Заболевания развиваются в результате внутриутробного (анте- и/или интранатального) инфицирования плода. При этом в подавляющем большинстве случаев источником инфекции для плода является мать. Истинная частота врожденных инфекций до настоящего времени не установлена, но, по данным ряда авторов, распространенность данной патологии в человеческой популяции может достигать 10%. В структуре перинатальной смертности ВУИ составляет более 30% [1, 5–7].
Кроме этого, ВУИ относятся к тяжелым заболеваниям и во многом определяют уровень младенческой смертности.
Согласно данным многих авторов, причиной внезапной смерти грудных детей является инфекционное заболевание, протекающее без ясной симптоматики. В числе причин или фоновых состояний скоропостижной смерти могут быть ВУИ [2].
Под внутриутробным инфицированием понимают процесс внутриутробного проникновения микроорганизмов к плоду, при котором отсутствуют признаки инфекционной болезни плода. Как правило, инфекционный процесс затрагивает плаценту, в которой развивается плацентит, хориоамнионит и т. д. Диагноз внутриутробного инфицирования у новорожденного устанавливается на основании выделения возбудителя из клеток крови, ликвора и других источников, выявления IgM и низкоавидных IgG в пуповинной крови, а также при морфологическом исследовании плаценты [1, 5–7].
Внутриутробное инфицирование не означает неизбежного развития инфекционного заболевания. Для выявления ВУИ необходимо наличие данных лабораторного исследования в сочетании с клинической картиной инфекционного заболевания. Под ВУИ подразумевают не только процесс распространения инфекционных агентов в организме плода, но и вызванные ими морфофункциональные нарушения различных органов и систем, характерные для инфекционной болезни (сепсис, пневмония, менингит, гепатит и т. д.), возникшей анте- или интранатально и выявляемой пренатально или после рождения [10, 11].
Инфекционно-воспалительные заболевания во время беременности имеют особенности: инфицирование плода и новорожденного может быть вызвано как острой инфекцией матери, так и активацией хронической, персистирующей инфекции во время беременности; большая часть заболеваний беременных, приводящих к внутриматочной инфекции, протекает в латентной или субклинической форме; активация персистирующей инфекции возможна при любом нарушении гомеостаза в организме беременной (стресс, острые респираторные вирусные инфекции, переохлаждение и др.) [1, 2].
Возможный спектр возбудителей внутриутробной инфекции весьма разнообразен и широк. Это бактерии (грамположительные и грамотрицательные; аэробные и анаэробные), грибы, простейшие, внутриклеточные микроорганизмы (микоплазмы, хламидии), вирусы. Чаще всего наблюдается сочетание возбудителей — бактериально-вирусная смешанная инфекция [3, 4, 10, 11].
Зачастую ВУИ ассоциируются с наличием инфекций TORCH — то есть синдромом комплекса. Данный термин образован первыми буквами латинских названий наиболее часто верифицируемых врожденных инфекций: T — токсоплазмоз (Тoxoplasmоsis), R — краснуха (Rubella), С — цитомегалия (Cytomegalia), Н — герпес (Herpes) и О — другие инфекции (Оther). К последним относят сифилис, листериоз, вирусные гепатиты, хламидиоз, ВИЧ-инфекцию, микоплазмоз и др. [9, 11].
Принимая во внимание, что источником инфекции для плода всегда является его мать, особое значение приобретают следующие факторы риска внутриутробных инфекций:
- хронические очаги инфекции в организме матери (в том числе наличие воспалительных заболеваний органов малого таза, урогенитальные инфекции);
- первичное инфицирование во время беременности, активация инфекционного процесса;
- патологическое снижение общего и местного иммунитета;
- наличие экстрагенитальной патологии (анемия, тромбофилии, аутоиммунные заболевания);
- повышение проницаемости плацентарного барьера во II и III триместрах беременности при невынашивании беременности и плацентарной недостаточности;
- отягощенный акушерско-гинекологический диагноз;
- неблагоприятные социально-бытовые факторы [1, 9, 11].
Патогенетические механизмы возникновения, развития и воздействия ВУИ разнообразны и зависят от многих факторов:
- срока беременности, при котором происходит инфицирование (чем раньше, тем прогноз будет более неблагоприятным);
- вида возбудителя, его вирулентности, массивности обсеменения;
- первичности или вторичности инфекционного процесса у беременной;
- путей проникновения инфекции к плоду (восходящий, нисходящий, гематогенный);
- степени распространенности и интенсивности воспалительного процесса;
- состояния организма матери, его иммунологической толерантности.
Влияние инфекции на эмбрион и плод заключается в воздействии комплекса следующих факторов:
- патологическое воздействие микроорганизмов и их токсинов (инфекционное заболевание, гипоксия плода, задержка развития плода);
- нарушение процесса имплантации и плацентации (низкая плацентация, предлежание плаценты);
- снижение метаболических процессов и иммунологической защиты плода [1, 9, 11].
Таким образом, реализуется ли внутриутробное инфицирование в ВУИ или нет, зависит от ряда факторов, которые мы представили выше.
Учитывая неспецифичность клинических проявлений ВУИ во время беременности, диагностика данной патологии в большинстве случаев затруднена и возможна лишь в результате сочетания клинических и лабораторно-диагностических методов обследования.
Клинический метод исследования позволяет выявить различные осложнения гестационного периода, такие как невынашивание беременности и синдром задержки роста плода (СЗРП). Кроме этого, немаловажное значение имеет наличие проявлений инфекции у матери (отит, гайморит, пиелонефрит, цистит и т. д.).
Методы, позволяющие оценить состояние фетоплацентарной системы:
- эхография (плацентометрия, поведенческая активность плода, его тонус, количество околоплодных вод, степень зрелости плаценты);
- допплерография (МПК, ФПК);
- кардиотокография (КТГ).
Микробиологические и серологические исследования:
- микроскопия влагалищных мазков (повышенное содержание лейкоцитов, кокковая флора, признаки дисбиоза, грибковая флора);
- бактериальный посев (наличие анаэробных и аэробных бактерий, грибковой флоры);
- ПЦР-диагностика (геномы ВПГ-1, ВПГ-2, ЦМВ, микоплазмы, уреаплазмы, хламидии);
- иммуноферментный анализ (ИФА): обнаружение в сыворотке специфических антител к возбудителям (IgM, IgG, IgA) в диагностически значимых титрах.
Исследование хориона (биопсия хориона): бактериологический метод, ПЦР-диагностика.
Исследование околоплодных вод (амниоцентез): бактериологический метод, ПЦР-диагностика.
Исследование пуповинной крови плода (кордоцентез): бактериологический метод, ПЦР-диагностика и специфический иммунный ответ (IgM) плода.
Морфологическое исследование плаценты, данные аутопсии.
Предположительный диагноз внутриутробного инфицирования и ВУИ помогают поставить косвенные методы:
- наличие у матери клиники инфекционного заболевания;
- наличие специфического иммунного ответа;
- результаты УЗИ, допплерометрии, КТГ.
К прямым методам диагностики внутриутробного инфицирования и ВУИ относятся: выявление возбудителя в материале, полученном при биопсии хориона, амниоцентезе (ПЦР, бактериологический метод), кордоцентезе (ПЦР, бактериологический метод и определение уровня специфических IgM).
Характер течения беременности при внутриутробной инфекции зависит от срока воздействия возбудителя.
На ранних этапах зародыша (1–3 недели беременности) из-за отсутствия механизмов взаимодействия инфекционного агента и плодного яйца реализации воспалительной реакции чаще всего не происходит. Контакт с инфекцией может закончиться альтернативным процессом и гибелью плодного яйца. Повреждение эмбриона инфекцией на 4–12 неделях беременности связано с вирусной инфекцией, проникновением микроорганизмов через хорион. Плод еще не имеет защитных механизмов. Нарушение закладки органов и систем вызывает тератогенный и эмбриотоксический эффект [13, 15].
В I триместре беременности специфических клинических признаков наличия ВУИ нет, косвенно о ней свидетельствуют некоторые эхографические признаки:
- повышенный локальный тонус матки;
- отслойка хориона;
- изменение формы плодного яйца (деформация);
- прогрессирование истмико-цервикальной недостаточности (функционального характера);
- гипоплазия хориона;
- увеличение или персистенция желточного мешка;
- несоответствие размеров эмбриона размерам полости плодного яйца (увеличение, уменьшение);
- отсутствие редукции хорионической полости.
Инфекционные фетопатии возникают с 16-й недели, когда происходит генерализация инфекции у плода. Могут возникать такие пороки развития, как фиброэластоз эндокарда, поликистоз легких, микро- и гидроцефалия (ранние фетопатии) [12–15].
В III триместре плод реагирует на внедрение возбудителя локальной реакцией. Могут возникнуть энцефалит, гепатит, пневмония, интерстициальный нефрит. Влияние вирусов чаще всего проявляется признаками незрелости, дисэмбриогенетическими стигмами, затяжным адаптационным периодом, значительной потерей массы тела в раннем постнатальном периоде. Данные эхографии во II и III триместрах беременности, указывающие на развитие инфекции у плода:
- СЗРП;
- гипоксия плода;
- фетоплацентарная недостаточность;
- многоводие или маловодие;
- неиммунная водянка плода;
- увеличение или уменьшение толщины плаценты, наличие патологических включений;
- контрастирование базальной мембраны;
- наличие взвеси в околоплодных водах;
- кальцификаты в печени и селезенке и головном мозге плода;
- поликистоз легких, почек плода;
- эхогенные фиброзные включения на папиллярных мышцах и створках клапанов сердца плода;
- расширение петель кишечника плода (гипоксия, энтерит) [12–15].
После верификации диагноза ВУИ лечебные мероприятии проводят с помощью этиотропной, антимикробной терапии: препараты пенициллинового ряда и макролиды. Целесообразность назначения антимикробных препаратов не вызывает сомнения, если ВУИ обусловлено наличием патогенных возбудителей (бледная спирохета, токсоплазма, хламидии, гонококк и т. д.) [8, 14].
В настоящее время одним из наиболее дискутабельных вопросов в акушерстве является выяснение истинной этиологической роли генитальных микоплазм (Mycoplasma hominis, Mycoplasma genitalis, Ureaplasma urealyticum) в развитии патологии матери и плода. Инфицирование плода генитальными микоплазмами происходит преимущественно интранатально: в 18–55% — у доношенных новорожденных и в 29–55% — у недоношенных [3, 16, 20].
Актуальность проблемы урогенитального микоплазмоза обусловлена не только значительным распространением этой инфекции в популяции, но и неоднозначностью ее оценки как эпидемиологами, так и клиницистами [16].
По данным различных исследователей, микоплазмы являются возможной причиной развития конъюнктивитов, врожденных пневмоний, респираторного дистресс-синдрома, хронических заболеваний легких, менингита и неонатального сепсиса. Вопрос о терапии микоплазменной инфекции до настоящего времени остается открытым. В схемах терапии предусматривается 7–10-дневные курсы макролидов [1, 3, 21, 22].
Во время беременности противовирусная терапия при генитальном герпесе, цитомегаловирусной инфекции, вирусе ветряной оспы проводится с помощью этиотропных препаратов (ацикловир) начиная со II триместра гестационного периода. Целью лечения является профилактика рецидивирования и антенатального инфицирования [14, 17, 19].
Трихомонадная инфекция относится к группе негонококковых воспалительных заболеваний мочеполовых органов. Лечение трихомониаза во время беременности осуществляется с помощью метронидазол-содержащих препаратов начиная со II триместра гестационного периода [8].
Появление новых методов диагностики, разработка и внедрение новых лекарственных средств не изменяют ситуацию с внутриутробными инфекциями, оставляя это по-прежнему актуальной проблемой в акушерстве. Все это обуславливает неуклонный рост инфекции в человеческой популяции, высокий процент рецидивов инфекции даже у пациентов, получавших курс антибиотикотерапии в соответствии с действующими инструкциями и схемами лечения. Проблема осложняется тем, что в настоящее время отсутствует единая концепция механизма рецидивирования, недостаточно изучена роль микст-инфекции в возникновении, течении и персистировании инфекции, не учитываются особенности гормонального и иммунного статуса больного, не сформированы диагностические критерии контроля излеченности патологического процесса. Это все вместе взятое является стимулом для продолжения исследований, направленных на решение данных проблем. Несмотря на то что роль вирусных и бактериальных инфекций в этиологии и патогенезе многих патологических процессов не вызывает сомнений, вопрос о значении инфекций в качестве моновозбудителя на сегодняшний день окончательно не решен. Актуальным по-прежнему остается вопрос разработки алгоритма лабораторной диагностики заболеваний.
Только совершенствование диагностических подходов, разработка оптимальных алгоритмов и методов обследования и предупреждение распространения резистентных штаммов путем адекватного отношения к каждому пациенту индивидуально (обязательное проведение посевов на определение чувствительности к антибиотикам до назначения терапии) может изменить данную ситуацию.
Исследование выполнено за счет гранта Российского научного фонда (проект № 15-15-00109).
Литература
В. Н. Кузьмин 1 , доктор медицинских наук, профессор
К. Н. Арсланян, кандидат медицинских наук
Э. И. Харченко, кандидат медицинских наук
ГБОУ ВПО МГМСУ им. А. И. Евдокимова МЗ РФ, Москва
Хориоамнионит — это инфекционное воспаление плодных оболочек и амниотической жидкости, вызванное полимикробными ассоциациями. Проявляется гипертермией, болью в области матки, гнойными или сукровичными выделениями из влагалища. Возможно субклиническое течение заболевания с минимальной симптоматикой. Диагностируется с помощью гинекологического осмотра, КТГ плода, лабораторных исследований, УЗИ малого таза. Тактика ведения беременной предполагает срочное родоразрешение через естественные родовые пути или путем кесарева сечения с одновременным назначением интенсивной антибактериальной, противовоспалительной, инфузионной терапии.
МКБ-10
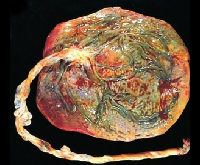
Общие сведения
Хориоамнионит (интраамниотическая инфекция, амниотический инфекционный синдром) чаще возникает во II триместре и, по данным разных авторов, выявляется у 0,9-10,5% беременных. Развитие заболевания в III триместре обычно связано с длительным безводным периодом после преждевременного излития вод. Патологию чаще обнаруживают у женщин, страдающих хроническими генитальными и экстрагенитальными инфекциями. Актуальность своевременной диагностики и лечения антенатального инфицирования обусловлена тем, что хориоамнионит является одной из наиболее распространенных причин преждевременного прерывания беременности, повышает вероятность возникновения угрожающих жизни осложнений для плода и женщины.

Причины хориоамнионита
Воспаление окружающих плод оболочек — полимикробное инфекционное заболевание, вызванное ассоциацией из двух и более патогенных или условно-патогенных микроорганизмов. Непосредственными возбудителями хориоамнионита могут стать стрептококки группы В, пептострептококки, стафилококки, кишечные палочки, микоплазмы, уреаплазмы, энтерококки, хламидии, трихомонады, гонококки, гарднереллы, кандиды, бактероиды, вирус простого герпеса, цитомегаловирус и др. Для начала воспалительного процесса, как правило, требуется сочетание нескольких предрасполагающих условий, основными из которых являются:
- Наличие инфекционного очага. Инфицирование амниотических оболочек обычно происходит восходящим путем. Риск развития хориоамнионита повышается при наличии бактериального вагиноза, вульвовагинита, кольпита, эндоцервицита, эндометрита. Нисходящее инфицирование возможно при сальпингитах, оофоритах, аднекситах. Не исключен гематогенный занос микроорганизмов из существующих экстрагенитальных очагов хронической инфекции.
- Доступ к матке и плодному пузырю. В 98% случаев физиологической беременности амниотическая жидкость стерильна. От инфицирования ее защищают плодные оболочки и слизь, замыкающая канал шейки матки. Действие этих защитных механизмов ослабляется при истмико-цервикальной недостаточности, подтекании околоплодных вод, разрыве плодного пузыря. Вероятность воспаления особенно возрастает в родах с безводным промежутком более 24 часов.
- Инвазивные диагностические и лечебные манипуляции. В некоторых случаях при осложненном течении беременности, подозрении на аномалии развития или болезни плода выполняют исследования с проникновением в полость матки и плодный пузырь. Наиболее опасными в плане развития хориоамнионита являются амниоскопия, амниоцентез, кордоцентез, плацентоцентез. Инфицирование также возможно в ходе амниоинфузии и внутриутробного переливания крови.
- Снижение иммунитета. Более активное размножение условно-патогенных и патогенных микроорганизмов происходит при ослаблении защитных сил организма. Провоцирующими факторами иммунной недостаточности становятся простудные заболевания, обострения экстрагенитальной патологии, длительные или интенсивные физические и психические нагрузки, прием медикаментов с прямым или вторичным иммуносупрессорным эффектом.
Риск возникновения хориоамнионита также возрастает с началом естественных родов, особенно если в их ходе многократно проводятся пальцевые влагалищные исследования после вскрытия плодных оболочек или выполняется внутренняя кардиотокография плода для получения объективных данных о его состоянии и характеристиках сократительной активности матки.
Патогенез
При нормальном течении беременности развитию воспалительных изменений в хорионе и других плодных оболочках препятствуют естественные плацентарные механизмы защиты, представленные несколькими видами Toll-подобных рецепторов, которые определяют присутствие лигандов микроорганизма и инициируют протективную реакцию в ответ на повреждение эпителия. Выделение дефензинов, секреторных лейкоцитарных ингибиторов протеиназ, элафинов способствует лизису бактерий и инактивации их повреждающих факторов. Массивное восходящее, нисходящее или гематогенное поступление инфекционных агентов провоцирует срыв местного иммунитета, а вырабатываемые ими протеазы разрушают волокна коллагена, входящего в состав плодных оболочек, оказывают прямое повреждающее действие на плаценту.
Опосредованные эффекты, способствующие развитию воспалительного процесса при хориоамнионите, связаны с выделением цитотоксичных цитокинов и матриксных металлопротеаз, апоптозом. Повышенная концентрация микробных фосфолипаз в околоплодной жидкости способствует усиленному синтезу простагландинов из тканевых фосфолипидов, что сопровождается преждевременным началом родовой деятельности. Заглатывая инфицированную амниотическую жидкость, плод внутриутробно заражается. Более чем в 80% случаев заболевания страдает фетоплацентарный комплекс – воспаление распространяется на межворсинчатое пространство, тромбируются сосуды базальной децидуальной оболочки.
Классификация
При систематизации клинических форм хориоамнионита учитывают течение патологического процесса — скорость его развития и выраженность клинических проявлений. С остротой воспаления напрямую связаны морфологические изменения, происходящие в тканях околоплодных оболочек, и вероятность возникновения осложнений. Специалисты в сфере акушерства и гинекологии, различают два вида хориоамнионита:
- Острый. Наиболее распространенная форма заболевания. Воспаление развивается быстро, проявляется выраженной симптоматикой. В оболочках, окружающих плод, формируются лейкоцитарные инфильтраты, в процесс обычно вовлечены плацента, хорион, амнион, пуповина. Характерно поражение сосудов в виде хориональных васкулитов, фуникулита.
- Хронический. Наблюдается крайне редко, преимущественно у пациенток с герпесом, сифилисом, токсоплазмозом. Сочетается с артериальной гипертензией, сахарным диабетом, Rh-конфликтом. Определяется по наличию осложнений. Морфологически обнаруживается лимфоцитарная инфильтрация внеплацентарных оболочек и хронический виллит.
Симптомы хориоамнионита
При остром течении заболевания у беременной появляются боли различной интенсивности в нижней части живота. Она могут иррадиировать в паховую область, крестец, усиливаться при прощупывании матки через переднюю брюшную стенку. Температура тела зачастую повышена до 38° С и выше, у пациентки возникает выраженный озноб, пульс учащается до 100 сокращений в минуту и выше. Общее самочувствие женщины ухудшается, она испытывает слабость, быструю утомляемость. Могут наблюдаться патологические влагалищные выделения с неприятным запахом — серо-зеленые (гнойные) или с примесью крови. В ряде случаев хориоамнионит протекает бессимптомно и диагностируется после внезапно прервавшейся беременности или по наличию характерных осложнений послеродового периода.
Осложнения
Наиболее серьезными осложнениями хориоамнионита являются фетоплацентарная недостаточность, преждевременный разрыв плодных оболочек, отслоение нормально расположенной плаценты, досрочные роды во 2-3 триместрах. У таких беременных чаще возникают бактериемия, слабость родовой деятельности, атонические послеродовые кровотечения, тромбоэмболии, послеродовые эндометриты, акушерские перитониты, тазовые абсцессы, инфекционные осложнения травматических ран, полученных в родах. Возможны коагулопатии, септический шок, респираторный дистресс-синдром.
Нарушение нормального функционирования фетоплацентарного комплекса при хориоамнионите может спровоцировать задержку развития плода. У новорожденных повышен риск получения травм в родах, развития врожденных неонатальных инфекций (пневмонии, сепсиса, менингита), церебрального паралича и смерти.
Диагностика
Поскольку хориоамнионит представляет серьезную угрозу дальнейшему течению беременности, при подозрении на развитие заболевания все обследования выполняются в экстренном порядке. Диагностический поиск направлен на выявление признаков локального воспаления околоплодных оболочек, оценку состояния плода и определение возможных возбудителей. Наиболее информативны для постановки диагноза:
- Осмотр на кресле. Бимануальное влагалищное исследование позволяет обнаружить болезненность маточной стенки, расширение цервикального канала. За счет отека тканей размеры беременной матки могут быть больше гестационного срока. При осмотре в зеркалах заметны характерные выделения.
- Кардиотокография плода. Признаком нарушения работы фетоплацентарного комплекса и возможного внутриутробного инфицирования ребенка при хориоамнионите считается компенсаторная тахикардия. Частота сердечных сокращений плода при воспалении оболочек превышает 160 ударов в минуту.
- Лабораторные анализы. Типичными лабораторными признаками расстройства являются лейкоцитоз свыше 15∙10 9 /л и ускорение СОЭ в общем анализе крови. Об общевоспалительных изменениях также свидетельствует сдвиг лейкоцитарной формулы влево. Уровень C-реактивного белка превышает 5,0 мг/л.
- УЗИ матки и плода. УЗ-критерии хориоамнионита включают утолщение плацентарной ткани, расширение межворсинчатого и субхориального пространств. Хориальная пластинка обычно гипоэхогенна. Выявляются признаки преждевременного созревания плаценты, изменено количество и качество околоплодных вод.
- Бактериологические исследования. Микроскопия и бактериальный посев влагалищного мазка дают возможность определить возможных возбудителей инфекционно-воспалительного процесса. По показаниям микробиологические анализы дополняют специальными методами выявления инфекций (РИФ, ИФА, ПЦР).
Дополнительными признаками воспалительного поражения плодных оболочек служат падение уровня эстриола, увеличение содержания хорионического гонадотропина, усиление тромбоагрегации в сочетании с нарушениями плазменного звена гемостаза. После родов наличие воспаления обнаруживается при гистологическом исследовании плодных оболочек. Дифференциальная диагностика проводится с эндометритом, другими воспалительными заболеваниями репродуктивных органов, острой хирургической патологией брюшной полости. При необходимости назначают консультации хирурга, инфекциониста, уролога, неонатолога.
Лечение хориоамнионита
Воспаление оболочек плода является показанием для экстренной госпитализации беременной и ее перевода на постельный режим. Тактика ведения пациентки предполагает как можно более быстрое родоразрешение (стимулированные роды или кесарево сечение) с назначением массивной антибактериальной и симптоматической терапии, которые продолжаются в послеродовом периоде. Выбор метода родоразрешения зависит от выраженности воспалительных изменений, срока безводного периода (при преждевременном излитии околоплодных вод), состояния женщины и плода. Схема медикаментозного лечения направлена на решение таких терапевтических задач, как:
- Борьба с инфекционными агентами. Обычно при хориоамнионите еще до получения результатов антибиотикограммы применяют антибиотики широкого спектра действия, воздействующие в том числе на хламидии и микоплазмы. В последующем возможна коррекция назначений в зависимости от чувствительности флоры.
- Профилактика осложнений антибиотикотерапии. С учетом фаркотерапевтических и фармакодинамических характеристик антибактериальных средств пациентке могут быть рекомендованы противогистаминные, противокандидозные препараты. Для восстановления нормальной микрофлоры используют эубиотики.
- Инфузионная терапия. При выраженных нарушениях гемодинамики, признаках общей интоксикации назначают дезинтоксикационные, коллоидные и солевые растворы. По показаниям возможно капельное введение препаратов, улучшающих сердечную деятельность, периферическую микроциркуляцию, показатели гемостаза.
- Воздействие на воспалительные процессы. Применение нестероидных противовоспалительных средств позволяет уменьшить секрецию медиаторов воспаления, снизить температуру тела при значительной гипертермии. НПВС также способны ослабить боль за счет повышения порога болевой чувствительности рецепторов.
Назначение пациенткам с хориоамнионитом витаминно-минеральных комплексов, иммуностимулирующих средств ускоряет процесс выздоровления и снижает вероятность осложнений. Во время восстановительного периода показано физиотерапевтическое лечение с использованием УВЧ-терапии, инфракрасной лазеротерапии, электроимпульсной терапии.
Прогноз и профилактика
При своевременной постановке диагноза прогноз хориоамнионита для беременной благоприятный. Вероятность положительного исхода для плода повышается по мере увеличения гестационного срока, на котором возникло заболевание. Профилактические мероприятия предполагают раннюю постановку на учет в женской консультации для выявления и лечения генитальных инфекций, экстрагенитальной патологии. Рекомендованы обоснованный подход к назначению инвазивной пренатальной диагностики, экстренная госпитализация и выбор оптимальной тактики ведения беременности и родов при преждевременном отхождении околоплодных вод.
Внутриутробные инфекции – группа заболеваний плода и новорожденного, развивающихся вследствие заражения в дородовом периоде или в родах. Внутриутробные инфекции могут приводить к гибели плода, самопроизвольному аборту, задержке внутриутробного развития, преждевременным родам, формированию врожденных пороков, поражению внутренних органов и ЦНС. Методы диагностики внутриутробных инфекций включают микроскопические, культуральные, иммуноферментные, молекулярно-биологические исследования. Лечение внутриутробных инфекций проводится с использованием иммуноглобулинов, иммуномодуляторов, противовирусных, антибактериальных препаратов.

Общие сведения
Внутриутробные инфекции – патологические процессы и заболевания, обусловленные антенатальным и интранатальным инфицированием плода. Истинная распространенность внутриутробных инфекций не установлена, однако, согласно обобщенным данным, с врожденными инфекциями рождается не менее 10% новорожденных. Актуальность проблемы внутриутробных инфекций в педиатрии обусловлена высокими репродуктивными потерями, ранней неонатальной заболеваемостью, приводящей к инвалидизации и постнатальной гибели детей. Вопросы профилактики внутриутробных инфекций лежат в плоскости рассмотрения акушерства и гинекологии, неонатологии, педиатрии.

Причины внутриутробных инфекций
Внутриутробные инфекции развиваются в результате инфицирования плода в дородовом периоде или непосредственно во время родов. Обычно источником внутриутробной инфекции для ребенка выступает мать, т. е. имеет место вертикальный механизм передачи, который в антенатальном периоде реализуется трансплацентарным или восходящим (через инфицированные околоплодные воды) путями, а в интранатальном - аспирационным или контактным путями.
Реже происходит ятрогенное инфицирование плода в период беременности при проведении женщине инвазивной пренатальной диагностики (амниоцентеза, кордоцентеза, биопсии ворсин хориона), введении плоду препаратов крови через сосуды пуповины (плазмы, эритроцитарной массы, иммуноглобулинов) и т. д.
В антенатальном периоде инфицирование плода обычно связано с вирусными агентами (вирусами краснухи, герпеса, цитомегалии, гепатита В и С, Коксаки, ВИЧ) и внутриклеточными возбудителями (токсоплазмоза, микоплазмоза).
В интранатальном периоде чаще происходит микробная контаминация, характер и степень которой зависит от микробного пейзажа родовых путей матери. Среди бактериальных агентов наиболее распространены энтеробактерии, стрептококки группы В, гонококки, синегнойная палочки, протей, клебсиелла и др. Плацентарный барьер непроницаем для большинства бактерий и простейших, однако при повреждении плаценты и развитии фетоплацентарной недостаточности, может произойти антенатальное микробное инфицирование (например, возбудителем сифилиса). Кроме этого, не исключается и интранатальное вирусное заражение.
Факторами возникновения внутриутробных инфекций служат отягощенный акушерско-гинекологический анамнез матери (неспецифические кольпиты, эндоцервициты, ЗППП, сальпингофориты), неблагополучное течение беременности (угроза прерывания, гестозы, преждевременная отслойка плаценты) и инфекционная заболеваемость беременной. Риск развития манифестной формы внутриутробной инфекции существенно выше у недоношенных детей и в том случае, когда женщина инфицируется первично во время беременности.
Известно, что тяжесть проявлений инфекционного процесса у беременной и у плода может не совпадать. Бессимптомное или малосимптомное течение инфекции и у матери может вызвать тяжелые поражения плода, вплоть до его гибели. Это связано с повышенным тропизмом вирусных и микробных возбудителей к эмбриональным тканям, преимущественно ЦНС, сердца, органа зрения.
Классификация
Этиологическая структура внутриутробных инфекций предполагает их деление на:
- вирусные (вирусный гепатит, герпес, краснуха, ОРВИ, цитомегалия, эпидемический паротит, энтеровирусная инфекция)
- бактериальные (туберкулез, сифилис, листериоз, сепсис)
- паразитарные и грибковые (микоплазмоз, токсоплазмоз, хламидиоз, кандидоз и др.)
Для обозначения группы наиболее распространенных внутриутробных инфекций используется аббревиатура TORCH-синдром, объединяющий токсоплазмоз (toxoplasmosis), краснуху (rubella), цитомегалию (cytomegalovirus), герпес (herpes simplex). Буквой О (other) обозначаются другие инфекции, в числе которых - вирусные гепатиты, ВИЧ-инфекция, ветряная оспа, листериоз, микоплазмоз, сифилис, хламидиоз и др.).
Симптомы внутриутробных инфекций
Наличие внутриутробной инфекции у новорожденного может быть заподозрено уже во время родов. В пользу внутриутробного инфицирования может свидетельствовать излитие мутных околоплодных вод, загрязненных меконием и имеющих неприятный запах, состояние плаценты (полнокровие, микротробозы, микронекрозы). Дети с внутриутробной инфекцией часто рождаются в состоянии асфиксии, с пренатальной гипотрофией, увеличенной печенью, пороками развития или стигмами дисэмбриогенеза, микроцефалией, гидроцефалией. С первых дней жизни у них отмечается желтуха, элементы пиодермии, розеолезных или везикулезных высыпаний на коже, лихорадка, судорожный синдром, респиратрные и кардиоваскулярные расстройства.
Ранний неонатальный период при внутриутробных инфекциях нередко отягощается интерстициальной пневмонией, омфалитом, миокардитом или кардитом, анемией, кератоконъюнктивитом, хориоретинитом, геморрагическим синдромом и др. При инструментальном обследовании у новорожденных могут обнаруживаться врожденная катаракта, глаукома, врожденные пороки сердца, кисты и кальцификаты мозга.
В перинатальном периоде у ребенка отмечаются частые и обильные срыгивания, мышечная гипотония, синдром угнетения ЦНС, серый цвет кожных покровов. В поздние сроки при длительном инкубационном периоде внутриутробной инфекции возможно развитие поздних менингитов, энцефалитов, остеомиелита.
Рассмотрим проявления основных внутриутробных инфекций, составляющих TORCH-синдром.
Врождённый токсоплазмоз
Внутриутробное инфицирование одноклеточным протозойным паразитом Toxoplasma Gondii приводит к тяжелым поражениям плода – задержке развития, врожденным порокам развития мозга, глаз, сердца, скелета.
После рождения в остром периоде внутриутробная инфекция проявляется лихорадкой, желтухой, отечным синдромом, экзантемой, геморрагиями, диареей, судорогами, гепатоспленомегалией, миокардитом, нефритом, пневмонией. При подостром течении доминирую признаки менингита или энцефалита. При хронической персистенции развивается гидроцефалия с микроцефалией, иридоциклит, косоглазие, атрофия зрительных нервов. Иногда встречаются моносимптомные и латентные формы внутриутробной инфекции.
К числу поздних осложнений врожденного токсоплазмоза относятся олигофрения, эпилепсия, слепота.
Врождённая краснуха
Внутриутробная инфекция возникает из-за заболевания краснухой при беременности. Вероятность и последствия инфицирования плода зависят от гестационного срока: в первые 8 недель риск достигает 80%; последствиями внутриутробной инфекции могут служить самопроизвольное прерывание беременности, эмбрио- и фетопатии. Во II триместре риск внутриутробного инфицирования составляет 10-20%, в III – 3-8%.
Дети с внутриутробной инфекцией обычно рождаются недоношенными или с низкой массой тела. Для периода новорожденности характерна геморрагическая сыпь, длительная желтуха.
Классические проявления врожденной краснухи представлены триадой Грега: поражением глаз (микрофтальмией, катарактой, глаукомой, хориоретинитом), ВПС (открытым артериальным протоком, ДМПП, ДМЖП, стенозом легочной артерии), поражением слухового нерва (сенсоневральной глухотой). В случае развития внутриутробной инфекции во второй половине беременности у ребенка обычно имеется ретинопатия и глухота.
Кроме основных проявлений врожденной краснухи, у ребенка могут выявляться и другие аномалии: микроцефалия, гидроцефалия, расщелины нёба, гепатит, гепатоспленомегалия, пороки развития мочеполовой системы и скелета. В дальнейшем внутриутробная инфекция напоминает о себе отставанием ребенка в физическом развитии, ЗПР или умственной отсталостью.
Врождённая цитомегалия
Внутриутробное заражение цитомегаловирусной инфекцией может приводить к локальному или генерализованному поражению многих органов, иммунодефициту, гнойно-септическим осложнениям. Врожденные дефекты развития обычно включают микроцефалию, микрогирию, микрофтальмию, ретинопатию, катаракту, ВПС и др. Неонатальный период врожденной цитомегалии осложняется желтухой, геморрагическим синдромом, двусторонней пневмонией, интерстициальным нефритом, анемией.
К отдаленным последствиям внутриутробной инфекции относятся слепота, нейросенсорная глухота, энцефалопатия, цирроз печени, пневмосклероз.
Врождённая герпетическая инфекция
Внутриутробная герпес-инфекция может протекать в генерализованной (50%), неврологической (20%), слизисто-кожной форме (20%).
Генерализованная внутриутробная врожденная герпетическая инфекция протекает с выраженным токсикозом, респираторным дистресс-синдромом, гепатомегалией, желтухой, пневмонией, тромбоцитопенией, геморрагическим синдромом. Неврологическая форма врожденного герпеса клинически проявляется энцефалитом и менингоэнцефалитом. Внутриутробная герпес-инфекция с развитием кожного синдрома сопровождается появлением везикулярной сыпи на кожных покровах и слизистых оболочках, в т. ч. внутренних органов. При наслоении бактериальной инфекции развивается сепсис новорожденных.
Внутриутробная герпес-инфекция у ребенка может приводить к формированию пороков развития - микроцефалии, ретинопатии, гипоплазии конечностей (кортикальной карликовости). В числе поздних осложнений врожденного герпеса - энцефалопатия, глухота, слепота, задержка психомоторного развития.
Диагностика
В настоящее время актуальной задачей является пренатальная диагностика внутриутробных инфекций. С этой целью на ранних сроках беременности проводится микроскопия мазка, бактериологический посев из влагалища на флору, ПЦР-исследование соскоба, обследование на TORCH-комплекс. Беременным из группы высокого риска по развитию внутриутробной инфекции показана инвазивная пренатальная диагностика (аспирация ворсин хориона, амниоцентез с исследованием амниотической жидкости, кордоцентез с исследованием пуповинной крови).
Возможно выявление эхографических маркеров внутриутробных инфекций с помощью акушерского УЗИ. К косвенным эхографическим признакам внутриутробного инфицирования относятся маловодие или многоводие; наличие гиперэхогенной взвеси в околоплодных водах или амниотических тяжей; гипоплазия ворсин хориона, плацентит; преждевременное старение плаценты; отечный синдром плода (асцит, перикардит, плеврит), гепатоспленомегалия, кальцификаты и пороки развития внутренних органов и др. В процессе допплерографического исследования кровотока выявляются нарушения плодово-плацентарного кровотока. Кардиотокография обнаруживает признаки гипоксии плода.
После рождения ребенка с целью достоверной верификации этиологии внутриутробной инфекции используются микробиологические (вирусологические, бактериологические), молекулярно-биологические (ДНК-гибридизация, ПЦР), серологические (ИФА) методики обследования. Важное диагностическое значение имеет гистологическое исследование плаценты.
По показаниям новорожденные с внутриутробными инфекциями в первые сутки жизни должны быть осмотрены детским неврологом, детским кардиологом, детским офтальмологом и др. специалистами. Целесообразно провести ЭхоКГ, нейросонографию, офтальмоскопию, исследование слуха методом вызванной отоакустической эмиссии.
Лечение внутриутробных инфекций
Общие принципы лечения внутриутробных инфекций предполагают проведение иммунотерапии, противовирусной, антибактериальной и посиндромной терапии.
Иммунотерапия включает применение поливалентных и специфических иммуноглобулинов, иммуномодуляторов (интерферонов). Противовирусная терапия направленного действия осуществляется, главным образом, ацикловиром. Для противомикробной терапии бактериальных внутриутробных инфекций используются антибиотики широкого спектра действия (цефалоспорины, аминогликозиды, карбапенемы), при микоплазменной и хламидийной инфекциях – макролиды.
Посиндромная терапия внутриутробных инфекций направлена на купирование отдельных проявлений перинатального поражения ЦНС, геморрагического синдрома, гепатита, миокардита, пневмонии и т. д.
Прогноз и профилактика
При генерализованных формах внутриутробных инфекций летальность в неонатальном периоде достигает 80%. При локальных формах возникают серьезные поражения внутренних органов (кардиомиопатии, ХОБЛ, интерстициальный нефрит, хронический гепатит, цирроз и т. д.). Практически во всех случаях внутриутробные инфекции приводят к поражению ЦНС.
Профилактика внутриутробных инфекций заключается в проведении предгравидарной подготовки, лечении ЗППП до наступления беременности, исключении контактов беременной с инфекционными больными, коррекции программы ведения беременности у женщин групп риска. Женщины, ранее не болевшие краснухой и не получавшие прививки против краснухи, должны быть вакцинированы не позднее, чем за 3 месяца до предполагаемой беременности. В ряде случаев внутриутробные инфекции могут являться основанием для искусственного прерывания беременности.
Подтекание околоплодных вод — патологическое состояние, вызванное высоким разрывом плодных оболочек или образованием в них микротрещин. Проявляется постоянным выделением небольшого количества водянистой амниотической жидкости. Для диагностики применяется осмотр с зеркалами, амниотесты, амниоцентез с безопасным красителем, исследование влагалищного мазка под микроскопом, трансабдоминальное УЗИ. Акушерская тактика определяется сроком беременности, состоянием матери и плода, наличием осложнений. При выжидательном ведении назначают антибиотики, глюкокортикоиды, токолитики. Активная тактика предусматривает прерывание беременности или индукцию родовой деятельности.
Общие сведения
Повреждение плодного яйца с незначительным подтеканием вод наблюдается почти в половине случаев преждевременного разрыва амниона. По данным разных авторов, такое патологическое состояние возникает в 2-5% беременностей и является причиной почти 10% случаев перинатальной смертности. В связи с минимальными клиническими проявлениями подтекание зачастую не выявляют вовремя, что существенно повышает риск инфекционных и других осложнений. Именно разрыв оболочек провоцирует преждевременные роды, является основной причиной недоношенности, гипоплазии легких и сепсиса плода — трех ключевых факторов, повышающих риск смерти новорожденного. Использование современных методов диагностики и рациональное ведение беременных с поврежденными плодными оболочками позволяет существенно улучшить прогноз для матери и ребенка.

Причины подтекания околоплодных вод
Постоянное выделение незначительного количества амниотической жидкости наблюдается при нарушении целостности оболочек плода. В отличие от обильного преждевременного излития околоплодных вод в результате разрыва нижнего полюса плодного яйца, подтекание обычно возникает при так называемом высоком боковом надрыве или образовании микротрещин. Существует несколько групп причин, приводящих к повреждению амниотической оболочки:
- Инфекционные процессы. Самопроизвольный разрыв оболочек плода чаще наблюдается у беременных, страдающих эндометритом, кольпитом, цервицитом, аднекситом. Прочность амниона существенно снижается при хориоамнионите.
- Нарушения в маточно-плацентарной системе. Вероятность повреждения амниотического мешка увеличивается при наличии двурогой или удвоенной матки, ИЦН, плацентарной недостаточности, оболочечном креплении или преждевременной отслойке плаценты.
- Ятрогенные воздействия. Подтекание вод может стать результатом многократных бимануальных исследований, трансвагинальных УЗИ, амниоцентеза, биопсии хориона и укрепления шейки матки швами при ИЦН.
- Плодные факторы. Стенки амниотического пузыря испытывают повышенное давление при многоплодной беременности, гидроцефалии плода, аномалиях его положения и вставления предлежащей части.
- Патология оболочек. Чрезмерное растяжение амниона возникает при многоводии, вызванном первичной и вторичной гиперпродукцией околоплодных вод или нарушением их резорбции. Эластичность оболочек также уменьшается при их гиалиновом перерождении (преждевременной дегенерации).
- Травмы живота. Оболочки плода могут разрываться при резком ударе в живот, проникающих ранениях брюшной полости и матки.
Специалисты в сфере акушерства и гинекологии выделяют ряд предрасполагающих факторов, которые повышают риск самопроизвольного разрушения оболочек плода. Вероятность подтекания выше у женщин с преждевременным излитием околоплодных вод во время предыдущей беременности (рецидив наблюдается в 20-30% случаев), при наличии хронических воспалительных заболеваний половых органов и рубцовой деформации шейки матки. Патология чаще диагностируется у пациенток, длительно употребляющих глюкокортикоидные препараты, с системными заболеваниями соединительной ткани, анемией, никотиновой зависимостью. По мнению некоторых авторов, определенную провоцирующую роль играет низкий уровень благосостояния женщины, который приводит к несбалансированному питанию, значительным физическим и психоэмоциональным нагрузкам.
Патогенез
Ключевое значение в патогенезе подтекания околоплодных вод играют причины, приводящие к повреждению амниона. Стартовым звеном процесса обычно являются структурные изменения в оболочках плода, вызванные воспалением, дегенеративными изменениями или значительным растяжением. Пусковым моментом разрыва с последующим подтеканием становится чрезмерное повышение давления околоплодных вод либо резкое травматическое воздействие (удар, грубая пальпация, прокол), нарушающие целостность оболочек.
При высоком боковом расположении дефект амниотического мешка находится над внутренним маточным зевом, поэтому скорость вытекания околоплодных вод ограничена за счет примыкания поврежденного участка к стенке матки. Поскольку разрывы амниона не рубцуются, защитная функция плодного пузыря снижается, увеличивается риск инфицирования плода. Кроме того, ферменты, которые содержатся в амниотической жидкости, способны спровоцировать отслойку плаценты и, в зависимости от гестационного срока, самопроизвольный аборт или преждевременные роды.
Классификация
При выборе тактики ведения беременной определяющую роль играет время повреждения оболочек плода. На основании этого критерия выделяют следующие виды подтекания вод:
- При преждевременном дородовом разрыве — до 37 недели беременности (подтекание при недоношенной беременности);
- При дородовом разрыве — с 37 недели гестационного срока (подтекание при доношенной беременности);
- При раннем боковом разрыве — во время родов до раскрытия шейки на 4 см и более.
Симптомы подтекания околоплодных вод
Если вытекание амниотической жидкости не сочетается с другой акушерской или гинекологической патологией – субъективные ощущения отсутствуют, состояние в ряде случаев может оставаться незамеченным. Объем живота, как правило, не уменьшается. Обычно беременная жалуется на постоянное выделение из влагалища водянистой жидкости без цвета и запаха, количество которой увеличивается при изменении позы, напряжении брюшного пресса во время кашля, чихания, физических нагрузок и в горизонтальном положении.
Осложнения
Диагностика
Подтекание околоплодных вод — одно из наиболее сложных в плане диагностики патологических состояний при беременности. Скудная клиническая симптоматика и высокий риск последующих осложнений требуют особо тщательного обследования пациенток с подозрением на повреждение оболочек плода. Диагностические мероприятия направлены на подтверждение амниотического характера выделений и выявление возможных осложнений. План обследования обычно включает:
- Осмотр в зеркалах. В заднем своде определяется небольшое количество прозрачной жидкости, которая подтекает при покашливании беременной.
- Трансабдоминальное УЗИ. При подтекании этот метод менее информативен, однако позволяет вовремя диагностировать возможные осложнения — отслойку плаценты, признаки страдания плода и т. п.
- Микроскопия влагалищного мазка. О наличии амниотической жидкости свидетельствует кристаллизация в виде характерных листьев папоротника. Однако данный метод считается недостаточно чувствительным и специфичным.
- Амниотест. Изменения цвета тест-полосок выявляет ощелачивание кислой среды влагалища околоплодными водами, а обнаружение в выделениях плацентарного микроглобулина в 99,9% случаев свидетельствует о повреждении плодных оболочек.
- Амниоцентез с красителем. Метод является высокоинвазивным и предполагает введение в амниотический мешок безопасного красителя через прокол брюшной стенки. Если через 20-30 минут после введения тампон, установленный во влагалище, окрашивается, диагноз разрыва оболочек считается подтвержденным.
Дифференциальная диагностика проводится с воспалительными заболеваниями женских половых органов (вагинитом, цервицитом, эндометритом, сальпингоофоритом), амнионитом, преждевременной отслойкой плаценты. При выявлении осложнений к ведению пациентки привлекают анестезиолога-реаниматолога, неонатолога, терапевта.
Лечение подтекания околоплодных вод
При выборе схемы ведения беременной в первую очередь учитывается срок гестации. С учетом нежизнеспособности плода и высокого риска опасных осложнений беременность до 22 недели рекомендуется прервать. Пациенток на более поздних сроках госпитализируют в акушерские стационары 3-го уровня и обеспечивают максимальный физический покой. С 22 по 34 неделю включительно тактика является выжидательной. Пролонгация беременности противопоказана при хориоамнионите, грубых пороках развития, острой гипоксии или гибели плода, начале родовой деятельности, преэклампсии и эклампсии, отслойке плаценты и ряде других состояний. В остальных случаях рекомендованы:
- Превентивная антибактериальная терапия. Для снижения риска инфекционных осложнений антибиотики назначают курсом с первого дня госпитализации.
- Препараты для профилактики РДС. Чтобы ускорить синтез сурфактанта и созревание легочной ткани, применяют глюкокортикоиды.
- Токолитическая терапия. Использование селективных β2-адреномиметиков, сернокислой магнезии, ингибиторов циклооксигеназы, блокаторов медленных кальциевых каналов и окситоциновых рецепторов уменьшает сократительную активность миометрия.
- Амниотрансфузия. Применяется в исключительных случаях по требованию беременной на 22-24 неделе при больших объемах выделений и значительном снижении количества околоплодных вод.
Лечение проводится на фоне регулярного мониторинга состояния плода и беременной: термометрии, оценки показателей крови и гемодинамики, ежедневной кардиотокографии, еженедельного УЗИ, допплерометрии фетоплацентарного кровотока каждые 3 дня. При этом особое внимание уделяется профилактике внутрибольничной инфекции.
При выявлении подтекания вод у женщины с 34-36-недельной беременностью используют как выжидательную, так и активную тактику. Поскольку нет достоверных данных, что индукция родовой деятельности в этом сроке ухудшает неонатальный исход, второй вариант является предпочтительным. Выжидание зачастую провоцирует развитие хориоамнионита и компрессию пуповины. Длительность наблюдения обычно не превышает 1 суток. После начала родов с профилактической целью назначают антибиотики.
На 37 и более неделе гестации при выявлении в выделениях околоплодных вод и отсутствии родовой деятельности показана стимуляция родов. Антибактериальная терапия применяется при диагностике хориоамнионита. Превентивное назначение антибиотиков рекомендуется только в тех случаях, когда предполагаемая длительность подтекания вод превышает 18 часов.
Прогноз и профилактика
Прогноз при подтекании околоплодных вод зависит от срока беременности. Рациональное использование выжидательной тактики позволяет плоду максимально созреть и минимизирует риск инфекционных осложнений. Прекращение подтекания при 22-33-недельной беременности позволяет пролонгировать ее до доношенных сроков, если состояние женщины и плода является удовлетворительным, а количество амниотической жидкости сохраняется на нормальном уровне. При продолжении подтекания вод, отсутствии признаков воспаления, удовлетворительном состоянии беременной и плода пролонгация возможна не более чем на 1-3 недели. Риск перинатальной смертности существенно уменьшается при преждевременных родах с 31-33 недели беременности, а заболеваемость новорожденных — с 34 и более. Профилактика преждевременного подтекания вод предусматривает ограничение тяжелых физических нагрузок, отказ от курения, своевременную постановку на учет и регулярные посещения акушера-гинеколога, обоснованное назначение инвазивных диагностических процедур (особенно при обнаружении факторов риска).
Читайте также:

