Инотропная поддержка при септическом шоке
Обновлено: 24.04.2024
Куликов А.В., Шифман Е.М.
Введение
В настоящее время в мире инфекции стоят на третьем месте в структуре материнской смертности и составляют 15%, а в развивающихся странах септический шок, связанный с септическим абортом и послеродовым эндометритом по-прежнему занимает одно из ведущих мест, несмотря на значительный прогресс в отношении профилактики и лечения гнойно-септических осложнений в акушерстве.
В России материнская смертность (МС), связанная с сепсисом во время родов и в послеродовом периоде в общей структуре МС составляет 3,4%, но если учесть все случаи, связанные с абортами (больничными и внебольничными) а это 10%, то проблема становится весьма актуальной. В структуре пациенток акушерского профиля, поступающих в критическом состоянии ОАР ОКБ № 1 г. Екатеринбурга из ЛПУ Свердловской области 43,2% - гнойно-септические осложнения.
В формате данныхклинических рекомендаций мы остановимся на конкретных особенностях сепсиса и септического шока в акушерстве и протоколе начальной целенаправленной (первые 1-24 ч) интенсивной терапии септического шока, поскольку адекватность лечебных мероприятий именно в этот промежуток времени и будет определять исход заболевания
Основные положения
Положение 1. Диагностика сепсиса, тяжелого сепсиса и септического шока основана на критериях, предложенных R. Bone в 1992 г., и руководствах SSC 2008, 2012 г.г.
Положение 2. Для постановки диагноза и определения дальнейшей тактики необходимо контролировать количество лейкоцитов, С-реактивный белок и особенно уровень прокальцитонина.
Положение 4. В течение первого часа от постановки диагноза тяжелый сепсис и септический шок обеспечивается венозный доступ, контроль диуреза, лабораторный контроль и берутся пробы на бактериологическое исследование.Начинается внутривенная инфузия кристаллоидов в объеме до 30 мл/кг (при отсутствии эффекта применяются растворы ГЭК и/или альбумина 20%) и вводятся антибактериальные препараты широкого спектра действия. Каждый час задержки адекватной антибактериальной терапии снижает выживаемость пациенток.
Положение 5. При отсутствии эффекта от инфузионной терапии 30 мл/кг необходимо подключить вазопрессоры – оптимальный препарат норадреналин. При снижении сердечного индекса менее 2,5 л/м/м2 к терапии подключаются инотропные препараты (добутамин, левосимендан) и уже при отсутствии эффекта – глюкокортикойды.
Положение 6. В течение 3-х часов необходимо оценить эффективность коррекции нарушений гемодинамики, получить данные об уровне лактата.
Положение 7. К 6 часам после постановки диагноза необходимо санировать очаг инфекции и достичь необходимых параметров гемодинамики, транспорта кислорода и диуреза.
Положение 9. Дальнейшая поддерживающая терапия должна проводиться в поливалентном отделении интенсивной терапии, которое имеет возможность протезировать не только функцию легких, но и почек (раннее начало почечной заместительной терапии)
Этиология тяжелого сепсиса и септического шока в акушерстве
O08.0 Инфекция половых путей и тазовых органов, вызванная абортом, внематочной и молярной беременностью.
O08.3 Шок, вызванный абортом, внематочной и молярной беременностью.
O41.1 Инфекция амниотической полости и плодных оболочек.
O75.1 Шок матери во время родов или после родов и родоразрешения.
O85 Послеродовой сепсис.
O86 Другие послеродовые инфекции.
O86.0 Инфекция хирургической акушерской раны.
O86.1 Другие инфекции половых путей после родов.
O86.2 Инфекция мочевых путей после родов.
O86.3 Другие инфекции мочеполовых путей после родов.
O86.4 Гипертермия неясного происхождения, возникшая после родов.
O86.8 Другие уточненные послеродовые инфекции.
O88.3 Акушерская пиемическая и септическая эмболия.
Факторы риска развития сепсиса в акушерстве:
- Внебольничный, инфицированный аборт.
- Низкий социально-экономический статус.
- Иммунодефицитное состояние.
- Хронические очаги инфекции (урогенитальный тракт).
- Сахарный диабет.
- Оперативные вмешательства (кесарево сечение).
- Преждевременные роды.
- Кровопотеря, геморрагический шок (предлежание плаценты, отслойка плаценты).
- Внутриматочные манипуляции.
- Анемия.
- Преэклампсия и эклампсия.
Основные возбудители сепсиса
- Escherichiacoli, Bacteroidesspp., Clostridiumspp., Klebsiellaspp., Pseudomonasaeruginosa., GroupAC-hemolyticstreptococcus, Staphylococcusaureus, Fungalspp., Группа Bstreptococcus, Peptostreptococcus, Peptococcus spp., Enterococcus spp., Listeria monocytogenes, Enterobacter spp., Proteus spp
- Септический аборт: энтеробактерии (чаще E.coli), грамположительные кокки (Streptococcus gr. B, Enterococcus spp., S.aureus и др.) и неспорообразующие анаэробы (Bacteroides spp., Peptococcus spp., PeptoStreptococcus spp.). В отдельных случаях (особенно при криминальных абортах) возбудителем может быть C. perfringens.
- Посеродовый эндометрит: Факультативные анаэробы Enterobacteriaceae: E. coli (17–37%), реже Proteus spp., Klebsiella spp., Enterobacter spp Enterococcus: E. faecalis (37–52%). Облигатные анаэробы Bacteroides fragilis (40–96%), реже Fusobacterium spp., Peptococcus spp., PeptoStreptococcus spp. Несколько реже обнаруживаются Streptococcus gr. B, Staphylococcus spp. (S.aureus 3–7%) и др.
Современные определения и диагностика тяжелого сепсиса и септического шока.
Синдром системной воспалительной реакции - это реакция на воздействие агрессивных факторов (травма, операция, инфект) Характеризуется двумя или более из следующих признаков:
Сепсис - системный воспалительный ответ на инвазию микроорганизмов. Наличие очага инфекта и 2-х или более признаков СВР.
Тяжелый сепсис:
- Вызванная сепсисом гипотония
- Увеличение лактата.
- Диурез менее 0,5 мл/кг/ч больше 2 ч при адекватной инфузии
- ALI с PaO2/FiO2 менее 250 в отсутствие пневмонии как источника инфекции
- ALI с PaO2/FiO2 менее 200 в присутствии пневмонии как источника инфекции
- Креатинин более 2.0 мг/дл (176,8 - мкмоль/л)
- Билирубин более 2 мг/дл (34,2 -мкмоль/л)
- Количество тромбоцитов менее
- Коагулопатия (МНО более 1,5)
Сепсис-индуцированная гипотония - снижение систолического ДА менее 90 мм рт.ст. у "нормотоников" или на 40 мм рт.ст. и более от "рабочего" АД у лиц с артериальной гипертензией при условии отсутствия других причин. Гипотония устраняется в короткий срок с помощью инфузии
Септический шок - тяжелый сепсис с тканевой и органной гипоперфузией, артериальной гипотонией.
- АДсист
- САД
- Артериальная гипотония сохраняется после введения инфузионных растворов - 20-40 мл/кг
- Требует применения вазопрессоров и инотропной поддержки
Рефрактерный септический шок - сохраняющаяся артериальная гипотония, несмотря на адекватную инфузию и применение инотропной и сосудистой поддержки.
Общие клинические и лабораторные особенности сепсиса
Маркеры сепсиса
Общие параметры
- Температура>38.3°C или
- Частота сердечных сокращений> 90 уд. в мин.
- Тахипноэ (частота дыхания> 20 дыханий в мин.)
- Измененный психический статус
- Значительный отек или положительный гидробаланс более 20 мл/кг
- Гипергликемия более 7,7 ммоль/л (при отсутствии сахарного диабета)
Воспалительные показатели
- Лейкоцитарная формула> 12 000 в мкл, 10% незрелых форм.
- C-реактивный белок в плазме > 2 раза выше нормы
- Прокальцитонин в плазме > 2 раза выше нормы
Гемодинамические параметры
Переменные дисфункции органа
- Артериальная гопоксемия (PaO2/FIO2<300)
- Диурез
- Креатинин > 0.5 мг/дл
- Международное нормализованное отношение (INR, МНО)> 1,5 или АПТВ> 60 секунд
- Парез кишечника
- Количество тромбоцитов < 100 000 в мкл.
- Гипербилирубинемия (общий билирубин более 70 мкмоль/л)
Показатели тканевой перфузии
- Гиперлактатемия > 1 ммоль/л
- Мраморность кожного покрова, снижение наполнения капилляров
Некоторые из лабораторных маркеров сепсиса
Факторы облегчающие и усложняющие течение сепсиса у беременных женщин
- Молодой возраст
- Отсутствие преморбидного фона
- Локализация очага в полости малого таза – доступность для диагностики и лечения
- Чувствительность микрофлоры к антибактериальным препаратам широкого спектра действия
- Материнская толерантность - снижение активности клеточного звена иммунитета (изменение соотношения Th1/Th2 –большая восприимчивость к внутриклеточным возбудителям (бактерии, вирусы, паразиты)
- Увеличение количества лейкоцитов
- Увеличение уровня D-димера
- Дисфункция эндотелия сосудов
- Снижение антитромбина III, протеина С, протеина S
- Рост уровня провоспалительных цитокинов в родах
- Наличие воспалительной реакции при осложнениях беременности (преэклампсия, эклампсия, преждевременные роды) –материнский воспалительный ответ - (MSIR - maternal systemic inflammatory response)
Начальная терапия тяжелого сепсиса и септического шока
- Стабилизация гемодинамики (инфузия, вазопрессоры и инотропные препараты)
- Антибактериальная терапия
- Адъювантная терапия (кортикостеройды,рекомбинантный активированный протеин С)
Общие мероприятия при тяжелом сепсисе и септическом шоке
При установлении диагноза тяжелого сепсиса или септического шока терапия должна быть начата еще до поступления больной в реанимацию!
Первые 30 мин.:
- Венозный доступ (периферическая и центральная вена).
- Оценка АД, ЧСС, сатурации кислорода и диуреза.
- Взятие посевов крови и других сред.Бактериологические посевы (дважды) должны быть взяты до начала антибиотикотерапии, но не должны её задерживать.
- Лабораторное исследование: лейкоциты и лейкоцитарная формула, уровень прокальцитонина, количество тромбоцитов, АПТВ, МНО, кислотно-основное состояние и газы крови, уровень билирубина, АСТ, АЛТ. Общий анализ мочи.
- Рентгенография легких.
- Независимо от других условий в первые 30-60 мин после постановки диагноза внутривенно ввести антибактериальные препараты: эмпирическая терапия (карбапенемы, цефалоспорины III-IV и др.): цефепим +/- метронидазол, цефоперазон/сульбактам, имипенем, меропенем, В дальнейшем могут применяться: ванкомицин или линезолид. (дозы препаратов указаны в табл. ).
- Инфузионная терапия проводится кристаллойдами и/или синтетическими коллойдами. Преимущества одних растворов перед другими не установлены. (уровень 1В).В первые 30 мин вводятся 1000 мл кристаллоидов или 500 мл синтетических коллоидов. Средний инфузии – 30-40 мл/кг, в дальнейшем требуется титрование инфузии в зависимости от уровня сердечного выбраса.ЦВД должно быть выше 8 мм.рт.ст.Ограничение объема инфузии требуется, когда ЦВД или ДЗЛА увеличиваются без гемодинамической стабилизации (АД, ЧСС).
После выполнения указанных выше мероприятий необходимо оценить:
- Ответ АД на введение инфузионных растворов 30 мл/кг в течение 60 мин:
- При подъеме среднего АД более 65 мм рт.ст. – продолжить инфузионную терапию для достижения ЦВД > 8 мм рт.ст.
- При отсутствии эффекта от проводимой инфузионной терапии: подключить вазопрессоры в/в: цель –достичь среднего артериального давления>65 мм рт.ст. (уровень 1С). Для стартовой терапии (уровень 1С):
- норадреналин 0,1-0,3 мкг/кг/мин
- адреналин 1-10 мкг/мин
- мезатон 40-300 мкг/мин
- вазопрессин 0,03 ед/мин
- допмин 5-20 мкг/кг/мин
- Темп диуреза – он должен быть более 0,5 мл/кг/ч.
- Допмин не должен использоваться для защиты почек в любой дозе (уровень 1А)
- Добутамин должен использоваться при миокардиальной дисфункции и повышении ДЗЛА (уровень 1С) – максимум 20 мкг/кг -1 /мин -1
Последующие 6 ч:
Необходимо как можно раньше (оптимально в первые 6 ч) решить главный вопрос в лечении сепсиса и септического шока: своевременная и адекватная санация очага инфекции, независимо от того связан ли он с маткой или нет. При этом вопрос о необходимости удаления матки должен стоять постоянно, поскольку велика вероятность и вторичного инфицирования и существуют объективные трудности: ни бимануальное исследование, ни данные УЗИ матки часто не дают необходимой информации.
Когда вопрос об удалении матки должен быть поставлен:
- Помимо матки не выявлено других очагов инфекции, обусловливающих тяжесть состояния.
- При несоответствии ухудшения клинической картины и симптомов основной патологии.
- Нарастание воспалительной реакции на фоне интенсивной терапии - неэффективность консервативной терапии.
- Рост прокальцитонинового теста.
- Антенатальная гибель плода на фоне инфекционного процесса любой локализации.
- Признаки полиорганной недостаточности (снижение АД, олигурия, ОПЛ/ОРДС, желтуха, энцефалопатия, ДВС-синдром,тромбоцитопения).
Когда не нужно удалять матку:
- Верифицирован и санирован очаг инфекции любой локализации, определяющий тяжесть состояния (менингит, пневмония, отит, флегмоны, абсцессы, синусит, пиелонефрит, панкреонекроз, перитонит и др.) – это может служить показанием для родоразрешения, но не для удаления матки.
- Не прогрессирует воспалительная реакция - эффективная консервативная терапия.
- Не прогрессирует полиорганная недостаточность.
- Не увеличен прокальцитониновый тест.
- Живой плод.
- Нет клиники септического шока (но и наличие септического шока - показание для родоразрешения, а при верифицированном и санированном очаге инфекции другой локализации - не показание для удаления матки).
Дальнейшие задачи интенсивной терапии
В ситуации, когда после проведения инфузионной терапии 30 мл/кг и введения вазопрессоров и инотропных препаратов не происходит стабилизации гемодинамики подключаются кортикостеройды: только водорастворимый гидрокортизон в/в и только у взрослых в дозе не более 300 мг/сутки (уровень 1А). Кортикостеройды должны быть отменены как только прекращается ведение вазопрессоров. Кортикостеройды не должны применяться при отсутствии клиники шока
Дальнейшее лечение (6 ч и далее)
Компоненты крови
- Поддерживается уровень гемоглобина 70-90 г/л (уровень 1В).
- Свежезамороженная плазма в дозе не менее 15 мл/кг используется при наличии кровотечения и при инвазивных процедурах на фоне коагулопатии.
- Свежезамороженная плазма не должна использоваться только для коррекции лабораторных изменений при отсутствии кровотечения или инвазивных процедур (уровень 2А).
- Поддерживается количество тромбоцитов выше 50 000 в мкл.
Поддерживающая терапия
Искусственная вентиляция легких (инвазивная, неинвазивная) при остром повреждении легких/остром респираторном дистресс-синдроме (ALI/ARDS).
- Отсутствие самостоятельного дыхания и патологические ритмы дыхания
- Нарушение проходимости верхних дыхательных путей
- Снижение респираторного индекса менее 200 мм рт.ст.
- Септический шок
- Нарушения гемодинамики (жизнеопасные нарушения ритма, стойкая тахикардия более 120 в мин, гипотензия)
- Снижение респираторного индекса менее 300 мм рт.ст. при комбинации с другими критериями
- Развитие септической энцефалопатии и отека головного мозга с угнетением сознания и нарушением ФВД
- Гиперкапния или гипокапния (paCO2 менее 25 мм.рт.ст.)
- Тахипноэ более 40 в мин (или 24 при обострении хронического обструктивного заболеваниях легкого) и прогрессирующее увеличение минутного объема вентиляции
- Снижение ЖЕЛ менее 10 мл/кг массы тела
- Снижение податливости менее 60 мл/см вод.ст.
- Увеличение сопротивления дыхательных путей более 15 см вод.ст./л/с.
- Усталость пациента, вовлечение вспомогательных дыхательных мышц
- Применение дыхательного объема менее 10 мл/кг массы тела (рекомендуется 6 мл/кг).
- Оптимальное ПДКВ (выше 10 см вод.ст.)
- Предпочтительно применение вспомогательных режимов респираторной поддержки.
- Применение маневров открытия альвеол.
- При отсутствии эффекта от изложенного в пп.1-4 применение вентиляции в положении лежа на животе
Седативная терапия, аналгезия, и нервно-мышечная блокада
- При проведении седации необходимо придерживаться протокола. В протокол должны быть включены такие критерии, как глубина седации, оцениваемая на основании стандартных шкал.
- Режим проведения седации может быть основан либо на болюсном введении препаратов, или на их постоянной инфузии с ежедневным прерыванием седации в дневное время (или переводом больного в менее седированное состояние).
- Применения мышечных релаксантов при сепсисе необходимо по возможности избегать. Если необходимость в их применении все же есть, то необходим мониторинг глубины блока (TOF).
Контроль глюкозы (внутривенный инсулин) – менее 8,3 ммоль/л (150 мг/дл)
Почечная заместительная терапия рекомендована при наличии почечной недостаточности, а постоянная гемофильтрация показана для регулирования водного баланса у гемодинамически нестабильных пациентов.
Инотропная поддержка при сепсисе.
Помимо инфузионной терапии важное значение в стабилизации гемодинамических показателей принадлежит инотропной поддержке, обеспечивающей наряду с купированием гемодинамических нарушений адекватный уровень тканевой перфузии. К препаратам, обеспечивающим инотропную поддержку, относятся допамин и добутамин.
Допамин. Допамин, являющийся прямым альфа- и бета-адреномиметиком и стимулирующий допаминэргические рецепторы, обладает дозозависимыми эффектами. Препарат в дозе 2-5 мкг/кг • мин (влияние на допаминэргические рецепторы) увеличивает кровоток в мезентериальных, коронарных и почечных сосудах, в дозе 5-10 мкг/кг • мин (преимущественное влияние на бета-адренорецепторы) увеличивает работу сердца, в дозах более 20 мкг/кг • мин (стимуляция преимущественно альфа-адренорецепторов) - увеличивает ОПСС.
Особенности фармакологических эффектов допамина при септическом шоке.
1. Альфа-адреномиметические эффекты неблагоприятны.
2. DO2 и VO2 увеличиваются меньше чем при использовании добутамина.
3. Диуретический эффект более выражен, но кратковременен.
4. Уменьшает кровоток слизистой оболочки ЖКТ и снижает рН Желудочного сока.
5. Уменьшает DO 2 к внутренним органам.
6. Обладает супрессивным действием в отношении гормонов гипофиза, функции лейкоцитов и иммунного ответа.
7. В условиях септического шока не имеет преимуществ перед добутамином.
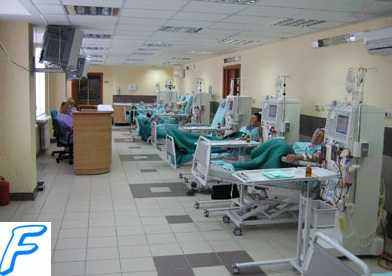
Добутамин. Синтетический адреномиметик добутамин, обладающий положительным инотропным действием (стимуляция бета-адренорецепторов) и не имеющий вазопрессорных эффектов, используется в дозе от 2,5 до 20 мкг/кг • мин. Препарат увеличивает ЧСС, но, в отличие от допамина, не влияет на ОПСС.
Небольшие дозы добутамина (5 мкг/кг • мин), наряду с увеличением доставки кислорода, повышают рН желудочного сока, что происходит вследствие дилятации сосудов спланхнической области (влияние на бета-2-адренорецепторы) и увеличения кровотока в слизистой оболочки желудка.
При использовании добутамина в терапии септического шока у больных, несмотря на увеличение сердечного выброса и доставки кислорода, возможно углубление артериальной гипотензии, что диктует необходимость проведения нагрузки объемом или использования добутамина (5 мкг/кг • мин) в сочетании с допамином (10-15 мкг/кг • мин) и/или норадреналином (0,15 мкг/кг • мин).
Особенности действия добутамина при септическом шоке.
1. Более эффективен, чем допамин.
2. Агрессивное использование (неконтролируемое применения значительных доз) может иметь неблагоприятный результат.
3. Добутамин в условиях септического шока редко адекватен в качестве монотерапии.
Вазопрессоры при сепсисе
Неэффективность лечения септического шока инфузионной поддержкой в сочетании с инотропными препаратами служит основанием для включения в комплекс интенсивной терапии вазопрессоров - норадреналина и адреналина.
Норадреналин. Норадреналин, влияя на альфа-адренорецепторы, увеличивает тем самым инотропизм миокарда, вызывает вазоконстрикцию, увеличение артериального давления без ухудшения сердечного выброса, рост постнагрузки, снижение мезентериального кровотока. При медленном введении норадреналина почечный кровоток после короткого периода снижения улучшается, почечное сосудистое сопротивление уменьшается. На фоне инфузии норадреналина в дозе 0,15-0,25 мкг/кг • мин среднее артериальное давление и ОПСС увеличиваются соответственно на 40% и 50%.
В условиях септического шока при снижении СИ менее 4 л/мин • \г усиление инотропного эффекта норадреналина достигается его комбинацией с добумином в дозе 5,0-7,5 мкг/кг • мин, что позволяет улучшить показатели гемодинамики, увеличить транспорт кислорода, снизить уровень лактата крови при неизменных значениях ДЗЛК, причем спланхнический кровоток улучшается, а рН желудочного сока увеличивается.
В целом использование норадреналина в комплексе интенсивной терапии септического шока достоверно повышает выживаемость больных. Однако следует помнить, что избыточное введение норадреналина чревато прогрессированием нарушении микроциркуляции, возникновением нарушений ритма сердца, снижением диуреза.
Особенности применения норадреналина в условиях септического шока.
1. Улучшение инотропной функции миокарда.
2. Изменения доставки и потребления кислорода непостоянны.
3. Отсутствует специфический эффект в отношении почечного кровотока.
4. Изменение кровотока внутренних органов менее выражено, чем при использовании допамина.
5. Часто необходимо применение дополнительных вазопрессоров.
Инотропная терапия септического шока - добутамин, препараты кальция
Несмотря на положительное влияние инфузионной терапии у больных септическим шоком, сократительная функция миокарда может нарушаться из-за расширения полости желудочков, снижения фракции изгнания, возрастания остаточного объема левого желудочка. Механизм дисфункции миокарда является комплексным и связан не столько с ишемией миокарда, сколько с нарушением внутриклеточного обмена кальция, а-адренергическим эффектом и участием некоторых медиаторов (цитокины, фактор активации тромбоцитов, оксид азота), которые способны приводить к снижению сократительной способности миокарда.
Необходимо отметить, что при септическом шоке инотропная терапия не имеет стратегического значения, так как обычно сердечный выброс не снижен. Однако у пациентов со сниженным сердечным выбросом применение инотропной терапии показано, так как она способствует его восстановлению. Для оценки эффективности инотропной терапии, кроме комплексной оценки клинических параметров, желательно проведение мониторинга сердечного выброса прямым методом.
При системной гипоперфузии и связанным с ней снижением сатурации кислорода в смешанной венозной крови этот показатель может быть важным параметром мониторинга. Еще одним параметром может быть уровень лактата крови, снижение которого при проведении инотропной терапии является благоприятным прогностическим признаком.
Добутамин — адренергический агонист, стимулирующий b1-адренергические рецепторы. Гемодинамический эффект добутамина у больных сепсисом и септическим шоком исследован достаточно хорошо. В диапазоне доз 2—28 мкг/кг в минуту препарат способен повышать сердечный индекс на 25—50 % за счет увеличения ударного индекса и частоты сердечных сокращений.
Этот эффект не приводит к повышению АД. Увеличение перфузии спланхнического бассейна происходит исключительно в результате увеличения сердечного индекса. У пациентов с тяжелым сепсисом препарат способствует увеличению доставки и потребления кислорода тканями. У больных сепсисом препарат показан в тех случаях, когда после восстановления объема циркулирующей крови остаются признаки миокардиальной недостаточности (низкий сердечный индекс).
Препараты кальция не оказывают достоверного положительного влияния кальция на гемодинамические показатели у пациентов с септическим шоком. В экспериментах на животных применение препарата приводило к увеличению летальности.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Патогенетическая терапия септического шока - коррекция гемодинамики
Гемодинамическая поддержка при септическом шоке. Шок представляет собой дисбаланс между доставкой и потреблением клетками кислорода и других метаболических веществ в результате нарушения тканевой перфузии с формированием дисфункции органов. Септический шок, кроме того, включает патофизиологические изменения, наступающие в результате генерализованного воспаления и участия широкого спектра медиаторов: цитокинов, простагландинов, оксида азота и многих других.
Септический шок характеризуется артериальной гипотензией со снижением среднего уровня АД ниже 65—70 мм рт. ст. Обычно гипотензия сопровождается нарушением тканевой перфузии: олигурией, микроциркуляторными нарушениями, снижением восприятия окружающей обстановки. Адекватность регионарной перфузии оценивается на основании клинических симптомов, функции органов, степени коагуляционных нарушений, лабораторных тестов, указывающих на органную или полиорганную недостаточность.
Адекватность тканевой перфузии при септическом шоке. Целью трансфузионной терапии септического шока является восстановление тканевой перфузии и нормализация метаболизма клеток. Применение трансфузионной терапии достоверно увеличивает сердечный выброс, доставку кислорода и других метаболитов, является средством коррекции гипотензии и восстановления гемодинамической стабильности. Выбор оптимального объема инфузии не всегда является простой задачей, и для оценки адекватности объемной нагрузки обычно применяют такие показатели, как достижение определенного уровня АД, частоты сердечных сокращений и темпа диуреза. Измерение центрального венозного давления используется для оценки исходного соотношения объема циркулирующей крови и насосной функции сердца, так как определение оптимального давления заполнения правого сердца является слишком сложным для рутинной клинической практики.
Необходимо помнить, что увеличение объема циркулирующей крови и плазмы приводит к увеличению сердечного выброса и снижению летальности больных септическим шоком.
Виды инфузионных растворов при септическом шоке. В лечении больных септическим шоком используют инфузии коллоидных и кристаллоидных растворов. До настоящего времени оживленно обсуждается практика применения этих видов растворов, причем в Европе предпочтение отдается коллоидным растворам, в Северной Америке — кристаллоидам. Коллоидные растворы разделяются на натуральные (альбумин, препараты плазмы) и синтетические (желатины, декстраны, гидроэтилкрахмал).
В принципе инфузионная терапия применяется для повышения конечного диастолического давления в сердце и, согласно закону Старлинга, увеличения сердечного выброса. Для достижения гемодинамической цели лечения может быть использован любой из имеющихся растворов. Гемодинамический эффект может быть достигнут несколько быстрее с помощью коллоидных растворов, чем кристаллоидных. Однако стоимость коллоидных растворов существенно превосходит стоимость кристаллоидных. В связи с этим качество, вид, объем, соотношение коллоидных и кристаллоидных растворов выбирается в зависимости от особенностей конкретной клинической ситуации и противопоказаний к применению того или иного лекарственного препарата.
Чем тяжелее состояние пациента, нуждающегося в инфузионной терапии, тем точнее требуется подбор (титрование) объема инфузионной терапии из-за опасности гипергидратации.
До настоящего времени не получено убедительных данных, подтверждающих преимущество кристаллоидных или коллоидных растворов для улучшения результатов лечения септического шока. Известно, что для достижения одинакового улучшения перфузии тканей объем кристаллоидов должен превышать объем коллоидов в 2—4 раза, следовательно, инфузия кристаллоидов требует более продолжительного периода времени.
Альбумин составляет около 80 % белков плазмы и определяет коллоидно-осмотическое давление у здоровых людей. В условиях высокой сосудистой проницаемости, интерстициального отека тканей, характерных для больных тяжелым сепсисом и септическим шоком, для привлечения в кровяное русло избытка интерстициальной жидкости необходимо применять гипертонические растворы альбумина (20—25 %). Следует помнить, что суточная потребность организма в альбумине в норме составляет 80 г, т. е. для ее компенсации требуется 400 мл 20 % раствора альбумина. Однако такой объем ежедневных инфузии альбумина, по-видимому, необходим только пациентам с тяжелым нарушением белково-синтетической функции печени, поэтому растворы альбумина целесообразно вводить только в концентрированном виде для коррекции гипоальбуминемии или низкого онкотического давления крови.
Объем инфузии концентрированного раствора подбирается индивидуально в соответствии с указанными показателями пациента. С целью коррекции гемодинамических нарушений применение раствора альбумина нецелесообразно.
Гидроэтилкрахмал (ГЭК) представляет собой 6 % синтетический коллоид в изотоническом солевом растворе. Имеются экспериментальные данные, указывающие на то, что ГЭК обладает способностью снижать степень эндотелиальных повреждений и выраженность синдрома высокой сосудистой проницаемости. Однако из-за способности взаимодействовать с VIII фактором свертывания и удлинения времени свертывания объем инфузии ГЭК должен быть ограничен.
Раствор желатина оказался существенно дешевле, но и значительно менее эффективным.
В целом необходимо отметить, что внутривенная трансфузия коллоидных и кристаллоидных растворов направлена на повышение давления заполнения правого предсердия, что по закону Старлинга приводит к увеличению сердечного выброса и оптимизации кровотока. Выбор растворов для коррекции гемодинамических нарушений определяется традициями отделения, возможностями адекватного мониторинга гемодинамических параметров, индивидуальными предпочтениями лечащего врача. Исследований, которые бы доказывали преимущества коллоидных препаратов над кристаллоидными, или каких-то определенных соотношений коллоидных и кристаллоидных препаратов не имеется. Общий объем суточной инфузии растворов у больных с септическим шоком заранее определить невозможно, поэтому обычно применяют методику титрования объема вводимых растворов в зависимости от их эффекта на центральную гемодинамику, диурез и другие показатели тканевого кровотока.
Переливание крови при септическом шоке. Переливание крови показано только при снижении концентрации гемоглобина ниже уровня 90 г/л. Однако известно, что анемия до 70 г/л достаточно хорошо переносится больными сепсисом. Основными признаками, указывающими на необходимость гемотрансфузии, следует считать очень низкую сатурацию смешанной венозной крови (SvО2) и электрокардиографические признаки ишемии сердца. При трансфузии крови с целью улучшения оксигенации преимущество имеет свежезаготовленная кровь.
Применение вазопрессоров при септическом шоке. Если внутривенная трансфузия растворов оказывается неспособной поддерживать приемлемый уровень АД и тканевой перфузии, возникает необходимость применения вазопрессорных препаратов.
Определение АД непрямым методом у больных септическим шоком может быть недостаточно точным, поэтому рекомендуется производить прямое измерение с помощью катетеризации артерии. Для оценки эффективности вазопрессоров обычно проводят мониторинг среднего АД. В экспериментальных исследованиях показано, что при среднем АД выше 60 мм рт. ст. имеются условия для адекватной ауторегуляции коронарных, почечных и мозговых сосудов. Однако у пожилых и пациентов с хронической артериальной гипертонией для обеспечения тканевой перфузии возникает необходимость в поддержании более высокого уровня среднего АД, которое определяется адекватностью диуреза (50— 100 мл/ч).
Во многих исследованиях доказано, что при применении адекватных доз вазопрессоров происходит улучшение перфузии почек. Нормальный почечный кровоток обычно обеспечивается средним АД на уровне 75 мм рт. ст., однако возможны индивидуальные колебания. У большинства пациентов поддержание среднего АД на уровне 60—65 мм рт. ст. позволяет получить адекватный диурез. У некоторых олигурия может оставаться даже при нормальном почечном кровотоке из-за снижения гломерулярного перфузионного давления или необратимых ишемических повреждений почек. Перфузия спланхнического бассейна (мезентериальные, печеночные и селезеночные артерии) и сохранность слизистой кишечника играют важную роль в патогенезе полиорганной недостаточности, причем адреналин способен снизить объем кровотока в этом бассейне.
Низкие дозы допамина увеличивают доставку кислорода органам спланхнического бассейна на 65 %, при этом потребление кислорода возрастает только на 16 %. Этот феномен до настоящего времени не получил объяснения. Для минимизации ятрогенного эффекта на кровообращение рекомендуется комбинированная инфузия норадреналина и допамина. Однако одновременное введение норадреналина и низких доз допамина (1— 4 мкг/кг в минуту) у пациентов с септическим шоком не приводило к снижению летальности.
Для оценки гемодинамического эффекта допамина необходимо вспомнить соотношение основных параметров центральной гемодинамики. Минутный объем кровообращения является величиной, характеризующей в целом объем крови, который проходит через сердце и необходим для поддержания жизненных функций организма. Минутный объем кровообращения вычисляется по произведению ударного объема на частоту сердечных сокращений. Из-за значительных различий абсолютной величины ударного объема у людей с разным конституционным типом часто применяют показатель ударного индекса, представляющий собой частное от деления ударного объема на площадь тела. Этот показатель в большей степени позволяет сравнивать насосную функцию сердца различных пациентов.
Сердечный индекс представляет собой произведение ударного индекса на частоту сердечных сокращений. Если рассчитать периферическое сосудистое сопротивление, т. е. то сопротивление, которое создается периферическими сосудами объему крови, который выбрасывается сердцем, можно определить работу левого желудочка сердца. Таким образом, увеличение ударного и сердечного индекса нужно трактовать как позитивный эффект применения вазопрессоров. Возрастание работы сердца за счет увеличения частоты сердечных сокращений или повышения сосудистого тонуса, не соответствующего ударному индексу (объему), нужно рассматривать как отрицательное влияние применения вазопрессоров.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Септический шок – это тяжелое патологическое состояние, возникающее при массивном поступлении в кровь бактериальных эндотоксинов. Сопровождается тканевой гипоперфузией, критическим снижением артериального давления и симптомами полиорганной недостаточности. Диагноз ставится на основании общей клинической картины, сочетающей в себе признаки поражения легких, сердечно-сосудистой системы (ССС), печени и почек, централизации кровообращения. Лечение: массивная антибиотикотерапия, инфузия коллоидных и кристаллоидных растворов, поддержание деятельности ССС за счёт введения вазопрессоров, коррекция респираторных нарушений путем ИВЛ.
МКБ-10
Общие сведения
Септический шок (СШ) также называют инфекционно-токсическим (ИТШ). Как самостоятельная нозологическая единица патология впервые была описана в XIX веке, однако полноценное изучение с разработкой специфических противошоковых мер началось не более 25 лет назад. Может возникать при любом инфекционном процессе. Наиболее часто встречается у пациентов хирургических отделений, при менингококковой септицемии, брюшном тифе, сальмонеллезе и чуме. Распространен в странах, где диагностируется наибольшее количество бактериальных и паразитарных заболеваний (Африка, Афганистан, Индонезия). Ежегодно от ИТШ погибает более 500 тысяч человек по всему миру.

Причины
В абсолютном большинстве случаев патология развивается на фоне ослабления иммунных реакций. Это происходит у пациентов, страдающих хроническими тяжелыми заболеваниями, а также у людей пожилого возраста. В силу физиологических особенностей сепсис чаще диагностируется у мужчин. Список самых распространенных заболеваний, при которых могут возникать явления ИТШ, включает в себя:
- Очаги гнойной инфекции. Признаки системной воспалительной реакции и связанных с ней нарушений в работе внутренних органов отмечаются при наличии объемных абсцессов или флегмоны мягких тканей. Риск генерализованного токсического ответа повышается при длительном течении болезни, отсутствии адекватной антибактериальной терапии и возрасте пациента старше 60 лет.
- Длительное пребывание в ОРИТ. Госпитализация в отделение реанимации и интенсивной терапии всегда сопряжена с риском возникновения сепсиса и инфекционного шока. Это обусловлено постоянным контактом с резистентной к антибактериальным препаратам микрофлорой, ослаблением защитных сил организма в результате тяжёлой болезни, наличием множественных ворот инфекции: катетеров, желудочных зондов, дренажных трубок.
- Раны. Нарушения целостности кожных покровов, в том числе возникшие во время операции, существенно повышают риски инфицирования высококонтагиозной флорой. ИТШ начинается у больных с загрязненными ранами, не получивших своевременной помощи. Травматизация тканей в ходе оперативного вмешательства становится причиной генерализованной инфекции только при несоблюдении правил асептики и антисептики. В большинстве случаев септический шок возникает у пациентов, перенесших манипуляции на желудке и поджелудочной железе. Еще одна распространенная причина – разлитой перитонит.
- Приём иммунодепрессантов. Лекарственные средства, угнетающие иммунитет (меркаптопурин, кризанол), используются для подавления реакции отторжения после трансплантации органов. В меньшей степени уровень собственной защиты снижается при употреблении химиотерапевтических средств – цитостатиков, предназначенных для лечения онкологических заболеваний (доксорубицина, фторурацила).
- СПИД.ВИЧ-инфекция в стадии СПИДа приводит к развитию нетипичного сепсиса, спровоцированного не бактериальный культурой, а грибком рода Candida. Клинические проявления болезни характеризуется малой степенью выраженности. Отсутствие адекватного иммунного ответа позволяет патогенной флоре свободно размножаться.
Возбудитель сепсиса – грамположительные (стрептококки, стафилококки, энтерококки) и грамотрицательные (Enterobacter cloacae, Clostridium pneumoniae) бактерии. Во многих случаях культуры нечувствительны к антибиотикам, что затрудняет лечение пациентов. Септический шок вирусного происхождения в настоящее время вызывает споры специалистов. Одни представители научного мира утверждают, что вирусы неспособны стать причиной патологии, другие – что внеклеточная форма жизни может спровоцировать системную воспалительную реакцию, являющуюся патогенетической основой ИТШ.
Патогенез
В основе симптомов лежит неконтролируемое распространение медиаторов воспаления из патологического очага. При этом происходит активация макрофагов, лимфоцитов и нейтрофилов. Возникает синдром системного воспалительного ответа. На фоне этого снижается периферический сосудистый тонус, объем циркулирующей крови падает за счет повышения проницаемости сосудов и застоя жидкости в микроциркуляторном русле. Дальнейшие изменения обусловлены резким уменьшением перфузии. Недостаточное кровоснабжение становится причиной гипоксии, ишемии внутренних органов и нарушения их функции. Наиболее чувствителен головной мозг. Кроме того, ухудшается функциональная активность легких, почек и печени.
Помимо СВР в формировании септического шока важную роль играет эндогенная интоксикация. В связи со снижением работоспособности экскреторных систем в крови накапливаются продукты нормального обмена веществ: креатинин, мочевина, лактат, гуанин и пируват. Во внутренних средах повышается концентрация промежуточных результатов окисления липидов (скатол, альдегиды, кетоны) и бактериальных эндотоксинов. Всё это вызывает тяжелые изменения гомеостаза, расстройства кислотно-щелочного баланса, нарушения в работе рецепторных систем.
Классификация
Симптомы септического шока
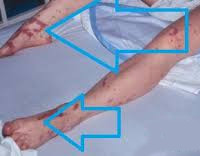
90% случаев СШ сопровождается дыхательной недостаточностью различной степени тяжести. Пациенты с декомпенсированным и терминальным течением болезни нуждаются в аппаратной респираторной поддержке. Печень и селезенка увеличены, уплотнены, их функция нарушена. Может отмечаться атония кишечника, метеоризм, стул с примесью слизи, крови и гноя. На поздних стадиях возникают симптомы диссеминированного внутрисосудистого свертывания: петехиальная сыпь, внутреннее и наружное кровотечения.
Осложнения
Септический шок приводит к ряду тяжелых осложнений. Наиболее распространённым из них считается полиорганная недостаточность, при которой нарушается функция двух и более систем. В первую очередь страдает ЦНС, легкие, почки и сердце. Несколько реже встречается поражение печени, кишечника и селезенки. Летальность среди пациентов с ПОН достигает 60%. Часть из них погибает на 3-5 сутки после выведения из критического состояния. Это обусловлено органическими изменениями во внутренних структурах.
Еще одним распространенным последствием ИТШ являются кровотечения. При формировании внутримозговых гематом у пациента развивается клиника острого геморрагического инсульта. Скопление экстравазата в других органах может приводить к их сдавлению. Уменьшение объема крови в сосудистом русле потенцирует более значимое снижение артериального давления. ДВС на фоне инфекционно-токсического шока становится причиной гибели пациента в 40-45% случаев. Вторичное поражение органов, спровоцированное микротромбозами, возникающими на начальном этапе формирования коагулопатии, отмечается практически у 100% больных.
Диагностика
- Осмотр и физикальное исследование. Реализуется непосредственно лечащим врачом. Специалист обнаруживает характерные клинические признаки шокового состояния. Для этого проводится тонометрия, визуальная оценка цвета кожных покровов, особенностей дыхательных движений, подсчет пульса и ЧДД, аускультация сердца и легких. При подозрении на наличие осложнений необходима оценка неврологического статуса на предмет симптоматики кровоизлияния в мозг.
- Аппаратное исследование. Имеет вспомогательное значение. Пациенту показан контроль состояния с использованием анестезиологического монитора. На экран устройства выводится информация о величине артериального давления, частоте сердечных сокращений, степени насыщения крови кислородом (при легочной недостаточности SpO2<90%) и коронарном ритме. На фоне нарушений дыхания и токсического поражения миокарда может отмечаться тахикардия, аритмия и блокады внутрисердечной проводимости.
- Лабораторное исследование. Позволяет выявить имеющиеся нарушения гомеостаза, сбои в работе внутренних органов. У пациентов с шоком септического происхождения обнаруживается повышенный уровень креатинина (> 0,177 ммоль/л), билирубина (>34,2 мкмоль/л), лактата (>2 ммоль/л). О нарушении коагуляции свидетельствует тромбоцитопения (
Лечение септического шока
Пациентам показана интенсивная терапия. Лечение проводят в отделениях ОРИТ с использованием методов аппаратной и медикаментозной поддержки. Лечащий врач – реаниматолог. Может потребоваться консультация инфекциониста, кардиолога, гастроэнтеролога и других специалистов. Требуется перевод больного на искусственную вентиляцию лёгких, круглосуточное наблюдение среднего медицинского персонала, парентеральное кормление. Смеси и продукты, предназначенные для введения в желудок, не используются. Все методы воздействия условно делятся на патогенетические и симптоматические:
- Патогенетическое лечение. При подозрении на наличие сепсиса больному назначают антибиотики. Схема должна включать в себя 2-3 препарата различных групп, обладающих широким спектром действия. Подбор медикамента на начальном этапе проводят эмпирическим путем, в соответствии с предполагаемой чувствительностью возбудителя. Одновременно с этим производят забор крови на стерильность и восприимчивость к антибиотикам. Результат анализа готовится в течение 10 дней. Если к этому времени подобрать эффективную лекарственную схему не удалось, следует использовать данные исследования.
- Симптоматическое лечение. Подбирается с учетом имеющейся клинической картины. Обычно больные получают массивную инфузионную терапию, глюкокортикостероиды, инотропные средства, антиагреганты или гемостатики (в зависимости от состояния свертывающей системы крови). При тяжелом течении болезни используют препараты крови: свежезамороженную плазму, альбумин, иммуноглобулины. Если пациент находится в сознании, показано введение анальгетических и седативных лекарств.
Прогноз и профилактика
Септический шок имеет неблагоприятный прогноз для жизни. При субкомпенсированном течении погибает около 40% больных. Декомпенсированная и терминальная разновидности оканчиваются гибелью 60% пациентов. При отсутствии своевременной медицинской помощи смертность достигает 95-100%. Часть больных умирает через несколько дней после устранения патологического состояния. Профилактика ИТШ заключается в своевременном купировании очагов инфекции, грамотном подборе антибиотикотерапии у хирургических больных, соблюдении антисептических требований в отделениях, занимающихся инвазивным манипуляциями, поддержке адекватного иммунного статуса у представителей ВИЧ-инфицированной прослойки населения.
2. Тактика ведения пациентов с сепсисом и септическим шоком в многопрофильном стационаре/ Сапичева Ю.Ю., Лихванцев В.В. – 2015.
Читайте также:

