Интегральные лейкоцитарные индексы интоксикации
Обновлено: 23.04.2024
86 пациентам с острым аппендикулярным перитонитом было проведено цитологическое исследование мазков-отпечатков, взятых из брюшной полости, где выявлено, что с возрастанием степени эндогенной интоксикации уменьшается число нейтрофилов с неизмененной структурой ядер, возрастает число дегенеративных нейтрофильных лейкоцитов, которое свидетельствует о развитии иммунной недостаточности и ослаблении реактивности организма. Кроме того, у этих же больных, по результатам электрогастроэнтерографии в предоперационном периоде, выявлена прямая зависимость, чем выше тяжесть эндогенной интоксикации, тем более выражен парез желудочно-кишечного тракта. Эти показатели следует рассматривать как важные диагностические критерии для определения степени эндогенной интоксикации. Патогенетически обоснованной антибиотикотерапией у больных с острым аппендикулярным перитонитом, имеющих 3 степень эндогенной интоксикации, является применение антибиотиков цефалоспоринов 3-го поколения (цефотаксим), карбопенемов (имипенем), фторхинолонов (ципрофлоксацин).
Ключевые слова: эндогенная интоксикация, лейкоцитарный индекс интоксикации, средние молекулы, билирубин, общий белок, трансаминазы, гастроэнтерография, лейкоцитоз.
Проблема лечения острых аппендикулярных перитонитов является одной из сложных проблем в неотложной хирургии, которая остается в центре внимания исследователей на протяжении всего периода медицинской науки.
Такой высокий интерес к этому заболеванию связан с социальной значимостью, доминированием в общей структуре хирургических заболеваний и высоким уровнем летальности, которые по данным большинства исследователей, как в России, так и за рубежом, составляют в среднем около 20%, а при тяжелых формах в случае развития инфекционно-токсического шока и полиорганной недостаточности – 76% [6].
В патофизиологическом аспекте причиной смерти при перитоните служит прогрессирование эндогенной интоксикации, которая в конечном итоге приводит к срыву компенсаторно-приспособительных механизмов, к функциональному и структурному повреждению органов естественной детоксикации, развитию полиорганной недостаточности [6, 7].
К сожалению, современные способы оценки эндогенной интоксикации далеки от совершенства и не в полной мере удовлетворяют практических хирургов. Среди их многообразия нет единых интегральных показателей степени тяжести эндотоксикоза [1, 6].
Сложность и многогранность патологических звеньев течения аппендикулярного перитонита предъявляют особые требования к лечению больных с этой тяжелой патологией. В настоящее время успех лечения аппендикулярного перитонита определяют хирургическая тактика, рациональная антибактериальная терапия, борьба с эндогенной интоксикацией и комплексная интенсивная терапия [1].
Таким образом, в многогранной и сложной проблеме перитонита остается много вопросов требующих углубленного изучения. Среди них можно выделить показатели интегральной оценки степени эндогенной интоксикации.
Цель исследования: уточнить показатели эндогенной интоксикации, характерные для острого аппендикулярного перитонита и определить наиболее оптимальные принципы патогенетической терапии этого патологического состояния.
Задачи исследования
- Провести анализ клинических и лабораторных показателей эндогенной интоксикации у больных с острым аппендикулярным перитонитом.
- Иммунологическая оценка эндогенной интоксикации у больных с острым аппендикулярным перитонитом, на примере, мазков отпечатков, взятых из брюшной полости.
- Произвести анализ показателей изменения моторной функции желудочно-кишечного тракта у больных с острым аппендикулярным перитонитом при разных степенях эндогенной интоксикации (по данным электрогастроэнтерографии).
- Патогенетическое обоснование антибиотиков, которые могут быть использованы для лечения больных с острым аппендикулярным перитонитом, имеющих 3 степень эндогенной интоксикации.
Материал и методы
Нами было проанализировано 576 больных с острым аппендицитом, лечившихся в хирургических отделениях больницы скорой медицинской помощи г. Энгельса Саратовской области за период с 2003 по 2005 годы. У 86 больных (14,9%) течение заболевания осложнилось развитием перитонита. Из них мужчин было 46 человек, женщин — 40 (соответственно 53% и 47%). Возраст больных был от 15 лет до 71 года (средний возраст 43±28лет). Во время операции местно-неограниченный перитонит встретился у 59 (68,6%), диффузный у 10 (11,6%), разлитой у 17 (19,8%) больных. При этом до операции положительные симптомы раздражения брюшины были выявлены у 50 (58,3%) больных, у 34 (39,5%) они были расценены как сомнительные, у 2 (2,2%) отсутствовали. Общая смертность от аппендицита за исследуемый период составила 1,38 %, а в случаях осложненных перитонитом 9,3%. Всем больным выполнена аппендэктомия. Сроки выполнения аппендэктомий были различными. 89,5% больных оперированы в течение 1 суток, а остальные 10,5% на 2-3 сутки.
Для разработки методики динамической оценки патогенеза и тяжести эндогенной интоксикации у больных с острым аппендикулярным перитонитом исследовались клинические и лабораторные показатели (частота пульса, частота дыхания, нарушение функции ЦНС, цвет кожных покровов, суточный диурез, перистальтика кишечника, лейкоцитарный индекс интоксикации, концентрация средних молекул, мочевина сыворотки крови, общий белок, билирубин, уровень трансаминаз).
Для исследования функционального состояния желудочно-кишечного тракта в патогенезе эндогенной интоксикации был использован электрогастроэнтерограф, который вместе с низкоамплитудным электростимулятором разработан в лаборатории кибернетики НИИ Хирургии им. А.В. Вишневского РАМН в 1996 г.
Результаты и их обсуждение
При оценке показателей эндогенной интоксикации в зависимости от стадии развития перитонита 86 исследуемых больных с острым аппендикулярным перитонитом нами были разделены на 3 группы (таб. 1)
Маркеры эндогенной интоксикации. Диагностика эндогеннной интоксикации.
1. Лейкоцитоз (увеличение количества лейкоцитов в венозной крови (более 10-10 /л). При оценке степени выраженности интоксикации лейкоцитоз следует учитывать наряду с другими признаками, свидетельствующими о длительности заболевания, распространенности патоло-ТОческого процесса и его динамики.
2. Лейкоцитарный индекс интоксикации (Кальф-Калиф Я. Я., 1941). Нормальные значения ЛИИ колеблются от 0,3 до 1,5.

3. Ядерный индекс интоксикации (Даштаянц Г. А., 1978). При ЯИИ, равном 0,05-0,08, состояние больного оценивается как удовлетворительное, 0,3-1,0 - средней степени тяжести, более 1,0 -тяжелое.
У больных в стадии токсемии ЛИИ и ЯИИ может снижаться, что свидетельствует о декомпенсации систем кроветворения и детоксикации. В этих случаях значительная часть токсичных продуктов белковой природы и эндотоксинов фиксируется на микросгустках и агрегатах и, выключаясь из общего кровотока, снижает токсичность крови.
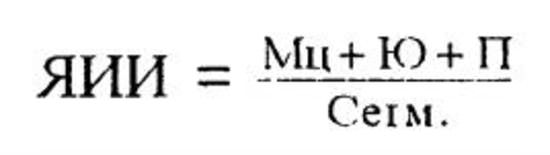
4. Индекс интоксикации (Гринев М. В., 1989). При ИИ, равном 35, прогноз заболевания неблагоприятный, при ИИ выше 45 в 100% случаев - летальный исход.
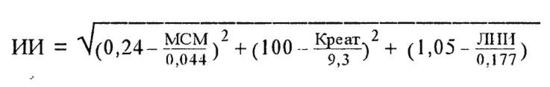
5. Концентрация общего белка в плазме крови.
- снижение уровня общего белка в плазме крови до 45 г/л указывает на тяжелую эндогенную интоксикацию и неблагоприятный исход болезни;
- уменьшение концентрации общего белка за счет альбуминовой фракции отражает использование альбумина как важнейшего фактора плазменной детоксикации, связывания и удаления токсинов;
- увеличение альфа-2-глобулинов в два раза огражает активность процесса с нарушением дезаминирования;
- увеличение гамма-глобулинов указывает на рост продукции грубодисперсных белков;
- снижение альбумино-глобулинового коэффициента (отношение количества альбуминов к количеству глобугашов) обусловливает при выраженной интоксикации переход альбуминов в ткани вследствие нарушенной проницаемости стенок сосудов, снижение интенсивности синтеза альбуминов в почечной ткани, ускорение их распада и превращения в другие белки, частично в глобулины, а также усиление синтеза альфа-2- и гамма-глобулинов. В норме атъбумино-глобулиновый коэффициент колеблется от 1,5 до 2,3.
6. Билирубин. Уровень билирубина более 30 ммоль/л вызывает выраженньш мембранотоксический эффект. Встраиваясь в мембраны и проникая в клетку, билирубин повреждает липиды митохондрий, вызывая их необратимое набухание, ингибирует утилизацию глюкозы, нарушает активность ферментов, ионную клеточную проницаемость. При эндогенной интоксикации билирубин плохо связывается с белками вследствие как гипоальбуминемии, так и вытеснения его из комплекса с альбумином лекарственными препаратами (гормонами, салуретиками).
7. Мочевина и креатинин. Увеличение уровня мочевины более 16 ммоль/л и креатинина более 0,2 ммоль/л указывает на наличие эндогенной интоксикации и сопровождается нарушением нейрогумо-рального контроля ЦНС.
8. Токсическая энзимопатия.
- увеличение уровней АЛТ, ACT, ЛДГ (изоферменты 1, 2, 5) указывает на нарушение проницаемости клеточных мембран;
- гипергликемия, увеличение концентрации лактата и пирувата отражает энергетическую несостоятельность клетки;
- увеличение концентрации молочной кислоты без повышения концентрации пировиноградной кислоты свидетельствует о повреждении ферментативных клеточных процессов;
- увеличение ДНКазы, РНКазы, кислой фосфатазы, катапрессина Д отражает степень деструкции клеток, лизиса внутриклеточных белков, а также энергодефицит клетки.
9. Молочная кислота. Увеличение концентрации молочной кислоты отражает уровень энергодефицита и гипоксии. Концентрация молочной кислоты более 4 ммоль/л расценивается как прогностически неблагоприятный признак.
10. Молекулы средней массы (МСМ) - являются олигопептидами с массой от 500 до 5000 Д, по своей природе относящимися к белковым токсинам с высоким содержанием дикарбоновых и низким - ароматических кислот.
МСМ обладают прямым мембранотоксическим действием и инициируют появление пептидов, близких по структуре к биорегуляторам. Среди них выделяют гепатоцеребральные, уремические, ишеми-ческие, ожоговые МСМ. На 80% МСМ состоят из белков и их метаболитов, в том числе продуктов гидролиза фибриногена и глобулинов, катаболизма глюкокортикоидов. В состав средних молекул входят биологически активные вещества (паратгормон, нейротоксин X, ингибиторы фагоцитоза, гемопоэза, хрупкости мембран эритроцитов, утилизации глюкозы и др.). Этим и определяется токсичность МСМ: нарушение эритропоэза, снижение розеткообразования, ингибирование дыхания митохондрий, нарушение синтеза ДНК в гепатопитах и лимфоцитах. Нейротоксические эффекты МСМ связаны с образованием ложных медиаторов: МСМ, взаимодействуя с инсулином, инактивируют гормон, ингибируя фосфорилирование, нарушают энергетический обмен в клетке.
Увеличение уровня МСМ - один из самых чувствительных признаков эндогенной интоксикации.
11. Коэффициент нейтрофилы/лимфоциты (отношение клеток неспецифической и специфической защиты). В норме коэффициент равен 2,0.
Увеличение коэффициента до 4,0 и более свидетельствует о нарастании тяжелой интоксикации.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Оценка степени тяжести синдрома эндогенной интоксикации СЭИ строится на клинических и лабораторных данных. Последние включают в себя следующие группы исследований (Н. А. Беляков, М. Я. Малахова, 1994).
1. Гематологические:
• НСТ-гест (отражает активацию пероксидазных систем нейтрофилов);
• лизосомально-катионный тест (определение катионных белков гранулоцитов);
• дегенеративные изменения лейкоцитов (токсигенная зернистость, включения Князькова-Деле, зерна Амато, гиперсегментация ядер и др.);
• угнетение миграции и спонтанный лизис лейкоцитов;
• гемолитическая устойчивость эритроцитов;
• способность к транспорту веществ низкой и средней молекулярной массы (ВНСММ).
2. Биохимические и биофизические:
• вещества средней молекулярной массы (ВСММ) в биологических жидкостях и олигопептические фракции (ОП); компоненты перекисного окисления липидов (ПОЛ) и анти-оксидантной системы (АОС);
• хемилюминесценция биологических жидкостей и гомогенатов; электронный парамагнитный резонанс (ЭПР); ядерно-магнитный резонанс (ЯМР);
• определьные углеводороды в выдыхаемом воздухе; компоненты медиаторов воспаления (биогенные амины, кал-ликреин-кининовая система, некоторые классы простаглан-динов (ПГ) и др.;
• метаболиты, характеризующие виды обмена и функции жизненно важных органов.
3. Микробиологические и иммунологические:
• бактериальные токсины (лимулюс-тест — определение бактериальных липополисахаридов (Л ПС), иммунологические методы выявления бактериальных антигенов);
• динамика микрофлоры ротовой полости, зева и кожи;
• определение компонентов комплемента;
• интегральная оценка выраженности иммуносупрессии;
4. Расчетные критерии:
• лейкоцитарный индекс интоксикации (ЛИИ);
• клинические и лабораторные индексы (Марчука, Шугаева, Габриэлян, Малаховой, Гринева и др.).
5. Биологическое тестирование
1. ВНСММ представляют собой небелковые вещества любой природы: мочевина, креатинин, мочевая кислота, глюкоза, молочные и другие органические кислоты, аминокислоты, жирные кислоты, холестерин, фосфолипиды и их дериваты, продукты свободнорадикально-ю окисления, промежуточного метаболизма и т. д.. накапливающиеся в организме в превышающих нормальные концентрациях. ВНСММ можно подразделить на 2 пула: катаболические и анаболические. Как концентрация, так и распределение ВНСММ поддерживается в условиях нормы в оргашиме на постоянном и индивидуальном уровне (М. Я. Малахова, 1994).
Синонимами ВНСММ являются термины: средние молекулы, вещества средней молекулярной массы, вещества низкой и средней молекулярной массы.
2. ОП представляют собой пептиды с молекулярной массой не более 10 кД. ОП состоят, по крайней мере, из двух пулов: регуляторные (РП) и нерегуляторные (НП) пептиды. РП — тканевые гормоны, играющие важную роль в процессе жизнедеятельности, концентрация которых в крови строго контролируется. НП имеют несколько вариантов образования, главными из которых являются поступившие извне (бактериальные, ожоговые, кишечные токсины) и образовавшиеся внутри организма (продукты аутолиза, ишемии, гипоксии органов) процессы внеклеточного (в крови) неорганического протеолиза, т. е. пептиды с нерегулируемым уровнем и непредсказуемыми свойствами (М. Я. Малахова, 1994).
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Гематология: Лейкоцитарная формула в норме и при болезнях
При морфологическом исследовании окрашенных мазков периферической крови производится дифференцированный подсчет различных видов лейкоцитов, основанный на физических и биохимических характеристиках этих клеток.
В таблице ниже приведена нормальная лейкоцитарная формула и абсолютное содержание различных видов лейкоцитов.
Абсолютное и относительное содержание различных видов лейкоцитов в норме
| Виды лейкоцитов | Относительное количество (%) лейкоцитов | Абсолютное количество (10 9 /л) лейкоцитов |
| Нейтрофилы палочкоядерные | 1-6 | 0,04-0,3 |
| Нейтрофилы сегментоядерные | 47-72 | 2,0-7,5 |
| Эозинофилы | 0,5-5 | 0,02-0,3 |
| Базофилы | 0-1 | 0-0,1 |
| Лимфоциты | 19-37 | 1,5-3,5 |
| Моноциты | 2-10 | 0,02-0,8 |
Лейкоцитарная формула дает представление только об относительных величинах (процентное содержание). Необходимо также вычислять абсолютное количество клеток каждого вида (в 10 9 /л). Это имеет значение при лейкопениях и умеренных лейкоцитозах. Например, общее количество лейкоцитов — 3,0 • 10 9 /л, из них 50% составляют лимфоциты (относительный лимфоцитоз). Абсолютное количество лимфоцитов = 50% • 3,0 • 10 9 /л : 100% = 1,5 • 10 9 /л (т. е. в пределах нормы).
При подсчете лейкоцитарной формулы важна также качественная оценка лейкоцитов (наличие гипер- или гипосегментации, гигантских форм, токсической зернистости нейтрофилов, размер и окраска цитоплазмы, форма и структуры ядра).
Клиническое значение изменений лейкоцитарной формулы
Изменения лейкоцитарной формулы могут встречаться при негематологических заболеваниях и в этих случаях неспецифичны. Лейкоцитарная формула имеет большое значение для диагностики многих онкогематологических заболеваний, оценки их тяжести и определения эффективности проводимой терапии.
Сдвиг в лейкоцитарной формуле влево — увеличение количества незрелых нейтрофилов в периферической крови (миелоцитов, метамиелоцитов, палочкоядерных нейтрофилов; при гемобластозах нередко появляются промиелоциты и бластные клетки). Появление в крови сегментоядерных нейтрофилов увеличенных размеров, с гиперсегментированными ядрами (6 и более сегментов) называется сдвигом в лейкоцитарной формуле вправо.
Полисегментированные нейтрофилы встречаются при мегалобластных анемиях, миелодиспластических синдромах, лучевой болезни, солидных опухолях, врожденной гиперсегментации нейтрофилов. Полисегментированные и гигантские нейтрофилы появляются также на фоне терапии некоторыми цитостатическими средствами (литалир, цитозар, метотрексат).
Гипосегментация и асегментация нейтрофилов встречается при наследственной пельгеровской аномалии (это нередко ошибочно расценивается как палочкоядерный сдвиг).
При миелодиспластических синдромах, неходжкинских лимфомах, хронических миелопролиферативных заболеваниях наблюдается так называемая пельгеризация нейтрофилов (псевдопельгеровская аномалия).
Снижение числа нейтрофилов менее 1,5 • 10 9 /л (нейтропения) обычно сочетается с лейкопенией и наблюдается при вирусных инфекциях, хронических воспалительных заболеваниях, многих гемобластозах, после лучевой терапии, приема ряда лекарственных препаратов. Агранулоцитоз (нейтрофильных гранулоцитов в крови менее 0,5 • 10 9 /л) — тяжелая степень нейтропении.
При выраженной лейкопении подсчет лейкоцитарной формулы и обнаружение патологических элементов (например, бластов при острых лейкозах) резко затрудняется. В этих случаях необходимо исследовать лейкоконцентрат.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Маркеры эндогенной интоксикации. Диагностика эндогеннной интоксикации.
1. Лейкоцитоз (увеличение количества лейкоцитов в венозной крови (более 10-10 /л). При оценке степени выраженности интоксикации лейкоцитоз следует учитывать наряду с другими признаками, свидетельствующими о длительности заболевания, распространенности патоло-ТОческого процесса и его динамики.
2. Лейкоцитарный индекс интоксикации (Кальф-Калиф Я. Я., 1941). Нормальные значения ЛИИ колеблются от 0,3 до 1,5.

3. Ядерный индекс интоксикации (Даштаянц Г. А., 1978). При ЯИИ, равном 0,05-0,08, состояние больного оценивается как удовлетворительное, 0,3-1,0 - средней степени тяжести, более 1,0 -тяжелое.
У больных в стадии токсемии ЛИИ и ЯИИ может снижаться, что свидетельствует о декомпенсации систем кроветворения и детоксикации. В этих случаях значительная часть токсичных продуктов белковой природы и эндотоксинов фиксируется на микросгустках и агрегатах и, выключаясь из общего кровотока, снижает токсичность крови.
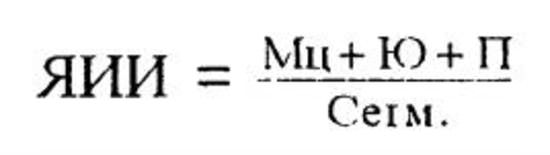
4. Индекс интоксикации (Гринев М. В., 1989). При ИИ, равном 35, прогноз заболевания неблагоприятный, при ИИ выше 45 в 100% случаев - летальный исход.
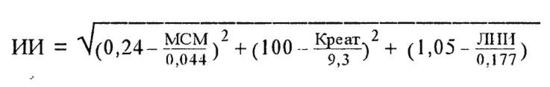
5. Концентрация общего белка в плазме крови.
- снижение уровня общего белка в плазме крови до 45 г/л указывает на тяжелую эндогенную интоксикацию и неблагоприятный исход болезни;
- уменьшение концентрации общего белка за счет альбуминовой фракции отражает использование альбумина как важнейшего фактора плазменной детоксикации, связывания и удаления токсинов;
- увеличение альфа-2-глобулинов в два раза огражает активность процесса с нарушением дезаминирования;
- увеличение гамма-глобулинов указывает на рост продукции грубодисперсных белков;
- снижение альбумино-глобулинового коэффициента (отношение количества альбуминов к количеству глобугашов) обусловливает при выраженной интоксикации переход альбуминов в ткани вследствие нарушенной проницаемости стенок сосудов, снижение интенсивности синтеза альбуминов в почечной ткани, ускорение их распада и превращения в другие белки, частично в глобулины, а также усиление синтеза альфа-2- и гамма-глобулинов. В норме атъбумино-глобулиновый коэффициент колеблется от 1,5 до 2,3.
6. Билирубин. Уровень билирубина более 30 ммоль/л вызывает выраженньш мембранотоксический эффект. Встраиваясь в мембраны и проникая в клетку, билирубин повреждает липиды митохондрий, вызывая их необратимое набухание, ингибирует утилизацию глюкозы, нарушает активность ферментов, ионную клеточную проницаемость. При эндогенной интоксикации билирубин плохо связывается с белками вследствие как гипоальбуминемии, так и вытеснения его из комплекса с альбумином лекарственными препаратами (гормонами, салуретиками).
7. Мочевина и креатинин. Увеличение уровня мочевины более 16 ммоль/л и креатинина более 0,2 ммоль/л указывает на наличие эндогенной интоксикации и сопровождается нарушением нейрогумо-рального контроля ЦНС.
8. Токсическая энзимопатия.
- увеличение уровней АЛТ, ACT, ЛДГ (изоферменты 1, 2, 5) указывает на нарушение проницаемости клеточных мембран;
- гипергликемия, увеличение концентрации лактата и пирувата отражает энергетическую несостоятельность клетки;
- увеличение концентрации молочной кислоты без повышения концентрации пировиноградной кислоты свидетельствует о повреждении ферментативных клеточных процессов;
- увеличение ДНКазы, РНКазы, кислой фосфатазы, катапрессина Д отражает степень деструкции клеток, лизиса внутриклеточных белков, а также энергодефицит клетки.
9. Молочная кислота. Увеличение концентрации молочной кислоты отражает уровень энергодефицита и гипоксии. Концентрация молочной кислоты более 4 ммоль/л расценивается как прогностически неблагоприятный признак.
10. Молекулы средней массы (МСМ) - являются олигопептидами с массой от 500 до 5000 Д, по своей природе относящимися к белковым токсинам с высоким содержанием дикарбоновых и низким - ароматических кислот.
МСМ обладают прямым мембранотоксическим действием и инициируют появление пептидов, близких по структуре к биорегуляторам. Среди них выделяют гепатоцеребральные, уремические, ишеми-ческие, ожоговые МСМ. На 80% МСМ состоят из белков и их метаболитов, в том числе продуктов гидролиза фибриногена и глобулинов, катаболизма глюкокортикоидов. В состав средних молекул входят биологически активные вещества (паратгормон, нейротоксин X, ингибиторы фагоцитоза, гемопоэза, хрупкости мембран эритроцитов, утилизации глюкозы и др.). Этим и определяется токсичность МСМ: нарушение эритропоэза, снижение розеткообразования, ингибирование дыхания митохондрий, нарушение синтеза ДНК в гепатопитах и лимфоцитах. Нейротоксические эффекты МСМ связаны с образованием ложных медиаторов: МСМ, взаимодействуя с инсулином, инактивируют гормон, ингибируя фосфорилирование, нарушают энергетический обмен в клетке.
Увеличение уровня МСМ - один из самых чувствительных признаков эндогенной интоксикации.
11. Коэффициент нейтрофилы/лимфоциты (отношение клеток неспецифической и специфической защиты). В норме коэффициент равен 2,0.
Увеличение коэффициента до 4,0 и более свидетельствует о нарастании тяжелой интоксикации.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

