Интоксикация головного мозга при циррозе печени
Обновлено: 17.04.2024
Марина Викторовна Маевская, профессор:
- Спасибо, Владимир Трофимович. Добрый день, дорогие коллеги.
Печеночная энцефалопатия – это, к сожалению, обычное явление в гастроэнтерологической (более точно, в гипотологической практике). Это одно из основных осложнений цирроза печени, которое встречает каждый врач, сталкивающийся в своей профессиональной жизни с пациентами, страдающими циррозом печени.
Печеночная энцефалопатия – это комплекс потенциально обратимых нервно-психических нарушений, которые возникают либо в результате печеночной недостаточности, либо в результате портосистемного шунтирования крови. Как правило, у пациента присутствует тот и другой фактор.
Если пояснить, что это означает, то печеночная энцефалопатия класса А – это энцефалопатия, которая развивается у пациентов с острой печеночной недостаточностью без цирроза печени. Например, острый вирусный гепатит, протекающий с угнетением функций печени, острый алкогольный гепатит без цирроза печени. Аббревиатура А появилась от слова "acute".
Портосистемное шунтирование в отсутствие заболевания печени приводит к развитию печеночной энцефалопатии класса В. То, с чем мы работаем в своей повседневной практике, наиболее частая форма печеночной энцефалопатии – та, которая наблюдается у пациентов с циррозом печени.
Формы клинически манифестной печеночной энцефалопатии, в основном служат основанием для госпитализации пациентов. Острая, рецидивирующая или хроническая (или персистирующая) энцефалопатия. Она требует непрерывного наблюдения за пациентом и искусства относительно его лечебной тактики.
Если говорить о том, с какой частотой встречаются различные формы энцефалопатии, то следует сказать, что минимальная энцефалопатия наблюдается по данным разных авторов от 32% до 85% случаев.
Чуть позже я более подробно остановлюсь на этой форме энцефалопатии. Это пациент, который, как правило, находится в амбулаторных условиях. У него клинических проявлений энцефалопатии нет. Но есть определенные аспекты жизни, которые представляют и весьма достойны пристального врачебного внимания. Клинически выраженная энцефалопатия у пациентов с циррозом печени встречается почти у половины и очень часто служит поводом для госпитализации.
Печеночная энцефалопатия – это клинический эквивалент печеночной недостаточности. Она определяет жизненный прогноз пациента. Около 42% пациентов живут в течение первого года появления этого осложнения. Трехлетняя выживаемость этих пациентов составляет всего 23%.
Мы больше привыкли в своей клинической работе к разделению печеночной энцефалопатии на следующие стадии: 1, 2, 3 и 4. Это фигурирует в нашем клиническом диагнозе. Стадии 1, 2, 3 и 4 отражают степень нарушения сознания и других (в том числе интеллектуальных и ментальных) функций у пациентов с циррозом печени с клинически выраженной энцефалопатией.
Стадия 1 – нарушение ритма сна, сонливость, снижение концентрации внимания. Пациент нуждается в дополнительном времени для того, чтобы отвечать на вопросы. Стадия 2 – летаргия или апатия. Стадия 3 – это уже сомноленция и дезориентация. Очень редко пациенты с циррозом и энцефалопатией бывают агрессивными. Но это тоже встречается в нашей практике. Стадия 4 – это печеночная кома. Минимальная энцефалопатия (раньше ее называли латентной энцефалопатией) требует применения психометрических тестов для того, чтобы этот диагноз можно было поставить.
Если пытаться количественно выразить степень глубины энцефалопатии, то при стадии 3 и 4 можно использовать шкалу для оценки глубины комы Глазго. Она включает в себя такие критерии как открывание глаз от спонтанного до отсутствия вообще какого-то ответа и измерения в баллах этого признака, речь и движение. Сумма колеблется от 3-х до 15-ти баллов. Чем меньше сумма по шкале Глазго, тем хуже прогноз пациента, тем глубже нарушение его сознания.
Тест связи чисел хорошо знаком тем, кто работает с пациентами, страдающими циррозом печени. Он стандартизован. Его количественное выражение представлено на слайде справа. Делается поправка на возраст пациента.
Прежде чем оценивать тест связи чисел, пациенту обязательно нужно дать возможность потренироваться, потому что это тоже влияет на скорость его выполнения. Первый раз он соединяет цифры в том порядке, в котором это положено – это тренировочный тест. Когда он это делает повторно, то уже оценивается время. Но расположение цифр должно быть другим.
Клинически выраженная энцефалопатия – это, как правило, пациент стационарный. Минимальная энцефалопатия (или латентная, как ее называли раньше) – пациент амбулаторный. Соответственно, принципы лечения и наблюдения за этими пациентами немного отличаются.
Но, когда речь идет об энцефалопатии, самое важное – устранение разрешающего фактора. Разрешающие факторы могут быть разными. Это может быть какая-то инфекция (вплоть до острой вирусной инфекции). Это может быть кровотечение. Может быть любая стрессовая ситуация для организма.
Очень важно контролировать какие-то сопутствующие патологические состояния, которые часто встречаются при циррозе печени. Это электролитные нарушения.
Я помню, что когда у нас была монотематическая конференция по циррозу печени в 2009-м году в Суздале, Владимир Трофимович Ивашкин читал лекцию по гипонатриемии при циррозе печени. У пациентов с циррозом гипонатриемия разведения может иметь разную природу и сама по себе вызывать нарушение сознания, весьма серьезные и глубокие.
В тот период времени Владимир Трофимович уделял в своей лекции время дифференциальному диагнозу энцефалопатии при циррозе. Это результат электролитных нарушений или проявления печеночной недостаточности (гипогликемия, уремия). Все это может вносить свой вклад в развитие энцефалопатии.
Это очень разумно, потому что в патогенезе практически всех осложнений цирроза печени (в том числе печеночной энцефалопатии) играет роль бактериальная транслокация. Это происходит на фоне застойных явлений в тонкой и в толстой кишке. В условиях портальной гипертензии бактериальная транслокация выступает как пусковой фактор порочного круга. Играет роль в развитии гепаторенального синдрома, варикозных кровотечений (которые, казалось бы, далеки от этого феномена) и, естественно, печеночной энцефалопатии. Изучение эффективности антибиотиков представляется весьма рациональным в этих условиях.
Рациональность для использования какого-либо препарата и результаты клинических исследований – это два процесса, которые идут параллельно, но не всегда взаимно дополняют друг друга. В данной ситуации можно сделать ссылки на весьма убедительные клинические исследования.
Минимальная печеночная энцефалопатия. Последний результат говорит о том, что пациенты с минимальной печеночной энцефалопатией – это объект для исследования. Минимальная энцефалопатия клинически, как правило, не проявляется. Но она может переходить в клинически манифестную энцефалопатию и служить поводом для госпитализации пациента и экономических затрат.
Тем не менее, пациенты с минимальной энцефалопатией, когда она выявляется только с использованием специальных тестов, в обычных условиях с точки зрения врача имеют определенные особенности. У них снижены внимание и память. Снижена концентрация внимания.
Они послужили объектом исследования в очень интересном аспекте. Исследование, результаты которого были опубликованы в 2004-м году, было призвано оценить их способность к вождению автомобиля. Этих пациентов разделили на 2 группы. Часть пациентов была с минимальной энцефалопатией. Часть без печеночной энцефалопатии вообще, но с циррозом печени.
В результате было показано, что пациенты с минимальной энцефалопатией и группой контроля вели себя за рулем совершенно по-другому. Правильно оценивать ситуацию, адаптироваться в сложной дорожной ситуации, хорошо концентрировать свое внимание на дороге пациенты с минимальной энцефалопатией не могли.
Их было 14 человек. В пяти случаях потребовалось вмешательство инструктора, чтобы предотвратить дорожно-транспортное происшествие. Пациенты с циррозом, у которых признаков минимальной энцефалопатии не было, никоим образом по своему водительскому мастерству не отличались от группы контроля (группы здоровых).
Не буду здесь приводить, чтобы не терять время, ужасные клинические наблюдения, которые связаны с этим аспектом. Но это исследование лишний раз иллюстрирует то, что пациент с циррозом печени должен очень тщательно мониторироваться на амбулаторном этапе. Минимальную энцефалопатию тоже нужно лечить.
Суммируя все, о чем я говорила, нужно акцентировать внимание на том, что энцефалопатия – это неблагоприятный фактор прогноза для больных циррозом печени. Ранняя диагностика, правильное и своевременное лечение энцефалопатии могут предупредить прогрессирование этого осложнения вплоть до комы.
Что такое цирроз печени? Причины возникновения, диагностику и методы лечения разберем в статье доктора Васильева Романа Владимировича, гастроэнтеролога со стажем в 15 лет.
Над статьей доктора Васильева Романа Владимировича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Цирроз печени (ЦП) — это хроническое дегенеративное заболевание печени, связанное с диффузным патологическим процессом, при котором нормальные клетки печени повреждаются, а затем замещаются рубцовой тканью, образуя избыточный фиброз и структурно-анатомические регенераторные узлы.
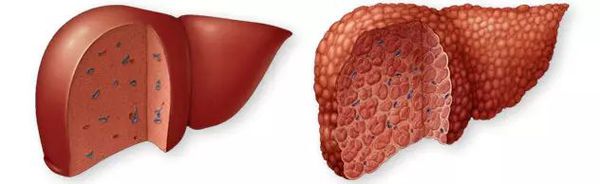
Этиология
По этиологическим характеристикам можно выделить:
- распространённые формы ЦП;
- редкие формы ЦП.
К распространённым относят вирусные (В, С, D), алкогольные и метаболические формы цирроза печени.
Редкими формами ЦП являются:
- аутоиммунные, лекарственные, токсические, первичные и вторичные билиарные циррозы;
- генетически обусловленные патологии — гемохроматоз (нарушение обмена железа), болезнь Вильсона — Коновалова, дефицит белка альфа-1-антитрипсина, гликогеноз IV типа (недостаток ферментов), галактоземия, наследственная тирозинемия и непереносимость фруктозы;
- нарушение венозного оттока из печени — венокклюзионные формы ЦП (болезнь Бадда — Киари);
- тяжёлая правожелудочковая сердечная недостаточность;
- флебопортальные циррозы (типа Банти).
Пути заражения
Заразиться циррозом печени нельзя. Однако, если он вызван вирусным гепатитом, то возбудитель может передаться через кровь, при половых контактах и от матери к ребёнку.
Основную роль в возникновении и развитии вирусного ЦП играют симптомные, малосимптомные и бессимптомные формы острого вирусного гепатита В, С, а также одновременное заболевание гепатитами В и D с последующим переходом в активный хронический вирусный гепатит. У большинства больных интервал между острым гепатитом С и клинически выраженными проявлениями ЦП превышает 30 лет. Только у мужчин, употребляющих более 50 г спирта в день, выраженные формы ЦП возникают через 13-15 лет.
Наиболее частыми причинами смерти больных ЦП является:
- большая печёночная недостаточность;
- кровотечение из варикозно расширенных вен пищевода;
- первичный рак печени;
- иммунопротективная недостаточность, влекущая за собой активизацию инфекционных (микробных) процессов, в первую очередь спонтанного бактериального перитонита и пневмонии, а также возникновение оксидативного стресса.
У больных в терминальной (заключительной) фазе заболеваний печени в основном наблюдаются декомпенсированные формы цирроза печени: асцит, варикозное расширение вен пищевода и желудка, энцефалопатия и желтуха.
Особенности цирроза печени у детей
Заболевание у детей встречается крайне редко и обычно связано:
- с аутоиммунным поражением печени;
- кардиогенными заболеваниями — лёгочной гипертензией и хронической сердечной недостаточностью;
- болезнью Бадда — Киари;
- врождёнными болезнями накопления — наследственным гемохроматозом, лизосомальными болезнями накопления, болезнью Вильсона — Коновалова;
- флебопортальным циррозом (типа Банти).
Прогноз у таких детей неблагоприятный, чаще всего они погибают, так как не успевают попасть к гепатологу и выяснить диагноз. Также они обычно страдают от множества сопутствующих болезней, в том числе от основного заболевания, ставшего причиной цирроза.
Проявления заболевания у детей и взрослых схожи. Единственный эффективный метод лечения цирроза у детей — это пересадка печени. Поэтому крайне важно вовремя диагностировать заболевание и встать в очередь на пересадку печени.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы цирроза печени
Цирроз печени в течение длительного времени может протекать латентно, т. е. бессимптомно.
Клиническая картина ЦП зависит от его формы и течения, активности основного заболевания, а также наличия или отсутствия печёночно-клеточной недостаточности, синдрома портальной гипертензии, холестаза и внепечёночных проявлений.
Основные общие симптомы, которые чаще всего встречаются при ЦП:
- повышенная утомляемость;
- похудение;
- нарушения сознания и поведения;
- ухудшение аппетита и чувство дискомфорта в животе;
- пожелтение кожи, белковых оболочек глаз и слизистой;
- осветление или обесцвечивание кала;
- потемнение мочи;
- болевые ощущения в животе;
- отёки;
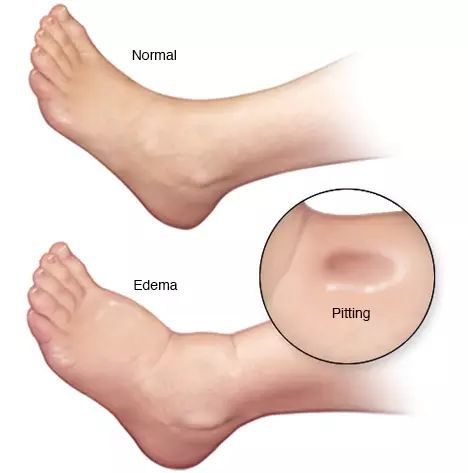
- асцит (скопление жидкости в брюшной полости);
- кровотечения из носа, желудочно-кишечного тракта, дёсен или геморроидальных узлов, а также подкожные кровоизлияния;
- часто возникающие бактериальные инфекции (например, органов дыхания);
- снижение полового влечения;
- кожный зуд.
Симптомы распространённых форм ЦП
При высокоактивном ЦП, кроме общей утомляемости, осветления стула и потемнения мочи, может возникать тупая боль в правом подреберье и вздутие живота.
Во время осмотра часто выявляют:
- субиктеричность (желтушность) склер;
- расширение вен брюшной стенки, напоминающее голову медузы;
- венозный шум при выслушивании в эпигастральной области живота (шум Крювелье — Баумгартена);
- серо-коричневатый цвет шеи;
- гинекомастию (увеличение грудных желёз);
- гипогонадизм (у мужчин);
- контрактуру Дюпюитрена (укорочение сухожилий ладоней).
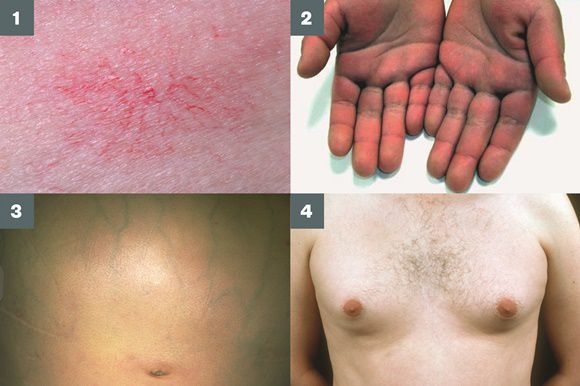
Три последних признака цирроза печени зачастую наблюдаются при алкогольных ЦП.
В области грудной клетки в 50-80% случаев наблюдаются телеангиэктазии кожи (расширения мелких сосудов), чаще при алкогольных ЦП. Пальпаторно печень отчётлива уплотнена, имеет неровный нижний край. Размеры печени различны — от значительного увеличения до уменьшения.
Часто при пальпации выявляется умеренно увеличенная селезёнка, причём её край может выступать из-под рёберной дуги на 1-3 см.
При развитии ЦП появляются симптомы белково-энергетической недостаточности, асцит, отёки, а также печёночный запах при тяжёлой печёночной недостаточности.
Симптомы при малоактивных и начальных стадиях ЦП
Данные формы ЦП зачастую протекают бессимптомно и выявляются в ходе периодических медицинских осмотров, диспансеризации, а также как случайная находка при обследовании пациента со смежной патологией или внепечёночными проявлениями.
При малоактивном ЦП, как правило, не возникают жалобы, связанные с печенью. Во время активного расспроса можно выявить весеннее снижение работоспособности, частые болезни, после которых возможны кровоточивость дёсен и потемнение мочи. Такие пациенты хуже, чем раньше, переносят длительные физические и нервно-психические нагрузки.
Желтухи и выраженного увеличения билирубина, за исключением периода интеркурентного острого гепатита, нет. Неяркая телеангиоэктазия кожи (сосудистые звёздочки) в области грудной клетки наблюдаются у 40-60% людей с ЦП.
Телеангиоэктазии кожи, плотная печень с фестончатым краем и умеренно увеличенная селезёнка — ценная клинико-диагностическая триада, которая с вероятностью 80-90% свидетельствует о ЦП или далеко зашедшем активном хроническом гепатите.
Патогенез цирроза печени
В основе патофизиологии цирроза лежит повреждение и некроз паренхимы (основной ткани) печени с деструкцией и гибелью гепатоцитов (клеток печени), а также системное поражение интерстициальной ткани.
При всех формах ЦП нарушается иммунологическое равновесие организма, преобладающими становятся аутоиммунные процессы: иммунная система человека принимает собственные клетки печени за чужеродные и повреждает их. В конечном итоге, это приводит к разрушению гепатоцитов и структуры печени в целом. Однако при этом каждая форма ЦП имеет свои патогенетические особенности:
- при вирусных гепатитах повреждающим агентом является сама вирусная частица, которая, размножаясь в клетке, разрушает её, вызывая цитолиз;
- при алкогольном ЦП прямое токсическое воздействие на мембраны гепатоцитов оказывает ацетальдегид с развитием алкогольной жировой болезни печени и алкогольного стеатогепатита;
- при метаболическом ЦП ведущую роль в патогенезе играет ожирение и сахарный диабет через стадию неалкогольного стеатогепатита с инсулинорезистентностью и последующей запрограммированной гибелью клеток печени.
В основе патогенеза более редких причин цирроза печени лежат ещё более частные механизмы развития повреждения и разрушения гепатоцитов и структуры печени:
- нарушение обмена и накопления железа при гемохроматозе;
- накопление меди при болезни Вильсона — Коновалова;
- окклюзия в системе воротной вены при гепатопортальном склерозе.
Цирроз формируется на протяжении многих лет. С течением времени происходят изменения генетического аппарата клеток печени, в результате чего появляются новые патологические клетки. Этот процесс в печени является иммуновоспалительным, он поддерживается чужеродными агентами, в роли которых могут выступать разные субстраты:
- вирус гепатита В;
- алкогольный гиалин;
- денатурированные белки;
- некоторые лекарственные средства;
- медьбелковые и железобелковые комплексы (ферритин).
В итоге повреждения паренхимы печени развивается гепатоцеллюлярная (печёночно-клеточная) недостаточность за счёт диффузного фиброза и трансформации ткани печени в анормальные узлы-регенераты. [3] [4] [5]
Классификация и стадии развития цирроза печени
В 1974 году на съезде гепатологов в Акапулько (Мексика) была принята единая морфологическая классификация, которую позже уточнили и несколько доработали эксперты ВОЗ. В настоящее время она является общепринятой.
Какие клинические симптомы позволяют диагностировать ПЭ? Каковы проявления неврологических нарушений на разных стадиях развития ПЭ? В чем заключаются особенности развития ПЭ при алкоголизме? Каких ошибок должен избежать врач при лечении ПЭ?
Какие клинические симптомы позволяют диагностировать ПЭ?
Каковы проявления неврологических нарушений на разных стадиях развития ПЭ?
В чем заключаются особенности развития ПЭ при алкоголизме?
Каких ошибок должен избежать врач при лечении ПЭ?
Этиология и патогенез
Печеночная энцефалопатия (ПЭ) представляет собой потенциально обратимое расстройство нервной и психической деятельности, возникающее при любом из заболеваний печени, протекающем с недостаточностью печеночно-клеточной функции. В большинстве случаев ПЭ осложняет течение терминальной стадии хронических диффузных заболеваний печени или острого некротизирующего (фульминантного) гепатита. Установлено, что при поражении печени любой этиологии ПЭ может привести к развитию комы и стать непосредственной причиной смерти пациента (см. таблицу 1).
Патогенез ПЭ не до конца установлен. Считается, что развитие ПЭ является результатом сочетанного влияния на ЦНС нескольких механизмов, активность которых инициируется и поддерживается выраженным нарушением печеночного клиренса токсинов и метаболитов (см. рисунок 1). Наиболее существенным для развития ПЭ считают:
- быстро нарастающее увеличение концентрации аммиака в плазме;
- увеличение плазменной концентрации и нарушение баланса между синтезом и катаболизмом нейротрансмиттеров и их предшественников в ЦНС.
Механизм развития ПЭ
К ранним признакам нарушений сознания (НС) при ПЭ относят уменьшение спонтанных движений, фиксированный взгляд, заторможенность, апатию. Для нарушения сознания при ПЭ в принципе характерны сонливость и инверсия нормального ритма сна и бодрствования. При этом ухудшение состояния и переход сонливости в кому могут произойти в течение очень короткого времени. Для определения степени НС нередко применяют шкалу Глазго (см. таблицу 2). Однако в клинической практике для оценки глубины НС именно при ПЭ используют более простую качественную шкалу, в соответствии с которой:
- для I стадии НС характерны ослабление концентрации внимания, эйфория и тревожность;
- для II стадии характерны появление сонливости, дезориентация, изменения личности и неадекватное поведение;
- на III стадии НС развиваются ступор, гиперсомния и спутанность сознания, однако больной может выполнять простые команды и произносить слова членораздельно;
- при IV степени НС пациент впадает в кому и контакт с ним оказывается невозможен.
Наиболее надежным способом определить степень нарушений интеллекта при ПЭ является проведение теста связывания чисел (тест Рейтана). Изменения личности и интеллекта при ПЭ наиболее трудны для диагностики, поскольку всегда накладываются на конституциональные, приобретенные ранее нарушения и всегда требуют оценки в динамике. Наибольшие трудности в клинической практике встречаются при дифференциальной диагностике ПЭ и нарушений личности, развивающихся при хроническом злоупотреблении алкоголем (токсическая или алкогольная энцефалопатия, наличие которой прямо не влияет на исход острой ПЭ, однако определяет риск развития делирия на фоне алкогольного абстинентного синдрома). Важно, что при алкоголизме острая ПЭ может развиться при любой из клинико-морфологических форм алкогольной болезни печени (см. рисунок 2).
Характерной особенностью ПЭ является изменчивость клинической картины. Диагностировать ПЭ легко, например, у больного с циррозом печени,
с массивным желудочно-кишечным кровотечением или сепсисом, при обследовании которого определяют спутанность сознания и хлопающий тремор. В случае, когда очевидных причин ухудшения состояния выявить не удается и признаков цирроза печени также нет, распознать начало ПЭ невозможно, если не придать должного значения малозаметным признакам синдрома. Большое значение при этом могут иметь данные анамнеза, полученные от членов семьи, заметивших изменения в состоянии или поведении больного.
У больных с острой ПЭ без признаков хронической портальной гипертензии (варикозные вены передней стенки живота, отечно-асцитический синдром, спленомегалия, заболевание печени или алкоголизм в анамнезе) диагностика на догоспитальном этапе особенно затруднена. В этих случаях она должна базироваться, во-первых, на тщательном изучении анамнеза, если это возможно; во-вторых — на анализе эффективности применения стандартной неспецифической терапии комы. Дифференциальный диагноз у больных без цирроза печени необходимо проводить с рядом заболеваний, приводящих к внезапному и выраженному нарушению сознания (см. таблицу 4).
У больных циррозом печени и активным портосистемным шунтированием важнейшим вопросом диагностики также является определение причин, приведших к развитию ПЭ (см. таблицу 5).
- нарушения электролитного баланса (прием диуретиков, массивная рвота, выраженная диарея)
- длительное голодание
- прекращение приема алкоголя (абстинентный синдром)
- массивный лапароцентез
- из варикозных вен пищевода и желудка
- из острых гастродуоденальных язв (печеночная портальная гастропатия)
- при синдроме Мэллори-Вейсса
- при хирургическом пособии или травме
- острый алкогольный эксцесс
- прием опиатов, бензодиазепинов, барбитуратов
- cпонтанный бактериальный перитонит
- инфекции мочевыводящих путей
- бронхолегочная инфекция
В большинстве случаев любой из перечисленных выше факторов либо напрямую подавляет функции ЦНС, либо нарушает их опосредованно — угнетая функцию печени, увеличивая концентрацию азотсодержащих продуктов в кишечнике и количество крови, протекающей, минуя печень, через портокавальные анастомозы.
Лабораторные данные занимают довольно скромное место в диагностике ПЭ. Известно, что ни функциональные печеночные пробы, ни повышенная концентрация аммиака в плазме прямо не коррелируют с выраженностью нарушений сознания.
Лечение ПЭ
Лечение ПЭ преследует три базовые цели:
- выявление и немедленное устранение факторов, провоцирующих ПЭ;
- уменьшение количества аммиака и других токсинов, образующихся в кишечнике в процессе пищеварения и жизнедеятельности микробной флоры;
- нормализацию обмена нейромедиаторов.
Схематично лечение ПЭ (III и IV стадии) представлено в таблице 6.
- Поддержание калорийности рациона на уровне 2000 ккал/сут
- Поддержание водно-электролитного баланса:
- контроль гиповолемии: для коррекции гиповолемии под контролем ЦВД вводить 5-или 10-процентный р-р глюкозы или альбумина, а не изотонический р-р;
- коррекция гипокалиемии до уровня выше 3,5 ммоль/л;
- отмена диуретиков.
Объем лечебных мероприятий при ПЭ относится к числу стандартных и выверенных клинической практикой алгоритмов неотложной помощи, поскольку эффективность лечения прямо зависит от как можно более раннего начала терапии. В этом смысле фармакотерапия ПЭ прямо относится к презумпции скорой медицинской помощи. Тем не менее на практике оказывается, что пациенты с ПЭ, как на догоспитальном этапе, так и в условиях стационара, нередко не получают адекватного лечения. Более того, во многих случаях больным назначают фармакотерапию, которая способна спровоцировать ухудшение состояния сознания и нарушение вегетативных функций. К числу наиболее распространенных ошибок лечения можно отнести:
- недостаточную инфузию концентрированных растворов глюкозы, обладающих помимо энергонесущей активности также ярким осмотическим действием, что важно при угрожающем отеке мозга;
- необоснованное и неконтролируемое введение изотонического и других неконцентрированных полиионных растворов, что влечет за собой прямую угрозу развития отека мозга и легких;
- недооценку важности планового назначения осмотических слабительных и экстренной очистки кишечника высокими осмотическими клизмами (эффективно уменьшают всасывание аммиака в кишечнике и его бактериальную контаминацию, способствуют снижению портального давления);
- недооценку опасности диуретической терапии, массивного лапароцентеза и назначения седативных средств в отношении углубления стадии ПЭ.
- К 70.0: алкогольная жировая дистрофия печени
- К 70.1: алкогольный гепатит
- К 70.2: алкогольный фиброз/склероз печени
- К 71: токсические поражения печени:
- 71.0 — с холестазом
- 71.1 — с некрозом
- 71.2 — по типу острого гепатита
- 71.5 — по типу хронического гепатита
- 71.7 — с фиброзом и циррозом печени
- К 72.0: острая и подострая печеночная недостаточность
- К 71.1: хроническая печеночная недостаточность
- К 76.6: портальная гипертензия
- G 31.2: дегенерация ЦНС, вызванная алкоголем
- G 61.1: алкогольная полинейропатия
- F 10.0: острое отравление, вызванное употреблением алкоголя
- F 10.3: абсистентное состояние, вызванное употреблением алкоголя
- F 10.4: абсистентное состояние с делирием, вызванное употреблением алкоголя
- F 10.2: хронический алкоголизм (алкогольная зависимость)
При выявлении ПЭ на догоспитальном этапе пациенты с III и IV стадиями нарушения сознания должны быть немедленно госпитализированы в отделение интенсивной терапии.
Прогноз ПЭ
Прогноз ПЭ всецело зависит от выраженности печеночно-клеточной недостаточности и времени начала лечения. При циррозе печени у больных с относительно сохранной функцией паренхимы и интенсивным коллатеральным кровообращением прогноз лучше, а у больных с острым гепатитом — хуже. Прогноз существенно улучшается, если удается быстро устранить факторы, ведущие к усугублению ПЭ: инфекцию, передозировку диуретиков или кровопотерю. Однако наиболее эффективным способом улучшить прогноз является как можно более точная диагностика и раннее начало лечения ПЭ.
Показатели состояния системы регуляции у больных циррозом печени вирусной этиологии подтвердили усиление симпатической и ослабление парасимпатической активности. Рекомендуется выявление и коррекция вегетативных нарушений у таких больных. Как основной гепа
The indices of the state of the system of regulation in patients with cirrhosis of virus etiology confirmed strengthening of sympathetic and weakening of parasympathetic activity. Development and correction of vegetative disorders in such patients are recommended. S-adenozil-L-methionine is stated as a main hepatoprotector.
Циррозы печени (ЦП) занимают значительное место в структуре заболеваний органов пищеварения, оставаясь крайне актуальной социально-экономической и клинико-эпидемиологической проблемой здравоохранения всех стран мира. В настоящее время в мире заболеваемость ЦП составляет около 20–40 больных на 100 тыс. населения, и этот показатель неуклонно растет [1]. Чаще всего встречаются ЦП алкогольной и вирусной этиологии.
Вирусные ЦП (в исходе хронических гепатитов В, С, В + D) составляют от 10% до 23,5% всех циррозов [2]. Доминирующее место среди всех болезней печени занимают вирусные гепатиты В, С и D, что связано с их широкой распространенностью и высоким уровнем заболеваемости [3, 4]. В США вирусный гепатит С (ВГС) в качестве причины ЦП вышел на первое место — он является причиной формирования ЦП в 26% случаев, ВГС в сочетании с алкоголем добавляет к этой статистике еще в 15% случаев, гепатит В и гепатиты В + D вызывают ЦП 15% случаев. В последние годы структура вирусных ЦП несколько изменилась: до 30,3% увеличилась доля циррозов в исходе вирусного гепатита С [5, 6]. Это согласуется с данными Европейской ассоциации по изучению печени (European Association for the Study of the Liver, EASL) (1999) о том, что ведущую роль в формировании ЦП играет хроническая инфекция ВГС, которая является причиной 40% случаев развития ЦП [7]. Особенность течения ЦП определяется, по-видимому, не только этиологическим фактором, но и другими дополнительными регулирующими механизмами, которые на настоящий момент еще не вполне изучены.
Для оценки тяжести ЦП и прогноза в течение последних почти 50 лет, с 1964 года с пересмотром-дополнением в 1973 г., используется классификация Чайлда–Пью (Чайлда–Туркотта–Пью). Эпидемиологические исследования показывают, что оценка класса по Чайлду–Пью может предсказать продолжительность жизни у пациентов с ЦП. Оценка в 10 баллов или больше связана с 50% вероятностью смерти в течение 1 года [8]. Не ясно, чем определяется выживаемость оставшихся 50%, возможно, степенью компенсаторных возможностей регуляторных систем. Следует отметить, что система оценки по Чайлду–Туркотту–Пью не является идеальной для данной группы пациентов, так как при оценке тяжести состояния больных во внимание принимаются параметры, отражающие функцию печени, но не учитываются показатели, регистрирующие функцию почек, дыхательной и сердечно-сосудистой систем. В связи с этим появились новые системы, которые являются более подходящими у данной категории больных.
С 2002 г. широко используемой системой оценки тяжести пациентов с заболеваниями печени стала шкала MELD (Model for end-stage liver disease — модель для конечной стадии заболевания печени), которая была предложена в Клинике Мэйо (США), оценка по которой варьируется от 6 до 40 баллов. Шкала применяется для прогноза летальности у пациентов с декомпенсированными ЦП. Так, было показано, что при количестве баллов по шкале MELD менее 20 трехмесячная летальность составила 27%, а при более 20 баллов — 76%. В настоящее время количество баллов по шкале MELD является приоритетным при определении неотложности трансплантации печени в США [9].
Что же определяет, кроме этиологического фактора, выживаемость пациентов с ЦП? Возможно, продолжительность жизни связана со степенью компенсаторных возможностей регуляторных систем, основой которых является функционирование вегетативной нервной системы. Вегетативная нервная система — часть нервной системы, которая управляет деятельностью внутренних органов, регулирует процессы обмена веществ, состояние тканей и органов в ходе их приспособления к текущей деятельности организма в изменяющихся условиях окружающей среды. Вегетативная нервная система регулирует сердечно-сосудистую деятельность, температуру тела, работу желудочно-кишечного тракта (атонические запоры, слабая перистальтика при симпатикотонии; гипермоторные дисфункции, спастические запоры, поносы при ваготонии), мочеиспускание, половую функцию, все виды обмена веществ, эндокринную систему, сон и др. Усиление функционирования одного отдела (например, симпатического) в нормальных физических условиях приводит к компенсаторному напряжению аппарата другого отдела (парасимпатического), возвращая функциональную систему к нормальному гомеостазу [10].
Утомляемость, слабость, усталость в диапазоне от легкой усталости в повседневной жизни до выраженной слабости являются частой жалобой больных с ЦП [17]. Усталость у пациентов с заболеваниями печени может развиться в любое время, но степень выраженности этого симптома, по мнению Newton J. L. и соавт. (2008), не коррелирует с тяжестью заболевания печени [18]. Тяжесть усталости у пациентов с ЦП коррелирует с более серьезными симптомами ВД и поэтому может быть основным фактором в оценке тяжести синдрома вегетативных нарушений [19]. С другой стороны, слабость может быть и проявлением анемического синдрома, следствием нарушения сна, побочным действием лекарств (бета-блокаторы, антидепрессанты, бензодиазепины). Кроме того, у таких пациентов может снизиться толерантность к физической нагрузке, как выявили K. Cauch-Dudek и соавт. (1996) [20]. Симптомы вегетативных нарушений моторики органов пищеварения включают в себя раннее насыщение, тошноту, рвоту, боли в эпигастрии. Задержка опорожнения желудка связана с постпрандиальной гипогликемией, по данным B. Ohlsson и соавт. (2006) и поэтому может ухудшить течение ЦП [21]. Замедление перистальтики кишечника в результате вегетативной дисфункции при ЦП имеет особое значение, поскольку оно способно привести к избыточному бактериальному росту в тонкой кишке, повышению риска развития печеночной энцефалопатии и спонтанного бактериального перитонита и может быть плохим прогностическим признаком у этих пациентов [22]. Согласно исследованиям C. Kibune Nagasako и соавт. (2009), нарушения желудочно-тонкокишечной моторики наряду с дисфункцией сфинктеров толстой кишки и мочевого пузыря могут вызывать диарею, запоры и недержание мочи, которые усиливаются на фоне назначения мочегонных и слабительных препаратов. По данным V. Gomez-Lobo и соавт. (2006), у пациентов с ЦП наблюдается дисфункция мочевого пузыря [23]. Распространенность ВД может достигать 67% и повышать смертность в группе пациентов с ЦП [16, 24, 25]. Эта взаимосвязь ВД и ЦП имеет большое значение для клиницистов, работающих с пациентами с хроническими заболеваниями печени.
В настоящее время активно ведутся исследования вариабельности ритма сердца у больных с ЦП различной степени тяжести и различной этиологии, причем выявляется высокая частота встречаемости вегетативных дисфункций. Выраженность и частота дисфункций связана не с этиологией цирроза печени, а со степенью его тяжести [28]. A. Somasundaram и соавт. (2009) предложили использовать оценку вариабельности ритма сердца в качестве предиктора оценки тяжести больного с ЦП [29].
По результатам исследования F. Szalay и соавт. (1998), при HBsAg-положительных заболеваниях печени дисфункция парасимпатического отдела вегетативной нервной системы (ПВНС) встречается в 85% случаев, дисфункция симпатического отдела вегетативной нервной системы (СВНС) — в 43%; при анти-ВГС-позитивных заболеваниях печени дисфункция ПВНС наблюдается в 58% случаев, дисфункция СВНС — в 42% [30]. M. T. Hendrickse и соавт. (2006) установили, что у пациентов с хроническим заболеванием печени, отягощенным ВД, 4-летняя смертность на 30% выше по сравнению с данными для больных хроническими заболеваниями печени без вегетативной дисфункции, у которых 4-летняя смертность составляет 6%, а также выявили, что у больных первичным билиарным циррозом, которые жалуются на усталость, смертность повышается [31, 32]. J. F. Fleckenstein и соавт. (1996) сделали вывод, что вегетативная нейропатия является независимым фактором риска смертности в случаях компенсированного и декомпенсированного цирроза [33].
Таким образом, имеющиеся данные свидетельствуют о целесообразности изучения наличия и степени выраженности вегетативных дисфункций у больных ЦП. В то же время данные об особенностях объективной оценки вегетативных дисфункций при помощи анализа вариабельности ритма сердца у больных с ЦП, особенно в отечественной медицине, крайне малочисленны, что обусловило актуальность настоящего исследования.
Целью исследования было оценить частоту и выраженность синдрома вегетативной дисфункции у больных циррозом печени вирусной этиологии разной степени тяжести.
Материалы и методы исследования
Было обследовано 103 пациента с ЦП вирусной этиологии. Контрольную группу составили 35 пациентов, пол и возраст которых соответствовали аналогичным характеристикам больных в испытуемых группах. Для изучения частоты клинических проявлений, наличия и выраженности вегетативной дисфункции пациенты были разделены на 3 группы в зависимости от степени тяжести цирроза печени по критериям Чайлда–Пью. В первую группу вошли пациенты с компенсированным ЦП (класс А), оценка по критериям Чайлда–Пью составила 5–6 баллов (36 больных — 34,9%). Во вторую группу вошли пациенты с субкомпенсированным циррозом (класс B), оценка по критериям Чайлда–Пью составила 7–9 баллов (34 человека — 33%). В третью группу вошли пациенты с декомпенсированным циррозом (класс С), оценка по критериям Чайлда–Пью составила 10–15 баллов (33 человека — 32,1%).
Результаты и обсуждение
При опросе пациенты жаловались на слабость, быструю утомляемость, снижение работоспособности, нарушения сна в виде сонливости днем и бессонницы ночью; периодически отмечались головокружения в ортостазе. Из других вегетативных жалоб реже встречались нарушения моторики кишечника в виде чередования запоров и поносов, нарушения мочеиспускания (поллакиурия, недержание мочи). Частота встречаемости жалоб нарастала с увеличением тяжести ЦП, что отражено в табл. 1.
Показатели состояния системы регуляции сердечного ритма у исследуемых пациентов с ЦП подтвердили усиление симпатической активности и ослабление парасимпатической активности по всем параметрам, при этом симпатическое влияние усиливалось при нагрузке. Индексы регуляторных систем вегетативной нервной системы (индекс напряжения и индекс вегетативной регуляции) достоверно указывали на преобладание симпатикотонии в покое и в активном ортостазе. Степень напряжения регуляторных систем распределилась следующим образом: удовлетворительная адаптация (норма) в покое выявлена у 21 (58,3%) пациентов первой группы, у 16 (47%) больных второй группы, у 8 (24,2%*) человек из третьей группы и у 33 (94,2%) человек контрольной группы; состояние функционального напряжения, проявляющееся мобилизацией защитных механизмов, в том числе повышением активности симпатоадреналовой системы, регистрировалось в покое у 13 (36,1%) пациентов первой группы, у 15 (44,2%) больных второй группы, у 20 (60,7%*) человек третьей группы и только у 1 пациента (2,9%) из группы контроля. Также оценивались аналогичные показатели при нагрузке (в активном ортостазе): удовлетворительная адаптация выявлена у 21 (58,3%) пациента из первой группы, у 10 (29,4%*) больных из второй, у 4 (12,1%*) человек из третьей группы; состояние функционального напряжения отмечено у 14 (38,9%) больных из первой группы, у 21 (61,8%) пациента из второй и у 19 (57,6%*) человек из третьей группы; в третьей группе у 10 (30,3%) пациентов выявлено состояние перенапряжения, для которого характерны недостаточность адаптационных защитно-приспособительных механизмов и их неспособность обеспечить адекватную реакцию организма на воздействие различных факторов (*р ≤ 0,05 в отличие от первой группы). Сравнительные данные математического анализа сердечного ритма представлены в табл. 2.
Все обследованные пациенты получали комплексное лечение своего заболевания. В качестве базовой терапии в зависимости от показаний — лактулозу (Дюфалак, производства Эбботт Биолоджикалз Б. В., Нидерланды) 15–45 мл в сутки до достижения трехкратного мягкого стула; анаприлин 10 мг 4 раза в сутки или карведилол 12,5 мг 2 раза в сутки, L-орнитин-L-аспартат (Гепа Мерц, производства Мерц Фарма ГмбХ и Ко.КГаА., Германия) 5 мг 3 раза в сутки (при более выраженной печеночной энцефалопатии внутривенные инфузии до 40 мл в сутки); рифаксимин (Альфа Нормикс, производства Альфа-Вассерманн С.п.А, Италия); курсами по 800–1200 мг в сутки; спироналактон и фуросемид в дозах, обеспечивающих положительный диурез; по показаниям — инфузии альбумина, плазмы, эритроцитарной массы, реополиглюкина, ремаксола; кортикостероиды; пентоксифиллин; урсодезоксихолевую кислоту (Урсосан, производства ПРО.МЕД.ЦС Прага а.о., Чехия); силимарин (Легалон, производства Мадаус АГ, Германия). По показаниям некоторые пациенты получали противовирусное лечение.
Большинство пациентов, которых мы обследовали, в качестве гепатопротектора получали S-аденозил-L-метионин (препарат Гептрал производства компании Hospira, S.p.A., Италия). S-аденозил-L-метионина в гепатологии применяется главным образом в следующих областях [35]:
- острые и хронические заболевания печени, протекающие с синдромом внутрипеченочного холестаза;
- лекарственные гепатиты;
- алкогольная болезнь печени:
- жировой гепатоз;
- алкогольный гепатит;
- фиброз печени;
- цирроз печени;
- острая печеночная недостаточность.
Опыт перорального и парентерального применения S-аденозил-L-метионина, накопленный на протяжении более чем 20 лет, показал, что препарат эффективен в лечении внутрипеченочного холестаза при заболеваниях печени и беременности. До настоящего времени более 2700 пациентов с внутрипеченочным холестазом и/или хроническими заболеваниями печени принимали участие в клинических исследованиях адеметионина и 1983 из них принимали этот препарат. В большинстве этих исследований адеметионин сравнивали с плацебо ввиду практически полного отсутствия альтернативной терапии. Почти в 90% случаев холестатический компонент был связан с хроническими заболеваниями печени. Остальные пациенты были с алкогольным поражением печени, острым и хроническим гепатитом или внутрипеченочным холестазом беременных. Параметры эффективности, которые использовались в клинических исследованиях, включали основные субъективные симптомы холестаза (зуд, желтуха, утомляемость), биохимические маркеры холестаза и повреждения печени, такие как общий и конъюгированный билирубин, щелочная фосфатаза, желчные соли, трансаминазы, гамма-глутамилтрансфераза. При внутривенном, внутримышечном или пероральном применении адеметионина уменьшалась выраженность проявления внутрипеченочного холестаза при хронических заболеваниях печени, холестазе беременных и алкогольном ЦП. Эффективность внутривенного или внутримышечного введения адеметионина проявляется через 1–2 недели терапии, тогда как назначение адеметионина перорально подходит для поддерживающей терапии [35].
В продолжительном двойном слепом плацебо-контролируемом исследовании при участии 123 мужчин и женщин с алкогольным циррозом печени было выявлено, что применение адеметионина в дозе 1200 мг/сут на протяжении 2 лет может улучшать выживаемость и удлинять период до необходимости трансплантации печени эффективнее, чем плацебо [36]. В целом смертность или необходимость трансплантации печени в конце исследования уменьшилась с 30% в группе плацебо до 16% в группе адеметионина, хотя различие было статистически не значимо. Продолжительное применение адеметионина уменьшает смертность или необходимость трансплантации печени, особенно у больных с менее выраженным заболеванием печени.
В результате лечения S-аденозил-L-метионином нормализуется текучесть (проницаемость) клеточных мембран, повышается активность Na + /K + -АТФазы, увеличивается энергетический потенциал клетки и таким образом улучшается захват компонентов желчи из крови, их внутриклеточный транспорт и выделение в канальцы. В клетках увеличивается синтез и содержание тиолов (глутатиона, таурина, сульфатов), которые обладают защитным действием от цитотоксического эффекта свободных радикалов, желчных кислот и других токсических компонентов, поступающих или образующихся в гепатоците, в том числе и биологических субстанций, ответственных за появление кожного зуда [37, 38].
Основными показаниями для назначения S-аденозил-L-метионина является гепатоцеллюлярный и/или каналикулярный холестаз, в механизме которого ведущая роль принадлежит следующим факторам:
1) снижению текучести (проницаемости) базолатеральной и/или каналикулярной мембраны гепатоцитов в результате алкогольных и лекарственных поражений печени, а также при беременности;
2) ингибированию Na + /K + -АТФазы и других мембранных переносчиков при токсических воздействиях на печень (лекарства, бактериальные субстанции, эндотоксины, например, при сепсисе);
3) нарушению целостности цитоскелета, включая каналикулы с блокадой внутриклеточного и каналикулярного транспорта компонентов желчи при острых и хронических гепатитах и циррозах печени различного генеза, при сепсисе, при возвратном (доброкачественном) внутрипеченочном холестазе, при эндотоксемии, при использовании пероральных контрацептивов [39, 40].Эффективность S-аденозил-L-метионина в лечении холестатических заболеваний печени, в основе которых лежат аутоиммунные повреждения эпителия билиарных протоков с их некрозами и облитерацией (первичный билиарный цирроз, первичный склерозирующий и аутоиммунный холангит, идиопатическая дуктопения, склерозирующий холангит после трансплантации печени и др.), оценивается неоднозначно. Если на ранней стадии первичного билиарного цирроза ряд авторов отмечали положительный эффект от назначения препарата (уменьшение зуда, снижение активности щелочной фосфатазы), то при развернутой картине болезни наблюдалось лишь кратковременное улучшение [41].
S-аденозил-L-метионин (Гептрал) нашим пациентам мы назначали вначале парентерально по 800 мг внутривенно или внутримышечно в течение 10–14 дней, а затем по 400 мг (1 таблетка) 2 раза в день. Продолжительность курса лечения составляла в среднем 1–2 месяца.
Выводы
Показатели состояния системы регуляции — частотный, спектральный анализ ритма сердца — у исследуемых пациентов с ЦП подтвердили усиление симпатической активности и ослабление парасимпатической активности по всем параметрам, степень выраженности которых у больных нарастала от класса А к классу С, при этом симпатическое влияние усиливалось при нагрузке. Исходя из вышеизложенного, возникает необходимость раннего выявления и коррекции вегетативных нарушений у исследуемых групп больных. В качестве основного гепатопротектора мы рекомендуем назначать S-аденозил-L-метионин (Гептрал).
Литература
Е. Ю. Плотникова*, доктор медицинских наук, профессор
Е. Н. Баранова*
М. В. Краснова**, кандидат медицинских наук
К. А. Краснов**, кандидат медицинских наук*ГБОУ ВПО КемГМА МЗ РФ, **Кузбасский областной гепатологический центр МБУЗ ГКБ № 3 им. М. А. Подгорбунского, Кемерово
Энцефалопатия определяется как патологическое изменение функций головного мозга невоспалительного генеза, вызванное различными факторами и проявляющееся разнообразными нервно-психическими нарушениями. Под термином печеночная энцефалопатия (ПЭ) понимают весь комплекс церебральных нарушений, развивающихся вследствие острого или хронического поражения печени. Потенциально обратимые неврологические и психические нарушения варьируют по интенсивности и могут наблюдаться в различных комбинациях, что позволяет выделить стадии ПЭ, которые, по сути, с учетом их обратимости, являются степенями тяжести.
острое или хроническое заболевание печени, сопровождающееся выраженным снижением ее детоксицирующей функции;
формирование функциональных или анатомических шунтов между системами портального и общего кровообращения, ведущее к проникновению токсических продуктов кишечного происхождения в головной мозг.
Знание указанных механизмов дает врачу возможность в определенной степени предвидеть развитие ПЭ у пациента с тем или иным патологическим состоянием. Так, при фульминантной печеночной недостаточности ПЭ наблюдается почти у всех больных, после хирургического наложения портокавального шунта - у 25-40%. У больных циррозом в патогенезе ПЭ участвуют как "внутренний", так и "внешний" механизмы, что ведет к развитию клинически манифестной энцефалопатии у 30-50%, а латентной - у 50-70%.
Знание патогенетических факторов ПЭ важно для выбора оптимального метода лечения.
Многолетнее изучение патогенеза ПЭ позволяет прийти к выводу, что, по всей видимости, рассмотренные механизмы действуют в комплексе. Комбинация неблагоприятных факторов у больного с острой или хронической патологией печени ведет к развитию комплекса нервно-психических нарушений, обозначаемых как ПЭ.
Вместе с тем многочисленные результаты исследований дают основание утверждать роль аммиака, как одного из важнейших нейротоксических метаболитов. Наиболее значительные количества аммиака образуются вследствие дезаминирования аминокислот в печени; в качестве дополнительных его источников могут выступать мышцы, почки и пищеварительный тракт. Являясь основным источником аммиака, печень в то же время служит главным местом его обезвреживания за счет синтеза мочевины в функционирующем в перипортальных гепатоцитах орнитиновом цикле. Меньшая часть аммиака участвует в синтезе глутамина в перивенозных гепатоцитах, мышцах и головном мозге.
Заболевания печени ведут как к снижению скорости детоксикации аммиака, так и к избыточному поступлению последнего в системную циркуляцию за счет портокавального шунтирования. Накопление аммиака в головном мозге обусловливает нарушение синтеза белков астроцитов, снижение активности нейрональных хлорных каналов, подавление образования АТФ и возбуждающих нейротрансмиттеров - глутамата и аспартата.
Важное значение для клинициста имеет знание разрешающих (триггерных) факторов, действие которых приводит к дебюту или углублению выраженности ПЭ.
ПЭ представляет собой гетерогенную группу состояний, которая подразделяется на 5 форм.
Цирроз печени вследствие развития портальной гипертензии и печеночной недостаточности ведет к портосистемной ПЭ (ПСЭ) в одном из указанных вариантов, которые могут переходить один в другой. Вместе с тем ПСЭ у больных циррозом следует дифференцировать с псевдо-ПСЭ, описанной H. Kalk в 1958 г. и известной также под названиями "ложная печеночная кома" и "электролитная кома". Ведущая роль в патогенезе псевдо-ПСЭ принадлежит электролитному дисбалансу, представленному гипокалиемией и/или гипонатриемией, а также гипомагниемией, обусловливающим гипотоническую дегидратацию клеток головного мозга. Наиболее частая причина "электролитной комы" - передозировка петлевых диуретиков.
частота латентной ПСЭ у больных циррозом достигает 50-70%, то есть представляет собой наиболее частое осложнение заболеваний печени вне зависимости от этиологии;
латентная ПСЭ сопровождается неадекватной реакцией пациента в экстремальных условиях, в том числе при вождении автомобиля, что сопряжено с повышенным риском создания аварийных ситуаций.
С целью ранней диагностики ПСЭ в клинической практике широко применяются психометрические тесты: связи чисел, число-буква, линии, почерка, арифметический и др.
Следует учитывать, что за простотой и удобством психометрических тестов скрываются определенные недостатки, к которым в первую очередь относится влияние на их результаты многочисленных экзогенных и эндогенных факторов. Вероятность гиподиагностики ПСЭ можно свести к минимуму, используя несколько тестов у одного пациента и интерпретируя результаты в комплексе.
Острая и подострая рецидивирующая формы ПСЭ проявляются клинической манифестацией энцефалопатии у больного хроническим заболеванием печени. Как правило, у таких пациентов имеется фоновая латентная ПСЭ, которая остается нераспознанной при отсутствии целенаправленного диагностического поиска. Манифестация может быть различной степени выраженности - от I до IV стадии (ниже) и нередко, хотя и не всегда, обусловлена действием одного или нескольких триггерных факторов. Элиминация разрешающего фактора и терапевтические мероприятия обычно ведут к ликвидации всех клинических симптомов.
Хроническая персистирующая ПСЭ наблюдается редко, преимущественно у больных с выраженными портосистемными коллатералями, в том числе созданными в результате хирургического вмешательства. Помимо типичной психоневрологической симптоматики, наблюдаются постепенно проявляющиеся симптомы миелопатии: атаксия, хореоатетоз, параплегия, колющие или сверлящие боли. Нарушения обычно необратимы и ведут к церебральной атрофии и деменции.
Определение стадии ПЭ имеет важное значение для оценки прогноза пациента, так как этот критерий входит в наиболее надежную систему определения тяжести цирроза - функциональную классификацию Чайлд-Пью. Как уже отмечалось, стадии ПЭ, в сущности, являются степенями тяжести ввиду их потенциальной обратимости.
Достаточно характерен для ПЭ II-III стадии т.н. хлопающий тремор или астериксис, проявляющийся быстрыми сгибательными и разгибательными движениями в лучезапястных суставах.
ПЭ также сопровождается изменениями ЭЭГ, которые становятся явными на II стадии: уплощение кривой a-ритма, затем появление t- и d-активности. При ПЭ 0-I стадии ЭЭГ-диагностика осуществляется с использованием зрительных вызванных потенциалов.
Для оценки состояния сознания больного с ПЭ, в том числе в динамике на фоне терапии, может также применяться шкала Глазго. Сумма баллов определяет сознание пациента от ясного (15 баллов) до атонической комы (3 балла).
Эндогенная печеночная кома (вследствие потери паренхимы печени) имеет худший прогноз по сравнению с экзогенной (вследствие сброса нейротоксинов кишечного происхождения по портосистемным шунтам).
Важнейшее значение принадлежит объему остаточной паренхимы печени (косвенно определяется по выраженности печеночной недостаточности).
Следует учитывать возможность и скорость элиминации триггерных факторов; в первую очередь это относится к остановке желудочно-кишечного кровотечения.
1. Элиминация этиологического фактора заболевания печени - в тех случаях, когда это возможно (например, в случае алкогольного цирроза). При циррозах вирусной этиологии назначение a-интерферона нередко вызывает усиление ПЭ, что ограничивает его применение. Однако при циррозе в исходе HBV-инфекции может с успехом применяться нуклеотидный аналог ламивудин, подавляющий активность вируса и, как следствие, улучшающий функциональное состояние печени.
2. Элиминация триггерных и отягощающих факторов ПЭ: остановка кровотечения, коррекция гиповолемии, поддержание кислотно-щелочного и электролитного баланса, ликвидация инфекции и т.д.
3. Санация кишечника. Очищение толстой кишки преследует цель удаления азотсодержащих субстанций, особенно важного в случаях желудочно-кишечного кровотечения, пищевой перегрузки белком и запора.
Эффективно применение высоких клизм, позволяющих очистить толстую кишку на максимальном протяжении, вплоть до слепой. Это может быть достигнуто путем перемены положения тела пациента: введение раствора начинают в положении больного на левом боку, затем продолжают в позиции на спине с приподнятым тазом и завершают в положении на правом боку. Общий объем вводимого раствора должен быть не менее 1000 мл дважды в день. В качестве растворов применяются натриево-ацетатный буфер (рН 4,5) или лактулоза (300 мл на 700 мл воды).
Пероральные слабительные при выраженной ПЭ лучше вводить через назогастральный зонд. Инфузия 1000 мл 10%-ного раствора маннитола в течение 60-90 минут, вызывая осмотическую диарею, обеспечивает практически полную элиминацию кишечного содержимого на протяжении последующих 3-4 часов. В случае желудочно-кишечного кровотечения маннитол следует вводить через зонд до выделения чистого раствора из прямой кишки. Помимо маннитола, могут применяться 20-30%-ный сульфат магния (50-100 мл), а также комплексный раствор, состоящий из гидрокарбоната натрия, хлорида натрия, хлорида калия, сульфата натрия и полиэтиленгликоля.
4. Диета. У больных с любой стадией ПЭ целесообразно ограничение поступления белка с пищей. При латентной ПЭ белок рекомендуется ограничить приблизительно до 40 г/сут (0,6 г/кг массы тела), на I-II стадии - до 30 г/сут (0,4 г/кг). На III-IV стадиях оптимален перевод пациента на зондовое и парентеральное питание с содержанием белка около 20 г/сут. Белок в рационе больного ПЭ должен быть представлен преимущественно протеинами растительного происхождения и лактальбумином ввиду их лучшей переносимости. Растительные белки более богаты орнитином и аргинином и содержат меньше метионина и ароматических аминокислот. В отдельных случаях из рациона должны быть полностью исключены мясо, рыба, яйца и сыры. В то же время длительное и резкое ограничение белка способствует распаду эндогенных протеинов, что ведет к повышению концентрации азотсодержащих соединений в крови, поэтому поступление пищевого белка после улучшения состояния следует увеличивать в среднем на 10 г в 3 дня. После ликвидации признаков ПЭ (в том числе по результатам психометрических тестов) суточное количество белка может быть доведено до 80-100 г/сут (1-1,5 г/кг). Необходимо учитывать, что у каждого больного циррозом свой порог переносимости пищевого белка, и при белковой интолерантности его дефицит нужно восполнять парентеральными инфузиями.
Калорийность пищи (1800-2500 ккал/сут) обеспечивается адекватным поступлением жиров (70-140 г) и углеводов (280-325 г). Углеводы способствуют уменьшению концентрации аммиака и триптофана в плазме, однако следует помнить, что больным циррозом свойственно развитие нарушения толерантности к глюкозе, что иногда требует назначения инсулина. Применение фруктозы, сорбитола и ксилитола нецелесообразно вследствие повышенного риска лактат-ацидоза.
Пища больного циррозом должна также содержать адекватные количества витаминов и микроэлементов; при нарушении всасывания жирорастворимых витаминов показано их парентеральное введение.
Лактулоза. Представляя собой невсасывающийся дисахарид (1,4-b-галактозид-фруктоза), лактулоза снижает внутрикишечный рН, препятствует размножению бактерий-аммониепродуцентов, всасыванию аммиака и аминосодержащих соединений, расщеплению глутамина в слизистой кишке. Лактулоза назначается 2-3 раза в сутки, дозировка препарата индивидуальна; в качестве простого, но надежного критерия эффективности рассматривается увеличение частоты стула до 2-3 раз в сутки. Наступление этого эффекта отражает снижение рН толстой кишки < 6,0.
Побочные эффекты лактулозы включают тошноту, рвоту, потерю аппетита, вздутие живота, диарею и тенезмы. Длительная диарея может приводить к дегидратации и электролитному дисбалансу, поэтому при подборе дозы следует придерживаться правила, относящегося к частоте стула: "не реже чем два, не чаще чем три". Некоторые пациенты плохо переносят лактулозу из-за ее сладкого вкуса; для улучшения вкусовых качеств рекомендуется добавление лимонного сока.
стимуляции ферментов, участвующих в детоксикации аммиака - орнитин-карбамоил-трансферазы и глутаминсинтетазы;
включении орнитина и аспартата в качестве субстратов в орнитиновый цикл мочевинообразования Кребса (образование мочевины из аммиака).
Стандартная схема применения предусматривает внутривенное капельное введение 20-30 г препарата в течение 7-14 дней с последующим переходом на пероральный прием 9-18 г в сутки. При длительном применении (6-месячный курс по 9 г в сутки перорально) препарат эффективно предотвращает рецидивы ПЭ.
Бензоат и фенилацетат натрия с успехом используются для лечения пациентов с врожденными дефектами ферментов орнитинового цикла. Способность препаратов к связыванию аммиака в крови служит основанием для его применения у больных ПЭ, однако эффект их непродолжителен.
Аминокислоты с разветвленной цепью (АКРЦ). Хотя аминокислотный дисбаланс рассматривается в качестве одного из патогенетических факторов ПЭ, корреляции между соотношением ароматических аминокислот и АКРЦ, с одной стороны, и выраженностью ПЭ, с другой, не обнаружено. Вероятно, положительный клинический эффект инфузий АКРЦ обусловлен уменьшением белкового катаболизма в печени и мышцах, а также улучшением обменных процессов в головном мозге. Следует учитывать, что АКРЦ являются важным источником белка для больных с ПЭ, которым требуется ограничение пищевого белка. Рекомендуемая дозировка - 0,3 г/кг/сут.
Антибиотики назначаются с целью подавления аммониепродуцирующей кишечной микрофлоры. Неомицин (доза 6-8 г/сут) и паромоцицин (3-4 г/сут) в настоящее время применяются редко ввиду их ото- и нефротоксичности. В последние годы предпочтение отдается более безопасному рифаксимину (суточная доза 1200 мг, длительность курса 1-2 недели). К другим антибиотикам, применяемым у больных ПЭ, относятся ципрофлоксацин, метронидазол и рифаксимин.
Рассматривая возможность назначения антибиотиков больным с ПЭ, важно учитывать не только их побочное действие, но и соотношение стоимость/эффективность. Можно констатировать, что терапевтическая ниша антибиотиков при ПЭ представлена двумя группами пациентов: нуждающимися в усилении действия лактулозы; не переносящими стандартную терапию.
Флумазенил - антагонист бензодиазепиновых рецепторов - назначается внутривенно струйно в дозе 0,2-0,3 мг, затем капельно 5 мг/ч. После улучшения состояния больного осуществляется переход на пероральный прием в дозе 50 мг/сут. Эффективность препарата выше, если причиной манифестации ПЭ явился прием барбитуратов или бензодиазепинов.
Литература
1. Ивашкин В.Т., Надинская М.Ю., Буеверов А.О. Печеночная энцефалопатия и методы ее метаболической коррекции. Бол. орг. пищевар. 2001; 3: 25-7.
2. Лебезев В.М., Губский Л.В. Печеночная энцефалопатия при хирургическом лечении больных с портальной гипертензией. Клин. мед. 1995; 73: 37-9.
3. Conn H.O., Bircher J. (eds.). Hepatic encephalopathy: syndromes and therapies. Bloomington, Illinois: Medi-Ed Press 1994: 243 p.
4. Hepatic encephalopathy. In: Kuntz E., Kuntz H.-D. Hepatology. Principles and practice. Springer 2002: 234-54.
5. Plauth M., Egberts E.-H. Was ist gesichert in der therapie der hepatischen enzephalopathie? Internist 1993; 34: 35-42.
6. Stauch S., Kircheis G., Adler G. et al. Oral L-ornithine-L-aspartate therapy of chronic hepatic encephalopathy: results of placebo-controlled double-blind study. J. Hepatol. 1998; 28: 856-64.Читайте также:

