Интоксикация мозга после операции
Обновлено: 19.04.2024
Посттравматическая энцефалопатия – это состояние, включающее комплекс психических и неврологических расстройств, обусловленных развитием в течение года или более стойких последствий перенесенной черепно-мозговой травмы вследствие рубцовых, атрофических, дистрофических и дегенеративных изменений ткани мозга. Проявления и степень выраженности зависят от локализации и тяжести травмы, возраста больного, эффективности лечения, наличия или отсутствия сосудистых нарушений, хронических интоксикаций, в том числе алкогольной.
В развитии заболевания можно выделить следующие этапы:
- Непосредственное поражение нервной ткани (как правило, лобных и височных долей) в момент травмы.
- Изменение кровоснабжения мозга вследствие отёка головного мозга.
- Нарушение циркуляции спинномозговой жидкости из-за сдавления желудочков.
- При отсутствии регенерации нервных клеток происходит замещение их соединительной тканью с образованием рубцов и спаек.
- Патологический ответ иммунной системы, которая начинает воспринимать собственные нервные клетки как чужеродный агент (аутонейросенсибилизация).
Самый первый сигнал, говорящий о возможных посттравматических изменениях, это нарушения памяти. Другой распространенный симптом – проблемы с вниманием и концентрацией. Помимо этого, встречаются нарушения мышления, которые сказываются в медлительности реакции, неспособности к анализу, логике и другим инструментам когнитивных процессов.
Также возможно появление вегетативных симптомов. Беспричинные приступы рвоты и тошноты, головные боли и головокружения, скачки артериального давления, бледность, холодный пот.
Наиболее частым проявлением энцефалопатии травматического генеза является головная боль. Характерны также головокружение, нарушения сна, слабость, снижение работоспособности, повышенная утомляемость, эмоциональная лабильность (неустойчивое, резко меняющееся настроение), болезненная чувствительность к слабым раздражителям (звукам, свету и т.д.). Возможны ипохондрические и депрессивные расстройства.
Кроме психоэмоциональных расстройств, при посттравматической энцефалопатии может развиваться ряд синдромов:
Гипертензионно-гидроцефальный синдром (посттравматическая внутричерепная гипертензия). Проявляется головной болью с тошнотой и рвотой, приступообразными вегетативными нарушениями.
Эписиндром (посттравматическая эпилепсия). Возникает вследствие очагового поражения или спаечно-рубцовых изменений в головном мозге. Характерны приступы различных форм — как с утратой сознания, так и без таковой.
Посттравматический паркинсонизм. Развивается в результате длительной гипоксии мозга в период травмы. Отмечается постоянное устойчивое повышение мышечного тонуса по экстрапирамидному типу, акинезия (малоподвижность в силу скованности).
Посттравматическая вестибулопатия. Сопровождается головокружениями, рвотой, тошнотой, неуверенностью при стоянии и ходьбе.
В исходе травм средней и тяжелой степени могут формироваться двигательные, речевые дефекты различной выраженности, расстройства чувствительности, тазовые нарушения.
Для подтверждения диагноза необходимо выполнить компьютерную или магниторезонансную томографию, нейропсихологическое тестирование. При этих исследованиях врач получает детальную информацию об очаговых или диффузных изменениях вещества головного мозга. Кроме того, это позволяет исключить другую патологию центральной нервной системы, сопровождающуюся сходной симптоматикой.
В качестве дополнительного метода обследования желательно выполнить электроэнцефалографию, которая помогает выявить патологический очаг эпилептической активности и скорректировать на основе полученных данных лечение.
Лечение посттравматической энцефалопатии должно быть направлено на нейропротекцию (защиту нервных клеток от негативных факторов), нормализацию процессов циркуляции крови, а также восстановление всех когнитивных функций и метаболизм клеток мозга. Также важно симптоматическое лечение, особенно при наличии синдрома гидроцефалии (необходимы специфические средства, снимающие отек мозга), эпилепсии (требуется хороший подбор противоэпилептических препаратов и их доз). Курсы такой комплексной терапии, в зависимости от выраженности проявлений посттравматической энцефалопатии, следует проводить 1-2 раза в год.
Прогноз для жизни, трудоспособности и способности к самообслуживанию, как правило, становится ясен в течение первого года после травмы. Именно в это время важно проводить комплексные реабилитационные мероприятия. Оставшийся неврологический и физический дефицит спустя указанное время достаточно сложно поддается дальнейшей коррекции. Однако даже в случае наличия грубых нарушений их следует пытаться компенсировать в той или иной степени.
Осложнения наркоза – это непредусмотренные негативные эффекты, возникающие в ходе общего обезболивания или вскоре после пробуждения. Проявляются в форме дыхательной недостаточности, нарушений кровообращения, чрезмерного угнетения ЦНС, рвоты, регургитации. После пробуждения возможно развитие психозов, галлюцинаторного синдрома, парезов и параличей. В некоторых случаях выявляется динамическая непроходимость кишечника. Диагноз устанавливается на основании клинических признаков, данных аппаратного мониторирования жизненных функций, лабораторного исследования биологических сред организма.
МКБ-10
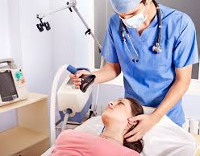
Общие сведения
Осложнения наркоза относятся к категории ятрогенных состояний, возникающих в результате действий медицинского работника. Чаще всего являются предотвратимыми при достаточном объеме профилактических мероприятий и тщательной подготовке врача-анестезиолога к оперативному вмешательству. Число непредусмотренных проблем с каждым годом снижается. По данным за 1956 год, летальность по причинам, связанным с общим обезболиванием, достигала 15%. Сегодня этот показатель не превышает 0,02% при использовании эндотрахеального метода подачи смеси, современных анестетиков, непрерывного мониторирования состояния пациента. Количество нелетальных проблем, по статистике за 2014 год, достигает 2,5%.

Причины
Абсолютное большинство проблем, возникающих в ходе анестезии, вызвано неправильными действиями анестезиолога или медсестры-анестезиста. Осложнения наркоза также могут быть обусловлены нарушением рекомендаций врача со стороны больного. Манифестация аллергических реакций, которые невозможно предусмотреть, встречается лишь в 1% случаев от общего числа жизнеугрожающей патологии. Еще реже диагностируется злокачественная гипертермия – состояние мышечного гиперметаболизма, развивающееся как реакция на введение миорелаксантов деполяризующего действия. Причины патологии удобнее рассматривать по системам организма:
Патогенез
Механизм развития зависит от типа осложнения наркоза. При гиповентиляции наблюдается гипоксия и гиперкапния, нарушаются метаболические процессы в тканях организма, имеет место респираторный ацидоз. Отмечается расстройство жизненно важных реакций. При критическом снижении АД развивается шоковое состояние, централизация кровообращения, уменьшается тканевая перфузия, снабжение органов и систем кислородом, питательными веществами. На фоне недостаточности кровообращения наступают обратимые, а потом необратимые изменения в структуре тканей центральной нервной системы.
При чрезмерном угнетении ЦНС происходят сбои в регуляции работы внутренних органов, в том числе сердца, легких, печени, почек. Рвота – результат раздражения соответствующего центра. При эндотрахеальном методе подачи наркозного средства не представляет значительной опасности. Если пациент находится на самостоятельном дыхании, существует риск аспирации рвотных масс. Осложнениями аспирации становятся пневмонии, повреждение трахеи и бронхов кислым желудочным содержимым.
Классификация
Деление всех возможных осложнений производится по признакам поражения той или иной системы. Принято разграничивать 5 основных групп, каждая из которых включает в себя несколько разновидностей патологических состояний. Наиболее опасно поражение дыхательной системы и системы кровообращения. Выделяют следующие типы негативных реакций, встречающихся во время общей анестезии или после нее:
- Поражение органов дыхания. Возникает чаще всего. Проявляется в форме механической асфиксии при западении языка, ларингоспазме, обструкции дыхательных путей рвотными массами, мокротой, кровью. При внутривенной анестезии без интубации возможна блокировка дыхательного центра на фоне превышения допустимой дозы медикаментов или индивидуальной реакции.
- Поражение системы кровообращения. Основные проявления – тахикардия, экстрасистолия, фибрилляция предсердий или желудочков. Возможно развитие острой сердечной недостаточности, при которой сердце перестает справляться с нагрузкой. Изменения сосудистого тонуса приводят к гипотонии или гипертонии, могут осложняться компенсаторными реакциями, в частности – тахиаритмией, инфарктом миокарда.
- Поражение ЦНС. Глубокие повреждения головного мозга сопровождаются угнетением самостоятельного дыхания, чрезмерным погружением в наркоз, что осложняет выход из него. При нейрогенном нарушении кровообращения мозг подвергается гипоксии, что впоследствии провоцирует постгипоксическую энцефалопатию. Специфические эффекты некоторых препаратов – бред, галлюцинации, психомоторное возбуждение на стадии погружения в наркоз или выхода из него, мышечная гиперреактивность. Встречаются при использовании кетамина, пропофола, ингаляционных анестетиков.
- Поражение ЖКТ. Симптомами являются рвота, послеоперационный парез кишечника. Рвота легко купируется введением противорвотных средств. При парезе развиваются запоры, требуются комплексные лечебные мероприятия. Парезы чаще всего наблюдаются после операций на кишечнике, при которых сочетается механическое и медикаментозное негативное воздействие на пищеварительную систему.
- Аллергические реакции. Осложнения такого типа не считаются ятрогенными, относятся к группе непредугадываемых происшествий. Могут проявляться в форме крапивницы (сыпь красного цвета, приподнятая над уровнем кожи), ангионевротического отека дыхательных путей или других участков тела больного, анафилактического шока. Последний является самой тяжелой реакцией на контакт с триггерным фактором, при отсутствии своевременной диагностики часто приводит к гибели пациента.
Симптомы осложнений наркоза
Дыхательные нарушения проявляются в виде классических признаков гипоксии. Обнаруживается диффузный цианоз, компенсаторная тахикардия, возможно повышение уровня артериального давления. Снижается SpO2, нарастает гиперкапния. При накоплении мокроты слышны хрипы, бульканье. Аппаратура сигнализирует о недостаточной проходимости дыхательных путей. Объем вдоха уменьшается. Осложнения наркоза, вызванные поражением сердечно-сосудистой системы, приводят к увеличению или снижению частоты пульса выше 90 или ниже 60 ударов в минуту соответственно. При падении АД кожа бледная, покрыта холодным липким потом, слизистые синеватого цвета. Повышение давления в сосудах может сопровождаться как гиперемией, так и бледностью кожи, возникает при рефлекторном спазме капилляров.
Поражение ГМ при операции включают нарушения гемодинамики, сердечного ритма. Пробуждение затягивается. Сознание восстанавливается долго, часто не полностью. Менее тяжелые обратимые сбои диагностируются по наличию галлюциноза, неадекватного поведения. Больной не понимает, где находится, что с ним произошло, нецензурно бранится. Отсутствует критическая оценка действий. Нормальное состояние восстанавливается в течение нескольких часов. К числу симптомов поражения ЖКТ относят рвоту, тошноту, запоры или диарею, отсутствие шумов кишечника при аускультации.
Диагностика
Осложнения наркоза выявляет анестезиолог, ведущий пациента. Для этого проводится предоперационный и постоперационный осмотр. В процессе вмешательства врач неотлучно находится в изголовье больного, наблюдая за его состоянием и предпринимая меры по коррекции возникающих нарушений. Диагноз выставляется по клиническим признакам и результатам мониторирования. Степень тяжести имеющихся сбоев и особенности их течения определяют по информации, полученной лабораторными методами. Перечень диагностических мероприятий включает:
Лечение осложнений наркоза
Терапия проводится с учетом причин, вызвавших патологическое состояние. При респираторных нарушениях осуществляется корректировка состава и объема газовоздушной смеси, санация эндотрахеальной трубки с помощью электроотсоса. Если полностью очистить дыхательные пути не представляется возможным, вызывают дежурную эндоскопическую бригаду для проведения экстренной бронхоскопии. Для купирования ларингоспазма применяют наркотические анальгетики, атропин, спазмолитики, адреномиметики. Для насыщения крови O2 аппарат выставляют в режим усиленной оксигенации (100%). Поддержание сонного состояния обеспечивают за счет внутривенных анестетиков.
Нарушения со стороны ССС лечат посимптомно. При брадикардии требуется введение атропина, адреналина. Снижение АД на фоне ослабления сердечной деятельности – показание для перевода больного на введение прессорных аминов через шприц-насос. Может потребоваться снижение дозы анестезирующего средства. Аритмии купируют с использованием кордарона, амиодарона, новокаинамида, лидокаина. Фибрилляция, не поддающаяся химическому воздействию, требует проведения электрической дефибрилляции. При повышении АД вводятся антигипертонические средства, при снижении – гипотонические препараты, инфузионные растворы для восполнения ОЦК, стероидные гормоны.
Купирование кратковременных послеоперационных психозов медикаментозными средствами не выполняется. При выраженном психомоторном возбуждении допускается назначение нейролептиков, наркотических анальгетиков. Долговременные нарушения работы ЦНС требуют терапии с применением ноотропов, антиоксидантов, общеукрепляющих средств (поливитаминные комплексы, адаптогены). Тонус кишечника обычно восстанавливается самостоятельно за 1-2 дня. При затяжном течении пареза вводится прозерин.
Злокачественная гипертермия является показанием для введения датролена – миорелаксанта, способного блокировать рианодиновые рецепторы. Кроме того, назначают препараты симптоматического лечения, физические способы снижения температуры (лед на крупные сосуды, смачивание простыни и тела пациента холодной водой, вентилят ор). При аллергических реакциях вливают антигистаминные препараты, глюкокортикостероиды, симптоматические лекарственные средства. Тяжелые проявления требуют обязательной интубации трахеи, перевода на ИВЛ, если это не было сделано ранее.
Прогноз и профилактика
Прогноз по большинству осложнений благоприятный при их своевременном обнаружении. Лечебные мероприятия позволяют купировать явления дыхательной и сердечно-сосудистой недостаточности без отсроченных последствий. К необратимым изменениям приводит длительная гипоксия (постгипоксическая энцефалопатия или смерть мозга), ишемия миокарда (ОИМ). Тяжелые последствия в виде аспирационной пневмонии может иметь вдыхание рвотных масс. При отсутствии помощи прогноз неблагоприятный. Смерть пациента наступает от удушья, фибрилляции предсердий, шока.
Предотвратить осложнения наркоза можно при тщательном сборе анамнеза. Специалист выясняет, отмечались ли у больного или его родственников аллергические реакции на наркозные средства, эпизоды злокачественной гипертермии. Пациента информируют о запрете на употребление любой пищи за 10 часов до поступления в операционную. В ходе обезболивания анестезиолог поддерживает адекватную вентиляцию легких больного, глубину сна, отслеживает основные показатели жизнедеятельности и работу аппаратуры.
Токсическая энцефалопатия – это сочетание неврологических расстройств, обусловленных воздействием токсинов, ядов или производственных химикатов. Клинические проявления многообразны, зависят от этиологического фактора, могут включать в себя атактический и судорожный синдром, галлюцинации, расстройства речи, зрения, слуха и когнитивной сферы, поражения черепно-мозговых нервов, специфические кожные проявления. При диагностике используются данные анамнеза, результаты общего осмотра, лабораторных и инструментальных тестов. Лечение включает антидотную, дезинтоксикационную, патогенетическую и симптоматическую терапию.
МКБ-10
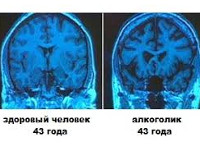
Общие сведения

Причины
Все токсические энцефалопатии возникают на фоне отравления организма токсичным для центральной нервной системы веществом. Причиной может быть как однократный контакт или прием (острые ТЭ), так и продолжительное насыщение токсином (хронические ТЭ). К наиболее распространенным причинам этой группы патологий относятся:
- Злоупотребление алкоголем, наркотики. Включает хроническое употребление больших доз алкоголя с последующим дефицитом витамина В1. Также токсическое влияние на ЦНС оказывают наркотические вещества – героин, кокаин, амфетамин и др.
- Работа на вредных производствах. Причиной энцефалопатии может стать продолжительный контакт с такими веществами как метанол, этиленгликоль, свинец, марганец, ртуть, фосфорорганические соединения, угарный газ при работе на заводе или в шахте. Возможно одномоментное получение большой дозы химиката при техногенных катастрофах, ошибочном употреблении в пищу.
- Бесконтрольный прием медикаментов. Чрезмерно высокие дозы или сочетание большого количества фармакотерапевтических средств могут оказывать пагубное воздействие на центральную нервную систему. Развитие ТЭ способны вызывать бензодиазепиновые производные, барбитураты, антидепрессанты, холинолитики и нестероидные противовоспалительные препараты (в первую очередь – салицилаты).
- Патологии печени и почек. Печень и почки – органы, отвечающие за утилизацию токсичных продуктов метаболизма. При выраженной почечной или печеночной недостаточности усиливается негативное воздействие экзогенных ядов, накапливаются естественные метаболиты, токсичные для ЦНС – аммиак, органические кислоты.
Патогенез
Механизмы развития различных форм токсических энцефалопатий досконально не изучены. Также не установлена четкая взаимосвязь между клиническими проявлениями и морфологическими изменениями в нервной системе. Принято считать, что в основе ТЭ лежит как прямое воздействие токсичного вещества, так и нарушение кровоснабжения головного мозга вследствие повреждения церебральных сосудов. Это, в свою очередь, приводит к дегенеративно-дистрофическим изменениям в тканях и отеку мозговых оболочек.
Возникают гемодинамические и ликвородинамические нарушения, что еще больше усугубляет токсическое и гипоксическое воздействие на ЦНС. В результате формируются диссеминированные участки некроза коры и подкорковых структур, фрагментации миелиновых оболочек. С учетом конкретного вещества могут выявляться определенные особенности, связанные с повышенной восприимчивостью некоторых структур нервной системы и способностью соединений накаливаться в различных органах.
Тетраэтилсвинец и ртуть могут депонироваться в паренхиматозных органах и нервной системе. При сатурнизме наблюдается повреждение нейронов в ЦНС, сегментарная демиелинизация с последующим аксональным поражением периферических нервов. Ртуть оказывает токсическое действие на нейроны коры затылочных долей и гранулярные клетки мозжечка, патология сопровождается аксональной дегенерацией и демиелинизацией периферических нервов. Угарный газ вызывает острую гипоксию головного мозга, взаимодействуя с гемоглобином и создавая стойкое соединение – карбоксигемоглобин.
ФОС вызывают нарушение функции ацетилхолинэстеразы, фермента одного из основных медиаторов ЦНС – ацетилхолина, что ведет к перевозбуждению М- и N-холинорецепторов. Сероводород оказывает негативное влияние путем связывания активных аминокислот, блокирования медьсодержащих энзимов, нарушения метаболизма серотонина, триптофана, никотиновой кислоты и витамина В6. При отравлении салицилатами и этиленгликолем ведущую роль играет формирующийся метаболический ацидоз.
Симптомы токсической энцефалопатии
Клинические проявления напрямую зависят от токсина, вызвавшего заболевание. При передозировке салицилатов вначале возникает общее недомогание, тошнота с рвотой, звон или шум в ушах, нарушение речи, звуковые и зрительные галлюцинации. Иногда наблюдается судорожный синдром, когнитивные расстройства, коматозное состояние. Отравление угарным газом сопровождается общемозговыми симптомами, нарушением памяти, галлюцинациями, атаксией, гипертонусом скелетных мышц, хореическими гиперкинезами и угнетением сознания.
Свинцовая ТЭ характеризуется сильной разлитой головной болью, общей слабостью, недомоганием, ухудшением памяти, статическим тремором, выраженным ухудшением зрения, центральными парезами и параличами. В некоторых случаях определяется поражение двигательных и смешанных черепных нервов, эпилептические приступы. Типичное проявление – лилово-серая кайма, возникающая вдоль зубного ряда (симптом Брутона). При отравлении этиленгликолем отмечается горизонтальный нистагм и общее состояние, имитирующее алкогольную интоксикацию. При тяжелом отравлении возникает судорожный синдром, сопорозное состояние или кома.
Острая алкогольная энцефалопатия характеризуется ярко выраженными общемозговыми симптомами, офтальмоплегией, страбизмом, нистагмом, выпадением сухожильных и периостальных рефлексов, гиперкинезами, мозжечковым нарушением координации движений, вегетососудистой дисфункцией и психическими расстройствами. При хронической форме алкогольной ТЭ возникают вегетативные и нейроэндокринные нарушения, бессонница или тревожные сны, тремор, деменция.
Диагностика
В процессе диагностики врач-невролог руководствуется анамнестическими сведениями, жалобами больного, результатами физикального, лабораторного и инструментального методов исследований. С учетом формы токсической энцефалопатии решающую роль в постановке заключительного диагноза могут играть различные диагностические методики. Общая программа обследования пациента с подозрением на ТЭ состоит из следующих пунктов:
- Сбор жалоб и анамнеза. Зачастую позволяет выявить токсическое вещество, спровоцировавшее нарушение состояния пациента. На вероятную этиологию могут указывать установленные в ходе беседы поражения других органов и систем. Акцентируется внимание на характере речи – наличии дизартрий, бессвязности сказанного.
- Внешний осмотр. При физикальном обследовании оценивается пульс, уровень артериального давления, состояние кожных покровов и видимых слизистых оболочек, объем активных и пассивных движений с целью поиска парезов, параличей и самопроизвольных мышечных подергиваний, тонус надкостных и сухожильных рефлексов. Исследуются функции черепных нервов, острота зрения и слуха на предмет быстро развивающейся слепоты и глухоты, нистагма и других симптомов.
- Общеклинические лабораторные тесты. В ОАК может определяться анемический синдром, лейкопения, нейтрофильный лейкоцитоз, панцитопения, базофильная зернистость эритроцитов и повышение СОЭ. В ОАМ могут выявляться свежие эритроциты, оксалаты, гиалиновые цилиндры, протеинурия, гематопорфирин и остатки тяжелых металлов. В биохимическом анализе крови отмечаются изменения водно-электролитного и кислотно-основного баланса, признаки нарушения порфиринового обмена.
- Электроэнцефалография.ЭЭГ применяется при наличии судорожного синдрома, глубокого нарушения сознания. На электроэнцефалограмме могут присутствовать медленные волны высокой амплитуды, угнетение α-ритма, общее подавление биоэлектрической активности или проявления судорожных очагов.
- Дополнительные методы диагностики. С учетом клинической ситуации и необходимости дифференциальной диагностики с другими патологиями дополнительно назначается электромиография, спинномозговая пункция, компьютерная или магнитно-резонансная томография головного мозга, токсикологические исследование волос и ногтей.
Лечение токсической энцефалопатии
Целью лечения патологии является выведение из организма химического вещества, минимизация поражений головного мозга, коррекция неврологического дефицита. В зависимости от тяжести общего состояния пациента терапия проводится в отделении клинической неврологии или блока реанимации и интенсивной терапии, включает в себя следующие мероприятия:
- Эвакуация токсина из организма. При острых интоксикациях, спровоцированных попаданием химиката внутрь через ЖКТ, производится промывание желудка дистиллированной водой или специфическими реагентами, после чего применяются энтеросорбенты.
- Дезинтоксикационная терапия. Направлена на связывание или выведение токсина, циркулирующего в крови. Представлена внутривенной инфузией плазмозаменителей и специфических антидотов, хелатной терапией, гемодиализом.
- Симптоматическая и патогенетическая терапия. Может состоять из масочной ингаляции кислорода, искусственной вентиляции легких, назначения противоэпилептических и мочегонных препаратов, транквилизаторов, нестероидных противовоспалительных средств, кортикостероидов.
Прогноз и профилактика
Исход токсической энцефалопатии зависит от степени поражения ЦНС и свойств вещества. Выраженные интоксикации тяжелыми металлами, ФОС и этиленгликолем зачастую приводят к летальному исходу. Клинические проявления при отравлениях органическими растворителями могут самостоятельно регрессировать спустя несколько дней либо недель после прекращения контакта. Профилактика ТЭ основывается на соблюдении правил техники безопасности, использовании средств индивидуальной защиты при работе с токсическими веществами в быту и в условиях вредных производств, четком соблюдении рекомендаций врача при проведении медикаментозной терапии, отказе от вредных привычек.
3. Неврологические симптомы, синдромы и болезни. Энциклопедический справочник / Гусев Е.И., Никифоров А.С., Камчатнов П.Р. – 1999.
Раковая интоксикация – патологическое состояние, обусловленное распространенным онкологическим процессом и распадом злокачественной опухоли. Возникает на поздних стадиях онкологического заболевания. Может провоцироваться активной противораковой терапией. Проявляется слабостью, утомляемостью, бледностью кожи, сухостью слизистых, тошнотой, рвотой, потерей веса и аппетита, потливостью, гипертермией, костно-суставными болями, нарушениями сна, психическими расстройствами, анемией и снижением иммунитета. Диагноз выставляется на основании анамнеза, клинической симптоматики, результатов анализов и инструментальных исследований. Лечение симптоматическое.
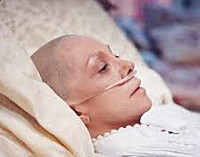
Общие сведения
Раковая интоксикация – комплекс расстройств, возникающих у онкологических больных при отравлении организма продуктами распада злокачественной опухоли. Выявляется преимущественно на терминальных стадиях заболевания, рассматривается как одна из основных причин гибели пациентов. Кроме того, раковая интоксикация часто наблюдается при проведении химиотерапии, является закономерным следствием активного противоракового лечения, вызывающего разрушение опухоли.
Раковая интоксикация может провоцировать нарушения деятельности различных органов и систем, в том числе – почечную и печеночную недостаточность, сепсис и другие тяжелые инфекционные осложнения, что обуславливает важность продуманного подбора дозировок и видов лекарственных препаратов с учетом общего состояния больного, а также наличия тех или иных хронических заболеваний. Лечение осуществляют специалисты в области онкологии.

Причины раковой интоксикации
Одной из отличительных особенностей злокачественной опухоли является ее способность к быстрому неконтролируемому росту. Как правило, темпы роста сосудов, обеспечивающих кровоснабжение новообразования, отстают от скорости роста опухолевой ткани. Злокачественные клетки достаточно устойчивы к гипоксии и могут некоторое время существовать в условиях недостаточного кровоснабжения, однако рано или поздно умирают. Обычно этот процесс наблюдается при опухолях достаточно большого размера. Массовая гибель клеток становится причиной распада новообразования и вызывает раковую интоксикацию.
В организм попадает большое количество продуктов распада, которые провоцируют расстройства всех видов обмена веществ и нарушения деятельности различных органов и систем. Раковая интоксикация становится причиной повышения уровня мочевины. Кристаллы мочевины оседают в почечных канальцах, вызывая развитие почечной недостаточности, которая еще больше усугубляет обменные нарушения. Из-за увеличения количества фосфатов возникает дефицит ионов кальция, следствием которого становятся нарушения работы нервной системы. Повышение уровня кальция негативно влияет на работу сердца. У пациентов с раковой интоксикацией возникают аритмии, в тяжелых случаях возможно прекращение сердечной деятельности. Увеличение количества свободных радикалов стимулирует распад эритроцитов и развитие анемии.
Проявления раковой интоксикации весьма вариабельны. Формирование клинической картины определяется тяжестью состояния пациента, скоростью разрушения новообразования, количеством токсических веществ, попадающих в основной кровоток, особенностями локализации и течения онкологического процесса, масштабом хирургического вмешательства, наличием и объемом кровопотери (как возникшей в ходе операции и послеоперационном периоде, так и связанной с распадом опухоли), присоединением воспалительных осложнений, дозой химиопрепарата и другими факторами.
Симптомы раковой интоксикации
Наиболее постоянными признаками раковой интоксикации являются прогрессирующая слабость и беспричинная утомляемость. Наблюдаются характерные изменения внешнего вида: дефицит массы тела (в тяжелых случаях – вплоть до кахексии), бледный, землистый или желтоватый оттенок кожи, сухость кожи и слизистых оболочек. Возможен цианоз дистальных отделов конечностей. У больных с нарушениями функции печени выявляется иктеричность склер. Пациенты с раковой интоксикацией предъявляют жалобы на усиленное потоотделение. Как правило, потливость более выражена в ночное время.
В ходе опроса врач устанавливает, что резкое снижение веса произошло в течение короткого промежутка времени и сопровождалось нарушениями аппетита: отвращением к еде (особенно – к мясным продуктам), извращением вкуса и т. д. Кроме того, при раковой интоксикации наблюдаются диспепсические расстройства: тошнота, рвота и нарушения стула. Возможны запоры, поносы или чередование запоров и поносов. Отмечается длительное повышение температуры до субфебрильных (при некоторых заболеваниях – до фебрильных) цифр. Возникают боли в костях и суставах.
Больные с раковой интоксикацией могут сообщать о периодических мигренях и приступах головокружения. Расспрос пациентов и их родственников позволяет выявить изменения психического и эмоционального статуса. Могут наблюдаться апатия, раздражительность и эмоциональная лабильность. Раковая интоксикация нередко сопровождается депрессивными расстройствами. Возможны нарушения сна: бессонница, поверхностный сон, трудности при засыпании, ночные и ранние пробуждения. Часто обнаруживаются нарушения сердечного ритма. При раковой интоксикации существует высокая вероятность развития тромбозов и склонность к возникновению инфекционных осложнений. В анализе крови обнаруживаются признаки анемии (обычно – умеренной нормохромной).
Диагностика раковой интоксикации
Диагноз выставляется с учетом анамнеза, жалоб, данных объективного осмотра и результатов дополнительных исследований. Решающую роль в определении причины раковой интоксикации играет выявление основной патологии. При характерной клинической картине и отсутствии установленного диагноза онкологического заболевания пациентам с подозрением на раковую интоксикацию назначают комплексное обследование, которое включает в себя общие анализы крови и мочи, биохимический анализ крови, анализ крови на онкомаркеры, рентгенографию грудной клетки, сцинтиграфию костей скелета, УЗИ брюшной полости, УЗИ малого таза, гинекологический осмотр и другие исследования. План обследования определяется индивидуально.
При уже диагностированном онкологическом заболевании требуется оценка выраженности раковой интоксикации для определения тактики лечения (составления плана химиотерапии, принятия решения об оперативном вмешательстве, подбора симптоматических препаратов и т. д.). Для оценки тяжести раковой интоксикации используются стандартные показатели крови: уровень мочевины, креатинина и С-реактивного белка, реактивный ответ нейтрофилов, лейкоцитарный индекс интоксикации и т. д. Наряду с перечисленными показателями могут потребоваться данные о состоянии различных органов и систем больного с раковой интоксикацией, полученные при проведении ЭКГ, анализов мочи, анализов крови на гормоны и других исследований.
Лечение раковой интоксикации
Лечение симптоматическое, включает в себя мероприятия по детоксикации, устранению или смягчению клинических проявлений и коррекции нарушений деятельности различных органов и систем. Осуществляют энтеросорбцию, гемосорбцию и аппликационную сорбцию. Пациентам выписывают сорбенты для приема внутрь. При тяжелой раковой интоксикации применяют гемодиализ или плазмаферез. При наличии открытых ран в области распада опухоли проводят перевязки с сорбентами местного действия.
При рвоте больным с раковой интоксикацией назначают противорвотные средства (домперидон, метоклопрамид), при запорах – слабительные для перорального приема и ректальные свечи (макрогол, препараты сены, бисакодил, касторовое масло и пр.). При анемии используют препараты железа внутрь и парентерально, применяют эритропоэтин. Выбор медикаментов при раковой интоксикации, сопровождающейся психическими расстройствами, зависит от вида и тяжести расстройств. При эмоциональной лабильности назначают мягкие седативные средства, при нарушениях сна – снотворные, при депрессии – транквилизаторы и антидепрессанты.
Прогноз определяется причинами раковой интоксикации, тяжестью основного процесса, возрастом и общим состоянием больного, наличием и тяжестью сопутствующей соматической патологии. Состояния, возникающие при распаде крупных распространенных опухолей в запущенных стадиях заболевания, являются прогностически неблагоприятными. Больные с раковой интоксикацией погибают от кровотечений, нарушений деятельности органов, пораженных первичной опухолью или гематогенными метастазами, а также от истощения, инфекционных осложнений, почечной недостаточности, тромбозов, нарушений сердечной деятельности или полиорганной недостаточности, обусловленной обменными расстройствами и ослаблением организма. При раковой интоксикации, возникшей в процессе химиотерапии, прогноз может быть благоприятным. При приеме химиопрепаратов это – временное состояние, являющееся частью лечебного процесса.
Токсическая энцефалопатия представляет собой рассеянное органическое поражение головного мозга, которое может развиться как после тяжелых острых отравлений нейротропными ядами, так и при хронических профессиональных нейроинтоксикациях.
Ранними клиническими проявлениями различных хронических интоксикаций в большинстве случаев являются функциональные нарушения центральной нервной системы. При прогрессировании интоксикации происходит постепенное перерастание нейродинамических нарушений в стадию органических изменений - развивается картина токсической энцефалопатии. Органическая природа заболевания нередко может длительное время маскироваться астеническими или невротическими чертами, в связи с чем переход из функциональной стадии в органическую не всегда выявляется своевременно.
К веществам, которые способны вызывать рассеянные повреждения мозговых тканей, относятся:
- пестициды,
- продукты нефтеперегонки,
- соли тяжёлых металлов,
- химические составы бытового предназначения,
- нейротропные медицинские препараты (снотворные, транквилизаторы),
- угарный газ,
- пары ртути,
- свинец,
- мышьяк,
- марганец,
- спиртосодержащие жидкости,
- бактериальные токсины, образующиеся при ботулизме, кори, дифтерии.
Основные типы интоксикаций при энцефалопатии
Выделяют два основных типа интоксикаций: острую и хроническую:
- Острая токсическая энцефалопатия наступает в результате однократного, сильного воздействия отравляющего вещества на организм. Острое состояние требует срочной медицинской помощи и последующих реабилитационных мероприятий.
- В условиях систематического влияния отравления имеет место хроническая форма повреждения тканей мозга. Она наступает на поздних стадиях развития болезни, когда организм уже не способен противостоять длительному воздействию отравления. Больному требуется долгий курс лечения.
Клиническая картина
Для начальной формы токсической энцефалопатии характерна следующая симптоматика: жалобы на упорные головные боли, головокружение, снижение памяти, общую слабость, повышенную утомляемость, нарушение сна и др. На фоне резкой астенизации появляется рассеянная органическая симптоматика, которая не укладывается в картину какой-либо четко очерченной нозологической единицы (асимметрия лицевой иннервации, девиация языка, легкая гипомимия, рефлексы орального автоматизма, высокие сухожильные рефлексы, часто анизорефлексия, ослабление или исчезновение кожных рефлексов). Наряду с этим наблюдаются нарушения психоэмоциональной сферы: снижение памяти, внимания и умственной работоспособности, медлительность, заторможенность, апатия, немотивированная тревога, угнетенное настроение, выраженная эмоциональная лабильность.
Наиболее часто при токсических энцефалопатиях страдают стволовой и диэнцефальный отделы, нередко в процесс вовлекаются мозжечковая, оптико-вестибулярная и экстрапирамидная системы. Общей особенностью токсических энцефалопатий является рассеянность поражения. Однако каждое токсическое вещество придает заболеванию свои клинические особенности. Так, при марганцевой энцефалопатии на фоне диффузной патологии головного мозга начинают вырисовываться очаговые подкорковые симптомы. При энцефалопатиях, обусловленных хроническим воздействием окиси углерода, клинической особенностью является развитие церебрально-кардиальных ангиодистонических расстройств, протекающих на фоне органического диффузного поражения головного мозга. Нарушения координации движений, потливость, дрожание конечностей, галлюцинации, приступы раздражения и агрессии характерны для отравлений алкоголем.
Нарушения психики при различных энцефалопатиях также имеют некоторые особенности. Так, для сероуглеродной энцефалопатии характерны понижение активности, отсутствие инициативы, угнетенное настроение, тоска, равнодушие ко всем, прежде интересовавшим больного сторонам жизни. Такой же астенодепрессивный синдром часто возникает при энцефалопатиях, развившихся вследствие хронической интоксикации этилированным бензином. Ртутной энцефалопатии свойственно сочетание повышенной эмоциональной возбудимости с растерянностью, болезненной застенчивостью, нерешительностью и неуверенностью в себе.
Сроки развития токсических энцефалопатий различны. Так, при интоксикациях сероуглеродом и марганцем энцефалопатия развивается значительно быстрее, чем при хронической интоксикацией алкоголем, ртутью, свинцом или окисью углерода.
Течению токсических энцефалопатий свойственны стойкость патологических проявлений, наличие остаточных явлений в отдаленном периоде и наклонность к прогрессированию вне контакта с токсическим агентом. Патологоанатомические данные указывают, что в основе токсических энцефалопатий лежат сосудистые поражения головного мозга и рассеянные дегенеративные изменения мозговой ткани.
Лечение токсической энцефалопатии головного мозга
Устранение причин, давших толчок болезни, является безотлагательной мерой в тактике лечения токсических энцефалопатий. Контакт больного с ядовитой средой должен быть прекращён. В большинстве случаев пациенту предлагается госпитализация. Первичные назначения врача состоят в детоксикационных мерах. Пациенту назначаются антидоты, нейтрализующие действие ядов. Лекарство подбирается в соответствии с типом отравляющего вещества. Общие мероприятия по детоксикации заключаются в очистительных клизмах, стимуляции диуреза, проведении плазмафереза и гемодиализа.
Следующим этапом лечения являются меры по улучшению кровообращения в сосудах мозга и активизации метаболических процессов. Больному показаны внутривенные и внутримышечные вливания следующих препаратов:
- кавинтон,
- пирацетам,
- церебролизин,
- актовегин,
- цераксон,
- глиатилин.
Для внутримышечного введения назначаются витамины В, С, Р. Перорально пациент принимает биостимуляторы и адаптогены: экстракт женьшеня, лимонника, элеутерококка, препараты на основе алоэ.
По симптоматическим показаниям могут быть назначены транквилизаторы, миорелаксанты, противосудорожные и седативные средства, антидепрессанты:
- реланиум,
- карбамазепин,
- мидокалм,
- сирдалуд,
- амитриптилин,
- тералиджен,
- паксил,
- анафранил.
После стабилизации состояния в курс лечения включаются физиотерапевтические комплексы. Эффективными признаны массаж, иглорефлексотерапия, гидротерапия, грязелечение.
Последствия и прогноз токсических энцефалопатий
Успех лечения больных с поражением мозговых структур во многом зависит от степени тяжести состояния, при которой пациент стал получать медицинскую помощь.
Запущенные болезни не могут быть полностью излечены, а глубокие церебральные изменения не поддаются корректировке. Квалифицированная помощь будет наиболее действенной на ранних стадиях процесса.
Наличие остаточных явлений и прогрессирование болезни без контакта с ядовитыми агентами характерно для отравлений. Но это не означает, что больной лишается надежды на исцеление. Даже в случае инвалидизации самочувствие может стать вполне удовлетворительным при условии проведения полного курса лечебных процедур.
Регулярные реабилитационные мероприятия необходимо проводить на протяжении дальнейшей жизни. Эти меры позволят замедлить дегенеративные процессы в тканях мозга и восстановить многие утраченные функции.
Читайте также:

