Интоксикация печени при химиотерапии
Обновлено: 22.04.2024
Профессор Драпкина О.М.: – Мы сейчас, так сказать, переносимся, в проблемы онкологии. И помочь разобраться нам с лекарственными поражениями печени при проведении химиотерапии поможет как раз профессор Ларионова Вера Борисовна.
Профессор Ларионова В.Б.: – Лекарственные повреждения печени – это очень важная проблема развитых стран. Во-первых, высок удельный вес лекарственной гепатотоксичности в структуре острой печёночной недостаточности, здесь привожу данные зарубежных авторов. (Демонстрация слайда). Также серьёзные этические проблемы и финансовые расходы лечения этого осложнения, которые ложатся бременем не только для учреждения, не только в целом для здравоохранения, но и порой для семьи, в которой находится пациент. А так же, малоутешительны результаты до сих пор при развитии фульминантной печёночной недостаточности, обусловленной лекарственной гепатотоксичностью несмотря на то, что сейчас в арсенале врачей находятся и экстракорпоральные методы детоксикации и методы заместительной терапии трансплантации печени, летальность остаётся достаточно высока.
Что же такое - лекарственная гепатотоксичность в онкологии? Я хочу остановиться на этом понятии. Это процессы патологические, которые развиваются в печени при введении лекарственных препаратов, - хочу подчеркнуть, - в терапевтических дозах. Это очень сложная задача для врача потому, что при лечении онкологического пациента… в программы сопроводительной терапии, без которой сейчас невозможно представить себе лечение онкологического пациента, входит масса других лекарственных средств. А также это важный, лимитирующий фактор проведения противоопухолевого лечения.
Очень много лекарственных средств, в частности хим. препаратов, которые обладают генетической гепатотоксичностью. Хочу обратить ваше [внимание], вот здесь представлены препараты, которые часто дают лекарственную гепатотоксичность, но хочу обратить ваше внимание на то, что применение комплекса хим. препаратов усугубляет лекарственную гепатотоксичность. Вот я привела здесь одну из схем, которая достаточно часто используется в онкологии, и лекарственная гепатотоксичность при использовании этой схемы может достигать 80%.
Контроль органной токсичности полихимиотерапии очень важен. Это один из разделов изучения Международной ассоциации сопроводительной терапии рака, которая была организована в 1991-м году и ещё раз подчёркивает важность сопроводительной терапии в привлечении онкологических пациентов.
ВОЗ классифицируют более 20 видов побочных действий противоопухолевой химиотерапии и среди них выделяют и гепатотоксичность. Однако до сих пор остается много неразрешённых проблем. Одна из них – это отсутствие документальной регистрации гепатотоксичности при проведении химиотерапии. Также ведущие, научные общества, которые занимаются изучением лечения онкологических пациентов, здесь я представила, они также не представили практических рекомендаций по лечению гепатотоксичности.
Чем же обусловлена лекарственная гепатотоксичность или гепатотоксичность противоопухолевых препаратов? Во-первых, это неизбирательность действия большинства цитостатиков, что сопровождается разнообразными поражениями печени, и сопровождается функциональными нарушениями различных органов. Естественно, при развитии того или иного осложнения, в частности гепатотоксичности, нарушаются протоколы лечения, то есть мы вынуждены прерывать курсы лечения, вынуждены редуцировать дозы препаратов. Конечно, это сказывается и на успехи самого онкологического заболевания. То есть итог – ухудшение результатов лечения. Таких работ достаточно много.
Другая проблема, которая существует при использовании хим. препаратов у онкологических пациентов. Что мы знаем о механизмах и патогенезе гепатотоксичности при химиотерапии? Механизмы лекарственного поражения печени – гораздо сложнее, чем мы себе это представляем. Вот здесь я представила наиболее важные моменты. Это нарушение метаболических процессов в гепатоцитах, токсическая деструкция субклеточных структур, индукция иммунных реакций, канцерогенез, нарушение кровоснабжения гепатоцитов и обострение ранее имевшегося гепатоцеллюлярного поражения.
В данной табличке представлены группы противоопухолевых препаратов, которые могут вызывать различные виды гепатотоксичности. К ним относятся алкилирующие агенты, и антиметаболиты, и производные нитрозомочевины, и противоопухолевые антибиотики. Так же это винкаалколоиды, производные платины, интерфероны, интерлейкины, гормонотерапия, а так же модные сейчас, современные таргетные препараты. И как вы видите, они в той или иной степени повреждают сам гепатоцит – основную клетку печёночную паренхимы.
И чтобы также не быть голословным, я здесь представила работу, достаточно новую, не одну, в которой очень чётко представлено, что при использовании хим. препаратов неоднократно усугубляется лекарственная токсичность, что сопровождается также вероятностью более частого летального исхода при развитии стеатогепатита.
Однако патогенез гепатотоксичности в онкологии при химиотерапии до сих пор остаётся неизвестным. Обсуждается очень много теорий в литературе, наиболее обсуждаемые вот эти теории. Это действия провоспалительных цитокинов самой опухоли, а также истощение системы детоксикации, системы глутатиона печени, взрыв оксидантного стресса и накопление активных кислородных метаболитов.
Следующая проблема. Как же диагностировать и оценить гепатотоксичность? Отсутствуют специфические биомаркеры для постановки диагноза лекарственного поражения печения при химиотерапии. Чувствительность традиционных функциональных проб очень низка. Они информативны лишь в диагностике имеющейся патологии, но малополезны в оценке метаболического и экскреторного потенциала печени, и врачу приходится порой очень задумываться, когда он встречается с лекарственным поражением печени. В чём же причина? Как поступить в данной ситуации? В клинике мы для оценки гепатотоксичности используем классификацию, которая предложена национальным институтом рака, в которой выделены 4 степени поражения печени в зависимости от изменений тех или иных биохимических показателей, как представлено в это табличке. Я не буду её комментировать, потому что при желании вы найдёте её в специальной литературе, она достаточно широко обсуждается.
В клинике, всё-таки, в первичной диагностике лекарственных поражений печени мы чаще всего используем вот эти критерии диагностики, которые были представлены ещё в 90-х годах Советом международных медицинских научных организаций, до сих пор не претерпели каких-либо изменений. И особенность этих критериев заключается в том, что здесь нам не нужно никакого специального инструментального исследования, и учитываются лишь абсолютные значения активности ферментов. Хочу только подчеркнуть их относительные величины к высшей границе нормы. В зависимости от этого выделяют гепатоцеллюлярные поражения, холестатические поражения и смешанный тип поражения.
Мониторинг АЛТ, как метод диагностики в онкологии при лекарственной гепатотоксичности, всё-таки имеет право на существование. Здесь я представила достаточно новую работу, где показано, что чувствительность, специфичность и диагностическая точность достаточно высоки. Но этот метод имеет и свои ограничения, потому что мы знаем, что повышение трансаминаз больше 3 норм отмечается у 1% пациентов при использовании плацебо. Мониторинг АЛТ не позволяет нам идентифицировать идиосинкразические реакции, которые наиболее часто мы отмечаем при использовании хим. препаратов. И режим мониторинга АЛТ часто нарушается в реальной клинической практике.
Почему мы говорим об S-адеметионине или о гептрале? Это физиологический метаболит, дефицит которого наблюдается при всех патологиях печени, в том числе при гепатотоксичности. Он выполняет важную роль в метаболических процессах, реакциях трансметилировании, транссульфировании, аминопропилировании. Назначая гептрал, врач всегда предполагает его детоксикационный эффект, антиоксидантный, антидепрессивный, нейропротективный, регенерирующий, холеретический и холекинетический эффекты.
Каковы же преимущества гептрала перед другими препаратами целенаправленного действия на печёночную клетку? Это достаточная абсорбция, естественный метаболизм при патологии печени – наличие эффекта первого прохождения через печень и отсутствие токсичности. Немножечко поясню. Очень часто, открывая инструкцию, пациент видит, что при пероральном приёме лишь 5% обладает биодоступностью. Да, действительно, вы должны объяснить пациенту 5%, потому что 95% этого препарата непосредственно включается в метаболизм в печени. Выраженная способность предупреждать или нейтрализовать образование высокоактивных повреждающих соединений, снижать воспаление, подавлять формирование соединительной ткани, стимулировать процессы регенерации – это реакция аминопропилирования. И наличие двух форм применения, что тоже очень важно, особенно в онкологии для достижения быстрого эффекта, потому что у онколога порой не бывает времени для того, чтобы не продолжить химиотерапию этой серьёзной болезни.
Как же применять гептрал у онкологических пациентов при проведении химиотерапии? Это парентеральное введение, пероральный приём, ступенчатая терапия, и комбинация внутривенного и перорального способов применения для того, чтобы ускорить эффект действия данного препарата. И гептрал в программах сопроводительной терапии в онкологии при лекарственных поражениях печени обладает лечебным и профилактическим эффектом, повышая эффективность химиотерапии, а так же антидепрессивный эффект и лечение разных форм печёночной энцефалопатии. Улучшение субъективного состояния и изменения качества жизни пациентов, потому что это очень важно, немножко позже я скажу об этом.
Каковы же проблемы ещё, которые встают при развитии гепатотоксичности при химиотерапии? Профилактика или лечение – какой же подход выбрать, какой оптимален? И вот я хочу представить наш опыт в практику врача-онколога. Во-первых, при развитии гепатотоксичности нам приходится снижать дозы цитостатиков при критерии, которые представлены ВОЗ. Но не всегда в практике мы придерживаемся этого, особенно если брать больных гематологического профиля в онкогематологии, когда есть первичное поражение печени, когда мы можем подарить шанс на излечение нашему пациенту.
Рациональный подход к предупреждению гепатотоксичности лекарственных средств при невозможности их отмены – предшествующее или одновременное назначение препарата гептрал. Предшествующее или одновременное назначение гептрала у многих пациентов позволяет проводить полноценные протоколы химиотерапии, не изменяя их режимов, не изменяя их доз. И вот здесь показана в этой работе, достаточно недавно эта работа опубликована, показана эффективность профилактического использования адеметионина на больных онкологического профиля. Здесь больные, которые имеют раковую опухоль толстой кишки, использовалась FolFox-терапия, которая включала фторурацил, оксаплатин, лейковарин и элоксатин. И показано, что у пациентов, которые принимали адеметионин в дозе 800 миллиграмм, профилактически у них ни одноного пациента не было отмены терапии, и лишь у 11% пациентов был отсрочен курс, если сравнивать с группой, у которой адеметионин не использовался в качестве профилактики. И снижение доз также было значительно меньше у пациентов, которые получали адеметионин.
Говоря о гепатотоксичности, я не могу остановиться и не сказать о печёночной энцефалопатии. Мы знаем, что печень – это центральный орган образования и обезвреживания аммиака, и развитие печёночной энцефалопатии – это комплекс потенциально обратимых нервно-психических нарушений, которые возникают в результате печёночной недостаточности и портосистемного шунтирования крови. То есть мы знаем, что наши многие пациенты получают амбулаторную химиотерапию, и при развитии печёночной комы, печёночной энцефалопатии, мы обязаны этих пациентов госпитализировать в стационар, потому что это возможно излечить и дать шанс больному продолжить полноценную жизнь. Говоря о печёночной энцефалопатии, хочу особое внимание обратить на минимальную печёночную энцефалопатию, которая регистрируется у 85% пациентов. Как я уже говорила, что наши пациенты многие получают амбулаторную химиотерапию, и это развитие минимальной печёночной энцефалопатии, которая требует специальных тестов диагностики, которые не всегда используются в клинике, она может быть стадией – предвестником развития клинически выраженной печёночной энцефалопатии. И психические нарушения, которые возникают у пациентов, мы очень часто говорим, пациент, который получает химиотерапию, у него меняется характер, он становится скверным. Это может оказывать отрицательное влияние на качество жизни пациентов.
Терапия минимальной печёночной энцефалопатии остаётся предметом дискуссий. Здесь я привожу схему, которую мы используем при лечении наших пациентов. И при хронической печёночной энцефалопатии в период ремиссии, также необходимо принимать курсовые дозы, которые режимы, и длительность приёма определяется врачом, который с данным пациентом работает.
И необходимо, хочу призвать всех врачей, разрабатывать стандарты сопроводительной терапии и создавать междисциплинарные протоколы профилактики гепатотоксичности при химиотерапии в Российской Федерации, потому что их нет, а тема очень актуальна. Это приведёт к повышению эффективности лечения онкологических пациентов.
Благодарю за внимание!
Профессор Драпкина О.М.: – Спасибо большое, Вера Борисовна! У нас ещё 7 минут, и вам пришли вопросы. Можно ли назначать химиотерапию пациентам с высоким уровнем трансаминаз на фоне вирусного гепатита?
Профессор Ларионова В.Б.: – Вопрос сложный. Я думаю, что вы не будете на фоне высоких трансаминаз назначать. Во-первых, причина повышения трансаминаз. Обусловлена она самим вирусным гепатитом или она обусловлена всё-таки воздействием хим. препаратов? Это очень важно, потому что порой я сама занимаюсь химиотерапией гемобластозов, и порой мы пациенту проводим сначала противовирусную терапию, проводим применение гепатопротекторов, а потом назначаем уже химиотерапию, потому что риск огромный потерять пациента на фоне лечения. У нас есть такие пациенты, достаточно много, особенно в гематологии.
Профессор Драпкина О.М.: – Вопрос по поводу гептрала: во время или после химиотерапии?
Профессор Ларионова В.Б.: – Это вопрос дискутабельный. Я уже сказала, у нас есть свой опыт уже ведения этих больных. Если больной относится к группе риска, мы этим пациентам даём на фоне химиотерапии гептрал – обязательно. У нас это уже отработано.
Профессор Драпкина О.М.: – Есть ли противопоказания у пациентов с онкологическими заболеваниями в применении гептрала?
Профессор Ларионова В.Б.: – Нет.
Профессор Драпкина О.М.: – Нет. И последний вопрос: какая группа препаратов для химиотерапии требует наиболее пристального мониторинга поражения печени?
Профессор Ларионова В.Б.: – Я вот показала те препараты, которые уже генетически имеют токсичность. К ним относятся метотрексат, циклофосфан, препараты платины, а также полихимиотерапия. И вот мы уже наблюдали таргетные препараты, в частности препарат велкейд, когда мы у пациентов из группы риска, пациент, который был курильщиком, который принимал алкоголь, у него трансаминазы зашкаливали уже после первого курса велкейда. Мы ему провели лечение гептралом, но это заняло, больной с миеломной болезнью, достаточно длительно, где-то около трёх недель, но в последующем, мы немного редуцировали дозы велкейда, изменили режим, но продолжили на фоне гептрала и сейчас он проводит трансплантацию с успехом этот пациент.
Профессор Драпкина О.М.: – Спасибо большое, Вера Борисовна! Спасибо!
Причина заблуждения химиотерапевтов была порождена ограниченностью диагностических возможностей. В то время для адекватной диагностики было недостаточно УЗИ и биохимического анализа крови, а МРТ и КТ были недоступны.

Лекарственный гепатит
Сегодня основные диагностические критерии поражения печени цитостатиками в результате химиотерапии также опираются на биохимический анализ крови, но высокочувствительные тесты позволяют исключить вирусные гепатиты, лучевая визуализация – КТ и МРТ выявляют мельчайшие метастазы в печени, специфические маркёры диагностируют аутоиммунные гепатиты, установлены морфологические критерии алкогольных поражений печени. А когда исключено всё, на повестке дня остаётся токсический лекарственный гепатит, развивающийся при применении стандартных доз химиопрепаратов.
Факторами риска лекарственного гепатита является непосредственно токсический потенциал цитостатика, а порой и генетические особенности пациента, не позволяющие адекватного разложения и выведения метаболитов. Влияет пол и возраст, жизненный анамнез, нездоровое питание и злоупотребление алкоголем. Влияют лекарства, принимаемые не по поводу рака, а в связи с другим хроническим заболеванием, и их количество. Влияют сопутствующие болезни и локализация опухолевого процесса.
Комплекс факторов в различных сочетаниях не даёт возможности печени выстоять под натиском химиотерапии, и она снижает или утрачивает свои функциональные возможности.
Поражение печени после химиотерапии
При тяжёлом поражении печени проведение химиотерапии невозможно, но при лёгкой и средней степени возможно лечение со снижением дозы химиопрепаратов. Только польза от такой сокращенной химиотерапии тоже может стать редуцированной. Что же делать? Разумеется, поражение печени лекарством легче предотвратить, чем лечить, но и лечить тоже можно и нужно. Ещё недавно химиотерапевты скептично относились к возможности развития лекарственного гепатита ещё и потому, что не было эффективных препаратов для лечения и профилактики. Сегодня для этих целей применяется абсолютно физиологичный метаболит, дефицитный при любой печёночной патологии.
Есть ещё один неприятный момент: поражение печени в результате химиотерапии приводит к развитию печёночной энцефалопатии, проявляющейся постхимиотерапевтической астенией и депрессией. Лёгкая энцефалопатия отмечается, как минимум, у трети всех прошедших химиотерапию, но поскольку пациенты практически не попадают к невропатологу, у них это состояние не диагностируется.
Насколько опасна депрессия, рассказывать не нужно. Лечение энцефалопатии проходит по пятиступенчатой методике, включающей не только устранение провоцирующего фактора и усугубляющих его моментов, но санацию кишечника от содержащих азот субстанций. Назначаются специальный диетический режим и препараты, помогающие связывать токсические продукты и выводить их.
Осложнения после химиотерапии в той или иной комбинации симптомов разной выраженности обязательны при каждом цикле, поэтому клинические исследования учитывают эффективность химиопрепарата, спектр и частоту встречаемости побочных реакций. При противоопухолевой терапии невозможен баланс между результативностью и токсичностью, что обусловлено неизбирательным действием лекарств.
Виды осложнений после химиотерапии
Химиотерапия (ХТ) вредит каждой клетке организма, только прошедшие полноценный этап развития здоровые клетки более устойчивы к цитостатикам. Злокачественные клетки растут быстрее, пренебрегая собственной структурой, их главная задача — стремительность размножения. Первый контакт злокачественной опухоли с противораковым лекарством смертелен для её клеток, но дальше создается система защиты от ХТ, что позволяет ей выживать и захватывать новые области.
Не устойчивы к химиотерапии и быстро созревающие нормальные клетки, как лейкоциты и тромбоциты, половые и формирующие слизистые покровы, потому что их популяции не запрограммированы на длительное существование.
По механизму развития осложнения после химиотерапии подразделяются на 4 больших группы:
- обусловленные действием препарата, включая местное повреждение и системные специфичные для определенного цитостатика и характерные для всех лекарств эффекты. Пример местной реакции — цистит после иринотекана, системного специфического повреждения — пневмотит после блеомицина, неспецифического — лейкопения;
- обусловленные нарушениями иммунитета, в том числе аллергические и аутоиммунные процессы. Например, на таксаны развивается системная аллергия вплоть до анафилаксии, общее снижение иммунной защиты проявляется легкостью развития воспалительных заболеваний и активацией вируса герпеса;
- непереносимость ХТ, так отсутствие клеточного фермента приводит к необыкновенно высокой токсичности фторурацила;
- неблагоприятное взаимодействие лекарств особенно ярко проявляется при комбинированной ХТ, так таксаны с цисплатиной вдвойне вредят нервной системе.
Осложнения возникают в разное время:
- острые — во время введения цитостатика и в первые сутки после ХТ;
- ближайшие случаются на вторые сутки после цикла;
- отсроченные развиваются после 7 суток;
- отдаленные — минимально через месяц и могут появиться через годы.
Со стороны пищеварительной системы
Побочные эффекты со стороны слизистых оболочек составили химиотерапии плохую славу:
- тошнота и рвота в ближайшее время;
- отсроченные мукозиты — отсроченное разрушение слизистых ротовой полости (стоматит), пищевода (эзофагит), желудка (гастрит), тонкой кишки (энтерит), толстого кишечника (колит) и прямой кишки (ректит);
- гепатотоксичность появится в отдалённый период, после нескольких курсов терапии.
Тошноту, а особенно рвоту, можно предотвратить и уменьшить. Мукозит разнообразен по выраженности и локализации, начинается с воспаления и отека, дальше формируются участки омертвения от микроскопических до видимых. При стоматите невозможно ни пить, ни есть, эзофагит и гастрит проявляется изжогой, поражение кишки — нарушениями стула, всегда беспокоит боль, подташнивание и анорексия.
Токсическое поражение печени формируется исподволь, когда изменяется только биохимия крови, печеночная ткань сама не болит, боль вызывается растяжением капсулы при увеличении печени. В тяжелых случаях возможна желтуха с температурой и интоксикацией, но самое опасное — печеночная недостаточность острая или через несколько лет в результате фиброза печени.

Со стороны иммунной системы
Иммунотерапия моноклональными антителами избыточно активирует систему защиты, приводя к аутоиммунным проявлениям. Иммуноопосредованная токсичность охватывает несколько систем органов, проявляясь аутоиммунным гепатитом, пульмонитом, поражениями кожи и сосудов, как правило, с интоксикацией, температурой и ухудшением состояния.
Со стороны кровеносной системы
Особенность большинства химиопрепаратов — раздражение слизистой кровеносных сосудов, которую снижают изменением технологии внутривенного введения. В большей мере от цитостатиков страдают вены верхних конечностей, получающие контактный химический ожог.
Некоторые лекарства приходится вводить либо очень быстро — болюсом, другие, наоборот, очень медленно капельно, затрачивая на одно введение от пары часов до нескольких суток. Клинически повреждение сосудов проявляется флебитами: болью и внутренним воспалением, отеком и покраснением кожи над сосудом. Воспаленная слизистая утолщается, замедление тока крови приводит к тромбозу. После неоднократного введения цитостатика просвет вены сужается и может полностью облитерироваться.
Особый вид осложнения химиотерапии экстравазация — разрыв сосуда с выходом химиопрепарата в окружающие ткани. Это происходит не из-за неловкости медсестры, расслаивается хрупкая сосудистая стенка, неоднократно пережившая ожог цитостатиком.
Со стороны опорно-двигательного аппарата
Скелет страдает от длительной гормональной терапии, для бисфосфонатов специфичен некроз нижней челюсти. Химиотерапия повреждает слизистую суставов, аналогично мукозиту, что проявляется воспалением с отеком, болью и ограничением движений. Иммунные и таргетные препараты приводят к аутоиммунным артритам.
Поражение цитостатиками мышечного скелета опосредовано нейротоксичностью, когда мышечные судороги и боль вызываются повреждением нервов, но не самой мышечной ткани.
Со стороны нервной системы
Нейротоксичность противоопухолевой терапии заслуживает отдельного разговора. Побочный эффект присущ нескольким группам цитостатиков и проявляется повреждением периферических нервов и нечасто — головного и спинного мозга. В подавляющем большинстве нарушается чувствительность, движения страдают реже.
Определены критичные дозы лекарств, сопряженные с развитием нейротоксичности, время развития повреждения вариабельно, может появиться и через несколько месяцев после завершения лечения. Особенность — в продолжительности клинических симптомов, у некоторых пациентов полного восстановление не случается.
Органы-мишени
Другой пример органа-мишени для цитостатика — повреждение почечных канальцев цисплатиной, приводящее к развитию почечной недостаточности. Аналогично работают и антрациклины, избирательно повреждающие клетки миокарда.
Орган-мишень для иммуно-онкологических препаратов — лимфоциты, их активация помогает бороться с меланомой и раком легкого, но с другой стороны они вызывают специфические иммунологические побочные эффекты, описанные выше.
Внешность
Большинство препаратов не вызывает тотального облысения — алопеции, но частичная алопеция с пушащимися от внутренней слабости волосками и гнездами проплешин травмирует женщину не меньше полностью лысой головы. Впоследствии волосы изменяют цвет и структуру — утолщаются и завиваются.
Иммуно-онкологические препараты вызывают специфическое воспаление кожи с последующим обильным шелушением стоп и ладоней или распространенными прыщами — акне. Все проявления уходят без следа — шрамов не остается, но до полного восстановления проходит несколько месяцев моральных страданий.
Самочувствие после химиотерапии
Самочувствие после химиотерапии зависит не только от использованной комбинации лекарств и их доз, но и от исходного состояния здоровья, пола — у женщин осложнений больше, и психологических особенностей. Однозначно, что после цикла самочувствие хуже, чем до него.
Все циклы переносятся по-разному, и побочные реакции после первой химиотерапии не похожи на токсичность последующих циклов. Негативные проявления со стороны крови, сердечной мышцы, почек и нервной системы могут усугубиться. Мукозит, наоборот, протекает легче, потому что уже погибли самые чувствительные пласты слизистых клеток и вместо них образовалась прочная рубцовая ткань.
Самочувствие можно улучшить, ускорить восстановление тканей тоже возможно, при будущем курсе часть побочных реакций удается перевести в легкую степень или серьёзно нивелировать, как это умеют делать в нашей клинике.
Степени осложнений
Побочные эффекты по выраженности классифицируют так:
Для каждого цитостатика в процентах рассчитана токсичность 3-4 степени, но использование комбинаций лекарств может привести к внеплановым последствиям.
Сколько времени длятся побочные эффекты?
Продолжительность токсических явлений зависит от скорости восстановления поврежденной ткани, стандартное время — 21 день, за этот срок полностью восстанавливается кишечная слизистая и костный мозг. Для восстановления лейкоцитов и тромбоцитов достаточно недели, эритроциты потребуют более 4 месяцев.
Мукозиты могут растянуться на пару недель, но уже к концу первой недели симптоматика уменьшается.
Восстановление печени и почек, нервной системы может занять до года без каких-либо гарантий на 100% репарацию.
Волосы начинают расти к началу следующего цикла, ногти полностью сменяться через полгода.
Обследование после химиотерапии
Диагностика осложнений химиотерапии осуществляется при осмотре и по анализу крови — биохимическому и клиническому с лейкоцитами и тромбоцитами.
Анализ крови покажет истинную степень угнетения кроветворения, поэтому его сдают часто, после восстановления показателей достаточно сделать перед следующим циклом.
Мукозит потребует дополнительного обследования только при 3-4 степени. Поражение печени и почек первоначально обнаруживают по биохимии крови.
При симптомах неблагополучия со стороны сердечно-сосудистой системы необходимо безотлагательное обследование с ЭКГ, эхокардиографией и специфическими кардиальными маркерами в крови.
Что делать после химиотерапии?
После окончания химиотерапии надо жить дальше, не замыкаясь в болезни и не погружаясь в прошедшие переживания. Дальнейшее наблюдение, возможно, потребует физической и психологической реабилитации.
Активный отдых — хорошее продолжение восстановления после химиотерапии, можно вернуться на работу, главное —уйти от неприятных воспоминаний тягот лечения.
В нашей клинике каждому пациенту составляется индивидуальный план наблюдения с графиком обследований, о которых пациента известят звонком, предлагая удобное время визита. Наблюдение после лечения злокачественного заболевания — наша забота, пациент должен жить дальше без лишних проблем.
Лечение осложнений
Лечение осложнений в традиционном плане не всегда возможно. Хорошо контролируется рвота, лекарства отлично справляются с лейкопенией, при высокой вероятности 3-4 степени угнетения белого ростка крови и до появления лейкопении — заблаговременно начинается введение колониестимулирующих факторов.
Нет специфических препаратов для купирования нейротоксичности химиотерапии, поэтому актуальна потребность в физиотерапии и разнообразных методиках нейрореабилитации.
При осложнениях со стороны органов ЖКТ, преимущественно слизистых и печени, возможно только симптоматическое лечение, поэтому так важен профессионализм врачебной команды и возможности клиники в организации интенсивной терапии и проведении вспомогательного восстановительного лечения, подборе адекватного питания.
Беременность после химиотерапии
Цитостатическая терапия не способствует репродукции и во время лечения беременность практически исключается. Немногочисленные исследования показали неопасность беременности для излечившихся от злокачественной опухоли, но ремиссия рака не совсем подходящее время для продолжения рода. После завершения химиотерапии беременность должна быть не только плановой, но и продуманной, следует помнить, что рак — хроническое заболевание, о полном излечении можно говорить по прошествии десятилетия.
Прием тамоксифена может поспособствовать неплановой беременности, поэтому молодым женщинам рекомендуется контрацепция. Адекватный способ предохранения предложит гинеколог, специализирующийся на онкологической патологии.
Секс после химиотерапии
Никаких препятствий для сексуальных отношений не существует, если купированы токсические реакции химиотерапии. При молочнице и других неблагоприятных симптомах со стороны слизистой оболочки половых путей — наследии противоопухолевого лечения у женщины, о перспективах возвращения к половой жизни необходимо посоветоваться с гинекологом.
Химиотерапия неблагоприятно сказывается на потенции, но с течением времени эректильная дисфункция должна пройти, но лучше обсудить проблемы с андрологом-урологом, сегодня выпускается достаточно средств для купирования временных проблем интимной жизни.

Месячные после химиотерапии
Средний срок восстановления менструального цикла после завершения последнего цикла химиотерапии — 6 месяцев, но до первых месячных может пройти и существенно меньший срок, всё зависит от гормонального возраста женщины. У входящей в климактерический период женщины лекарственная аменорея может плавно перетечь в постменопаузу без менопаузы — последней менструации.
Продолжительность жизни после химиотерапии
Наблюдательные исследования доказали большую частоту сердечно-сосудистых болезней и вероятность развития вторых злокачественных процессов через несколько десятилетий после лечения рака, но пока нет доказательств, что противоопухолевая терапия сокращает жизнь излечившихся от первичного злокачественного процесса.
Инвалидность после химиотерапии
Получение инвалидности после завершения радикального лечения злокачественного заболевания не обязательная опция. Инвалидность, как и пребывание на больничном, свидетельство нетрудоспособности, только более продолжительной.
Профилактика осложнений после химиотерапии
Вероятность осложнений заложена в саму суть химиотерапии, часть побочных реакций можно ослабить, но невозможно предотвратить токсичность на 100%. В практической онкологии предупреждают рвоту и лейкопению, специфическая профилактика остальных неблагоприятных последствий не разработана. Онкологическая наука предлагает активно следить за состоянием и анализами, и при малейших неблагоприятных сдвигах начинать помогать организму пациента справляться с наименьшими потерями для здоровья.
Профессионализм химиотерапевта и лечебно-диагностические возможности клиники позволяют поддерживать защитные силы организма до начала цикла и во время него. В нашей Клинике не только проводят мониторинг показателей и самочувствия, но предлагают специальную нутритивную поддержку, разнообразные восстановительные процедуры и методики купирования токсичности.
Химиотерапия — это метод лечения онкологических заболеваний, основанный на уничтожении быстро делящихся клеток или остановке процесса их деления. Соответственно все химиопрепараты делятся на цитотоксические и цитостатические.


Как работает химиотерапия
Одно из главных отличий раковых клеток от нормальных — быстрое деление. Скорость деления раковых клеток зависит от степени их злокачественности, или дифференцировки.
Высокодифференцированные клетки мало чем отличаются от нормальных. Скорость их деления незначительно превышает норму. Такие опухоли медленно растут, редко рецидивируют после удаления. Прогноз лечения, как правило, благоприятный.
Среднедифференцированные клетки уже существенно отличаются от нормальных, но их все еще можно отнести к тому или иному типу тканей.
Низко дифференцированные раковые клетки уже не имеют ничего общего с нормальными. Они утрачивают свои функции и единственное, что они делают — это стремительно делятся. Такие злокачественные опухоли наиболее опасны. Они быстро растут, активно дают метастазы, с трудом поддаются лечению и часто рецидивируют после удаления.
Проблема состоит в том, что быстрым делением отличаются не только раковые клетки, но также некоторые нормальные клетки организма, в частности, слизистых поверхностей тракта, костного мозга, волосяных фолликулов.
Препараты химиотерапии воздействуют на все быстро делящиеся клетки без разбора. Поэтому наряду с раковыми клетками они уничтожают и нормальные.
Это вызывает неизбежные побочные эффекты, которые требуют коррекции состояния, включая детоксикацию организма.
Причины интоксикации при химиотерапии
Интоксикация организма при химиотерапии возникает в силу трех причин:
- присутствие в крови химиопрепаратов и продуктов их распада,
- проникновение в кровь погибших раковых клеток,
- нарушение работы печени, почек, которые играют ключевую роль в очищении организма от токсинов.
Симптомы интоксикации организма при химиотерапии
Повреждение костного мозга при химиотерапии приводит к нарушению процесса кроветворения. Это проявляется изменением картины крови, в частности, снижением уровня лейкоцитов (лейкопенией), красных кровяных телец (эритроцитов), уровня гемоглобина.
От химиотерапии страдает иммунная система. Это проявляется частыми инфекционными заболеваниями дыхательных путей, быстрым развитием осложнений ОРВИ, ОРЗ (в частности, пневмонии), рецидивирующим герпесом, проявлением грибковых инфекций и другими признаками пониженного иммунитета.
Интоксикация организма при химиотерапии проявляется такими симптомами, как:
- тошнота, рвота,
- потеря аппетита (анорексия),
- снижение массы тела,
- слабость,
- высокая утомляемость.
Наряду с этими симптомами химиотерапия может вызвать:
- выпадение волос,
- диарею,
- одышку,
- посинение кожи (цианоз),
- стоматит (образование язв в полости рта),
- развитие эзофагита, гастрита, энтероколита,
- анемию,
- учащенное мочеиспускание,
- нарушение менструального цикла и функциональную недостаточность яичников у женщин,
- функциональную недостаточность яичек у мужчин, нарушение сперматогенеза,
- развитие полинейропатии,
- нарушения психики,
- дерматиты,
- возникновение аллергии.
Закажите обратный звонок. Мы знаем, как помочь
Степени тяжести побочных эффектов химиотерапии
Различают пять степеней тяжести побочных эффектов химиотерапии.
Нулевая (0) степень означает отсутствие симптомов и изменений в лабораторных анализах крови и мочи.
Первая (1) степень означает наличие минимальных отклонений в лабораторных анализах, которые не влияют на самочувствие.
Вторая (2) степень означает умеренные изменения в анализах, самочувствии, работе внутренних органов. На этой стадии возникает необходимость коррекции состояния пациента.
Третья (3) степень означает существенные отклонения в лабораторных анализах, нарушения работы внутренних органов и серьезное ухудшение самочувствия пациента. Это требует немедленной коррекции курса химиотерапии (или его прерывания, отмены), проведения лечебных мероприятий, включая снятие интоксикации.
Четвертая (4) степень означает угрозу жизни пациента и требует прерывания или отмены курса химиотерапии.
Как избежать интоксикации
- Премедикация.
До начала химиотерапии в международной клинику Медика24 проводится премедикация, чтобы подготовить организм к действию химиопрепаратов. - Коррекция.
На протяжении всего курса химиотерапии состояние пациента находится под постоянным мониторингом, контролем .
Легче всего это обеспечить в условиях стационара международной клиники Медика24. В этом случае всегда есть возможность отследить изменения в самочувствии пациента, вовремя принять необходимые меры для коррекции состояния — показателей крови, работы внутренних органов, кроветворной, дыхательной, , пищеварительной, выделительной, иммунной систем.
Если потребуется, курс химиотерапии может быть скорректирован с отменой тех или иных препаратов и заменой их другими.
В этом случае можно гарантировать, что побочные эффекты химиотерапии будут минимальными при высокой эффективности лечебного курса с максимально быстрым восстановлением после его окончания. - Детоксикация.
Лечение после химиотерапии состоит в очищении крови от продуктов распада раковых клеток, а также разрушенных нормальных клеток (костного мозга, слизистых поверхностей ЖКТ, печени, почек), выведении компонентов химиопрепаратов с восстановлением нормальной работы системы самоочищения организма (печени, почек).
Плазмаферез
Главное место накопления токсинов — плазма крови. Плазмаферез — это удаление загрязненной, насыщенной токсинами плазмы и ее замещение.
Обычно при детоксикации замещается до 30% плазмы крови.
Кровь забирается из сосудистого русла и поступает на сепаратор, где она разделяется на две фракции — массу кровяных телец (лейкоцитов, эритроцитов, тромбоцитов) и плазму.
Насыщенная токсинами плазма крови сливается и утилизируется. Ее объем восполняется чистой донорской плазмой с плазмозамещающим раствором, в состав которого могут входить физраствор, полиглюкин, реополиглюкин.
Для снятия интоксикации организма после химиотерапии обычно бывает достаточно1 — 4 процедур плазмафереза.
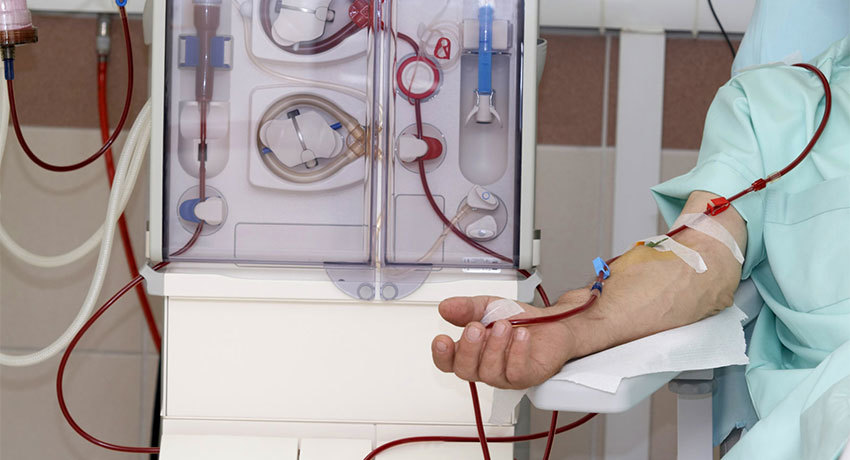
Гемодиализ
Гемодиализ — это очищение крови от токсинов с одновременным восстановлением электролитного, баланса.
При гемодиализе кровь забирается из сосудистого русла и поступает в . Там она омывает частично проницаемую мембрану, за которой находится раствор, схожий по своему составу с плазмой крови.
Диализирующий раствор содержит электролиты (магний, хлор, фосфор, калий, натрий, кальций) в концентрациях, соответствующих норме.
Снятие интоксикации организма достигается одним из двух способов или их сочетанием. Первый — это диффузия. В этом случае давление со стороны крови и со стороны диализирующего раствора одинаковы. Кровь просто омывает мембрану, через которую из нее выходят токсины, происходит обмен электролитами.
Второй способ основан на эффекте фильтрации. В этом случае кровь подается на мембрану под давлением.
Сочетание этих методов позволяет удалить все виды токсичных веществ, как низкомолекулярные, так и средне- и высокомолекулярные.
Гемодиализ в международной клинику Медика24 проводится на самом современном оборудовании, это обеспечивает максимальную эффективность, безопасность процедур, отсутствие побочных эффектов.
Инфузионная терапия
Посредством капельницы после химиотерапии внутривенно вводится физраствор с добавлением глюкозы, альбумина, бикарбоната натрия и/или других компонентов по показаниям.
Объем раствора, введенного посредством капельницы после химиотерапии, может доходить до нескольких литров. После этого делается инъекция мочегонного средства (фуросемида или иного диуретика).
Другой вариант инфузионной терапии — непрямое окисление крови.
В этом случае внутривенно вводится препарат гипохлорита натрия. Очищение от токсинов происходит благодаря образованию активного кислорода. Длительность процедуры может доходить до 6 часов. Для достижения выраженного эффекта обычно требуется 2 — 3 лечебных сеанса.
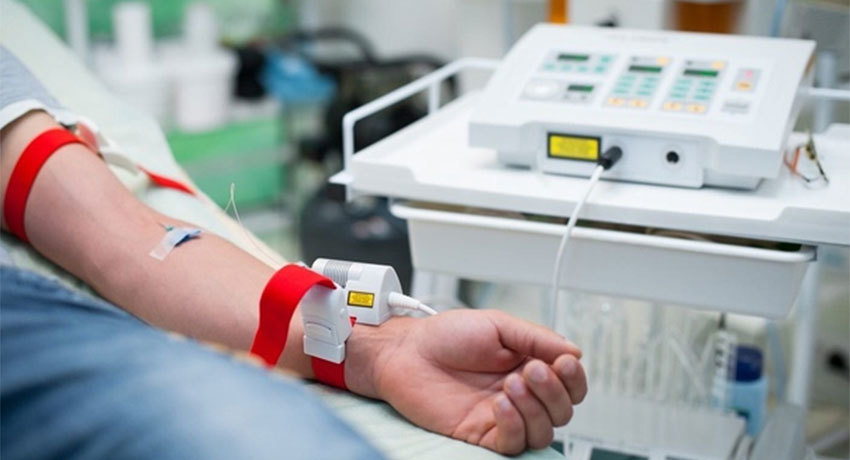
Внутривенное лазерное очищение крови — физиотерапевтический метод лечения после химиотерапии. Очищение крови достигается благодаря поглощению лазерного излучения кровяными тельцами в сосудистом русле.
Для этого в вену вводится тонкая игла, на конце которой находится излучатель лазерного света. При его поглощении кровяными тельцами улучшаются реологические свойства крови, кислородное питание тканей и органов, обменные процессы, стимулируется работа системы естественного самоочищения организма.
Перитонеальный диализ
Принцип этого метода тот же, что и в случае гемодиализа. Только роль полупроницаемой мембраны выполняет брюшина. В брюшную полость через катетер вводится диализирующий раствор, в которой из крови выходят токсины.
Длительность процедуры может составлять от получаса до нескольких (4 — 12) часов, после этого насыщенная токсинами жидкость сливается из брюшной полости через дренаж. Для снятия интоксикации организма после химиотерапии требуется проведение нескольких процедур.
Гемосорбция
Процедура состоит в очищении крови от токсинов с помощью сорбентов. Для этого делается забор крови из венозного русла. После этого она пропускается через аппарат, где находится сорбент, впитывающий токсины. Обычная длительность процедуры составляет около часа. Для снятия интоксикации требуется проведение нескольких процедур.
Применение этих и других методов снятия интоксикации организма после химиотерапии (как и само проведение химиотерапевтического лечения) требует постоянного мониторинга состояния пациента. Лучшие условия для этого — стационар международной клиники Медика24.
Пожелтение кожи и склер глаз при онкологических заболеваниях — тревожный симптом. Это значит, что заболевание перешло на 3, а то и на 4 стадию, и опухоль сдавила общий желчный проток (холедох) или печеночные протоки.


Почему возникает желтуха?
Клетки печени называются гепатоцитами. Одной стороной они соединяются с мельчайшими кровеносными сосудами, а другой — с желчными протоками.
Мелкие желчные протоки и кровеносные сосуды сливаются в более крупные и в конечном итоге образуют общий желчный проток (холедох) с одной стороны и печеночную вену с другой.
Желчь — это щелочное вещество цвета, необходимое для переваривания жиров и усвоения жирорастворимых витаминов. Она вырабатывается клетками печени.
В норме желчь постоянно поступает в желчный пузырь и далее в кишку, где соединяется с панкреатическим соком — секретом поджелудочной железы. Вместе они переваривают жиры.
Сдавление холедоха приводит к тому, что желчь застаивается в желчном пузыре и печени.
Поскольку клетки печени соединены с кровеносной системой, желчь из них поступает в кровь. Развивается интоксикация, которая сопровождается пожелтением кожи и склер глаз. Это и есть желтуха.
Поскольку причиной поступления желчи в кровь служит механическое сдавление холедоха (или других протоков), желтуха называется механической.
Вв международной клинике Медика24 применяются самые эффективные методы быстрого лечения этого синдрома и нейтрализации его опасности.
Закажите обратный звонок. Мы работаем круглосуточно
Чем опасна желтуха
Желтуха при онкологических заболеваниях свидетельствует о поздней стадии развития опухоли. В таких случаях возможности лечения существенно ограничены.
Сама по себе механическая желтуха представляет смертельную опасность. При поступлении желчи в кровь она насыщается билирубином.
В норме он выводится вместе с желчью в кишку и далее эвакуируется естественным образом через тонкий и толстый кишечник.
Когда поступление желчи в кишку нарушается, билирубин вместе с желчью попадает в кровь.
Это очень опасно, поскольку билирубин — токсичное вещество, по существу яд. Его максимальное содержание в крови не должно превышать 20 — 21 мкмоль/л. В случае механической желтухи его концентрация возрастает до сотен мкмоль/л.
Это приводит к тотальному отравлению организма, нарушению практически всех жизненно важных биохимических процессов и может за короткое время привести к смерти.
Поэтому первое, что должен сделать врач в случае механической желтухи — это любыми средствами снизить концентрацию билирубина в крови ниже критического уровня.

Лечение
Пациентам с механической желтухой при раке печени и других заболеваниях оказывается быстрая и эффективная помощь в международной клинике Медика24.
Это дает возможность провести химиотерапию, лучевую терапию, хирургическую операцию (если она еще возможна).
С другой стороны, предотвращаются осложнения, угрожающие жизни пациента.
В нашей клинике применяются самые современные технологии, методики, а специалисты имеют большой опыт лечения механической желтухи, как при раке печени, так и во всех других случаях.
Методики
Прежде всего, мы приводим в норму уровень билирубина, чтобы можно было лечить рак печени.
В нашу клинику нередко поступают пациенты в тяжелом состоянии механической желтухи. В качестве экстренного средства может быть использовано переливание крови, хотя это дает лишь временный эффект.
Задача — восстановить эвакуацию желчи из печени. Для этого применяется один из четырех методов:
- Наружное дренирование.
Через брюшную стенку устанавливается зонд, который выводит желчь наружу. Благодаря этому устраняется застой в печени, желчь перестает поступать в кровь, и уровень билирубина снижается.
Недостаток этого метода состоит в том, что его можно использовать относительно недолго. Зонд раздражает брюшную стенку, при ношении он может в любой момент сместиться или даже выпасть. Он требует постоянного ухода, гигиенических процедур, снижает качество жизни.
Кроме того, наружное дренирование не восстанавливает поступление желчи в кишку, а значит, не восстанавливает усвоение жиров, жирорастворимых витаминов.
С другой стороны, зонд может быть использован для введения химиопрепаратов чтобы воздействовать на рак печени, желчного пузыря.
С помощью пункционной холангиографии врач находит место сдавления желчного протока. Здесь он разрезается и пришивается напрямую к кишечнику. Этот метод называется шунтированием, или созданием анастомоза — то есть искусственного пути эвакуации желчи в обход опухоли.
В этом случае наружное и внутреннее дренирование дополняют друг друга, то есть установка зонда совмещается с созданием анастомоза. В нашей клинике такие операции преимущественно выполняются щадящими, малоинвазивными способами — эндоскопическим, лапароскопическим.
Восстановить или увеличить просвет желчного протока можно с помощью пластикового или металлического стента — расширителя.
Стент вводится в желчный проток и при раскрытии расширяет его. Благодаря этому эвакуация желчи из печени и ее поступление в кишку улучшается, уровень билирубина снижается, исчезают симптомы интоксикации организма.
Лечение желтухи при раке печени и других органов гепатобилиарной системы имеет симптоматический характер. Его задача — предотвратить тяжелые осложнения интоксикации, снизить уровень билирубина и подготовить человека к основному лечению онкологического заболевания — химиотерапии, хирургической операции, лучевой терапии.
На 4 стадии рака, когда хирургическое лечение уже невозможно, методы устранения механической желтухи применяются в нашей клинике в паллиативных целях.
Симптомы механической желтухи
Пожелтение кожи и склер глаз — характерные, но не единственные симптомы механической желтухи. Еще один признак этого состояния — кожный зуд.
- потемнение мочи,
- обесцвечивание кала,
- горький привкус во рту,
- тяжесть и боль в правом подреберье,
- повышение температуры, озноб,
- тошнота,
- рвота, не приносящая облегчения,
- пожелтение слизистых поверхностей рта,
- увеличение живота,
- расширение поверхностных вен на животе, груди, шее, лице.
Кроме того, механическая желтуха проявляется:
- потерей аппетита,
- снижением веса,
- головными болями,
- головокружениями,
- шумом, звоном в ушах.

того что желчь не поступает в кишку, ухудшается переваривание жиров и усвоение жирорастворимых витаминов (А, К, Е). Это проявляется симптомами анемии, авитаминоза, в частности, слабостью, высокой утомляемостью.
Читайте также:

