Интоксикация при болезни паркинсона
Обновлено: 26.04.2024
Факторы провоцирующие паркинсонизм. Токсический паркинсонизм
Среди разнообразных провоцирующих факторов, непосредственно вызывающих паркинсонические симптомы, наибольшей тропностью к дофаминергическим системам обладают некоторые токсические агенты, в том числе лекарственные средства. Имеются указания на то, что нейролептики способны вызвать синдром паркинсонизма не только у лиц, предрасположенных к этому заболеванию (наличие семейной отягощенности), но и у лиц, явно не отягощенных; однако в первой группе больных лекарственный паркинсонизм возникал почти в семь раз чаще, чем во второй (соответственно в 22 и 3% случаев), что подтверждает значение предрасположенности наследственного характера в генезе лекарственного паркинсонизма. Высокая частота паркинсониче-ских синдромов, наблюдаемых в процессе лечения нейролептиками и другими препаратами, связана с химическим тропизмом используемых веществ.
Остальные провоцирующие факторы (сосудистые, травматические, воспалительные и пр.) не обладают специфической тропностью к дофаминергическим системам и поэтому реже вызывают синдром паркинсонизма.
Промежуточное положение между этими двумя классами этиологических факторов занимают психотравмы, поскольку имеются указания на участие дофаминергических систем мозга в механизме эмоционального стресса. Если этот факт будет окончательно подтвержден, то можно и психотравмы отнести к таким этиологическим факторам, которые обладают тропностью (хотя и менее выраженной, чем у нейролептиков) к дофаминергическим системам.
Определение удельного веса каждой этиологической формы паркинсонизма представляет объективно трудную задачу. Наиболее очевидным и легко учитываемым этиологическим фактором является лекарственная интоксикация. Однако и в данном случае большое значение часто приобретают другие факторы, участвующие в генезе паркинсонизма (предрасположенность наследственного или ненаследственного характера).
Не исключено также сочетание нескольких причин, сложным образом взаимодействующих друг с другом (одновременно или последовательно) и приводящих к появлению соответствующего заболевания. Вследствие объективных трудностей, возникающих на пути уточнения этиологии паркинсонизма, во многих публикациях по различным аспектам данной патологии авторы вообще не приводят этиологического диагноза, стараясь не касаться этого вопроса, или сознательно ссылаются на отсутствие общепризнанных и достоверных критериев этиологической диагностики заболевания. Не случайно в последнем американском руководстве по неврологии при обсуждении этиологии паркинсонизма авторы вообще не приводят процентного соотношения отдельных этиологических форм паркинсонизма.
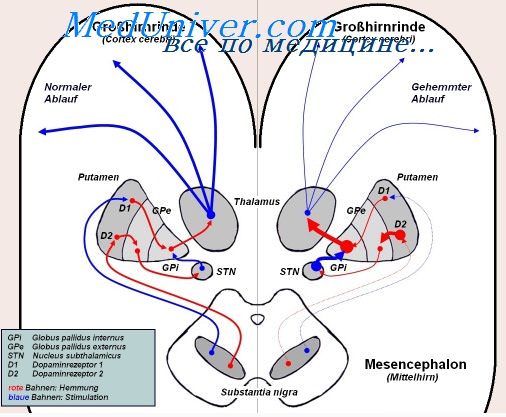
Этому общему клиническому ядру соответствуют сходные патоморфологические нарушения, обнаруживаемые при разных этиологических формах заболевания. Таким образом, разные этиологические факторы вызывают аналогичные изменения на клеточном уровне. Аналогичные изменения при разных этиологических формах паркинсонизма можно обнаружить также при биохимических, электрофизиологических, экспериментально-психологических и других исследованиях.
Эти данные указывают на общие патогенетические механизмы, лежащие в основе разных этиологических форм этой патологии. Лечение паркинсонизма также основано на патогенетической и симптоматической терапии, учет же этиологического фактора пока мало что привносит в эффективность лечения.
Правда, необходимо помнить, что, несмотря на известные успехи, достигнутые в последние годы в изучении паркинсонизма, эффективность терапии этого заболевания до сих пор остается сравнительно низкой. Именно поэтому необходимы дальнейшие поиски в изучении сущности паркинсонизма и его этиологии в частности.
Таким образом, результаты многочисленных исследований, посвященных проблеме этиологии паркинсонизма, с наибольшей вероятностью позволяют принять гипотезу, которая постулирует существование предрасположенности к паркинсонизму и множества этиологических факторов, способных реализовать указанную предрасположенность в прогредиентно текущий патологический процесс.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Нормотензивная гидроцефалия. Гемиатрофия-гемипаркинсонизм. Гипокинезии при интоксикациях.
Нормотензивная гидроцефалия является формой сообщающейся гидроцефалии. Приблизительно одна треть больных с указанным расстройством имеет в анамнезе спонтанное или травматическое субарахноидальное кровоизлияние, менингит, которые могли привести к нарушению механизмов абсорбции ЦСЖ над поверхностью мозга. Хотя давление ЦСЖ, измеренное при люмбальной пункции, в норме, существует избыточное давление на стенки расширенных боковых желудочков, особенно в передних рогах, ведущее к компрессии окружающих структур.
Применение методов нейровизуализации при нормотензивной гидроцефалии. Наблюдается расширение боковых желудочков (особенно передних и боковых рогов), которое происходит непропорционально выраженности корковой атрофии. МРТ обнаруживает перивентрикулярную гиперинтенсивность протонной плотности, свидетельствующую о наличии трансэпендимального тока ЦСЖ. Разграничение данных признаков с неспецифическим увеличением перивентрикулярных изменений в Т2-режиме у пожилых людей может быть затруднительным.

Изотопная цистернография, хотя и демонстрирует нарушение абсорбции ЦСЖ у некоторых пациентов, не рассматривается как надежный метод прогнозирования эффекта шунтирования. с Другие тесты. Тест Фишера состоит в удалении 30-50 мл ЦСЖ и наблюдении за улучшением клинической картины в течение следующих 24 ч. Это информативный тест, который не требует какой-либо сложной лабораторной техники. Мониторирование внутричерепного давления позволяет наблюдать периоды высокого давления ЦСЖ (b-волны) и прогнозировать эффект шунтирования.
Гемиатрофия-гемипаркинсонизм. При этом заболевании сравнительно рано на стороне гемиатрофии появляются признаки асимметричного синдрома паркинсонизма. У таких больных в анамнезе имеются указания на патологические роды, а также признаки атрофии контралатерального полушария. В совокупности это увеличивает вероятность неврологических расстройств в раннем детстве, а в дальнейшем обнаруживаются явления паркинсонизма. Медленное прогрессировать заболевания, редкое сочетание с дистонией и выраженная асимметрия проявлений являются основой для разграничения с ИБП.
Гипокинезии при интоксикациях.
- МФТП (1 -метил-4-фенил-1,2,3,6-тетрагидропиридин). Неумышленный прием этого токсического вещества привел к развитию острого выраженного паркинсо-нического симптомокомплекса у нескольких лиц с наркотической зависимостью. В лабораториях МФТП широко применяется для моделирования ИБП у животных. Новые случаи паркинсонизма, обусловленного его приемом, у людей в настоящее время встречаются редко.
- Окись углерода (СО). Паркинсонизм может развиваться вследствие острого или хронического отравления СО. Это вещество вызывает некроз бледного шара и полосатого тела. Экстрапирамидные нарушения могут возникать внезапно сразу же после инцидента, однако значительно чаще развиваются в течение нескольких дней или недель после выхода пациента из комы. Анамнестические данные (интоксикация СО), недостаточный эффект леводопы или его отсутствие подтверждают диагноз.
- Интоксикация марганцем может приводить к развитию синдрома паркинсонизма. Она часто сопровождается появлением необычных поведенческих расстройств (галлюцинации и эмоциональная лабильность), а также других двигательных нарушений, например, дистонии.
- Интоксикация цианидами и метанолом также может вызывать двусторонние некрозы базальных ганглиев и явления паркинсонизма.
Цереброваскулярные заболевания. Лакунарное состояние с множеством мелких инфарктов в области базальных ганглиев, как и подострая атеросклеротическая энцефалопатия, сопровождаются нарушением связей базальных ганглиев, что приводит к развитию паркинсонизма. При этих состояниях также часто наблюдается деменция. Тремор покоя у таких больных обычно отсутствует. Нарушения ходьбы могут быть очень заметными и иногда являются единственным неврологическим расстройством, что дает основание для термина «паркинсонизм нижней части тела*. Применение леводопы дает ограниченный положительный эффект.
Травма. Травматическая энцефалопатия боксеров — это прогрессирующий неврологический симптомокомплекс, состоящий из паркинсонизма, деменции и атаксии. Он наблюдается у боксеров с повторными травмами головы в анамнезе. Лечение обычно малоэффективно. Острое очаговое повреждение среднего мозга и черной субстанции или субдуральная гематома являются двумя другими возможными причинами посттравматического паркинсонизма.
Энцефалит. Приблизительно 50 % выживших после летаргического эпидемического энцефалита в 1917—1925 годах в дальнейшем, часто через несколько десятилетий, заболевали паркинсонизмом. С тех пор данная разновидность энцефалита в эпидемической форме не наблюдается. Соответственно, новые случаи постэнцефалитического паркинсонизма в настоящее время редки.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Идиопатическая болезнь Паркинсона. Вторичные паркинсонические расстройства.
Идиопатическая болезнь Паркинсона является наиболее частым вариантом паркинсонических расстройств. Это дегенеративное заболевание неизвестной, вероятно, многофакторной этиологии (результат влияния средовых и наследственных факторов). Возрастает количество доказательств того, что генетические факторы играют важную роль в развитии ИБП. Наблюдается высокая частота заболевания ИБП вторым из монозиготных близнецов, когда один из них заболел в молодом возрасте.
Мутация гена на 4 хромосоме, кодирующего синтез синаптического белка а-синуклеина, была обнаружена в семьях с редкой аутосомно-доминантно наследуемой разновидностью заболевания. При аутосомно-рецессивном варианте паркинсонизма ген на 6 хромосоме кодирует паркин — белок с неизвестными функциями. Однако дальнейшие исследования, проводимые с другими родственниками и пациентами, страдающими спорадическиой формой ИБП, убеждают в том, что ИБП лишь изредка возникает вследствие таких мутаций.
При ИБП была обнаружена метаболическая дисфункция митохондриального комплекса I, приобретенная или наследственная. Преобладание нарушений в pars compacta черной субстанции и нигростриарных проводящих путях приводит к дефициту дофамина в полосатом теле. Широкий спектр симптомов и устойчивость некоторых из них (депрессия) к препарату леводопа подтверждают представления о том, что дегенеративный процесс также затрагивает другие ядра ствола мозга и подкорковые структуры.

1. Клиническая картина болезни Паркинсона. Кардинальными симптомами являются тремор покоя, брадикинезия, ригидность и нарушение равновесия. Заболевание начинается асимметрично и чаще всего с появления тремора. Постуральная неустойчивость, затруднения ходьбы, вегетативная дисфункция обнаруживаются с прогрессированием болезни. Примерно у 30 % больных развивается деменция, однако она редко достигает тяжелой степени и никогда не бывает основным проявлением болезни.
Частота болезни Паркинсона резко увеличивается с возрастом, хотя заболевание может начинаться в любом периоде жизни человека. Заболевание, начинающееся между 21 и 39 годами, классифицируется как ИБП с началом в молодом возрасте. У таких пациентов происходит более постепенное развитие симптомов и в качестве раннего признака может наблюдаться дистония. Дискинезии, вызванные леводопой, а также колебания выраженности двигательных расстройств, которые могут появляться при ИБП в любом возрасте, чаще наблюдаются в данной возрастной группе. Дифференциальный диагноз ювенильного паркинсонизма (в возрасте до 21 года) требует рассмотрения широкого круга состояний, включая наследственные и метаболические расстройства.
2. Результаты применения методов нейровизуализации. МРТ и КТ головного мозга обычно неинформативны при ИБП. ПЭТ обнаруживает уменьшение захвата флуородопы в полосатом теле.
3. Невропатология. Тельца Леви (эозинофильные интрацитоплазматические включения), преимущественно в черной субстанции, являются патогистологическим маркером данного заболевания. При ИБП эти включения окрашивают на а-синуклеин, белок, продуцируемый мутантным геном при редкой аутосомно-доминантной форме ИБП.
4. Другие тесты. Специфические тесты для диагностики ИБП отсутствуют.
Вторичные паркинсонические расстройства.
Вторичные паркинсонические расстройства могут быть обусловлены множеством патологических процессов и факторов поражения мозга, особенно в области базальных ганглиев. Это инфекции, цереброваскулярные расстройства, интоксикации, метаболические нарушения, травма, опухоли, применение медикаментов, гипоксемия и гидроцефалия. Отдельные варианты синдрома паркинсонизма приведены ниже.
Другие атипичные нейролептики, рисперидон и оланзапин, могут вызывать явления паркинсонизма, особенно при назначении высоких доз. Внезапно развивающийся на фоне приема медикаментов паркинсонизм может быть частично объяснен определенной предрасположенностью к развитию паркинсонических нарушений. Обратное развитие паркинсонизма, вызванного приемом лекарственных средств, может занять несколько месяцев после отмены соответствующего препарата.
Что такое болезнь Паркинсона? Причины возникновения, диагностику и методы лечения разберем в статье доктора Полякова Т. А., невролога со стажем в 13 лет.
Над статьей доктора Полякова Т. А. работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Болезнь Паркинсона — это одно из самых распространенных нейродегенеративных заболеваний, поражающее преимущественно дофамин-продуцирующие (дофаминергические) нейроны в определенной области мозга, называемой чёрной субстанцией с накоплением в клетках белка альфа-синуклеина и особых внутриклеточных включений (телец Леви). Это заболевание — самая частая причина синдрома паркинсонизма (80% всех случаев). Распространенность болезни Паркинсона составляет около 140 (120-180) случаев на 100 000 населения. [1] Заболевание чаще всего проявляет себя после 50 лет, однако нередки случаи дебюта болезни и в более раннем возрасте (с 16 лет). Мужчины страдают немного чаще женщин.
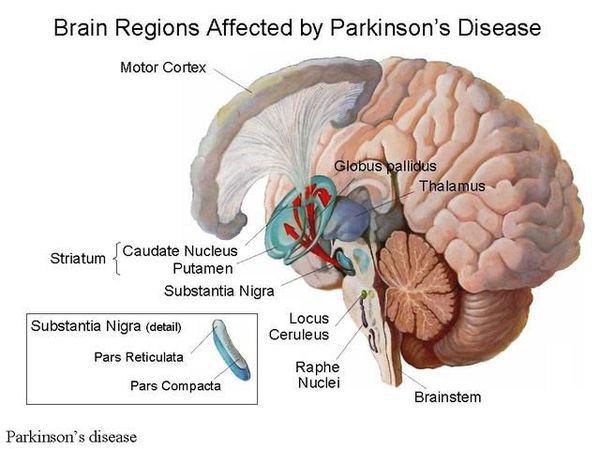
Причина остается в значительной степени неизвестной. Предполагается, что на возникновение заболевания влияют генетические факторы, внешняя среда (возможное воздействие различных токсинов), процессы старения. Генетические факторы имеют доминирующее значение при раннем развитии болезни Паркинсона. Молодые пациенты с этим заболеванием и с семейной историей болезни с большей вероятностью переносят гены, связанные с болезнью Паркинсона, такие, как SNCA, PARK2, PINK1 и LRRK2. В одном из последних исследований показано, что 65% людей с ранним началом болезни Паркинсона в возрасте до 20 лет и 32% людей с началом от 20 до 30 лет имели генетическую мутацию, которая, как полагают, увеличивает риск развития болезни Паркинсона. [2]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы болезни Паркинсона
- нарушение обоняния;
- расстройства сна;
- когнитивные симптомы (снижение памяти, легкомысленность);
- запор;
- расстройства мочеиспускания;
- повышенное потоотделение;
- сексуальную дисфункцию;
- усталость;
- боль (особенно в конечностях);
- покалывание;
- беспокойство и депрессию. [3]
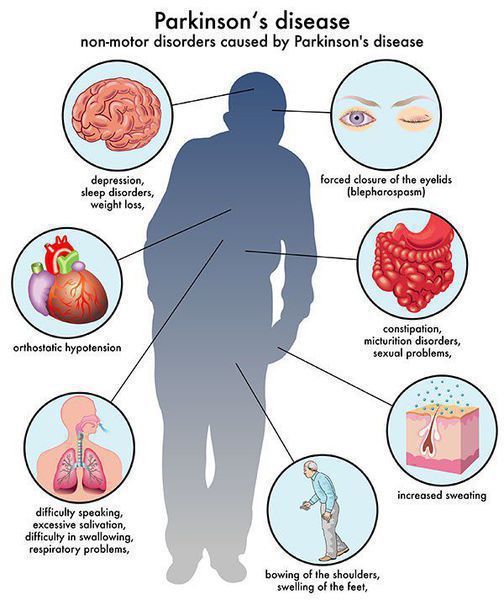
В начале заболевания нередко ставится неверный диагноз — плечелопаточный периартрит, проявляющийся болью и напряжением в мышцах руки и спины.
Синдром паркинсонизма является основным клиническим проявлением болезни Паркинсона, его симптомы: [1]
- замедленность всех движений;
- истощаемость быстрых повторяющихся движений в руках и ногах;
- скованность мышц (мышечная ригидность);
- дрожание рук и ног (но почти никогда — головы), наиболее выражено в покое;
- неустойчивость при ходьбе;
- укорочение длины шага и шарканье при ходьбе, топтание на месте, застывания при ходьбе, отсутствие cодружественных движений руками при ходьбе.
Вначале симптомы возникают только с одной стороны тела, но постепенно приобретают двусторонний характер. Симптомы остаются выраженными на той стороне, где возникли в начале заболевания. Симптомы на другой стороне тела часто не становятся такими же тяжелыми, как симптомы на начальной стороне. Движения становятся все более замедленными (основной симптом паркинсонизма). Симптомы заболевания колеблются в течения дня и зависят от многих факторов.
Патогенез болезни Паркинсона
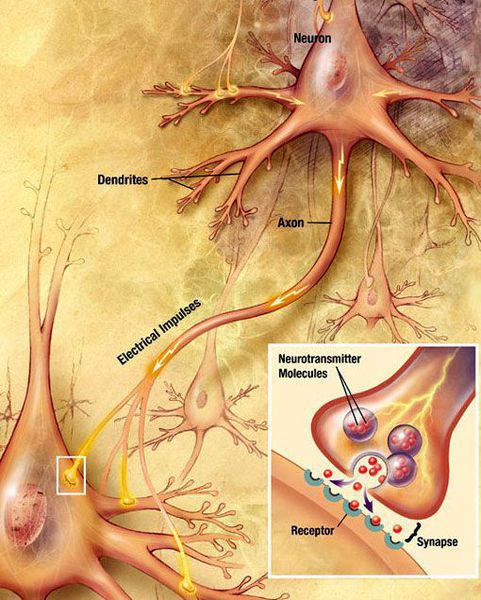
Болезнь Паркинсона относится к группе синуклеинопатий, так как избыточное накопление в нейронах альфа-синуклеина приводит к их гибели. Повышенный уровень альфа-синуклеина может быть следствием нарушения внутриклеточной системы клиренса белков, осуществляемого лизосомамии и протеосомами. У пациентов обнаружено нарушение функционирования указанной системы, среди причин которого указывают старение, окислительный стресс, действие воспаления, токсины окружающей среды. Клетки гибнут предположительно из-за активации генетически запрограмированного механизма (апоптоза). [4]
Классификация и стадии развития болезни Паркинсона
Болезнь Паркинсона классифицируется по форме, стадии и темпу прогрессирования заболевания.
В зависимости от преобладания в клинической картине того или иного симптома выделяют следующие формы: [1]
1. Смешанная (акинетико-ригидная-дрожательная) форма характеризуется наличием всех трёх основных симптомов в разном соотношении.
2. Акинетико-ригидная форма характеризуется выраженными признаками гипокинезии и ригидности, к которым обычно рано присоединяются нарушения ходьбы и постуральная неустойчивость, при этом тремор покоя отсутствует или выражен минимально.
3. Дрожательная форма характеризуется доминированием в клинической картине тремора покоя, признаки гипокинезии уходят на второй план.

Для характеристики стадий Болезни Паркинсона используется шкала Хен–Яра, 1967:
- на 1-й стадии акинезия, ригидность и тремор выявляются в конечностях с одной стороны (гемипаркинсонизм);
- на 2-й стадии симптоматика становится двусторонней;
- на 3-й стадии присоединяется постуральная неустойчивость, но сохраняется способность к самостоятельному передвижению;
- на 4-й стадии симптомы паркинсонизма резко ограничивают двигательную активность;
- на 5-й стадии в результате дальнейшего прогрессирования заболевания больной оказывается прикованным к постели.
Выделяют три варианта темпа прогрессирования заболевания:
- При быстром смена стадий заболевания от первой к третьей занимает 2 года или менее.
- При умеренном — от 2 до 5 лет.
- При медленном — более 5 лет.
Осложнения болезни Паркинсона
Болезнь Паркинсона — не смертельное заболевание. Человек умирает с ним, а не от него. Однако поскольку симптомы ухудшаются, они могут вызвать инциденты, которые приводят к смерти. Например, в сложных случаях затруднение глотания может привести к тому, что пациенты начнут аспирировать пищу в легкие, что приведет к пневмонии или другим легочным осложнениям. Потеря равновесия может привести к падению, которое, в свою очередь, может привести к серьезным травмам или смерти. Серьезность этих инцидентов во многом зависит от возраста пациента, общего состояния здоровья и стадии заболевания.
На более поздних стадиях заболевания проявляются более выраженные симптомы болезни Паркинсона: дискинезия (непроизвольные движения или подергивание частей тела, которые могут возникнуть в результате длительного использования леводопы, застывания (внезапное отсутствие возможности двигаться) или семенящая походка (короткие, почти бегущие шаги, которые как будто ускоряются сами по себе).
Следует помнить, что болезнь Паркинсона очень индивидуальна по своему течению и у каждого протекает по своему сценарию.
Диагностика болезни Паркинсона
Паркинсонизм относится к числу тех расстройств, которые можно диагностировать на расстоянии, особенно при развёрнутой картине заболевания. Однако диагностировать болезнь Паркинсона на ранней стадии сложно. Ранняя и точная диагностика заболевания очень важна для разработки лучших стратегий лечения и поддержания высокого качества жизни как можно дольше. В практике возможна недооценка или переоценка болезни Паркинсона. Невролог, специализирующийся на расстройствах движения сможет поставить наиболее точный диагноз. Первоначальная оценка проводится на основе анамнеза, неврологического обследования с использованием специальных тестов для оценки симптомов заболевания. Неврологическое обследование включает в себя оценку координации, ходьбы и мелких моторных задач, оценку нейропсихологического статуса.
Практика получения второго мнения в значительной степени зависит от личного выбора пациента. Но имейте в виду, что болезнь Паркинсона часто трудно диагностировать точно, особенно когда симптомы незначительно выражены. Простейшего диагностического теста нет, и примерно 25% диагнозов болезни Паркинсона неверны. Болезнь Паркинсона начинается с мало видимых симптомов, поэтому многие врачи, которые не обучены в сфере двигательных расстройств, не могут поставить точный диагноз. На самом деле даже лучшие неврологи могут ошибаться. Если врач не имеет особого опыта в этой области, то необходимо консультироваться со специалистом по расстройствам движения. Хороший невролог поймет ваше желание подтвердить диагноз. Второе мнение может помочь принять своевременно правильные решения относительно диагноза и терапии.
Лечение болезни Паркинсона
Несмотря на то, что излечения болезни Паркинсона не существует, есть множество методов, которые могут позволить вести полноценную и продуктивную жизнь на многие годы вперед. Многие симптомы могут облегчаться лекарствами, хотя со временем они могут утратить свою эффективность и вызвать нежелательные побочные эффекты (например, непроизвольные движения, известные как дискинезия).
Существует несколько методов лечения, замедляющих появление моторных симптомов и улучшающих двигательные функции. Все эти методы лечения предназначены для увеличения количества дофамина в головном мозге либо путем его замещения, либо продления эффекта дофамина путем ингибирования его распада. Исследования показали, что терапия на ранней стадии может задержать развитие двигательных симптомов, тем самым улучшая качество жизни. [5]
На характер и эффективность лечения влияет ряд факторов:
- выраженность функционального дефицита;
- возраст больного;
- когнитивные и другие немоторные нарушения;
- индивидуальная чувствительность к препаратам;
- фармакоэкономические соображения.
Задача терапии при болезни Паркинсона — восстановить нарушенные двигательные функции и поддержать оптимальную мобильность в течение максимально длительного периода времени, сведя к минимуму риск побочных действий препаратов. [1]
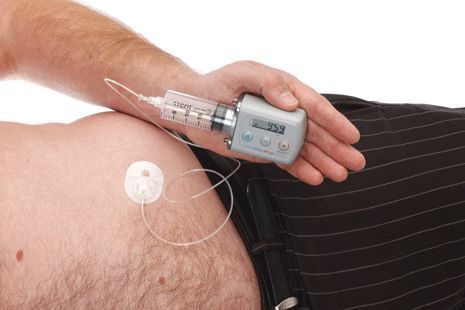
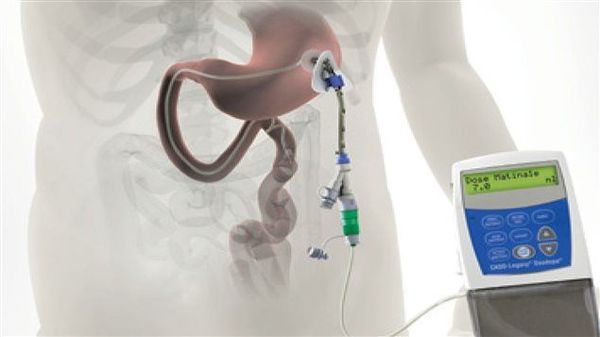
Исследуется альтернативный подход, использование допаминовых продуцирующих клеток, полученных из стволовых клеток. Хотя терапия стволовыми клетками имеет большой потенциал, требуется больше исследований, прежде чем такие клетки могут стать инструментом в лечении болезни Паркинсона. [8] [9]
При болезни Паркинсона очень полезна физическая нагрузка. Если дважды в неделю по 1–2 часа выполнять упражнения, то можно замедлить развитие заболевания: походка, осанка и когнитивные способности будут ухудшаться гораздо медленнее [12] .
Прогноз. Профилактика
Болезнь Паркинсона уникальна для каждого человека, никто не может предсказать, какие симптомы появятся и когда именно. Существуют общее сходство картины прогрессирования болезни, но нет никакой гарантии, что то, что наблюдается у одного, будет у всех с аналогичным диагнозом. Некоторые люди оказываются в инвалидных колясках; другие все еще участвуют в марафонах. Некоторые не могут застегнуть ожерелье, в то время как другие делают ожерелья вручную.
Пациент может сделать всё, чтобы активно повлиять на течение болезни Паркинсона и, по крайней мере, на одну очень вескую причину: ухудшение симптомов часто значительно медленнее у тех, кто проявляет позитивную и активную позицию по отношению к своему состоянию, чем те, кто этого не делает. В первую очередь рекомендуется найти врача, которому доверит пациент, и который будет сотрудничать по развивающемуся плану лечения. Снижение стресса обязательно — стресс ухудшает каждый симптом болезни Паркинсона. Рекомендуются занятия образовательного направления: рисование, пение, чтение стихов, рукоделие, изучение языков, путешествия, работа в коллективе, занятия общественной деятельностью.
К сожалению, даже если адекватно подобрать медикаментозную терапию, это не гарантирует того, что клетки перестанут гибнуть при болезни Паркинсона. Терапия должна быть направлена на создание благоприятных условий для двигательной активности с учётом индивидуальных особенностей клинической картины заболевания. Как показывают результаты многочисленных исследований, профессиональная двигательная реабилитация является необходимым условием для замедления прогрессирования заболевания и улучшения его прогноза. На сегодняшний день по данным клинических исследований показана эффективность реабилитационной программы по протоколам LSVT LOUD, LSVT BIG, теоретическая основа которых сводится к развитию нейропластичности вещества мозга. Она направлена на коррекцию дрожания, ходьбы, постуры, равновесия, мышечного тонуса и речи. [10]
Реабилитационные методики должны быть направленные не только на поддержание сохранившихся двигательных способностей, но и выработку новых навыков, которые бы помогали человеку с болезнью Паркинсона преодолевать ограниченность его физических возможностей, чему способствует программа танцевально-двигательной терапии при болезни Паркинсона, работающая более чем в 100 сообществах по всему миру, включая Россию. Танцевальная терапия позволяет частично решить конкретные проблемы болезни Паркинсона: потеря равновесия, ухудшение координации, шаркающая походка, тремор, застывания, социальная изоляция, депрессия и повышенный уровень тревожности.
Согласно американскому исследованию с участием 52 больных болезнью Паркинсона, регулярная практика аргентинского танца уменьшает симптомы болезни, улучшает баланс и улучшает выполнение сложных движений при болезни Паркинсона. [11]
Вторичный паркинсонизм — клинический термин, объединяющий все случаи появления синдрома паркинсонизма, обусловленные воздействием различных поражающих ЦНС факторов или наличием первичного заболевания. В отличие от болезни Паркинсона вторичный паркинсонизм имеет более острое начало, характеризуется первоначальной симметричностью паркинсонических проявлений и присутствием других симптомов поражения ЦНС. Диагностируется на основании анамнестических и клинических данных с учетом результатов МРТ головного мозга. Лечение направлено на купирование основного этиологического фактора и блокирование патогенетических механизмов развития паркинсонизма.
МКБ-10
Общие сведения
Вторичный паркинсонизм — обобщающее клиническое понятие, включающее все случаи возникновения симптомов болезни Паркинсона, связанные с повреждением нейронов базальных ядер мозга под воздействием различных экзо- и эндогенных факторов. В отличие от паркинсонизма вторичного характера идиопатическая болезнь Паркинсона возникает самостоятельно, без связи с какими-либо поражающим головной мозг фактором. Вторичный паркинсонизм составляет около 30%, в остальных случаях диагностируется болезнь Паркинсона. В соответствии с этиологией выделяют лекарственный, посттравматический, токсический, постгипоксический, постинфекционный, сосудистый паркинсонизм. Наиболее распространен лекарственный паркинсонизм. Большинство его случаев приходится на злокачественный нейролептический синдром, развивающийся при длительном или неадекватном приеме нейролептиков. Вопрос дифференцировки болезни Паркинсона и вторичного паркинсонизма имеет принципиальное значение для практиков в области неврологии, поскольку подходы в их терапии существенно отличаются.

Причины вторичного паркинсонизма
Паркинсонические проявления могут возникать в связи с перенесенной тяжелой ЧМТ (ушибом и сдавлением головного мозга) или частыми ЧМТ легкой степени (сотрясениями головного мозга). Причинами постинфекционного паркинсонизма бывают энцефалит и общие инфекции (корь, ВИЧ, эпидемический паротит, герпес и др.). Различные отравления (тяжелыми металлами, угарным газом, синильной кислотой, метанолом), в случае не проведения своевременной дезинтоксикации, способны вызывать токсический паркинсонизм. Возникновение синдрома паркинсонизма возможно при интоксикации марганцем, что наблюдается при наркомании с употреблением синтетических наркотиков (синтетического героина, экстази). К фармпрепаратам, при приеме которых существует риск развития вторичного паркинсонизма, относятся антипсихотики (нейролептики, некоторые антидепрессанты), антиконвульсанты, симпатолитики, противорвотные (метоклопрамид).
Этиофакторами сосудистого паркинсонизма выступают обширный ишемический инсульт, множественные лакунарные инфаркты мозга, хроническая ишемия головного мозга при атеросклерозе. Паркинсонизм может наблюдаться после перенесенной гипоксии не зависимо от ее генеза, в том числе у пациентов, выживших после реанимационных мероприятий. Спровоцировать развитие вторичного паркинсонизма способны: гидроцефалия, повторные эпизоды гипогликемии, внутримозговые опухоли. Синдром паркинсонизма может наблюдаться при различных дегенеративных заболеваниях ЦНС: болезни Вильсона, деменции с тельцами Леви, прогрессирующем надъядерном параличе, кортикобазальной дегенерации, рассеянном склерозе и пр. В отношении таких случаев употребляют термин "паркинсонизм плюс".
Симптомы вторичного паркинсонизма
Основными клиническими проявлениями паркинсонизма выступают брадикинезия, мышечная ригидность и постуральный тремор. Брадикинезия представляет собой уменьшение количества и скорости движений; пациенты становятся медлительными, постепенно у них исчезает жестикуляция, обедняется мимика, ходьба перестает сопровождаться сопутствующими движениями рук. Мышечная ригидность — это постоянное напряжение мышц, которое вначале обнаруживается при попытке пассивных движений в конечности, а затем становиться заметно по постоянно полусогнутым в локтях и коленях конечностям. Постуральный тремор обычно выражен в руках и голове, мелкое дрожание которых происходит в покое и исчезает при двигательных актах. Со временем указанные симптомы приводят к значительной обездвиженности больного, сопровождаются постуральными расстройствами (нарушениями согласованности движений, способности удерживать определенную позу); происходят характерные изменения личности, присоединяются мнестические нарушения.
Отличительной чертой клиники вторичного паркинсонизма является более быстрое развитие симптомов при манифестации заболевания и их ускоренное прогрессирование в дальнейшем. Типична симметричность проявлений, в то время как при болезни Паркинсона симптомы возникают вначале на одной стороне и приобретают двусторонний характер только спустя некоторое время. При вторичном характере паркинсонизма его проявления сочетаются с другими симптомами церебрального поражения: пирамидным синдромом, мозжечковой атаксией, ранними интеллектуальными нарушениями и пр. В анамнезе пациентов, как правило, имеется указание на предшествовавшее появлению паркинсонического синдрома действие того или иного этиофактора (ЧМТ, инсульт, прием нейролептиков, энцефалит и т. п.). В лечении отмечается незначительная эффективность дофаминергических средств, а устранение этиофактора иногда способствует значительному регрессу паркинсонических проявлений.
Диагностика вторичного паркинсонизма
Существенное диагностическое значение при наличии симптомокомплекса паркинсонизма имеет выявление признаков его вторичного характера: существование этиофактора в анамнезе, быстрая манифестация, наличие в статусе других неврологических симптомов. При появлении психопатологических проявлений необходима консультация психиатра. Осмотр офтальмолога позволяет определить наличие свойственных гидроцефалии изменений на глазном дне или патогномоничную для болезни Вильсона пигментацию по периферии радужки (кольцо Кайзера-Флейшера).
Выявление вероятных причин вторичного синдрома паркинсонизма осуществляется при помощи МРТ головного мозга, которая более информативна в сравнении с КТ при визуализации дегенеративных очагов и дифференциации внутримозговых объемных образований. При гидроцефалии МРТ определяет расширенные желудочки мозга, при постинсультных состояниях — зоны инфарктов и т. д. Однако выявление подобных изменений само по себе не говорит о вторичности паркинсонизма. Интерпретировать результаты томографии необходимо только соотнося их с клиническими данными, поскольку нельзя исключить наличие комбинации болезни Паркинсона с рядом других церебральных заболеваний или, например, существование вторичного не сосудистого паркинсонизма на фоне сосудистых нарушений.
Лечение вторичного паркинсонизма
Основу терапии составляют препараты, используемые для лечения болезни Паркинсона. К ним относятся агонисты дофаминовых рецепторов (пирибедил, прамипексол, бромокриптин), фармпрепараты левадопы, селективные необратимые ингибиторы МАО (моклобемид, пирлиндол, бефол). Лечение стартует с монотерапии. Препаратом выбора, как правило, выступает проноран. В отличие от болезни Паркинсона при вторичном паркинсонизме левадопа показывает слабую эффективность.
Параллельно с противопаркинсоническим лечением осуществляется терапия, направленная на причину поражения базальных ядер. При токсическом паркинсонизме осуществляется дезинтоксикация, при постгипоксическом — оксигенотерапия и нейрометаболическое лечение, при сосудистом — сосудистая терапия (винпоцетин, ницерголин, пентоксифиллин). Лекарственный паркинсонизм является показанием к отмене или замене обусловившего его возникновение препарата. При посттравматическом и постинфекционном паркинсонизме показаны курсы нейрометаболической терапии (пирацетам, пиритинол, витамины гр. В, липоевая к-та). направленной на замедление происходящих в нейронах дегенеративных процессов. Основное лечение дополняется массажем для уменьшения ригидности и ЛФК для как можно более длительного сохранения двигательной активности пациента.
Читайте также:

