Исследование воздуха на инфекции
Обновлено: 19.04.2024
Лабораторные исследования при инфекционных заболеваниях. Методы
Отбор проб для анализа при инфекционных заболеваниях. Для микробиологического исследования может быть отобрана любая ткань или физиологическая жидкость организма.
Выделение чистой культуры способствует увеличению количества бактерий и их точной идентификации. Для этого используют питательные среды. Если в образце присутствует нормальная микрофлора, то применяют избирательные (селективные) среды, позволяющие создать условия, неблагоприятные для роста непатогенных микроорганизмов и способствующие росту патогенной микрофлоры.
Для получения точных результатов следует выбрать оптимальный метод отбора проб и подойти к этому процессу с должной аккуратностью. При несоблюдении правил асептики контаминация проб крови микроорганизмами извне может привести к назначению неправильного лечения.
Большинство бактерий не способны существовать вне организма хозяина: облигатные анаэробы погибают под действием кислорода воздуха, а некоторые возбудители очень чувствительны к высыханию (Neisseria gonorrhoeae). Именно поэтому анализируемые образцы сразу после отбора должны быть помещены на подходящие среды или посеяны на среды для транспортировки.
Лабораторные методы исследования при инфекционных заболеваниях
Образцы могут быть проанализированы невооружённым глазом (например, для определения взрослых гельминтов в фекалиях или крови в мокроте). Микроскопия — быстрый и недорогой метод исследования, но требует высокого технического мастерства, характеризуется низкой чувствительностью: для точного определения необходимо присутствие большого количества возбудителей.
Кроме того, очень часто условно-патогенные микроорганизмы принимают за патогенные, что связано с недостаточной специфичностью метода.
Для определения возбудителя могут быть использованы различные красители (например, аурамин или окрашивание по Цилю—Нильсену для идентификации микобактерий). Уротропиновый серебряный окрашивает хитин клеточной стенки грибов и Pneumocystis jiroveci. Краситель Гимза применяют для окрашивания возбудителей малярии, лейшманий и других паразитов.
В основе иммунофлюоресцентного метода лежит применение специфических антител, помеченных флюоресцентными маркёрами. Микроскопию осуществляют в ультрафиолетовом свете, при этом возбудитель и связанные с ним антитела светятся ярко-зелёным цветом.
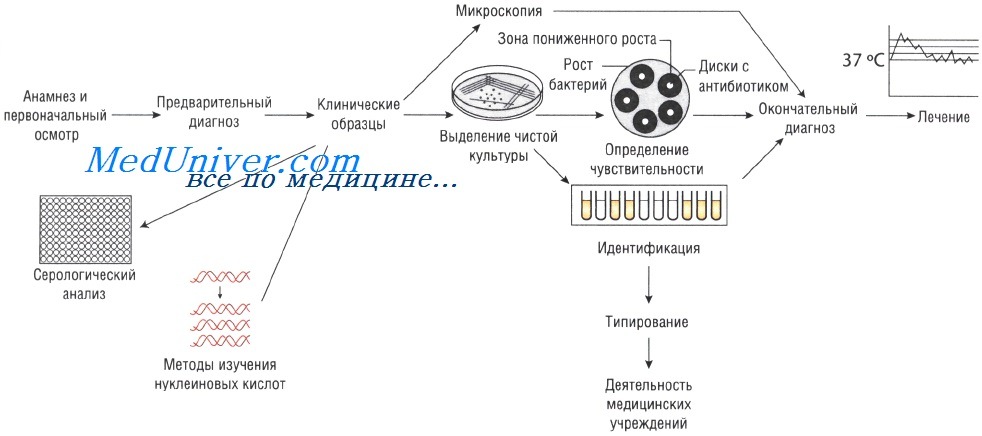
Лабораторные исследования при инфекционных заболеваниях
Выделение чистой культуры возбудителя при инфекционных заболеваниях
Иногда, даже при выраженных клинических симптомах, возбудитель может присутствовать в очаге инфекции в количестве, недостаточном для микроскопического определения. В этом случае выделение чистой культуры позволяет увеличить численность микроорганизмов в исследуемом субстрате.
Существует два способа выращивания микроорганизмов: на жидких (увеличивается количество возбудителей) и твёрдых (исследуют отдельные колонии, в том числе и на чувствительность к антибиотикам) питательных средах. Большинство возбудителей инфекций человека достаточно требовательны к условиям культивирования. Именно поэтому питательные среды для их выращивания должны содержать белки, сахарозу и нуклеиновые кислоты (присутствующие в крови и сыворотке).
Кроме того, необходимо поддерживать соответствующий газовый состав: для культивирования анаэробов необходимо отсутствие кислорода, в то время как для облигатных аэробов (Bordetella pertussis) — наоборот. Оптимальная температура выращивания большинства патогенных микроорганизмов составляет 37 °С; культивирование некоторых фибов осуществляют при 30 С.
Идентификация возбудителя инфекционного заболевания
Симптомы заболеваний зависят от вида возбудителей, вызвавших их. Именно поэтому идентификация микроорганизма позволяет предположить клиническую картину вызываемого им заболевания (например, симптомы инфекции, вызванной Vibrio cholerae, отличны от таковых при заражении Shigella sonnei). Большое значение имеет выделение Neisseria meningitidis именно из спинномозговой жидкости. Идентификация микроорганизмов основана на:
• изучении морфологических свойств их колоний в агаре;
• различной окраске по Граму;
• способности возбудителей к образованию спор;
• изучении биохимических свойств (каталазный или коагулазный тесты).
Точное определение штамма обычно зависит от результатов биохимического анализа (например, уреазный тест) или обнаружения продуктов жизнедеятельности бактерий (индол). Возбудителей, которые не могут быть выращены на питательных средах, идентифицируют при помощи молекулярно-генетического метода ДНК и секвенирования (например, Trophyrema whippelii).

Определение чувствительности возбудителя инфекционного заболевания к антибиотикам
Если для эрадикации микроорганизмов достаточно стандартной дозы антимикробного препарата, то их считают чувствительными, если необходимо увеличение дозы лекарственного средства — относительно устойчивыми. Абсолютно устойчивыми (резистентными) называют возбудителей, в отношении которых антибиотикотерапия неэффективна. Существует широкий спектр различных методов определения чувствительности к антимикробным препаратам.
Методы Британской ассоциации антимикробной химиотерапии (British Society of Antimicrobial Chemotherapy — BSAQ и Института клинических лабораторных стандартов (Clinical Laboratory Standards Institute — С LSI) основаны на определении диаметра зоны слабого роста микроорганизмов на твёрдой питательной среде при применении антимикробного препарата.
Минимальную подавляющую концентрацию антибиотика измеряют с помощью Е-теста, растворения препарата в питательном бульоне или нанесения его на плотный агар. В последнем случае на засеянный исследуемыми микроорганизмами агар наносят бумажные диски, пропитанные различными антибиотиками (метод бумажных дисков).
Уровень чувствительности зависит от диаметра зоны пониженного роста бактерий. Однако тестирование in vitro предоставляет лишь приблизительные данные, так как в клинической практике многое зависит от состояния больного.

Серологический анализ при инфекционном заболевании
Различные виды инфекций можно идентифицировать с помощью определения иммунного ответа, возникающего при внедрении возбудителя. Для этого существует большое количество различных методов: реакция агглютинации (РА), реакция связывания комплемента (РСК), реакция нейтрализации (РН) и иммуноферментный анализ (ИФА). Диагноз устанавливают на основании:
• определения уровня антител (IgM) в ответ на попадание в организм чужеродного белка (антигена);
• определения антигена.
Молекулярный анализ при инфекционном заболевании
Южный блоттинг и метод гибридизации нуклеиновых кислот. Методы основаны на связывании меченой ДНК с анализируемым образцом, при условии, что он имеет определённую последовательность аминокислот. Связанный комплекс определяют по активности метки. Это достаточно быстрый и надёжный способ, который, тем не менее, уступает по чувствительности молекулярно-генетическим методам.

Метод молекулярно-генетический (NAAT)
Для диагностики инфекционных заболеваний используют несколько молекулярно-генетических методов. Механизм выделения патогенной ДНК или РНК в количестве, достаточном для постановки диагноза, для каждого метода индивидуален. Так, при молекулярно-генетическом методе ДНК возбудителя разделяют на отдельные цепи, затем синтезируют праймеры для связывания с целевыми последовательностями. Образование новой ДНК катализирует полимераза.
Основное преимущество — достижение результата даже при наличии всего лишь одной копии ДНК. Благодаря автоматизированным системам и большому выбору специальных наборов эти методы стали доступны большинству диагностических лабораторий. Новые аппараты способны выдавать результат в режиме реального времени. Генетические методы позволяют идентифицировать микроорганизмы, выращивание которых отличается сложностью или сопряжено с риском для человека (например, Mycobacterium tuberculosis и Chlamydia trachomatis).
Кроме того, их можно использовать для определения генов, кодирующих устойчивость к действию антибиотиков (например, мутационный ген rpoВ, обеспечивающий устойчивость М. tuberculosis к рифампицину). Это позволяет заранее выбрать альтернативный путь лечения инфекционных заболеваний.
Иногда необходимо проводить типирование микроорганизмов в случае их распространения в больницах или в окружающей (внебольничной) среде.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
ГлавнаяHelixbook Посев на аэробную и факультативно-анаэробную флору с определением чувствительности к расширенному списку антибиотиков и подбором минимальной эффективной дозировки препарата
Посев на аэробную и факультативно‑анаэробную флору с определением чувствительности к расширенному списку антибиотиков и подбором минимальной эффективной дозировки препарата
Микробиологическое исследование на анализаторе VITEK bioMerieux, позволяющее с более высокой чувствительностью и специфичностью, чем обычный посев, идентифицировать около 200 видов клинически значимых бактерий и подобрать антибиотикотерапию с расчетом минимальной эффективной дозировки препарата. Преимущества исследования по сравнению с обычным посевом: срок выполнения короче на 24 часа; чувствительность определяется к расширенному списку антибиотиков (до 20 шт.); результат выдается как в виде критических значений (чувствителен, умеренно-устойчив, устойчив), так и в виде значений минимальных ингибирующих концентраций антибиотика (МИК). Что, в свою очередь, позволяет выбрать наиболее эффективную минимальную дозу антибиотика, снизив его негативное влияние на человеческий организм. * Чувствительность к антибиотикам будет определена при выявлении патогенных и/или условно-патогенных микроорганизмов. При обнаружении микроорганизмов, составляющих нормальную микрофлору, чувствительность к антибиотикам не определяется, т.к. не имеет диагностического значения.
Синонимы русские
Бактериологическое исследование клинического материала с определением чувствительности к антибиотикам на анализаторе VITEK bioMerieux; посев на микрофлору в аэробных условиях.
Метод исследования
Какой биоматериал можно использовать для исследования?
Грудное молоко, мазок из десневого кармана, мазок из зева, мазок с конъюнктивы, мазок из носа, мазок из носоглотки, мазок урогенитальный (с секретом предстательной железы), мокроту, отделяемое уха, рвотные массы, синовиальную жидкость, смыв из бронхов, соскоб с кожи, среднюю порцию утренней мочи, эякулят.
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Анаэробная микрофлора – это микроорганизмы, для жизнедеятельности и размножения которых не требуется кислород, для многих из них он, наоборот, является губительным. Анаэробы населяют организм человека в норме (в пищеварительном тракте, органах дыхания, мочеполовой системе). При снижении иммунитета или травмах, повреждениях возможна активация инфекции с развитием воспалительного процесса. Организм человека тогда может становиться по сути источником заражения сам для себя (эндогенное инфицирование). Реже анаэробы попадают в организм снаружи (глубокая колотая рана, инфицированный аборт, ранения брюшной и грудной полости, введение спиц и протезов). Развиваясь в толще кожи, мягких тканей и мышц, анаэробные организмы способны вызывать целлюлиты, абсцессы, миозиты. Симптомы, позволяющие заподозрить анаэробную инфекцию мягких тканей: плотный отёк, газообразование (ощущение, что лопаются пузырьки воздуха под кожей при надавливании), гнилостное воспаление, зловонный запах.
Основное лечение анаэробного воспаления – хирургическое. При этом необходимо устранить источник воспаления либо раскрыть рану, обеспечив доступ кислорода, губительного для анаэробов.
Жизнедеятельность аэробной флоры возможна лишь при наличии свободного кислорода. В отличие от анаэробов, у них он участвует в процессе выработки энергии, необходимой им для размножения. Эти бактерии не имеют выраженного ядра. Они размножаются почкованием или делением, при окислении образуя токсичные продукты. Культивирование аэробных бактерий подразумевает не только использование подходящей для них питательной среды, но также и количественный контроль кислородной атмосферы и поддерживание оптимальных температур. Для каждого микроорганизма данной группы существует минимум и максимум кислородной концентрации в среде, окружающей его, необходимой для его нормального размножения и развития.
Факультативные анаэробы – организмы, которые существуют и выполняют все энергетические и репродуктивные циклы по анаэробному пути, но при этом при этом способны существовать и развиваться в присутствии кислорода. Последней характеристикой облигатные и факультативные анаэробы и отличаются, т.к. облигатные не способны существовать в условиях кислорода и при его появлении гибнут. Всю необходимую для своего существования, развития и размножения энергию факультативные анаэробы получают с помощью расщепления органических и неорганических соединений.
Для дифференциальной диагностики анаэробной и аэробной инфекции проводят посев биоматериала на флору, так как принципы лечения в том или ином случае будут разные. По выросшей культуре определяется вид микроорганизмов, которые участвуют в формировании воспалительной реакции. Зная вид возбудителя, можно подобрать антибактериальный препарат, который способен успешно влиять на данные микроорганизмы.
В ходе данного исследования определяется наличие аэробной и факультативно-анаэробной флоры.
Микробиологическое исследование на анализаторе VITEK bioMerieux позволяет с более высокой чувствительностью и специфичностью, чем обычный посев, идентифицировать около 200 видов клинически значимых бактерий и подобрать антибиотикотерапию с расчетом минимальной эффективной дозировки препарата. Система анализатора предназначена для идентификации грамотрицательных палочек, грамположительных кокков, анаэробных бактерий, нейссерий, гемофильных палочек, других прихотливых бактерий, коринбактерий, лактобактерий, бацилл, грибов (более 450 таксонов). Система анализатора состоит из анализатора бактериологического и персонального компьютера. Автоматизация процесса снижает риск контаминации материала и ошибок в результатах исследования.
После выявления культуры бактерий целесообразно провести определение их чувствительности к разным антибиотикам. Зная вид возбудителя, можно подобрать антибактериальный препарат, который способен успешно влиять на данные микроорганизмы. В связи с тем что все чаще наблюдается развитие антибиотикорезистентности микроорганизмов, подбор антибиотиков по их спектру действия на бактерии может привести к малоэффективному или вообще безрезультатному лечению. Преимуществом метода определения чувствительности к антибиотикам является точное определение антибактериального препарата, имеющего наивысшую эффективность в конкретном случае.
Для чего используется исследование?
- Дифференциальная диагностика анаэробной и аэробной инфекций, подбор адекватного терапевтического лечения с учетом обнаруженной микрофлоры.
- Диагностика латентных, скрытых и хронических инфекций: обнаружение персистирующих, труднокультивируемых и/или некультивируемых форм микроорганизмов.
- Для выбора антибиотика для успешного лечения инфекции.
Когда назначается исследование?
- При различных патологиях воспалительно-инфекционного генеза - для своевременной, быстрой идентификации возможного возбудителя.
- При симптомах, позволяющих заподозрить анаэробную инфекцию (газообразование, гнилостное воспаление).
Что означают результаты?
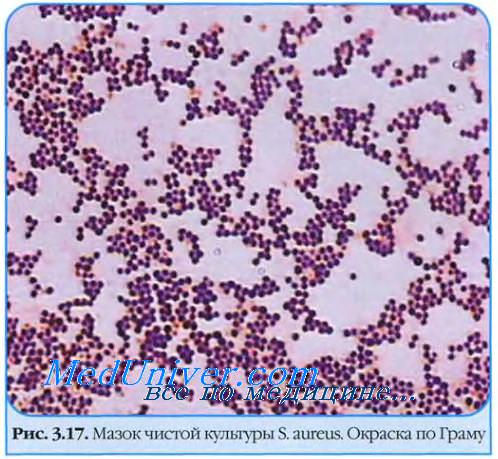
Причина выявления микроорганизмов - присутствие роста колоний данного вида микроорганизмов на питательной среде (при этом данная микрофлора может быть нормальной: Streptococcus mitis, Neisseria mucosa, Staphylococcus aureus, Streptococcus viridans group).
Данное исследование не предусматривает выделение анаэробной микрофлоры, вирусов, хламидий, а также микроорганизмов, требующих особых условий культивирования, таких как Neisseria meningitidis, Neisseria gonorrhoeae, Bordetella pertussis, Bordetella parapertussis, Corynebacterium diphtheriae, Mycoplasma spp, Ureaplasma spp, Mycobacterium tuberculosis. При отсутствии роста диагностически значимой микрофлоры при бактериологическом посеве и наличии клинической картины рекомендуется назначение дополнительных исследований.
Также рекомендуется
Кто назначает исследование?
Инфекционист, терапевт, гинеколог, врач общей практики, оториноларинголог, педиатр.
Воздух не является благоприятной средой для жизнедеятельности микроорганизмов. Однако, попадая в воздух, многие микроорганизмы способны какое-то время находиться в жизнеспособном состоянии. Среди них большая
группа патогенных и условно-патогенных микроорганизмов. Человек, болеющий инфекциями верхних дыхательных путей, выделяет микроорганизмы при разговоре, чихании, кашле и т.д. Через воздух передается группа заболеваний, которая так и называется — инфекции дыхательных путей с воздушно-капельным и воздушно-пылевым механизмами передачи. К таким инфекциям относятся грипп, корь, коклюш, скарлатина, дифтерия, натуральная оспа, легочная форма чумы, менингит, туберкулез, ветряная оспа, паротит и другие.
Задачами санитарно-микробиологического исследо-вания воздуха являются гигиеническая и эпидемиоло-гическая оценка воздушной среды, и, как следствие, разработка комплекса мероприятий, направленных на профилактику аэрогенной передачи возбудителей инфекционных болезней. Объектами санитарно-микробиологического исследования воздуха закрытых помещений являются: воздух больниц (операционные, отделение реанимации, родильные залы роддомов, и т.п.), детских садов, школ, поликлиник, аптек, производственных цехов и вспомогательных помещений на предприятиях различного профиля (пищевых, микробного синтеза и т.п.), а также мест массового скопления людей -кинотеатров, спортивных залов и т. д.
В последнее время внимание санитарных микробиологов привлекают крупные животноводческие комплексы и птицефабрики. Так было показано, что в воздухе птицефабрик содержится большое количество микроорганизмов — до 8 млн в 1 м3, которые, попадая в атмосферный воздух, переносятся потоками воздуха на большие расстояния; среди них микроорганизмы p.p. Staphylococcus, Streptococcus, Clostridium, Bacillus, грибы рода Aspergillus и др.
Санитарно-микробиологическое исследование атмосферного воздуха в крупных городах проводится в плановом порядке и в некоторых случаях по эпидемическим показаниям. Исследование атмосферного воздуха в местах орошения земледельческих полей сточными водами методом дождевания проводится с целью обнаружения микроорганизмов p.p. Salmonella, Escherichia.
При оценке санитарного состояния закрытых помещений в зависимости от задач исследования определяется общая бактериальная обсемененность (общее микробное число), присутствие санитарно-показательных микроорганизмов (стафилококков, а- и р -гемолитических стрептококков), а также непосредственно патогенных микроорганизмов (в зависимости от характера помещений — микобактерий туберкулеза, коринебактерий дифтерии, дрожжей и мицелиальных грибов и пр.). Например, при исследовании воздуха медицинских учреждений определяется присутствие микроорганизмов, относящихся к условно-патогенной флоре (синегнойная палочка, бактерии рода Proteus и ряд других грамотрицательных палочек), вызывающих внутрибольничные инфекции.
При исследовании воздуха на предприятиях пищевого профиля, общественного питания помимо показателя общей обсемененности определяют те группы микроорганизмов, которые являются характерными возбудителями порчи данных видов продукции или могут встречаться в данном производственном помещении (дрожжи и грибы — в холодильниках, стафилококки — в цехе производства мороженого и т.п.).
На предприятиях микробиологической промышлен-ности, где в производстве используются актиномицеты, грибы, спорообразующие бациллы, дрожжеподобные грибы рода Candida и др., изучается присутствие и количественное содержание в воздухе микробов-продуцентов с целью предупреждения воздействия их на организм работающих людей (возможность заболевания и развития сенсибилизации).
При изучении присутствия микроорганизмов различных физиологических групп в воздухе используют питательные среды разного назначения (как стандартные, так и элективные или дифференциально-диагностические), в зависимости от цели исследования.
Методы отбора проб воздуха и приборы
Санитарно-микробиологическое исследование воздуха можно разделить на 4 этапа:
2) обработка, транспортировка, хранение проб, получение концентрата микроорганизмов (если необходимо);
3) бактериологический посев, культивирование микроорганизмов;
4) идентификация выделенной культуры.
Отбор проб, как и при исследовании любого объекта, является наиболее ответственным. Правильное взятие проб гарантирует точность исследования. В закрытых помещениях точки отбора проб устанавливаются из расчета на каждые 20 м2 площади — одна проба воздуха, по типу конверта: 4 точки по углам комнаты (на расстоянии 0,5 м от стен) и 5-я точка — в центре. Пробы воздуха забираются на высоте 1,6—1,8 м от пола — на уровне дыхания в жилых помещениях. Пробы необходимо отбирать днем (в период активной деятельности человека), после влажной уборки и проветривания помещения. Атмосферный воздух исследуют в жилой зоне на уровне 0,5—2 м от земли вблизи источников загрязнения, а также в зеленых зонах (парки, сады и т.д.) для оценки их влияния на микрофлору воздуха.
Следует обратить внимание на то, что при отборе проб воздуха во многих случаях происходит посев его на питательную среду.
Все методы отбора проб воздуха можно разделить на седиментационные и аспирационные.
Седиментационный — наиболее старый метод, широко распространен благодаря простоте и доступности, однако является неточным. Метод предложен Р. Кохом и заключается в способности микроорганизмов под действием силы тяжести и под влиянием движения воздуха (вместе с частицами пыли и капельками аэрозоля) оседать на поверхность питательной среды в открытые чашки Петри. Чашки устанавливаются в точках отбора на горизонтальной поверхности. При определении общей микробной обсемененности чашки с мясопептонным агаром оставляют открытыми на 5—10 мин или дольше в зависимости от степени предполагаемого бактериального загрязнения. Для выявления санитарно-показательных микробов применяют среду Гарро или Туржецкого (для обнаружения стрептококков), молочно-солевой или желточно-солевой агар (для определения стафилококков), суслоагар или среду Сабуро (для выявления дрожжей и грибов). При определении санитарно- показательных микроорганизмов чашки оставляют открытыми в течение 40—60 мин.
По окончании экспозиции все чашки закрывают, помещают в термостат на сутки для культивирования при температуре, оптимальной для развития выделяемого микроорганизма, затем (если этого требуют исследования) на 48 ч оставляют при комнатной температуре для образования пигмента пигментообразующими микроорганизмами.
Седиментационный метод имеет ряд недостатков: на поверхность среды оседают только грубодисперсные фракции аэрозоля; нередко колонии образуются не из единичной клетки, а из скопления микробов; на применяемых питательных средах вырастает только часть воздушной микрофлоры. К тому же этот метод совершенно непригоден при исследовании бактериальной загрязненности атмосферного воздуха.
Более совершенными методами являются аспирационные, основанные на принудительном осаждении микроорганизмов из воздуха на поверхность плотной питательной среды или в улавливающую жидкость (мясо-пептонный бульон, буферный раствор, изотонический раствор хлорида натрия и др.). В практике санитарной службы при аспирационном взятии проб используются аппарат Кротова, бактериоуловитель Речменского, прибор для отбора проб воздуха (ПОВ-1), пробоотборник аэрозольный бактериологический (ПАБ-1), бактериально-вирусный электропреципитатор (БВЭП-1), прибор Киктенко, приборы Андерсена, Дьяконова, МБ и др. Для исследования атмосферы могут быть использованы и мембранные фильтры № 4, через которые воздух просасывается с помощью аппарата Зейтца. Большое разнообразие приборов свидетельствует об отсутствии универсального аппарата и о большей или меньшей степени их несовершенства.
Прибор Кротова. В настоящее время этот прибор широко применяется при исследовании воздуха закрытых помещений и имеется в лабораториях СЭС.
Принцип работы аппарата Кротова (рис. 2) основан на том, что воздух, просасываемый через клиновидную щель в крышке аппарата, ударяется о поверхность питательной среды, при этом частицы пыли и аэрозоля прилипают к среде, а вместе с ними и микроорганизмы, находящиеся в воздухе. Чашку Петри с тонким слоем среды укрепляют на вращающемся столике аппарата, что обеспечивает равномерное распределение бактерий на ее поверхности. Работает аппарат от электросети. После отбора пробы с определенной экспозицией чашку вынимают, закрывают крышкой и помещают на 48 ч в термостат. Обычно отбор проб проводят со скоростью 20-25 л/мин в течение 5 мин.
Таким образом, определяется флора в 100-125 л воздуха. При обнаружении санитарно-показательных микроорганизмов объем исследуемого воздуха увеличивают до 250 л.
Приемник перед забором пробы воздуха заполняется 3—5 мл улавливающей жидкости (водой, мясопептонным бульоном, изотоническим раствором хлорида натрия).
Прибор Речменского работает по принципу пульверизатора: при прохождении воздуха через узкое отверстие воронки жидкость из приемника через капилляр в виде капелек поднимается в цилиндр. Капли жидкости еще больше дробятся, ударяясь о стеклянную лопаточку и стенки сосуда, создавая облачко из мелких капелек, на которых и адсорбируются находящиеся в воздухе микроорганизмы. Насыщенные бактериями капли жидкости стекают в приемник, а затем опять диспергируются, что обеспечивает максимальное улавливание бактерий из воздуха. При работе прибор помещают под углом 15—25°, что обеспечивает стекание улавливающей жидкости в приемник. Скорость отбора проб воздуха через аппарат Речменского — 10-20 л/мин. По окончании работы жидкость из приемника забирают стерильной пипеткой и засевают (по 0,2 мл) на поверхность плотных питательных сред. Преимуществом бактериоуловителя Речменского является высокая эффективность улавливания бактериальных аэрозолей. Недостатки прибора заключаются в трудности его изготовления, нестандартности получаемых аппаратов, их большой хрупкости и сравнительно низкой производительности.
Большим преимуществом являются серийный выпуск этого прибора (что дало возможность оснастить им лаборатории СЭС), его портативность, более высокая производительность (20—25 л/мин). Колба прибора, в которую помещается улавливающая жидкость, изготовляется из термостойкого плексигласа, капилляр из нержавеющей стали. В колбу вмонтирован пульверизатор, вызывающий диспергирование улавливающей жидкости при просасывании воздуха. Такое устройство дает возможность легко очищать и стерилизовать колбу с диспергирующим устройством простым кипячением в течение 30 мин (автоклавирование недопустимо, так как оно вызывает деформацию цилиндра).
Перед забором проб воздуха в колбу вносят 5-10 мл улавливающей жидкости (чаще всего мясопептонный бульон) и устанавливают ее под углом 10°, что обеспечивает естественное стекание жидкости после диспергирования. Воздух, проходя через колбу и пульверизатор, вызывает образование мелких капелек улавливающей жидкости, на которых оседают микроорганизмы. Прибор ПОВ-1 применяется для исследования воздуха закрытых помещений на общую микробную обсемененность, для обнаружения патогенных бактерий (например, микобактерий туберкулеза) и респираторных вирусов в воздухе больничных палат.
Пробоотборник аэрозольный бактериологический (ПАБ-1). Механизм действия ПАБ-1 основан на принципе электростатического осаждения частиц аэрозоля (а следовательно, и микроорганизмов) из воздуха при прохождении его через прибор, в котором эти частицы получают электрический заряд и осаждаются на электродах с противоположным знаком. На электродах для улавливания аэрозолей помещают в горизонтальном положении металлические поддоны с твердыми средами в чашках Петри или жидкой питательной средой (15—20 мл). Прибор переносной с большой производительностью 150-250 л/мин, т.е. за 1 ч можно отобрать 5—6 м3 воздуха. Его рекомендуют применять для исследования больших объемов воздуха при обнаружении условно-патогенных и патогенных микроорганизмов, например, при выявлении в воздухе палат больниц возбудителей внутрибольничных инфекций (Pseudomonas aeruginosa. Staph, aureus и др.), определении сальмонелл и эшерихий в атмосферном воздухе в местах дождевания при орошении земледельческих полей сточными водами.
Бактериально-вирусный электропреципитатор (БВЭП-
1). Прибор основан на аспирационно-ионизационном принципе действия. БВЭП-1 состоит из осадительной камеры, в которую вмонтированы электроды: отрицательный в виде приводящей трубки, через которую поступает воздух (и частички аэрозоля соответственно заряжаются отрицательно), и положительный, на котором оседают бактерии.
При использовании любого из перечисленных приборов получаемые результаты являются приблизительными, однако они дают более правильную оценку обсемененности воздуха в сравнении с седиментационным методом. Поскольку и отбор и санитарно-микробиологические исследования воздуха не регламентированы ГОСТ, то можно использовать любой прибор для оценки бактериальной загрязненности воздуха. Во многих случаях отбор проб совмещен с этапом посева.
Для снижения численности микроорганизмов в воздухе закрытых помещений применяют следующие средства: а) химические — обработка озоном, двуокисью азота, распыление молочной кислоты, б) механические — пропускание воздуха через специальные фильтры, в) физические — ультрафиолетовое облучение.
Определение общей численности сапрофитных бактерий
Общая бактериальная обсемененность воздуха или микробное число — это суммарное количество микроорганизмов, содержащихся в 1 м3 воздуха. Для определения общего количества бактерий в воздухе закрытых помещений забирают две пробы (объемом по 100 л каждая) на чашки Петри с МПА при помощи любого прибора (чаще всего аппарата Кротова), либо седиментационным методом, расставляя чашки с питательной средой по принципу конверта. Чашки с посевом помещают в термостат на сутки, а затем на 48 ч оставляют при комнатной температуре. Экспозиция чашек с посевами на свету дает возможность подсчитать раздельно количество пигментных колоний (желтых, белых, розовых, черных, оранжевых и др.), количество спорообразующих бацилл, грибов и актиномицетов.
Подсчитывают количество колоний на обеих чашках, вычисляют среднее арифметическое и делают перерасчет на количество микроорганизмов в 1 м3 воздуха. Бациллы образуют колонии, как правило, крупные, круглые, с неровными краями, сухие, морщинистые. Колонии грибов с пушистым налетом (Мисог и Aspergillus) и плотные -зеленоватые или сероватые (Penicillium). Актиномицеты образуют беловатые колонии, вросшие в агар. Количество каждой группы колоний (пигментных, беспигментных, плесеней, бацилл, актиномицетов) выражают в процентах по отношению к общему числу.
При определении микробного числа методом седиментации по Коху подсчитываются колонии, выросшие на МПА в чашках Петри, и расчет ведется по B.J1. Омелянскому. Если придерживаться этой методики, на чашку площадью 100 см2 за 5 мин оседает такое количество микробов, которое содержится в 10 л воздуха.
Определение стафилококков
Стафилококки являются одним из наиболее распространенных микроорганизмов в воздухе закрытых помещений, что обусловливается значительной устойчивостью их к различным факторам окружающей среды. Обнаружение патогенных стафилококков в воздухе закрытых помещений имеет санитарно-показательное значение и свидетельствует об эпидемическом неблагополучии. Отбор проб воздуха проводится с помощью аппарата Кротова в количестве 250 л на 2—3 чашки с молочно-желточно-солевым агаром (или молочно- солевым, желточно-солевым) и на чашку с кровяным агаром. Чашки инкубируют при температуре 37°С в течение 48 ч. Изучают культуральные признаки всех видов колоний (см. приложение 3), из подозрительных готовят мазки и окрашивают по Граму.
Помимо качественной характеристики отдельных колоний, подсчитывают количество выросших колоний стафилококков в 1 м3 воздуха.
Стрептококки также являются санитарно-показательными микроорганизмами воздуха, в который они попадают от больных скарлатиной, тонзиллитами, ангиной и носителей стрептококков. Отбор проб воздуха при исследовании на наличие а- и р-гемолитических стрептококков производят с помощью аппарата Кротова на чашки с кровяным агаром, средами Гарро и Туржецкого. Забирают 200—250 л воздуха, чашки с посевами выдерживают в термостате 18—24 ч и затем еще 48 ч при комнатной температуре (после предварительного просмотра и учета). Идентификацию проводят по общепринятой методике (см. приложение 3).
Определение патогенных микроорганизмов в воздухе
Ввиду малой концентрации патогенных микроорганизмов в воздухе закрытых помещений, их выделение является достаточно трудной задачей.
При расшифровке внутрибольничных инфекций определяют в воздухе присутствие стафилококков, стрептококков, синегнойной палочки, сальмонелл, протеев и др. Отбор проб воздуха производят с помощью ПАБ-1 в объеме не менее 1000 л. Посев производят на соответствующие элективные среды. Если используется жидкая среда как улавливающая жидкость, то пробирку с жидкостью помещают в термостат на сутки для подращивания (получение накопительной культуры), а затем высевают на элективную среду.
При исследовании воздуха на наличие микобактерий туберкулеза отбор проб производят с помощью прибора ПОВ-1 в объеме 250—500 л воздуха. В качестве улавливающей жидкости берут среду Школьниковой, которую затем обрабатывают 3% раствором серной кислоты (для подавления сопутствующей микрофлоры) и центрифугируют. Осадок засевают в пробирки на одну из яичных сред, чаще среду Левенштейна — Иенсена. Инкубируют при 37°С до 3 мес. Отсутствие роста в течение 3 мес дает возможность выдать отрицательный ответ. Пробирки первый раз просматривают через 3 нед, затем каждые 10 дней. Выделенную культуру идентифицируют, определяют ее вирулентность (заражением морских свинок — биопроба) и при необходимости определяют устойчивость к лекарственным препаратам.
При определении в воздухе коринебактерий дифтерии для посева воздуха используют чашки со средой Клауберга.
В последние годы определяют в атмосферном воздухе в районах дождевания земледельческих полей, при орошении их сточными водами, сальмонеллы в случае появления заболевания среди персонала станций орошения или населения. Отбор проб производят с помощью аппарата Кротова на чашки с висмут- сульфитным агаром. Исследуют не менее 200 л воздуха. Выделенная культура идентифицируется по обычной схеме определения сальмонелл.
В связи с развитием микробиологической промышленности возникла необходимость исследования воздуха с целью обнаружения грибов-продуцентов при производстве антибиотиков, ферментных препаратов, при изготовлении кормовых дрожжей и др. Для исследования воздуха на плесневые грибы рода Candida отбор проб производят с помощью аппарата Кротова в объеме от 100 до 1000 л на чашки со средой Чапека, суслоагаром (для обнаружения плесневых грибов) и с метабисульфит-натрий- агаром (МБС-агар) с добавлением антибиотиков (для обнаружения дрожжеподобных грибов рода Candida). Чашки инкубируют в термостате при температуре 26—27°С в течение 3—4 сут (для плесневых грибов) и при 35—37°С в течение 2—3 сут (для грибов — продуцентов и дрожжеподобных рода Candida). Идентификация проводится с учетом особенностей плодоносящих гиф и характера мицелия. Считают, что концентрация дрожжеподобных грибов в количестве 500—600 клеток в 1 м3 воздуха рабочего помещения является предельной, превышение ее ведет к развитию аллергических реакций у рабочих.
Санитарно-микробиологическое исследование воздуха. Микрофлора воздуха.
Основная задача санитарно-микробиологического исследования воздуха — гигиеническая и эпидемиологическая оценка воздушной среды, а также разработка комплекса мероприятий, направленных на профилактику аэрогенной передачи возбудителей инфекционных болезней. При оценке санитарного состояния закрытых помещений в зависимости от задач исследования определяют ОМЧ, наличие СПМ (стафилококков, а- и бета-гемолитических стрептококков, являющихся показателями контаминации микрофлорой носоглотки человека). В связи с развитием биотехнологической промышленности, использующей различные микроорганизмы-продуценты БАВ, существенно возрос риск выброса в атмосферу больших концентраций микробов, в том числе с изменённым генотипом. При этом, технология производства некоторых веществ прямо включает периодический выпуск микроорганизмов. Указанное придаёт проблеме контроля за микрофлорой атмосферного воздуха и обеззараживания выбросов биотехнологических предприятий особую актуальность.
Микрофлора воздуха
Микробная загрязнённость воздуха имеет непостоянный и локальный характер, то есть микрофлора воздуха зависит от места и времени отбора проб. Летом обсеменённость воздуха в несколько раз выше, чем зимой. Особенно насыщен атмосферный воздух микроорганизмами над крупными городами. При рассмотрении качественного состава микрофлоры воздуха следует различать микрофлору атмосферного воздуха и воздуха жилых помещений.
Микрофлора атмосферного воздуха. В атмосферном воздухе СПМ (стафилококки и стрептококки) обнаруживают лишь в 3,7% проб, взятых в местах большого скопления людей. Среди микроорганизмов доминируют виды, обитающие в почве. В атмосферном воздухе в основном встречают три группы микроорганизмов.
• Пигментообразующие кокки в солнечные дни составляют до 70-80% всей флоры (пигмент защищает бактерии от инсоляции).
• Почвенные споровые и гнилостные микроорганизмы. Их содержание резко увеличивается в сухую и ветреную погоду.
• Плесневые грибы и дрожжи. Их содержание увеличивается при повышении влажности воздуха.
В отличие от воздуха закрытых помещений, в атмосферном воздухе постоянно происходят процессы самоочищения. Этот процесс происходит благодаря осадкам, инсоляции, температурным воздействиям и другим факторам. В свою очередь атмосферный воздух сам по себе — фактор очищения воздуха жилых помещений.
Микрофлора воздуха закрытых помещений более однообразна и относительно стабильна. Среди микроорганизмов доминируют обитатели носоглотки человека, в том числе патогенные виды, попадающие в воздух при кашле, чихании или разговоре. Основной источник загрязнения воздуха патогенными видами — бактерионосители. Уровень микробного загрязнения зависит главным образом от плотности заселения, активности движения людей, санитарного состояния помещения, в том числе пылевой загрязнённости, вентиляции, частоты проветривания, способа уборки, степени освещённости и других условий. Так, регулярные проветривания и влажная уборка помещений снижает обсеменённость воздуха в 30 раз (по сравнению с контрольными помещениями). Самоочищения воздуха закрытых помещений не происходит.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

