Источник помогающий от вич
Обновлено: 01.05.2024
Есть немало лекарств, которые применяются для борьбы с ВИЧ. Но такого, чтобы позволяло излечиться от вируса иммунодефицита человека, пока, увы, не изобретено.
Чем сегодня лечат ВИЧ? Какие результаты дает лечение? Об этом мы побеседовали с Наталией Сизовой, кандидатом медицинских наук, заведующей поликлиническим инфекционным отделением городского Центра по профилактике и борьбе со СПИДом и инфекционными заболеваниями.
– Наталия Владимировна, многие годы ученые ищут препарат, который полностью излечит от ВИЧ, от СПИДа. Почему до сих пор не удалось придумать такое лекарство?
– Это связано с тем, что вирус встраивается в геном человеческой клетки, и выбить эту информацию о нем, записанную в геноме клетки, чрезвычайно сложно. Поэтому до сих пор такого радикального средства, которое бы полностью убрало вирус, к сожалению, нет.
– Чудо-вакцины нет, но, тем не менее, ВИЧ-положительные люди могут вести нормальный образ жизни. Благодаря каким лекарствам, какому лечению?
У нас в Санкт-Петербурге есть пациенты, диагноз которым поставили в 1987 году. Столько лет эти люди прожили с ВИЧ-инфекцией, и надо учесть, что в самом начале не было антриретровирусных препаратов. А когда они появились, то были более тяжелые, более токсичные, чем сегодня… Тем не менее, люди живут. На моей памяти много пациентов, которые вырастили своих детей, стали бабушками, дедушками.
– Чтобы так долго жить, какие правила надо соблюдать?
– Есть люди, которым поставили диагноз, к примеру, в 2000 году, а они после этого не наблюдались у врачей. И сегодня они обращаются к нам уже в очень тяжелом состоянии, некоторым мы даже не успеваем помочь. Чудес не бывает. Самое главное для человека, которому поставлен диагноз ВИЧ — обязательно наблюдаться и своевременно лечиться, принимать антиретровирусную терапию. Сейчас большинство медиков склоняются к тому, что терапию надо начинать как можно раньше. Потому что мы знаем и на собственном опыте, и по зарубежной научной информации, что чем дольше человек ходит с иммунодефицитом (хотя он себя, может, неплохо чувствует), тем быстрее у него развивается ВИЧ-инфекция, и не исключено, что у него впоследствии появятся другие болячки, например, онкология…
– Очень важно, чтобы человек обследовался на ВИЧ, особенно если у него есть какие-то к тому показания: клинические или эпидемиологические. Например, если у него были не защищенные половые контакты. Иллюзия, что вирус поражает группу риска.
К нам всё чаще становятся на учет социально адаптированные люди, вполне благополучные. Потому что сейчас начинает превалировать половой путь передачи ВИЧ-инфекции.
Когда мы принимаем решение о начале антиретровирусной терапии, мы смотрим прежде всего на самочувствие пациента. Если человек начинает себя плохо чувствовать, у него есть какие-то клинические проявления (даже если анализы хорошие), то мы ему предлагаем начать терапию. Другой вариант: пациент чувствует себя хорошо. Главными маркерами прогрессирования заболевания являются два анализа: анализ на иммунитет (начинаем предлагать терапию, когда CD-лимфоциты в клетках снижаются ниже 350; раньше планка была 200) и такой показатель, как вирусная нагрузка (это количество вирусов в миллилитре крови). Чем выше вирусная нагрузка, тем быстрее заболевание прогрессирует. И чем выше вирусная нагрузка, тем более человек заразен. Мы предлагаем пациенту начать терапию, если вирусная нагрузка превышает 100 тысяч. Это помогает остановить быстрое прогрессирование заболевания и снизить заразность человека. Как бы там ни было, если у человека есть постоянный половой партнер и высокая вирусная нагрузка, ему обязательно нужно начинать терапию. Это не только сохранит здоровье ВИЧ-положительному, но и убережет от ВИЧ его партнера.
– Говорят, что у антиретровирусных препаратов немало побочных эффектов. Насколько они опасны и в каких случаях?
– Конечно, антиретровирусные препараты — не карамельки. Побочные эффекты можно разделить на ранние и поздние. Ранние возникают в течение первых шести недель приема препаратов. Эти побочные эффекты, как правило, тоже делятся на два вида: те, которые надо переждать, и они пройдут (например, тошнота — первый месяц тошнит, потом проходит; бывает аллергическая сыпь, которая тоже со временем проходит), и тяжелые — когда препарат не подходит человеку. Причем, зачастую побочные эффекты генетически запрограммированы. Например, у некоторых пациентов есть реакция гиперчувствительности на абакавир… Это ранние побочные эффекты. Здесь правило такое: ни в коем случае в начале терапии не отрываться от доктора, никуда не уезжать, чтобы доктор держал, что называется, руку на пульсе. Он сразу определит, не угрожают ли эти побочные эффекты жизни. Тогда можно будет успокоить больного, переждать эти эффекты.
Если же побочные эффекты жизнеугрожающие (например, у пациента резко снижается гемоглобин в крови), то тогда надо менять препараты.
Что касается поздних побочных действий… Здесь тоже самое главное — хорошо наблюдаться. Человек должен вовремя сдавать анализы, инструментально обследоваться. Доктор увидит и предупредит эти побочные действия, поменяет схему приема препаратов.
В любом случае, когда мне люди говорят, что лекарства вредны… Понимаете, мы из двух зол выбираем меньшее. Ничего страшнее вируса нет.
– Наталия Владимировна, а если не принимать терапию, пустить болезнь, как говорится, на самотек…
К сожалению, наши люди… Они полечились немного, у них стало все хорошо (то есть им кажется, что все хорошо) — и они бросают терапию. А в результате все моментально скатывается на прежние позиции. Поэтому мы постоянно объясняет нашим пациентам: надо лечиться, от этого никуда не денешься. И только тогда вы будете жить долго, активно, практически так, как живут здоровые люди.
Оригинал статьи на сайте "Курьер-Медиа"
Вы имеете возможность дать независимую оценку качества оказания медицинских услуг в нашем учреждении, заполнив АНКЕТУ на сайте Министерства здравоохранения Российской Федерации.
В середине 1980-х ученые идентифицировали вирус иммунодефицита человека и сразу же стали искать лекарство. История антиретровирусной терапии началась в 1987 году, когда для лечения ВИЧ-инфекции стали использовать препарат зидовудин. Но его эффективность была невысокой, а побочные эффекты слишком сильными. Первая высокоэффективная терапия появилась только через десять лет — в 1996 году. Эта комбинация из нескольких лекарств блокирует размножение попавшего в организм вируса сразу на нескольких этапах его цикла. С тех пор ВИЧ-инфекция — не смертельное, а хроническое заболевание, которое можно контролировать при должном лечении.
Антиретровирусные препараты (АРВ) подавляют размножение ВИЧ, но неспособны полностью удалить вирус из организма, именно поэтому их нужно принимать постоянно в течение всей жизни. Как только концентрация препарата в крови падает ниже порогового значения, вирус снова начинает размножаться. Это особенно опасно, ведь если вирус размножается в присутствии небольшого количества лекарства, то он вырабатывает устойчивость к этому препарату.
Пить таблетки на протяжении всей жизни с точностью до минут — не самая простая задача. Этому мешают и банальная забывчивость, и разные случайные обстоятельства. А чем чаще человек нарушает время приема терапии, тем выше риск развития у вируса устойчивости. Именно поэтому врачи стараются назначать схемы с приемом лекарств один раз в день и с минимальным числом таблеток — чем реже и меньше нужно принимать лекарств, тем проще соблюдать режим. Правильное соблюдение режима приема терапии называют высокой приверженностью лечению.
Сейчас лучшими схемами считаются те, при которых пациенту нужно принимать одну таблетку один раз в день, да еще и независимо от приема пищи. Но настоящим прорывом в АРВТ станет разработка схем, при которых лекарство достаточно будет принимать всего один или несколько раз в месяц, — пролонгированных схем терапии. Хотя в настоящее время неизвестно, как поведут себя пролонгированные режимы в рутинной практике. Будет ли к ним сохраняться высокая приверженность — как это показывают исследования?
по теме

Общество
Грудное молоко VS смеси при ВИЧ: что говорят эксперты в 2020 году?
Основной недостаток таких таблеток — срок их действия ограничено временем нахождения таблетки в кишечнике и не превышает 12—24 часов. В случае же диареи таблетка может покинуть организм гораздо быстрее, а значит, уменьшится концентрация лекарства в крови, что может быть опасно. Для антиретровирусных препаратов создание таблеток или капсул с замедленным высвобождением лекарственного вещества не очень перспективно — современные схемы уже позволяют принимать терапию один раз в день. То есть удобство применения терапии такие таблетки не повысят.
Если нужно добиться продления эффекта препарата на дни и недели, а лекарство всасываться через кожу упорно не хочет, приходится прибегать к парентеральным пролонгированным формам. Можно зашить под кожу специальную стерильную таблетку, которая будет медленно растворяться и выделять лекарственное вещество: на коже делается небольшой разрез, в него вводят таблетку и зашивают рану.
Помимо таблеток, под кожу можно вводить специальные полимерные импланты, содержащие нужное лекарство. Преимущество имплантов — они могут выделять лекарственное вещество очень долго, до нескольких лет. Чаще всего такие импланты используют для гормональной контрацепции. Так как гормоны действуют в очень маленьких дозах, даже в небольшой по размерам имплант можно сразу поместить запас препарата на несколько лет. Например, противозачаточный препарат Имплантон, который вводится под кожу, продолжает действовать три года. Если действие препарата нужно прекратить — достаточно просто извлечь имплант.
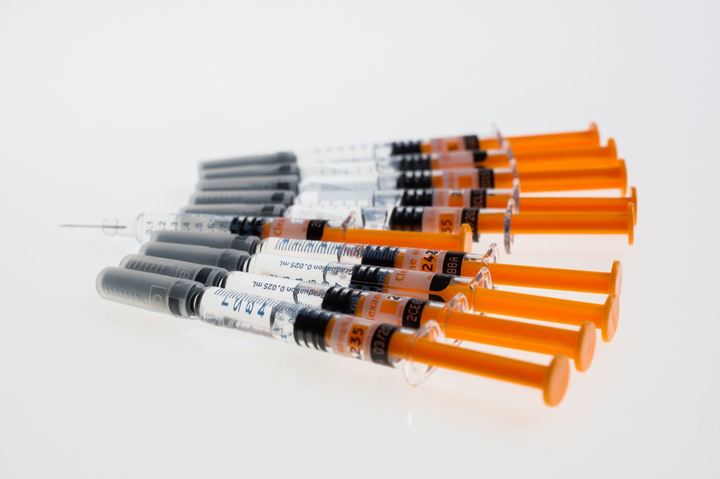
Более простой вариант — ввести в мышцу взвесь маленьких крупинок лекарства в подходящем растворителе. Выглядит это как обычный укол, при этом крупинки лекарства задерживаются в мышце, медленно растворяются и попадают в кровь. Такие способы введения лекарства особенно удобны в случаях, когда пациент может часто пропускать прием препарата, или забывать, принял ли он лекарство. Например, в случае лечения психических заболеваний. Но есть и недостатки: вводить такой препарат должен медицинский работник, а в случае непереносимости или выраженных побочных эффектов лекарство очень трудно быстро удалить из организма.
Что уже доступно на рынке?
Многие фармацевтические компании проводят исследования пролонгированных АРВ-препаратов, но разработка одного такого препарата сама по себе очень большой пользы не принесет — ведь для лечения ВИЧ-инфекции необходимо сочетание нескольких препаратов, то есть нужна комбинированная пролонгированная схема.
Такую схему, разработанную ViiV Healthcare совместно с Janssen, одобрили в марте 2020 года в Канаде — первый пролонгированный комбинированный АРВ-препарат Cabenuva. Схема показала высокую эффективность и безопасность в клинических исследованиях LATTE-2, FLAIR, ATLAS с участием более тысячи пациентов. В состав Cabenuva входят каботегравир и рилпивирин, то есть это двухкомпонентная схема. Препарат вводят один раз в месяц внутримышечно.
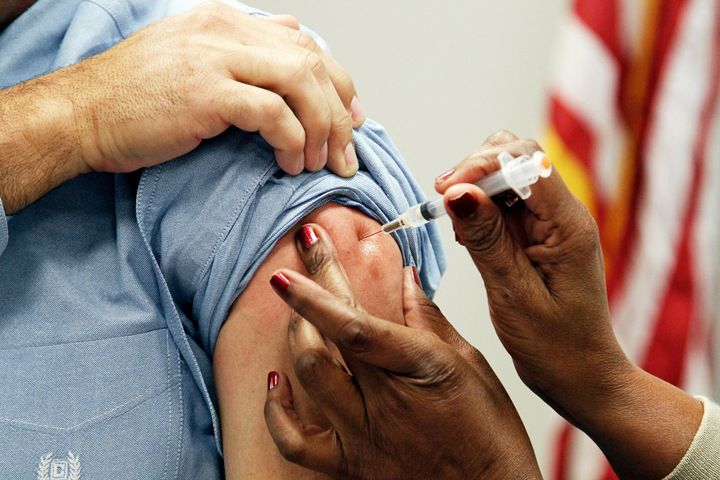
Перед началом применения Cabenuva пациент не менее месяца принимает каботегравир в таблетках (называется Vocabria) в комбинации с Эдюрантом — таблетками рилпивирина. Это необходимо, чтобы проверить переносимость такой схемы у конкретного пациента и оценить побочные эффекты. Если схема переносится хорошо, пациенту вводят первую нагрузочную дозу Cabenuva — 3 миллилитра суспензии, содержащей 600 миллиграммов каботегравира, и 3 миллилитра суспензии, содержащей 900 миллиграммов рилпивирина. Суспензии вводятся в разные участки ягодичной мышцы, то есть делают два укола. После этого поддерживающие дозы вводят ежемесячно: 2 мл (400 мг) каботегравира и 2 мл (600 мг) рилпивирина. Если по каким-то причинам введение очередной ежемесячной поддерживающей дозы невозможно, пациент до момента следующей инъекции может принимать пероральную схему (Vocabria + Эдюрант). Пролонгированная форма каботегравира также имеет большие перспективы для использования в качестве доконтактной профилактики ВИЧ-инфекции.
Еще один препарат, который уже применяется в клинической практике, — ибализумаб (Трогарзо) — можно назвать пролонгированным с несколькими оговорками. По химической природе ибализумаб — моноклональное антитело, то есть близок к человеческим иммуноглобулинам. Ибализумаб связывается с некоторыми белками на поверхности вируса и мешает проникновению ВИЧ в клетки. Препарат вводят внутривенно один раз в две недели и часто сочетают с другими АРВ-препаратами. Такая схема — не самый удобный вариант, поэтому сейчас ибализумаб используется только для лечения ВИЧ с множественной лекарственной устойчивостью, когда другие схемы оказываются неэффективными. Поэтому ибализумаб правильнее будет отнести к нишевым препаратам.
К сожалению, на этом и заканчивается не очень длинный перечень пролонгированных АРВ-препаратов, которые уже применяются на практике. Дальше пойдет речь о препаратах, находящихся на разных стадиях исследований.
Что сейчас находится в разработке?
PRO 140
С точки зрения места в клинической практике на ибализумаб похоже еще одно моноклональное антитело, находящееся в стадии клинических исследований, — PRO 140. Этот препарат также можно будет использовать для лечения ВИЧ-инфекции, если у пациента не работают другие схемы. А по механизму действия PRO 140 похож на уже существующий на рынке препарат маравирок (Целзентри). Он связывается с CCR-5 рецепторами на поверхности клеток-мишеней и мешает проникновению вируса в клетку. Строение активного центра молекулы PRO 140 отличается от маравирока, поэтому он активен даже в тех случаях, когда вирус выработал устойчивость к маравироку. Как и маравирок, PRO 140 активен только против CCR-5-тропных подтипов ВИЧ, то есть подойдет не всем пациентам. Препарат вводят внутривенно, один раз в неделю.
Нейтрализующие антитела
На разных стадиях клинических исследований находятся несколько перспективных антител, которые связываются с вирусным белком gp120 и нейтрализуют вирус: VRC01, 3BNC117 и 10-1074. Предполагается, что эти препараты достаточно будет вводить раз в месяц или даже реже и их можно будет применять совместно с другими пролонгированными АРВ-препаратами.
Албувиртид
Аналог уже применяющегося на практике энфувиртида (Фузеон). Этот препарат связывается с вирусным белком gp-41 и мешает проникновению вируса в клетку. Основное отличие в том, что Фузеон вводят подкожно два раза в сутки, что очень неудобно, а албувиртид — только один раз в 2—4 недели. Препарат должен применяться совместно с другими АРВ-лекарствами.
С самого зарождения эпидемии ВИЧ медицинское научное сообщество было занято поиском эффективного способа предотвращения передачи ВИЧ-инфекции.
Кроме использования средств барьерной контрацепции (презервативов) существуют и иные способы обезопасить себя от ВИЧ-инфекции. Самый главный из них — PrEP, или так называемая доконтактная профилактика (ДКП).
Препараты PrEP — это те же вещества, которыми лечат ВИЧ, но принимаются они по усеченной, неполной схеме. Механизм действия ДКП прост: если лекарство успело попасть в организм заранее, то при попадании в него вируса оно способно убить ВИЧ еще до того, как тот успеет закрепиться в нем.
Защита, которую предлагает PrEP, достаточно надежна и приближается к 100 %, если принимать таблетки правильно.
Что это за таблетки?
Сразу стоит дать названия, существуют две схемы ДКП, которые рекомендованы для использования:
(в одной таблетке — тогда они называются Трувада, либо по отдельности);
Почему именно эти препараты? Для того чтобы ответить на вопрос, можно или нет использовать конкретное лекарство для ДКП, надо провести клиническое исследование. Без клинических исследований подтвердить такой тезис невозможно. Поэтому придерживаться стоит тех схем, которые уже были испытаны и утверждены в качестве PrEP.
Именно поэтому, когда мы говорим о доконтактной профилактике, как правило, речь идет о двух препаратах, как это уже было сказано: тенофовире и эмтрицитабине. Если вы обратитесь в аптеку, то их комбинация в одной таблетке будет стоить порядка 14 000 рублей. Однако допустимо применение и других апробированных для ДКП лекарств. Например, тенофовира и ламивудина. Эта схема также одобрена Всемирной организацией здравоохранения (ВОЗ), они, купленные по отдельности, будут стоить не 14 000, а порядка 1000 рублей.
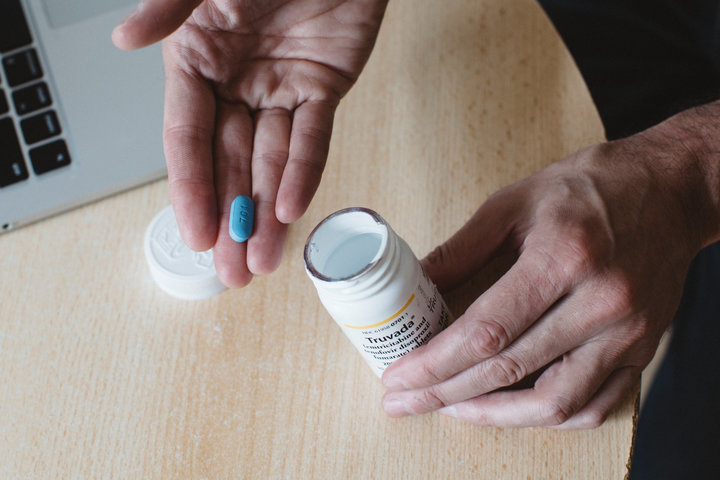
Какой схемой воспользоваться — решать вам. В целом ДКП сейчас доступна в разных формах для пациентов с разным достатком, и самые дешевые ее схемы могут стоить не более двух тысяч рублей в месяц.
А можно подробнее про механизм действия?
Можно. Итак, доконтактная профилактика заключается в приеме двух препаратов, относящихся к классу ингибиторов обратной транскриптазы, ВИЧ-отрицательными людьми. То есть людьми, в чьем организме вируса пока еще нет.
Что делают эти препараты? На картинке ниже вы можете увидеть жизненный цикл вируса иммунодефицита, как он прикрепляется к клетке и вбрасывает внутрь нее свой генетический материал.
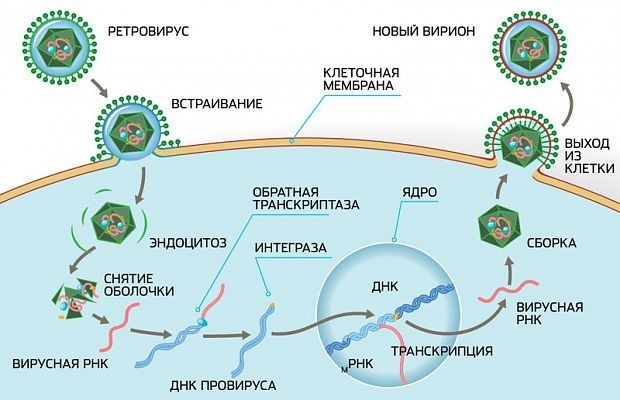
Этот генетический материал под воздействием особого фермента — обратной транскриптазы — запускает процесс репликации новых вирусов.
Два исследования — iPrEx и Partners (оба они проводились в США и Западной Европе) — продемонстрировали крайне высокую эффективность защиты PrEP, в отдельных случаях приближающуюся к 99 %.
В обоих лекарство тенофовир + эмтрицитабин, известное как Трувада, тестировалось на людях, относящихся к ключевым, то есть наиболее уязвимым для эпидемии, группам, — на мужчинах, практикующих секс с мужчинами, и трансгендерных женщинах (mtf). И именно у них этот метод профилактики показал свою наибольшую эффективность.
(Противо)показания к началу ДКП
В настоящее время в России ДКП одобрена Министерством здравоохранения в качестве дополнительного метода профилактики ВИЧ-инфекции и даже попала в клинические рекомендации, так что врач, пусть пока и не имеет возможности выдавать ее бесплатно, как выдаются препараты АРВТ, все же может легально рассказать своим пациентам, где можно приобрести необходимые таблетки, что для этого нужно сделать и как их принимать.
Главным противопоказанием к началу ДКП, конечно, является наличие у пациента ВИЧ-инфекции или симптомов, указывающих на так называемую острую фазу ВИЧ, которая имеет место примерно через две недели после проникновения вируса в организм.
Побочные эффекты
Безопасна ли ДКП? Да. Она безопасна. Оба режима одинаково эффективны. Всего в настоящий момент мы знаем лишь о семи случаях получения вируса на PrEP. А учитывая, что во всем мире примерно полмиллиона человек принимают доконтактную профилактику, семь случаев — это весьма немного.
Два из них были связаны с низкой приверженностью (пропуском приема профилактического препарата), два — с наличием резистентного к эмтрицитабину штамма ВИЧ. Два человека были инфицированы еще до начала доконтактной профилактики. Буквально недавно мировые СМИ сообщили о еще одном случае инфицирования ВИЧ на доконтактной профилактике. На этот раз вирус получил активист в Австралии, который более пяти лет принимал PrEP именно в разовом режиме.
Сейчас идет расследование этого инцидента, и мы пока не знаем точно, в чем была его причина. Что же касается побочных эффектов, они встречаются крайне редко и при должном внимании врача легко контролируются.
Долгосрочные эффекты, например деминерализация костной ткани, появляются не сразу, и, по большому счету, слишком бояться их не стоит. Деминерализация костной ткани, связанная с тенофовиром, проходит в течение, как правило, месяца после остановки приема и не является необратимой. То же самое касается снижения функции почек.
Когда он появится на наших прилавках — сказать сложно. Но в любом случае стоит помнить: даже если это лекарство и появится в России, ДКП — это не витамины, которые можно принимать самостоятельно. Любые побочные эффекты должен отслеживать врач, равно как и назначать сам препарат. Кому стоит обратиться к ДКП, а кому повременить? В идеале такое решение должен принимать не сам пациент в режиме самолечения, а специалист, обладающий достаточной квалификацией.
Как правильно приостановить прием ДКП?
Если вы мужчина или трансгендерная женщина и хотите безопасно прекратить прием доконтактной профилактики, вам необходимо принимать ДКП как минимум еще два дня после последнего рискованного полового контакта. И только через два дня в случае отсутствия в течение этого времени опасных контактов перестать пить таблетки.
Для женщин на ДКП необходимо как минимум семь дней приема ДКП после последнего рискованного контакта. Это связано с особенностями женского организма и того, как ведут себя препараты PrEP в нем.
Чтобы возобновить прием доконтактной профилактики, вы должны быть уверены в отсутствии рисков в период без ДКП. Если риски все же были, то необходимо сделать тест на ВИЧ. Но помните про период серонегативного окна — 4-6 недель с момента последнего риска.
Чтобы начать пить доконтактную профилактику на постоянной основе, необходимо непрерывно принимать ДКП на протяжении семи дней до первого рискованного контакта. Либо (только для мужчин) можно принять двойную дозировку, а затем каждые 24 часа принимать по одной дозе ДКП.
Постконтактная профилактика ВИЧ (ПКП)
Если опасный контакт все-таки случился, а вы не успели обезопасить себя ни с помощью презерватива, ни с помощью препаратов ДКП, и со времени контакта прошло не более 72 часов, избежать инфицирования вам может помочь так называемая постконтактная профилактика.
Заключается она в том, что в указанный срок вам необходимо начать прием препаратов, которыми обычно лечат ВИЧ-инфекцию, но, в отличие от PrEP, тут принимать лекарства придется в полной дозировке, такой, какую принимают люди, у которых уже диагностирована инфекция.
Многочисленными исследованиями доказано: если начать такой прием вовремя, есть большой шанс, что вирус не успеет закрепиться в организме и заболевания удастся избежать. Идеально начать прием лекарств в первые два часа или хотя бы в первые сутки после контакта. Чем позже будет начат такой прием, тем меньше вероятность, что терапия сработает.
Курс профилактики длится 28 дней, и по завершении его необходимо сделать тест, чтобы удостовериться в его эффективности.
Важно! Лекарства, которые вам придется принимать, по факту продаются БЕЗ РЕЦЕПТА, но найти их можно не в каждой аптеке. Поэтому времени на раздумья у вас немного. Возможно, на то, чтобы собрать необходимую комбинацию таблеток, у вас может уйти более суток, так что поиск стоит начать прямо сейчас.
Всего вам придется купить три препарата и принимать нужно будет все три. По отдельности они не работают.

Почему ВИЧ сложно лечить
Вирус иммунодефицита человека (ВИЧ) вызывает хроническое инфекционное заболевание, прогрессирующее без лечения. Это один из уникальных вирусов, которые поражают клетки иммунной системы — так называемые CD4+ Т-лимфоциты, функция которых состоит в распознавании и уничтожении чужеродных для организма агентов.
Без лечения ВИЧ-инфекция медленно прогрессирует, истощая иммунную систему организма. Через 5–10 лет после инфицирования начинается стадия вторичных проявлений, когда у ВИЧ-положительного развиваются другие сопутствующие заболевания.
Профилактика: значимое снижение рисков инфицирования ВИЧ
Доконтактная профилактика (ДКП или PrEP) — это прием неполной схемы тех же препаратов, которые принимают люди, живущие с ВИЧ: сочетания тенофовир + эмтрицитабин или тенофовир + ламивудин.
Если препараты ДКП успели попасть в организм заранее, то при проникновении в него вируса вещества ДКП убивают ВИЧ еще до того, как тот успеет закрепиться в теле человека. Препараты нужно принимать ежедневно в одно и то же время.
Защита, которую обеспечивает PrEP при правильном приеме таблеток, — почти 100%. Требуется консультация и контроль врача.
В экстренных случаях, когда есть риск заболевания после незащищенного контакта с инфицированным, используют постконтактное лечение (ПКП, PEP). Это месячный курс терапии. При быстром начале лечения в течение первых 24–72 часов есть высокие шансы избежать инфицирования. Но эти шансы никогда не равны 100%.
Лечение ВИЧ: антиретровирусная терапия
Основной способ взять ВИЧ-инфекцию под контроль — антиретровирусная терапия. Она включает в себя препараты, останавливающие жизненный цикл ВИЧ на разных этапах.
Антиретровирусная терапия меняет качество жизни пациентов с ВИЧ:
- останавливает размножение вируса;
- позволяет иммунной системе самой восстановиться;
- предотвращает передачу ВИЧ половому партнеру;
- позволяет женщине родить детей без вируса.
Ученые доказали, что ВИЧ-положительный человек, принимающий эффективную терапию, не может передать вирус при незащищенных сексуальных контактах.
Прорыв 2021 года в лечении ВИЧ — регистрация первых инъекционных форм антиретровирусной терапии на рынках Канады, США и Европы. В ближайший год эта форма должна появиться в России. Исследования доказали эффективность терапии при однократных инъекциях каждые 1–2 месяца (вместо ежедневного приема терапии). Следующее поколение лечения — инъекционный препарат с введением один раз в полгода. Потенциально эти же лекарства можно будет использовать для снижения риска инфицирования с той же продолжительностью действия.
Исследования новых методов лечения ВИЧ: генетические ножницы
Известные случаи излечения от ВИЧ связаны с пересадкой костного мозга от доноров с мутацией генов CCR5, делающих носителей этой мутации неуязвимыми для ВИЧ. В настоящее время ученые отслеживают состояние еще 38 пациентов с ВИЧ, которым был трансплантирован устойчивый к вирусу материал.
Этот метод не может быть масштабирован по двум причинам: ущерб для здоровья от трансплантации несоизмеримо выше, чем от ВИЧ-инфекции (излечившиеся пациенты проходили процедуру не в связи с ВИЧ, а из-за онкологических заболеваний), а сама мутация не может служить надежной защитой перед быстро мутирующим вирусом, новые штаммы которого могут стать невосприимчивы к этой естественной защите.
Тем не менее случаи излечения именно этим путем создали значительное поле для исследований: на их основе появились как возмутивший общественность эксперимент на генетически модифицированных детях, итог которого общественности неизвестен, так и испытание метода редактирования гена CCR5 в организме живого человека, которое завершатся в Санкт-Петербурге в 2022 году.
Разработки вакцин от ВИЧ
Эффективной вакцины против ВИЧ не существует — пока.
За все время в клинических исследованиях испытывали более 40 вакцин. Максимальный эффект в сокращении новых случаев ВИЧ — только 25%. Созданию вакцины препятствует особенность жизненного цикла ВИЧ и его высокая изменчивость — особенно его внешней оболочки. Это позволяет вирусу быстро обходить искусственный иммунитет.
Продолжается исследование бельгийской вакцины Mosaico. В 2022 году планируется публикация исследования перспективной кадидатной вакцины HIVconsvX от Оксфордского университета.

Диагностика: шесть видов анализов
Рынок средств диагностики ВИЧ активно растет. Согласно исследованию американского агентства GMI, к 2024 году объем мирового рынка средств диагностики ВИЧ превысит $5 млрд.
Диагностика включает скрининг и подтверждающие тесты для проверки на заболеваемость ВИЧ-1, 2 и группы О. Эти тесты имеют основное применение для скрининга и дифференциации различных групп и подтипов вируса иммунодефицита человека. Благодаря технологическому развитию стали доступны экспресс-тесты на уровень клеток CD4, нуклеиновые кислоты NAT, антиген p24 и диагностика для новорожденных EID.
Антитела к ВИЧ появляются после начала активного размножения вируса. Они обычно обнаруживаются в сыворотке крови через 6–12 недель после инфицирования. Тесты на антитела ВИЧ высоко надежны при относительно низкой стоимости.
При определении антигена p24 в крови ВИЧ-инфекция может быть выявлена раньше, чем традиционными тестами для определения антител. Тесты на антиген имеют низкую чувствительность. Они не дают ложноположительных результатов, но возможны ложноотрицательные. То есть отрицательный результат не исключает инфицирование, а положительный — подтверждают с помощью тестов на антитела. Тест на антиген p24 всегда применяется вместе с тестами на антитела.
- Тесты на ВИЧ четвертого поколения
В тестах четвертого поколения объединили разные технологии, чтобы обнаружить как антиген p24, так и антитела. Тесты четвертого поколения менее дорогие, чем NAT. Широко распространены в России.
- Тесты на нуклеиновые кислоты (NAT\NAAT)
Определяет наличие и количество ВИЧ в миллилитре крови и других биологических жидкостях. Имеет высокую точность и стоимость, для скрининга не применяется. Используется для определения вирусной нагрузки у ВИЧ-положительных пациентов.
Этот тест не выявляет ВИЧ, а служит для измерения уровня клеток CD4 или Т-лимфоцитов — показатели, важные для для качества жизни пациентов с ВИЧ. Это белые клетки крови, предназначенные для распознавания болезнетворных организмов в нашем теле, которые должны уничтожаться иммунной системой. Снижение уровня CD4-клеток ниже 200 означает очень серьезные нарушения иммунной системы.
Эпидемия ВИЧ началась раньше пандемии коронавируса. Согласно UNAIDS, в 2020 году во всем мире насчитывалось не менее 37,6 млн пациентов с ВИЧ. Но главный тренд — за последние десятилетия инновации существенно изменили качество и продолжительность их жизни, а доступность диагностики и лечения снизили смертность на 61% по сравнению с максимумом в 2004 году. Также с 1996 года более чем на 30 лет выросла общая продолжительность жизни человека с ВИЧ при условии раннего обнаружения и использования терапии.
Подробнее о подходах к лечению и о том, как инновации продолжают улучшать качество жизни с ВИЧ, расскажут ученые-медики из разных стран на онлайн-конференции PROHIV 2021, которая пройдет 20–21 сентября.
Читайте также:

