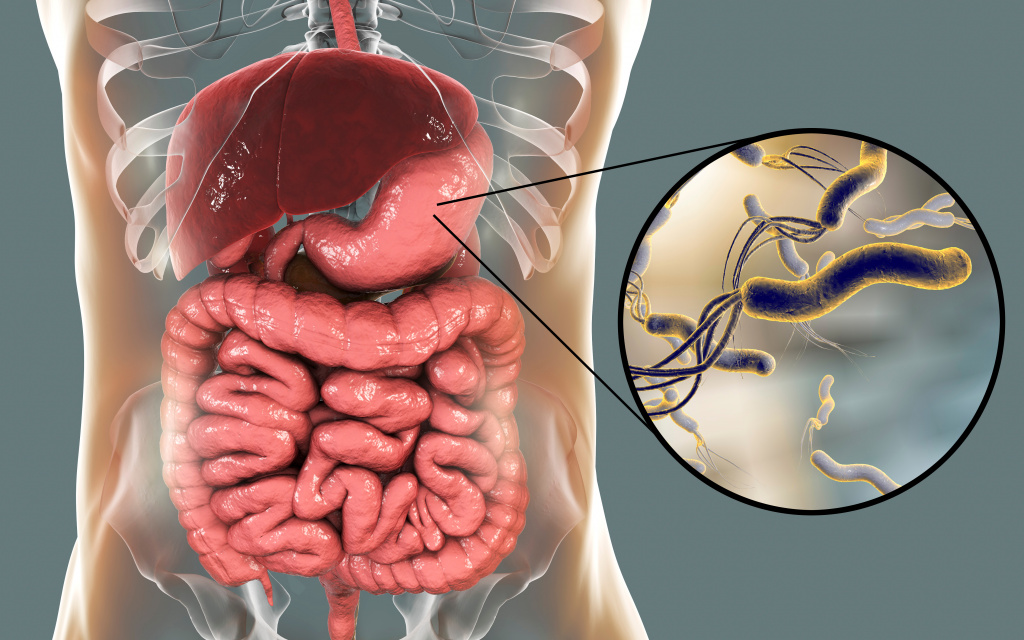
Из-за хеликобактер могут болеть суставы
Обновлено: 19.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Гельминтоз (глистная инвазия): причины появления, симптомы, диагностика и способы лечения.
Определение
Гельминтозы - болезни человека, животных и растений, вызываемые паразитическими червями (гельминтами).
Причины появления гельминтозов
В настоящее время в России встречается более 70 видов из известных 250 гельминтов, паразитирующих в организме человека. Наиболее распространены круглые черви (аскариды, острицы, трихинеллы, власоглав), ленточные черви (свиной, бычий и карликовый цепни, широкий лентец, эхинококки), сосальщики (печеночная и кошачья двуустки).
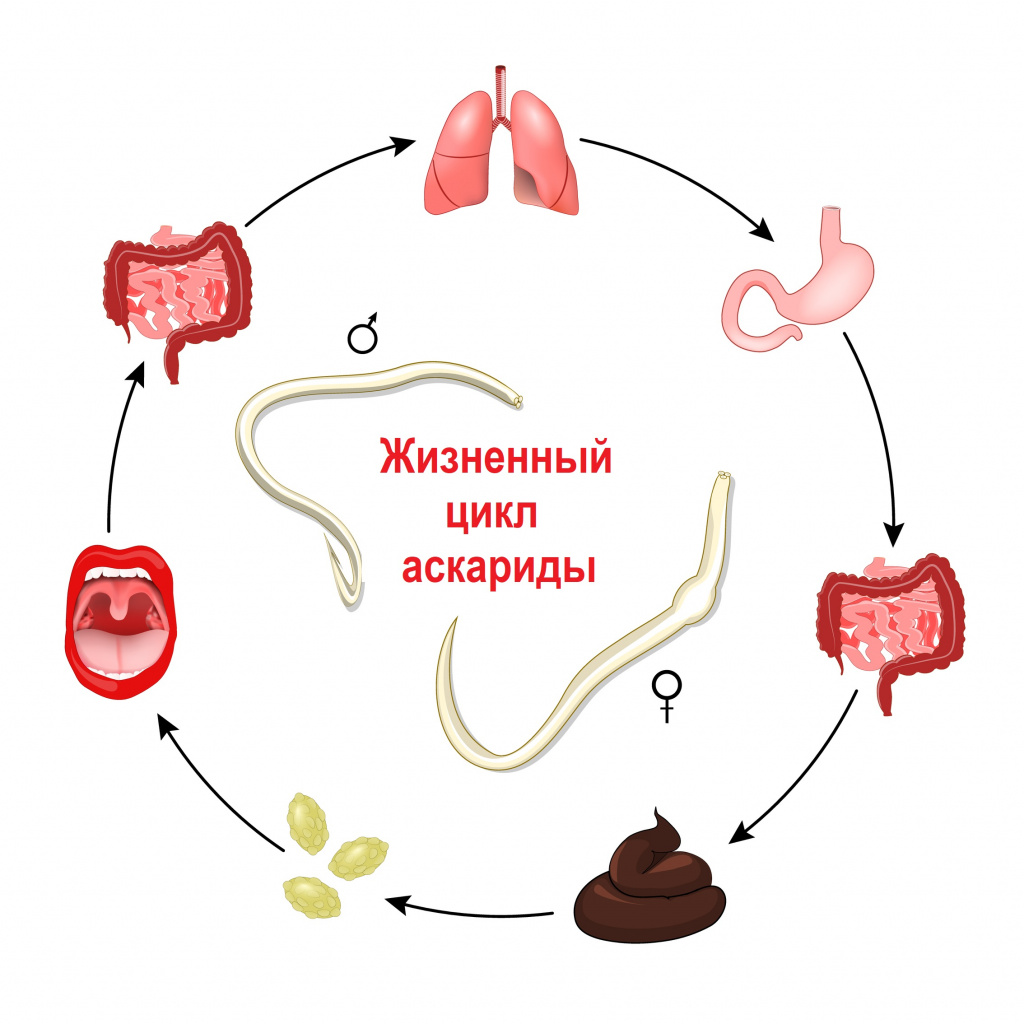
Заражение гельминтами чаще всего происходит после попадания в организм их яиц и/или личинок. В зависимости от механизма заражения и путей передачи гельминтозы подразделяются на: геогельминтозы, биогельминтозы и контактные гельминтозы. Геогельминты развиваются без промежуточных хозяев, биогельминты - с последовательной сменой одного-двух-трех хозяев, контактные гельминты передаются контактным путем.
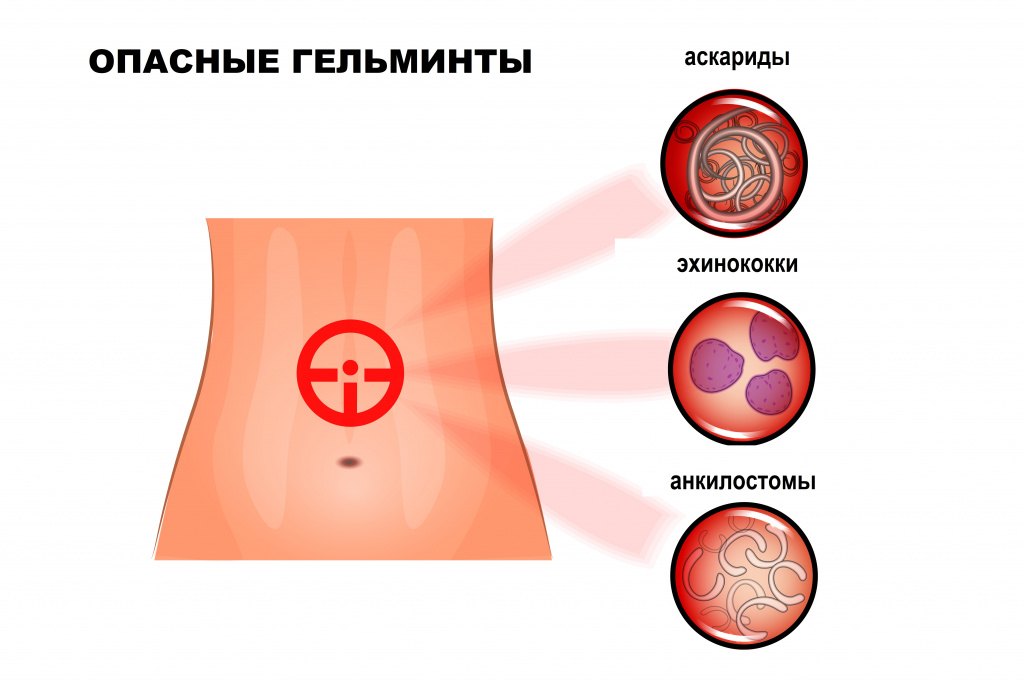
Свиной цепень, бычий цепень, эхинококк и другие виды червей развиваются с последовательной сменой одного-двух-трех хозяев. Промежуточными хозяевами могут быть рыбы, моллюски, ракообразные, насекомые. Человек заражается этими гельминтами, употребляя в пищу продукты, не прошедшие полноценную термическую обработку:
- мясо говядины, инфицированную финнами (личинками) бычьего цепня;
- свинину, пораженную финнами свиного цепня;
- малосоленую и сырую рыбу с личинками описторхиса или широкого лентеца;
- сырую воду или обработанные этой водой овощи, фрукты.
Контактным путем - то есть при личном контакте здорового человека с зараженным, при пользовании общей посудой, предметами туалета, бельем, при вдыхании пыли в помещении, где находится зараженный человек - передаются энтеробиоз (возбудитель – острица) и гименолепидоз (возбудитель – карликовый цепень). В случае энтеробиоза часто случается самозаражение.
Гельминты определенного вида паразитируют в определенных органах, вызывая различные гельминтозы:
- в толстой кишке - свиной, бычий, карликовый цепни, нематоды (анкилостомы, аскариды, стронгилоиды), острицы, власоглав. Из просвета кишки личинки свиного цепня могут попадать в кровоток и распространяться по организму, оседая в жировой клетчатке, сосудах мышц, камерах глаза, мозге;
- в печени и желчных путях - трематоды (описторхис, клонорхис, фасциола). В печени первично располагаются эхинококковые кисты, а после их разрыва дочерние пузыри можно обнаружить в брыжейке, листках брюшины, селезенке и других органах;
- в органах дыхания - эхинококки, альвеококки, легочные сосальщики, вызывающие парагонимоз;
- в нервной системе - шистосомозы, парагонимоз, эхинококкоз и альвеококкоз;
- в органах зрения - онкоцеркоз, лоаоз, осложненные формы тениоза;
- в органах кровообращения - некатороз, шистосомозы, дифиллоботриоз;
- в лимфатической системе - филяриатозы, трихинеллез;
- в коже и подкожной клетчатке - анкилостомидоз, онкоцеркоз, лоаоз, личиночная стадия шистосомозов;
- в костной системе - эхинококкоз;
- в скелетной мускулатуре - трихинеллез, цистицеркоз мышечной ткани.
Срок жизни гельминтов в организме окончательного хозяина может быть различным, зависит от вида паразита и колеблется от нескольких недель (острицы) до нескольких лет (цепни) и десятилетий (фасциолы).
Классификация заболевания
У человека паразитируют черви двух видов:
- Nemathelminthes – круглые черви, класс Nematoda;
- Plathelminthes – плоские черви, которые включают в себя классы
- Cestoidea – ленточных червей,
- Trematoda – класс сосальщиков.
- биогельминтозы;
- геогельминтозы;
- контактные гельминтозы.
На организм человека гельминты оказывают различное воздействие:
- антигенное воздействие, когда развиваются местные и общие аллергические реакции;
- токсическое действие (продукты жизнедеятельности гельминтов вызывают недомогание, слабость, диспепсические явления);
- травмирующее действие (при фиксации паразитов к стенке кишечника происходит нарушение кровоснабжения с некрозом и последующей атрофией слизистой оболочки; могут нарушаться процессы всасывания; механическое сдавление тканей гельминтами);
- вторичное воспаление в результате проникновение бактерий вслед за мигрирующими личинками гельминтов;
- нарушение обменных процессов;
- в результате поглощения крови некоторыми гельминтами возникает анемия;
- нервно-рефлекторное влияние - раздражение гельминтами нервных окончаний провоцирует бронхоспазм, дисфункцию кишечника и т.д.;
- психогенное действие, проявляющееся невротическими состояниями, нарушением сна;
- иммуносупрессивное действие.
Для гельминтозов характерна стадийность развития. Каждая стадия характеризуется своими клиническими симптомами.
Жалобы пациентов в острой стадии:
- повышение температуры от нескольких дней до двух месяцев (субфебрильная или выше 38ºС, сопровождающаяся ознобом, резкой слабостью и потливостью);
- зудящие рецидивирующие высыпания на коже;
- локальные или генерализованные отеки;
- увеличение регионарных лимфатических узлов;
- боли в мышцах и суставах;
- кашель, приступы удушья, боль в грудной клетке, длительные катаральные явления, бронхит, трахеит, симптомы, симулирующие пневмонию, астматический синдром, кровохарканье;
- боль в животе, тошнота, рвота, расстройства стула.
Для кишечных гельминтозов характерны следующие синдромы:
- диспепсический (дискомфорт в животе, чувство переполнения после еды, раннее насыщение, вздутие живота, тошнота);
- болевой;
- астеноневротический (чувство сильной усталости, повышенная нервная возбудимость и раздражительность).
Кишечные цестодозы (тениаринхоз, дифиллоботриоз, гименолепидоз, тениоз и другие) протекают бессимптомно или с малым количеством симптомов (с явлениями диспепсии, болевым синдромом, анемией).
Трематодозы печени (фасциолез, описторхоз, клонорхоз) вызывают:
- хронический панкреатит;
- гепатит;
- холецистохолангит;
- неврологические нарушения.
Мочеполовой шистомоз проявляется появлением в самом конце мочеиспускания крови, частыми позывами к мочеиспусканию, болью во время мочеиспускания.
Альвеококкоз, цистицеркоз, эхинококкоз могут длительное время протекать бессимптомно. На позднем этапе нагноение или разрыв кист, содержащих паразитов, приводит к анафилактическому шоку, перитониту, плевриту и другим тяжелейшим последствиям.
Для заболеваний, обусловленных паразитированием мигрирующих личинок зоогельминтов, когда человек не является естественным хозяином, различают кожную и висцеральную формы. Кожная форма обусловлена проникновением под кожу человека некоторых гельминтов животных: шистосоматид водоплавающих птиц (трематоды), анкилостоматид собак и кошек, стронгилид (нематоды). При контакте человека с почвой или водой личинки гельминтов проникают в кожу. Возникает чувство жжения, покалывания или зуда в месте внедрения гельминта. Может наблюдаться кратковременная лихорадка, признаки общего недомогания. Через 1-2 недели (реже 5-6 недель) наступает выздоровление.
Висцеральная форма развивается в результате заглатывания яиц гельминтов с водой и пищевыми продуктами. В начале заболевания может быть недомогание, аллергическая экзантема (кожная сыпь). В кишечнике человека из яиц гельминтов выходят личинки, которые проникают через кишечную стенку в кровь, достигают внутренних органов, где растут и достигают 5-10 см в диаметре, сдавливают ткани и нарушают функцию органов. При расположении личинок цепней (цистицерки, ценура) в оболочках и веществе головного мозга наблюдается головная боль, признаки церебральной гипертензии, парезы и параличи, эпилептиформные судороги. Личинки также могут располагаться в спинном мозге, глазном яблоке, серозных оболочках, межмышечной соединительной ткани и др.
Исходом гельминтозов может быть полное выздоровление с ликвидацией гельминтов или развитие необратимых изменений в организме хозяина.
Диагностика гельминтоза
Диагноз гельминтоза устанавливается на основании совокупности жалоб, полученных от пациента сведений о течении болезни, данных лабораторных и инструментальных методов обследования.В острой фазе гельминтозов имеется реакция крови на присутствие гельминта в организме, поэтому рекомендованы следующие исследования:
-
клинический анализ крови: общий анализ, лейкоформула, СОЭ (с микроскопией мазка крови при наличии патологических сдвигов);
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Ключевые слова: H. pylori, НПВП, НПВП-гастропатия, эрадикация, нифурател.
Для цитирования: Каратеев А.Е., Цурган А.В., Мороз Е.В. Helicobacter pylori у больных ревматическими заболеваниями: частота инфицированности и оценка эффективности альтернативной схемы эрадикационной терапии. РМЖ. 2017;17:1220-1224.
Helicobacter pylori in patients with rheumatic diseases: the incidence of infection and evaluation of the effectiveness of the alternative scheme of eradication therapy
Karateev A.E. 1 , Tsurgan A.V. 1 , Moroz E.V. 21 Scientific Research Institute of Rheumatology named after V.A. Nasonovа, Moscow
2 The main military clinical hospital named after Acad. N.N. Burdenko, MoscowHelicobacter pylori (H. pylori) is the main cause of peptic ulcer and chronic gastritis, and a serious risk factor for complications in the upper gastrointestinal tract caused by non-steroidal anti-inflammatory drugs (NSAIDs). Eradication of H. pylori is considered to be an important element of treatment and prevention of NSAID-gastropathy.
The aim of the study was to evaluate the infection of H. pylori in patients with rheumatic diseases (RDs), the effect of this microorganism on the development of NSAID- gastropathy and the possibility of its eradication by nifuratel.
Patients and methods: the urease test was used to assess the presence of H. pylori in patients who regularly took NSAIDs and underwent an endoscopic examination at the Clinic of Scientific Research Institute of Rheumatology named after V.A. Nasonovа for the period from 01.02.2017 to 31.03.2017 (2 months, total sampling). A total of 109 patients, 72.5% of women and 27.5% of men with an average age of 53.5 ± 13.6 years were examined. The frequency of erosions and gastric ulcers in patients with or without H. pylori was compared. After that, 32 patients infected with H. pylori with erosions, ulcers and / or ulcerative anamnesis received anti-Helicobacter therapy (omeprazole 20 mg + amoxicillin 1000 mg + nifuratel 400 mg 2 r. / day for 10 days). The achievement of eradication was evaluated by polymerase chain reaction (PCR) in the feces 6 weeks after completion of the course of treatment.
Results: H. pylori was detected in 56% of the examined patients. In infected patients erosion and ulcers were detected significantly more often than in uninfected patients: 47,5% и 23,0% (OR 3,68; 95% Cl 1,56–8,68), р Conclusion: most Russian patients with RDs are infected with H. pylori. The presence of H. pylori is associated with a greater incidence of NSAID-gastropathy. Eradication therapy with nifuratel is effective and well tolerated.Key words: H. pylori, NSAIDs, NSAID-gastropathy, eradication, nifuratel.
For citation: Karateev A.E., Tsurgan A.V., Moroz E.V. Helicobacter pylori in patients with rheumatic diseases: the incidence of infection and evaluation of the effectiveness of the alternative scheme of eradication therapy // RMJ. 2017. № 17. P. 1220–1224.Представлены результаты исследования частоты инфицированности и оценки эффективности альтернативной схемы эрадикационной терапии Helicobacter pylori у больных ревматическими заболеваниями
Материал и методы
Результаты исследования
Уреазный тест оказался положительным у 61 больного (56,0%). Эрозии и язвы верхних отделов ЖКТ выявлены у 40 пациентов (36,7%), причем единичные эрозии (менее 10) – у 23 (21,1%), множественные эрозии (более 10) – у 8 (7,3%), язвы желудка – у 9 больных (8,3%).
Группы больных, инфицированных и не инфицированных H. pylori, достоверно не различались по среднему возрасту и полу (p<0,05). Имелась четкая достоверная разница в частоте эрозий и язв у больных, инфицированных и не инфицированных H. pylori (рис. 1). Как видно, эти изменения гораздо чаще отмечались у пациентов с положительным уреазным тестом (p <0,001). В частности, язвы желудка были выявлены у 7 инфицированных больных и лишь у 2-х неинфицированных.
Суммарно риск (ОШ) выявления эрозии и/или язвы желудка у больных, инфицированных H. pylori, составил 3,68 (95% ДИ 1,56–8,68). Следует также отметить, что наличие гастралгий существенно чаще отмечалось у больных с H. pylori – у 19 (31,1%), чем у больных с отрицательным уреазным тестом – у 7 (14,6%), p=0,027.
Эрадикация H. pylori проводилась у 32 больных. Полный курс антибиотиков проведен практически у всех пациентов, лишь у одного из них лечение было прервано из-за развития кожной аллергической реакции. Кроме этого случая, других значимых НР не отмечено.
Через 6 нед. после окончания антихеликобактерной терапии эрадикация H. pylori (отрицательная ПЦР) была достигнута у подавляющего большинства больных (рис. 2). Инфицированность этим микроорганизмом сохранилась лишь в 4-х случаях. Результаты лечения еще 2-х пациентов остались неизвестными.
1. Маев И.В., Самсонов АА., Андреев Д.Н. и др. Клиническое значение инфекции Helicobacter pylori // Клиническая медицина. 2013. №8. С.4–12 [Maev I.V., Samsonov A.A., Andreev D. N. i dr. Klinicheskoe znachenie infekcii Helicobacter pylori // Klinicheskaja medicina. 2013. №8. S.4–12 (in Russian)].
2. Pilotto A., Franceschi M. Helicobacter pylori infection in older people // World J Gastroenterol. 2014. Jun 7. Vol. 20(21). P.6364–6373. doi: 10.3748/wjg.v20.i21.6364
3. Testerman T.L., Morris J. Beyond the stomach: an updated view of Helicobacter pylori pathogenesis, diagnosis, and treatment // World J Gastroenterol. 2014. Sep 28. Vol. 20(36). P.12781–1808. doi: 10.3748/wjg.v20.i36.12781
4. Malfertheiner P., Megraud F., O'Morain C.A. et al.Management of Helicobacter pylori infec-tion-the Maastricht V/Florence Consensus Report // Gut. 2017. Vol. 66(1). P. 6–30. doi: 10.1136/gutjnl-2016-312288. Epub 2016 Oct 5.
5. Лазебник Л.Б., Ткаченко Е.И., Абдулганиева Д.И. и др. Национальные рекомендации по диагностике и лечению кислотозависимых и ассоциированных с Helicobacter pylori заболеваний (V Московские соглашения) // Терапия. 2015. №2(2). С.9–18 [Lazebnik L.B., Tkachenko E.I., Abdulganieva D.I. i dr. Nacional'nye rekomendacii po diagnostike i lecheniju kislotozavisimyh i associirovannyh s Helicobacter pylori zabolevanij (V Moskovskie soglashenija) // Terapija. 2015. №2(2). S.9–18 (in Russian)].
6. McGeachie J., Robinson G., Black D. Antibacterial activity of nifuratel in urine and serum // J Clin Pathol. 1972, May. Vol. 25(5). P.447–449.
7. Nijevitch A.A., Sataev V.U., Akhmadeyeva E.N., Arsamastsev A.G. Nifuratel-containing initial anti-Helicobacter pylori triple therapy in children // Helicobacter. 2007, Apr. Vol. 12(2). P.132–135.
8. Успенский Ю.П., Барышникова Н.В. Использование препаратов нитрофуранового ряда в схемах эрадикационной терапии первой линии // РМЖ. 2012. №35. С.1694 [Uspenskij Ju.P., Baryshnikova N.V. Ispol'zovanie preparatov nitrofuranovogo rjada v shemah jeradikacionnoj terapii pervoj linii // RMZh. 2012. №35. S.1694 (in Russian)].
9. Абдулхаков Р.А., Абдулхаков С.Р. Эпидемиология Helicobacter pylori // Практическая медицина. 2006. №4(18). С.2–3 [Abdulhakov R.A., Abdulhakov S.R. Jepidemiologija Helicobacter pylori // Prakticheskaja medicina. 2006. №4(18). S.2–3 (in Russian)].
10. Герман С.В., Зыкова И.Е., Модестова А.В., Ермаков Н.В. Распространенность инфекции H. pylori среди населения Москвы // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2010. №2. С. 25–30 [German S.V., Zykova I.E., Modestova A.V., Ermakov N.V. Rasprostranennost' infekcii H. pylori sredi naselenija Moskvy // Rossijskij zhurnal gastrojenterologii, gepatologii, koloproktologii. 2010. №2. S.25–30 (in Russian)].
11. Huang J., Sridhar S., Hunt R. Role of Helicobacter pylori infection and non-steroidal anti-inflammatory drugs in peptic-ulcer disease: a meta-analysis // Lancet. 2002. Vol. 359. P.14–22.
12. Sostres C., Carrera-Lasfuentes P., Benito R. et al. Peptic Ulcer Bleeding Risk. The Role of Helicobacter Pylori Infection in NSAID/Low-Dose Aspirin Users // Am J Gastroenterol. 2015, May. Vol. 110(5). P.684–689. doi: 10.1038/ajg.2015.98. Epub 2015 Apr 21.
13. Vergara M., Catalán M., Gisbert J.P., Calvet X. Meta-analysis: role of Helicobacter pylori eradication in the prevention of peptic ul- cer in NSAID users // Aliment Pharmacol Ther. 2005. Vol. 21(12). P.1411–1418 [PMID: 15948807. doi: 10.1111/j.1365-2036.2005.02444.x]
14. Tang C.L., Ye F., Liu W. et al. Eradication of Helicobacter pylori infection reduces the incidence of peptic ulcer disease in patients using nonsteroidal anti-inflammatory drugs: a meta-analysis // Helicobacter. 2012. Vol. 17. P.286–296 [PMID: 22759329 doi: 10.1111/j.1523-5378.2012.00942.x]
15. Hawkey C., Tulassay Z., Szczepanski L. et al. Randomised controlled trial of Helicobacter pylori eradication in patients on non-steroidal anti-inflammatory drugs: HELP NSAIDs study. Helicobacter Eradication for Lesion Prevention // Lancet. 1998, Sep 26. Vol. 352(9133). P.1016–1021.
16. Каратеев А.Е., Муравьев Ю.В., Раденска-Лоповок С.Г., Насонова В.А. Эффективность антихеликобактерной терапии при НПВП-индуцированной гастропатии // Клин. мед. 2003. № 4. С.37–41 [Karateev A.E., Murav'ev Ju.V., Radenska-Lopovok S.G., Nasonova V.A. Jeffektivnost' antihelikobakternoj terapii pri NPVP-inducirovannoj gastropatii // Klin. med. 2003. № 4. S.37–41 (in Russian)].
17. Корниенко Е.А., Базрова Ф.В. Региональные особенности гастродуоденальной патологии, ассоциированной с инфекцией Helicobacter pylori у детей Северной Осетии // Журнал инфектологии. 2011. № 3(3). С.86–90. doi:10.22625/2072-6732-2011-3-3-86-90 [Kornienko E.A., Bazrova F.V. Regional'nye osobennosti gastroduodenal'noj patologii, associirovannoj s infekciej Helicobacter pylori u detej Severnoj Osetii // Zhurnal infektologii. 2011. № 3(3). S.86–90. doi:10.22625/2072-6732-2011-3-3-86-90 (in Russian)].
18. Шадрин О.Г., Зайцева Н.Е., Гарынычева Т.А. Helicobacter pylori у детей: современные подходы к диагностике и пути оптимизации терапии // Современная педиатрия. 2014. №5(61). С.119–127. doi 10.15574/SP.2014.61.119 [Shadrin O.G., Zajceva N.E., Garynycheva T.A. Helicobacter pylori u detej: sovremennye podhody k diagnostike i puti optimizacii terapii // Sovremennaja pediatrija. 2014. №5(61). S.119–127. doi 10.15574/SP.2014.61.119 (in Russian)].
19. Wallace J.L. Mechanisms, prevention and clinical implications of nonsteroidal anti-inflammatory drug-enteropathy // World J Gastroenterol. 2013, Mar 28. Vol. 19(12). P.1861–1876. doi: 10.3748/wjg.v19.i12.1861
20. Lué A., Lanas A. Protons pump inhibitor treatment and lower gastrointestinal bleeding: Balancing risks and benefits // World J Gastroenterol. 2016, Dec 28. Vol. 22(48). P. 10477–10481. doi: 10.3748/wjg.v22.i48.10477
21. Scarpignato C., Dolak W., Lanas A. et al. Rifaximin Reduces Number and Severity of Intestinal Lesions Associated With use of Non-steroidal Anti-inflammatory Drugs in Humans // Gastroenterology. 2016, Dec 19. Vol. 152(5). P.980–982. pii: S0016-5085(16)35504-4. doi: 10.1053/j.gastro.2016.12.007 [Epub ahead of print]Helicobacter pylori – самая распространенная инфекция человека. H. pylori известен как причина хронического гастрита и язвы желудка и двенадцатиперстной кишки. Однако взаимодействие H. pylori и макроорганизма не ограничивается лишь слизистой оболочкой желудка – механизмы, определяющие адаптацию этой бактерии к условиям жизни в человеческом организме, могут вызывать системные нарушения иммунного равновесия, провоцируя развитие разнообразных аутоиммунных реакций. В статье рассмотрены исследования, демонстрирующие возможную роль H. pylori в качестве пускового или отягощающего фактора при ревматических заболеваниях, таких как ревматоидный артрит (РА), а также синдром и болезнь Шёгрена, системная красная волчанка и прогрессирующий системный склероз. Взаимосвязь между H. pylori и развитием аутоимунных заболеваний подтверждается большей частотой более агрессивных штаммов этого микроорганизма при ревматических заболеваниях. Имеются также клинические исследования, которые показывают позитивное влияние эрадикации H. pylori на активность РА.
Ключевые слова
Об авторах
Литература
1. Насонов ЕЛ. Почему необходима ранняя диагностика и лечение ревматоидного артрита? Русский Медицинский Журнал. 2002;10(22):1009-12. [Nasonov EL. Why the early diagnosis and treatment of rheumatoid arthritis is necessary? Russkii Meditsinskii Zhurnal. 2002;10(22):1009-12. (In Russ.)].
4. Балабанова РМ, Эрдес ШФ. Динамика распространенности ревматических заболеваний, входящих в ХIII класс МКБ-10, в популяции взрослого населения Российской Федерации за 2000–2010 гг. Научно-практическая ревматология. 2012;50(3):10–2. [Balabanova RM, Erdes ShF. Trends in the prevalence of rheumatic diseases in ICD-10 in the adult population of the Russian Federation over 2000-2010. Nauchno-prakticheskaya revmatologiya = Rheumatology Science and Practice. 2012;50(3):10–2. (In Russ.)]. doi: 10.14412/1995-4484-2012-702
5. Marshall BJ, Warren JR. Unidentified curved bacilli in the stomach of patients with gastritis and peptic ulceration. Lancet. 1984 Jun 16;1(8390):1311-5.
6. Smyk DS, Koutsoumpas AL, Mytilinaiou MG, et al. Helicobacter pylori and autoimmune disease: cause or bystander. World J Gastroenterol. 2014 Jan 21;20(3):613-29. doi: 10.3748/wjg.v20.i3.613.
7. Kusters JG, van Vliet AH, Kuipers EJ. Pathogenesis of Helicobacter pylori Infection. Clin Microbiol Rev. 2006 Jul;19(3):449-90. doi:10.1128/CMR.00054-05.
8. Goodwin CS, Armstrong JA. Microbiological aspects of Helicobacter pylori (Campylobacter pylori). Eur J Clin Microbiol Infect Dis. 1990 Jan;9(1):1-13.
9. Sato F, Saito N, Konishi K, et al. Ultrastructural observation of Helicobacter pylori in glucose-supplemented culture media. J Med Microbiol. 2003 Aug;52 (Pt 8):675-9.
11. Chaput C, Ecobichon C, Pouradier N, et al. Role of the N-Acetylmuramoyl-lAlanyl Amidase, AmiA, of Helicobacter pylori in Peptidoglycan Metabolism, Daughter Cell Separation, and Virulence. Microb Drug Resist. 2016 Sep;22(6):477-86. doi: 10.1089/mdr.2016.0070. Epub 2016 Jul 22.
12. Маев ИВ, Самсонов АА, Андреев ДН, Гречушников ВБ. Клиническое значение инфекции Helicobacter pylori. Клиниче- ская медицина. 2013;91(8):4-13. [Maev IV, Samsonov AA, Andreev DN, Grechushnikov VB. Clinical significance of Helicobacter pylori infection. Klinicheskaya meditsina. 2013;91(8):4-13. (In Russ.)].
13. Eusebi LH, Zagari RM, Bazzoli F. Epidemiology of Helicobacter pylori infection. Helicobacter. 2014 Sep;19 Suppl 1:1-5. doi: 10.1111/hel.12165.
14. Khalifa MM, Sharaf RR, Aziz RK. Helicobacter pylori: a poor man's gut pathogen? Gut Pathog. 2010 Mar 31;2(1):2. doi: 10.1186/1757-4749-2-2.
15. Mana F, Vandebosch S, Miendje Deyi V, et al. Prevalence of and risk factors for H. pylori infection in healthy children and young adults in Belgium anno 2010/ 2011. Acta Gastroenterol Belg. 2013 Dec; 76(4):381-5.
17. Benajah DA, Lahbabi M, Alaoui S, et al. Prevalence of Helicobacter pylori and its recurrence after successful eradication in a developing nation (Morocco). Clin Res Hepatol Gastroenterol. 2013 Nov;37(5): 519-26. doi: 10.1016/j.clinre.2013.02.003. Epub 2013 Apr 6.
20. Sierra MS, Hastings EV, Fagan-Garcia K, et al. Epidemiology, transmission and public health implications of Helicobacter pylori infection in Western countries. Helicobacter pylori: a worldwide perspective. 2014: 25-79. doi: 10.2174/9781608057375114010006
21. Yokota S, Konno M, Fujiwara S, et al. Intrafamilial, preferentially mother-to-child and intraspousal, Helicobacter pylori infection in Japan determined by mutilocus sequence typing and random amplified polymorphic DNA fingerprinting. Helicobacter. 2015 Oct;20(5):334-42. doi: 10.1111/hel. 12217. Epub 2015 Feb 9.
22. Roesler BM, Rabelo-Goncalves EM, Zeitune JM. Virulence Factors of Helicobacter Pylori: A Review. Clin Med Insights Gastroenterol. 2014 Mar 27;7:9-17. doi: 10.4137/CGast.S13760. eCollection 2014.
23. Montecucco C, Rapuolli R. Living dangerously: how Helicobacter pylori survives in the human stomach. Nat Rev Mol Cell Biol. 2001 Jun;2(6):457-66.
24. Schoep TD, Fulurija A, Good F, et al. Surface properties of Helicobacter pylori urease complex are essential for persistence. PLoS One. 2010 Nov 29;5(11):e15042. doi: 10.1371/journal.pone.0015042.
25. Schreiber S, Konradt M, Groll C, et al. The spatial orientation of Helicobacter pylori in the gastric mucus. Proc Natl Acad Sci U S A. 2004 Apr 6;101(14):5024-9. Epub 2004 Mar 25.
26. Smolka AJ, Backert S. How Helicobacter pylori infection controls gastric acid secretion. J Gastroenterol. 2012 Jun;47(6):609-18. doi: 10.1007/s00535-012-0592-1. Epub 2012 May 8.
27. Cadamuro AC, Rossi AF, Maniezzo NM, Silva AE. Helicobacter pylori infection: host immune response, implications on gene expression and microRNAs. World J Gastroenterol. 2014 Feb 14;20(6):1424-37. doi: 10.3748/wjg.v20.i6.1424.
28. Lee MS, Kim YJ. Signaling pathways downstream of pattern-recognition receptors and their cross talk. Annu Rev Biochem. 2007;76:447-80.
29. Wang G, Ge Z, Rasko DA, Taylor DE. Lewis antigens in Helicobacter pylori: biosynthesis and phase variation. Mol Microbiol. 2000 Jun;36(6):1187-96.
30. Andersen-Nissen E, Smith KD, Strobe KL, et al. Evasion of toll-like receptor 5 by flagellated bacteria. Proc Natl Acad Sci U S A. 2005 Jun 28;102(26):9247-52. Epub 2005 Jun 13.
32. Satin B, Del Giudice G, Della Bianca V, et al. The neutrophil-activating protein (HP-NAP) of Helicobacter pylori is a protective antigen and a major virulence factor. J Exp Med. 2000 May 1;191(9):1467-76.
33. Schwartz JT, Allen LA. Role of urease in megasome formation and Helicobacter pylori survival in macrophages. J Leukoc Biol. 2006 Jun;79(6):1214-25. Epub 2006 Mar 16.
35. O’Keeffe J, Moran AP. Conventional, regulatory, and unconventional T cells in the immunologic response to Helicobacter pylori. Helicobacter. 2008 Feb;13(1):1-19. doi: 10.1111/j.1523-5378.2008.00559.x.
36. Kä bisch R, Mejias-Luque R, Gerhard M. Involvement of Toll-like receptors on Helicobacter pylori-induced immunity. PLoS One. 2014 Aug 25;9(8):e104804. doi: 10.1371/ journal.pone.0104804. eCollection 2014.
37. Showji Y, Nozawa R, Sato K, Suzuki H. Seroprevalence of Helicobacter pylori infection in patients with connectivetissue diseases. Microbiol Immunol. 1996; 40(7):499-503.
38. Aragona P, Magazzu G, Macchia G, et al. Presence of antibodies against Helicobacter pylori and its heat-shock protein 60 in the serum of patients with Sjö gren's syndrome. J Rheumatol. 1999 Jun;26(6):1306-11.
39. Sorrentino D, Faller G, DeVita S, et al. Helicobacter pylori associated antigastric autoantibodies: role in Sjö gren's syndrome gastritis. Helicobacter. 2004 Feb;9(1):46-53.
40. Thieblemont C, Bertoni F, Copie-Bergman C, et al. Chronic inflammation and extra-nodal marginal-zone lymphomas of MALT-type. Semin Cancer Biol. 2014 Feb;24:33-42. doi: 10.1016/j.semcancer.2013.11.005. Epub 2013 Dec 9.
41. Theander E, Nilsson I, Manthorpe R, et al. Seroprevalence of Helicobacter pylori in primary Sjö gren's syndrome. Clin Exp Rheumatol. 2001 Nov-Dec;19(6):633-8.
42. Francis L, Perl A. Infection in systemic lupus erythematosus: friend or foe? Int J Clin Rheumtol. 2010 Feb 1;5(1):59-74.
43. Magen E, Delgado JS. Helicobacter pylori and skin autoimmune diseases. World J Gastroenterol. 2014 Feb 14;20(6):1510-6. doi: 10.3748/wjg.v20.i6.1510.
44. Sawalha AH, Schmid WR, Binder SR, et al. Association between systemic lupus erythematosus and Helicobacter pylori seronegativity. J Rheumatol. 2004 Aug;31(8):1546-50.
45. Hamamdzic D, Kasman LM, LeRoy EC. The role of infectious agents in the pathogenesis of systemic sclerosis. Curr Opin Rheumatol. 2002 Nov;14(6):694-8.
46. Yazawa N, Fujimoto M, Kikuchi K, et al. High seroprevalence of Helicobacter pylori infection in patients with systemic sclerosis: association with esophageal involvement. J Rheumatol. 1998 Apr;25(4):650-3.
48. Radic M, Kaliterna DM, Bonacin D, et al. Is Helicobacter pylori infection a risk factor for disease severity in systemic sclerosis? Rheumatol Int. 2013 Nov;33(11):2943-8. doi: 10.1007/s00296-012-2585-z. Epub 2012 Dec 6.
49. Yamaguchi K, Iwakiri R, Hara M, et al. Reflux esophagitis and Helicobacter pylori infection in patients with scleroderma. Intern Med. 2008;47(18):1555-9. Epub 2008 Sep 16.
50. Gasbarrini A, Massari I, Serricchio M, et al. Helicobacter pylori eradication ameliorates primary Raynaud’s phenomenon. Dig Dis Sci. 1998 Aug;43(8):1641-5.
51. Savarino V, Sulli A, Zentilin P, et al. No evidence of an association between Helicobacter pylori infection and Raynaud phenomenon. Scand J Gastroenterol. 2000 Dec;35(12):1251-4.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Официальной классификации локальных жировых отложений в области 7-го шейного позвонка не существует, поэтому врачи ориентируются на выраженность процесса и симптоматику.
Таким образом, выделяют:
Увеличение массы тела по абдоминальному (андроидному) типу с распределением жировых отложений в верхней части туловища.
Если у пациента присутствует артериальная гипертензия и/или сахарный диабет, то тяжесть метаболических изменений в организме усугубляется.
Нарушение осанки – еще один фактор, следствием которого становится формирование локальных жировых отложений в области седьмого шейного позвонка. У пожилых пациентов осанка может меняться из-за остеопороза, остеохондроза, возрастных изменений в межпозвонковых дисках и слабости связочного аппарата, а у молодых - в результате травм и остеохондроза, когда параллельно с накоплением жировых отложений происходит разрастание соединительной ткани.
![Осанка.jpg]()
У людей, много времени проводящих за компьютером, наблюдается хронический спазм мышц шейно-воротниковой зоны из-за постоянного нахождения шеи в напряженном положении, в результате чего снижается сократительная способность мышц и их функциональная активность. Со временем в области 7-го шейного позвонка появляется изгиб, провоцирующий нарушение лимфо- и кровотока, застой, а как результат - формирование локальных отложений жира.
Основные диагностические мероприятия направлены на установление причины отложения локального жира в области холки.
-
УЗИ мягких тканей и сосудов шеи позволяет оценить степень нарушения кровотока.
Исследование, позволяющее оценить кровоток в позвоночных и сонных артериях.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Хеликобактериоз: причины появления, симптомы, диагностика и способы лечения.
Определение
Хеликобактериоз – инфекционное заболевание, поражающее пилорический отдел желудка, или привратник, и двенадцатиперстную кишку. Его возбудителем является уникальная патогенная микроаэрофильная грамотрицательная бактерия хеликобактер пилори (H. pylori). Свое название бактерия получила за счет отдела желудка, в котором она обитает – пилорического.В результате микроорганизм еще сильнее колонизирует слизистую оболочку, формирует ее повышенную восприимчивость к соляной кислоте и провоцирует воспаление, приводящее к развитию язвенных дефектов.
![Хеликобактериоз.jpg]()
Хеликобактер пилори – спиралевидная бактерия длиной 3,5 и шириной 0,5 микрон. Она имеет жгутики, с помощью которых свободно перемещается по стенке желудка либо надежно на ней закрепляется. Бактерия H. pylori очень изменчива, ее штаммы (разновидности) отличаются друг от друга способностью прикрепляться к слизистой оболочке желудка, вызывать воспалительный процесс и обладают разной степенью патогенности.
![Helicobacter pylori.jpg]()
Хеликобактер пилори, колонизирующая слизистую оболочку желудка, — частая причина ее воспалительных изменений, она признана этиологическим фактором гастрита, а сам гастрит — инфекционным заболеванием. В зависимости от состояния защитных факторов желудка возникший инфекционный процесс может протекать латентно или с выраженной клинической симптоматикой воспаления. Согласно современным представлениям, H. pylori вызывает хронический гастрит у всех зараженных лиц. Это может привести к язвенной болезни, атрофическому гастриту, аденокарциноме желудка или низкодифференцируемой лимфоме желудка. H. pylori относится к канцерогенам первого порядка.
Результаты многочисленных исследований дают основание предполагать возможную патогенетическую или опосредованную роль инфекции H. pylori в развитии и/или течении заболеваний, не относящихся к пищеварению: кардио-, цереброваскулярных, аутоиммунных заболеваний, заболеваний крови, кожи, нервной системы и многих других.
Патоген отличается относительной устойчивостью к окружающей среде: при кипячении хеликобактерии гибнут практически мгновенно, при обработке дезинфицирующими составами — в течение нескольких минут.
Причины появления хеликобактериоза
Заразиться бактерией можно при контакте с загрязненной водой или продуктами питания. Инфицирование возможно во время проведения эндоскопии и при использовании других плохо стерилизованных медицинских инструментов, которые имели прямой контакт со слизистой желудка пациента.Бытовой способ передачи (например, через поцелуи, личные вещи и проч.) также возможен, о чем свидетельствует выделение бактерии из слюны и зубного налета.
Распространенность инфекции варьируется в зависимости от географического региона, возраста пациента, его этнической принадлежности и социально-экономического статуса. По данным Департамента здравоохранения г. Москвы (2019), распространенность этой инфекции в Москве составляет 60,7–88%, в Санкт-Петербурге - 63,6%, в Восточной Сибири достигает 90%.
Классификация заболеваний
Заболевания, связанные с H. pylori:- гастрит,
- дуоденит,
- гастродуоденит,
- эзофагит,
- язвенная болезнь желудка,
- язвенная болезнь двенадцатиперстной кишки,
- железодефицитная анемия неясного генеза,
- рак желудка,
- рак двенадцатиперстной кишки.
Основной жалобой, с которой больные с признаками Helicobacter-инфекции обращаются к врачу, являются желудочные боли. Локализация симптома может меняться и переходить в область расположения двенадцатиперстной кишки.
Боли бывают острыми, ноющими, тупыми, возникают в верхних отделах живота слева и по центру в околопупочной области. Дискомфорт может возникать при длительном голодании, натощак или через определенное время после приема пищи.
Симптоматика хеликобактериоза зависит от клинической формы заболевания и может включать:
- чувство тяжести в животе после еды;
- нарушение аппетита, связанное с внезапными приступами тошноты (если слизистая желудка сильно травмирована);
- беспричинная рвота на фоне нормальной температуры тела;
- изжога (жгучие ощущения в пищеводе и даже гортани) и отрыжка с неприятным кислым или горьким привкусом;
- хронические запоры (отсутствие дефекации в течение трех суток и более);
- разжижение каловых масс, появление пенистой или водянистой консистенции;
- кишечные спазмы и вздутие живота.
- снижение аппетита до полного его отсутствия;
- тошнота может сменяться рвотой со сгустками крови;
- резкое снижение массы тела, не являющееся нормой;
- сухость во рту и привкус металла;
- появление белого налета на языке;
- неприятный запах изо рта при отсутствии кариеса;
- заеды в уголках рта;
- кровоточивость десен.
Диагностика хеликобактериоза
Долгое время хеликобактериоз может никак себя не проявлять, при этом провоцируя развитие язвы, аденокарциномы или мальтомы желудка. В особой зоне риска люди, чьи родственники имеют эти заболевания в анамнезе.Диагностика может быть инвазивной (эндоскопия с последующей биопсией желудочных тканей) и неинвазивной (лабораторные исследования).
Согласно международным рекомендациям, методами выбора для диагностики бактерии и оценки эффективности лечения H. pylori служат дыхательный̆ тест с мочевиной, меченной 13С и определение специфических антигенов H. pylori в кале иммунохроматографическим методом.
Синонимы: Дыхательный тест с 13С-меченной мочевиной. 13 UBT; 13C-UBT. Краткая характеристика 13С-уреазного дыхательного теста Дыхательный тест в текущей модификации предназначен для лиц старше 12 лет. 13С-уреазный дыхательный тест относится к неинвазивным безопасным методам исследования.
Читайте также: