Изменения в костном мозге при сепсисе
Обновлено: 26.07.2024
Патологоанатомическая диагностика сепсиса : методические рекомендации / О.Д.Мишнёв, А.И.Щёголев, О.А.Трусов. — Москва, 2004.
библиографическое описание:
Патологоанатомическая диагностика сепсиса : методические рекомендации / Мишнёв О.Д., Щёголев А.И., Трусов О.А. — 2004.
код для вставки на форум:
Российское общество патологоанатомов
О.Д.Мишнев, А.И.Щеголев, О.А.Трусов
ПАТОЛОГОАНАТОМИЧЕСКАЯ ДИАГНОСТИКА СЕПСИСА
Введение
Сепсис – полиэтиологическое инфекционное заболевание, характеризующееся генерализованным характером, ацикличностью течения и особым образом измененной реактивностью. Сепсис развивается из местных очагов инфекции и рассматривается, как правило, в качестве осложнения заболеваний, послуживших причиной генерализации инфекции. Последние годы, несмотря на интенсивную терапию, характеризуются ростом числа больных сепсисом и высокой летальностью.
Сепсис представляет собой заболевание, в отношении этиологии, патогенеза, патологической анатомии, диагностики, лечения которого всегда были и ещё будут проводиться дискуссии. Клиницисты обращаются к патологоанатомам в надежде получить желаемое и в то же время, по их мнению, объективное и адекватное объяснение летального исхода при сепсисе. Однако, справедливости ради, следует констатировать, что, как правило, такое объяснение для них a priori, до вскрытия, в современных клиниках уже имеется, и оно может быть получено на основании комплекса клинических и лабораторных признаков доказательной медицины.
Именно эти показатели, очевидно, следует использовать и патологоанатому при анализе истории болезни и результатов вскрытия для решения своих диагностических проблем. Многие клиницисты интересуются на вскрытии, т.е. a posteriori, не столько познанием на морфологическом субстрате причины и действия, сколько прагматичным согласованием формальных параметров, определяемых при сличении клинического и патологоанатомического диагнозов. Это определяет первоочередную задачу совместной междисциплинарной работы – нахождения общих точек соприкосновения клиницистов и патологоанатомов для полноценного и современного анализа результатов патологоанатомического исследования умерших от сепсиса.
Теоретические аспекты проблемы сепсиса, представленные в мировой литературе конца ХХ – начала нынешнего века и воспринимаемые как революционные и во многом совершенные, дающие основания для разработки оптимальных методов лечения и недопущения летальных исходов при сепсисе, не были неожиданными для патологоанатомов России. В этом заслуга наших Учителей и в первую очередь И.В. Давыдовского, а также А.В.Смольянникова, Д.С.Саркисова, А.П.Авцына, Н.К.Пермякова и других, которые первоочередное внимание уделяли макробиологической составляющей сепсиса, не забывая при этом об этиопатогенетической роли возбудителей инфекции.
Принятие и выполнение решений Согласительной конференции пульмонологов и специалистов по интенсивной терапии (ACCP/SCCV), состоявшейся в 1991 году в Чикаго, привело к унификации терминологии и к упрощению клинической диагностики сепсиса. Однако отсутствие рандомизированных патологоанатомических исследований и, соответственно, клинико-морфологических сопоставлений является одной из важных причин неполного взаимопонимания клиницистов и патологоанатомов при оценке формы и танатогенеза заболевания, а также при обсуждении расхождений клинического и патологоанатомического диагнозов. К сожалению, до настоящего времени предметом дискуссий является отнесение тех или иных клинических и морфологических признаков к проявлениям сепсиса.
Также следует остановиться на распространённой ныне тенденции считать условным выделение разновидностей сепсиса по входным воротам, поскольку генерализованная реакция организма на инфекцию по своей сути является единой и требует незамедлительного лечения, а в Международной классификации болезней отсутствует подразделение сепсиса на разновидности по данному основанию. Возможно, что такой прагматичный подход является обоснованным, однако мы рекомендуем патологоанатомам не забывать о морфологических особенностях различных форм сепсиса в зависимости от входных ворот.
Действительно, для патологоанатома и клинициста не будет представлять большой сложности достижение взаимопонимания при анализе результатов секции больного, погибшего от сепсиса при наличии типичных морфологических признаков и соответствующих клинических данных. Гораздо большие трудности возникнут в том случае, когда больного лечили от сепсиса (и по результатам вскрытия довольно успешно – именно так!), а смерть наступила от другой причины, видимо не связанной с сепсисом. В этом случае необходимо учитывать не только медицинские составляющие (организационные, научно–практические), но также социальные и экономические вопросы, которые в настоящее время никогда не следует упускать из вида. Также сложными для патологоанатомической диагностики являются наблюдения лечённого сепсиса в плане танатогенеза и установления непосредственной причины смерти. Наконец, наблюдения посмертно диагностированного сепсиса, который не был выявлен в клинике, должны стать предметом обсуждения на клинико–патологоанатомических конференциях.
Определения терминов и понятий
Сепсис (в переводе с греческого sēpsis – гниение) – представляет собой особую форму тяжелой генерализованной инфекции, при которой макроорганизм не способен локализовать инфекционный процесс (Белянин В.Л., Рыбакова М.Г., 2004).
Бактериемия – симптом, обозначающий наличие в крови живых микроорганизмов (не обязательно только при сепсисе).
Диссеминация – употребляется, как правило, для характеристики распространения поражений при инфекционном процессе в пределах одного органа (например, диссеминированный туберкулез легких).
Генерализация – обозначает, как правило, поражение многих органов и систем (например, генерализованная вирусная, туберкулезная инфекция).
Синдром системного воспалительного ответа (ССВО) (Systemic Inflammatory Response Syndrome (SIRS), синдром системной воспалительной реакции (ССВР)) патологическое состояние, обусловленное одной из форм хирургической инфекции или альтерации ткани неинфекционной природы (травма, панкреатит, ожог, ишемия или аутоиммунные повреждения тканей и др.). Это понятие предложено классификацией ACCP/SCCV, что привело к существенному пересмотру концептуальных положений о патогенезе, клинике, лечении, профилактике возникновения сепсиса и его осложнений. ССВР (SIRS) характеризуется наличием более чем одного из четырёх следующих основных клинических признаков: гипертермия, тахикардия, тахипноэ, лейкоцитоз (или лейкопения). Подобные клинические признаки встречаются при сепсисе, но при этом обязательным является наличие инфекционного очага поражения в тканях или органах. Патологоанатомическая характеристика SIRS является объектом перспективных научных исследований.
Септицемия – клинико–патологоанатомическая форма сепсиса, при которой отсутствуют метастатические септические очаги. Септицемия – это сепсис без гнойных метастазов. По поводу правомочности применения этого понятия в качестве диагноза одной из форм сепсиса до сих пор продолжается дискуссия. Некоторые клиницисты и патологоанатомы советуют вообще отказаться от этого термина (Пермяков Н.К., 1992). Этот термин не представлен и в классификации ACCP/SCCV. Тем не менее, он рекомендован МКБ-10 как унифицированный для всех разновидностей сепсиса, и вплоть до нового пересмотра он должен применяться клиницистами и патологоанатомами при определении шифра большинства клинико–патологоанатомических форм сепсиса.
Септикопиемия – клинико–патологоанатомическая форма сепсиса. Для неё характерно наличие гнойного воспаления (абсцессов, апостем, флегмон, интерстициального гнойного воспаления) в различных органах и тканях, возникающего в результате гематогенного распространения микробных эмболов из септического очага. Септикопиемия – это сепсис с гнойными метастазами.
Термин септикопиемия не представлен в МКБ–10.
Термин сепсис носит обобщающий характер, как и термин септический процесс. Классификация ACCP/SCCV рекомендует в клинике использовать термин сепсис, а не септицемия или септикопиемия. В настоящее время не рекомендуется использовать термин септическое состояние, лишенный конкретной основы.
Тяжёлый сепсис (или сепсис-синдром) – форма сепсиса, предложенная в классификации ACCP/SCCV, при котором отмечаются признаки полиорганной недостаточности. В.Л.Белянин и М.Г.Рыбакова (2004) считают, что с точки зрения патоморфолога понятие тяжёлый сепсис (сепсис–синдром) нельзя признать удачной терминологической находкой.
Септический шок – другая форма тяжёлого сепсиса в классификации ACCP/SCCV, сопровождающаяся артериальной гипотонией, не устраняющейся с помощью инфузионной терапии и требующей назначения катехоламинов.
Септический (бактериальный, инфекционный) эндокардит (острый и подострый) характеризуется, прежде всего, воспалительными поражениями клапанного аппарата сердца, развивающимися наряду с септическими проявлениями. Представляет собой самостоятельное заболевание (первоначальную причину смерти) и имеет собственный шифр. Следует отличать от поражений эндокарда при других формах сепсиса.
Септический очаг – различают первичный и метастатические септические очаги. Первичный септический очаг представляет собой фокус воспаления, преимущественно гнойного, в котором происходит накопление микроорганизмов, распространяющихся затем гематогенно и лимфогенно по тканям и органам. Метастатические септические очаги (вторичные септические очаги, метастатические очаги при сепсисе, септические метастазы, метастатические гнойники, гнойные метастазы) представляют собой очаги воспаления, возникающие вследствие гематогенного перемещения септического процесса в ткани и органы из другого очага.
Системный инфекционный процесс – поражение какой-либо системы органов (например: нервной при клещевом энцефалите; пищеварительной при шигеллезе и т.д.).
Гнойно-резорбтивная лихорадка. Понятие гнойно-резорбтивной лихорадки предложено И.В.Давыдовским для обозначения клинических и патологоанатомических проявлений местного гнойно-некротического процесса, морфологически ограниченного демаркационным валом (в отличие от септических очагов) от окружающих тканей. В настоящее время этот термин почти не используется, а состояние больного обозначается как интоксикация или разновидность эндотоксикоза.
Эндотоксикоз – очень широкое понятие для обозначения осложнений и проявлений заболеваний и состояний организма. Основным фактором патогенеза эндотоксикоза является воздействие на организм токсических продуктов, образующихся в нем в результате нарушения тех или иных функций.
Этиология
Возбудителями сепсиса могут являться многие микроорганизмы (табл. 1). Это многочисленные бактерии: стрептококки, стафилококки, менингококки, пневмококки, кишечная палочка, синегнойная палочка, клебсиеллы, протей, сальмонеллы, а также грибы преимущественно Кандида и аспергиллус. Сепсисом может осложниться течение туберкулеза, сыпного тифа, брюшного тифа и других инфекционных заболеваний, возбудителями которых являются патогенные микроорганизмы. Генерализованные вирусные инфекции не принято рассматривать в качестве сепсиса, хотя об этом имеются указания в современных зарубежных клинических исследованиях.
Таблица. 1. Наиболее вероятная этиология сепсиса в зависимости от локализации первичного очага инфекции
Что такое остеомиелит челюсти? Причины возникновения, диагностику и методы лечения разберем в статье доктора Дунаевской Н. В., стоматолога-ортопеда со стажем в 16 лет.
Над статьей доктора Дунаевской Н. В. работали литературный редактор Вера Васина , научный редактор Пётр Козлов и шеф-редактор Маргарита Тихонова

Определение болезни. Причины заболевания
При острой форме остеомиелита в области повреждённого зуба возникает боль, которая усиливается при надавливании на челюсть. Наблюдается выраженный отёк, покраснение и припухлость, лицо становится несимметричным. Пациент жалуется на головные боли и общую слабость, температура тела повышается до 39 °C.
![Остеомилеит челюсти [19]](https://probolezny.ru/media/bolezny/osteomielit-chelyusti/osteomileit-chelyusti-19_s.jpg)
Распространённость
Острым и хроническим остеомиелитом болеют люди всех возрастов и обоих полов. Однако чаще заболевание встречается у мужчин, потому что они, как правило, несвоевременно обращаются за медицинской помощью [8] . Средний возраст пациентов составляет 39 лет [7] .
Выделяют следующие виды остеомиелита челюсти:
- Одонтогенные — развиваются из-за инфекции в зубе и составляют 74,2 % от всех случаев остеомиелита [18] .
- Травматические — возникают после травмы, например при переломе челюсти. Зачастую заболевание развивается, когда пациент обращается в больницу только на 7–10-й день после повреждения [5] .
- Гематогенные — инфекция попадает с током крови из какого-либо органа. Встречаются при хронических и острых инфекциях: скарлатине, дифтерии и хроническом тонзиллите.
Согласно статистике, 15 % больных остеомиелитом поступают в отделение в состоянии алкогольного опьянения и при опросе указывают на частый приём алкогольных напитков, 13 % сейчас или в прошлом употребляли наркотики, следовательно страдают иммунодефицитами.
У 45,7 % больных остеомиелитом, поступивших в стационар, выявлено обострение хронического процесса и нагноение мягких тканей, из которых 47,6 % случаев составляют флегмоны, а 52,4 % — абсцессы.
У 13 % пациентов с остеомиелитом челюсти выявляются гепатиты В и С, а у 2 % — ВИЧ-инфекция [5] .
Причины остеомиелита челюсти
- Позднее обращение к стоматологу — зуб долго болел, но дискомфорт подавлялся домашними методами лечения, например полосканиями с содой и солью.
- Хронические инфекционные и вирусные болезни: тонзиллит, синусит, гайморит и ангина.
- Инъекции или переливание крови, при которых инфекция может попасть в кровоток. В стоматологии часто применяют плазмолифтинг — в область слизистой оболочки дёсен инъекционно вводят обогащённую тромбоцитами плазму собственной крови пациента. При нарушении правил безопасности микробы могут попасть в кровоток.
- Травматизм, частые переломы и ранения.
- Туберкулёз и сифилис суставов.
- Аллергия.
- Иммунодефицит на фоне заболеваний или длительного приёма некоторых препаратов, например при химиотерапии.
- Стрессы, физическое и нервное истощение. При длительном стрессе нарушаются защитные функции организма и человек становится восприимчивым к инфекциям [17] .
- В очень редких случаях — нарушение функции височно-нижнечелюстного сустава.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы остеомиелита челюсти
Симптомы зависят от типа остеомиелита, течения болезни и степени поражения тканей.
Симптомы острой формы остеомиелита подразделяются на два вида:
После острой стадии наступает подострая. На десне образуется гнойничок или свищ, через который гнойные выделения и воспалительная жидкость выходят наружу.
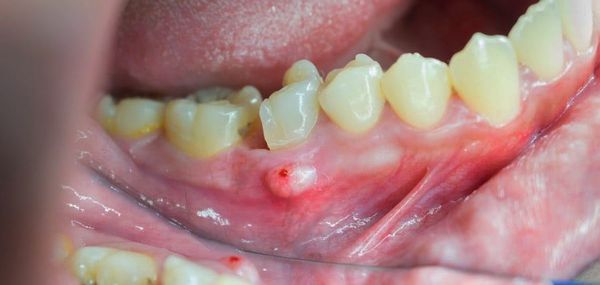
Затем боль утихает, но очаг инфекции остаётся, поэтому сохраняется высокая температура и нарастает слабость. Если в этот период не обратиться к врачу, то инфекция распространится по всему организму и человек может погибнуть.
Хроническая форма длится от нескольких месяцев до нескольких лет. Описанные выше симптомы то появляются, то стихают или даже полностью исчезают. При длительном течении болезни зубы становятся подвижными, челюсть утолщается и могут измениться контуры лица.
Как правило, при хроническом остеомиелите пациенты не обращают внимания на болезненные симптомы, а повышение температуры и слабость связывают с простудными заболеваниями [4] .
Патогенез остеомиелита челюсти
Выделяют три теории происхождения остеомиелита:
- Инфекционно-эмболическая теория. Основоположники этой теории считали, что костная ткань воспаляется из-за нарушения кровоснабжения. Инфекция оседает в кровеносных сосудах и закупоривает мелкие капилляры. В результате этого питательные вещества и кислород не поступают к кости, возникает гнойное воспаление и некроз. Данная теория признана некорректной после того, как было подробно исследовано строение кровеносной системы, костей и окружающих тканей [7] .
- Нервно-трофическая теория. Её приверженцы полагают, что остеомиелит развивается при обострениях болезней зубов, например при периодонтите. Также к болезни приводят нарушения в работе иммунной системы. При частых обострениях заболеваний зубов наступает сенсибилизация — иммунные клетки перестают распознавать инфекцию и развивается гнойно-некротический процесс.
- Гематогенная теория. Первоначально воспаление развивается в костном мозге и проявляется отёком и покраснением кожи. Из-за отёка увеличивается внутрикостное давление и, как следствие, сдавливаются сосуды в костном канале. Это приводит к закупорке сосудов и развитию гнойно-некротического процесса [13][14][15] .
Остальные причины — травмы, аллергия, стрессы, нарушение функции височно-нижнечелюстного сустава — провоцируют развитие остеомиелита без хронического воспаления в зубе. Такой остеомиелит можно отнести к неодонтогенному: травматическому и аллергическому. Но и в этом случае заболевание развивается на фоне нарушенного движения крови по сосудам, ухудшения её свёртываемости и гнойно-некротических процессов.
Классификация и стадии развития остеомиелита челюсти
Остеомиелит классифицируют в зависимости от распространённости, источника инфицирования и рентгенологических признаков.
Виды остеомиелита челюсти
Отдельно выделяют нетипичный остеомиелит челюсти, когда процесс протекает бессимптомно: температура тела не повышается, костная ткань разрушается незначительно, свищи не образуются. Такую форму называют первично-хроническим остеомиелитом [7] [8] .
Стадии остеомиелита челюстей
- Острая — длится 14 суток.
- Подострая — наступает на 15–20-е сутки.
- Хроническая — от 30 суток до нескольких лет.
- Обострение хронического остеомиелита [8] .
Осложнения остеомиелита челюсти
Среди осложнений остеомиелита можно выделить местные и общие. Местные возникают непосредственно в полости рта, а общие затрагивают весь организм. Общие осложнения приводят к тяжёлым последствиям, долго лечатся и иногда заканчиваются гибелью пациента.
Местные осложнения:
- разрушение кости;
- выпадение зубов из-за увеличения их подвижности;
- хроническое воспаление в полости рта;
- появление кист внутри челюсти, что характерно для острой фазы заболевания;
- контрактура височно-нижнечелюстного сустава — состояние, при котором сложно или невозможно открыть рот; ;
- флегмона — разлитое гнойное воспаление мягких тканей;
- лимфаденит — множественное увеличение лимфатических узлов [4][9] .
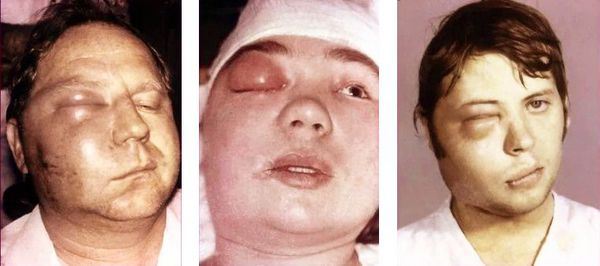
Общие осложнения:
Диагностика остеомиелита челюсти
Диагностика заболевания включает:
- сбор жалоб;
- визуальный осмотр;
- лабораторные исследования;
- инструментальные методы.
Сбор жалоб
- спрашивает о недавних травмах челюстно-лицевой области;
- выясняет, есть ли общие соматические заболевания, например сахарный диабет, болезни мочеполовой системы и желчнокаменная болезнь;
- уточняет, когда возникли симптомы, проявились ли они впервые или уже были раньше;
- узнаёт, как давно пациент посещал стоматолога.
Осмотр
Врач обращает внимание на бледность кожи и асимметричность лица, вызванную отёком мягких тканей. При ощупывании выявляется, что регионарные лимфатические узлы с поражённой стороны увеличены и болезненны. Пациент с трудом открывает рот, язык обложен налётом, изо рта исходит неприятный запах [7] .
При осмотре полости рта заметны покраснение и отёк слизистой оболочки в области больного зуба и близлежащих тканей. Зуб разрушен, подвижен при пальпации, боль усиливается при постукивании по нему. Подвижными и болезненными также могут быть несколько неповреждённых зубов в зоне поражения.
Лабораторные исследования
- Общий анализ крови. На активный воспалительный процесс указывают:
- повышение СОЭ до 40–70 мм/ч;
- лейкоцитоз, сдвиг лейкоцитарной формулы влево;
- положительная проба на С-реактивный белок;
- уменьшение альбуминов и повышение глобулинов;
- рост показателей активности щелочной и кислой фосфатазы.
- Биохимический анализ крови — позволяет исключить сахарный диабет и оценить функции почек и печени.
- Общий анализ мочи — при остеомиелите в ней появляется белок, клетки крови, гиалиновые и зернистые цилиндры.
Инструментальные методы диагностики
Компьютерная томография (КТ) — самый информативный метод диагностики остеомиелита челюсти. Это 3D-исследование, которое позволяет определить очаг инфекции и степень выраженности воспаления, его длительность и характер. С помощью КТ можно выявить не только крупные, но и мелкие образования, единичные и групповые, а также проанализировать, насколько далеко распространилась инфекция.

В некоторых случаях в свищевой ход вводят контрастное вещество. Такой метод исследования с контрастом называется фистулографией [9] [10] .
Рентгенография в первую неделю, как правило, не выявляет изменения в кости — в этот период воспалена только верхушка корня зуба. К концу второй недели кость разрушается и становится прозрачнее.
Дифференциальная диагностика
- между видами остеомиелита: одонтогенным, травматическим и гематогенным;
- острым периоститом;
- добро- и злокачественными новообразованиями;
- поражением полости рта специфическими инфекционными заболеваниями: туберкулёзом, сифилисом, актиномикозом.
Лечение остеомиелита челюсти
Лечение проводится только в стационаре под наблюдением врача и может быть медикаментозным и хирургическим [9] . По отдельности эти методы мало результативны и даже могут навредить пациенту. Схемы лечения зависят от стадии заболевания.
Лечение острого и подострого остеомиелита
При первом посещении срочно удаляют запущенный повреждённый зуб. Затем полость рта тщательно промывают антибиотиками. Это необходимо сделать, чтобы убрать из раны микробов и гной.
В следующие дни рану обрабатывают дезинфицирующими средствами и вводят инъекции противомикробных препаратов. С их помощью удаётся воздействовать непосредственно на очаг инфекции и не дать ей распространиться. В дополнение к основному лечению применяют питательные составы с витаминами С и группы В.
На подострой стадии болезни важно сдержать распространение инфекции и не дать воспалению перейти на окружающие ткани.
Для этого применяют:
- капельницы с антибиотиками;
- препараты, снижающие или подавляющие воспаление;
- резиновый дренаж для оттока экссудата.
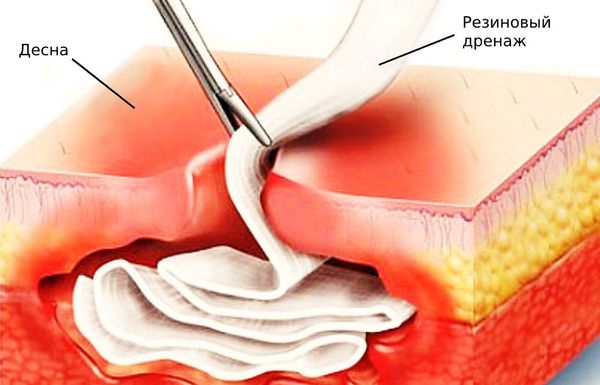
Также в кровоток вводят витаминные комплексы и препараты, очищающие организм от микробов и продуктов их жизнедеятельности. Конкретные лекарства и дозировки подбирает лечащий врач.
Дополнительной терапией после основного лечения могут стать методы физиотерапии: УВЧ-терапия или лечение непостоянными токами. Считается, что они ускоряют процессы заживления [7] [16] .
Лечение хронического остеомиелита
При появлении некротизированных полостей с распадом кости и окружающих её тканей потребуется операция. Для этого повреждённую область рассекают, поражённые участки убирают и накладывают шину. В дальнейшем с помощью рентгенологических методов врач контролирует, как восстанавливается костная ткань [11] .
Чтобы помочь организму бороться с инфекцией, дополнительно принимают антибиотики в таблетках. Чаще всего назначают Метронидазол и усиливают его эффект препаратами из группы цефалоспоринов 3–4-го поколения.
Если состояние пациента не улучшается, то добавляют фторхинолоны или Рифампицин. Основная задача антибиотиков — не дать бактериям размножаться [7] . Лекарства помогают уменьшить воспаление и удержать патологический процесс в пределах поражённого участка.
Также ротовую полость ежедневно обрабатывают бактерицидными средствами, применяют капельницы с витаминами и плазмозамещающими жидкостями, которые очищают организм от токсинов.
Дополнительно рекомендовано полоскать рот настоями ромашки, зверобоя, мяты и окопника. Фитосредства уменьшают воспаление, ускоряют выздоровление и практически не имеют побочных эффектов.
Прогноз. Профилактика
Если пациент при первых признаках остеомиелита обращается к врачу, то прогноз благоприятный. Если же болезнь запущена, то делать какие-либо выводы сложно: неизвестно, хватит ли у организма сил для борьбы с инфекцией. В тяжёлых случаях могут развиться опасные осложнения, от которых человек может погибнуть [9] .
Самым непредсказуемым является гематогенный остеомиелит. Развитие всех других форм, как правило, можно предотвратить. Для этого достаточно придерживаться простых правил:
Остеомиелит – воспаление костного мозга, при котором обычно поражаются все элементы кости (надкостница, губчатое и компактное вещество). В зависимости от этиологии остеомиелита он подразделяется на неспецифический и специфический (туберкулезный, сифилитический, бруцеллезный и т. п.); посттравматический, гематогеный, послеоперационный, контактный. Клиническая картина зависит от вида остеомиелита и его формы (острая или хроническая). Основу лечения острого остеомиелита составляет вскрытие и санация всех гнойников, при хроническом остеомиелите - удаление полостей, свищей и секвестров.
МКБ-10


Общие сведения
Остеомиелит (от лат. osteon кость + myelos костный мозг + itis воспаление) – воспаление костного мозга, при котором обычно поражаются все элементы кости (надкостница, губчатое и компактное вещество). По статистике, остеомиелит после травм и операций составляет 6,5% всех болезней опорно-двигательного аппарата. Чаще поражает бедренную и плечевую кость, кости голени, позвонки, нижнечелюстные суставы и верхнюю челюсть. После открытых переломов диафиза трубчатых костей посттравматический остеомиелит возникает в 16,3% случаев. Мужчины болеют остеомиелитом чаще женщин, дети и пожилые – чаще людей молодого и среднего возраста.
Классификация
Выделяют неспецифический и специфический остеомиелит. Неспецифический остеомиелит вызывают гноеродные бактерии: золотистый стафилококк (90% случаев), стрептококк, кишечная палочка, реже – грибки. Специфический остеомиелит возникает при туберкулезе костей и суставов, бруцеллезе, сифилисе и т. д.
В зависимости от пути, которым микробы проникают в кость, различают эндогенный (гематогенный) и экзогенный остеомиелит. При гематогенном остеомиелите возбудители гнойной инфекции заносятся через кровь из удаленного очага (фурункул, панариций, абсцесс, флегмона, инфицированная рана или ссадина, тонзиллит, синусит, кариозные зубы и пр.). При экзогенном остеомиелите инфекция проникает в кость при ранении, операции или распространяется с окружающих органов и мягких тканей.
В начальных стадиях экзогенный и эндогенный остеомиелит различаются не только по происхождению, но и по проявлениям. Затем отличия сглаживаются и обе формы болезни протекают одинаково. Выделяют следующие формы экзогенного остеомиелита:
- посттравматический (после открытых переломов);
- огнестрельный (после огнестрельных переломов);
- послеоперационный (после проведения спиц или операций на костях);
- контактный (при переходе воспаления с окружающих тканей).
Как правило, остеомиелит вначале протекает остро. В благоприятных случаях заканчивается выздоровлением, в неблагоприятных – переходит в хронический. При атипичных формах остеомиелита (абсцессе Броди, альбуминозном остеомиелите Оллье, склерозирующем остеомиелите Гарре) и некоторых инфекционных болезнях (сифилисе, туберкулезе и др.) острая фаза воспаления отсутствует, процесс носит первично-хронический характер.
Острый остеомиелит
Проявления острого остеомиелита зависят от пути проникновения инфекции, общего состояния организма, обширности травматического поражения кости и окружающих мягких тканей. На рентгенограммах изменения видны спустя 2-3 недели с начала заболевания.
Гематогенный остеомиелит
Как правило, развивается в детском возрасте, причем треть пациентов заболевает в возрасте до 1 года. Достаточно редкие случаи развития гематогенного остеомиелита у взрослых на самом деле являются рецидивами болезни, перенесенной в детском возрасте. Чаще поражает большеберцовую и бедренную кости. Возможно множественное поражение костей.
Из удаленного очага воспаления (абсцесс мягких тканей, флегмона, инфицированная рана) микробы с кровью разносятся по организму. В длинных трубчатых костях, особенно – в их средней части хорошо развита широкая сеть сосудов, в которой скорость кровотока замедляется. Возбудители инфекции оседают в губчатом веществе кости. При неблагоприятных условиях (переохлаждение, снижение иммунитета) микробы начинают усиленно размножаться, развивается гематогенный остеомиелит. Выделяют три формы заболевания:
Септико-пиемическая форма. Характерно острое начало и выраженная интоксикация. Температура тела поднимается до 39—40°, сопровождается ознобом, головной болью и повторной рвотой. Возможны потеря сознания, бред, судороги, гемолитическая желтуха. Лицо больного бледное, губы и слизистые оболочки синюшны, кожа сухая. Пульс учащенный, давление снижено. Селезенка и печень увеличиваются, иногда развивается бронхопневмония.
На 1-2 сутки болезни появляется точно локализованная, резкая, сверлящая, распирающая или рвущая, усиливающаяся при малейших движениях боль в области поражения. Мягкие ткани конечности отечны, кожа горячая, красная, напряженная. При распространении на близлежащие суставы развивается гнойный артрит.
Через 1-2 недели в центре поражения формируется очаг флюктуации (жидкость в мягких тканях). Гной проникает в мышцы, образуется межмышечная флегмона. Если флегмону не вскрыть, она может вскрыться самостоятельно с образованием свища или прогрессировать, приводя к развитию параартикулярной флегмоны, вторичного гнойного артрита или сепсиса.
Местная форма. Общее состояние страдает меньше, иногда остается удовлетворительным. Преобладают признаки местного воспаления кости и мягких тканей.
Адинамическая (токсическая) форма. Встречается редко. Характеризуется молниеносным началом. Преобладают симптомы острого сепсиса: резкое повышение температуры, тяжелый токсикоз, судороги, потеря сознания, выраженное снижение артериального давления, острая сердечно-сосудистая недостаточность. Признаки костного воспаления слабые, появляются поздно, что затрудняет постановку диагноза и проведение лечения.
Посттравматический остеомиелит
Возникает при открытых переломах костей. Развитию болезни способствует загрязнение раны в момент травмы. Риск развития остеомиелита увеличивается при оскольчатых переломах, обширных повреждениях мягких тканей, тяжелых сопутствующих повреждениях, сосудистой недостаточности, снижении иммунитета.
Посттравматический остеомиелит поражает все отделы кости. При линейных переломах зона воспаления обычно ограничена местом перелома, при оскольчатых переломах гнойный процесс склонен к распространению. Сопровождается гектической лихорадкой, выраженной интоксикацией (слабость, разбитость, головная боль и т. д.), анемией, лейкоцитозом, повышением СОЭ. Ткани в области перелома отечны, гиперемированы, резко болезненны. Из раны выделяется большое количество гноя.

МРТ стопы. Остеомиелит таранной и большеберцовой кости с наличием обширной зоны деструкции костной ткани.
Огнестрельный остеомиелит
Чаще возникает при обширных поражениях костей и мягких тканей. Развитию остеомиелита способствует психологический стресс, снижение сопротивляемости организма и недостаточная обработка раны.
Общие симптомы сходны с посттравматическим остеомиелитом. Местная симптоматика при остром огнестрельном остеомиелите нередко выражена слабо. Отек конечности умеренный, обильное гнойное отделяемое отсутствует. О развитии остеомиелита свидетельствует изменение раневой поверхности, которая становится тусклой и покрывается серым налетом. В последующем воспаление распространяется на все слои кости.
Несмотря на наличие очага инфекции, при огнестрельном остеомиелите обычно наступает сращение кости (исключение – значительная раздробленность кости, большое смещение отломков). При этом гнойные очаги оказываются в костной мозоли.
Послеоперационный остеомиелит
Является разновидностью посттравматического остеомиелита. Возникает после операций по остеосинтезу закрытых переломов, ортопедических операций, проведения спиц при наложении компрессионно-дистракционных аппаратов или наложении скелетного вытяжения (спицевой остеомиелит). Как правило, развитие остеомиелита вызвано несоблюдением правил асептики или большой травматичностью операции.
Контактный остеомиелит
Возникает при гнойных процессах окружающих кость мягких тканей. Особенно часто инфекция распространяется с мягких тканей на кость при панариции, абсцессах и флегмонах кисти, обширных ранах волосистой части головы. Сопровождается увеличением отека, усилением болей в области повреждения и образованием свищей.
Лечение
Только в стационаре в отделении травматологии. Выполняют иммобилизацию конечности. Проводят массивную антибиотикотерапию с учетом чувствительности микроорганизмов. Для уменьшения интоксикации, восполнения объема крови и улучшения местного кровообращения переливают плазму, гемодез, 10% раствор альбумина. При сепсисе применяют методы экстракорпоральной гемокоррекции: гемосорбцию и лимфосорбцию.
Обязательным условием успешного лечения острого остеомиелита является дренирование гнойного очага. На ранних стадиях в кости делают трепанационные отверстия с последующим промыванием растворами антибиотиков и протеолитических ферментов. При гнойных артритах выполняют повторные пункции сустава для удаления гноя и введения антибиотиков, в некоторых случаях показана артротомия. При распространении процесса на мягкие ткани образовавшиеся гнойники вскрывают с последующим открытым промыванием.
Хронический остеомиелит
При небольших очагах воспаления, комплексном и своевременном лечении, преимущественно у молодых пациентов восстановление костной ткани преобладает над ее разрушением. Очаги некроза полностью замещаются вновь образованной костью, наступает выздоровление. Если этого не произошло (примерно в 30% случаев), острый остеомиелит переходит в хроническую форму.
Примерно к 4 неделе при всех формах острого остеомиелита происходит секвестрация – образование омертвевшего участка кости, окруженного измененной костной тканью. На 2-3 месяц заболевания секвестры окончательно отделяются, на месте разрушения кости формируется полость и процесс становится хроническим.
Симптомы
При переходе острого остеомиелита в хронический состояние пациента улучшается. Боли уменьшаются, становятся ноющими. Формируются свищевые ходы, которые могут выглядеть, как сложная система каналов и выходить на поверхность кожи далеко от места повреждения. Из свищей выделяется умеренное количество гнойного отделяемого.
В период ремиссии состояние пациента удовлетворительное. Боли исчезают, отделяемое из свищей становится скудным. Иногда свищи закрываются. Продолжительность ремиссии при остеомиелите колеблется от нескольких недель до нескольких десятков лет, зависит от общего состояния и возраста больного, локализации очага и т. д.
Развитию рецидива способствуют сопутствующие заболевания, снижение иммунитета и закрытие свища, приводящее к скоплению гноя в образовавшейся костной полости. Рецидив болезни напоминает стертую картину острого остеомиелита, сопровождается гипертермией, общей интоксикацией, лейкоцитозом, повышением СОЭ. Конечность становится болезненной, горячей, краснеет и отекает. Состояние пациента улучшается после открытия свища или вскрытия гнойника.

КТ стопы. Посттравматический хронический остеомиелит пяточной кости с наличием секвестра (красная стрелка) и свищевого хода (синяя стрелка).
Осложнения
Хронический остеомиелит часто осложняется переломами, образованием ложных суставов, деформацией кости, контрактурами, гнойным артритом, малигнизацией (злокачественным перерождением тканей). Постоянно существующий очаг инфекции влияет на весь организм, вызывая амилоидоз почек и изменения внутренних органов. В период рецидива и при ослаблении организма возможен сепсис.
Диагностика
Постановка диагноза при хроническом остеомиелите в большинстве случаев не вызывает затруднений. Для подтверждения проводят МРТ, КТ или рентгенографию. Для выявления свищевых ходов и их связи с остеомиелитическим очагом выполняют фистулографию.
Лечение
Операция показана при наличии остеомиелитических полостей и язв, гнойных свищей, секвестров, ложных суставах, частых рецидивах с интоксикацией, выраженной болью и нарушением функции конечности, малигнизации, нарушении деятельности других органов и систем вследствие хронической гнойной инфекции.
Выполняют некрэктомию (секвестрэктомию) – удаление секвестров, грануляций, остеомиелитических полостей вместе с внутренними стенками и иссечение свищей с последующим промывным дренированием. После санации полостей проводят костную пластику.
4. Острый остеомиелит: клинический протокол/ Экспертная комиссия по вопросам развития здравоохранения - 2013
Гематогенный остеомиелит – это гнойное воспаление кости, возникающее в результате заноса микробов с током крови из гнойничков на коже, гнойных ран и воспалительных очагов в различных органах. В первые сутки преобладают симптомы общей интоксикации: высокая температура, тошнота, рвота, ознобы, слабость и головная боль. Затем возникают интенсивные боли и значительный отек конечности. В последующем гной проникает в мягкие ткани, образуя флегмону, и может прорываться через кожу с формированием свищей. Диагноз выставляется на основании симптомов и данных лабораторных исследований. Рентгенография информативна только с третьей недели болезни. Лечение – антибиотикотерапия, дезинтоксикационная терапия, вскрытие и дренирование гнойников.
МКБ-10
Общие сведения
Гематогенный остеомиелит (от лат. haematogenus происходящий из крови, osteon кость + myelos костный мозг + itis воспаление) – гнойный процесс в костной ткани, возникший в результате заноса инфекции через кровь. Этот вид остеомиелита является тяжелым заболеванием, поражающим преимущественно детей и подростков в возрасте от 7 до 15 лет. Могут страдать и дети младшей возрастной группы. У мальчиков встречается втрое чаще, чем у девочек. Взрослые заболевают очень редко. Начинается остро, но в последующем иногда переходит в хроническую форму и может тянуться в течение многих лет – этим обусловлено наличие определенного количества взрослых пациентов, страдающих гематогенным остеомиелитом. Гнойное воспаление может развиться в любой кости, но чаще поражаются длинные трубчатые кости (плечевая, бедренная, большеберцовая). Лечение гематогенного остеомиелита осуществляют травматологи-ортопеды.

Причины
Чаще всего возбудителем болезни становится золотистый стафилококк. Реже гематогенный остеомиелит вызывается пневмококком, стрептококком и кишечной палочкой. Началу заболевания предшествует бактериемия (наличие микробов в крови), которая может возникать из-за наличия крупных гнойных процессов, так и вследствие небольших очагов инфекции (фурункулы, нагноившиеся ссадины, гнойники в миндалинах при ангине, гной при остром отите). При этом специалисты в области травматологии отмечают, что остеомиелит может развиваться как на фоне существующей инфекции, так и спустя много месяцев или даже лет.
Предрасположенность детей к гематогенному остеомиелиту объясняется особенностями строения костей в детском возрасте. У детей метафиз имеет очень широкую разветвленную сеть сосудов с замедленным кровотоком, что обусловлено необходимостью поставлять большое количество питательных веществ в зону роста кости. Сосуды метафиза не сообщаются с сосудами эпифизарного хряща, поэтому многие артериолы слепо заканчиваются на границе метафиза и эпифиза, что создает благоприятные условия для задержки патогенных микроорганизмов. Попадая в эту зону, микробы создают очаги дремлющей инфекции, которая может активизироваться при ослаблении организма или незначительной травме.
Патогенез
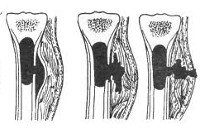
Вначале в толще костного мозга метафизарной зоны формируется небольшой гнойник. Поскольку устойчивость эпифизарного хряща к нагноению достаточно высока, гной распространяется в сторону диафиза, разрушая костный мозг и тем самым лишая кость питания изнутри. Через гаверсовы каналы гной проникает под надкостницу и отслаивает ее от кости, так кость лишается питания снаружи. Оставшаяся без питательных веществ кость разрушается, образуется участок остеонекроза.
Токсины из очага инфекции поступают в окружающие ткани и активно всасываются в кровь, что обуславливает развитие бурной интоксикации. А высокое давление гноя в полости, ограниченной костномозговым каналом, вызывает резкие, очень интенсивные боли. В последующем гной расплавляет надкостницу и проникает в мягкие ткани, вследствие чего формируется межмышечная флегмона. При прорыве флегмоны наружу образуется свищ на коже.
Симптомы гематогенного остеомиелита
Септико-пиемическая форма заболевания сопровождается выраженной интоксикацией и быстрым развитием местных изменений. Болезнь начинается с повышения температуры до 39-40 градусов. Состояние пациента тяжелое, характерны ознобы, повторная рвота и головные боли. Возможен бред и потеря сознания. Иногда выявляется гемолитическая желтуха. На вторые сутки появляются очень интенсивные, четко локализованные боли и быстро нарастающий отек мягких тканей. Конечность находится в вынужденном положении, движения невозможны из-за боли. Кожа над пораженной областью напряжена, отмечается местная гиперемия и гипертермия.
Гематогенный остеомиелит часто сочетается с артритом близлежащих суставов. По анализам выявляется метаболический ацидоз, гипонатриемия, гиперкальциемия и гиперкалиемия, а также циклические изменения свертывающей системы крови: вначале развивается гиперкоагуляция, в последующем – гипокоагуляция и фибринолиз. Нарушаются функции печени и почек. При развитии сепсиса формируются гнойные очаги в различных органах. Возможно множественное поражение костей, гнойный перикардит или гнойная деструктивная пневмония.
При местной форме гематогенного остеомиелита преобладает локальная симптоматика: боли, отек и гиперемия конечности. Общее состояние страдает меньше, чем при других формах, может незначительно ухудшаться, а иногда – даже оставаться удовлетворительным.
Токсическая (адинамическая) форма наблюдается достаточно редко. Характерно молниеносное развитие и очень тяжелое течение. В первые сутки возникает нарастающий токсикоз, сопровождающийся резким повышением температуры, появлением менингеальных симптомов, резким снижением артериального давления и развитием острой сердечно-сосудистой недостаточности. Наблюдаются судороги и потеря создания, сменяющиеся адинамией. Местная симптоматика на начальных стадиях слабо выражена, что существенно затрудняет постановку диагноза.
Диагностика
Диагноз гематогенный остеомиелит выставляется специалистом в сфере травматологии и ортопедии на основании клинической картины и данных лабораторных исследований, свидетельствующих об остром инфекционном процессе. При подозрении на нарушение работы внутренних органов и распространение инфекции назначаются консультации соответствующих специалистов: пульмонолога, гастроэнтеролога, нефролога. В зависимости от локализации выполняется рентгенография бедренной кости, рентгенография плечевой кости и т. д.
Рентгенологическое исследование повторяют в динамике, поскольку на начальных стадиях болезни изменения на рентгенограммах отсутствуют. Примерно спустя две недели от начала заболевания на снимках появляются признаки периостита, а несколько позже начинают выявляться признаки смазывания и разрежения губчатой кости в области метафиза. Через 2-4 месяца после появления первых симптомов на рентгенограммах обнаруживаются секвестры. Для уточнения расположения секвестров, свищевых ходов и полостей выполняется фистулография, радиотермия, МРТ кости и УЗИ пораженного сегмента.
Лечение гематогенного остеомиелита
Лечение проводится в условиях травматологического отделения. Для борьбы с инфекцией назначают внутримышечные и внутривенные инъекции полусинтетических пенициллинов, цефалоспоринов или линкомицина. В некоторых случаях раннее начало антибиотикотерапии позволяет остановить развитие воспалительного процесса и ликвидировать гнойный очаг до начала разрушения кости и образования секвестров. Одновременно проводится дезинтоксикационная терапия с использованием плазмы, кровезаменителей и кристаллоидных растворов. Назначаются препараты симптоматического действия.
Местное лечение включает в себя иммобилизацию пораженной конечности. При образовании гнойника в области метафиза или диафиза выполняют вскрытие, создавая фрезевые отверстия в кости, и осуществляют проточно-промывное дренирование. Межмышечные флегмоны широко вскрывают и дренируют. В полости гнойников, расположенных в кости и мягких тканях, вводят антибиотики. В послеоперационном периоде осуществляют антибиотикотерапию и дезинтоксикационную терапию. Иммобилизацию продолжают до полного купирования воспаления.
3. Современные представления о патологии и патанатомии гематогенного остеомиелита и их значение для клинической практики/ Григоровский В.В// Международный медицинский журнал - 2003 - №3
4. К вопросу о патогенезе острого и хронического остеомиелита у детей/ Горевой А.А.// Альманах клинической медицины - 2002 - №5

Сепсис и его последствия представляют собой континуум клинической и патологической степени тяжести. Континуум сепсиса имеет определенные фазы, которые характеризуют группы населения, подверженные риску заболеваемости и смертности. Важнейшим фактором, определяющим смертность, является не патоген, а степень и характер реакции хозяина. . Развитие синдрома полиорганной дисфункции при сепсисе является крайним в спектре и связано с высоким риском смерти.
Сепсис с острой дисфункцией органов (тяжелый сепсис) является результатом системного провоспалительного и прокоагулянтного ответа на инфекцию. Дисфункция органов у больного сепсисом связана с повышенной смертностью. Хотя большинство органов имеют дискретные анатомические границы и выполняют определенные функции, гематологическая система плохо очерчена и выполняет несколько несвязанных функций. Гематологические изменения присутствуют практически у каждого пациента с тяжелым сепсисом. Лейкоцитоз, анемия, тромбоцитопения, и активация каскада коагуляции являются наиболее распространенными нарушениями. Несмотря на теоретические преимущества использования гранулоцитарного колониестимулирующего фактора для улучшения функции лейкоцитов и / или количества циркулирующих веществ, крупные клинические испытания с этими факторами роста отсутствуют. Недавние исследования подтверждают снижение порога переливания эритроцитов и использование лечения эритропоэтином для снижения потребности в переливании крови. Лечение тромбоцитопении зависит от причины и клинического контекста, но может включать переливание тромбоцитов и прекращение приема гепарина или других подобных ему препаратов. Использование активированного белка С может обеспечить выживаемость у пациентов с тяжелым сепсисом. Иными словами гематологическая система не должна игнорироваться при оценке пациента с тяжелым сепсисом.
Ответ хозяина состоит из двух компонентов: неспецифического врожденного иммунного ответа и специфического или приобретенного иммунного ответа. Врожденный иммунный ответ (или острая фазовая реакция) является высоко эволюционно консервативным механизмом, который служит для борьбы с патогенными микроорганизмами, минимизирует повреждение тканей, способствует восстановлению хозяина и создает основу для приобретенного иммунного ответа. Врожденный иммунитет включает скоординированную активность как клеток, так и белков . Основными клеточными и растворимыми эффекторами являются моноциты / макрофаги и активированный комплемент соответственно; первичными коммуникаторами являются цитокины интерлейкин-1, интерлейкин-6 и фактор некроза опухоли альфа. Обычно врожденный иммунный ответ защищает хозяина от патогена и приводит к полному выздоровлению. Однако врожденный иммунный ответ может включать хозяина, что приводит к выраженной заболеваемости и смертности. Обсуждаемым в литературе вопросом является степень, в которой физиологические изменения врожденного иммунного ответа в любой момент времени в сепсисе являются адаптивными или патологическим для пациентов с сепсисом. Эта проблема важна, поскольку терапевтическая модуляция адаптивного ответа может оказывать вредное воздействие на пациентов.
Реакция на острую фазу (врожденный иммунитет) связана с несколькими изменениями в гематологической системе, включая воздействие на моноциты (активация коагуляции и воспаления, секвестрация железа), печень (высвобождение белков острой фазы), костный мозг (высвобождение и продуцирование). тромбоцитов и лейкоцитов (WBCs), почек (снижение выработки эритропоэтина ), эндотелия (проадгезивный и прокоагулянтный фенотип) и нейроэндокринной оси (выброс адреналина и глюкокортикоидов , в частности , кортизола).
Эритроциты
Индуцированные сепсисом изменения механических и мембранных свойств эритроцитов приводят к снижению деформируемости. Механизм неясен, но может включать повреждение мембран из-за активных форм кислорода, происходящих из циркулирующих лейкоцитов и ишемических тканей. Деформируемость эритроцитов является важной детерминантой кровотока, особенно в микроциркуляции. Действительно, снижение деформируемости приводит к увеличению времени прохождения и уменьшению потока. Эти изменения могут негативно повлиять на доставку кислорода в ткани и способствовать дисфункции органов.
Сепсис также связан с агрегацией эритроцитов. Важность этого явления в опосредовании фенотипа сепсиса неизвестна. Одним из проявлений этого процесса может быть повышенная скорость оседания эритроцитов.
Когда сепсис связан с повышенным разрушением эритроцитов, свободный гемоглобин может попасть в кровоток. В экспериментальных моделях было показано, что свободный гемоглобин увеличивает летальность при эндотоксемии с помощью механизма, который включает сенсибилизацию моноцитов и макрофагов, продуцирующих фактор некроза опухоли aльфа. Как часть реакции острой фазы, уровни гаптоглобина повышены. Гаптоглобин связывает свободный гемоглобин, защищая хозяина от вредного воздействия свободного гемоглобина.
Анемия часто встречается у критически больных пациентов с сепсисом или без него. В исследовании госпитализации отделения интенсивной терапии, в котором были исключены пациенты с терминальной стадией почечной недостаточности и первичным гематологическим заболеванием, средний уровень гемоглобина на момент поступления в отделение интенсивной терапии составил 12,1 г / дл, а у 77% пациентов была анемия во время их пребывания. В другом исследовании случаев госпитализации в стационар средний уровень гемоглобина у пациентов, поступивших в ОИТ, составил 11,3 г / дл, при этом у 29% уровень гемоглобина был ниже 10 г / дл. Влияние анемии отражается в высоких требованиях к переливанию крови у этой группы пациентов. В предыдущих исследованиях сообщалось, что критически больные пациенты получают в среднем 1 ед эритроцитов в день на пациента, что 16% пациентов в отделениях интенсивной терапии и 27% пациентов в отделениях интенсивной терапии получают переливания крови в любой день, и что от 37% до 60% всех пациентов, поступивших в отделение интенсивной терапии, получают как минимум 1 переливание.
Лейкоциты
У пациентов с сепсисом количество лейкоцитов в норме повышено (лейкоцитоз). Это наблюдение подтверждается на животных моделях сепсиса, в которых введение эндотоксина приводит к выраженному лейкоцитозу. Дифференциальное число лейкоцитов обычно показывает увеличение количества нейтрофилов (нейтрофилия). Иногда степень лейкоцитоза является экстремальной, с количеством лейкоцитов более 50 × 10 9 / л (лейкемоидная реакция). В некоторых случаях сепсис связан с уменьшением количества нейтрофилов (нейтропения), особенно в педиатрической популяции. А. Funke et.al. обнаружили, что 38% новорожденных с сепсисом имели нейтропению и что продолжительность нейтропении составляла менее 24 часов у 75% этих пациентов. Редко сепсис может привести к нейтропении или лейкемоидной реакции. Количество лейкоцитов может быть увеличено или уменьшено из-за основного заболевания, такого как рак и / или связанное лечение химиотерапией и кортикостероидами. Лейкоцитоз или лейкопения диагностируется на основании общего количества клеток крови. Современные автоматические счетчики клеток также обеспечивают точный дифференциал лейкоцитов. Проверка мазка периферической крови может показать токсические грануляции, вакуолизацию и / или присутствие телец Дёле в полиморфно-ядерных клетках. Лейкоцитоз и сдвиг влево, связанные с лейкемоидной реакцией, могут имитировать изменения хронической миелогенной лейкемии. Диагноз обычно очевиден в зависимости от клинического контекста. Однако в трудных случаях оценка щелочной фосфатазы лейкоцитов помогает дифференцировать 2 синдрома. Измерение щелочной фосфатазы лейкоцитов - это простой лабораторный тест, результаты которого повышены у пациентов с сепсисом и снижены у пациентов с хроническим миелогенным лейкозом.
Мобилизация резервов костного мозга может также привести к высвобождению увеличенного количества полос и / или более ранних миелоидных форм в периферической крови ("сдвиг влево"). Нейтропения может возникнуть в результате истощения предшественников костного мозга, задержки созревания в совершенном гранулоцитарном происхождении или дисбаланса между экстравазацией и продукцией. Развитие нейтропении связано с плохим прогнозом. Сепсис также связан с активацией циркулирующих моноцитов и нейтрофилов
Сепсис и реакция острой фазы приводят к демаргинации нейтрофилов с поверхности эндотелия, высвобождению и увеличению продукции нейтрофилов и / или моноцитов из костного мозга и активации циркулирующих лейкоцитов. Морфология нейтрофилов может выявить токсические грануляции, вакуолизацию и / или присутствие телец Дёле. Активация моноцитов или нейтрофилов приводит к высвобождению большого количества медиаторов воспаления, повышенной экспрессии тканевого фактора, усилению взаимодействия с эндотелием и / или изменениям биомеханических свойств. При сепсисе могут фактически снижаться различные функции нейтрофилов, включая хемотаксис, фагоцитоз и выработку активных форм кислорода. Повышенная продукция и активация циркулирующих нейтрофилов и / или моноцитов являются важными компонентами ответа хозяина на инфекцию. Однако чрезмерные или длительные изменения количества или функции лейкоцитов могут быть вредными для пациента. Например, нейтропения увеличивает риск септической смерти, а лейкемоидные реакции могут увеличить вязкость крови. Кроме того, чрезмерное высвобождение цитокинов из циркулирующих моноцитов или активных форм кислорода из нейтрофилов также может способствовать прогредиентности тяжелого сепсиса.
Лечение
В течение последних нескольких лет терапевтический потенциал рекомбинантного гранулоцитарно-макрофагального колониестимулирующего фактора (GM-CSF) или гранулоцитарного колониестимулирующего фактора (G-CSF) изучался на животных моделях сепсиса и у пациентов, у которых сепсис с или без нейтропении. Из этих 2 факторов роста G-CSF, по-видимому, имеет наиболее благоприятный профиль риск-польза. Действительно, было показано, что G-CSF не только избирательно стимулирует выработку и функционирование нейтрофилов (следовательно, более эффективный клиренс патогенов), но также потенциально ослабляет вредные аспекты провоспалительного ответа при сепсисе. Как правило, G-CSF хорошо переносится; наиболее распространенной токсичностью является боль в костно-мышечной системе. Хотя представляется разумным рассмотреть возможность применения G-CSF у пациентов с тяжелым сепсисом, осложненным нейтропенией, в настоящее время нет доказательств того, что эта терапия улучшает результаты лечения пациентов. Кроме того, роль GM-CSF или G-CSF в лечении "ненейротропного" взрослого пациента с сепсисом еще предстоит установить.
Читайте также:

