Как лечить головной мозг при вич
Обновлено: 22.04.2024
ВИЧ — вирус иммунодефицита человека
КТ — компьютерная томография
МРТ — магнитно-резонансная томография
ПМЛ — прогрессирующая многоочаговая лейкоэнцефалопатия
ЦМВИ — цитомегаловирусная инфекция
Одним из самых тяжелых вторичных заболеваний, возникающих при ВИЧ-инфекции, является прогрессирующая многоочаговая лейкоэнцефалопатия (ПМЛ). Эту инфекцию вызывает полиомавирус JC. Возбудитель широко распространен: антитела к нему обнаруживаются у 80% людей, однако реактивация вируса и клинические проявления возникают только при выраженном снижении клеточного иммунитета. Как правило, симптомы ПМЛ появляются у больных с уровнем лимфоцитов CD4 менее 100 В 1 мкл, но отмечены случаи развития заболевания и при количестве CD4, превышающем 200 В 1 мкл. ПМЛ диагностируется примерно у 2—5% больных инфекцией, вызванной вирусом иммунодефицита человека (ВИЧ) [1].
Вирус JC инфицирует и разрушает олигодендроциты головного мозга, продуцирующие миелин. Это приводит к множественной демиелинизации в полушариях головного мозга, мозжечке и стволе мозга. Для клинической картины ПМЛ характерны когнитивные расстройства, снижение остроты зрения, афазия, атаксия, моно- и гемипарезы, эпилептиформные припадки, а также другие признаки очаговых поражений головного мозга. Болезнь медленно прогрессирует в течение нескольких недель и даже месяцев и, как правило, приводит к летальному исходу [1, 2].
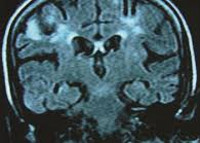
Прижизненная диагностика ПМЛ затруднена. Для заболевания не характерны изменения показателей периферической крови. При исследовании спинномозговой жидкости признаки воспаления отсутствуют, может отмечаться небольшое повышение уровня белка и двузначный цитоз. Возможно обнаружение JC-вируса в ликворе методом полимеразной цепной реакции. Однако чувствительность метода составляет около 80%, специфичность 90—99% [3]. Для установления диагноза наибольшее значение имеют лучевые методы исследования головного мозга, предпочтение отдается магнитно-резонансной томографии (МРТ), так как при компьютерной томографии (КТ) очаги пониженной плотности плохо визуализируются. Изменения на магнитно-резонансной томограмме при ПМЛ всегда начинаются с небольшого, единичного очага демиелинизации, постепенно приобретая картину многоочагового поражения мозга. Очаги могут располагаться в любой части головного мозга, как правило, они асимметричны [4].
Специфическое лечение ПМЛ с доказанной эффективностью в настоящее время отсутствует. Пока антиретровирусная терапия (АРВТ) является основным методом лечения ПМЛ при ВИЧ-инфекции. Но даже на фоне АРВТ прогноз у пациентов с развившейся клинической симптоматикой ПМЛ неблагоприятный. Средняя продолжительность жизни составляет 1—6 мес, крайне редко отмечаются случаи стабилизации и улучшения состояния больных на протяжении более 2 лет [5].
В виду трудности диагностики и лечения ВИЧ-инфицированных пациентов с ПМЛ, высокой летальности, наличия реальной возможности стабилизации их состояния представляем наш положительный опыт лечения ВИЧ-инфицированной пациентки с установленным диагнозом ПМЛ.
Пациентка Д., 33 года, поступила 20.06.14 в ГБУЗ ИКБ № 2 ДЗМ (ИКБ № 2) в профильное отделение для больных ВИЧ-инфекцией переводом из Научно-исследовательского института скорой помощи им. Н.В. Склифосовского (НИИ им. Н.В. Склифосовского) в тяжелом состоянии с направительным диагнозом: очаговые поражения головного мозга. ВИЧ-инфекция, стадия вторичных заболеваний. При поступлении уровень сознания — оглушение, выраженные нарушения когнитивных функций, выраженная дизартрия, тетрапарез.
23.06 состояние пациентки ухудшилось: в речевой контакт практически не вступала, стала заторможена, пассивно лежала в кровати, уровень сознания — оглушение. Больная переведена в отделение интенсивной терапии (ОИТ) для больных ВИЧ-инфекцией. Количество лимфоцитов CD4 339 в 1 мкл (20%), нагрузка ВИЧ в крови 160 761 копий/мл. В крови методом полимеразной цепной реакции обнаружена ДНК цитомегаловируса (ЦМВ) — 93 копий/мл. В ликворе зафиксирован подъем уровня белка до 0,69 г/л, цитоз до 5 лейкоцитов в 1 мкл, в мазке из 10 клеток все лимфоциты. В анализе ликвора на оппортунистические инфекции методом ПЦР обнаружена ДНК JC-вируса. Другие инфекции (ДНК ЦМВ, ДНК вируса Эпштейна—Барр, ДНК вируса герпеса VI типа, ДНК вируса простого герпеса I и II типа, ДНК Candida albicans, glabrata, krusei, parapsilosis, tropiccalis, ДНК Varicellae zoster virus, ДНК Toxoplasma gondii, ДНК Cryptococcus neoformans, Mycobacterium tuberculosis complex) не обнаружены. РНК ВИЧ в ликворе 341 копия в 1 мл.
Пациентка находилась в ОИТ с 23.06 по 10.09.14, где проводилась внутривенная дезинтоксикационная, антибактериальная, противоотечная, фунгицидная, седативная терапия, бисептол, цимевен, с последующим переходом на вальцит. Начата АРВТ по схеме: лопинавир/ритонавир, зидовудин и ламивудин в стандартных дозировках. Затем в связи с развитием цитопении (анемия, лейкопения) зидовудин заменен абакавиром.
У пациентки восстановилось сознание, она стала контактна, адекватна, ориентирована, критична. Дизартрия незначительная. По остальным органам и системам без динамики. К моменту выписки клинически значимых изменений в общем и биохимическом анализах крови не отмечалось. На фоне АРВТ нагрузка ВИЧ в крови снизилась до 709 копий в 1 мл, однако уровень лимфоцитов CD4 составлял 163 в 1 мкл (19%). После курса лечения цимевеном ДНК ЦМВ в клетках крови не обнаружена. В ликворе положительная динамика в виде снижения цитоза до 1 клетки в 1 мкл, снижения уровня белка с 0,69 до 0,55 г/л, РНК ВИЧ 20 копий в 1 мл. При последующих исследованиях ликвора ДНК JC-вируса обнаружить не удавалось. На повторном снимке МРТ головного мозга отмечалась отрицательная динамика в виде увеличения зоны патологических изменений с распространением диффузного билатерального симметричного поражения средних ножек мозжечка, определения патологической зоны в правой ножке мозга.
По настоятельной просьбе родственников пациентка выписана на амбулаторное лечение с диагнозом: ВИЧ-инфекция, стадия 4 В, фаза прогрессирования вне АРВТ: прогрессирующая мультифокальная лейкоэнцефалопатия, клинически проявляющаяся цитомегаловирусная инфекция (ЦМВИ) с поражением центральной и периферической нервной системы. Снижение массы тела более 10%. Осложнения: анемия.
За период наблюдения пациентка дважды госпитализирована в ИКБ № 2 с 17.09 по 23.10 и с 05.05.15 по 25.07 в связи с различными нарушениями сознания (переставала вступать в контакт, появлялись словесные эмболы, страх смерти, эпизоды возбуждения, агрессии, инверсия сна, дизартрия). При обследовании в период госпитализаций данные, подтверждающих присоединение вторичных заболеваний, не выявлялись. В отделении проводилась инфузионная, противоотечная, противогрибковая, антибактериальная, противосудорожная, ноотропная терапия, по назначению психиатра получала галоперидол и циклодол. АРВТ по прежней схеме беспрерывно.
При МРТ головного мозга (от 05.07.15) картина очаговых и диффузных изменений вещества (в лобных долях интрасубкортикально очаги повышенного МР-сигнала без признаков перифокального отека до 0,4×0,3 см, в гемисферах мозжечка — диффузные зоны повышенного МР-сигнала без признаков перифокального отека).
В настоящее время пациентка наблюдается амбулаторно в КДО СПИД с диагнозом: ВИЧ-инфекция, стадия 4 В, фаза ремиссии на фоне АРВТ: прогрессирующая мультифокальная лейкоэнцефалопатия. В анамнезе клинически проявляющаяся ЦМВИ с поражением нервной системы. Сопутствующий диагноз: энцефалопатия сложного генеза. Психоорганический синдром в связи с ВИЧ-инфекцией.
Продолжает получать АРВТ по прежней схеме (лопинавир/ритонавир, абакавир и ламивудин), карбамазепин (финлепсин). Состояние стабильное, без ухудшений, выраженные когнитивные расстройства не наблюдаются, ограниченно себя обслуживает. Сохраняется вялый парапарез нижних конечностей. В показателях общего и биохимического анализов крови значительных отклонений нет. От 07.06.16: количество лимфоцитов СD4 1115 кл/мкл (26%), РНК ВИЧ в крови не определяется.
Данное клиническое наблюдение подтверждает сложность диагностики ПМЛ, в связи с отсутствием специфической симптоматики и необходимостью подтверждения диагноза дополнительными инструментальными и лабораторными методами, не всегда доступными в повседневной практике.
В связи с отсутствием специфической профилактики и этиотропного лечения ПМЛ, ВИЧ-инфицированным пациентам необходимо своевременное начало АРВТ. Несмотря на неблагоприятный прогноз заболевания, у пациентов, приверженных АРВТ, при иммунологической и вирусологической эффективности лечения возможно замедление развития ПМЛ, стабилизация состояния и сохранение качества жизни пациента.
Неврологические проявления ВИЧ-инфекции (нейроСПИД) — обобщенное клиническое понятие, включающее многообразные первичные и вторичные синдромы и заболевания нервной системы, обусловленные ВИЧ. Проявлениями нейроСПИДа могут выступать менингоэнцефалит, полиневропатия, энцефало- и миелопатия, оппортунистические нейроинфекции, опухоли ЦНС, церебральные сосудистые нарушения и т. п. Диагностируется нейроСПИД при сопоставлении результатов анализов на ВИЧ, данных неврологического осмотра, нейропсихологического тестирования, ликворологических и томографических исследований, ЭФИ нервно-мышечного аппарата. Лечение нейроСПИДа осуществляется в рамках терапии ВИЧ-инфекции с назначением специфической и симптоматической терапии имеющихся неврологических проявлений.
Общие сведения

Причины возникновения нейроСПИДа
Несмотря на общепризнанность нейротропности ВИЧ, конкретные патогенетические механизмы его воздействия на нервную систему (НС) до конца не ясны. Предполагается, что нейроСПИД обусловлен как прямым, так опосредованным воздействием вируса на НС. Прямое влияние связывают с тропностью ВИЧ к CD4-рецепторам, которые имеются не только в мембране лимфоцитов, но и в глиальных клетках мозговой ткани.
Опосредованное воздействие ВИЧ реализуется несколькими путями. Во-первых, это развитие оппортунистических инфекций и опухолевых процессов за счет резкого снижения иммунного статуса организма. Во-вторых, предполагают наличие аутоиммунных механизмов (например, в развитии асептического менингита и полиневропатии при нейроСПИДе), связанных с синтезом антител к нервным клеткам, имеющим встроенный ВИЧ-антиген. Существует также гипотеза о нейротоксическом действии продуцируемых ВИЧ химических веществ. Кроме того, развитие нейроСПИДа возможно вследствие повреждения эндотелия мозговых сосудов провоспалительными цитокинами, приводящего к расстройству микроциркуляции и гипоксии, обуславливающей гибель нейронов.
Следует отметить, что отсутствие полной ясности в этиопатогенезе ВИЧ-инфекции и нейроСПИДа в частности, наличие существенного количества ложноположительных реакций на ВИЧ при его лабораторной диагностике, а также сложности с выделением вируса привели к появлению среди медиков и специалистов в области иммунологии лиц, считающих неправомочным само понятие ВИЧ-инфекция. При этом сторонники ВИЧ-отрицания признают существование синдрома иммунодефицита как такового, но опасаются, что с введением понятий ВИЧ-инфекция и нейроСПИД под эти диагнозы массово попадают пациенты с различными другими заболеваниями.
Классификация нейроСПИДа
В соответствии с прямым или опосредованным воздействием ВИЧ на нервную систему принято различать первичный и вторичный нейроСПИД. К базовым клиническим формам, которые включает первичный нейроСПИД, относят: острый асептический менингит, ВИЧ-энцефалопатию (СПИД-деменцию), ВИЧ-миелопатию (вакуолярную миелопатию), васкулярный нейроСПИД, поражения периферической НС (дистальная симметричная невропатия, синдром Гийена-Барре, множественная мононевропатия, хроническая воспалительная демиелинизирующая полинейропатия, синдром конского хвоста), поражение мышц (миопатии).
Вторичный нейроСПИД включает оппортунистические нейроинфекции и опухоли. Первые отличаются большим многообразием: церебральный токсоплазмоз, криптококковый менингит, герпесвирусная нейроинфекция (опоясывающий герпес, цитомегаловирусный и герпесвирусный энцефалиты, цитомегаловирусная полирадикулопатия, герпесвирусный миелит и ганглионевриты), прогрессирующая мультифокальная лейкоэнцефалопатия, туберкулезные поражения НС, нейросифилис. Наиболее часто встречающимися опухолями центральной НС при нейроСПИДе являются: первичная лимфома головного мозга, лимфома Беркитта, глионейробластома, диссеминированная саркома Капоши.
Симптомы нейроСПИДа
Первичный нейроСПИД зачастую имеет бессимптомное субклиническое течение. В 10-20% случаев неврологические симптомы дебютируют в первые 2-6 недель от заражения ВИЧ (период сероконверсии). В этот период на фоне фебрилитета, лимфаденопатии и кожных высыпаний у части пациентов манифестируют признаки асептического менингита и острой радикулоневропатии. Другие клинические формы первичного нейроСПИДа (ВИЧ-энцефалопатия, ВИЧ-миелопатия) возникают преимущественно в развернутой стадии ВИЧ-инфекции на фоне системных проявлений и выраженной иммуносупрессии. Вторичный нейроСПИД развивается в фазе симптомной хронической ВИЧ-инфекции (стадия вторичных заболеваний), которая наступает в период от 2 до 15 лет с момента первых клинических проявлений. Отдельные неврологические симптомы (головная боль, полиневропатия, нарушения сна, астения, депрессия, миопатия) могут быть вызваны токсичной антиретровирусной терапией.
Острая радикулоневропатия связана с острой воспалительной демиелинизацией корешков спинномозговых и черепных нервов. Характерны вялый тетрапарез, полиневритический тип нарушений чувствительности, корешковый синдром, поражение лицевого (реже глазодвигательного) нервов, бульбарные расстройства. Фаза нарастания симптомов может длиться от нескольких дней до месяца, затем после 2-4 недель стабильного состояния начинается регресс симптоматики. У 70% пациентов с этой формой нейроСПИДа отмечается полное восстановление, у 15% - выраженные остаточные парезы.
ВИЧ-энцефалопатия является самым частым проявлением первичного нейроСПИДа. Включает когнитивные, поведенческие и двигательные расстройства. Последние бывают представлены мозжечковой атаксией, тремором, пирамидной недостаточностью, вторичным паркинсонизмом, гиперкинезами. Отдельные симптомы и умеренный когнитивный дефицит отмечаются примерно у 75% пациентов со СПИДом. У 3-5% больных энцефалопатия выступает начальным синдромом нейроСПИДа. Морфологическим субстратом является мультифокальный гигантоклеточный энцефалит с поражением преимущественно лобных и височных долей, подкорковых структур, моста и мозжечка.
ВИЧ-миелопатия проявляется нижним спастическим парапарезом и тазовыми расстройствами. Отличается медленным течением и вариативностью тяжести клинических симптомов от легкого пареза до грубой плегии с недержанием мочи и кала. Это проявление нейроСПИДа отмечается у 20% пациентов с ВИЧ. Морфологически выявляется вакуолизация белого спинномозгового вещества, наиболее выраженная в грудных сегментах. Однако на МРТ позвоночника изменения зачастую не фиксируются.
Васкулярный нейроСПИД обусловлен васкулитом церебральных сосудов и зачастую приводит к развитию ишемического инсульта, отличительной чертой которого является волнообразное течение и частая трансформация в геморрагический инсульт. Характерны предшествующие инсульту ТИА, а также повторные инсульты, вследствие мультифокального поражения сосудов.
Диагностика нейроСПИДа
Учитывая частую встречаемость нейроСПИДа, консультация невролога рекомендована всем больным ВИЧ-инфекцией. В связи с тем, что первыми симптомами ВИЧ-энцефалопатии зачастую выступают когнитивные нарушения, исследование неврологического статуса целесообразно дополнять нейропсихологическим обследованием. Среди практических неврологов должна существовать определенная настороженность в отношении впервые обратившихся пациентов из групп риска, поскольку неврологические проявления у них могут являться симптомами первичного нейроСПИДа. В таких случаях следует обращать внимание на наличие у больного признаков иммуносупрессии и системных симптомов (снижения массы тела, лимфаденопатии, выпадения волос и т. п.).
Наряду с обязательными в диагностике ВИЧ-инфекции исследованиями крови путем ИФА, иммуноблоттинга и определения вирусной нагрузки при помощи ПЦР, в диагностике нейроСПИДа широко используются электрофизиологические, томографические и ликворологические методы. При необходимости проводятся консультации психиатра, нейрохирурга и др. специалистов. Диагностика и анализ результатов лечения поражений периферической НС при нейроСПИДе осуществляются преимущественно с помощью ЭФИ нервно-мышечной системы (ЭМГ, ЭНМГ, исследование ВП).
С целью диагностики поражений центральной НС при нейроСПИДе, для анализа их течения и эффективности проводимой терапии широко используются методы компьютерной томографии и магнитно-резонансной томографии. КТ головного мозга особенно информативна в диагностике вторичных объемных процессов церебральной локализации. МРТ головного мозга более эффективно визуализирует диффузные и мелкоочаговые изменения (участки атрофии и демиелинизации), расположенные в глубинных отделах мозга патологические очаги. Однако результаты аутопсии показывают, что современные методы нейровизуализации способны отображать не все морфологические изменения, происходящие в мозговой ткани при нейроСПИДе.
Немаловажное значение в диагностике нейроСПИДа имеет исследование цереброспинальной жидкости, полученной при люмбальной пункции. У серопозитивных пациентов даже при отсутствии неврологической симптоматики в ликворе зачастую наблюдается умеренный лимфоцитоз, повышение уровня белка и снижение концентрации глюкозы. При наличии неврологических проявлении эти изменения, наряду со снижением уровня CD4-лимфоцитов, говорят о возможном развитии нейроСПИДа. Иммунологические исследования ликвора, как правило, выявляют повышенное содержание IgG.
Лечение нейроСПИДа
Основу терапии и профилактики развития нейроСПИДа составляет лечение ВИЧ-инфекции. Эффективная антиретровирусная терапия (АРТ) фармпрепаратами, способными проходить через ГЭБ, позволяет блокировать репликацию ВИЧ, остановить нарастание иммунодефицита и таким образом уменьшить тяжесть клинических проявлений нейроСПИДа, снизить риск возникновения оппортунистических нейроинфекций и повысить эффективность их терапии. К наиболее апробированным средствам, применяемым при нейроСПИДе, относятся зидовудин, ставудин, абакавир. Учитывая токсичность большинства антиретровирусных препаратов, АРТ назначается по индивидуально подобранной схеме только при наличии показаний и с согласия пациента.
Параллельно с АРТ осуществляется специфическая и симптоматическая терапия возникшей клинической формы нейроСПИДа. Так, при ВИЧ-энцефалопатии применяют холина альфосцерат и мягкие ноотропы (мебикар, цитиколин, пирацетам, фенибут), при инсульте — антикоагулянты и пентоксифиллин, при полиневропатии — цитиколин, комбинированные препараты витаминов группы В, при острых психических нарушениях — антипсихотические средства (клозапин). При поражениях периферической НС отмечена эффективность плазмафереза. В лечении миопатий используют плазмаферез и кортикостероидную терапию.
При оппортунистических нейроинфекциях применяют этиотропные препараты: при криптококовых менингитах — фторцитозин с амфотерицином, токсоплазменных энцефалитах — кларитромицин, азитромицин, спирамицин, при герпетических поражениях — ацикловир, валацикловир, ганцикловир, абакавир, саквинавир. Лечение опухолей, возникающих как проявление вторичного нейроСПИДа, может потребовать хирургического вмешательства. Вопрос о необходимости операции рассматривается совместно с нейрохирургом.
Центральный НИИ эпидемиологии Роспотребнадзора, Москва
ГКУЗ ИКБ №2, Москва
Катамнез больных ВИЧ-инфекцией, перенесших церебральный токсоплазмоз
Журнал: Терапевтический архив. 2015;87(11): 42‑45
Центральный НИИ эпидемиологии Роспотребнадзора, Москва
Центральный НИИ эпидемиологии Роспотребнадзора, Москва
ГКУЗ ИКБ №2, Москва
Церебральный токсоплазмоз (ЦТ) — основная причина поражения центральной нервной системы у больных c инфекцией, вызванной вирусом иммунодефицита человека (ВИЧ). Для него свойственны высокая смертность, а также частое развитие рецидивов у выживших больных, что чаще связано с низкой мотивацией к лечению.
Материалы и методы
Результаты и обсуждение

Рис. 1. Исходы Ц.Т. у больных ВИЧ-инфекцией.
Больным с рецидивами этиотропное лечение начинали сразу после поступления, кроме одного больного, так как при госпитализации в клинической картине преобладали признаки выраженной анемии, и рецидив болезни не предполагался. Смерть больного наступила на 3-й день пребывания в стационаре, а патоморфологические проявления болезни оказались находкой патологоанатомов. Этот 30-летний пациент госпитализирован через 1,5 мес после перенесенного ЦТ с жалобами на слабость, повторные приступы потери сознания. Обращала внимание резкая бледность кожи, количество гемоглобина в крови составляло 20 г/л. Больной получал антиретровирусную терапию — АРВТ (эфавиренз в сочетании с комбинированным препаратом зидовудин + ламивудин), валганцикловир со времени первой госпитализации по поводу ЦТ и активной ЦМВ-инфекции, однако режим вторичной профилактики ЦТ не соблюдал. В отделении начато лечение анемии. Через 2 дня развился судорожный припадок с потерей сознания, нарушением деятельности сердечно-сосудистой системы и дыхания. Интенсивная терапия эффекта не дала, смерть наступила на 3-й день. Диагноз при вскрытии: токсоплазмоз головного мозга и сердца — множественные очаги некротического энцефалита и паренхиматозно-межуточного миокардита с поражением проводящей системы.
Из остальных 60 реконвалесцентов после выписки умерли еще 11. Из них 3 не закончили лечебный курс ЦТ, выписавшись из стационара по настоятельной просьбе и самостоятельно прервав лечение, — они умерли в результате прогрессирования ЦТ (по данным аутопсии). У 3 больных причиной смерти послужили прогрессирование ВИЧ-инфекции и развитие других вторичных заболеваний (генерализованный туберкулез, атипичный микобактериоз) через 0,5—3 года после выписки. У 5 больных смерть наступила через 1—5 лет после выписки, при этом причины смерти не связаны с ВИЧ-инфекцией (передозировка наркотиков, стафилококковый сепсис, острый панкреонекроз).

Рис. 2. Выживаемость больных ВИЧ-инфекцией после перенесенного ЦТ (кривая Каплана—Майера).
Заключение
Перенесшим ЦТ больным при диспансерном наблюдении нужно уделять более пристальное внимание в плане возможного развития рецидивов, особенно в течение первых 3 лет после выписки независимо от количества клеток CD4 + .
ВИЧ-деменция – стойкое прогрессирующее снижение интеллектуальных функций, развивающееся на фоне ВИЧ-инфекции. Проявляется триадой синдромов: интеллектуально-мнестическими нарушениями, изменениями поведенческих реакций, двигательными расстройствами. К основным симптомам относятся снижение динамики и целенаправленности познавательной деятельности, забывчивость, трудности концентрации внимания и абстрагирования. Диагностика включает беседу, неврологический осмотр, лабораторное, инструментальное и патопсихологическое обследование. Проводится противовирусная и симптоматическая медикаментозная терапия.
Общие сведения

Причины ВИЧ-деменции
ВИЧ-деменция – результат активности вируса иммунодефицита, JC вируса, вызывающего прогрессирующую мультифокальную лейкоэнцефалопатию, и некоторых других возбудителей, поражающих нервную систему при значительной иммуносупрессии. Точные причины энцефалопатии ВИЧ-инфицированных пациентов не выявлены, но определены факторы риска:
- Возраст. Деменция часто формируется у младенцев, рожденных от инфицированных матерей и перенесших интенсивную медикаментозную терапию. Другим возрастным пиком является пожилой и старческий период – после 55-60 лет вероятность слабоумия возрастает ежегодно.
- Отсутствие лечения. Пациенты, не получающие адекватную противовирусную терапию, наиболее подвержены энцефалопатии. Группу риска составляют жители стран с низким уровнем медицинской помощи и люди, добровольно отказывающиеся от своевременной диагностики и лечения инфекции ВИЧ.
- Токсическое поражение ЦНС. Слабоумие чаще развивается при наркотической и алкогольной зависимости. Осложнение возникает в результате поражения ЦНС токсинами.
Патогенез
ВИЧ обладает лимфо- и нейротропностью – поражает лимфоциты крови, ответственные за активность иммунной системы, а также определенные клетки нервной системы. Неврологическая симптоматика является наиболее ранней в клинической картине у 25% больных. При деменции определяется поврежденность астроцитов, эндотелиальных клеток сосудистых сплетений оболочек мозга и эпендимы желудочков. Наиболее отчетливые морфологические изменения обнаруживаются в субкортикальных структурах – белом веществе, подкорковых ядрах, зрительном бугре, стволе и в спинном мозге. Кора сохраняется относительно нетронутой. Вирусное поражение приводит к васкулиту головного и спинного мозга, воспалению мезенхимы нервной ткани, вторичной демиелинизации. Формируется картина рассеянного склероза, вакуольной миелопатии – возникает триада синдромов, включающая дефицит памяти и интеллекта, изменения поведения, двигательные расстройства.
Классификация
Классификация используется с целью определения стадии болезни, уточнения тактики лечения и составления прогноза. Основанием для различения видов ВИЧ-деменции является выраженность интеллектуальных, двигательных и поведенческих расстройств, способность пациента к выполнению ежедневных ритуалов, самообслуживанию. Выделяют шесть стадий болезни:
- Нулевая. Психические и двигательные функции в норме. Деменция отсутствует.
- Субклиническая. Отмечаются легкие когнитивные нарушения, замедленность двигательных актов. Больной может испытывать трудности при выполнении профессиональных задач. С повседневными бытовыми делами справляется самостоятельно.
- Легкая. Развивается замедленность психических функций, снижается концентрация и устойчивость внимания, с трудом запоминается объемный и слабоструктурированный материал, нарушается координация движений. Большинство бытовых навыков остаются сохранными, становятся недоступными действия, требующие точности движений, применения физической силы, высокого уровня интеллекта.
- Средней тяжести. Обнаруживается умеренный интеллектуально-мнестический дефект – больной не усваивает новый материал, неспособен самостоятельно действовать в незнакомой обстановке. Самостоятельно передвигается, справляется с простыми ежедневными ритуалами.
- Тяжелая. Формируются выраженные нарушения мышления, памяти, речи, движений. Затруднено общение с окружающими, ориентация в пространстве, координация. Ходьба возможна при помощи ходунков, поддержки со стороны. Пациент нуждается в уходе.
- Финальная. Определяются глубокие нарушения интеллекта, практически полное отсутствие двигательной активности. Больной не может принимать пищу, контролировать физиологические отправления, впадает в вегетативную кому.
Симптомы ВИЧ-деменции
В симптоматике доминируют признаки, характерные для субкортикальных деменций – снижение, колебания динамики психической деятельности и нарушения памяти. Пациенты становятся забывчивыми, медлительными, плохо концентрируются на выполнении сложных задач. Проявления нарастающего интеллектуально-мнестического дефицита на ранних стадиях замечаются у людей, занятых умственным трудом. У пожилых людей, детей раннего возраста когнитивное снижение часто выявляется на средних стадиях болезни.
В эмоциональной сфере нарастают симптомы апатии, депрессии. Больные становятся медлительными, социально отгороженными. Иногда развиваются атипичные аффективные реакции – психозы, истероподобные припадки. Поведение характеризуется стремлением к изоляции либо наоборот чрезмерной расторможенностью и дурашливостью. В двигательной сфере нарушения прогрессируют от мышечной слабости и снижения скорости движений в конечностях к частичному и полному параличу. У больных возникает тремор, походка становится неустойчивой и шаткой, движения дискоординированные, неуклюжие. Речь обедняется как результат интеллектуального снижения и дизартрии – нарушений смыслового и моторного компонента.
Осложнения
Отсутствие своевременного лечения ВИЧ-инфекции сопровождается быстрым нарастанием когнитивного дефицита и двигательных расстройств. На заключительной стадии развивается вегетативное состояние – частичный или полный паралич, неспособность есть, разговаривать, контролировать деятельность мочевого пузыря и кишечника. Исход прогрессирующей ВИЧ-энцефалопатии – кома, смерть. Выраженный иммунодефицит быстро завершается летальным исходом, деменция зачастую не успевает перейти в тяжелую и финальную стадии. При медленном течении болезни к стандартным проявлениям слабоумия присоединяются симптомы психоза – бред, галлюцинации, моторное возбуждение.
Диагностика
При диагностике ВИЧ-деменции врачи работают в нескольких направлениях: устанавливают наличие вируса (если диагноз отсутствует), определяют факт инфицирования ЦНС, чтобы исключить другие причины слабоумия, оценивают выраженность когнитивных, поведенческих, двигательных нарушений. Обследования проводятся врачом-инфекционистом, невропатологом, психиатром, клиническим психологом. Используются следующие методы:
- Беседа. Каждый специалист проводит опрос пациента и/или родственников, акцентируя внимание на специфических симптомах. Характерны жалобы на забывчивость, медлительность, трудности при письме, чтении, выполнении бытовых задач, апатию, социальную отгороженность.
- Осмотр. Неврологическое обследование направлено на выявление двигательных дисфункций. Обнаруживается тремор, нарушения координации и глазодвигательных функций, гипертонус мышц, генерализованная гиперрефлексия. Поздние стадии сопровождаются наличием очаговых симптомов, гиперкинезов.
- Лабораторные тесты. Наличие ВИЧ определяется по результатам иммуноферментных анализов и ПЦР. Инфицирование ЦНС подтверждается данными анализа спинномозговой жидкости, забор которой выполняется методом люмбальной пункции.
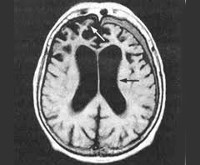
- Инструментальные исследования. Наиболее информативным методом, позволяющим определить факт поражения и структурные изменения ЦНС, является МРТ головного мозга (дополнительно назначается КТ и ПЭТ). Для поздних этапов болезни характерна диффузная гиперинтенсивность белого вещества, атрофия мозга, расширение желудочковой системы.
- Психодиагностика. Проводится патопсихологическое исследование когнитивной сферы. По итогам проб устанавливается снижение и неустойчивость динамики психомоторных процессов, недостаточность механической и смысловой памяти, функций активного внимания, преобладание конкретно-ситуационного типа мышления, недостаточная способность к абстрагированию.
Лечение ВИЧ-деменции
Терапия деменции основана на применении противовирусных препаратов с доказанной высокой эффективностью. По данным последних исследований, наиболее оправдано применение зидовудина – лекарственные средства на его основе препятствуют прогрессированию инфекционного процесса, тормозят развитие интеллектуального дефицита, а при раннем начале лечения отсрочивают развитие СПИД-энцефалопатии на период от 6 до 12 месяцев. Ограничением данного препарата является возникновение плохо переносимых побочных эффектов у ряда больных.
Относительное восстановление памяти и внимания происходит при последовательном или одновременном приеме зидовудина и диданозина. Положительный эффект становится заметен после 10-12 недель приема лекарств. К другим медикаментам с аналогичным действием относятся ламивудин, ставудин, залцитабин. Параллельно с противовирусной терапией проводится симптоматическое лечение деменции. Используются препараты, улучшающие мозговые функции (антагонисты NMDA-рецепторов), антидепрессанты, атипичные нейролептики.
Прогноз и профилактика
У ВИЧ-инфицированных пациентов с признаками деменции, не получающих лечения, прогноз неблагоприятный – высока вероятность летального исхода в течение года. При адекватной регулярной терапии процессы снижения познавательных функций и развития моторных нарушений замедляются, состояние больного стабилизируется, а в отдельных случаях наблюдается улучшение (регресс симптоматики). Снизить вероятность инфицирования клеток ЦНС при ВИЧ можно с помощью своевременной противовирусной терапии. Также существуют меры, позволяющие замедлить развитие деменции. Необходимо сохранять интеллектуальную, физическую и социальную активность. В режим дня нужно включить регулярные физические нагрузки, соответствующие уровню подготовленности, занятия творчеством, чтение научной и классической литературы с последующим обсуждением прочитанного.
Нейроинфекции – группа инфекционных патологий, которые вызываются бактериями, вирусами, грибками или простейшими, характеризуются преимущественной локализацией возбудителя в ЦНС и признаками поражения ее отделов. Клинические проявления представлены менингеальным, интоксикационным, ликвородинамическим синдромами, вегетососудистыми расстройствами. В процессе диагностики используются анамнестические данные, результаты физикального, общеклинического лабораторного, серологического, бактериологического или вирусологического исследования. В ходе лечения назначаются антибиотики или противовирусные препараты, патогенетические и симптоматические средства.
МКБ-10
Общие сведения
Нейроинфекции – сравнительно распространенная группа патологий. По данным статистики, инфекционные поражения ЦНС достигают 40% в структуре неврологической заболеваемости. Основную часть составляют бактериальные и вирусные менингиты, распространенность которых в различных географических регионах находится в пределах 5-12 случаев на 100 000 населения в год. Для большинства болезней, входящих в данную группу, характерна осенне-зимняя сезонность. Они могут встречаться среди всех возрастных категорий населения, но основную часть пациентов составляют дети до 10-12 лет и лица, не получившие вакцины согласно календарю прививок.

Причины нейроинфекций
Этиология инфекционного поражения структур центральной нервной системы зависит от вида заболевания. В большинстве эпизодов источником заражения становится больной или здоровый человек-носитель. Способствующими факторами являются постоянный контакт с большим количеством людей, ЧМТ, иммунодефицитные состояния, хронические соматические патологии, беспорядочная половая жизнь. Выделяют следующие механизмы инфицирования:
- Воздушно-капельный. Реализуется при кашле, чихании, разговоре. Характерен для возбудителей бактериальных и вирусных менингитов, энцефалитов, полиомиелита, герпетической инфекции.
- Контактно-бытовой. Подразумевает передачу инфекционного агента при прямом контакте с больным, носителем или инфицированными предметами быта. Это один из путей распространения герпес-вирусов, полиомиелита, сифилиса.
- Фекально-оральный. Тип передачи, при котором возбудитель выделяется вместе с испражнениями, проникает в организм с продуктами питаниями или водой. Может реализовываться при герпес-инфекции, вирусах ЕСНО и Коксаки, ботулизме, полиомиелите.
- Половой. При этом варианте заражение происходит во время полового акта через слизистые оболочки половых путей. Таким способом распространяется ВИЧ-инфекция, сифилис, реже – вирусы-возбудители менингитов, энцефалитов.
Патогенез
Для каждой формы нейроинфекции характерны свои патогенетические особенности, но механизмы развития большинства синдромов и симптомов, как правило, аналогичны при всех вариантах этой группы заболеваний. Инфекционный синдром обуславливают комплексы антиген-антитело и токсины возбудителей, которые оказывают деструктивное воздействие на ЦНС, провоцируя нарушения тонуса сосудов, метаболизма и гемодинамики в целом. Менингеальный синдром развивается при воспалительном поражении мозговых оболочек и повышении внутричерепного давления. Вегетативные расстройства вызываются как прямым контактом инфекционных агентов с центрами автономной нервной системы, так и опосредованным воздействием через внутричерепную гипертензию. Ликвородинамические изменения потенцируются усиленной продукцией спинномозговой жидкости на фоне раздражения сосудистых сплетений и блокадой пахионовых грануляций, усложняющей процесс ее резорбции.
Классификация
Использование систематизации обусловлено необходимостью объединить между собой большое количество разнородных инфекционных патологий с вовлечением нервной системы. В зависимости от характера морфологических изменений, клинических особенностей и конкретного возбудителя в неврологии различают несколько групп поражений ЦНС инфекционного происхождения. Основными вариантами нейроинфекций являются:
1. Энцефалиты. Заболевания с воспалением ткани головного мозга. Наиболее распространенными считаются клещевой, герпетический, ветряночный и краснушный энцефалиты. Проявления зависят от типа возбудителя, могут включать общемозговые, очаговые симптомы, системную интоксикацию разной степени выраженности.
2. Менингиты. Болезни, при которых наблюдается поражение мозговых оболочек. Характеризуются наличием менингеального и интоксикационного синдромов, с учетом особенностей воспалительного процесса подразделяются на:
- Гнойные. Провоцируются бактериями, простейшими или грибами, могут быть первичными либо вторичными. К первичным относятся менингиты, вызванные менингококком, пневмококками, гемофильной палочкой. Вторичные поражения являются осложнением гнойных процессов других локализаций – околоносовых пазух, среднего уха и пр.
- Серозные. Сопровождаются преимущественно лимфоцитарным плеоцитозом. В роли возбудителей выступают туберкулёзная палочка, вирус паротита, энтеровирусы Коксаки и ЕСНО.
3. Полиомиелит. Поражение ЦНС, вызванное РНК-содержащим вирусом полиомиелита. Может протекать в двух формах: непаралитической (менингеальной, абортивной, инаппарантной) и паралитической (спинальной, мостовой, бульбарной, энцефалитической).
4. Абсцесс головного мозга. Представляет собой ограниченное капсулой скопление гнойных масс в тканях мозга. Может иметь отогенное, риногенное, метастатическое или посттравматическое происхождение. Проявляется системной интоксикацией, очаговой неврологической симптоматикой, реже – эпилептическим и гипертензивным синдромами.
5. Опоясывающий лишай. Вариант хронической нейроинфекции, обусловленный герпесвирусом человека III типа – Варицелла-Зостер. Наблюдается персистенция возбудителя в спинномозговых ганглиях с активацией при снижении иммунитета или травмах. К основным симптомам относятся острая боль, герпетические высыпания в области 1-2 дерматомов.
6. Нейросифилис. Инфекционная патология, провоцируемая бледной трепонемой. На ранней стадии поражения ЦНС отмечаются общеинфекционные, общемозговые и очаговые симптомы с нарушением функций II, III, VI, VIII пар черепно-мозговых нервов. На поздних стадиях развивается прогрессирующая деменция, выявляются психические расстройства, инсультоподобная симптоматика.
7. Ботулизм. Инфекционное заболевание, вызываемое Clostridium botulinum и сопровождающееся прерыванием передачи нервных импульсов в холинэргических синапсах. Обнаруживаются признаки поражения двигательных ядер ствола мозга, передних рогов.
8. НейроСПИД. Обусловлено инфицированием вирусом иммунодефицита человека. Зачастую представлено первичными поражениями ЦНС: энцефалопатиями, рецидивирующими ВИЧ-менингитами, вакуолярной миелопатией. Проявления разнообразны, включают парезы, афазии, атаксию, мнестические расстройства, психопатологические нарушения.
Симптомы нейроинфекций
Менингальный синдром возникает при вовлечении в патологический процесс мозговых оболочек, состоит из общемозговой симптоматики, мышечно-тонических и корешковых симптомов. В первую группу входит интенсивная диффузная распирающая головная боль; фотофобия, повышенная чувствительность к звукам и свету, рвота без тошноты, не приносящая облегчения. Зачастую наблюдается нарушение сознания по типу галлюцинаций, бреда, оглушения, сопора. У детей возможны фебрильные судороги. Мышечно-тонические и радикулярные проявления включают в себя ригидность затылочных мышц, симптомы Кернига, Брудзинского, Лессажа, Гордона, Менделя, Бехтерева и др.
Вегетативно-сосудистые расстройства при нейроинфекциях могут носить симпатоадреналовый, вагоинсулярный или смешанный характер. В первом случае обнаруживается учащение сердечного ритма, повышение артериального давления, чрезмерная потливость и жажда, во втором – брадикардия, артериальная гипотония, обильное мочеиспускание. При смешанном варианте симптомы из разных групп сочетаются между собой. Нарушение нормальной циркуляции ликвора может протекать по гипертензивному и гипотензивному типу. Более характерной для нейроинфекций является внутричерепная гипертензия, сопровождающаяся угнетением сознания, судорожными и дислокационными синдромами.
Диагностика
Диагностическая программа при инфекциях ЦНС основывается на анамнезе, физикальном исследовании, общеклинических и специфических лабораторных тестах. Лучевые методы диагностики используются редко, зачастую – с целью дифференциации с объемными поражениями нервной системы. Программа обследования больного может включать следующие процедуры:
- Выяснение анамнеза. При общении с пациентом или его родственниками лечащий инфекционист или невролог осуществляет детализацию имеющихся жалоб, выясняет динамику их развития. Важную роль играет эпидемиологический анамнез – контакт с инфекционными больными или выезд за границу на протяжении последних 21 дней.
- Общий и неврологический статус. При осмотре врач определяет уровень сознания, изучает кожу и слизистые оболочки с целью поиска высыпаний, определяет частоту сердечных сокращений и артериальное давление. При установлении неврологического статуса специалист оценивает тонус затылочных мышц, выявляет специфические симптомы, характерные для различных неврологических синдромов.
- Общеклинические лабораторные тесты. В общем анализе крови помимо повышения СОЭ отмечаются следующие изменения: при бактериальной инфекции – высокий нейтрофильный лейкоцитоз, при вирусной – лейкоцитоз со смещением лейкоцитарной формулы вправо, при ВИЧ-инфекции и тяжелых иммунодефицитах – лейкопения. Показатели биохимического анализа крови зависят от сопутствующих поражений внутренних органов.
- Спинномозговая пункция. При нейроинфекциях существует два основных варианта изменений ликвора (белково-клеточных диссоциаций) – по гнойному и серозному типу. При первом типе СПЖ мутная, имеет определенный окрас (белый, желтоватый), наблюдается нейтрофильный плеоцитоз от 1 000, повышение уровня белка от 1,0 г/л. При серозной форме ликвор прозрачный, опалесцирует, при цитологическом исследовании обнаруживается лимфоцитарный плеоцитоз более 100, уровень белка составляет выше 0,4 г/л.
- Серологическое исследование. Заключается в определении повышенного уровня антител в крови при помощи реакций подавления гемагглютинации, связывания комплемента или нейтрализации. Применяется ИФА, в ходе которого выявляется специфический IgM к возбудителю. Проводится ПЦР для уточнения ДНК или РНК инфекционного агента.
- Вирусологическая или бактериологическая диагностика. Предполагает определение возбудителя заболевания в крови или спинномозговой жидкости пациента путем посева образцов на специфические питательные среды. После идентификации патогенного агента целесообразно уточнение чувствительности к основным антибактериальным препаратам.
Лечение нейроинфекций
Все нейроинфекции являются показанием к госпитализации больного в инфекционный или неврологический стационар. При тяжелом состоянии, необходимости непрерывного контроля жизненно важных функций (дыхание, сердцебиение), пациента транспортируют в отделение ОРИТ. Лечебная программа включает следующие мероприятия:
- Этиотропная терапия. Основной целью является элиминация возбудителя из организма больного. Вначале используются препараты широкого спектра действия. После получения результатов серологического и бактериологического исследований медикаменты заменяют антибактериальными или противовирусными средствами, к которым выявленный возбудитель проявил наибольшую чувствительность.
- Патогенетические препараты. Применяются для борьбы с системной интоксикацией, отеком головного мозга и нарушениями гомеостаза, для коррекции водно-электролитного баланса, десенсибилизации и стимуляции иммунитета. Назначаются плазмозаменители, диуретики, глюкокортикостероиды, антигистаминные средства, интерфероны, донорские и искусственные иммуноглобулины, антикоагулянты.
- Симптоматические средства. К этой категории относятся медикаменты, купирующие отдельные симптомы и улучшающие общее состояние больного: анальгетики, жаропонижающие, противорвотные медикаменты, антиконвульсанты, нейролептики.
- Хирургическое лечение. Характер оперативного вмешательства зависит от обнаруженных изменений. Операция может потребоваться в случае абсцесса, туберкуломы головного мозга, компрессии спинного мозга при туберкулезном спондилите, больших областях некроза при опоясывающем лишае.
Прогноз и профилактика
Исход нейроинфекции определяется типом заболевания, общим состоянием больного, своевременностью и полноценностью лечения. В большинстве случаев вовремя поставленный диагноз и адекватная терапия позволяют сохранить жизнь пациента, минимизировать риск развития осложнений. При некоторых формах нейроинфекций, например – энцефалитах, летальность достигает 50-80%. Специфическая профилактика представлена вакцинами против конкретных возбудителей: вирусов герпеса, ботулизма, клещевого энцефалита, кори, полиомиелита, менингококка и т. д. Неспецифические превентивные мероприятия направлены на укрепление иммунитета, своевременное лечение иммунодефицитных состояний и предотвращение контакта с потенциальными носителями инфекционных заболеваний.
1. Инфекционные поражения головного мозга: учебное пособие/ Гладкий П.А., Сергеева И.Г., Тулупов А.А. – 2015.
Читайте также:

