Как лечить стрептококк агалактия в моче у женщин
Обновлено: 23.04.2024
Высокая концентрация бактерии в анализе мочи свидетельствует о наличии стрептококковой инфекции. Возбудитель вызывает ряд серьезных заболеваний, затрагивающих многие органы или системы. Недуги, спровоцированные микроорганизмом, доставляют пациенту дискомфорт, могут угрожать его жизни.
Что такое стрептококк
Микроорганизмы семейства стрептококковых относятся к анаэробным бактериям, имеют шарообразную или яйцевидную форму, являются паразитами животных и человека. Бактерии размножаются и обитают в органах дыхания, желудочно-кишечном тракте, на кожных покровах, в мочеполовой системе. Большое количество стрептококков оседает в ротовой, носовой полости, горле, толстом кишечнике. Возбудитель встречается в уретре у мужчин, во влагалище у женщин. В природе стрептококки распространены на поверхности грибов, растений, в земле.
Стрептококковая бактерия относится к условно-патогенной микрофлоре, находится внутри человеческого организма постоянно. Микроорганизм не наносит вреда при небольшой концентрации, его количество контролируется иммунной системой. Когда защита организма ослабевает, стрептококки начинают активное размножение, выделяя токсины, отравляющие человека, приводящие к возникновению воспалений, инфекционных заболеваний.
Группы
Сегодня известно более 100 видов стрептококков, которые отличаются своей патогенностью. В зависимости от воздействия на эритроциты, выделяют 3 основные группы этих бактерий:
- Зеленящие или альфа-стрептококки – провоцируют неполный гемолиз.
- Бета-гемолитические стрептококки – вызывают полное разрушение эритроцитов, являются самыми опасными для человека.
- Гамма-стрептококки – негемолитические бактерии. Возбудители не вызывают разрушения красных кровяных телец.
Почему появляется стрептококк в моче
Норма содержания в моче стрептококков – 10 в 4 степени КОЕ/мл. Повышенная концентрация бактерии в урине возможна при наличии инфекции или некорректном заборе биоматериала. Патогенные возбудители начинают активно развиваться в период ослабления иммунитета, нахождения пациента в стрессовом состоянии или как сопутствующие заболевания. Колонии часто локализуются в кишечнике, горле или мочеполовой системе. Стрептококк может увеличить свою концентрацию в моче при заболеваниях мочевыводящих путей, возникающих как первичная инфекция или последствие других недугов.
Пути и условия инфицирования
Существует два условия, которые вызывают стрептококковые заболевания – ослабление иммунитета пациента, его непосредственный контакт с микроорганизмом. Различают аутоинфицирование (внутреннее) и инфицирование извне. Возбудитель может попасть внутрь организма следующими путями:
- Воздушно-капельным. Большую опасность для окружающих представляет больной, у которого инфекция локализована в дыхательных путях. Чихание и кашель – основные пути передачи стрептококка от человека к человеку.
- Воздушно-пылевым. Такой путь предполагает вдыхание патогенных микроорганизмов с подвешенными в воздухе частичками. Нахождение в запыленных помещениях существенно увеличивает риск заражения стрептококками.
- Контактно-бытовым. Инфицирование стрептококком происходит при использовании посуды, постельного белья, предметов личной гигиены совместно с заболевшим человеком. Вероятность заражения увеличивается при наличии травм кожных покровов, слизистых оболочек ротовой и носовой полости.
- Пищевым. Передача стрептококка осуществляется при употреблении зараженных продуктов.
- Половым. Проникновение возбудителя происходит при интимном контакте. Половой партнер может передать инфекцию, будучи носителем или больным. Стрептококк активно размножается во влагалище или уретре.
- Алиментарным (фекально-оральным). Заражение наступает при нарушении правил личной гигиены. Стрептококки попадают из прямой кишки на наружные половые органы.
- Медицинским. Возбудитель проникает внутрь организма при осмотре, стоматологическом, хирургическом вмешательстве, которые осуществляются с использованием инструментов, не прошедших дезинфекцию.
- Плацентарным. Передача стрептококка осуществляется от зараженной матери к ребенку.
Существует ряд патологических состояний, вызывающих активность стрептококков. Среди них выделяют ОРВИ, ВИЧ-инфекцию, туберкулез, сахарный диабет, тонзиллит, травмы слизистых оболочек горла, носа, мочеполовой системы, ротовой полости, переохлаждение организма, эндокринные нарушения. Помимо заболеваний специалисты определяют факторы, увеличивающие риск заражения:
- стрессы, постоянная усталость, нарушения сна;
- изменения гормонального баланса;
- вредные привычки (чрезмерное употребление алкоголя, наркотики, курение);
- ведение малоподвижного образа жизни;
- употребление вредной пищи, недостаток микроэлементов и витаминов в организме;
- трудовая деятельность в загрязненных помещениях, особенно без применения средств, защищающих дыхательные пути;
- осуществление процедур педикюра, маникюра, чистки кожи, пирсинга в салонах с сомнительной репутацией;
- злоупотребление антибиотиками, сосудосуживающими и другими медикаментозными препаратами.
Механизм воздействия на организм
Патологическое влияние на организм человека обусловлено свойством стрептококков производить в процессе своей жизнедеятельности токсины:
- эритрогенин – под его воздействием происходит расширение сосудов;
- стрептолизин – способствует разрушению сердечных тканей, клеток крови;
- ферменты (гиалуронидаза, амилаза, стрептокиназа, протеиназа) – помогают стрептококку быстро распространяться по организму;
- летальный токсин, некротоксин – вызывают омертвление тканей;
- лейкоцидин – наносит вред иммунитету, негативно воздействуя на лейкоциты.
Высокие показатели в моче стрептококка свидетельствуют о наличии заболеваний различных органов и систем. Возбудитель способен вызывать следующие патологии:
- ангину, скарлатину, тонзиллит, фарингит;
- уретрит, цервицит;
- бронхит, пневмонию;
- простатит, баланит;
- менингит;
- цистит;
- сепсис;
- пародонтит;
- пиелонефрит.
Симптомы появления повышенной концентрации стрептококка в моче
Наличие повышенного содержания бактерии в моче вызывает негативные проявления со стороны органов и систем. При заражении стрептококком характерны следующие симптомы:
- частые позывы к мочеиспусканию;
- повышение или снижение температуры тела;
- увеличение лимфоузлов в паховой области;
- сыпь в виде пятен на кожных покровах;
- болезненные ощущения, жжение при мочеиспускании;
- боль острого характера внизу живота;
- выделение мутной мочи;
- покраснение в местах поражения;
- боль в горле, глотке;
- образование белесого налета в виде хлопьев на слизистых щек, зеве, языке;
- тошнота, рвота;
- увеличение или снижение показателей артериального давления;
- боль ноющего характера в области поясницы.
У пациентов развивается аллергическая реакция на продукты жизнедеятельности возбудителя. Она проявляется пятнистой сыпью, которая покрывается желтыми корочками и содержит гной. Заражение стрептококком часто провоцирует аутоиммунные процессы, вызывающие разрушение суставов, сердца, почек. Нарушение функционирования фильтрующего органа приводит к увеличению уровня креатинина в крови больного.
При отсутствии своевременного лечения при инфицировании стрептококками может развиться эндометрит, уретрит, кандидоз влагалища, хроническое воспаление мочевого пузыря, предстательной железы. Из мочеиспускательного канала появляются гнойные выделения, пациенты испытывают сильные боли внизу живота, области поясницы, зуд, отечность. Аутоиммунное заболевание гломерулонефрит относится к поздним осложнениям инфекции, вызванной стрептококком. В почках происходит замещение здоровых тканей соединительной, нарушается работа органа.
У детей могут наблюдаться симптомы раннего и позднего инфицирования. В первом случае начало болезни приходится на первую неделю жизни малыша, может привести к пневмонии, сепсису, менингиту. Недуг сопровождается повышенной сонливостью, лихорадкой, проблемами с дыхательной системой. Позднее инфицирование образуется от 7 дней до 3 месяцев после появления ребенка на свет, провоцирует сепсис, менингит. Болезнь протекает с высокими показателями температуры тела, кашлем, заложенностью носа, сонливостью, судорогами, проблемами с приемом пищи.
Чем опасен стрептококк в моче при беременности
Если стрептококк агалактия в моче обнаруживается в гестационном периоде, женщине необходимо срочное лечение. При отсутствии своевременной терапии бактерия увеличивает риск возникновения патологических состояний матери и плода:
- преждевременного отхождения плодных оболочек, хориоамнионит;
- заболевания сепсисом, менингитом, пневмонией у новорожденного;
- преждевременных родов;
- внутриутробной гибели плода;
- появлением ребенка с детским церебральным параличом (ДЦП);
- проблем с обучением, слухом и других патологий у ребенка.
Диагностика
Мероприятия, предусмотренные для диагностики стрептококковой инфекции, разнятся в зависимости от локализации возбудителя. Предусмотрены следующие методы исследования:
- общий анализ мочи и крови;
- стрептотест;
- бактериологический посев биологического материала, взятого с зоны поражения (мокроты, мазков из ротоглотки, носа, уретры или влагалища, соскобы с поверхности кожи);
- биохимический анализ мочи, крови;
- рентгенография легких;
- ультразвуковое исследование (УЗИ) внутренних органов;
- электрокардиография.
Чтобы точно определить возбудителя, необходимо дополнительно проводить дифференциальную диагностику. Стрептококковую инфекцию нужно отличить:
- от недугов, имеющих схожую симптоматику (мононуклеоза, кори, дифтерии, краснухи, экземы, дерматитов);
- от инфекций, вызванных другими возбудителями (микоплазмой, стафилококком, трихомонадой, кандидами, уреаплазмой, хламидиями, гарднереллами).
Анализ мочи
Для определения стрептококковой инфекции мочевыводящих путей применяют бакпосев. Чтобы исследование было максимально точным и информативным, необходимо провести правильную подготовку к анализу, забор биоматериала. Надлежит соблюдать следующие рекомендации:
- Для забора мочи необходимо купить специальную стерильную емкость с плотно закручивающейся крышкой. Приобрести сосуд можно в аптеке.
- Чтобы микробы не проникли в анализ с рук, конечности следует хорошо вымыть и обработать антибактериальным гелем.
- Женщинам надлежит закрыть вход во влагалище, используя стерильный тампон, поскольку инфекция может попасть в пробу вместе с выделениями.
- Накануне исследования не рекомендуется есть морковь, свеклу или другие продукты, имеющие в составе яркие пигменты, которые изменяют цвет урины.
- При подготовке к анализу надлежит провести тщательную гигиену наружных половых органов.
- Без предварительного согласования с врачом запрещено принимать мочегонные или другие медикаменты, поскольку препараты могут исказить результаты посева.
- Активные занятия спортом требуется прекратить за 12–24 часа до начала исследования – физические нагрузки способствуют увеличению уровня белка в моче.
- Для анализа необходима первая утренняя урина. В таком биоматериале содержится максимальная концентрация бактерий. Потребуется не менее 70 мл образца.
- В контейнер надлежит собирать среднюю порцию мочи. Для этого необходимо спустить в унитаз начальную струю. Затем немного задержать процесс мочеиспускания, подставить емкость для образца. Собрав нужное количество урины, последнюю струю спустите в унитаз.
- Плотно закройте контейнер, обмойте, оботрите его, доставьте в лабораторию за 1,5–2 часа.
Лечение
При обнаружении в моче высокой концентрации стрептококков назначается комплексная терапия. Лечение ведется по следующим направлениям:
- антибактериальная терапия (предварительно проводится тест на чувствительность бактерий к разного вида препаратам);
- укрепление иммунной защиты организма;
- восстановление микрофлоры кишечника, нарушенной при приеме антибиотиков;
- детоксикационная терапия;
- симптоматическое лечение;
- назначение антигистаминных препаратов (необходимо детям, при наличии аллергии на антибиотики).
Каждое направление лечения предполагает применение медикаментозных средств. Используются следующие группы препаратов:
- антибактериальные лекарства для внутреннего применения (Пенициллин, Аугментин, Левофлоксацин, Цефтриаксон, Эритромицин);
- антибиотики местного воздействия (Биопарокс, Тонзилгон Н, Хлоргексидин);
- иммуномодулирующие средства (Иммунал, Имунорикс, Имудон, Лизобакт);
- пробиотики (Бифидумбактерин, Линекс, Бифиформ, Аципол);
- детоксикационные (Энтеросгель, Альбумин, Атоксил);
- антигистаминные (Супрастин, Кларитин, Цетрин);
- противовоспалительные (Парацетамол, Ибупрофен);
- сосудосуживающие (Фармазолин, Нокспрей);
- противорвотные (Церукал, Мотилиум).
Профилактика
Чтобы предотвратить появление streptococcus agalactiae в моче, необходимо соблюдать меры профилактики. Основные рекомендации специалистов:
- соблюдение правил личной гигиены;
- нормализация режима отдыха и труда;
- укрепление иммунной системы;
- проведение своевременной диагностики половых инфекций, их лечение;
- использование презерватива во время половых актов;
- исключение или сокращение стрессовых ситуаций.
Видео
Внимание! Информация, представленная в статье, носит ознакомительный характер. Материалы статьи не призывают к самостоятельному лечению. Только квалифицированный врач может поставить диагноз и дать рекомендации по лечению, исходя из индивидуальных особенностей конкретного пациента.
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: Трубачева Е.С., врач – клинический фармаколог
Темой сегодняшнего разговора будет группа зеленящих стрептококков – наименование не очень легитимное, но прочно вошедшее в практику, как и обзывательство антибактериальной терапии – антибиотикотерапией, а кто мы такие, чтобы отменять традиции.
Рассмотрим основных представителей семейства, на которых больше всего шансов наткнуться в антибиотикограммах.
- Streptococcussanguis – воистину могуч и вездесущ. Обнаруживается в зубных отложениях с самого прорезывания зубов и до конца жизни, где и есть основное место его обитания. Иногда может быть обнаружен на слизистой глотки и в фекалиях, куда попадают транзитом. При этом надо помнить, что этот микроб вносит существенный вклад в процессы, связанные с кариесом, занимая в последующем ведущее место в ассоциациях микроорганизмов, выделяемых из гнойного экссудата при воспалительных процессах в челюстно-лицевой области, включая одонтогенные абсцессы мозга и других органов. Кроме того, они же могут быть выделены их крови и сердечных клапанов больных инфекционным эндокардитом.
- Streptococcussalivarius – также является одним из основных компонентов нормальной микрофлоры полости рта, а также, но в меньшем количестве, может быть выделен со слизистых дыхательного, желудочно-кишечного и урогенитального тракта. Особенно часто выделяются при анализе микрофлоры языка, слюны и фекалий. И крайне редко из крови при менингитах, септицимии и эндокардитах.
- Streptococcusmutans – выделяется с поверхности зубов и фекалий. Этот микроб является кариесогенным, а значит, может в дальнейшем вызывать бактериемию и бактериальный эндокардит у пациентов, не занимающихся регулярной санацией кариозных очагов в полости рта.
- Streptococcusmitis – в норме выделяется из слюны, мокроты фекалий, при этом может выделяться из верхних дыхательных путей и крови при нозокомиальном инфицировании.
- Совсем неверно упоминать в этом блоке стрептококки группы Anginosus -Streptococcusintermedius/S.anginosus/S.constellatus, но так как мы обсуждаем в основном орофарингеальную флору, способную вызвать инфекционные эндокардиты (и чтобы не писать еще один, совсем малюсенький блок), мы упомянем их здесь. В норме они являются представителями пародонтогенной группы. Но стоит представителю группы S.intermedius оттуда выбраться, как он может вызывать абсцессы печени, мозга и эндокардиты, так как проявляет высокую тропность к их тканям.
Диагностические аспекты
Освоив вышеприведенный материал, мы видим, что только обнаружение данных микроорганизмов в стерильных средах может указывать на них как на потенциальных возбудителей. Почему все-таки потенциальных? Да потому, что в 80% случаев это может оказаться банальной контаминацией в связи с несоблюдением техники забора материала (все мы дышим, и если материал забирается с нарушением правил асептики и антисептики и без использования закрытых систем, то налететь в пробирку может много чего и не только из наших рта и носов). Таким образом, посевы нужно повторять.
Обнаружение этого же зоопарка в местах естественного его обитания не говорит нам практически ничего, если только пациент совсем не следит за полостью рта, и тогда ему можно настоятельно рекомендовать посещение стоматолога.
Аспекты антибактериальной терапии
Группа зеленящих стрептококков природно резистентна к тетрациклинам, макролидам и клиндомицину (до 50% штаммов), к биссептолу резистентно более 75%. Таким образом об этих группах мы даже не вспоминаем.
Само лечение должно быть комплексным и часто в сочетании с хирургическим. Выбор конкретных препаратов будет зависеть от локализации процесса, тяжести состояния пациента и выделенного возбудителя
Например, чувствительность Streptococcus mitis будет выглядеть так (нажмите на картинку для увеличения):
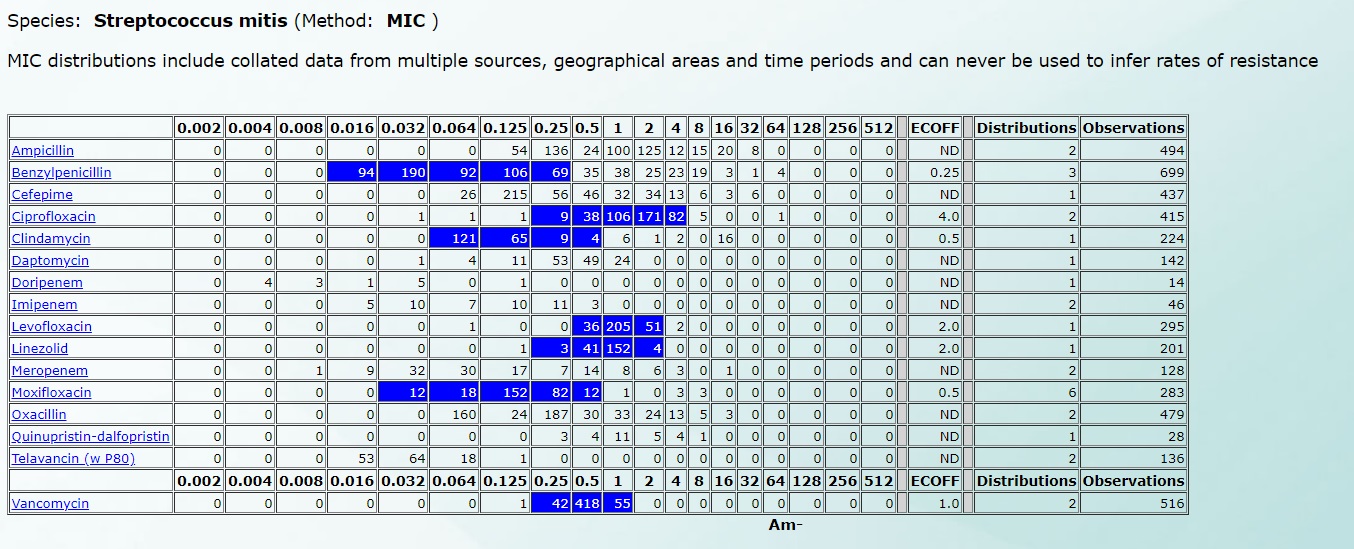
А чувствительность к Streptococcus mutans – вот так (нажмите на картинку для увеличения):
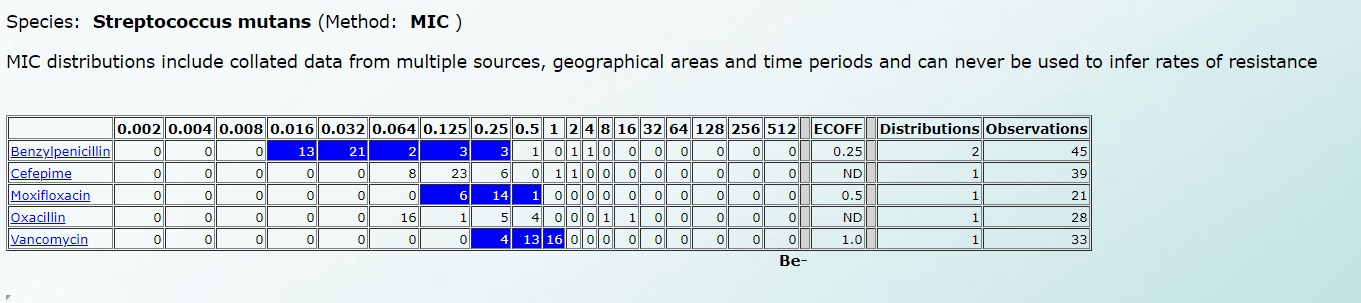
Подробнее все рассмотреть можно по этой ссылке, ведь именно на этой базе данных работают автоматические и полуавтоматические анализаторы в микробиологических лабораториях.
Препаратами выбора будут являться:
- Пенициллин в высоких дозировках (до 24 млн ЕД в сутки), возможно, в сочетании с аминогликозидами
- Цефтриаксон
- Ванкомицин
Как и в случае с любым стрептококком, крайне важно соблюдать длительность лечения, и она должна быть не менее 10-14 дней. Исключение составляет бактериальный эндокардит, там сроки лечения как минимум удваиваются.
В заключение хотелось бы сказать, что как ни прискорбно это сознавать, но недоступность, в первую очередь финансовая, адекватной стоматологической помощи вновь привела к всплеску заболеваний связанных с неблагополучием в полости рта, таким образом, мы вновь вынуждены вспоминать, что инфекционный эндокардит – это не только болезнь наркоманов и лиц со сниженным иммунным статусом, но и тех, у кого недостаточно средств на хорошего стоматолога, а потому и нам не лишне иногда осматривать полость рта у пациентов с инфекциями кровотока или абсцессами в головном мозге или печени.
В этой статье мы поговорим о более сложных темах на примерах тех представителей микробного мира, которые в большинстве случаев являются нашими добрыми соседями и очень редко, при очень специфических условиях, вызывают заболевания. Но так как лаборатории, особенно оснащенные автоматизированными системами детекции, все это определяют и буквально вываливают на врачей, ориентироваться и в этом море информации все-таки необходимо.
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: Трубачева Е.С., врач – клинический фармаколог
Почему за исключением S. pyogenes? Да потому что данного возбудителя мы рассмотрели в отдельной статье. Кроме того, мы уже говорим практически на одном языке, а потому можем себе позволить поговорить о более сложных темах на примерах тех представителей микробного мира, которые в большинстве случаев являются нашими добрыми соседями и очень редко, при очень специфических условиях, вызывают заболевания. Но так как лаборатории, особенно оснащенные автоматизированными системами детекции, все это определяют и буквально вываливают на врачей, ориентироваться и в этом море информации все-таки необходимо.
Микробиологические аспекты
Для начала разберемся с классификациями, чтобы понимать принципы разнесения стрептококков по группам. Так сложилось, что для классификации стрептококков используются их фенотипические характеристики, а именно характеристики по гемолитическим свойствам:
- β-гемолитические стрептококки вызывают полный гемолиз эритроцитов питательной среды с формированием прозрачной зоны вокруг колоний на кровяном агаре
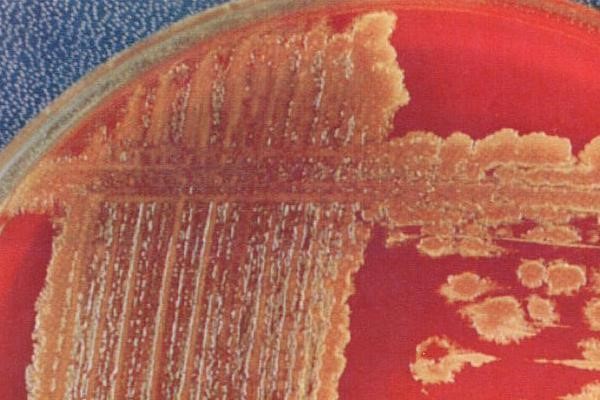
- α-гемолитические (зеленящие) образуют зеленоватый ореол вокруг колоний в результате неполного разложения гемоглобина
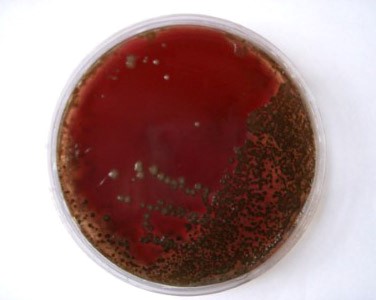
- γ-гемолитические по-другому именуются негемолитическими, то есть ничего никуда из крови не разлагают.
Собственно, почему кровь? Дело в том, что стрептококки крайне требовательны к питательным средам и к условиям, в которых их растят. И чтобы они выросли, в питательные среды (в основном, жидкие) необходимо или добавлять мясной экстракт, или использовать коммерческие питательные среды с добавлением крови барана, или 5%-й кровяной агар – и все это с большим количеством дополнительных компонентов. Для определения характера гемолиза традиционно используется среда с 5%-й дефибринированной кровью барана.
Подобное разделение по группам и типам гемолиза является решающим для деления стрептококков, имеющих медицинское значение, позволяя разделить патогенные и условно-патогенные микроорганизмы. Про патогенные мы уже поговорили ранее, теперь будем вести разговор о более обширной группе условно-патогенных представителей и начнем со стрептококков групп A, C, D и F, оставив для отдельного разговора группу В и единственного ее представителя – S. agalactiae.
Основными характеристиками представителей этих групп является то, что все они:
- Обладают β-гемолитической активностью
- Относятся к нормальной микрофлоре человека и животных
- Могут вызывать оппортунистические инфекции в различных локализациях
- Fc-антиген, способный взаимодействовать с Fc-фрагментом IgG, тем самым угнетая систему комплемента и подавляя активность фагоцитов. Кроме того, он же активирует выработку аутоиммунных антител, которые в дальнейшем участвуют в развитии иммунного воспаления;
- Р-антиген, обладающий иммуносупрессивной активностью и являющийся общим для всех стрептококков. Он подавляет выработку антител и усиливает реакции гиперчувствительности замедленного типа.
Кроме того, стрептококки имеют такой фактор патогенности, как М-протеин, который нарушает фагоцитарную активность путем маскировки рецепторов для комплемента, что очень затрудняет борьбу с этими возбудителями.
Клинические аспекты
1. Streptococcus dysgalactiae – объединяет двух представителей Streptococcus dysgalactiae subsp. dysgalactiae и Streptococcus dysgalactiae subsp. equisimilis. Первый живет на животных (и вызывает маститы у коров, на человеке в качестве возбудителя пока не ловили), второй на человеке – в верхних дыхательных путях и влагалище – и может быть причиной менингита, септических артритов и инфекций кожи (при условии наличия соответствующей симптоматики и в отсутствии других вероятных возбудителей).
2. Стрептококки группы Anginosus (S. anginosus, S. constellatus, S. intermedius) относятся к представителям нормальной флоры человека. Обрести зубы и стать возбудителями инфекции их могут заставить травмы, оперативные вмешательства, сахарный диабет, онкологические заболевания и иммунодефициты различной этиологии. Сами по себе на человека не бросаются и обнаружение оных вне клинической картины истребления не требует.
- S.anginosus – в норме обитает в полости рта, верхних дыхательных путях и влагалище. При патологии может быть высеян из урогенитальной и желудочно-кишечной локализаций.
- S. constellatus – в норме живет в верхних дыхательных путях и ЖКТ. При патологических процессах могут быть обнаружены где угодно.
- S. intermedius – в норме обитает в полости рта и верхних дыхательных путях. При патологических процессах в основном высевается из мозга, из крови при эндокардитах и из печеночных абсцессов (проще говоря оттуда, где в норме все должно быть стерильно).
3. S. equi клинического значения не имеет, так как является зоонозом и вызывает ветеринарные проблемы у коров, лошадей, морских свинок, овец и коз. Иногда – при употреблении зараженных молочных продуктов – может быть обнаружен у людей, больных нефритом.
4. S. canis, как понятно из названия, выделяют от собак. У людей могут вызывать инфекции мягких тканей, пневмонии, сепсис, остеомиелит.
5. S. iniae – обнаруживается у дельфинов и рыб. А также у людей, занятых на обработке замороженной рыбы. Крайне редко вызывает заболевание (описаны всего несколько случаев), хорошо лечится бета-лактамами и макролидами.
6. И несколько чисто зоонозных представителей, не имеющих медицинского значения, но иногда сеющихся с людей, которые за этими животными ухаживают или лечат:
- S. porcinus – вызывает абсцессы глотки свиней, пневмонию и аборты;
- S. didelphis – вызывает инфекции кожи, печени, легких и селезенки у опоссумов;
- S. phocae – выделяется у морских котиков при пневмонии у оных.
Как мы увидели, в большинстве своем перечисленные возбудители относятся к нормальной микрофлоре верхних дыхательных путей, кожи, ЖКТ и урогенитального тракта, а чтобы они вызвали заболевание, во внутреннюю среду организма должно проникнуть очень большое количество оных, при этом иммунная система должна быть подавлена тем или иным образом. Чаще всего такую роль играют медицинские вмешательства (инъекции, операции, катетеризация сосудов, гемодиализ и т. п.) на фоне тяжелых основных или сопутствующих заболеваний. Тогда стрептококки способны вызвать инфекции кожи и мягких тканей, верхних дыхательных путей, эндокардиты и сепсис, инфекции урогенитального тракта, при этом строгой локализации процесса соответствующим возбудителем уже не будет, а будет инфекция, связанная с медицинским вмешательством.
Что делать?
Как можно раньше провести бактериологическую диагностику и главным в ней будет правильная техника взятия биологического материала, чтобы точно исключить его контаминацию ни в чем не повинными мирными соседями, просмотрев истинного возбудителя. Техника взятия материала и правила транспортировки в лабораторию подробно расписаны здесь.
Чем лечить?
Этот вопрос мы можем задать только тогда, когда точно понимаем, что именно вышеуказанные зверушки являются возбудителями и никто за ними не прячется. Хорошая новость в том, что стрептококки до сих пор сохранили высокую чувствительность к бета-лактамам вообще и к пенициллинам в частности, то есть лечить их дешево. Плохая новость в том, что фактически утеряна чувствительность к макролидам, и поэтому они не могут быть препаратами выбора – это обязательно надо учитывать при назначении стартовой терапии.
Кроме того, стрептококки продолжают демонстрировать высокую чувствительность к ванкомицину, но в виду неоднозначности самого препарата в плане безопасности его применения, им тоже не следует злоупотреблять и включать его в схему лечения только в случае наличия аллергии к пенициллиновому ряду.
Итак, мы закончили краткое рассмотрение представителей стрептококков групп A, C, D, F и G, и нам осталось рассмотреть только одного представителя из группы В, а именно S.agalactiae, чем мы и займемся в следующей статье.
Тема эта очень узконаправленная, и вопрос в том, насколько она может быть интересна широкому кругу читателей. Однако ради одних только отдаленных последствий заболеваний, вызванных S. agalactiae, ее стоит рассмотреть.
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: Трубачева Е.С., врач – клинический фармаколог
Для начала капелька истории.
Микробиологические аспекты
Согласно современной классификации S. agalactiae относится к стрептококкам группы В и является единственным представителем в указанной группе. Общим с остальными стрептококками является то, что и этот зверь плохо растет в лабораторных условиях на обычных питательных средах, и ему тоже необходимы специальные среды с 5% бараньей кровью (вопрос капризности стрептококков мы обсуждали в первой статье этого года).
Несмотря на капризы вне естественной среды обитания (коей является кишечник), внутри организма человека S. agalactiae проявляет одно из своих главных свойств – устойчивость к фагоцитозу нейтрофилами и моноцитами, что позволяет ему спокойно выживать и колонизировать доступные слизистые оболочки.
Клинические аспекты
S. agalactiae способен вызывать следующие состояния:
- неонатальный сепсис
- менингиты у новорожденных
- хориоамниониты
- аборты в поздние сроки беременности
- спонтанные аборты
- инфекции мочевыводящих путей
- эндокардиты
- сепсис (у матерей)
- инфекции кожи и мягких тканей, как осложнение после кесарева сечения
- маститы и эндометриты у родильниц
- септический артрит
Наиболее чувствительны к S. agalactiae:
- беременные женщины
- новорожденные
- больные с сахарным диабетом
- дети с низкой массой тела и дистрофией
- пожилые пациенты
- иммунокопрометированные пациенты (вне зависимости от причины этих состояний)
Давайте рассмотрим наиболее уязвимые (и актуальные) категории, а именно беременных женщин и новорожденных.
Как мы знаем, основным местом жительства S. agalactiae в организме человека является ЖКТ, еще точнее – кишечник. Считается, что именно оттуда и происходит колонизация влагалища. Правда, тут же у автора возникает логичный вопрос – как? Стрептококки ног не отрастили, данный представитель также не является исключением. Проблемы с гигиеной? В таких масштабах и в странах с нормальным доступом к воде? Ответ нашелся достаточно быстро – колонизации S. agalactiae наиболее подвержены женщины, ведущее бурную сексуальную жизнь в течение года до развития заболевания/беременности, причем ведущие ее с многочисленными непостоянными партнерами. А судя по наличию кишечной флоры в непредназначенной для ее жизни локации, практики этой самой жизни тоже весьма разнообразны. Поэтому при сборе анамнеза, если, конечно, удастся, стоит выяснять регулярность анальных практик (автор с уверенностью может утверждать, что это сложно), и если удалось выяснить этот аспект, в голове должен прозвучать звоночек о том, что пациентка оказывается в группе риска, особенно если она уже беременна. Хотя следует отметь, что роль именно полового пути до сих пор вызывает определенные споры (даже несмотря на многочисленные исследования связи с ЗППП и с носительством S. agalactiae в уретре мужчин). Но автор согласен оставить этот вопрос дискутабельным.
Когда лучше всего определять факт носительства S. agalactiae для принятия адекватных мер по профилактике вышеперечисленных состояний? На 35-37 неделе беременности. Но следует учитывать, что носительство может быть непостоянным (транзиторным или перемежающимся), что затрудняет его обнаружение в скрининговых исследованиях, то есть если при исследованиях его нет, это не значит, что его там действительно нет, особенно если дама вела активную добеременную жизнь.
Какие факторы могут влиять на наличие носительства S. agalactiae?
- Женщины старшего возраста с репродуктивными проблемами ранее
- Расовые различия – у белых женщин частота колонизации в разы меньше (автор уже не может угадать, откуда его читают, поэтому решил указать и этот фактор)
- Количество предыдущих беременностей
Можно ли проводить скрининг до беременности? Можно, но смысла в нем не будет, ибо даже фаза менструального цикла влияет на выявляемость S. agalactiae.
Какие именно осложнения вызывает носительство S. agalactiae у беременных:
- преждевременные роды
- длительный безводный период
- малый вес новорожденных
- мертворождение
А к числу факторов риска развития этих состояний относят:
- кесарево сечение
- сахарный диабет
- общее снижение иммунитета
- массивную колонизацию S. agalactiae
Учитывая вышеперечисленное, массивная колонизация родовых путей матери создает серьезные угрозы инфекции у новорожденных – почти половина новорожденных от таких матерей будет иметь массированную колонизацию кожи и слизистых оболочек S. agalactiae. Заболеет ли каждый из них? Конечно, нет. Статистика говорит, что из таких детей-носителей заболеет не более 2%, которые будут иметь следующий набор факторов риска:
- Факторы, которые непосредственно связаны с матерью:
- Самый главный – наличие S. agalactiae на слизистой шейки матки у беременных
- Инфекции, связанные с S. agalactiae у ранее рожденных детей
- Длительный безводный период
- Преждевременные роды
- Подъем температуры во время родов
- Бактериурия
- Хориоамнионит
- Факторы, связанные непосредственно с новорожденным:
- Недоношенность и малый вес при рождении
- Кесарево сечение
- Длительное инструментальное обследование внутриутробно
У детей S. agalactiae может стать причиной:
- Менингитов
- Пневмоний
- Остеомиелитов
- Сепсиса
- Заболеваний глаз
- Артритов
- Ангин
- Нейтропений
У новорожденных заболевания могут развиваться в разные сроки. Чаще всего инфекции развиваются в течение первых 12 часов (сепсис, менингит, пневмония и нейтропения). Заражение происходит во время родов или внутриутробно перед родами через разорванный плодный пузырь. Летальность при раннем развитии колоссальная – более 50% и развивается в первые сутки. Как вы помните, в таких сроках антибиотики фактически бессильны (вспоминаем правило 48 часов для бактерицидных препаратов). У половины выживших детей затем могут развиваться осложнения со стороны ЦНС (например, ДЦП).
Значительно реже инфекция раскручивается в поздние сроки (от недели до трех месяцев), и чаще всего это будет менингит. Течет более благоприятно, летальность значительно ниже, но она есть. Также могут встречаться инфекции кожи и мягких тканей, септические артриты. После выздоровления в дальнейшем половина детей наблюдаются у неврологов в связи с серьезными неврологическими осложнениями.
Отдельного упоминания требует внутрибольничное распространение S. agalactiae в случае, когда мать не является его носителем и речь идет об инфекциях, связанных с медицинскими вмешательствами. Со всеми вытекающими, которые мы обсуждали в соответствующей статье.
Что со всем этим делать?
- Скрининг – мазок из влагалища и прямой кишки. То есть активное выявление беременных женщин – носителей S. agalactiae для последующей профилактики в родах, если наличие микроорганизма подтвердится. Руководства и рекомендации говорят о проведении скрининга в сроках 35-37 недель. Положительным считается наличие S. agalactiae в любом локусе.
- Далее должна быть проведена оценка факторов риска – если они есть, то рекомендуется назначение препаратов пенициллинового ряда во время родов (по аналогии с периоперационной антибиотикопрофилактикой, с одной существенной разницей – там препараты назначаются за 30-40 минут до оперативного вмешательства, а здесь непосредственно во время родов, и в идеале внутривенно капельно для создания максимальной времязависимой концентрации в тканях и крови, которые сдержат размножение патогенна).
- Если скрининг не проводился и женщина поступила в роддом как есть, то в случае длительного безводного периода и/или подъема температуры в родах выше 38°С также назначается пенициллин в родах.
- Если на скрининге S. agalactiae не выявлен, а также нет факторов риска (лихорадка и безводный период в родах), то профилактика не проводится.
Если имеется аллергия на пенициллиновый ряд, используем клиндамицин, так как эритромицин нам не помощник в виду высочайшего уровня резистентности у почти всех стерептококков.
К сожалению, профилактика не всесильна. Конечно, она предупреждает раннее развитие инфекции, но ничего не может сделать с мертворождением, преждевременными родами или инфекциями, развивающимися в более поздние сроки. Так что вопрос инфекций, связанных с S. agalactiae, будет еще достаточно длительное время очень актуальным, и в нем, к сожалению, нет простых решений.
Streptococcus agalactiae — представитель большой группы микроорганизмов, отличающихся характерными морфологическими, тинкториальными, культуральными и биохимическими свойствами. Этот условно-патогенный микроб является естественным обитателем организма человека и локализуется преимущественно в кишечнике, носоглотке и влагалище. Стрептококк способствует развитию заболеваний лишь при определенных негативных условиях, ослабляющих иммунную защиту и снижающих общую резистентность организма.
Стрептококк агалактия — нормальный обитатель влагалища здоровой женщины. В количестве, не превышающем 10 4 колониеобразующих единиц, микробы безвредны для организма. Недуг развивается только в случае активного размножения бактерий и приобретения ими болезнетворных свойств. Это происходит при развитии иммунодефицита или переохлаждении. Одномоментное внедрение ударной дозы патогенов заканчивается патологическим процессом. Обнаружение во влагалищных выделениях значительного числа микробов – признак неспецифического воспаления.
У мужчин стрептококк агалактия входит в состав нормоценоза кишечника и носовой полости. При исследовании кала на дисбактериоз количество микробов не должно превышать 10 5 или 10 6 . Микробиологическое исследование отделяемого слизистой носа на микрофлору обнаруживает у здоровых людей стрептококк в количестве 10 3 или 10 4 . Streptococcus agalactiae, проникая в мужские половые органы, вызывает острую форму заболевания.
Стрептококк агалактия представляет серьезную опасность для беременных женщин и новорожденных детей, особенно, недоношенных. В последние годы отмечается рост заболеваемости среди пожилых лиц, у которых инфекция протекает в форме сепсиса, воспаления легких или перитонита. В группу риска также входят лица с тяжелыми соматическими заболеваниями, ослабляющими их иммунитет.
Диагностика патологии, вызванной Streptococcus agalactiae, основывается на данных, полученных в ходе микробиологического исследования влагалищного секрета, мочи, кала. Всем больным показано этиотропное противомикробное лечение антибиотиками из группы пенициллинов, макролидов, цефалоспоринов, а также патогенетическая и симптоматическая терапия, назначенная врачом с учетом индивидуальных особенностей организма.
Этиология
Streptococcus agalactiae — бактерия специфической шарообразной или эллипсоидной формы, способная существовать как в присутствии кислорода, так и без него. Микробы аспорогенны, неподвижны, имеют капсулу и обладают группоспецифическим полисахаридом.

Streptococcus agalactiae под микроскопом
Микроорганизмы окрашиваются по Грамму в синий цвет и располагаются в мазке парами и цепочками. Они требовательны к питательным средам. Растут стрептококки исключительно на средах, содержащих кровь, сыворотку и глюкозу. Эти вещества они используют в качестве источника энергии. Инкубируют посевы в термостате при 37 °С, хотя бактерии способны расти и в более широком диапазоне температур. На кровяном агаре спустя сутки образуются сероватые, очень мелкие колонии с зоной полного просветления по периферии. В бульоне бактерии растут в виде диффузной мути и осадка на дне пробирки.
Патогенные свойства бактерии обусловлены следующими факторами:
- Стрептолизином, разрушающим окружающие ткани, в особенности клетки крови и сердца;
- Лейкоцидином, угнетающим иммунитет и уничтожающим иммунокомпетентные клетки;
- Некротоксином, вызывающим отмирание тканей и воздействующим на работу всего организма;
- Ферментами, обеспечивающими адгезию, инвазию, распространение микробов по организму, поражение здоровых тканей и развитие патологического процесса.
Стрептококки резистентны к замораживанию, высушиванию, прямым солнечным лучам. Погибают бактерии под воздействием антибиотиков, антисептиков и дезинфектантов.
Патогенетические звенья инфекции:
- Внедрение микроба в организм,
- Колонизация слизистой оболочки,
- Возникновение очага воспаления,
- Боль и отек,
- Бактериемия,
- Общее недомогание,
- Интоксикационный синдром,
- Дегидратация,
- Помутнение сознания,
- Регионарный лимфаденит.
Эпидемиология
В природе Streptococcus agalactiae широко распространены. В организме человека они колонизирует слизистую кишечника, носа, глотки, органов выделительной и половой систем. От 15 до 40 % женщин репродуктивного возраста являются бактерионосителями.
Существует три варианта пребывания стрептококка во влагалище:
- Безвредное существование бактерий в организме,
- Бактериальный вагиноз,
- патологический процесс.
Если бактерий в мазке из цервикального канала мало, а лактобактерий много, говорят о первом варианте. Когда количество стрептококков превышает количество молочнокислых бактерий, а число лейкоцитов в поле зрения находится в пределах 50, это признак дисбиоза влагалища. Если лейкоцитов гораздо больше, значит, имеет место воспалительный процесс, протекающий в форме цервицита, кольпита, эндометрита.
Пути распространения инфекции:
- Контактный — через общие бытовые предметы, при поцелуе, объятии,
- Самозаражение – микробы из анальной зоны могут проникать во влагалище,
- Вертикальный — заражение плода во время беременности или новорожденного в родах,
- Половой — во время коитуса без презерватива,
- Воздушно-капельный — при чихании, кашле, близком общении с больным человеком,
- Пищевой — при употреблении обсемененных продуктов питания,
- Гематогенный занос инфекции из первичных очагов – почек или носоглотки.
Новорожденные инфицируются в первые часы и сутки после рождения. Это может случиться и раньше: в пре- и интранатальном периоде.
Для Streptococcus agalactiae характерна осенне-зимняя сезонность. Эти микроорганизмы активизируются в тот момент, когда организм ослаблен вирусами. На фоне ОРВИ чаще всего развивается вторичная бактериальная инфекция.
Факторы, способствующие активации стрептококка и его размножению:
- Гормональный сбой,
- Иммунодефицит,
- Тяжелые соматические заболевания,
- Частое использование лубрикантов,
- Ношение нижнего белья из синтетических материалов,
- Эндокринопатии,
- Вирусные инфекции,
- Дисбиоз кишечника,
- Неправильное подмывании наружных половых органов,
- Редкая смена нижнего белья,
- Использование некачественных гигиенических средств,
- Половой акт без презерватива,
- Стрессы,
- Переохлаждения,
- Состояния после хирургических вмешательств,
- Длительная и бесконтрольная антибиотикотерапия,
- Лечение цитостатиками или гормонами,
- Физическое перенапряжение,
- Сложная экологическая обстановка.
В мужской организм бактерии попадают при незащищенном половом контакте с женщиной-бактерионосителем или в результате дисбиоза кишечника. Инфицирование происходит во время занятий нетрадиционными видами секса. Мужчина-носитель инфекции сам не болеет, но заражает своих партнерш.
При беременности изменяется гормональный фон, что выражается в повышенной секреции прогестерона, угнетающего локальную иммунную защиту. Подобные процессы позволяют сохранить беременность. При этом повышается риск развития инфекционных патологий и обострения хронических заболеваний органов репродуктивной системы.
Клиника
Инфекция, вызванная данным микроорганизмом, у лиц репродуктивного возраста обычно протекает бессимптомно. Клинические признаки воспаления органов мочевыделительной и репродуктивной систем вполне узнаваемы.
Streptococcus agalactiae способен вызвать воспаление мочевого пузыря, уретры, легких, эндокарда, суставов, мозговых оболочек.

- Цистит проявляется режущей болью при мочеиспускании, отсутствием удовлетворения от его опорожнения, императивными позывами, появлением мутной мочи с хлопьями. Острая форма патологии сопровождается интоксикацией, слабостью, цефалгией, резкой потерей работоспособности.
- Симптомами уретрита у мужчин являются: боль при мочеиспускании, неприятные ощущения, чувство жжения в уретре, усиливающиеся после эякуляции, обильное слизисто-гнойное отделяемое, гиперемия устья и отек губок уретры по утрам.
- Бактериальный вагиноз, обусловленный увеличением во влагалище стрептококка, проявляется жжением и зудом в промежности, ноющей болью внизу живота, болезненностью при половом сношении, отеком половых губ, обилием желтоватой слизи.
У женщины инфекция часто протекает скрыто, бессимптомно. Стрептококки очень опасны для появившихся на свет малышей. Если произошло заражение внутри утробы матери, ребенок рождается с лихорадкой, гематомами, выделением крови изо рта, тяжелым дыханием. При инфицировании плода развивается сепсис, воспаление легких, мозговых оболочек, сердечной мышцы. Больные дети погибают практически сразу после рождения.
Причиной антенатальной гибели плода также может стать Streptococcus agalactiae. Патологоанатомы на вскрытии обнаруживают признаки гипоксии, увеличенное кровенаполнение органов, петехиальные геморрагии на эпикарде, отечность мозга, размягчение и разжижение тканей. На плодных оболочках определяется очаговая лейкоцитарная инфильтрация.
Диагностика
Заболевание диагностируют на основании результатов анализов. Лабораторная диагностика — основной способ обнаружения Streptococcus agalactiae.

-
В микробиологической лаборатории исследуют мазки из цервикального канала, влагалища, зева, мочу, кал. Окрашенные препараты микроскопируют и обнаруживают кокковую флору. В лаборатории готовят жидкие и плотные питательные среды, содержащие стимуляторы роста для стрептококков и вещества, подавляющие постороннюю микрофлору. На основании полученных в ходе исследования данных о

Лечебные мероприятия
Чтобы избавиться от патологии и ее основных проявлений, необходимо воздействовать на первопричину — убить бактерии. Для этого больным назначают противомикробные препараты — антибиотики. В тяжелых случаях показано патогенетическое лечение, включающее дезинтоксикацию и коррекцию водно-электролитного баланса. Симптоматическая терапия заключается в применении жаропонижающих, антигистаминных, антисептических средств. Дополнительно проводят лечение иммуномодуляторами и иммуностимуляторами.

После купирования интоксикации назначают физиопроцедуры – электрофорез, УВЧ, индуктотермию, СВЧ-терапию, аэроионотерапию, ингаляции, а также массаж грудной клетки, иглоукалывание, ЛФК.
Большое значение в лечении патологии имеет режим. Больным рекомендуют находиться в постели, особенно лицам с выраженным интоксикационным синдромом. Активные движения в разгар болезни замедляют процесс выздоровления и повышают риск развития серьезных осложнений. Дезинтоксикационные мероприятия включают правильный питьевой режим — употребление в сутки до трех литров воды. При отсутствии эффекта от лечения и ухудшении общего состояния больным показана госпитализация в стационар.
Своевременное и правильное лечение делает прогноз инфекции благоприятным. В противном случае заболевание приобретает затяжное течение, развиваются тяжелые осложнения, возможен смертельный исход.
Видео: доктор Елена Березовская – стрептококк группы В и беременность
Профилактика
Мероприятия, предупреждающие развитие стрептококковой инфекции:
- Укрепление иммунитета,
- Правильное питание,
- Личная гигиена,
- Борьба с табакокурением,
- Профилактический прием витаминов,
- Оптимальная физическая нагрузка,
- Полноценный сон,
- Отказ от употребления спиртных напитков,
- Санация очагов хронической инфекции,
- Соблюдение санитарно-гигиенических норм и правил,
- Ношение одежды по сезону,
- Защита организма от переохлаждения и сквозняков.
Streptococcus agalactiae в определенном количестве постоянно обитает в организме здоровых людей. Его активация и быстрое размножение очень опасны. Микроб разрушает эритроциты и способствует развитию воспаления там, где его количество максимально. При своевременном обнаружении стрептококка и правильном этиотропном лечении прогноз на выздоровление улучшается, и значительно снижается риск развития опасных для жизни осложнений.
Читайте также:

