Как лечить токсокароз у человека народными средствами в домашних условиях
Обновлено: 25.04.2024
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут бы
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут быть также личинки других аскарид — кошки (T. mystax), коровы, буйвола, (T. vitulorum). Однако роль этих возбудителей в патологии человека практически не изучена
Половозрелые формы T. canis — крупные раздельнополые черви длиной 4 — 18 см локализуются в желудке и тонком кишечнике животных (собак). Интенсивность инвазии у собак может быть очень высокой, особенно у молодых животных. Средняя продолжительность жизни половозрелых особей составляет 4 месяца, максимальная — 6 месяцев. Самка паразита за сутки откладывает более 200 тыс. яиц. В 1 г фекалий может содержаться 10 000—15 000 яиц, так что в почву попадают миллионы яиц, обусловливая тем самым высокий риск заражения токсокарозом.
 |
Яйца токсокар округлой формы, крупнее яиц аскариды (65—75 мкм). Наружная оболочка яйца толстая, плотная, мелкобугристая. Внутри яйца располагается темный бластомер.
Цикл развития возбудителя следующий. Выделившиеся яйца токсокар попадают в почву, где, в зависимости от влажности и температуры почвы, созревают за 5—36 суток, становясь инвазионными. Инвазионность яиц сохраняется в почве длительное время, в компосте — несколько лет.
Жизненный цикл токсокары сложный. Выделяют основной цикл и два варианта вспомогательных. Основной цикл происходит по схеме: окончательный хозяин (псовые) — почва — окончательный хозяин (псовые). Передача инвазии осуществляется геооральным путем. Вспомогательный цикл (вариант 1) идет трансплацентарно, в этом случае паразит в личиночной стадии переходит от беременной самки к плоду, в организме которого совершает полную миграцию, достигая в кишечнике щенка половозрелой стадии. Инвазированный щенок становится функционально полноценным окончательным хозяином, источником инвазии.
Вспомогательный цикл (вариант 2) осуществляется по цепи: окончательный хозяин (псовые) — почва — паратенический хозяин. Паратеническим (резервуарным) хозяином могут быть грызуны, свиньи, овцы, птицы, земляные черви. Человек также выступает в роли паратенического хозяина, но не включается в цикл передачи инвазии, являясь для паразита биологическим тупиком. Дальнейшее развитие возбудителя происходит при условии, что паратенический хозяин будет съеден собакой или другим окончательным хозяином. Механизм передачи инвазии при этом варианте — геооральный — ксенотрофный.
В зависимости от возраста хозяина реализуются разные пути миграции личинок токсокар. У молодых животных (щенков до 5 недель) почти все личинки совершают полную миграцию с достижением половозрелых форм в кишечнике и выделением яиц во внешнюю среду. В организме взрослых животных большая часть личинок мигрирует в соматические ткани, где сохраняет жизнеспособность несколько лет. В период беременности и лактации у беременных сук возобновляется миграция личинок. Мигрирующие личинки через плаценту попадают в организм плода. Личинки остаются в печени пренатально инвазированных щенков до рождения, а после рождения личинки из печени мигрируют в легкие, трахею, глотку, пищевод и попадают в желудочно-кишечный тракт, где через 3—4 недели достигают половозрелой стадии и начинают выделять во внешнюю среду яйца. Кормящие суки могут передавать щенкам инвазию также через молоко.
У человека цикл развития возбудителя, его миграция осуществляется следующим образом. Из яиц токсокар, попавших в рот, затем в желудок и тонкий кишечник выходят личинки, которые через слизистую оболочку проникают в кровеносные сосуды и через систему воротной вены мигрируют в печень, где часть из них оседает, инцистируется или окружается воспалительными инфильтратами, образуя гранулемы. Часть личинок по системе печеночных вен проходит фильтр печени, попадает в правое сердце и через легочную артерию — в капиллярную сеть легких. В легких часть личинок также задерживается, а часть, пройдя фильтр легких, по большому кругу кровообращения заносится в различные органы, оседая в них. Личинки токсокар могут локализоваться в различных органах и тканях — почках, мышцах, щитовидной железе, головном мозге и др. В тканях личинки сохраняют жизнеспособность многие годы и периодически, под влиянием различных факторов, возобновляют миграцию, обусловливая рецидивы заболевания.
- Географическое распространение и эпидемиология
Токсокароз — широко распространенная инвазия, она регистрируется во многих странах. Показатели пораженности плотоядных являются высокими во всех странах мира. Средняя пораженность собак кишечным токсокарозом, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах у части животных достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз. Распространенность инвазии в различных регионах точно неизвестна, поскольку токсокароз не подлежит обязательной регистрации. Совершенно очевидно, что токсокароз имеет широкую геграфию распространения, и число больных значительно выше официально регистрируемых.
| Токсокароз широко распространен и регистрируется во многих странах. Средняя пораженность кишечным токсокарозом собак, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз |
- Патогенез и патологическая анатомия
Патогенез токсокароза сложный и определяется комплексом механизмов в системе паразит — хозяин. В период миграции личинки травмируют кровеносные сосуды и ткани, вызывая геморрагии, некроз, воспалительные изменения. Ведущая роль принадлежит иммунологическим реакциям организма в ответ на инвазию. Экскреторно-секреторные антигены личинок оказывают сенсибилизирующее действие с развитием реакций немедленного и замедленного типов. При разрушении личинок в организм человека попадают соматические антигены личинок. Аллергические реакции проявляются отеками, кожной эритемой, увеличением резистентности дыхательных путей к вдыхаемому воздуху, что клинически выражается развитием приступов удушья. В аллергических реакциях принимают участие тучные клетки, базофилы, нейтрофилы, но основную роль играют эозинофилы. Пролиферация эозинофилов регулируется Т-лимфоцитами при участии медиаторов воспалительных реакций, выделяемых сенсибилизированными лимфоцитами, нейтрофилами, базофилами. Образующиеся иммунные комплексы привлекают в очаг поражения эозинофилы. Вокруг личинок токсокар кумулируются сенсибилизированные Т-лимфоциты, привлекаются макрофаги и другие клетки — формируется паразитарная гранулома.
Патоморфологическим субстратом токсокароза является выраженное в различной степени гранулематозное поражение тканей. При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими. При токсокарозе находят многочисленные гранулемы в печени, легких, поджелудочной железе, миокарде, лимфатических узлах, головном мозге и других органах.
Наиболее характерным лабораторным показателем является повышенное содержание эозинофилов в периферической крови. Относительный уровень эозинофилии может колебаться в широких пределах, достигая в ряде случаев 70 — 80% и более. Повышается содержание лейкоцитов (от 20х109 до 30х109 на 1 л). При исследовании пунктата костного мозга выявляется гиперплазия зрелых эозинофилов. У детей нередко отмечается умеренная анемия. Некоторые исследователи отмечают прямую корреляцию между тяжестью клинических проявлений инвазии и уровнем эозинофилии и гиперлейкоцитоза периферической крови. Характерным лабораторным признаком является также ускорение СОЭ, гипергаммаглобулинемия. В случаях поражения печени наблюдается повышение билирубина, гиперферментемия.
В хронической стадии болезни острые клинические и лабораторные признаки затухают. Наиболее стабильным лабораторным показателем остается гиперэозинофилия периферической крови.
Выделяют субклиническое, легкое, среднетяжелое и тяжелое течение токсокароза. Возможна так называемая бессимптомная эозинофилия крови, когда явные клинические проявления инвазии отсутствуют, но наряду с гиперэозинофилией выявляются антитела к антигенам T.canis.
Одной из наиболее серьезных проблем, связанных с токсокарозом, является его взаимосвязь с бронхиальной астмой. При сероэпидемиологических исследованиях установлено, что у больных бронхиальной астмой нередко обнаруживаются антитела к антигенам T.canis классов Ig G и Ig E. В зависимости от остроты паразитарного процесса, его длительности и длительности клинических проявлений бронхиальной астмы преобладает тот или другой класс иммуноглобулинов. Имеются клинические наблюдения, свидетельствующие об улучшении течения бронхиальной астмы или выздоровлении после ликвидации токсокарозной инвазии.
Паразитологический диагноз устанавливается редко и только по наличию в тканях характерных гранулем и личинок и их идентификации при исследовании биопсийного и секционного материала. Это возможно при пункционной биопсии печени, легких, оперативном вмешательстве. Обычно диагноз токсокароза устанавливается на основании данных эпидемиологического анамнеза, клинической симптоматики и гематологических проявлений. Используют также иммунологические реакции, позволяющие выявлять антитела к антигенам токсокар. Обычно применяют ИФА с секреторно-экскреторным антигеном личинок токсокар второго возраста. В настоящее время в России выпускается коммерческий диагностикум. Диагностическим титром считают титр антител 1:400 и выше (в ИФА). Титр антител 1:400 свидетельствует об инвазированности, но не болезни. Титр антител 1:800 и выше свидетельствует о заболевании токсокарозом. Практика показывает, что прямая корреляция между уровнем антител и тяжестью клинических проявлений токсокароза существует не всегда. Не всегда имеется и корреляция между уровнем антител и гиперэозинофилии крови.
При постановке диагноза и определении показаний к специфической терапии следует учитывать, что токсокароз протекает циклически с рецидивами и ремиссиями, в связи с чем возможны значительные колебания клинических, гематологических и иммунологических показателей у одного и того же больного.
М. И. Алексеева и соавт. (1984) разработали алгоритм диагностики токсокароза, основанный на оценках в баллах значимости клинических симптомов и сопоставлении клинико-эпидемиологических и лабораторных показателей. Этот метод может быть перспективен при проведении массовых обследований населения.
Дифференциальный диагноз проводят с миграционной стадией других гельминтозов (аскаридоз, описторхоз), стронгилоидозом, эозинофильной гранулемой, лимфогранулематозом, эозинофильным васкулитом, метастазирующей аденомой поджелудочной железы, гипернефромой и другими заболеваниями, сопровождающимися повышенным содержанием эозинофилов в периферической крови. Следует иметь в виду, что у больных с системными лимфопролиферативными заболеваниями и серьезными нарушениями в системе иммунитета иммунологические реакции могут быть ложно положительными. В этих случаях необходим тщательный анализ клинической картины заболевания.
| При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими |
Глазной токсокароз. Патогенез этой формы токсокароза до конца не ясен. Существует гипотеза об избирательном поражении глаз у лиц с инвазией низкой интенсивности, при которой не развивается достаточно выраженная иммунная реакция организма из-за слабого антигенного воздействия небольшого числа поступивших в организм личинок токсокар.
Эта форма токсокароза чаще наблюдается у детей и подростков, хотя описаны случаи заболевания и у взрослых.
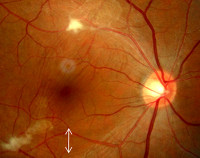
Для токсокароза характерно одностороннее поражение глаз. Патологический процесс развивается в сетчатке, поражается хрусталик, иногда параорбитальная клетчатка. В тканях глаза формируется воспалительная реакция гранулематозного характера. Патологический процесс часто принимают за ретинобластому, проводят энуклеацию глаза. При морфологическом исследовании обнаруживают эозинофильные гранулемы, иногда — личинки токсокар.
Клинически поражение глаз протекает как хронический эндофтальмит, хориоретинит, иридоциклит, кератит, папиллит. Глазной токсокароз — одна из частых причин потери зрения.
Диагностика глазного токсокароза сложна. Количество эозинофилов обычно нормальное или незначительно повышено. Специфические антитела не выявляются или выявляются в низких титрах.
Разработано недостаточно. Применяют противонематодозные препараты — тиабендазол (минтезол), мебендазол (вермокс), медамин, диэтилкарбамазин. Эти препараты эффективны в отношении мигрирующих личинок и недостаточно эффективны в отношении тканевых форм, находящихся в гранулемах внутренних органов.
Минтезол (тиабендазол) назначают в дозах 25—50 мг/кг массы тела в сутки в три приема в течение 5—10 дней. Побочные явления возникают часто и проявляются тошнотой, головной болью, болями в животе, чувством отвращения к препарату (в настоящее время препарат в аптечную сеть России не поступает).
Вермокс (мебендазол) назначают по 200 —300 мг в сутки в течение 1—4 недель. Побочные реакции обычно не наблюдаются.
 |
Медамин применяют в дозе 10 мг/кг массы тела в сутки повторными циклами по 10 — 14 дней.
Диэтилкарбамазин назначают в дозах 2 — 6 мг/кг массы тела в сутки в течение 2 — 4 недель. (В настоящее время препарат в России не производится, не закупается за рубежом. — Прим. ред.)
Альбендазол назначают в дозе 10 мг/кг массы тела в сутки в два приема (утро — вечер) в течение 7 — 14 дней. В процессе лечения необходим контроль анализа крови (возможность развития агранулоцитоза) и уровня аминотрансфераз (гепатотоксическое действие препарата). Небольшое повышение уровня аминотрансфераз не является показанием к отмене препарата. В случае нарастающей гиперферментемии и угрозы развития токсического гепатита требуется отмена препарата.
Критерии эффективности лечения: улучшение общего состояния, постепенная регрессия клинических симптомов, снижение уровня эозинофилии и титров специфических антител. Следует отметить, что клинический эффект лечения опережает положительную динамику гематологических и иммунологических изменений. При рецидивах клинической симптоматики, стойкой эозинофилии и положительных иммунологических реакциях проводят повторные курсы лечения.
Прогноз для жизни благоприятный, однако при массивной инвазии и тяжелых полиорганных поражениях, особенно у лиц с нарушениями иммунитета, возможен летальный исход.
Включает соблюдение личной гигиены, обучение детей санитарным навыкам.
Важным профилактическим мероприятием является своевременное обследование и дегельминтизация собак. Наиболее эффективно преимагинальное лечение щенков в возрасте 4 — 5 недель, а также беременных сук. Для лечения собак используют противонематодозные препараты. Необходимо ограничение численности безнадзорных собак, оборудование специальных площадок для выгула собак.
Следует улучшить санитарно-просветительскую работу среди населения, давать информацию о возможных источниках инвазии и путях ее передачи. Особого внимания требуют лица, по роду деятельности имеющие контакты с источниками инвазии (ветеринарные работники, собаководы, землекопы и другие).
Токсокароз — это паразитарное заболевание, которое вызвано личинками червей токсокаров. Передается через кошек и собак, если не соблюдаются правила личной гигиены. Опасно тем, что затрагивает жизненно важные органы и даже головной мозг человека. Без лечения патология может нанести серьезный вред. Терапия основана на приеме противогельминтных препаратов. Лечение токсокароза народными средствами назначается только в качестве дополнения к основной терапии или в целях профилактики заболевания.
12 проверенных народных лекарств
Прежде чем начать лечить токсокароз, необходимо подтвердить диагноз. Народные терапевтические методы назначаются одновременно с приемом лекарств. Беременные, кормящие женщины и дети лечатся с осторожностью только после консультации доктора. Некоторые средства могут вызвать серьезные аллергические реакции и осложнения.

Для лечения токсокароза врачи советуют использовать настойки и отвары, клизмы, приготовленные из горьких на вкус растений и продуктов. Черви не выносят компоненты таких средств, вследствие чего покидают организм.
Пижма и полынь
Эти растения содержат природные токсины, помогающие избавиться от токсокароза. Можно брать измельченную сухую либо свежую траву. Для концентрированного отвара из пижмы необходимо 3 ст.л. травы заварить 250 мл кипятка, настаивать примерно час. Принимать по 2 ст.л. до 4 раз за сутки одну неделю. После сделать семидневный перерыв и повторить лечение.
С отваром пижмы можно также делать лечебные клизмы. Для них концентрированный отвар не подходит. Он разводится теплой кипяченой водой в пропорции 1:1. Можно сразу приготовить слабое средство (в 250 мл воды настаивается 1 ст.л. травы). Клизма ставится перед сном. Лечение длится также 7 суток.
Полынь эффективна в сочетании с медом. 100 г меда перемешиваем с 1 ст.л. семян травы. Средство делим так, чтобы его хватило на день, и съедаем его каждый раз до еды общим курсом в 2 недели.
Полынные отвары противопоказаны при токсокарозе во время вынашивания ребенка и лактации.
Чеснок
Из чеснока готовят следующие лечебные средства:
Лечебный курс чесночными составами длится 7 суток.
Тыквенные семечки
От токсокароза у детей и взрослых помогут избавиться семена тыквы. В них содержится кукурбитин, который уничтожает гельминтов. Ребенку достаточно в сутки съедать по 150 г очищенных семян. Людям старше 18 лет дозировку следует увеличить вдвое и через час принять слабительное средство. Полезно семена заедать медом.
Важно, чтобы при очищении тыквенных семечек на ядрах оставалась пленка. Именно в ней содержится больше всего кукурбитина.
Для профилактики токсокароза полезно пить тыквенное масло. Оно хорошо очищает кишечник и печень от паразитов, следов их жизнедеятельности.
Девясил
Отвар с девясиловым корнем эффективно борется с токсокарозом. Обладает желчегонным, противовоспалительным, противогельминтным и антибактериальным действием. Измельченное средство в количестве 1 ст.л. заливаем 200 мл горячей воды, настаиваем примерно 10-12 часов, пьем по 3 ст.л. до 5 раз за сутки.
Лечебный курс длится неделю, после чего делаем двухдневный перерыв и процедуру повторяем до того, как паразиты полностью не выйдут из организма. Можно также принимать процеженный отвар каждые 2 часа по 1 ст. л., но через день.
Ясень
Лечение токсокароза народными средствами подразумевает использование корней, веток и коры дерева. Лекарства, содержащие компоненты ясеня, обладают противогельминтным, антибактериальным действием, заживляют слизистые, восстанавливают обменные процессы в организме.

1 ч.л. измельченных веток ясеня заливаем стаканом кипятка, провариваем на водяной бане 10 минут. Снимаем с огня, укутываем одеялом, настаиваем час.
Отвар процеживаем, принимаем натощак с утра и за несколько часов до сна по 150-200 мл ежедневно. Курс лечения длится как минимум 2 недели.
Сосновые шишки
Лечить токсокароз можно отваром из зеленых сосновых шишек. Средство готовится следующим образом: 10 шишек заливаем кипятком, провариваем пару часов. После емкость с отваром укутываем одеялом, оставляем на сутки, процеживаем. Пьем по 2 ст.л. несколько раз за день на протяжении 7 дней.
Это эффективное противогельминтное средство, которое помогает избавиться от токсокароза. Вот несколько рецептов с репчатым луком:
- Измельчаем 1 среднюю луковицу, заливаем стаканом кипящей воды. Состав настаиваем в течение ночи. Принимать лечебное средство следует по 1 ст.л. до 4 раз за сутки. Курс продолжается неделю.
- Половину луковицы заливаем 100 мл водки, настаиваем 10 дней. Принимаем по 1,5 ст.л. дважды в сутки перед едой.
- Для профилактики токсокароза можно ежедневно есть огурцы с луком. Овощи должны быть свежими.
Принимать луковый настой (кроме спиртового) можно детям, женщинам в положении, во время лактации, если нет противопоказаний.
Грецкие орехи
Для борьбы с личинками токсокар используют молодые грецкие орехи, точнее, их кожуру. Мелко нарезаем, перекладываем в банку, заливаем медицинским спиртом (500 мл на 20 плодов). Настаивать лечебное средство нужно 30-40 суток в темном прохладном месте.
Принимают состав по определенной схеме:
- В первые сутки 1 капля настоя разбавляем в 100 мл воды.
- Последующие 6 суток добавляем по 1 капле в аналогичное количество воды (7 день — 7 капель).
- С 8 дня дозировку повышаем до 1 ч.л. на 30 мл жидкости.
Лечебный курс от токсокароза длится месяц.
Кислица
Эффективна не только для лечения токсокароза у человека, но и в целях профилактики. Положительно влияет на деятельность желчного пузыря и печени, сокращая отрицательное воздействие паразитов на организм.

Готовится следующим образом: 1 ст.л. растения заливаем стаканом кипящей воды, остужаем несколько часов, принимаем по 3-4 ст.л. до 4 раз за сутки.
Продолжительность лечения — неделя, после чего делается двухдневный перерыв и курс продолжается.
Гранат
Те, кто предпочитает лечение токсокар народными средствами, может принимать отвар либо настойку из гранатовой кожуры. Этот плод способен устранить негативные последствия жизнедеятельности паразитов. Чтобы приготовить настойку:
- Измельчаем 50 г свежей кожуры граната, помещаем в эмалированную емкость.
- Заливаем 2 стаканами кипящей воды, оставляем на четверть суток.
- После кипятим до сокращения жидкости вдвое.
- Снимаем с огня, остужаем.
Лечебное средство надо пить единожды в сутки либо порционно на протяжении часа.
Можно также сделать отвар: кожуру граната заливаем 150 мл воды, кипятим 10 минут, настаиваем полтора часа. Средство от токсокароза пьем два раза в день. Затем следует воздержаться от еды на пару часов.
Петрушка и укроп
Чтобы приготовить отвар, 3 ст.л. мелко порубленной зелени заливаем 2 стаканами кипящей воды, процеживаем через час. Полученный настой смешиваем с аналогичным количеством меда, принимаем по 50 мл в течение суток.

Грибы лисички
При лечении токсокароза нередко используют лисички, измельченные до порошкообразного состояния. Чтобы приготовить лечебное средство, следует 1 ч.л. сырых грибов залить 150 мл качественной водки или медицинского спирта (70%). Состав оставить в темном прохладном месте на 10 дней. Бутылку с настойкой необходимо периодически встряхивать.
Готовое средство принимать по несколько чайных ложек ежедневно. Курс терапии длится 2 месяца.
Другие меры терапии
Несмотря на то, что народные средства менее токсичны, их нельзя использовать как основное лечение при токсокарозе. Их сочетают с препаратами, прописанными врачом. Дети и взрослые лечатся лекарствами на основе таких действующих веществ:
- альбендазол (Немозол, Зентел);
- мебендазол (Вермокс, Вормин).
Также прописываются лекарства, сокращающие симптомы болезни:
- антигистаминные (Зиртек, Цетрин);
- гепатопротекторы (Карсил, Гепатрин);
- противовоспалительные (Диклофенак, Ибупрофен);
- сорбенты (Бак-Сет, Энтеросгель).
Длительность лечения и дозировка зависит от степени поражения токсокарозом, возраста больного. Важно также придерживаться диеты: исключить сладкое, мясные продукты. Стараться кушать больше свежих фруктов и овощей, молочных продуктов и растительных масел. Необходимо пить до 2 литров воды ежедневно.
Рассмотрены факторы риска паразитозов у детей, действие паразитов на организм ребенка, подходы к диагностике паразитарной инвазии и принципы комплексного лечения паразитозов с тем чтобы предотвратить дальнейшее развитие функциональных нарушений с формиров
Risk factors of parasitosis in children was considered, as well as the influence of parasites on a child's body, approaches to the diagnostics of parasitic invasions and principles of integrated treatment of parasitic diseases in order to prevent the further development of functional disorders of the formation of organic pathology.
.jpg)
Паразитарное заболевание — развитие болезненных симптомов в результате жизнедеятельности гельминта или простейших в организме человека [1]. Основной фактор выживания и распространения паразитов — их необычайно высокая репродуктивная способность, а также постоянно совершенствующиеся механизмы приспособления к обитанию в теле человека. К сожалению, настороженность медицинских работников в отношении паразитарных заболеваний у населения в настоящее время чрезвычайно низка, а профилактика гельминтозов сведена к лечению выявленных инвазированных пациентов [12, 13]. Вместе с тем многие исследователи отмечают связь широкой распространенности паразитозов у детского населения с развитием функциональной патологии органов пищеварения на фоне нарушений регуляции и высокий риск формирования хронических заболеваний даже при условии естественной санации ребенка с течением времени.
Самые распространенные и изученные заболевания — аскаридоз, энтеробиоз (рис. 1) и лямблиоз — регистрируются повсеместно. В России ежегодно выявляется более 2 млн больных нематодозами. При оценке территориального распределения лямблиоза по России установлено, что самый высокий средний уровень показателей заболеваемости в течение многих лет отмечен в Санкт-Петербурге, причем пораженность детей, посещающих детские учреждения, составляет 35% [2].
Каждый человек в течение жизни неоднократно переносит различные паразитарные заболевания [9]. В детском возрасте паразитозы встречаются чаще. У детей раннего возраста (до 5 лет) этому способствует широкая распространенность репродуктивного материала паразитов (цисты, яйца, личинки (рис. 2)) в окружающей среде и недостаточное развитие гигиенических навыков.
.jpg)
Значимость определенных факторов риска меняется в соответствии с возрастом ребенка. Доказано, что для детей младшего возраста более значимы санитарно-гигиенические условия проживания, а для подростков при сборе анамнеза необходимо уделить внимание социально-экономическим и географическим факторам (пребывание в лагере, туристическая поездка, наличие младшего брата или сестры) (рис. 3).
.jpg)
Транзиторное снижение противоинфекционного иммунитета как фактор риска возникновения паразитоза у детей регистрируется также в период реконвалесценции после вирусных заболеваний, вызываемых вирусами герпетической группы (цитомегаловирус, вирус простого герпеса I и II, вирус Эпштейна–Барр), может возникать в результате ятрогении (применение иммуносупрессивной терапии при аллергических и аутоиммунных заболеваниях). В настоящее время значимая доля детей находится в состоянии дезадаптации, которое также сопровождается снижением иммунной защиты.
Иммунную защиту желудочно-кишечного тракта (ЖКТ) ребенка можно условно разделить на специфическую и неспецифическую. К неспецифической защите относят комплекс условий нормального пищеварения: зрелость ферментативных систем, обеспечение кислотно-щелочного градиента в различных отделах ЖКТ, деятельность нормальной микрофлоры, адекватную моторику.
Отдельно необходимо отметить, что для такого заболевания, как лямблиоз, предрасполагающим фактором инвазии является нерегулярное и недостаточное отделение желчи в кишечник при аномалиях развития желчного пузыря (перетяжки, перегибы). Лямблиоз, выявленный у пациентов педиатрического отделения МОНИКИ, в 100% случаев сопровождался дисфункцией билиарного тракта.
.jpg)
У детей в восстановительном периоде после острых кишечных инфекций, после массивной антибиотикотерапии, а также у пациентов с хронической патологией органов пищеварения сопутствующие нарушения ферментного обеспечения, нормофлоры и моторики кишечника также делают ЖКТ более уязвимым для паразитов (рис. 4).
Специфическая защита слизистой оболочки органов пищеварения зависит от возраста ребенка и его зрелости. Механизм специфической иммунной защиты является одной из наиболее древних систем организма, так как гельминтозы сопровождают человечество в течение многих тысячелетий. Этот механизм представлен прежде всего эозинофилами крови и иммуноглобулином Е.
Классический развернутый антипаразитарный ответ может быть сформирован у ребенка не ранее достижения им 4 лет и тесно связан с качеством и количеством IgE, созревающего к этому возрасту. При контакте организма с паразитом в первую очередь выделяются медиаторы воспаления: интерлейкин, лейкотриен С4, D4, простагландины, тромбоксаны. Увеличивается количество лимфоцитов, продуцирующих IgM и IgG. В клиническом анализе крови отмечается рост уровня эозинофилов и базофилов, связанный с увеличением содержания этих клеток в тканях инвазированного органа. Встречаясь с личинками паразита, тканевые базофилы выделяют гепарин и гистамин, которые в сочетании с лейкотриенами и другими медиаторами воспаления вызывают общие проявления: зуд, реактивный отек, гиперемию, а также могут спровоцировать общие проявления: бронхоспазм, проявления крапивницы или диарею. Аллергическое воспаление при паразитозах развивается по классическому пути и призвано создать условия, приводящие к гибели и/или элиминации паразита [5].
Вместе с тем эозинофилы обладают выраженным цитотоксическим потенциалом, превышающим возможности других клеток крови, что объясняет первостепенное значение эозинофилов в антипаразитарных реакциях и их повреждающую роль при аллергии. Основное действие эозинофилы оказывают в барьерных тканях. В очаге инвазии они дегранулируют, оказывая гельминтотоксическое и цитотоксическое действие. Белки эозинофильных гранул (большой основной протеин, эозинофильная пероксидаза, эозинофильный катионный протеин, эозинофил-производный нейротоксин) токсичны не только для паразита, но и для клеток организма ребенка. Еще одной из важных причин системных и органных поражений, сопутствующих паразитозам, является образование иммунных комплексов [9, 10].
Действие паразитов на организм ребенка осуществляется с вовлечением многих систем. Практически все их виды могут вызывать сдвиг соотношения Th1/Th2 клеток в направлении, благоприятном для их выживания. Описаны случаи, когда продукты выделения паразита оказывали гормоноподобное действие на организм хозяина [5].
Местное влияние паразиты осуществляют, вызывая контактное воспаление слизистой оболочки и стимулируя вегетативные реакции. При этом нарушаются процессы кишечного всасывания, адекватная моторика ЖКТ и его микробиоценоз.
Системное влияние оказывается за счет использования паразитом энергетического и пластического потенциала пищи в ущерб организму ребенка, индукции аллергии и аутоиммунных процессов, целенаправленной иммуносупрессии и эндогенной интоксикации. Проведенными исследованиями показано, что аллергический синдром сопутствует аскаридозу и энтеробиозу в 71,3% случаев. Среди детей с атопическим дерматитом паразитозы выявляются у 69,1%, при этом лямблиоз из числа всех инвазий составляет 78,5% [4].
Особенно узнаваемую клиническую картину формирует токсокароз (рис. 5). Клиническими маркерами этой инвазии являются лейкемоидная реакция эозинофилов (от 20% и выше эозинофилов в формуле крови), сопровождающая ярко и упорно протекающий аллергический синдром в виде атопического дерматита с выраженным зудом и резистентностью к традиционной терапии или тяжелую бронхиальную астму с частыми приступами.
В 75,3% случаев паразитозы сопровождаются разнообразными функциональными нарушениями со стороны ЖКТ. Рядом работ доказано, что паразитарная инвазия способна вызывать нарушения углеводного обмена, а также дисахаридазную недостаточность за счет снижения уровня лактазы [7, 9].
У большинства детей нарушения адаптации являются одним из важных звеньев патогенетического процесса при паразитозе. Следует отметить, что состояние дезадаптации затрагивает в первую очередь лимфоцитарное звено иммуногенеза, что не может не сказываться на созревании и дифференцировке специфического иммунитета.
Диагностика паразитозов
До настоящего времени ведется поиск простого, доступного и надежного метода диагностики паразитозов. Разработанные методики прямого визуального обнаружения требуют минимальной экспозиции диагностического материала, многократных повторных исследований. Известные способы диагностики глистных инвазий и протозоозов, такие как метод толстого мазка фекалий по Като, метод формалин-эфирного осаждения, перианальный соскоб, микроскопия пузырной и печеночной желчи, имеют ряд недостатков, связанных как с особенностями развития паразита, так и с состоянием макроорганизма и его реактивностью.
Непрямые методы исследования (определение специфических антител) обладают недостаточной специфичностью и достоверностью. Известно, например, что, проходя сложный цикл развития от яйца до взрослого состояния, гельминты меняют свой антигенный состав. Антитела в организме хозяина вырабатываются в основном в ответ на поступление экскретов и секретов гельминта, тогда как в иммунодиагностических реакциях используются соматические антитела. Возникающая неспецифическая сенсибилизация организма, общность некоторых антигенов трематод, простейших и человека создают высокий удельный вес ложноположительных серологических реакций в титрах ниже достоверно диагностических. Таким образом, исследование методом иммуноферментного анализа (ИФА) на гельминты является высокочувствительным, но низкоспецифичным методом. Определение паразитов методом полимеразной цепной реакции (ПЦР) является высокоспецифичным и высокочувствительным методом, но из-за дороговизны и сложности не может быть скрининговым, когда, например, нужно обследовать группу детей из детского учреждения.
Не теряет своей актуальности клинический осмотр ребенка и внимательный учет косвенных признаков паразитоза. Важно отметить возможность течения паразитоза при аллергическом и астеническом синдроме, полилимфаденопатии неясного генеза, при нарушениях кишечного всасывания, углеводного обмена, при затяжном и хроническом течении болезней пищеварительного тракта, гепатоспленомегалии неясного генеза. Течение паразитарной инвазии имеет клинические особенности: обычно признаки поражения минимизированы, заболевание носит стертый характер, обострения полиморфны и неярки. Особенностью обострений заболеваний данной группы является их цикличность с периодом в 11–15 дней.
Косвенными лабораторными признаками паразитоза могут быть анемия, базофилия, эозинофилия, увеличение уровня аспартатаминотранферазы (АСТ).
Кроме того, признаки возможной паразитарной инвазии следует учитывать при оценке результатов инструментального исследования. При ультразвуковом исследовании органов брюшной полости у ребенка старше 3 лет косвенными признаками паразитоза являются гепатоспленомегалия, неравномерность паренхимы печени и селезенки за счет мелких гиперэхогенных сигналов, увеличенные лимфатические узлы в воротах селезенки.
Лечение гельминтозов
Лечение гельминтозов должно начинаться с применения специфических антигельминтных препаратов. Современный арсенал лекарственных средств, используемых для лечения кишечных паразитозов, включает значительное количество препаратов различных химических классов [11]. Они применяются как в клинической практике для лечения выявленных больных, так и с целью массовой профилактики.
Определяя препарат для специфической противопаразитарной терапии, следует понимать, что спектр действия этих препаратов не особенно широк. Практически все препараты этой группы применяются многие десятки лет и целесообразно предположить, что паразиты выработали системы приспособления и заболевание может быть резистентным к проводимой терапии. По данным Г. В. Кадочниковой (2004), эффективность такого традиционного препарата, как Декарис, в современных условиях не достигает 57%. Кроме того, эта группа противопаразитарных средств, к сожалению, имеет ряд побочных эффектов: тошноту, рвоту, абдоминальный синдром.
Таким образом, в современных условиях следует отдавать предпочтение более современным препаратам, которые, во-первых, являются универсальными для лечения как нематодозов, так и смешанных глистных инвазий и активны в отношении такого распространенного паразита, как лямблия. Во-вторых, использование одного противопаразитарного препарата, а не их комбинации, ощутимо снижает риск неприятных побочных эффектов. На сегодняшний день единственный представитель этой группы в нашей стране — альбендазол (Немозол).
Для лечения аскаридоза у детей старшего возраста или при рецидивировании заболевания в настоящее время под наблюдением врача может быть применен комбинированный прием антигельминтных средств (например, альбендазол в течение трех дней, затем — Вермокс в течение трех дней). Непременным условием успешной дегельминтизации больных энтеробиозом являются одновременное лечение всех членов семьи (коллектива) и строгое соблюдение гигиенического режима для исключения реинвазии. Следует отметить, что важное значение имеет ежедневная влажная уборка, так как были описаны казуистические случаи распространения репродуктивного материала остриц на частичках пыли на высоту до 1,5 метра.
В педиатрической клинике МОНИКИ разработаны принципы терапии паразитозов, учитывающие особенности патогенеза инвазии и позволяющие качественно и надежно вылечить данную группу заболеваний. Благодаря применению разработанной схемы терапии удается эффективно предотвратить реинвазию и развитие функциональных нарушений органов пищеварения у детей.
Принципы терапии больных паразитозами
1. Прием антипаразитарных препаратов проводится с учетом вида возбудителя инвазии.
Препараты, применяемые в лечениии аскаридоза:
- Вермокс (мебендазол) (для детей с 2 лет) — по 100 мг 2 раза в сутки в течение 3 дней;
- Пирантел — 10 мг/кг однократно;
- Немозол (альбендазол) (для детей с 2 лет) — 400 мг однократно.
Препараты, применяемые в лечении энтеробиоза:
- Вермокс (мебендазол) (для детей с 2 лет) — 100 мг однократно;
- Пирантел — 10 мг/кг однократно;
- Немозол (альбендазол) (для детей с 2 лет) — 400 мг однократно.
Препараты, применяемые в лечении лямблиоза:
- орнидазол 25–30 мг/кг (если масса тела больше 35 кг — 1000 мг) в два приема в течение 5 дней, 1 день — 1/2 дозы, повторный курс через 7 дней;
- Макмирор (нифурател) — по 15 мг/кг 2 раза в сутки в течение 7 дней;
- Немозол (альбендазол) — по 15 мг/кг однократно в течение 5–7 дней.
2. Лечение паразитоза предусматривает измененные в результате жизнедеятельности паразитов свойства пищеварительного тракта ребенка (функциональные нарушения органов пищеварения, ферментопатия, изменение микробиоценоза) и их коррекцию курсами ферментных препаратов и синбиотиков (табл. 1).
3. Обязательное применение энтеросорбентов и комплекса поливитаминов с микроэлементами (табл. 2 и 3).
Таким образом, разработанные в клинике педиатрии МОНИКИ принципы комплексной терапии паразитозов у детей предусматривают поэтапное восстановление функционального состояния ЖКТ, нарушенного в результате местного и системного влияния паразитов. Применение комплексной терапии позволяет предотвратить дальнейшее развитие функциональных нарушений с формированием органической патологии, а также избежать реинвазии.
Литература
Л. И. Васечкина 1 , кандидат медицинских наук
Т. К. Тюрина, кандидат медицинских наук
Л. П. Пелепец, кандидат биологических наук
А. В. Акинфиев, кандидат медицинских наук
Токсокароз – это хроническое инфекционное заболевание, вызываемое личинками круглого червя токсокары. Для инвазии характерна лихорадка, рецидивирующие высыпания и увеличение размеров печени. Патология сопровождается поражением глазных яблок и внутренних органов: сердца, головного мозга, легких. Диагностика заключается в обнаружении специфических антител к возбудителю. Лечение этиотропное (антигельминтные препараты), также применяются средства симптоматической терапии, в некоторых случаях производятся хирургические вмешательства.
МКБ-10
B83.0 Висцеральная форма заболеваний, вызываемых миграцией личинок гельминтов [висцеральная Larva migrans]
Общие сведения

Причины токсокароза
Возбудитель – круглый червь Toxocara, наиболее часто встречаются инвазии видами Т. сanis (собачий) и T. сati (кошачий). Основной цикл развития паразита не включает в себя человеческий организм, поэтому люди оказываются случайными хозяевами гельминта, который в подобных условиях неспособен достигать половозрелой формы. Источником инфекции является больное животное (чаще собака), больной человек эпидемиологически не опасен. Считается, что доля зараженных токсокарозом среди взрослых собак варьирует от 15 до 50%, щенков – до 80%.
Больные животные выделяют яйца гельминтов с фекалиями, сами паразиты в половозрелой форме находятся у постоянного хозяина в пищеварительном тракте. Наиболее опасными считаются дворы, детские площадки, парки, поскольку контаминация земли яйцами паразита встречается в 10-40% почвенных проб. Инфицирование людей происходит контактным и пищевым путем – при поглаживании, играх со зверями, особенно бродячими, употреблении в пищу немытых ягод, фруктов и овощей. Отмечено, что тараканы могут поглощать яйца токсокар с последующим выделением до 25% потенциально жизнеспособных особей, что играет важную роль в распространении инфекции в быту.
Патогенез
После попадания яиц токсокары в тонкий кишечник человека (преимущественно двенадцатиперстную кишку) высвобождаются личинки, проникающие в системный кровоток через слизистую оболочку. Сначала токсокары заносятся в печень и правую половину сердца, затем в легочную артерию и левый желудочек, откуда выходят в большой круг кровообращения. Распространяясь по организму, личинки оседают в различных органах и тканях, вызывая геморрагические и некротические изменения, образование воспалительных очагов в виде гранулем, в центре которых находится некротизированная ткань и личинка, вокруг – воспалительный инфильтрат.
При попадании в кровеносное русло продуктов жизнедеятельности возникают аллергические реакции. Часть личинок гибнет, оставшиеся гельминты выделяют особую маскирующую субстанцию, которая позволяет им персистировать в организме до 10 лет, периодически мигрируя по кровеносной системе и поражая новые ткани. Характерной особенностью токсокар является формирование гранулем в поджелудочной железе, головном мозге, печени, легких, миокарде и мезентериальных лимфатических узлах. Патогенез поражения глаз до конца не изучен, имеются гипотезы о низкой активности инвазии и малой выраженности иммунного ответа.
Патогенез эпилепсии при токсокарозе окончательно не ясен. Предполагается, что поражение головного мозга может привести к формированию волокнистых рубцов после острого воспаления или хронических гранулем. Другая теория объясняет появление эпилептических припадков при повреждении нейронов усиленным образованием провоспалительных цитокинов из-за повышения проницаемости гематоэнцефалического барьера, вызываемого паразитами, а также аутоантителами к нейрональным элементам, которые нередко обнаруживаются у больных токсокарозом.
Классификация
Классификация токсокароза у человека основывается на глубине инвазии в организм человека. Гельминтоз практически всегда протекает с минимальной либо неспецифической клиникой (субклинически), бессимптомная форма встречается в 13% случаев заболевания, органные поражения более характерны для детей. Выделяют следующие виды токсокароза:
- Глазной.Типичен для детей старше 8 лет, подростков и молодых взрослых. Поражение зрительного аппарата обычно одностороннее, протекает в виде хронического эндофтальмита, увеита, абсцессов стекловидного тела, папиллитов, кератитов и косоглазия. При длительном течении возможна слепота.
- Висцеральный.Протекает остро или хронически с вовлечением дыхательной системы, сердца, кожи, лимфатических узлов, селезенки, печени, суставов и мышц. Часто наблюдается диарея, тошнота и рвота. Описаны поражения головного мозга: рецидивирующие головные боли, менингоэнцефалит, эпилептические припадки.
Симптомы токсокароза
Инкубационный период определить сложно, считается, что он может занимать несколько лет. При остром начале наблюдается лихорадка до 38,5°C и выше, поражения дыхательной системы – от заложенности носа, сухого кашля и першения в горле до тяжелой одышки и астматического статуса. На коже появляется зудящая сыпь в виде волдырей и пятен, при подкожном расположении личинок видны приподнятые над поверхностью прямые или извилистые красновато-коричневые ходы. У детей нередко выявляются увеличенные плотноэластические безболезненные лимфоузлы. Пациенты с токсокарозом часто предъявляют жалобы на боли в животе, тошноту, иногда – рвоту и срывы стула.
Осложнения
Наиболее частые осложнения висцерального токсокароза – бронхиальная астма, хронический бронхит и эпилепсия, глазного – отслойка сетчатки и односторонняя слепота. Подкожное расположение личинок токсокар приводит к присоединению вторичной бактериальной инфекции, образованию инфильтраов, абсцессов и флегмон, поражение легких – к тяжелым пневмониям смешанной этиологии с нарастающей дыхательной недостаточностью. Массивная инвазия гельминтов, полиорганное поражение могут стать причиной летального исхода. У беременных женщин токсокароз часто выявляется невынашивание, задержка внутриутробного развития плода.
Диагностика
Диагноз токсокароза подтверждается врачом-инфекционистом. Для исключения сочетания висцерального и глазного гельминтоза обязательным является осмотр офтальмолога, по показаниям назначаются консультации других специалистов. Диагностические методы, необходимые для верификации токсокарозного поражения, включают следующие методики:
Дифференциальную диагностику проводят с аскаридозом, при котором нередко наблюдаются кишечная непроходимость, острая обструкционная дыхательная недостаточность. Необходимо исключить описторхоз и стронгилоидоз, которые протекают с желтухой, болями в правом подреберье и срывами стула. Глазную форму токсокароза дифференцируют от ретинобластомы, проявляющейся лейкокорией, косоглазием, слезотечением, светобоязнью, вторичной глаукомой. Кожные проявления могут быть следствием укусов насекомых, воздействия аллергенов.
Лечение токсокароза
Показанием для стационарного лечения являются висцеральные формы болезни. Постельный режим назначается только при наличии лихорадки и рекомендуется до 2-4 дней устойчивого отсутствия высоких цифр температуры тела. Специальной диеты нет, однако, учитывая некоторые побочные эффекты применяемых препаратов, рекомендуется воздержаться от приема жирной, жареной пищи, алкоголя, специй, маринадов, сладостей. Важно соблюдение питьевого режима, исключение контакта с возможными пищевыми и бытовыми аллергенами. Недопустимо самовольное прекращение начатого медикаментозного лечения.
- Антигельминтная терапия. Высокоэффективными антигельминтными средствами для разрушения мигрирующих личинок считаются албендазол, мебендазол, диэтилкарбамазин, которые применяются в таблетированных формах. В отношении токсокар, находящихся в гранулемах, данные препараты не обладают выраженным нейтрализующим эффектом.
- Хирургические методы лечения применяются при глазном токсокарозе и включают в себя микрохирургическое удаление гранулем, лазерную коагуляцию для расщепления личинок в средах глаза и коррекции отслойки сетчатки.
- Симптоматическая терапия проводится по показаниям. Включает жаропонижающие (парацетамол, целекоксиб), дезинтоксикационные (хлосоль, глюкозо-солевые растворы), десенсибилизирующие (глюконат, хлорид кальция), антигистаминные (хлорапирамин, дезлоратадин), отхаркивающие (ацетилцистеин, мукалтин), ферментативные (панкреатин) и другие средства.
Прогноз и профилактика
Прогноз при неосложненных формах благоприятный, летальных случаев не описано. Длительность приема лекарственных средств может составлять до 3-4 недель и более, иногда требуются несколько курсов с перерывами в 2-4 месяца. Критериями эффективности считаются исчезновение клиники, снижение уровня антител и эозинофилии крови. Описаны случаи диссеминированного токсокароза среди ВИЧ-инфицированных лиц в стадии СПИДа, а также пациентов, длительно принимающих системные глюкокортикостероиды или проходящих лучевую терапию по поводу онкологических болезней.
Профилактические вакцины на основе ДНК показали положительный эффект в экспериментах на мышах, исследования в настоящее время продолжаются. Рекомендуется осуществлять контроль за популяцией бродячих животных, проводить выгул собак на специально отведенных территориях. Важными мерами неспецифической борьбы с заболеваемостью являются отучение детей от поедания земли, привитие навыков личной гигиены после игр на улице, песочнице, общения с животными; тщательное мытье ягод, зелени, овощей и фруктов перед едой; назначение антигельминтных препаратов беременным собакам, новорожденным щенкам.
2. Токсокароз. Клиника. Диагностика. Лечение. Профилактика. Информационно¬методическое пособие. – 2004.
4. Токсокароз у детей/ Глазунова Л.В., Артамонов Р.Г., Бекташянц Е.Г., Куйбышева Е.В., Шиц О.Л., Кирнус Н.И., Иванова Е.Ю. // Лечебное дело. – 2008.

Самые распространенные виды глистов — острицы и аскариды
— Марина Зеноновна, о каких видах глистов стоит знать в первую очередь?
— Думаю, многие слышали о так называемом энтеробиозе — это разновидность гельминтоза, вызываемого червями из рода остриц (полостной червь некрупного размера, относится к группе круглых червей белого или серо-белого цвета). По последним данным, из большинства известных случаев до 37% людей страдают от поражения именно этими глистами. Хотя лично я уверена, что цифра занижена, так как, в основном, исследуются группы детей, но ведь взрослые заражаются тоже.
На втором месте аскаридоз — это разновидность гельминтоза, вызванная круглыми червями, принадлежащими к классу нематод, семейству аскариды (круглый червь красноватого цвета (после гибели цвет тела изменяется на желтовато-белый). Распространенность в популяции у него в несколько раз ниже, однако течение аскаридоза более тяжелое и характеризуется рядом серьезных осложнений.
Всего в Беларуси встречается около 20 видов гельминтов. Кроме того, заражение может быть комбинированным, когда в организме выявляются разные группы гельминтов.
Симптомы заражения редко проявляют себя сразу
— Где конкретно в теле человека живут эти паразиты?
— Их локализация сложная, существует много классификаций и в зависимости от вида, а также миграции личинок, обосноваться глисты могут где угодно: в печени, кишечнике, легких и даже головном мозге.
— Чем опасны гельминты?
— Опасность будет определяться степенью инвазированности, то есть количеством попавших в организм личинок и степенью их развития. Большую роль играет иммунитет, так как большинство паразитов погибает уже при поступлении благодаря слюне, желудочному соку, ферментам и так далее. Те гельминты, которым все-таки удалось выжить, поражают организм и мешают его гармоничной работе.
Симптомы и у детей, и у взрослых могут быть самыми разными:
- отсутствие аппетита;
- расстройство желудка;
- тошнота и рвота;
- неприятный запах изо рта;
- непроходящий насморк и кашель;
- высыпания на коже;
- ночной зуд вокруг ануса;
- боли в области пупка;
- повышенная утомляемость
Обычно вышеперечисленные сигналы организм подает на более поздних стадиях развития глистной инвазии. На ранних этапах заподозрить что-то достаточно сложно.
Глисты не любят лук и чеснок
— Почему считается, что дети больше подвержены заражению, чем взрослые?
— Во-первых, у взрослых организм крепче. Иммунитет, как правило, выше, и он лучше справляется с непрошеными гостями.
Во-вторых, уровень pH в желудке у малышей и их родителей разный. У деток он нейтральный. У взрослых — кислотность выше, а гельминты очень не любят кислую среду.
В-третьих, у взрослых другой рацион питания. Что повышает кислотность? Лук, чеснок, горчица, острые специи, горькие травы (вроде полыни, трифоли, зверобоя) и…алкоголь. При употреблении данных продуктов желудочный сок становится особенно едким, что не дает шансов на жизнь многим паразитам, попавшим туда. Хотя взрослые употребляют и термически не обработанные рыбу, мясо и морепродукты, в которых как раз-таки могут содержаться гельминты. Это определенный риск.
С модой на здоровый образ жизни на столах многих людей появились свежевыжатые соки. Это хорошо, они содержат фитонциды, которые подавляют развитие паразитов и даже убивают их. Особенное внимание я бы рекомендовала обратить на морковный, капустный и свекольный соки.

За питанием мальчиков и девочек следят родители, которые, скорее, согласятся дать младшеньким конфетку, нежели лук (хотя в маленьком количестве, если ребенок хочет, ему вполне можно разрешить попробовать этот овощ, разумеется, учитывая индивидуальные особенности здоровья малыша).
К сожалению, сегодня появился красивый и вкусный фастфуд, который дети очень любят. А ведь подобная пища — это быстрые, легко усвояеемые углеводы, которые меняют кислотность желудка не в сторону повышения, а как раз готовят уютную и приятную среду обитания для паразитов.
— Какое назначается лечение?
— Не стоит принимать решений самостоятельно, особенно по отношению к своим деткам. Если возникли какие-то подозрения, обратитесь к терапевту или педиатру. Врач назначит анализ, по результатам которого определит, есть ли заражение и какова его степень.
Для диагностики необходимо исследование кала на наличие гельминтов (кал на яйца глист). Помогает и общий анализ крови. О возможной проблеме говорит: пониженное содержание гемоглобина, повышенное СОЭ, повышенное количество эозинофилов. Эффективен также современный метод лабораторной диагностики — исследование крови с помощью ИФА.
Исходя из полученных данных, а также из особенностей конкретно вашего организма или организма ребенка, специалист подберет подходящий препарат и (что очень важно) его дозу.
Важно! Так как энтеробиоз отличается достаточно высокой контагиозностью (свойство инфекционных болезней передаваться от больных людей или животных здоровым восприимчивым людям (животным), то необходимо обследование и родственников инвазированного. Поэтому может понадобиться лечение не только человеку, у которого выявлен гельминтоз, но и всем членам семьи (и взрослым, и детям, и даже домашним животным).
Глисты достаточно долго живут в открытой среде, передаются при контактах и через предметы от инвазированного к здоровому человеку. Вот почему так важна личная гигиена.
Кормящим мамам и беременным женщинам нужно быть особенно внимательными
— Назначаются ли такие препараты беременным женщинам?
— Гельминтоз — это крайне нежелательная ситуация для беременных женщин. Хорошо бы постараться все проверить и уладить вопрос еще на стадии планирования беременности.
Если все же выявилось заражение, конечно, процесс нельзя запускать. Проблему необходимо решать. Специальных противогельминтных препаратов для беременных нет. Поэтому врач, внимательно изучив состояние женщины, пойдет по пути наименьшего сопротивления. Он должен подобрать индивидуальную схему лечения, которая будет эффективной, но при этом щадящей для организма в каждом конкретном случае.
— Передаются ли глисты от мамы к ребенку через молоко?
— Нет. В молоке как раз наоборот содержатся иммуноглобулины, защищающие ребенка. Но ведь мама контактирует с малышом, поэтому через прикосновение, бутылочки, одежду и так далее она все равно может передать личинки паразитов.

Кстати, думаю, все понимают, что если кормящей маме назначили противогельминтный препарат, ее должны предупредить, что на этот период необходимо перевести ребенка на искусственное питание, так как вместе с молоком выводятся и токсичные вещества принимаемого лекарственного средства. Организм малыша к таким серьезным нагрузкам не готов.
Глисты собак более опасны для человека, чем глисты кошек
— Как часто нужно сдавать анализ на наличие глистов?
— Мнения специалистов тут разнятся. Многие эпидемиологи считают, что необходимо проводить курсовые приемы профилактических препаратов целым группам (в детских садах, школах, рабочих учреждениях). Но ведь если хотя бы один человек отказался от этих действий, смысла в них особо нет. Даже если останется единственный инвазированный, как я уже говорила, шансы на дальнейшее распространение гельминтов очень высоки.
Но это не значит, что не стоит время от времени обследовать свой организм и помогать ему, если вдруг что-то не так. Вспышка заболевания наблюдается обычно весной (апрель-май) и осенью (октябрь-ноябрь). В данные периоды хорошо бы самостоятельно обратиться к педиатру, терапевту, сдать анализ и проверить, все ли хорошо, а заодно (если говорить о детях) при выявлении проблемы было бы неплохо предупредить об этом воспитателя группы в детском саду или учителя в школе, чтобы они сообщили всем другим родителям и приняли меры.
— Передаются ли гельминты от животных к хозяевам?
— Да, притом кошки, как правило, передают больше их видов, чем собаки, но гельминты последних более серьезны. Так, например, собаки могут стать причиной токсокароза у человека. Это гельминтоз из группы нематодозов, характеризующийся лихорадкой, бронхитом, пневмонией, гепатоспленомегалией, эозинофилией.

Если у вас есть домашнее животное, не забывайте о следующих правилах:
- не целуйте питомцев;
- не пускайте их в свою постель;
- не забывайте часто мыть руки, особенно перед едой;
- своевременно проводите осмотр животного у ветеринара;
- если у собаки обнаружились глисты, обратитесь к врачу, скорее всего, пропить лекарства будет необходимо всей семье;
- старайтесь выгуливать любимцев в положенном месте.
Хочу обратить внимание любителей всего необычного на тот факт, что прежде, чем приобрести экзотическое животное, подробно изучите информацию о его физиологии, убедитесь, что оно здорово, узнайте о возможных рисках. Ведь черепашки, обезьянки, игуаны, лемуры и так далее могут принести в ваш дом паразитов, с которыми совершенно незнаком наш организм. Все это иногда приводит к большим трудностям как в диагностике, так и в лечении.
Читайте также:

