Как определить очаг инфекции
Обновлено: 19.04.2024
Источники инфекций. Распространение инфекционных болезней
Источники инфекции. Инфекционный процесс может быть вызван как представителями нормальной микрофлоры организма хозяина (эндогенные инфекции), так и микроорганизмами извне (экзогенные инфекции).
Условно-патогенные бактерии нормальной микрофлоры кишечника становятся источниками инфекции только при определённых условиях (например, при перфорации кишечника). Энтеробактерии и неспорообразующие анаэробы (например, Bacteroides fragilis) вызывают внутрибрюшинные абсцессы. При попадании в лёгкие содержимого желудочного и ротоглотки, в котором присутствуют представители нормальной микрофлоры (факультативные и облигатные анаэробы), развивается пневмония или абсцесс лёгкого.
Обитающий на слизистой оболочке передних отделов носовых ходов Staphylococcus aureus может вызвать раневую инфекцию после хирургического вмешательства. Нейтропенический сепсис (бактериемия) возникает, когда бактериям удаётся преодолеть внутренние защитные механизмы слизистой оболочки кишечника или при снижении функции нейтрофилов во время химиотерапевтического лечения лейкемии. Различные изменения в организме хозяина повышают риск развития заболеваний: хирургическое вмешательство и катетеризация сосудов способствуют развитию инфекций, вызываемых представителями нормальной микрофлоры; применение иммунодепрессантов увеличивает риск возникновения оппортунистических инфекций, вызываемых возбудителями с низкой вирулентностью.
Источником экзогенных инфекций могут стать различные животные (зоонозныс инфекции). В этом случае заражение происходит контактно-бытовым и пищевым путями. Кроме того, инфекции могут быть вызваны микроорганизмами, обитающими в окружающей среде (например, Legionella или Clostridium).
Изменение условий окружающей среды ведёт к выраженному повышению риска заражения. Так, распространению зоонозных инфекций способствовало активное развитие сельского хозяйства и земледелия. Например, скармливание крупному рогатому скоту белков животного происхождения привело к возникновению эпидемии губчатой энцефалопатии, которая затем распространилась среди людей (вариантная болезнь Крейцфельдта—Якоба).
Развитие птицеводства способствовало распространению сальмонеллёза (факторы передачи — пух и перо домашней птицы), а механизация пищевой промышленности — повышению риска перекрёстной контаминации. Избежать подобных проблем позволяет совершенствование методов ведения сельского хозяйства и соблюдение санитарно-гигиенических норм.
Недостаточный контроль систем вентиляции в зданиях приводит к возникновению заболеваний, вызываемых Legionella pneumophila.
Сложный жизненный цикл некоторых микроорганизмов помогает им выжить в неблагоприятных условиях и способствует их распространению. Например, возбудители, выделяющиеся из организма хозяина с экскрементами, как правило, передаются посредством фекально-орального механизма. Многие возбудители часть своего жизненного цикла проводят в организме переносчика, и в этом случае заражение происходит во время укуса. Иногда в качестве промежуточного хозяина паразиты могут использовать не животных, а человека (например, при эхинококкозе).

Выживание и распространение возбудителей инфекций
Каждый микроорганизм по-своему приспосабливается к условиям окружающей среды. Так, бактерии способны долгое время выживать в неблагоприятных условиях в виде спор — покоящихся клеток со сниженным метаболизмом, снабжённых твёрдой многослойной оболочкой. Яйца гельминтов также снабжены твёрдой оболочкой, помогающей им выживать в окружающей среде. Распространению возбудителей способствует их длительное персистирование в организме хозяина, который в этом случае становится резервуаром инфекции.
Микроорганизмы, выделяющиеся в окружающую среду при чихании, могут долгое время находиться в воздухе в составе микроскопических капель (5 мкм). Инфекционный процесс возникает при их попадании в лёгкие здорового человека (воздушно-капельный путь передачи). Этим способом происходит распространение как возбудителей респираторных заболеваний (вирусы гриппа и др.), так и микроорганизмов, поражающих другие органы (например, Neisseria meningitides).
Возбудителей желудочно-кишечных расстройств (Salmonella) можно обнаружить в воде и пище (алиментарный путь передачи). Такое распространение инфекции наблюдают при токсоплазмозе и цистицеркозе, поражающих различные органы.
Через неповреждённый кожный покров проникают Leptospira, Treponema и Schistosoma. Передача ВИЧ происходит во время инъекций и переливаний крови (при нарушении кожного барьера). Представители нормальной микрофлоры кожного покрова (Staphylococcus epidermidis) могут проникать в организм через венозный катетер. Переносчиками некоторых инфекций служат насекомые, питающиеся кровью (например, малярию переносят самки комара рода Anopheles).
При половом контакте происходит передача микроорганизмов, не способных к жизни вне организма человека (например, Neisseria gonorrhoeae или Treponema pallidum). При этом заражению способствуют изъязвления слизистой оболочки половых органов.
Факторы распространения инфекций
Улучшение социальной обстановки и условий окружающей среды способствует снижению риска заражения и распространения инфекционных болезней. Например, соблюдение санитарно-гигиенических норм ведёт к уменьшению риска возникновения диареи, а улучшение жилищных условий препятствует распространению туберкулёза. Кроме того, полноценное питание уменьшает восприимчивость человека к инфекционным заболеваниям.
Однако как ни парадоксально, с увеличением уровня жизни возрастает и смертность от некоторых инфекционных заболеваний. Тяжесть осложнений инфекционного процесса прямо пропорциональна возрасту пациента, например при паралитическом полиомиелите или ветряной оспе.
Просвещение населения и распространение инфекций. Существует большое количество программ медицинского просвещения населения, охватывающих такие проблемы, как половое воспитание, рекомендации для беременных, соблюдение правил личной гигиены (гигиенические нормы при приёме пищи, рекомендации для путешественников и др.), использование одноразовых игл и шприцев.
Безопасность пищевых продуктов и распространение инфекций. В Европейском союзе существуют общепринятые стандарты безопасности пищевых продуктов. Контроль за их соблюдением осуществляют специалисты по вопросам гигиены окружающей среды, а также представители Министерства окружающей среды, продовольствия и сельского хозяйства. Пастеризация молока помогает снизить риск возникновения заболеваний, вызываемых Mycobacterium bovis и бактериями рода Campylobacter.
Борьба с переносчиками инфекций. Борьбе с переносчиками инфекций придают огромное значение в регионах, где промежуточными хозяевами возбудителей могут быть насекомые. Лица, посещающие тропические страны, могут существенно снизить риск развития заболевания, приняв меры, предотвращающие нападение и укусы насекомых. Попытки контролировать популяции насекомых с помощью инсектицидов могут быть неудачными вследствие наличия резистентности к этим препаратам.
Профилактика инфекционных заболеваний
Для профилактики некоторых заболеваний (например, дифтерия, менингококковая инфекция) применяют лекарственные препараты. Цель — уничтожение возбудителей заболевания в организме носителя для предупреждения развития острого состояния или распространения инфекции.
Например, для профилактики менингококковой инфекции применяют рифампицин или ципрофлоксацин, приём изониазида рекомендован пациентам с риском обострения туберкулёза при снижении иммунитета.
Значение эпидемиологии в распространении инфекций
Значение организации здравоохранения в распространении инфекционных заболеваний
В большинстве стран существует департамент здравоохранения, занимающийся изучением, профилактикой и лечением инфекционных заболеваний. Обязанности департамента:
• контроль за инфекционной заболеваемостью;
• эпидемиологическое обследование в очаге инфекционного заболевания;
• контроль за вакцинопрофилактикой;
• научные эпидемиологические исследования и обучение медицинского персонала.
Для предотвращения вспышек зоонозных инфекционных заболеваний необходимо тесное сотрудничество между учреждениями (министерствами) пищевой и сельскохозяйственной промышленности и органами санитарно-эпидемиологического надзора. В некоторых странах функции всех этих организаций выполняет одна из них, например Департамент здравоохранения в Великобритании и СДС — Центр по контролю и предупреждению распространения заболеваний — в США. Кроме того, в ведении этих организаций находится решение проблемы биологического терроризма. При этом особую важность приобретает быстрое определение вида возбудителя и своевременное оповещение населения о применении биологического оружия.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
- Вернуться в раздел "Микробиология"
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Сепсис: причины появления, симптомы, диагностика и способы лечения.
Определение
Сепсис – это патологический процесс, в основе которого лежит реакция организма в виде генерализованного воспаления на инфекцию различной природы. При сепсисе бактерии преодолевают иммунную защиту человека и распространяются из очага воспаления по всему организму. Местное воспаление, сепсис, тяжелый сепсис и септический шок – это различные формы выраженности воспалительной реакции организма на инфекционный процесс.
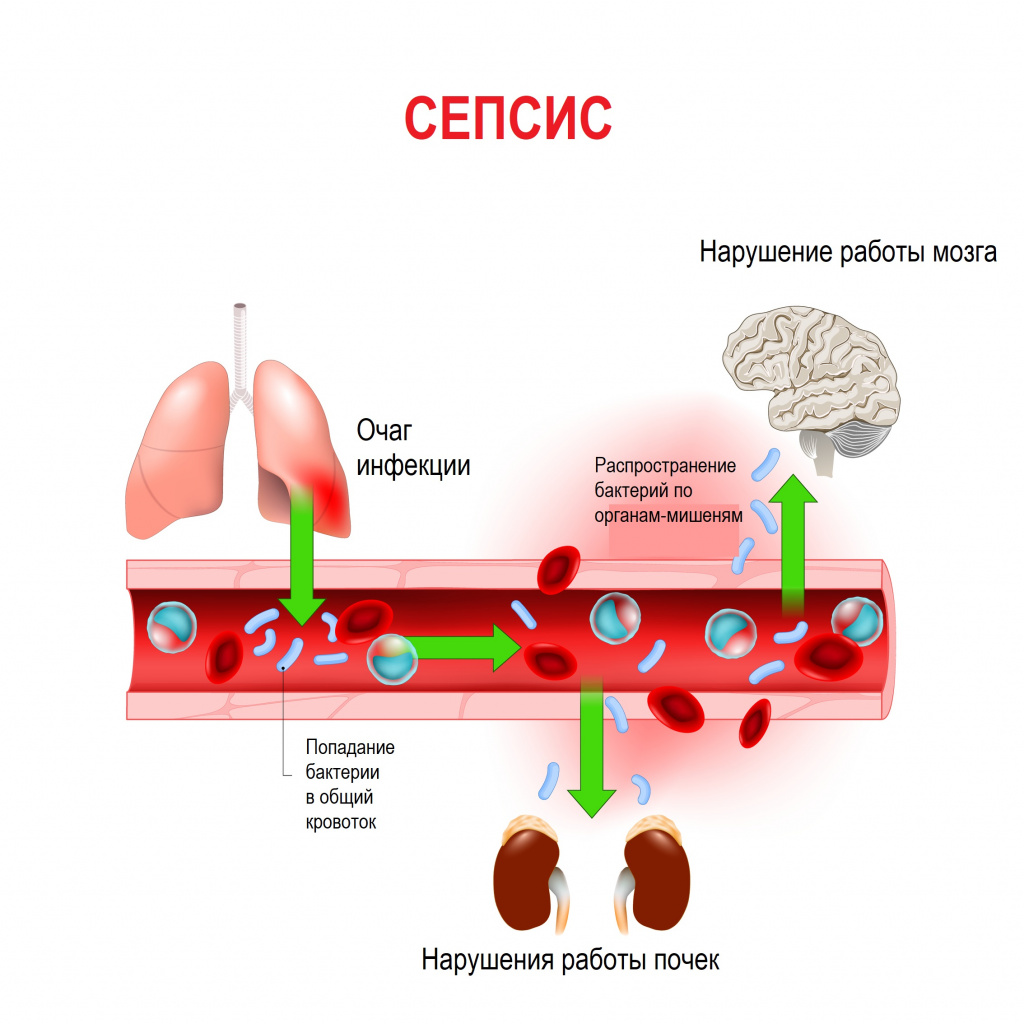
Истинная частота возникновения случаев сепсиса остается неизвестной, однако по оценкам исследователей, во всем мире сепсис является лидирующей причиной летальности у пациентов в критическом состоянии. Согласно результатам большого европейского исследования SOAP, включившего 3147 пациентов из 198 европейских медицинских центров, сепсис развился в 37,4% случаев, а госпитальная летальность от него колебалась от 14% случаев в Швейцарии до 41% в Португалии, в среднем составив 24,1%. Данные другого крупного исследования PROGRES (12 881 больной тяжелым сепсисом в 37 странах) показали, что госпитальная летальность в среднем составила 49,6%.
Причины возникновения сепсиса
Возбудителями сепсиса могут быть бактерии, вирусы или грибы. Но чаще сепсис имеет бактериальную природу - его причиной становятся стафилококки, стрептококки, пневмококки, менингококки, сальмонеллы, синегнойная палочка и др.
В большинстве случаев патологический процесс вызывают условно-патогенные микроорганизмы, которые присутствуют на коже, слизистых оболочках дыхательного и пищеварительного трактов, мочевыводящих путей и половых органов. Иногда при сепсисе выделяют сразу 2-3 микроорганизма.
Причиной сепсиса могут стать гнойно-воспалительные заболевания кожи (абсцессы, фурункулы, флегмоны), обширные травмы, ожоги, инфекционно-воспалительные заболевания мочевыводящей системы (пиелонефрит), живота (например, гнойно-некротический деструктивный панкреатит), тяжелая ангина, гнойный отит, пневмония, инфицирование во время родов или абортов и др.
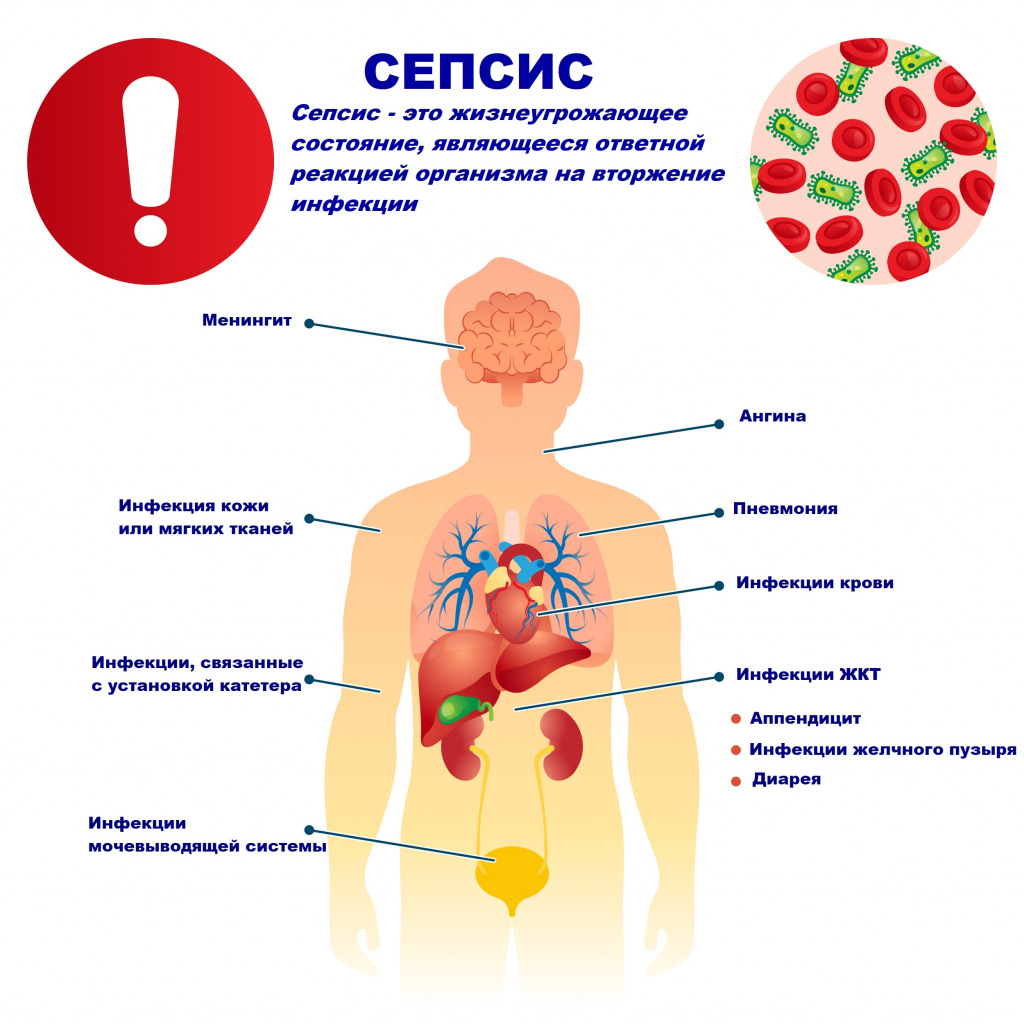
Возможность возникновения сепсиса зависит не только от свойств возбудителя, но и от состояния иммунной системы человека - нарушения в ее работе предрасполагают к распространению инфекции. Причинами таких нарушений могут быть врожденные дефекты иммунитета, хронические инфекционные болезни (ВИЧ, гнойные процессы), эндокринные заболевания (сахарный диабет), онкологические болезни, хронические интоксикации (алкоголизм, наркомания), проникающая радиация, прием иммуносупрессоров (кортикостероидов, цитостатиков) и др.
В ответ на внедрение возбудителя вырабатываются цитокины – особые белковые молекулы, которые выполняют защитные функции сначала на местном уровне, а затем, попадая в системный кровоток, продолжают работать уже на уровне всего организма. Цитокины бывают провоспалительными и противовоспалительными. В самом начале инфекционного процесса их количество находится в равновесии. Если регулирующие системы организма не способны поддерживать это равновесие, то цитокины накапливаются в кровотоке в сверхвысоких объемах, начинают доминировать их деструктивные, разрушающие эффекты, в результате повреждается сосудистая стенка, запускается синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром) и полиорганная дисфункция. Вследствие полиорганной дисфункции печени, почек, кишечника появляются новые повреждающие факторы (лактат, мочевина, билирубин и др.), которые усиливают деструктивные процессы. При ДВС-синдроме в сосудах микроциркуляторного русла образуются множественные тромбы в сочетании с несвёртываемостью крови, приводящей к множественным кровоизлияниям.
Классификация заболевания
В зависимости от локализации входных ворот и первичного очага сепсис подразделяют на:
- перкутанный (чрескожный) – развивается при попадании возбудителя в организм через поврежденный кожный покров (ранки, царапины, фурункулы и др.);
- акушерско-гинекологический – развивается после родов и абортов;
- оральный (одонтогенный и тонзиллогенный) – развивается в результате первичной инфекции в полости рта;
- оториногенный – развивается в результате распространения инфекции из полости уха и/или носа;
- пневмогенный – при наличии инфекционного очага в нижних дыхательных путях;
- хирургический;
- урологический;
- пупочный – развивается у новорожденных вследствие проникновения инфекционных агентов в кровь через пупочную ранку;
- криптогенный (идиопатический, эссенциальный, генуинный) – сепсис неизвестного происхождения: первичный очаг гнойного воспаления неизвестен.
- молниеносный сепсис,
- острый сепсис,
- подострый сепсис,
- хронический сепсис (хрониосепсис).
По клиническим признакам:
1. Синдром системного воспалительного ответа (ССВО) – системная реакция организма на воздействие различных сильных раздражителей (инфекции, травмы, операции и др.) характеризуется двумя или более признаками:
- температура тела ≥ 38°С или ≤ 36°С;
- частота сердечных сокращений (ЧСС) ≥ 90 ударов в минуту;
- частота дыхания (ЧД) > 20 в минуту или гипервентиляция (РаСО2 ≤ 32 мм рт. ст.);
- лейкоциты крови > 12х109 /л или < 4х109 /л, или незрелых форм >10%.
По виду и характеру возбудителя:
- аэробный сепсис,
- анаэробный сепсис,
- смешанный сепсис,
- грибковый сепсис,
- вирусный сепсис.
Клинические проявления сепсиса могут варьировать от незначительных до критических. При молниеносном течении патологическое состояние развивается бурно - за несколько часов или суток. При остром сепсисе симптомы развиваются за несколько дней. Для хрониосепсиса характерно вялое течение и наличие малозаметных изменений, формирующихся месяцами. Рецидивирующий сепсис протекает с эпизодами обострений и затуханий.
Инкубационный период после выявления ворот инфекции или первичного очага составляет от 1 до 3-5 суток. Начало сепсиса, как правило, острое, хотя иногда может быть подострым или постепенным. Интоксикация проявляется резкой слабостью, адинамией, анорексией, нарушением сна, головной болью, расстройством сознания, менингеальным синдромом (поражением оболочек головного и спинного мозга), тахикардией, артериальной гипотензией. Температура тела держится высокой, со скачками утром и вечером. Признаки интоксикации особенно выражены на высоте лихорадки. На коже у трети больных появляется геморрагическая сыпь.
Со стороны дыхательной системы наблюдаются одышка и хрипы в легких. При нарушении функции почек снижается количество выделяемой мочи (олигурия) вплоть до полного прекращения мочеиспускания (анурия), в моче появляются следы крови, гноя. Наблюдается ухудшение функции печени с развитием желтухи и явлениями гепатита, увеличивается селезенка. Повреждение органов ЖКТ проявляется нарушением пищеварения, отсутствием аппетита, язык сухой, обложенный, нередко наблюдаются упорные септические поносы, тошнота и рвота. Метастазирование возбудителя из первичного очага с образованием вторичных очагов инфекции может приводить к инфаркту легкого, гангрене легкого, гнойному плевриту, эндокардиту (поражению внутренней оболочки сердца), воспалению сердечной мышцы (миокардиту), воспалению околосердечной сумки (перикардиту), гнойному циститу, абсцессам мозга и воспалению оболочек мозга (гнойному менингиту), гнойным артритам, флегмонам и абсцессам в мышцах.
Недостаточность функции одного органа длительностью более суток сопровождается летальностью до 35%, при недостаточности двух органов – 55%, при недостаточности функции трех и более органов летальность к четвертому дню возрастает до 85%.
Производят посевы крови, мочи, ликвора, мокроты, гнойного экссудата из элементов сыпи, абсцессов, пунктатов плевры, суставов и других септических очагов. Посевы делают многократно, чтобы определить чувствительность к максимальному количеству антибиотиков. Используется также обнаружение антигенов в крови методом ИФА и определение генома возбудителя методом ПЦР.
Одним из наиболее специфичных и чувствительных маркеров бактериальной инфекции служит прокальцитониновый тест. Прокальцитонин – один из основных маркёров системного воспаления, вызванного бактериями.
Синонимы: Анализ крови на прокальцитонин; ПКТ. Procalcitonin; PCT. Краткая характеристика определяемого вещества Прокальцитонин Прокальцитонин является прогормоном кальцитонина, состоящим из 116 аминокислот с молекулярной массой 14,5 кDa. Биосинтез прокальцитонина в физиологических условиях прои.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
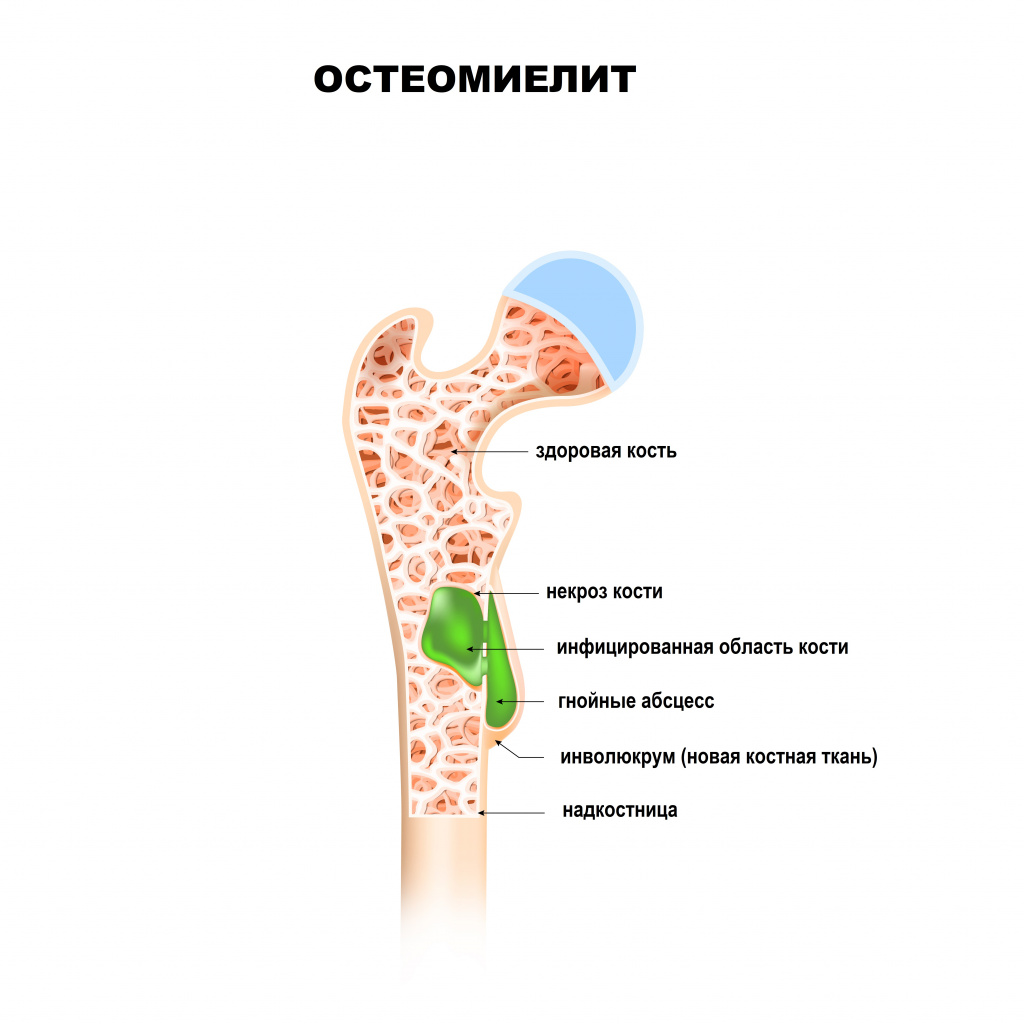
Остеомиелит: причины появления, симптомы, диагностика и способы лечения.
Определение
Причины появления остеомиелита
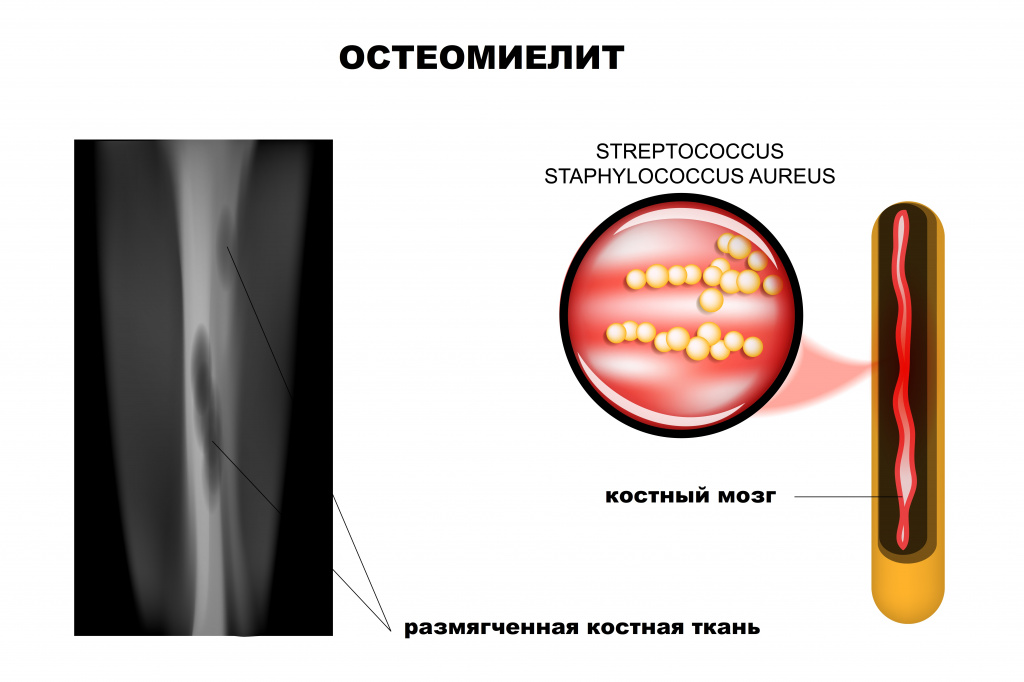
Ведущая роль в развитии заболевания принадлежит патогенным стафилококкам (золотистый стафилококк обнаруживается почти у 90% больных остеомиелитом), гемолитическим стрептококкам, грамотрицательной кишечной и анаэробной микрофлоре, грибковым инфекциям.
Специалисты считают, что в развитии остеомиелита имеют значение снижение реактивности организма больного (в результате травмы, переохлаждения, сенсибилизации) и нарушение кровоснабжения поражаемого отдела кости.
Основными путями проникновения инфекции в костную ткань являются:
- Гематогенный – патогенные микроорганизмы из какого-либо источника инфекции (например, фурункулов, кариозных зубов, воспалительных очагов в деснах, миндалинах или придаточных пазухах, легких, мочеполового тракта и др.) с током крови проникают в костную ткань, приводя к развитию остеомиелита. Воспалительный процесс начинается с внутренних слоев кости – в первую очередь поражается костный мозг, губчатое вещество кости. В последующем процесс переходит на компактное вещество (наружный плотный слой кости) и надкостницу. Данный вид остеомиелита часто встречается в детском возрасте. Особенностью костной ткани у детей является ее обильное кровоснабжение. В большинстве случаев остеомиелит развивается в зонах роста костей (метафизах). При этом чаще поражаются длинные (большеберцовая, бедренная или плечевая) кости конечностей ребенка. У взрослых гематогенный остеомиелит, как правило, поражает тело позвонков.
- Прямое инфицирование костной ткани может наблюдаться при открытых переломах, обширных, глубоких ранах. Посттравматический остеомиелит развивается вторично после открытых переломов. Особую группу составляет остеомиелитическое повреждение костей после ДТП, спортивных травм, огнестрельных и минно-взрывных ранений, поскольку в характере перелома играет роль обширное поражение окружающих тканей. При этом возникает не только дефицит костной, но и мягких тканей с образованием больших дефектов. В некоторых случаях данным путем может происходить проникновение патогенных бактерий при различных хирургических ортопедических вмешательствах.
- Инфицирование из близлежащих гнойных очагов (контактный путь) – патогенные бактерии проникают в костную ткань из длительно существующих гнойно-воспалительных очагов в окружающих мягких тканях. Данная форма в основном встречается у взрослых. В процесс обычно вовлечена одна кость, но иногда наблюдается поражение нескольких участков. Экзогенное распространение инфекции от сопредельных зараженных тканей или открытых ран вызывает около 80% случаев остеомиелита и часто имеет полимикробный характер. Факторами риска у взрослых являются мужской пол, пожилой возраст, истощение, ослабленный иммунитет, длительный прием глюкокортикоидов, гемодиализ, серповидноклеточная анемия (наследственное заболевание, которое характеризуется образованием патологического белка гемоглобина в эритроцитах) и употребление инъекционных наркотиков. Травмы, ишемия, инородные тела, пролежни, повреждение тканей лучевой терапией также предрасполагают к остеомиелиту.
Остеомиелит, обусловленный инфицированием окружающих тканей, часто локализуется в области стоп (у больных с сахарным диабетом или заболеваниями периферических сосудов).
Любой остеомиелит может перейти в хроническую форму, имея, в конечном счете, общую патофизиологию с нарушением целостности оболочки мягких тканей, наличием окружающей омертвевшей, инфицированной и реактивной новой костной ткани.
Классификация заболевания
Остеомиелит различают:
- по пути инфицирования: экзогенный и эндогенный;
- по этиологии:
- острый гематогенный остеомиелит, вызванный золотистым стафилококком, стрептококками, коагулаза-отрицательными стафилококками, Haemophilus influenzae, грамотрицательными микроорганизмами;
- остеомиелит позвоночника, вызванный золотистым стафилококком, грамотрицательными кишечными палочками, микобактериями туберкулеза, грибами;
- остеомиелит при наличии местного очага или сосудистой недостаточности, вызванный комбинацией аэробных и анаэробных микроорганизмов;
- остеомиелит, развившийся на фоне инфекции протезных аппаратов, вызванной коагулаза-отрицательными стафилококками, золотистым стафилококком, коринеформными бактериями, грамотрицательными микроорганизмами.
- острый гематогенный остеомиелит:
- генерализованный (септикотоксемия, септикопиемия),
- очаговая форма;
- после перелома,
- огнестрельный,
- послеоперационный;
- абсцесс Броди,
- альбуминозный (Оллье),
- склерозирующий (Гарре).
- острая (2-4 недели);
- подострая (от 2 недель и более):
- выздоровление,
- продолжение процесса;
- обострение,
- ремиссия,
- выздоровление.
- остеомиелит трубчатых костей (эпифизарный, метафизарный, диафизарный, тотальный);
- остеомиелит плоских костей.
К симптомам заболевания относят боль в области пораженной кости, сопровождающуюся общей реакцией организма (при остром остеомиелите) или без нее (при хроническом остеомиелите).
Первые признаки остеомиелита в острой форме:
- сильная распирающая боль в пораженной кости;
- выраженный локальный отек, который приводит к натяжению кожного покрова;
- температура тела поднимается до 38оС;
- при постукивании можно определить очаг воспаления – в этом месте пациент чувствует наибольшую болезненность.
![Кость.jpg]()
Признаки остеомиелита кости часто дополняются симптомами общей интоксикации, если инфекция распространяется на соседние ткани или проникает в кровь. У пациента в таком случае наблюдаются:
- высокая температура (около 39оС);
- сильная головная боль;
- лихорадка, озноб;
- бледные кожные покровы;
- учащенное сердцебиение;
- тошнота и рвота.
Если у пациента наблюдается хронический остеомиелит, симптомы кардинально меняются. Клиническая картина становится стертой. Основные признаки остеомиелита хронической формы:
- боль уменьшается, приобретает ноющий характер;
- появляются свищи (каналы, соединяющие гнойный очаг с внешней средой) с гнойным отделяемым, которые часто имеют выход далеко от локализации воспаления.
Развитие остеомиелита у детей сопровождается теми же симптомами что и у взрослых, хотя патология чаще протекает в легкой форме без общей интоксикации и осложнений.
Остеомиелит позвоночника обычно вызывает локальную боль в спине с паравертебральным (по сторонам позвоночного столба) мышечным спазмом, которые не поддаются консервативному лечению. На поздних стадиях заболевание может привести к компрессии спинного мозга или нервных корешков с радикулопатией и слабостью или онемением конечностей. Повышения температуры тела, как правило, не наблюдается.
Диагностика остеомиелита
При подозрении на остеомиелит необходимо выполнить следующие лабораторные исследования:
-
общий анализ крови и определение скорости оседания эритроцитов;
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
С-реактивный белок – белок острой фазы, чувствительный индикатор повреждения тканей при воспалении, некрозе, травме. Синонимы: Анализ крови на СРБ; С-реактивный белок сыворотки крови. C-reactive Protein (CRP), quantitative; C-reactive protein test; CRP test. Краткое описание опред.
Рентгенологическое исследование считается одним из наиболее эффективных методов диагностики остеомиелита. Признаки патологии у детей видны на снимке уже на 5-й день, а у взрослых — только через 2 недели от начала воспалительного процесса.
Самым точным и эффективным видом диагностики является радионуклидная сцинтиграфия костей. С помощью специальных препаратов, накапливающихся в зоне очага болезни, можно точно выявить начало поражения кости. Однако этот метод не позволяет провести дифференциальную диагностику между инфекцией, переломами и опухолями.
Скопление гноя в мягких тканях выявляют с помощью ультразвукового исследования.
Исследование мягких тканей для выявления патологических изменений и диагностики новообразований.
Для лечения большое значение имеет биопсия очага воспаления костной ткани (аспирационная или открытая) и посев гнойного отделяемого на флору с определением чувствительности к антибиотикам и бактериофагам.
К каким врачам обращаться
Лечение остеомиелита
Консервативные методы лечения в большинстве случаев стандартизированы и включают антибиотикотерапию с определением микробного возбудителя и чувствительности микроорганизмов к антибактериальным препаратам, противовоспалительную терапию. Большое значение имеет проведение иммуномодулирующей терапии, в том числе с использованием методов квантовой гемотерапии (реинфузия обработанной ауто- и донорской крови и др.), а в отдельных случаях гормонотерапии.
В большинстве случаев хирургическое лечение остеомиелита направлено, прежде всего, на ликвидацию очага гнойно-некротического поражения, замещение остаточных полостей или образовавшихся дефектов.
При остром гематогенном остеомиелите начальная антибиотикотерапия должна включать полусинтетические пенициллины или ванкомицин и цефалоспорины 3-го или 4-го поколения. При хроническом остеомиелите, возникающем в результате распространения инфекции с окружающих мягких тканей, особенно у больных диабетом, лечение проводят с использованием препаратов, эффективных как против грамположительных и грамотрицательных аэробов, так и против анаэробной флоры.
Осложняет лечение хронической формы заболевания нарушение кровоснабжения кости, которое затрудняет проникновение антибактериальных препаратов, снижает эффективность местного иммунного ответа в костной ткани.
Некоторые симптомы остеомиелита свидетельствуют о том, что болезнь перешла в крайне тяжелую форму. Нередко единственным выходом в этой ситуации становится хирургическое вмешательство. Главная его цель — удаление гнойного очага воспаления. Это в разы ускоряет процесс выздоровления и улучшает общее самочувствие больного.
Показания к операции:
- гнойная форма заболевания;
- флегмона надкостницы;
- наличие свищей и секвестров;
- обширное гнойное течение заболевания.
В последние годы широко разрабатываются методы закрытия костной полости, такие как мышечная или кожно-мышечная пластика.
Существуют современные методы, которые позволяют сохранить имплантаты при остеосинтезе (хирургической репозиции костных отломков при помощи различных фиксирующих металлических конструкций) в случае ранних нагноений. Это вакуумная терапия, применение гидрохирургической системы, ультразвуковой кавитации и других методов обработки ран, которые дают возможность предотвратить развитие так называемой бактериальной биопленки на поверхности имплантата, что, в свою очередь, позволяет сохранить имплантат и конечность.
Остеомиелит – тяжелое заболевание, поэтому даже при своевременном и компетентном лечении есть риск возникновения нежелательных последствий. Остеомиелит кости может вызвать как самостоятельные осложнения, так и такие, которые возникают как следствие хирургического вмешательства. Некоторые из них требуют отельного лечения. Прогрессирование гнойно-воспалительного процесса приводит к разрушению костной ткани, нарушается ее кровоснабжение, что еще больше усиливает некротические процессы в кости. Заболевание может вызвать такие нарушения:
- развитие абсцессов и свищей, нарывов в мягких тканях и на коже;
- возникновение флегмоны — пропитывания мышечных волокон гноем;
- развитие артрита с образованием гнойных масс в полостях;
- самопроизвольные переломы;
- анкилозные сращивания суставных частей;
- контрактурная неподвижность мышечных соединений.
Гнойно-воспалительные поражения костей приводят к инвалидизации около 55% пациентов. Остеомиелит может закончиться потерей конечности, если речь идет о поражении руки или ноги.
В связи с особенностью локализации остеомиелитического процесса у детей в последующем может наблюдаться замедление развития костей за счет повреждения воспалительным процессом зон роста.
Разрушение позвонков, сдавливание спинного мозга может приводить к двигательным и чувствительным нарушениям.
Профилактика остеомиелита
Для снижения риска развития остеомиелита рекомендуется:
- своевременно реагировать на возникновение инфекционных процессов в организме;
- проводить лечение гайморита, кариеса, воспаления носоглотки и верхних дыхательных путей;
- осуществлять тщательную обработку ран, обморожений и ожогов, чтобы исключить возможность их инфицирования;
- вести здоровый образ жизни, избегать чрезмерных физических нагрузок, недоедания, следить за сбалансированностью питания;
- не допускать переохлаждения организма.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Сепсис — это самая тяжелая, генерализованная форма инфекционного процесса, которая развивается либо при высокой патогенности возбудителя, либо при недостаточном ответе защитных систем организма. Международным консенсусом рекомендовано использовать следующее определение: сепсис — это опасная для жизни дисфункция внутренних органов, вызванная нарушением регуляции ответа организма на инфекцию. При сепсисе наблюдается общий интоксикационный синдром, тромбогеморрагический синдром (кровоизлияния) и поражение внутренних органов.
Причины возникновения сепсиса
Сепсис может быть вызван большинством известных в эпидемиологии микроорганизмов, среди которых бактерии, вирусы (в том числе сезонные вирусы гриппа), грибы, паразиты. Обычно возбудитель инфекции попадает в организм из внешней среды. При определенных условиях, например, при иммунодефицитах, заболевание может развиться от естественной, условно-патогенной флоры организма, которая в норме присутствует у каждого человека. [1]
![]()
Само по себе наличие инфекции еще не является гарантией развития сепсиса. Необходимы дополнительные условия, которые приведут к генерализации процесса и патологическому ответу организма. Вероятность таких событий увеличивается в следующих случаях:
- Возраст больного старше 75 лет.
- Выполнение операций или инвазивных процедур.
- Наличие травм и ожогов.
- Нарушения иммунной системы — СПИД, онкологические заболевания, проведение химиотерапии, необходимость применения иммуносупрессивной терапии (например, после трансплантации органов), необходимость приема высоких доз глюкокортикостероидов.
- Долгое лечение в условиях стационара.
- Наличие катетеров, канюль, зондов и других инвазивных устройств.
- Беременность и роды.
- Наличие химической зависимости — алкоголизм, наркомания.
- Наличие хронических заболеваний — хроническая почечная недостаточность, дыхательная недостаточность, сахарный диабет и многое другое.
Виды сепсиса
В зависимости от расположения первичного очага инфекции, выделяют первичный (криптогенный) и вторичный сепсис. При первичном, очаг инфекции установить не удается. При вторичном сепсисе таковой очаг имеется. В зависимости от его локализации, выделяют:
- Чрескожный сепсис. Первичный очаг находится на коже, это могут быть раны, ожоги, гнойные заболевания кожи (гнойные абсцессы, фурункулы и др).
- Одонтогенный сепсис. Причиной его развития может стать кариес, пульпит, периодонтит, челюстной остеомиелит и другие заболевания зубочелюстной системы.
- Отогенный сепсис. Первичным очагом является воспалительный процесс в ухе. Как правило, это гнойные отиты среднего уха.
- Гинекологический сепсис — первичный очаг располагается в половых органах женщины.
- Хирургический сепсис — развивается в результате инфицирования хирургической раны или при инфицировании во время проведения инвазивных процедур. 2
Первые признаки и симптомы сепсиса
Определить первые признаки сепсиса бывает непросто, даже для специалистов. Это связано с тем, что, во-первых, этот синдром развивается уже на фоне существующей патологии, которая может иметь самую разнообразную симптоматику, а во-вторых, при наличии иммунодефицита, клиническая картина может быть стертой. Тем не менее, есть некоторые симптомы, которые позволяют заподозрить начало сепсиса:
- Повышение или понижение температуры тела — выше 38 и ниже 36 градусов.
- Снижение давления ниже рабочего значения.
- Увеличение частоты пульса.
- Увеличение частоты дыхательных движений (одышка).
- Снижение количества выделенной мочи.
- Общая слабость, изможденность.
- Нарушение сознания или поведения.
Особое внимание возникновению этих признаков уделяют у хронических больных, при наличии лейкопении, онкологических заболеваний и у пациентов, перенесших травмы или хирургические вмешательства. При возникновении хотя бы 2-3 таких симптомов, следует немедленно связаться с врачом.
Диагностика сепсиса
Своевременная диагностика сепсиса имеет решающее значение для выздоровления больного. Чем раньше начато лечение, тем больше шансов на успех. Диагноз выставляется на основании данных клинического осмотра и лабораторно-инструментального обследования.
![]()
Клинические критерии:
- Температура тела более 38 градусов или менее 36 градусов.
- Частота сердечных сокращений более 90 или превышает возрастную норму.
- Частота дыхания более 20 раз в минуту.
- Наличие отеков.
- Спутанность сознания.
- Повышение уровня глюкозы в крови более 7,7 мкмоль/л при отсутствии диабета.
- Нарушение гемодинамических процессов — снижение систолического артериального давления менее 90 мм.рт.ст, либо его снижение более чем на 40 мм.рт.ст. от привычного значения. [5,6]
Лабораторные критерии
Проводят общий анализ крови с подсчетом лейкоцитарной формулы и определением количества тромбоцитов. При сепсисе определяется лейкоцитоз более 12*109/л или лейкопения, когда количество лейкоцитов ниже 4*109/л. Также отмечается выход в кровяное русло незрелых форм гранулоцитов и уменьшение количества тромбоцитов.
В биохимическом анализе крови отмечается увеличение С-реактивного белка, креатинина, билирубина. Но это неспецифичные признаки, которые могут наблюдаться и при других заболеваниях. Поэтому продолжается поиск более информативных методов диагностики.
На сегодняшний день главными таким маркерами являются прокальцитонин, пресепсин, СРБ. По данным этого лабораторного показателя устанавливают диагноз и отслеживают динамику заболевания.
Бактериологический посев
Обнаружение в крови микроорганизмов является важным, но не обязательным проявлением сепсиса. Даже при использовании самых современных диагностических систем и при тщательном соблюдении техники забора материала, выделить возбудитель из крови удается менее, чем в половине случаев. Поэтому отрицательный результат бакпосева при наличии клинической симптоматики не должен расцениваться как отсутствие сепсиса, и, наоборот, выделение микроорганизмов из крови при отсутствии симптоматики, должно расцениваться как транзиторная бактериемия или вирусемия, но не как сепсис.
Тем не менее, биологические исследования в любом случае должны присутствовать, как один из этапов диагностики сепсиса по следующим причинам:
- Возможность определения этиологии возбудителя.
- Подбор или смена режимов антибиотикотерапии.
- Контроль эффективности лечения.
- В некоторых случаях позволяет определить источник инфекции, например, катетер-связанная инфекция, эндокардиты и др.
Стадии развития сепсиса
Развитие и течение септического процесса индивидуально и зависит как от свойств возбудителя, так и от особенностей организма больного. Тем не менее, можно выделить несколько фаз течения данного заболевания:
Что касается продолжительности заболевания, то здесь все опять же индивидуально. У одних, более сильных пациентов, сепсис купируется в течение 3-4 недель, у других он может протекать годами, периодически стихая и вспыхивая.
Кроме того, при диагностике сепсиса выделяют следующие состояния.
Токсико-резорбтивная лихорадка
Токсико-резорбтивная лихорадка — состояние, которое развивается при всасывании бактериальных токсинов или продуктов тканевого распада из первичного патологического очага. Как правило, это характерно для бактериальных инфекций ран, катетеров и др. Характерны общие типовые синдромы, которые сопровождают инфекционные процессы — лихорадка, изменения в общем анализе крови и мочи (лейкоцитоз, протеинурия). При ликвидации первичного очага, состояние пациента стабилизируется.
Септицемия
Септицемия — форма сепсиса, при которой наблюдается выраженный интоксикационный синдром, гиперэргия (повышенная реакционность организма) и быстрое течение. Септические очаги либо выражены минимально, либо отсутствуют. Такая форма сепсиса больше характерна для детей первых лет жизни. Для клинической картины больше характерны общие проявления:
- Гемолитическая желтуха, сопровождающаяся пожелтением кожных покровов и склер.
- Сыпь. Сначала она проявляется в виде мелких розовых точек, которые разрастаются и сливаются между собой, образуя бледно-розовые или пурпурные пятна.
- У некоторых пациентов элементы сыпи могут покрываться пузырями или язвами. При глубоких поражениях может затрагиваться подкожная жировая клетчатка с развитием флегмонозного воспаления.
- Геморрагический синдром — кровоизлияния во внутренние органы.
![]()
Септикопиемия
Септикопиемия — это форма сепсиса, при которой в организме, помимо общей интоксикации, начинают возникать метастатические абсцессы в органах и тканях, которые являются результатом бактериальной эмболии. Чаще всего первые абсцессы обнаруживаются в легких, а затем процесс распространяется на другие органы: печень, печень, сердце, менингиальные оболочки, синовиальные оболочки. Абсцессы могут прорваться и вызвать развитие эмпиемы плевры, флегмоны, перитонита и др.
Клиническая классификация сепсиса по стадиям
Клиническое стадирование сепсиса играет важную роль, так как оно помогает врачам выбирать оптимальную тактику и добиваться наилучших из возможных в каждом конкретном случае результатов лечения. Выделяют следующие стадии:
- Сепсис диагностируют, когда внутренняя температура (измеряется на слизистых оболочках) тела поднимается больше 38 градусов или опускается ниже 36 градусов, частота сердечных сокращений 90 в минуту и более, частота дыхания 20 в минуту и более, либо парциальное давление углекислого газа в артериальной крови (PaCO2) опускается ниже 32 мм. рт. ст. При этом уровень лейкоцитов в крови поднимается более 12000/мкл или опускается ниже ≤4000/мкл, либо среди них появляется более 10% незрелых форм.
- Тяжелый сепсис – сепсис, который сочетается с острой органной дисфункцией.
- Септический шок диагностируют, когда у пациента имеется стойкая гипотензия (снижение артериального давления) или гипоперфузия (недостаточное кровоснабжение) тканей, несмотря на адекватную инфузионную терапию.
- Синдром полиорганной дисфункции – состояние, при котором у больного имеется органная дисфункция (нарушение работы внутренних органов), и его гомеостаз не удается поддерживать без медикаментозного вмешательства.
Лечение сепсиса
Лечение сепсиса базируется на трех принципах:
Санация первичного очага. Это может быть достигнуто с помощью хирургического вмешательства и/или адекватной антибактериальной терапии. При обнаружении первичного очага, который можно санировать хирургически, необходимо провести это как можно скорее. Это может быть вскрытие и дренирование абсцессов, удаление инфицированных инвазивных устройств (катетеры, имплантаты и др.), дренирование и лаваж брюшной полости, и др.
Антимикробная терапия является еще одним краеугольным камнем лечения сепсиса, при этом важна ее своевременность и адекватность. Например, при развитии септического шока, препараты должны быть введены в течение часа от начала симптомов. При этом препарат должен охватывать весь спектр предполагаемых возбудителей и, что немаловажно, проникать в первичный инфекционный очаг. При необходимости назначения комбинированной терапии из нескольких препаратов, их применяют не более 5 дней, после чего должны быть получены данные биологических методов исследования и произведена коррекция схемы лечения. [7]
Обеспечение транспорта кислорода — все клинические проявления сепсиса усугубляются в условиях недостатка кислорода, поэтому очень важно контролировать этот процесс. Для этого проводят:
- Гемодинамическую поддержку — вливание растворов, которые обеспечивают восполнение водно-электролитного баланса, назначаются препараты, поддерживающие артериальное давление и др.
- Респираторную поддержку — искусственную вентиляцию легких, кислородные маски и др.
Коррекция метаболических нарушений
Одним из эффективных способов лечения сепсиса является селективная сорбция на колонках TORAYMYXIN. Данная методика успешно применяется во многих странах мира. В настоящее время такое лечение прошли более 200 тысяч пациентов с септическим шоком и тяжелыми формами сепсиса. Эффективность и безопасность технологии подтверждена в ходе клинических исследований. [11,12]
![]()
Осложнения при сепсисе
- Осложнения со стороны дыхательной системы. Нарушение вентиляции легких приводит к повышению аэрогематического барьера и, как следствие, пропотеванию жидкости в альвеолы. Это еще больше нарушает газообмен и приводит к развитию шокового легкого и респираторного дистресс-синдрома, который усугубляется усталостью дыхательных мышц.
- Осложнения со стороны почек. Наблюдается снижение фильтрационной функции почек из-за повреждения канальцев, развившееся в результате снижения давления. Сопровождается резким уменьшением выделяемой мочи, протеинурией, азотемией.
- Нарушение свертывания крови из-за падения уровня тромбоцитов и развития ДВС-синдрома — грозного состояния, при котором сначала происходит массовое образование тромбов в кровеносном русле, а затем массивные кровотечения из-за недостаточности кровесвертывающих факторов.
- Неврологические осложнения. Длительно протекающий сепсис может привести к развитию полинейропатии, которая, в частности, приводит к ослаблению дыхательной мускулатуры и невозможности самостоятельного дыхания.
- Септический шок — самое тяжелое проявление сепсиса, сопровождающееся стойким снижением кровяного давления, которое сложно восстановить даже с применением инфузионной терапии и вазопрессоров. Он развивается из-за выхода жидкости из кровеносных сосудов и из-за общего обезвоживания. При этом, нарушения настолько тяжелые, что могут привести к гибели пациента от полиорганной недостаточности.[13]
Прогноз при сепсисе
Прогноз при сепсисе очень осторожный. На возможность выздоровления оказывают влияние особенности этиологической микрофлоры, общее состояние пациента в начале заболевания, а также своевременность и адекватность проводимого лечения. Наиболее неблагоприятно сепсис протекает у людей старческого возраста и у ослабленных пациентов, имеющих сопутствующие заболевания.
В целом в крупных клиниках летальность при данном состоянии составляет 30-40%. При развитии септического шока, ситуация усугубляется и согласно некоторым данным, в таком случае от него погибает до 90% больных.
Читайте также: