Как подобрать антибиотик при бактериальной инфекции
Обновлено: 17.04.2024
Принципы лечения бактериальной инфекции
Бактериальная инфекция развивается после преодоления бактериями кожных и слизистых барьеров и проникновения в ткани организма. Зачастую организм успешно справляется с возбудителями без внешних признаков заболевания за счет иммунного ответа. Тем не менее у некоторых возбудителей появилась сложная защитная система.
Несмотря на захват клетками хозяина в результате обычного фагоцитоза, они способны предотвратить слияние фагосомы с лизосомой и в результате избегают разрушения. Поскольку стенка защитной вакуоли проницаема для питательных веществ (аминокислоты, углеводы), бактерии растут и делятся до тех пор, пока не погибнет клетка, а выделяющиеся возбудители инфицируют новые клетки хозяина.
Данная тактика используется, например, видами Chlamydia и Salmonella, Mycobacterium tuberculosis, Legionella pneumophila, Toxoplasma gondii и Leishmania. Легко понять, что целенаправленная фармакотерапия особенно затруднена в этих случаях, т. к. препарату для достижения возбудителя необходимо пройти через клеточную мембрану и затем через мембрану вакуоли.
Если бактерии размножаются быстрее, чем защитные силы организма уничтожают их, развивается инфекционное заболеваниес признаками воспаления, например гнойная раневая инфекция и инфекция мочевых путей. Лечебными свойствами обладают вещества, которые повреждают бактерии, что останавливает их дальнейшее размножение без повреждения клеток организма хозяина.
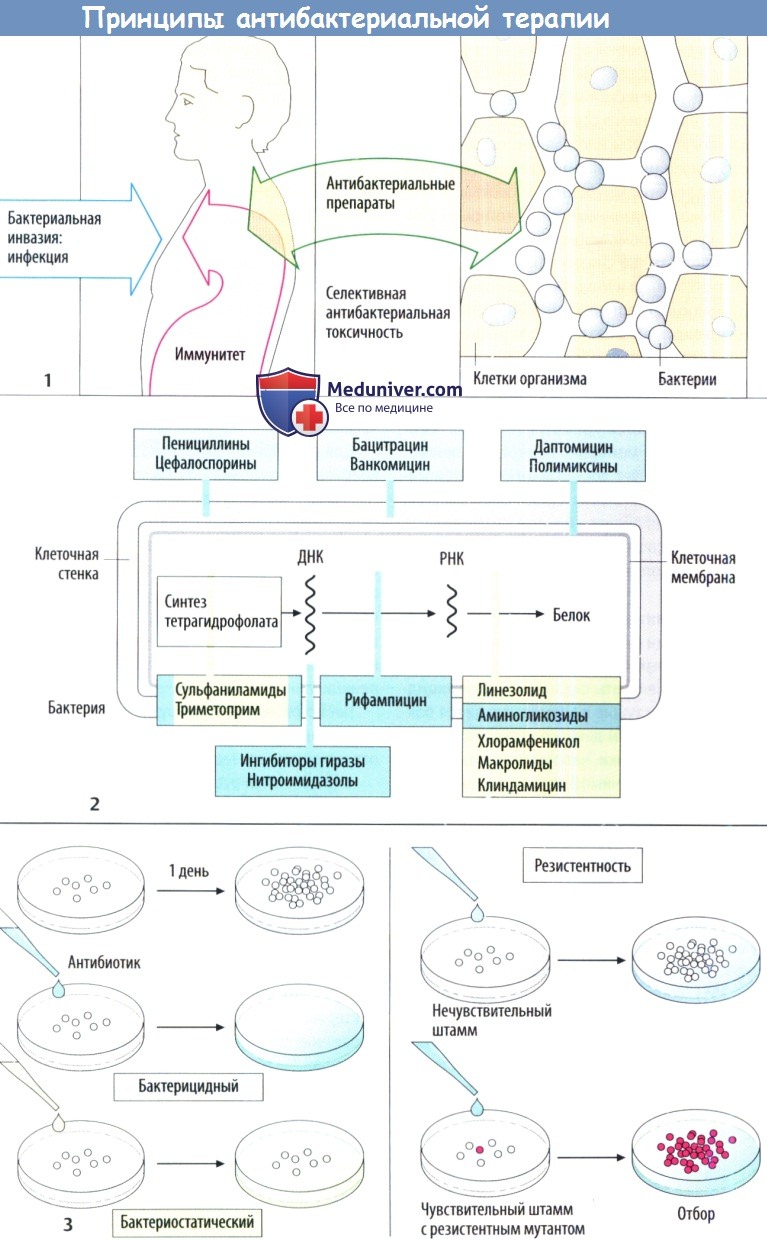
Изолированное повреждение бактерий возможно в случае, когда вещество нарушает метаболизм бактериальных клеток, а не клеток организма хозяина. Таким свойством, очевидно, обладают ингибиторы синтеза клеточной стенки, т. к. в клетках человека или животных отсутствует такая стенка. Точки воздействия антибактериальных препаратов проиллюстрированы с помощью упрощенной схемы строения бактериальной клетки
Действие антибактериальных препаратов можно наблюдать in vitro. Бактерии размножаются в питательной среде в контролируемых условиях. Если среда содержит антибактериальный препарат, то можно ожидать два результата:
а) бактерии уничтожаются — бактерицидный эффект;
б) бактерии выживают, но не размножаются — бактериостатический эффект. Несмотря на то что в организме эффекты могут быть разными, различные классы разделяют по основному механизму действия.
N!B! Просьба раз и навсегда запомнить, что бактериоцидные антибиотики не сочетают с бактериостатическими, так как получается что антибиотики будут действовать на разные фазы роста бактерий - одни во время роста, другие после завершения роста! Можно сочетать только бактериостические с бактериостиатическими, а бактериоцидные с бактериоцидными.
Если антибактериальный препарат не влияет на рост бактерий, то это говорит о бактериальной резистентности. Она может быть вызвана наличием определенных метаболических особенностей, которые обусловливают нечувствительность к препарату у конкретного штамма бактерий (естественная резистентность). В зависимости то того, поражает ли препарат лишь несколько или множество типов бактерий выделяют антибиотики с узким (бензилпенициллин) или широким спектром (тетрациклин).
Штаммы бактерий с естественной чувствительностью могут трансформироваться под влиянием антибактериальных препаратов в резистентные штаммы (приобретенная резистентность) при случайном изменении гена (мутация). Под влиянием препарата чувствительные бактерии погибают, а мутировавшие продолжают размножаться. Чем чаще вводится один и тот же препарат, тем вероятнее появление резистентных штаммов (госпитальные штаммы с множественной резистентностью)!
Резистентность в некоторых случаях приобретается, когда ДНК, ответственная за нечувствительность (так называемые плазмиды резистентности), передается от других резистентных бактерий путем конъюгации или трансдукции.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Бактериальные инфекции и лекарства. Классификация антибактериальных препаратов
Бактериальные инфекции очень широко распространены и все еще остаются существенной причиной заболеваемости и смертности.
Бактериальная диарея является основной причиной детской смертности во всем мире, а туберкулез часто служит причиной летального исхода инфекционных заболеваний. Применение антибактериальных лекарственных препаратов представляет собой одно из важнейших терапевтических достижений XX в., позволившее существенно изменить характер многих бактериальных заболеваний благодаря снижению смертности (например, от бактериального менингита и бактериального эндокардита) и заболеваемости. С другой стороны, в настоящее время антибиотики принадлежат к числу средств, очень часто назначаемых без достаточных оснований. Отчасти это происходит потому, что многие из них обладают высокой степенью безопасности. Это приводит к их неправильному использованию, например при вирусных инфекциях.
Кроме того, некоторые из старых, давно открытых антибиотиков используют в качестве стимуляторов роста животных, мясо которых употребляют в пищу, вследствие чего антибиотик включается в пищевую цепочку у человека в субтерапевтических дозах. В результате чрезмерного использования антибиотиков все более актуальной становится глобальная проблема возникновения резистентности к антибиотикам. Особую тревогу вызывает распространение резистентных к метициллину стафилококковых инфекций как в больницах, так и среди населения.
Антибактериальные препараты в зависимости от их происхождения (способа получения) классифицируют на антибиотики, химиотерапевтические или синтетические лекарства и полусинтетические лекарства.
• Продукты жизнедеятельности микроорганизмов (антибиотики).
• Лекарства, получаемые исключительно в лабораторных условиях (химиотерапевтические или синтетические).
• Лекарства, которые готовят, используя комбинацию двух указанных способов (полусинтетические).
Когда говорят, что антибиотики обладают избирательной токсичностью, имеют в виду, что они нарушают жизненно важные функции бактерий, не оказывая влияния (или оказывая минимальное влияние) на клетки инфицированного организма. Причина такой избирательности заключается в том, что бактерии обладают специализированной и особым образом построенной клеточной стенкой, тогда как клетки млекопитающих — обычной клеточной мембраной. В связи с этим вещества, нарушающие синтез или целостность стенки бактериальной клетки, являются токсичными для бактерий, но безвредными для клеток организма-хозяина.
Подобным же образом прокариотическая бактериальная рибосома (70S) настолько сильно отличается от рибосомы эукариот (80S), что служит хорошей мишенью для антибактериальных препаратов. На рис. 6.7 изображены места действия антибиотиков различных классов. В результате избирательной токсичности многие антибиотики имеют высокий терапевтический индекс (т.е. соотношение между токсической и терапевтической дозами). Разумеется, как врожденный иммунный ответ, так и специфические иммунологические механизмы способствуют устранению бактериальной инфекции вместе с антибиотиками, назначаемыми для ускорения этого процесса и предотвращения развития генерализованной инфекции. Применение антибиотиков в борьбе с инфекциями особенно важно в тех случаях, когда функции иммунной системы у пациентов нарушены, например при ВИЧ-инфекции или нейтропении.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Современные антибиотики: препараты широкого спектра действия, при ангине, кашле и бронхите, при гайморите, при гинекологических заболеваниях. Как выбрать антибиотик?
16 января, 2022 год
Содержание
Антибиотики – препараты, которые подавляют размножение или разрушают бактерии. Это средства с различной химической структурой, у них разные механизмы и спектр действия, показания к применению и побочные эффекты. Антибиотики бывают природные и полусинтетические.
Как выбрать антибиотик
Чтобы правильно выбрать антибиотик, нужно учесть многие факторы. Лишь тогда лечение будет эффективным и безопасным. Итак, на что обратить внимание?
- нужно определить, какая именно бактерия вызвала воспаление;
- выбрать самую подходящую форму антибиотика, чтобы он быстро попал в очаг воспаления;
- учесть состояние печени и почек;
- помнить о возможных хронических заболеваниях и возрасте, чтобы избежать побочных эффектов;
- важный фактор – наличие беременности или кормления грудью.
Если вы начали принимать антибиотик, учитывайте также такие моменты:
- посмотрите на динамику лечения через 48 часов (эффективно ли лечение);
- контролируйте резистентность к антибиотику;
- обращайте внимание на побочные эффекты (как на клинические проявления, так и на лабораторные анализы);
- обязательно придерживайтесь того курса лечения, который назначил врач.
Список самых эффективных антибиотиков
В нашем рейтинге – самые лучшие антибиотики, поскольку мы учли рекомендации врачей и отзывы тех, кто принимал эти препараты. Мы разделили антибиотики по группам: широкого спектра действия, антибиотики при ангине, кашле и бронхите, антибиотики при гайморите и препараты, применяемые в гинекологии.
Лучшие антибиотики при кашле, бронхите и ангине
Большинство антибиотиков имеют широкий спектр действия и влияют сразу на несколько видов бактерий. Но для более эффективного лечения кашля, бронхита или ангины лучше все-таки выбирать препараты, предназначенные для верхних дыхательных путей.
Азитромицин
Азитромицин
ЗАО ВЕРТЕКС, Россия; Оболенское (OBL Pharm), Россия; ОЗОН, Россия; ОАО "Фармстандарт-Лексредства", Россия; Zentiva, Чехия; АКРИХИН, Россия; ПроМед, Россия; ОАО Дальхимфарм, Россия
Азитромицин - антибиотик широкого спектра действия. Антибиотик-азалид, представитель новой подгруппы макролидных антибиотиков. При создании в очаге воспаления высоких концентраций оказывает бактерицидное действие.
Назначение антибактериальных препаратов требует соответствующих знаний клинической фармакологии и изучения основ сравнительно новой дисциплины -- клинической микробиологии. Только тогда терапию инфекционных заболеваний можно будет отнести к истинно этиот
Назначение антибактериальных препаратов требует соответствующих знаний клинической фармакологии и изучения основ сравнительно новой дисциплины -- клинической микробиологии. Только тогда терапию инфекционных заболеваний можно будет отнести к истинно этиотропному виду лечения, в отличие от других видов фармакотерапии. Сталкиваясь с проблемой выбора антибактериального препарата, врач должен определить ряд факторов, связанных с пациентом (макроорганизм), возбудителем заболевания (микроорганизм) и с лекарственным препаратом.
 |
В настоящее время проблема рациональной антибиотикотерапии представляет серьезные трудности и остается одной из самых сложных в практической фармакотерапии. Это связано во-первых, с огромным количеством существующих и вновь создаваемых лекарственных препаратов антибактериального действия (только одних цефалоспоринов известно около 2 тыс. соединений), во-вторых, изменением спектра возбудителей инфекционных заболеваний, а также увеличением и распространением их резистентности.
Следует отметить, что около 30-40% госпитальных больных терапевтического профиля нуждаются в проведении антибактериальной терапии и, по данным зарубежной статистики, 45-50% из них получают неадекватную терапию. По-видимому, это обусловлено тем, что для правильного выбора антибактериального препарата необходимо располагать не только данными анамнеза и результатами обследования конкретного пациента, но также уметь интерпретировать и применять на практике существующие представления о вероятном патогенном микроорганизме, что принципиально отличает антибактериальную терапию от фармакотерапии других видов.
Из клинической практики хорошо известно, что показанием для назначения антибактериальных препаратов часто служит повышение температуры, необъяснимая слабость, утомляемость и некоторые другие, неспецифические признаки инфекционных заболеваний. В то же время причиной данной симптоматики могут быть и иные, не связанные с инфекцией заболевания, такие как ревматизм, аутоиммунные заболевания, опухоли, естественно не требующие назначения антибактериальных препаратов. Но и не редки случаи, когда в амбулаторных условиях при определении диагноза ОРВИ уже подразумевается вирусная этиология заболевания, что тем не менее не ограничивает применение антибактериальных препаратов. Их назначение при вирусной природе заболевания объясняется необходимостью профилактики присоединения бактериальной инфекции, однако это лишено каких-либо разумных обоснований. Говорить о целесообразности подобной профилактики можно лишь в случае крайне тяжелых вирусных заболеваний, в том числе гриппа, при тяжелой сопутствующей патологии, когда врач вправе ожидать у больного значительного снижения иммунитета. В случае легкого и среднетяжелого течения ОРВИ назначение антибиотиков и других антибактериальных препаратов может не только оказаться бесполезным, но и причинить больному вред. Таким образом, поводом для назначения антибактериальных препаратов должно служить наличие инфекционного процесса именно бактериального происхождения.
Сопутствующие заболевания и неблагоприятный социальный профиль больного. Сопутствующие хронические заболевания можно рассматривать как фактор дополнительной иммунодепрессии, чаще всего требующей коррекции проводимой антибактериальной терапии. Такие заболевания, как сахарный диабет, недостаточность кровообращения, хроническая почечная и/или печеночная недостаточность, особенно де- и субкомпенсированные формы, хронический алкоголизм, заболевания, требующие назначения стероидных препаратов, — типичные состояниями, влияющие и иногда определяющие течение инфекционного процесса. Больным с сопутствующими заболеваниями целесообразно рекомендовать антибактериальные препараты с большей активностью, особенно в отношении таких возбудителей, как E.coli, Proteus, Klebsiella, Staphylococcus, поскольку они чаще встречаются у данной категории пациентов. Асоциальный профиль больного (наркоманы, бомжи, проститутки и др.), длительный авитаминоз, угнетенный иммунитет извращают реакцию больного на инфекционный агент и значительно снижают эффективность традиционной антибактериальной терапии.
Таблица 1. Частота встречаемости возбудителей пневмонии у детей в зависимости от возраста.
Возраст больного. Влияние возрастного фактора при выборе антибактериального препарата определяется, с одной стороны, фармакокинетикой препарата, с другой – изменяющимся с возрастом спектром вероятной микрофлоры, вызывающей те или иные заболевания (табл. 1). Назначение некоторых лекарственных препаратов противопоказано детям и новорожденным в связи с недостаточностью ферментов печени: левомицетин может вызвать развитие острой сердечно-сосудистой недостаточности; сульфаниламиды — нарушение обмена билирубина, желтуху; тетрациклин и фторхинолоны — нарушение роста костной и хрящевой ткани. У пожилых и престарелых пациентов в связи с нарушением элиминации должно быть ограничено применение аминогликозидов и полимиксина. Возрастные изменения физиологии желудочно-кишечного тракта могут приводить к нарушению всасывания, метаболизма и других фармакокинетических процессов превращения лекарственных препаратов.
Среди свойств, характеризующих патогенный микроорганизм, следует особо отметить патогенность, чувствительность и резистентность. Под патогенностью и степенью ее выраженности — вирулентностью — подразумевают способность микроорганизма в результате инфекционного процесса вызывать развитие инфекционного заболевания. В связи с этим можно выделить две группы микроорганизмов: патогенные и условно-патогенные. К первой относятся некоторые виды Shigella, ко второй — Streptococcus группы A, E coli и ряд других. Следует отметить, что основная причина возникновения неспецифических инфекционных заболеваний в клинике внутренних болезней — именно условно-патогенная флора.
С точки зрения практикующего врача, больший интерес представляет чувствительность микроорганизмов и их резистентность к проводимой антибактериальной терапии. О чувствительных бактериях говорят тогда, когда рост возбудителя прекращается при создании терапевтических концентраций лекарственного препарата в крови. К резистентным относят те штаммы, антибактериальный эффект в отношении которых может быть достигнут лишь в условиях эксперимента при высоких концентрациях, неприемлемых для клинического применения. В случае когда группа или вид бактерий не чувствительны к антибактериальному препарату, говорят о так называемой природной резистентности (устойчивость кишечной палочки к пенициллину, грибов к антибиотикам, атипических бактерий к цефалоспоринам). Все другие случаи развития устойчивости, связанные с мутацией и селекцией таких микроорганизмов, относят к приобретенной резистентности. О первичной резистентности в этом случае говорят, когда она возникает до начала проведения антибактериальной терапии у конкретного больного (нарастающая резистентность пневмококка к пенициллину, гонококка к ампициллину, гемофильной палочки к цефаклору). Вторичная развивается непосредственно в процессе конкретного курса проводимой антибактериальной терапии (устойчивость респираторных патогенов к макролидам). Именно проблема резистентности требует ограничения необоснованно широкого использования антибактериальных препаратов, разработки стандартов и алгоритмов проведения антибактериальной терапии.
Таблица 2. Наиболее часто встречающиеся возбудители неспецифической инфекции в клинике внутренних болезней.
Последнее время в литературе особое внимание уделяется проблеме атипической инфекции и трудностям терапии заболеваний, вызываемых этими возбудителями. Еще 25—30 лет назад их удельный вес среди прочих патогенов был значительно ниже и не представлял серьезной проблемы. Сложности терапии такой инфекции (хламидия, микоплазма и легионелла) связаны с внутриклеточным расположением микроорганизмов, что диктует необходимость использования антибактериальных средств, проникающих внутрь клетки (например, тетрациклины, фторхинолоны, макролиды, в меньшей степени ко-тримоксазол). Однако следует отметить и тот факт, что реальный вес атипической флоры в этиологической структуре респираторных заболеваний не превышает 8—12% в течение календарного года. Если говорить об атипической инфекции как причине летальных исходов, то данная цифра не превышает 2—6% в год. В то же время в период эпидемий, описываемых каждые три-четыре года, частота такой инфекции достигает 25—35%. Хотя утверждать, что эти данные отражают истинную картину, трудно, так как на амбулаторном этапе микробиологические и серологические исследования, необходимые для этиологической диагностики, проводятся крайне редко.
По-видимому, именно в периоды верифицированной эпидемии, а также в соответствующие месяцы года следует внимательнее относиться к диагностике атипических инфекций (табл. 3).
Гр- бактерии
Выбор конкретного антибиотика должен строиться на основании следующих данных.
Таблица 3. Частота встречаемости наиболее вероятных респираторных патогенов в зависимости от времени года.
2. Накопление препарата в тканях призвано обеспечивать достаточную концентрацию антибиотика против конкретного возбудителя. Например, широко используемые в клинической практике пенициллин и ампициллин не создают достаточно высоких концентраций к основным респираторным патогенам в мокроте, придаточных пазухах носа и барабанной полости, что значительно ограничивает целесообразность их использования при лечении инфекций верхних и нижних дыхательных путей.
Таким образом, для адекватной антибиотикотерапии важно выбрать антибиотик, с одной стороны, действующий на верифицированного или вероятного возбудителя, с другой — накапливающийся в пораженном органе в необходимой концентрации.
4. Связь с белками для практического врача, как правило, не представляет большого интереса, хотя иногда знание этого параметра может оказаться необходимым. Связь с белками учитывается при определении терапевтической дозы препарата. В то же время при назначении двух и более лекарственных препаратов с высокой связью с белками дозу препаратов необходимо уменьшать. Рассмотрим случай одновременного использования цефтриаксона (связь с белками — 99%) и нестероидного противовоспалительного препарата — бутадиона (связь с белками — 97—98%). Терапевтическая доза бутадиона рассчитывается исходя из 1—2% активной фракции. При появлении цефтриаксона с высоким сродством к альбуминам плазмы значительно большая доля бутадиона (в норме не более 1—2% от общей сывороточной концентрации) высвободится из связи с белками. Это приведет к резкому повышению концентрации его свободной активной фракции в плазме, что, в свою очередь, грозит серьезными побочными эффектами.
 |
6. Элиминация препарата представляет интерес для практического врача с точки зрения возможного влияния других лекарственных средств на выведение антибактериального препарата и с позиции выбора препарата, элиминируемого через здоровый орган (например, при заболевании почек со сниженной функцией предпочтение следует отдавать препаратам с печеночной элиминацией).
- Оценка эффективности антибактериальной терапии
Оценка клинической эффективности антибактериальной терапии позволяет сориентироваться в отношении выбора антибиотика и рекомендовать его замену в случае недостаточного антибактериального эффекта. Оценка эффективности антибактериальной терапии должна проводиться у каждого больного не менее трех раз: вторые и третьи сутки с момента ее начала с целью убедиться в правильности выбора препарата; по окончании курса для решения вопроса об ее отмене и к 3-му месяцу — после ее окончания во избежание персистенции, рецидива инфекционного заболевания.
Для наиболее полной оценки эффективности антибактериальной терапии необходимо контролировать не только данные клинического состояния больного, но и результаты бактериологического исследования.
Смена антибактериального препарата, как указывалось выше, проводится на вторые-третьи сутки, однако при ургентной ситуации, а именно при крайне тяжелом состоянии больного, такую замену можно произвести уже к концу первых суток.
Учитывая объективные трудности при выборе антибактериальных препаратов, а также недостаточный уровень подготовки врачей в вопросах практической химиотерапии, весьма целесообразной может оказаться разработка необходимых стандартов терапии инфекционных заболеваний на первичных этапах лечения. Это позволит определить оптимальный перечень наиболее эффективных и безопасных антибактериальных препаратов, контролировать сложный процесс антибиотикотерапии и создать условия для профилактики бактериальной резистентности. В то же время процесс выбора антибактериальной терапии — это творческий процесс, несомненно предполагающий определенный уровень компетентности врачей в вопросах практической химиотерапии.
Читайте также:

