Как при панкреатите лечить молочницу
Обновлено: 25.04.2024
Для цитирования: Бурова С.А. Комплексный подход к терапии больных с кандидозом органов пищеварительного тракта. РМЖ. 2015;13:760.
Грибы Candida – условно-патогенные микроорганизмы, заселяют пищеварительный тракт в норме, участвуют в процессе брожения, переваривания пищи и др. Этот феномен, называемый колонизацией, клинически протекает бессимптомно. Исследование взрослых здоровых добровольцев показало, что Candida albicans присутствует у них в орофарингеальной зоне в 20–30%, в тонком кишечнике – в 50–54%, в толстом кишечнике – в 55–70%, в фекалиях – в 65–70% случаев.
Итак, при физиологическом благополучии между макро- и микроорганизмами существует определенное равновесие, в котором играют роль, с одной стороны, факторы устойчивости организма к микроскопическим грибам, с другой – факторы патогенности грибов. Устойчивость организма зависит от принадлежности к группам риска и компетентности его иммунной системы. Для защиты важен также макрофагальный и нейтрофильный фагоцитоз, препятствующий диссеминации грибковой, особенно кандидозной инфекции.
По мнению большинства исследователей, бессимптомное пребывание грибов в желудочно-кишечном тракте (ЖКТ) может прекратиться, когда они приобретают патогенные свойства, а у пациента обнаруживается несостоятельность иммунной системы.
Наиболее частыми микозами пищеварительного тракта являются кандидоз пищевода и кандидоз кишечника, которые встречаются как у иммунокомпетентных, так и (гораздо чаще) у иммуносупрессированных лиц. Первичные микозы желудка, в т. ч. и кандидоз, диагностируют редко, что связано с физиологической кислотной средой желудка, где грибковые клетки погибают.
Факторами риска развития кандидоза пищевода и кишечника являются:
1. Заболевания ЖКТ:
- заболевания слизистых оболочек полости рта;
- гастроэзофагеальная рефлюксная болезнь;
- обсемененность желудка Helicobacter pylori;
- атрофический гастрит, гипоацидность желудка, ахалазия, бульбит;
- эрозивно-язвенные заболевания пищевода и кишечника;
- микст-инфекция кишки, дисбиоз;
- дивертикулез, полипоз;
- энтероколит, болезнь Крона, синдром раздраженного кишечника и др.
2. Другие заболевания:
- онкологические;
- гематологические;
- эндокринологические;
- аллергические;
- СПИД и ВИЧ-инфицированность.
3. Травмирование слизистой оболочки ЖКТ:
- пищеводно-желудочным зондом;
- ожоги пищевода;
- оперативные вмешательства.
4. Прием лекарственных препаратов:
- антибиотиков;
- цитостатиков;
- гормонов и других химиопрепаратов.
Нарушение питания, голодание, алкоголизм, курение, наркомания способствуют развитию кандидоза. К факторам риска относится также пожилой возраст, когда происходит старение иммунной системы, присоединяются многочисленные соматические заболевания, уменьшаются амплитуда продольных сокращений пищевода и сила сокращений сфинктеров, нарушаются процессы всасывания и т. д.
Клинически кандидоз пищеварительного тракта подразделяется на:
- орофарингеальный кандидоз (псевдомембранозный, атрофический, эритроматозный, ромбовидный глоссит, ангулярный хейлит);
- кандидозный эзофагит (эрозивный и без эрозий);
- кандидоз желудка (эрозивно-фибринозный и вторичный на фоне язвенной болезни);
- кандидоз кишечника (псевдомембранозный, коллагеновый, лимфоцитарный);
- кандидозный проктосигмоидит;
- перианальный кандидоз;
- секреторную диарею, ассоциированную с кандидозом.
Кандидозный эзофагит в стационарах общего профиля встречается у 1,3–2,8% больных, в отделениях трансплантации – до 4%, при диссеминированном карциноматозе – от 2,8 до 6,7%. Это заболевание протекает часто без субъективных жалоб и выявляется случайно при исследованиях населения в 1–7% случаев. Иногда больные отмечают боль и дискомфорт при прохождении твердой и жидкой пищи, дисфагию, гиперсаливацию. По глубине поражения эндоскопически выделяют 4 типа: от легкого отека, гиперемии, единичных белых налетов
Кандидоз желудка, как правило, развивается вторично на фоне язвенной и гастроэзофагеальной рефлюксной болезни. Ахлоргидрия в свою очередь способствует колонизации грибов на слизистой с последующей инвазией, особенно в зонах дефекта (язвы, эрозии), что замедляет репарацию (заживление), появляется болевой синдром, иногда кровоточивость язвы.
В большинстве случаев грибковые поражения ЖКТ сопровождаются изменением микробиоценоза и снижением колонизационной резистентности организма. Для лечения кандидоза ЖКТ применяют самые разнообразные антимикотики как системного, так и местного действия. Также одной из задач терапии является создание условий для роста и функционирования нормальной микрофлоры.
В современной научной литературе препараты для коррекции дисбиозов делят на 3 основные группы: пробиотики – содержат жизнеспособные микроорганизмы; пребиотики – содержат стимуляторы роста микрофлоры; синбиотики – содержат живые микроорганизмы и пребиотики. Существуют пробиотические комплексы, представляющие собой комбинацию из перечисленных выше компонентов, а также сорбентов, витаминов и микроэлементов. Средств коррекции нарушений микрофлоры кишечника достаточно много, постоянно появляются новые варианты и разновидности.
В состав комплекса Бактистатин включены дополняющие друг друга природные компоненты: сорбент, пробиотик, пребиотик. Одним из преимуществ комплекса Бактистатин является отсутствие живых бактерий, чужеродных для ЖКТ человека, длительное присутствие которых в больших количествах нежелательно. Вместо живых бактерий в состав комплекса Бактистатин включены продукты их жизнедеятельности – активные метаболиты. Поэтому Бактистатин начинает работать сразу, и его действие направлено на восстановление собственной нормальной микрофлоры, которая уникальна у каждого человека.
Нами проведено исследование по оценке эффективности и безопасности пробиотического комплекса Бактистатин в схемах терапии больных с кандидозным эзофагитом и энтероколитом.
В ходе исследования оценивались эффективность и безопасность 2-х схем лечения кандидоза пищевода и кишечника в 2-х группах: 1-я группа – контрольная, в которой пациенты получали этиотропную противогрибковую терапию; 2-я – основная группа пациентов, у которых в схему вышеназванной терапии включен комплекс Бактистатин.
В обеих группах больных проводили селективную деконтаминацию современными эффективными противогрибковыми препаратами направленного действия в течение 7–14 дней. Пациенты основной группы дополнительно получали Бактистатин по 2 капсулы 2 р./сут 20 дней.
Для изучения клинических, эндоскопических и лабораторных показателей в динамике на фоне лечения больных кандидозным эзофагитом и энтероколитом была разработана специальная анкета, включающая физикальное обследование, гастроскопию, колоноскопию, бактериологическое исследование кала.
Результаты сравнения балльной оценки клинической симптоматики показали, что на фоне приема комплекса Бактистатин быстрее уходили проявления кандидоза пищевода и кишечника. Так, до лечения общий балл выраженности симптоматики кандидозного эзофагита был 355, после лечения этот показатель снизился до 123 в контрольной группе и до 60 у пациентов основной группы, принимающих Бактистатин (рис. 1). В отношении кандидозного энтероколита до лечения общий балл выраженности симптоматики составлял 645, после лечения – 317 в контрольной группе и 120 в основной группе (рис. 2).
Кроме того, применение комплекса Бактистатин в лечении кандидоза ЖКТ существенно влияло на восстановление микробиоценоза толстой кишки за счет увеличения числа бифидо- и лактобактерий и уменьшения количества энтеробактерий, неферментирующих бактерий и грибов.
Полученные данные свидетельствуют, что использование метабиотика Бактистатин позволяет избежать побочного действия системных антимикотиков на микрофлору кишечника, улучшить состояние пищевода и кишечника в короткие сроки за счет более выраженного снижения степени тяжести заболевания.
Таким образом, применение комплекса Бактистатин в схемах терапии грибковых поражений ЖКТ способствует быстрому созданию условий для роста и функционирования нормальной микрофлоры и уменьшению побочных эффектов системных антимикотиков.
Статистика утверждает, что молочницей хоть раз в жизни переболела каждая вторая женщина. Это неудивительно, поскольку возбудитель заболевания – грибок из рода Candida – всегда присутствует на слизистых оболочках вагинальной области. Заболевание (кандидоз) развивается, когда для жизнедеятельности грибка создаются оптимальные условия, и его популяция стремительно увеличивается.

Классификация
Семейство Candida насчитывает около полутора сотен видов грибков. Из них в организме человека способны жить 20 видов. В 90% случаев заболевание вызывают грибки разновидности Candida albicans.
- при первичном заражении – при родах или в течение первого года жизни;
- при вторичном заражении – во время интимной близости (практически 100% вероятность), контактно-бытовым путем (белье, предметы обихода, пища).
- у женщин – в виде вульвовагинита (кольпита);
- у мужчин – в виде баланопостита.
Основные признаки молочницы у женщин:
- зуд, жжение, раздражение, набухание, краснота слизистых оболочек;
- творожистые выделения из половых органов, запах выделений – кисломолочный;
- боль при половом акте;
- жжение при мочеиспускании.
Заниматься сексом до полного излечения молочницы нельзя. Если заболевание диагностировано у вашего полового партнера, а вас симптомы не беспокоят, пролечиться все равно придется.
Основные признаки заражения грибком Кандида у мужчин:
- зуд, чувство жжения;
- покраснение, отечность головки, крайней плоти, белесый налет;
- боль во время полового акта.

Кандида диагностируется у женщин и мужчин
Кандидоз диагностируют по:
- внешним признакам;
- результатам бакпосева мазков из влагалища и уретры;
- ПЦР.
Как вылечить молочницу у женщины?
Candida любит теплые влажные места с минимальным доступом воздуха, поэтому на слизистой влагалища грибку более чем комфортно. Чтобы избавиться от неприятного соседства, нужно использовать препараты:
- местного действия: вагинальные свечи, таблетки, кремы с эконазолом, клотримазолом, миконазолом, эконазолом (Клотримазол, Пимафукорт);
- системного действия: таблетки, капсулы с флуконазолом, итраконазолом (Нистатин, Флуконазол, Дифлузол, Дифлюкан);
- препараты для укрепления иммунитета, пробиотики, симбиотики (Вобэнзим, Лактовит, Дактиале, Дерма-Про, Вагилак, Виферон).

Невылеченное заболевание быстро распространяется
В среднем курс лечения занимает от 3 до 6 дней. Споры грибка созревают в течение 20 дней, поэтому может понадобиться повторный курс лечения. Некоторые препараты (например, Бетадин) можно применять во время менструации.
В 20% случаев назначенное врачом лечение не помогает. Если через неделю молочница продолжает вас беспокоить:
- это – не кандидоз. Придется пересдать анализы, пройти дополнительные обследования.
- заболевание вызвано не Candida albicans, а другой разновидностью грибка, которая уничтожается сложнее;
- это – рецидив, возможный при диабете, во время антибиотикотерапии, сниженном иммунитете.
Если рецидивы кандидоза случаются более 4 раз в год, врач назначит профилактическое лечение. Исследования показали удлинение безрецидивного периода до 1,5 лет у пациенток, которые применяли препарат ГЕПОН®. Он действует на источник инфекции и корректирует симптомы молочницы. У 83% пациенток с кандидозом через два дня после применения проходили краснота, отечность, раздражение и боль.

Хронический и рецидивирующий кандидоз требует смены образа жизни
Препараты местного действия могут причинять неудобства – вытекать, пачкать одежду. Чтобы они равномерно распределялись по поверхности слизистой влагалища и не причиняли дискомфорт, лучше всего использовать их перед сном. Свечи и таблетки нужно располагать приблизительно посредине влагалища. Расположенные слишком близко лекарства вытекут, а слишком далеко – могут травмировать нежную шейку матки.
Как вылечить молочницу у мужчины?
Побороть кандидоз помогут:
- местно – кремы с клотримазолом;
- системно – флуконазол (препараты Флуконазол, Дифлазон, Форкан, Медофлюкон, Микосист).
Длительность среднестатистического курса лечения – 5 дней.
Во время лечения нижнее белье и полотенца следует менять ежедневно. Гигиенические процедуры проводятся средствами без ароматизаторов и добавок. Несмотря на то, что большинство препаратов применяется местно, во время лечения нельзя употреблять алкоголь.

Мужчинам назначают препараты местного и системного действия
Как избежать рецидива кандидоза?
Candida – условно-патогенный микроорганизм, который обычно присутствует в составе микрофлоры интимных зон. Чтобы вновь не спровоцировать его чрезмерное размножение:
- укрепляйте иммунитет;
- не носите тесное синтетическое нижнее белье;
- соблюдайте правила личной гигиены;
- употребляйте достаточное количество витаминов, сократите количество быстрых углеводов;
- сократите количество продуктов и напитков, в которых содержатся плесень и дрожжи;
- используйте средства контрацепции;
- избегайте стрессов.

Во время лечения молочницы придется подкорректировать рацион
Независимо от образа жизни молочница может развиться:
- при изменении гормонального фона (беременность, прием противозачаточных таблеток, эндокринные заболевания);
- после операций;
- в результате антибиотикотерапии;
- в ходе серьезных заболеваний;
- при дисбактериозе влагалища;
- после переохлаждения.
Что будет, если не лечить молочницу?

Невылеченная вовремя молочница чревата серьезными проблемами
- снизит иммунитет, в результате чего разовьются вторичные половые инфекции;
- спровоцирует эрозию слизистой;
- нарушит менструальный цикл;
- станет причиной воспаления шейки матки.
-
приведет к простатиту, везикулиту, способным спровоцировать бесплодие.
Как вылечить молочницу при беременности?
Статистика утверждает, что грибки Candida выявляются у 80% будущих мам. До родов с ними нужно обязательно распрощаться. Если это мероприятие отложить на потом, во время родов произойдет инфицирование малыша. Передача грибка возможна и после – во время кормления или гигиенических процедур. Это чревато молочницей во рту, у девочек – на половых органах, и чередой последующих проблем со здоровьем малыша.
Для лечения будущих мам гинекологи предпочитают использовать препараты местного действия – свечи, таблетки, кремы. Суппозитории Пимафуцин и Примафунгин можно использовать в любом триместре беременности, таблетки Тержинан – во втором. Препараты системного действия назначаются в случае, если местно вылечить заболевание не удалось. Назначает препараты и расписывает схему лечения только врач в зависимости от клинической картины, самодеятельность здесь недопустима.

Самолечение кандидоза недопустимо
Как вылечить молочницу во рту?
Поскольку грибки рода Кандида живут на всех слизистых оболочках, они могут провоцировать заболевания в полости рта. Характерные признаки:
Невылеченный вовремя кандидоз переходит с языка на щеки, затем – на губы и глотку. При попытке соскоблить налет появляется кровь.
Кандидоз слизистых оболочек ротовой полости диагностируется визуально (на запущенных стадиях), по результатам бакпосева и ларингоскопии. При лечении детей препараты подбираются с учетом возрастной категории.
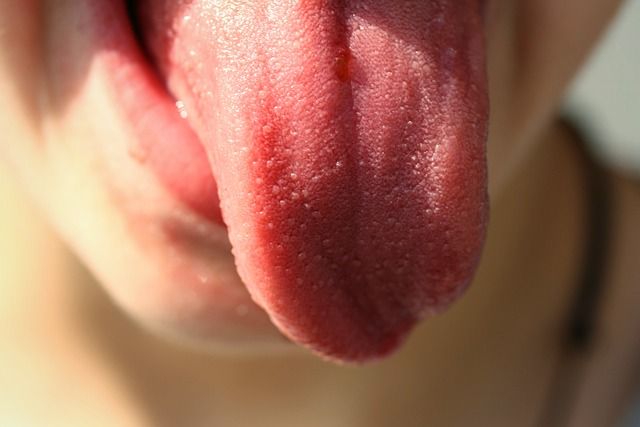
Грибки Кандида способны жить даже во рту
Молочница во рту особенно опасна для грудничков. Дискомфорт в ротовой полости заставляет их отказываться от сосания, из-за чего быстро развиваются обезвоживание и истощение. Грибковая инфекция способна распространяться на другие жизненно важные органы – кишечник, легкие и т. д. У девочек развивается влагалищный кандидоз, который провоцирует воспаления и развитие синехий.

Запущенная молочница угрожает жизни младенца
Чтобы побороть заболевание на начальной стадии, достаточно обрабатывать ротовую полость и пораженные участки антисептическим раствором (например, Мирамистином, Гексоралом, Максиколдом) и противогрибковым препаратом (например, Кандидом, Нистатином). Можно полоскать рот содовым раствором. На более тяжелых стадиях применяются препараты системного действия – Флуконазол, Микосист, Фуцис, Дифлюкан. Губы и кожу можно обрабатывать антигистаминными препаратами (Фенистил). Избегайте их попадания на слизистые (глаза, нос, ротовая полость).
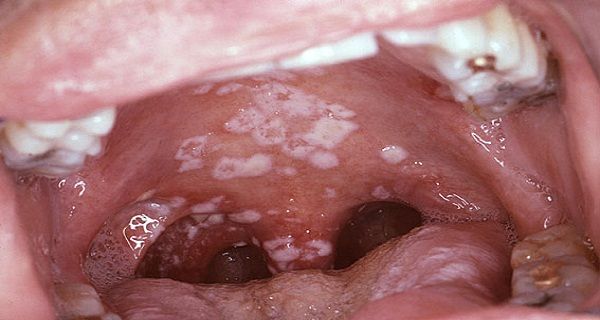
Невылеченный грибок колонизирует небо, пищевод, легкие, другие органы
На период лечения сократите потребление сладостей, избегайте копченостей, острых, соленых блюд, продуктов с содержанием дрожжей, плесени.
Ни в коем случае не смазывайте пораженные участки слизистых и кожи вареньем из розы. Это способствует разрастанию колоний грибка.
Лечение всех видов молочницы нужно проводить под контролем врача. Укрепляйте иммунитет, следуйте рекомендациям диетологов, используйте контрацептивы, и неприятное соседство с большой долей вероятности вам не грозит. Будьте здоровы!
Источники
- Богомолова, Н.С. Кандидозы в хирургической клинике: видовой состав возбудителей, чувствительность к антибиотикам, превентивная терапия / Н.С. Богомолова [и др.] // Анестезиология и реаниматология. - 2011. - №5. - С. 43-48;
- Вознесенский, А.Г. Клиническая фармакология противогрибковых препаратов / А.Г. Вознесенский // Гедеон Рихтер в СНГ. - 2001. - № 2(6). - С. 50-53;
- Волосач, О.С. Метод комбинированной иммунотерапии пациентов с хроническими воспалительными заболеваниями, осложненными кандидозом : инструкция по применению № 084-0909 : утв. 17.09.2009 г. / Министерство здравоохранения Республики Беларусь ; сост. О.С. Волосач, В.М. Цыркунов, С.Б. Позняк, С.М. Дешко.
Как лечить молочницу (отвечает гинеколог Л.Шупенюк)
Как вылечить молочницу у женщин и мужчин. Простые советы. Эффективные средства
Заболевания поджелудочной железы являются одними из наиболее распространенных поражений органов пищеварения. Среди больных преобладают женщины.
Заболевания поджелудочной железы являются одними из наиболее распространенных поражений органов пищеварения. Среди больных преобладают женщины. Это, по-видимому, связано с более высокой частотой встречаемости у них желчно-каменной болезни (ЖКБ) и нарушений жирового обмена. Значительную часть больных составляют пожилые и престарелые лица, однако в последнее время поражения поджелудочной железы все чаще встречаются и у детей различного возраста. В настоящее время существуют различные рекомендации и стандарты, посвященные ведению больных с панкреатитом. Наиболее известными являются критерии Атланты 1992 г. [1] и консенсунс, принятый в 1999 г. в Сантрони [2], с пересмотром в 2003 г.
Среди воспалительных заболеваний поджелудочной железы различают острый и хронический панкреатит. Причины поражения поджелудочной железы многообразны. В частности, к ним относятся: обструкция панкреатического протока, воздействие лекарственных препаратов или токсическое отравление различными веществами, метаболические нарушения как самой поджелудочной железы, так и других органов и систем, инфекционные и паразитарные заболевания, сосудистые нарушения и травмы.
Острый панкреатит является полиэтиологическим заболеванием. В основе острых панкреатитов лежит ферментативное поражение поджелудочной железы, носящее автокаталитический характер. Выделяют две группы причин заболевания. К первой относятся факторы, вызывающие затруднение оттока панкреатического сока по протокам поджелудочной железы и приводящие вследствие этого к острому повышению давления в них, с развитием гипертензионно-протоковой формы острого панкреатита. Вторую группу составляют факторы, приводящие к первичному поражению ацинозных клеток с развитием первично-ацинарной формы заболевания.
Острое поражение поджелудочной железы может возникать при приеме различных лекарственных препаратов, таких как метилдопа, 5-аминосалицилаты, азатиоприн, циметидин, фуросемид, метронидазол, тетрациклины, при переполнении паренхимы поджелудочной железы рентгеноконтрастными препаратами во время проведения инструментальных эндоскопических исследований. Кроме того, причинами развития острого панкреатита как у взрослых, так и у детей могут явиться метаболические нарушения, в частности гипертриглицеридемия — гиперлипидемия I, IV или V типа.
Из инфекционных заболеваний наиболее частой причиной развития панкреатитов являются: вирусные заболевания (цитомегалия, герпес, гепатиты А, В, С), бактериальные (микобактериоз, лептоспироз), грибковые поражения (криптококки, кандида), а также паразитарные инвазии (аскариды, закупоривающие просвет выводного протока поджелудочной железы, или пневмоцистоз).
Хронический панкреатит представляет собой длительно текущее, как правило, прогрессирующее воспалительное заболевание поджелудочной железы. При этом развивается очаговая или диффузная деструкция ткани железы с постепенным замещением ее соединительной тканью. Основными этиологическими факторами развития хронического панкреатита являются те же, что и для острого панкреатита, которые непосредственно повреждают ацинозные элементы или способствуют повышению давления в панкреатических протоках, однако действующие более длительно и менее интенсивно.
В соответствии с Атлантскими критериями правильный диагноз острого панкреатита должен быть установлен у всех пациентов в течение 48 часов после поступления (уровень рекомендации C). Этиология острого панкреатита должна быть определена, по крайней мере, в 80% случаев и не больше чем в 20% должна быть классифицирована как идиопатическая (уровень рекомендации B) [3].
Если причину развития заболевания установить не удается, следует говорить об идиопатическом хроническом панкреатите.
Исследования, необходимые для определения этиологических факторов, вызвавших острый панкреатит, в зависимости от стадии течения болезни, а также анамнестические данные, позволяющие исключить другие причины развития острого панкреатита, представлены в таблице.
Длительные нарушения функции поджелудочной железы могут приводить к развитию хронических изменений, проявляющихся в виде хронического кальцифицирующего панкреатита, хронического воспалительного панкреатита или хронического обструктивного панкреатита.
Врожденные нарушения деятельности поджелудочной железы, которые в дальнейшем могут проявиться развитием воспалительной реакции, связаны с аутосомно-доминантными аномалиями гена или хромосомы 7G, ассоциированными с раком головки поджелудочной железы.
Нарушение деятельности поджелудочной железы, не сопровождающееся, как правило, воспалительной реакцией, однако имеющее определенную клиническую симптоматику, получило название панкреатической недостаточности.
Различают первичную и вторичную панкреатические недостаточности. Первичная панкреатическая недостаточность развивается вследствие воздействия так называемых немодифицируемых факторов, на которые человек (сам пациент или врач) воздействовать и влиять не может. К ним относятся такие заболевания, как кистозный фиброз поджелудочной железы, врожденное нарушение проходимости панкреатического протока, синдром Shwachman, изолированный дефицит липазы, изолированная недостаточность трипсина, наследственный рецидивирующий панкреатит.
В клинической практике чаще встречается вторичная или относительная недостаточность поджелудочной железы (панкреатопатия), вызываемая, как правило, приемом необычной пищи, ее избыточным количеством или временными расстройствами функционирования поджелудочной железы. Вторичная недостаточность может сопровождать различные воспалительные заболевания верхнего отдела пищеварительного тракта (ВОПТ).
Клиническими проявлениями панкреатической недостаточности являются признаки нарушения деятельности поджелудочной железы — боль в животе, изменение аппетита (уменьшение или полное исчезновение), тошнота, урчание в животе, метеоризм и флатуленция, стеаторея. Интенсивность и выраженность этих признаков зависит от степени поражения поджелудочной железы.
Диагностика вторичной панкреатической недостаточности нередко может представлять значительные трудности из-за нечеткости клинических симптомов, незначительных изменений при инструментальных методах исследования. Поэтому для правильной диагностики и своевременного назначения адекватного лечения врач должен использовать весь арсенал средств, находящийся в его распоряжении. При панкреатической недостаточности боли локализуются в эпигастрии, левом подреберье или бывают опоясывающими, иррадиируют в левое подреберье, под левую лопатку, в спину. Боли могут быть приступообразными и постоянными, они усиливаются после переедания, употребления жирной, острой и жареной пищи, алкоголя. Тепло усиливает боли, применение холода несколько уменьшает. Боли с трудом купируются лекарственными препаратами. Боли несколько ослабевают при вынужденных положениях больного — коленно-локтевом, сидя, согнувшись вперед, лежа на боку с притянутыми к груди коленями. Болевой синдром сопровождается симптомами кишечной диспепсии и нарушениями стула, при этом больные жалуются на вздутия и урчание в животе, могут быть запоры и поносы. Стул при поносах обильный, жидкий, пенистый, светло-желтого цвета из-за большого количества жира. Характерны также признаки желудочной диспепсии — тошнота и рвота, которая не приносит облегчения.
При недостаточности поджелудочной железы применяются различные лекарственные средства, содержащие ферменты. Традиционно для этого используется панкреатин — препарат, приготовленный из поджелудочной железы животных [8]. Однако в условиях интенсивного кислотообразования в желудке наступала его частичная инактивация, и препарат не оказывал ожидаемого лечебного эффекта. В дальнейшем, с развитием фармацевтической промышленности, знаний о механизме процессов пищеварения, появились новые формы препаратов, содержащих панкреатин в виде таблеток, драже, гранул с защитной оболочкой и микросфер, помещенных в капсулу. В настоящее время ферментные препараты, используемые в клинической практике, должны отвечать определенным требованиям: 1) нетоксичность; 2) хорошая переносимость; 3) отсутствие существенных побочных реакций; 4) оптимум действия в интервале рН 5–7; 5) устойчивость к действию соляной кислоты, пепсинов и других протеаз; 6) содержание достаточного количества активных пищеварительных ферментов; 7) иметь длительный срок хранения [9].
В зависимости от фазы развития патологического процесса можно выделить четыре формы острого панкреатита: острый интерстициальный, соответствующий фазе отека (серозного, геморрагического, серозно-геморрагического), острый некротический, выражающий фазу образования некроза (с геморрагическим компонентом или без него); инфильтративно-некротический и гнойно-некротический, соответствующий фазе расплавления и секвестрации некротических очагов.
Для облегчения выбора тактики лечения, объема инфузионной терапии и правильной интерпретации формы панкреатита выделяют легкую, среднюю и тяжелую степени интоксикации.
Легкая степень (встречающаяся обычно при серозном отеке поджелудочной железы) характеризуется удовлетворительным общим состоянием больного, умеренными болями в эпигастрии, тошнотой, однократной рвотой, отсутствием симптомов раздражения брюшины, неизмененным цветом кожных покровов, частотой пульса в пределах 88–90 ударов в минуту, нормальным или слегка повышенным артериальным давлением (АД), высокими цифрами уроамилазы, небольшой активностью трипсина и липазы, сохраненным или слегка сниженным объема циркулирующей крови (ОЦК) (дефицит 7–15%), умеренным лейкоцитозом, субфебрильной температурой.
Средняя степень интоксикации (наблюдается при мелкоочаговом некрозе железы) проявляется упорными болями в эпигастрии, которые не исчезают при применении спазмолитиков и анальгетиков, бледностью и цианотичностью кожных покровов, повторными рвотами, напряжением мышц в эпигастральной области, частотой пульса до 100–110 уд./мин, падением АД ниже исходного уровня, повышением периферического и снижением центрального венозного давления (ЦВД), высокими цифрами уроамилазы, ранней высокой активностью трипсина и липазы, снижением уровня Са и повышенным содержанием сиаловых кислот, уменьшением ОЦК (дефицит 16–35%), снижением диуреза, подъемом температуры тела до 38 °С.
Тяжелая степень интоксикации (возникает при распространенном некрозе железы) отличается тяжелым общим состоянием больного, жестокими болями в эпигастральной области, мучительной рвотой, резко бледными или цианотичными кожными покровами, нередко желтухой, появлением симптомов перитонита, частотой пульса свыше 120 уд./мин, падением уровня АД и ЦВД, снижением уроамилазы, активности трипсина и липазы, уровня Са, низким диурезом, вплоть до полной анурии, резким снижением ОЦК (дефицит 36–50%), высокой температурой, значительным нарушением функции сердца, печени, легких, почек.
В лечении острого панкреатита с самого начала превалировал оперативный метод, предложенный немецким хирургом Korbe в 1894 г. Однако высокая летальность (90–100%) даже в то время заставила сдержанно относиться к этому методу [10]. На 5-м Всероссийском съезде хирургов академик В. С. Савельев (1978) подчеркнул, что в настоящее время общепризнан преимущественно консервативный метод лечения острого панкреатита. Однако лечебная тактика диктуется главным образом формой заболевания. Если при интерстициальном и некротическом панкреатите решающее значение имеет своевременное проведение консервативной терапии и, в меньшей степени, операции, а при инфильтративно-некротическом — только консервативное лечение, то гнойно-некротическая форма требует обязательного оперативного вмешательства.
Современная консервативная терапия острого панкреатита решает следующие задачи:
1) ликвидация боли и спазма, улучшение микроциркуляции в железе;
2) борьба с шоком и восстановление гомеостаза;
3) подавление экзокринной секреции и активности ферментов железы;
4) борьба с токсемией;
5) нормализация деятельности легких, сердца, почек, печени;
6) профилактика и лечение осложнений.
В лечении панкреатита ведущее значение имеет обеспечение уменьшения панкреатической секреции, так как усиленная секреция богатого ферментами сока поджелудочной железы, особенно при значительной закупорке протока, приводит к прогрессированию процесса. Больные с тяжелым острым панкреатитом должны лечиться в отделении интенсивной терапии.
При любом варианте течения острого панкреатита лечение начинают с назначения голода, который в зависимости от тяжести заболевания назначают на 3–5 дней. При легком процессе спустя этот срок больные способны принимать пищу без боли, расширяют рацион питания, постепенно выздоравливают и в дальнейшем не требуют продолжения лечения. При более тяжелом заболевании в первые дни осуществляется постоянная аспирация желудочного содержимого и быстро определяется оптимальная тактика ведения больного. Необходимо отметить, что при грамотном ведении больные острым панкреатитом средней степени тяжести без развития панкреонекроза и парапанкреатической флегмоны могут быть излечены консервативными методами.
При выборе тактики лечения больных острым панкреатитом наиболее важно дифференцировать отечные и интерстициальные формы острого панкреатита. Показателями начавшегося некротического процесса являются изменения в сыворотке крови концентрации С-реактивного белка и эластазы. Пациенты с отечной формой панкреатита нуждаются в консервативной терапии и динамическом наблюдении, тогда как пациенты с панкреонекрозом в интенсивной терапии. Выбор тактики ведения больных определяется и функциональной состоятельностью органов и наличием сопутствующей патологии. Пациентов без сопутствующей органной патологии и с ограниченным некрозом можно лечить консервативно, тогда как пациенты с полиорганной недостаточностью или прогрессированием сопутствующей патологии являются кандидатами для хирургического лечения.
Важнейшее значение в остром периоде панкреатита придается ликвидации ведущего болевого синдрома, для чего чаще всего используют сочетание ненаркотических анальгетиков и спазмолитиков.
- Метамизол натрия внутрь по 250–300 мг 2–3 р/сут
или - 50% раствор в/м или в/в 0,1–0,2 мл/10 кг до купирования болевого синдрома
или - Парацетамол внутрь 0,5 г 2–3 р/сут до купирования болевого синдрома
в сочетании с:
- Гиосцина бутилбромид внутрь 20 мг 3–4 р/сут, до купирования болевого синдрома
или - Дротаверин внутрь по 30–40 мг 3–4 р/сут
или - Папаверин внутрь или ректально по 15–20 мг 3–4 р/сут, до купирования болевого синдрома
или - Платифиллин внутрь или п/к 3–4 мг 2–3 р/сут до купирования болевого синдрома.
В случае выраженного болевого синдрома рационально использовать наркотические анальгетики, такие как Промедол [11].
Заместительная ферментная терапия панкреатита направлена на устранение нарушений переваривания жиров, белков и углеводов. Среди большого количества панкреатических ферментов, используемых в гастроэнтерологии, предпочтение отдается лекарственным средствам, в наибольшей степени отвечающим современным требованиям:
- устойчивость к действию соляной кислоты, наличие кислотоустойчивой оболочки;
- активность липазы не менее 25000 ЕД на прием, оптимум действия ферментов в диапазоне рН 5–7;
- равномерное и быстрое перемешивание с пищей, размер микрокапсул не более 2 мм;
- быстрое высвобождение ферментов в 12-перстной кишке.
Традиционные панкреатические ферменты в виде таблеток или драже, как правило, разрушаются соляной кислотой желудочного сока, что требует увеличения суточной дозы препаратов для коррекции внешнесекреторной недостаточности. Лучшим эффектом обладают микрогранулированные ферменты [12].
Диета при панкреатите играет важную роль на всех этапах наблюдения за больными и основывается на механическом, термическом и химическое щажении поджелудочной железы, подавлении гиперферментемии, уменьшении стаза в протоках и 12-перстной кишке, уменьшении рефлекторной возбудимости желчного пузыря.
Нутритивная поддержка — это полноценное питание за счет частичного или полного парентерального и энтерального питания. Ее основная цель: обеспечение организма донаторами энергии (углеводами, липидами), пластическим материалом (аминокислотами); коррекция метаболических расстройств и восстановление трофологического статуса больного. Раннее парентеральное и энтеральное питание ускоряет репаративные процессы в ЖКТ.
Алгоритм нутритивной поддержки составляется с учетом оценки состояния больного и включает этапы парентерального, энтерального или смешанного питания и собственно диетическую терапию (диета № 5П). Лечебное питание рассматривается как фармакотерапия различных метаболических нарушений и является основным путем качественного обеспечения энергопластических потребностей организма больного.
Эффективность терапии панкреатита оценивается по динамике болевого и диспептического синдромов, нормализации уровня ферментов крови и мочи, показателей копрограммы, фекальной эластазы и увеличения массы тела больного.
Литература
- Bradley E. L. III. A clinically based classification system for acute pancreatitis. Summary of the International Symposium on Acute Pancreatitis, Atlanta, Ga, September 11 through 13, 1992 // Arch Surg. 1993; 128: 586–590.
- Dervenis C., Johnson C. D., Bassi C. et al. Diagnosis, objective assessment of severity, and management of acute pancreatitis. Santorini consensus conference // Int J Pancreatol. 1999; 25: 195–210.
- Toouli J., Brook-Smith M., Bassi C. et al. Guidelines for the management of acute pancreatitis // J Gastroenterol Hepatol. 2002; (Suppl 17): S15–39.
- Johnson C. D., Abu-Hilal M. Persistent organ failure during the first week as a marker of fatal outcome in acute pancreatitis // Gut. 2004; 53: 1340–1344.
- McKay A. J., Imrie C. W., O’Neill J. et al. Is an early ultrasound scan of value in acute pancreatitis? // Br J Surg. 1982; 69: 369–372.
- Hogan W. J., Sherman S., Pasricha P. et al. Sphincter of Oddi manometry // Gastrointest Endosc. 1997; 45: 342–48.
- Brown A., Baillargeon J. D., Hughes M. D. et al. Can fluid resuscitation prevent pancreatic necrosis in severe acute pancreatitis? // Pancreatology. 2002; 2: 104–107.
- Graham D. Y. Enzyme replacement therapy of exocrine insufficiency in man. Relation between in-vitro potency in commercial pancreatic extracts // N. Engl. J. Med. 1977. 296. P. 1314–1317.
- Златкина А. Р, Белоусова Е. А., Никитина Н. В., СиливерстоваТ. Р. Современная терапия хронического панкреатита. 2-я Гастр. неделя. 1996. Отдельн. выпуск. 4 с.
- Li H., Qian Z., Liu Z., Liu X., Han X., Kang H. Risk factors and outcome of acute renal failure in patients with severe acute pancreatitis // J Crit Care. Sep 23, 2009.
- Минушкин О. Н. Хронический панкреатит: вопросы патогенеза, диагностики и лечения // Трудный пациент. М., 2003. № 1. С. 26–30.
- Ивашкин И. Т. Современные вопросы клинической панкреатологии // Вестник РАМН. 1993. № 4. С. 29–34.
П. Л. Щербаков, доктор медицинских наук, профессор
ЦНИИ гастроэнтерологии, Москва
Что такое вагинальный кандидоз (молочница)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Соснина А. С., гинеколога со стажем в 15 лет.
Над статьей доктора Соснина А. С. работали литературный редактор Вера Васина , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Вагинальный кандидоз (кандидозный вагинит) — поражение слизистой оболочки влагалища дрожжеподобными грибами рода Candida. В быту эту болезнь называют молочницей .
Краткое содержание статьи — в видео:
Candida — это условно-патогенные микроорганизмы, факультативные анаэробы (организмы, способные жить как в присутствии кислорода, так и без него). Они обладают тропизмом — направлением роста на клетки богатые гликогеном, в частности клетки слизистой оболочки влагалища. Самый распространённый вид возбудителя, который встречается в 70—90 % случаев, — Candida albicans.
В последние годы растёт заболеваемость кандидозом, вызванным другими представителями рода Candida. Наиболее часто выявляются:
- С. glabrata (15 %);
- C. dubliniensis (6 %);
- C. tropicalis (3—5 %);
- C. parapsilosis (3 %);
- C. krucei (1—3 %).
Распространение новых видов микроорганизмов связано в первую очередь с бесконтрольным самолечением пациенток, приводящем к возрастающей устойчивости грибов к препаратам [3] [4] .
Частота кандидозного вагинита среди инфекционных заболеваний влагалища и вульвы составляет 30—45 %. Патология занимает второе место среди всех инфекционных заболеваний влагалища и является крайне распространённым поводом для обращения женщин за медицинской помощью. По данным J. S. Bingham (1999):
- к 25 годам около 50 % женщин репродуктивного возраста сталкивались с хотя бы одним диагностированным врачом эпизодом вагинального кандидоза;
- к началу периода менопаузы — около 75 % [17] .
Кандидозный вагинит редко наблюдается в постменопаузе, за исключением тех пациенток, которые получают гормональную заместительную терапию.
Предрасполагающими факторами заболевания являются:
- Механические — ношение синтетического белья, первый половой контакт, травматическое повреждение тканей влагалища, длительное применение внутриматочной спирали.
- Физиологические — беременность, менструация.
- Эндокринные — гипотиреоз, сахарный диабет.
- Иммунодефицитные состояния.
- Ятрогенные (приём антибиотиков, кортикостероидов, иммуносупрессоров, лучевая терапия, химиотерапия, онкологические заболевания, оральные контрацептивы).
- Прочие (авитаминоз, аллергические заболевания, хронические патологии гениталий и желудочно-кишечного тракта).
Заболевание, как правило, не передаётся половым путём, но установлено, что оно связано с характером половых контактов: анально-вагинальным и орогенитальным. Также не исключается вероятность развития кандидозного баланопостита у половых партнёров пациенток с вагинальным кандидозом.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы вагинального кандидоза
Основные симптомы при вагинальном кандидозе:
- жжение и зуд в области влагалища и вульвы;
- творожистые выделения из влагалища;
- расстройства мочеиспускания;
- боль при половом акте.
Зуд может усиливаться после водных процедур, полового акта, ночью во время сна и в период менструации [1] .
В целом симптомы вагинального кандидоза нарастают перед менструацией. При беременности проявление болезни также усугубляется, это связано со снижением иммунитета у беременных женщин.
Объективные признаки вагинального кандидоза:
- отёк и гипермия слизистой оболочки влагалища и наружных половых органов;
- белые или зеленовато-белые наложения на стенках влагалища;
- покраснение слизистой влагалища.
При осложнённом кандидозе на коже наружных половых органов появляются везикулы — пузырьки, возвышающиеся над уровнем кожи или слизистой и заполненные прозрачным или мутным содержимым, которые могут вскрываться и образовывать эрозии. При вагинальном кандидозе также могут наблюдаться трещины слизистой вульвы, задней спайки и перианальной области [2] .
Патогенез вагинального кандидоза
Грибы рода Candida относятся к условно-патогенной микрофлоре, которая присутствует как в окружающей среде, так и на поверхности кожных покровов и слизистых оболочках здорового человека (в полости рта, кишечнике, влагалище). При снижении защитных сил организма возможно повышение адгезивных свойств (способности прилипать) грибов с прикреплением их к клеткам эпителия влагалища, колонизацией слизистой оболочки и развитием воспалительной реакции [7] .
Вагинальный кандидоз зачастую затрагивает только поверхностные слои эпителия влагалища без проникновения возбудителя в более глубокие слои слизистой оболочки. Однако в редких случаях эпителиальный барьер преодолевается и происходит инвазия в подлежащую ткань с последующей гематогенной диссеминацией (распространением возбудителя инфекции из первичного очага заболевания по всему органу или организму посредством кровотока) [8] [9] .
Основные этапы патогенеза:
- Адгезия (прилипание) грибов на слизистой и колонизация.
- Инвазия (проникновение) в эпителий.
- Преодоление эпителиального барьера.
- Проникновение в соединительную ткань.
- Преодоление защитных механизмов ткани.
- Попадание в сосуды.
- Гематогенная диссеминация.
При вагинальном кандидозе воспаление происходит в верхних слоях эпителия влагалища. Причина состоит в том, что поддерживается динамическое равновесие между грибом, который не может проникнуть в более глубокие слои, и организмом, который сдерживает его распространение. Соответственно инфекция может долго развиваться в одном месте, проявляясь творожистыми выделениями из влагалища. Обострение заболевания происходит при сдвиге равновесия между развитием грибов и защитными силами организма.
Классификация и стадии развития вагинального кандидоза
Согласно национальным клиническим рекомендациям [18] , выделяют две формы вагинального кандидоза:
- острую — до трёх обострений в год;
- хроническую (рецидивирующую) — не менее четырёх обострений в год.
По классификации, предложенной D.A. Eschenbach, вагинальный кандидоз подразделяют на два типа:
У женщин различают три формы заболевания:
- вагинит (воспаление влагалища); (воспаление влагалища и вульвы); (воспаление шейки матки).
У мужчин выделяют:
- баланит (воспаление головки полового члена);
- баланопостит (воспаление крайней плоти и головки полового члена); (воспаление мочеиспускательного канала).
Для острой формы вагинального кандидоза характерны выраженные симптомы: обильные выделения из влагалища, жжение и зуд во влагалище и наружных половых органах. На фоне таких симптомов нередко снижается трудоспособность пациентки и развиваются неврозы. Острая форма вагинального кандидоза встречается наиболее часто и формируется в результате увеличения количества грибов рода Candida во влагалище на фоне снижения иммунитета пациентки.
Рецидивирующий вагинальный кандидоз — встречается у 10—15 % женщин репродуктивного возраста и проявляется четырьмя и более обострениями за год [11] .
Неосложнённая форма заболевания предполагает впервые выявленный или возникающий менее четырёх раз в год вагинальный кандидоз с умеренными проявлениями вагинита у пациенток без сопутствующих факторов риска (сахарный диабет, приём глюкокортикоидов, цитостатиков и др.).
При осложнённом вагинальном кандидозе наблюдаются яркие объективные симптомы: покраснение, отёк, образование язв, трещин слизистых оболочек и кожи перианальной области. Также характерны рецидивы четыре и более раз в год. Заболевание часто возникает на фоне сахарного диабета, ВИЧ-инфекции, терапии глюкокортикоидами и цитостатиками. Возбудителем заболевания в данном случае являются как C. albicans, так и другие грибы рода Candida.
Осложнения вагинального кандидоза
К осложнениям вагинального кандидоза у женщин относятся:
- стеноз влагалища;
- воспалительные патологии органов малого таза — сальпингит, оофорит и другие;
- заболевания мочевыделительной системы — цистит, уретрит[2] .
Стеноз влагалища развивается при воспалении стенок влагалища. При этом просвет влагалища сужается, а стенки влагалища становятся плохо растяжимы. Пациентки испытывают боль при половом акте.
Сальпингит — инфекционно-воспалительное заболевание фаллопиевой (маточной) трубы. Возникает при переходе инфекции восходящим путем из влагалища, не исключен также и гематогенный путь передачи. Сальпингит чаще всего протекает в сочетании с оофоритом — воспалением яичника. Поражение может быть как односторонним, так и двусторонним. Пациентки испытывают боль в области придатков, внизу живота слева или справа, повышается температура тела, возникает общее недомогание, слабость, а иногда и тошнота со рвотой. При несвоевременном лечении данного осложнения высок риск бесплодия, наступления внематочной беременности, возникновения спаечного процесса, приводящего к оперативному вмешательству, инфицированию органов брюшины и малого таза. Сальпингит особенно опасен в случаях, когда с кандидозом сочетаются другие инфекции [1] .
Уретрит — воспаление слизистой мочеиспускательного канала. Проявляется болезненным мочеиспусканием, чувством жжения в области уретры, выделением с мочой крови или гноя, дискомфортом при соприкосновении с бельём, слипанием краёв уретры, покраснением области вокруг мочеиспускательного канала.
Цистит — воспаление мочевого пузыря. Патология возникает при попадании возбудителя восходящим путём через уретру в мочевой пузырь. Симптомы цистита схожи с симптомами уретрита, однако есть некоторые отличия: частые позывы к мочеиспусканию при небольшом количестве мочи, чувство неполного опорожнения мочевого пузыря, боль, резь в конце мочеиспускания, помутнение мочи, повышение температуры тела, боли внизу живота.
На фоне вагинального кандидоза возрастает частота осложнений при беременности, а также увеличивается риск инфицирования плода.
Кандидоз плода может вызвать его внутриутробную гибель или приводить к преждевременным родам. После родов у женщин возможно развитие кандидозного эндометрита — воспалительного процесса в тканях, выстилающих внутреннюю полость матки.
Диагностика вагинального кандидоза
Диагностика вагинального кандидоза основывается на характерных жалобах пациентки, данных анамнеза, клинических проявлениях, выявленных при гинекологическом осмотре. В зеркалах видна гиперемия, отёк слизистой, белые налёты на стенках влагалища.
Независимо от этих признаков, подтверждение диагноза должно основываться на лабораторных данных:
- Микроскопия мазков вагинального отделяемого — позволяет выявить споры и мицелий гриба.
- Культуральный метод — посев влагалищного содержимого на искусственные питательные среды. Метод определяет количество, видовую принадлежность, чувствительность к противогрибковым препаратам, а также характер и степень заселения другими микроорганизмами. Культуральный метод дополняет микроскопию.
- Серологическая диагностика (РСК). Определяет антитела против антигенов грибов рода Candida. Такая диагностика имеет значение при генерализации процесса.
- Молекулярно-биологические методы. Направлены на обнаружение специфических фрагментов ДНК Candida spp. Применяют метод полимеразной цепной реакции (ПЦР).
- Иммунофлюоресцентная диагностика (Candida Sure Test) проводится в случае рецидивирующего течения вагинального кандидоза [15] .
К дополнительным методам диагностики относятся: изучение микробиоценоза кишечника, обследование на инфекции, передаваемые половым путём, внутривенный тест на толерантность к глюкозе [16] .
Дифференциальную диагностику проводят со следующими заболеваниями:
- генитальным герпесом; ;
- аэробным вагинитом;
- кожными заболеваниями (экземой, красным плоским лишаём, склеродермией, болезнью Бехчета и др.).
Лечение вагинального кандидоза
Показаниями к назначению терапии вагинального кандидоза являются жалобы пациентки, клинические проявления и лабораторное подтверждение наличия грибов рода Candida. Лечение не требуется при обнаружении грибов без каких-либо клинических проявлений (кандидозоносительство). Это правило обусловлено тем, что грибы рода Candida могут содержаться в небольшом количестве во влагалище и являются частью нормальной микрофлоры, если их количество не превышает пороговое значение 10 4 .
Механизм действия противогрибковых препаратов — нарушение синтеза эргостерола (вещества в составе клеточных мембран грибов), что приводит к образованию дефектов в мембране микроорганизма. В зависимости от дозы антимикотики проявляют фунгистатическое (замедление роста) или фунгицидное (полное уничтожение) действие [15] .
Существуют различные группы препаратов для лечения вагинального кандидоза:
- антибиотики (пимафуцин, амфотерицин В, нистатин, леворин);
- имидазолы (клотримазол, сертаконазол, кетоконазол, гино-певарил, миконазол);
- триазолы (итраконазол, флуконазол);
- комбинированные препараты ("Тержинан", "Полижинакс", "Пимафукорт", "Клион Д", "Макмирор комплекс");
- препараты разных групп (флуцитозин, гризеофульвин, дафнеджин, нитрофунгин, йодат поливинилпирролидон).
Лечение подбирается гинекологом индивидуально для каждой пациентки, учитывая клиническую картину, форму заболевания и степень выраженности симптомов. Но важно отметить, что при лечении молочницы при беременности флуконазол противопоказан, так как он может негативно повлиять на развитие плода [19] [20] .
При лечении острых форм вагинального кандидоза назначают местное лечение. Препарат не всасывается в системный кровоток, а действует в области влагалища и слизистой. Примеры схем лечения:
-
150 мг в виде вагинальных свечей один раз в сутки в течение трёх дней; один аппликатор крема на ночь вагинально в течение трёх дней; одна свеча на ночь один раз в сутки в течение восьми дней; одна таблетка на ночь в течение 10 дней.
При хроническом кандидозе наряду с местным лечением применяют системные антимикотики:
-
150 мг один раз внутрь; 200 мг внутрь два раза с интервалом 12 часов в течение одного дня или 200 мг в сутки в течение трёх дней.
При рецидивирующей форме заболевания (более четырёх эпизодов в год) применяют схему:
-
150 мг внутрь три раза с интервалом 72 часа в 1,4 и 7 день лечения.
Для купирования рецидивов препарат применяют в дозировке 150 мг один раз в неделю в течение шести месяцев.
В последние годы всё больше исследуется способность C. albicans формировать биоплёнки — вещества на поверхности колонии микроорганизмов, которые служат барьером для проникновения лекарственных средств и обеспечивают выживание. Основным полисахаридом, определяющим развитие резистентности к антибиотикам, является глюкан. Его рассматривают как одну из причин формирования резистентности к антимикотическим препаратам. Этим объясняется отсутствие эффекта при лечении у некоторых больных. Таким пациенткам можно порекомендовать препарат фентиконазол 600 мг в сутки с интервалом в три дня. Лекарство отличается от других способностью преодолевать биоплёнки, тем самым повышая эффективность лечения при резистентности к другим препаратам.
Прогноз. Профилактика
При своевременном обращении пациентки к врачу, лабораторном обследовании и отсутствии самолечения прогноз благоприятный. Самолечение опасно из-за риска рецидива заболевания, его хронизации и возникновения резистентности к препарату, неверно выбранному пациенткой или при неадекватной дозе.
Чтобы повысить эффективность терапии пациентки должны следовать схеме лечения, индивидуально назначенной гинекологом. Во время лечения и диспансерного наблюдения необходимо соблюдать половой покой или применять барьерные методы контрацепции. Повторно обратиться к врачу для контроля анализов следует через 7-10 дней [12] .
Читайте также:

