Как проваливается нос от вич
Обновлено: 24.04.2024
У кого высокий риск заболеть СПИДом? Передается ли ВИЧ при поцелуях и укусе насекомых?
Вирус иммунодефицита человека, который называют вкратце ВИЧ, является возбудителем ВИЧ-инфекции. Поражает он иммунную систему человека, точнее убивает специфические белые кровяные клетки - лимфоциты СД4, которые являются важными клетками иммунной системы. Без них ослабляются и разрушаются защитные свойства организма, в результате чего возрастает угроза инфекционных и опухолевых заболеваний, неврологических расстройств, которые приводят к летальному исходу. Чем меньше этих лимфоцитов в организме, тем больше человек беззащитен перед любыми инфекциями.
Источником заражения ВИЧ являются носители вируса иммунодефицита и больные СПИДом (синдром приобретенного иммунодефицита). Многие думают, что ВИЧ и СПИД - это разные наименования одного и того же заболевания. Но это не совсем так. СПИД - это последняя стадия ВИЧ-инфекции. С момента заражения ВИЧ-инфекцией до развития СПИДа может пройти 3 - 15 лет, а иногда и больше.
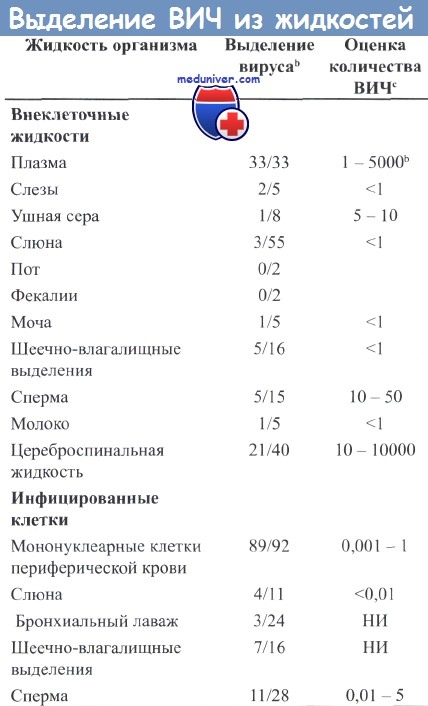
Согласно медицинской статистике, в мире около 38 млн. человек живут с ВИЧ, а приблизительно 35 млн. уже умерли от СПИДа. В организме ВИЧ может присутствовать во всех жидкостях, в том числе в моче, поте, слюне и слезах. Но через мочу, пот, слезу и слюну он не передается, так как в них вирус не содержится в достаточном для заражения количестве.
Заразиться ВИЧ-инфекцией можно только через кровь, сперму, выделения из влагалища и грудное молоко. Существует только 3 пути заражения ВИЧ-инфекцией:

1. Половой. Частота заражений ВИЧ-инфекций половым путем наиболее высока, поэтому этот путь считается во всем мире основным. Даже один половой контакт без презерватива может привести к заражению. Передача ВИЧ может произойти как при вагинальном, так и при анальном и оральном половом контакте. Контакт через анус (прямую кишку) считается наиболее опасным и травматичным, так как слизистая прямой кишки обладает хорошей способностью всасывания и адсорбции. Риск заражения при анальном сексе в 3 раза выше по сравнению вероятностью инфицирования при вагинальном контакте.
При оральном контакте тоже происходит контакт со спермой и вагинальном секретом, поэтому вероятность заражения в этом случае также существует. В зависимости от способа полового контакта риск инфицирования резко возрастает при наличии микротравм слизистой и кожи половых органов, травматизации заднего прохода и прямой кишки, при наличии ран, язвочек и кровотечений на слизистой ротовой полости.
2. Парентеральный. Инфицирование в этом случае может произойти при переливании крови, при внутривенных инъекциях нестерильным инструментом, во время медицинских и косметологических процедур. Например, во время нанесения татуировки, пирсинга, маникюра, педикюра и даже бритья. Также возможно заражение ВИЧ через инфицированные органы и ткани, полученные от донора.
3. Вертикальный. При этом пути ВИЧ передается от зараженной матери к ребенку. Произойти это может в любой срок беременности, во время родов и кормления грудью, если у мамы имеются трещины на соске или передаваться с материнским молоком.
Риск заболеть ВИЧ резко возрастает с увеличением частоты незащищенных половых контактов и количества сексуальных партнеров. Во много раз увеличивается вероятность заражения, если заниматься сексом во время менструации или с половым партнером, у которого есть болезни передаваемые половым путем, особенно такие как генитальный герпес или сифилис.
Женщины заражаются ВИЧ-инфекцией в 4 раза чаще, чем мужчины. Связано это с тем, что объем и концентрация спермы, которая попадает во влагалище женщины при половом акте, значительно больше, чем у влагалищного секрета.
Самый высокий риск заражения ВИЧ-инфекцией у гомосексуалов, проституток и наркоманов. Связано это с тем, что ткани заднего прохода и прямой кишки не так эластичны, как у влагалища, поэтому в них легче образуются микротрещины и травмы. Заражению у гомосексуалистов способствует и то обстоятельство, что в слизистой прямой кишки много СД4 лимфоцитов, являющихся главной мишенью для ВИЧ.
Доказанный научно факт, что у проституток вероятность заражения ВИЧ выше в десятки раз. Чтобы определить точнее, ученые рекомендуют умножить количество половых партнеров на число партнеров каждого из них, так как если человек имеет несколько половых партнеров, то каждый из них может вступать еще в сексуальную связь с другими.
С 1996 года в России основным путем заражения ВИЧ стал не половой, а парентеральный путь. Причина этого распространение эпидемии среди наркоманов, которые используют для внутривенного введения наркотических веществ общие нестерильные шприцы, иглы и растворы.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
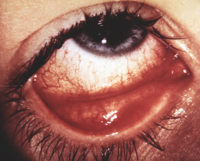
Глазные проявления ВИЧ – это специфические изменения органа зрения, вызванные присоединением оппортунистической инфекции у пациентов с ВИЧ-инфекцией в анамнезе. Клиническая картина определяется характером поражения. Общие симптомы для большинства форм – снижение остроты зрения, скотомы, фотопсии, нарушения цветовосприятия, фотофобия, повышенное слезотечение. Постановка диагноза базируется на применении ПЦР, ИФА, инструментальных методов диагностики (визометрия, офтальмоскопия, периметрия, тонометрия, биомикроскопия, УЗИ, КТ головы). Для лечения используется антиретровирусная и симптоматическая терапия.
Общие сведения
Глазные проявления встречаются у 70-80% больных ВИЧ-инфекцией. Примерно у 50% пациентов отмечается симметричное вовлечение в патологический процесс обоих глазных яблок. Распространенность цитомегаловирусной ретинопатии у людей, инфицированных вирусом иммунодефицита, составляет 30-40%. В 5% случаев наблюдается необратимое поражение зрительного нерва. У 30-35% лиц с данной патологией отмечается высокий риск необратимой потери зрения. У 30-50% внутриорбитальные проявления осложняются поражением нервной системы. Глазные проявления с одинаковой частотой встречаются среди лиц мужского и женского пола. Географических особенностей распространения не отмечается.

Причины глазных проявлений ВИЧ
Причина поражения глаз – инфицирование вирусом иммунодефицита человека, который относится к семейству ретровирусов, и присоединение оппортунистической инфекции. Источник распространения – больной человек. Вирус содержится в биологических средах организма (кровь, сперма, грудное молоко, влагалищные выделения, спинномозговая жидкость). Инфицирующая доза – 10 000 вирусных частиц. Пути передачи инфекции: половой, гематогенный и вертикальный (от матери к ребёнку). Глаза поражаются при попадании заражённой крови на открытые слизистые оболочки (конъюнктива) или проникновении вируса через гематоофтальмический барьер.
Патогенез
Вирус иммунодефицита удаётся идентифицировать в оболочках глаза и водянистой влаге, однако патологические изменения вызывает не собственно возбудитель, а ассоциации других микроорганизмов. Активация оппортунистической инфекции становится причиной рецидивирующих воспалительных процессов внутриглазной локализации. Инфицирование цитомегаловирусом ведёт к лизису клеток и развитию гранулоцитарной реакции. Из-за нарушения реологических свойств крови возникают ишемические проявления, обусловленные окклюзивным артериитом, перифлебитом. Придатки глаза (веки, слезные пути) наиболее часто поражаются вирусом опоясывающего герпеса, саркомой Капоши, реже – контагиозным моллюском.
Центральная форма токсоплазмоза приводит к очаговому некротизирующему хориоретиниту. Внелегочные проявления инфицирования пневмоцистой провоцируют поражение увеального тракта. При травматическом повреждении глаз наблюдается высокая вероятность возникновения аспергиллеза. Повышение уровня триглицеридов влечёт за собой увеличение синтеза цитокинов. Этот механизм лежит в основе развития липемии сетчатки. Усугубляет нарушение липидного обмена приём ингибиторов протеаз. Интенсивное поражение клеток, на поверхности которых расположены CD4-рецепторы, ведёт к прогрессированию патологических изменений.
Симптомы глазных проявлений ВИЧ
Неврологическая симптоматика представлена светобоязнью, двоением перед глазами, мелкоразмашистыми движениями глазных яблок при попытке фиксации взгляда. В ряде случаев возникает блефароспазм, вызванный параличом черепных нервов. При внутриутробном инфицировании плода существует высокий риск развития аномалий органа зрения (анофтальм, колобома роговицы). Саркома Капоши с локализацией на веках или орбитальной конъюнктиве длительное время характеризуется бессимптомным течением. Рост новообразования затрудняет процесс смыкания век, приводит к развитию местных воспалительных реакций в виде гиперемии и отека оболочек переднего сегмента глаз.
Осложнения
Кровоизлияние в стекловидное тело может достигать степени тотального гемофтальма. Реже возникает гипопион, гифема. Продолжительное течение аспергиллеза приводит к образованию бельма и множественных эрозивных дефектов на поверхности роговицы с риском ее перфорации. Высока вероятность бактериальных и инфекционных поражений переднего отдела глаз (конъюнктивит, кератит). Возможно развитие вторичного дакриоцистита. В редких случаях патологический процесс распространяется на кости черепа и ткани мозга. У 20% пациентов наблюдается отслойка сетчатки, обусловленная некрозом отдельных участков внутренней оболочки глаз. Осложнения со стороны нервной системы представлены криптококковым менингитом, лимфомой мозговых оболочек, нейросифилисом.
Диагностика
Для диагностики ВИЧ-инфекции проводится полимеразная цепная реакция (ПЦР), которая даёт возможность выявить фрагменты РНК или ДНК вируса. Иммуноферментный анализ (ИФА) позволяет обнаружить специфические антитела к вирусу. С целью оценки тяжести иммунодефицита изучают содержание CD4-лимфоцитов. В комплекс специфического офтальмологического обследования входит:
Лечение глазных проявлений ВИЧ
Этиотропная терапия ВИЧ-инфекции не разработана, однако применение антиретровирусных средств позволяет замедлить прогрессирование заболевания. Эффективность симптоматического лечения зрительных нарушений повышается при использовании противовирусных препаратов, угнетающих персистенцию вируса в организме. При развитии инфекционного кератита, ретинита или везикулобуллезного дерматита, вызванного опоясывающим герпесом, показано внутривенное введение ацикловира, фамцикловира. Сухой кератоконъюнктивит в сочетании с ксерофтальмией требует назначения препаратов искусственной слезы, увлажняющих мазей.
Лечение токсоплазмозного ретинохориоидита основывается на применении пириметамина, сульфаниламидов, клиндамицина. Острое течение иридоциклита у ВИЧ-инфицированных больных требует инстилляций глюкокортикостероидов в комбинации с короткими курсами антибактериальной терапии. При цитомегаловирусном ретините используют цидофовир, фоскарнет, ганцикловир. Тактика лечения пациентов с саркомой Капоши сводится к назначению химио- или криотерапии, оперативного иссечения новообразования, внутриопухолевого введения цитостатиков. При аспергиллезном поражении структур глазного яблока показана антифунгальная терапия. Доказана целесообразность внутривенного использования амфотерицина В, итраконазола.
Прогноз и профилактика
Исход заболевания определяется вирусной нагрузкой, особенностями поражения глаз и течения основной патологии. По собранным в офтальмологии статистическим данным риск полной потери зрения составляет 40%. Неспецифические превентивные меры сводятся к предупреждению инфицирования вирусом иммунодефицита (использование средств контрацепции, стерилизация медицинского инструментария, борьба с инъекционной наркоманией). Пациентам рекомендовано отдавать предпочтение очковой коррекции остроты зрения перед контактными линзами. Специфические методы профилактики не разработаны, однако применение антиретровирусной терапии значительно улучшает прогноз.
Среди большого числа проявлений ВИЧ-инфекции поражения кожи занимают особое место. Поражения кожи могут иметь важное диагностическое значение как для острой стадии болезни, так и для определения стадий вторичных заболеваний.
Among a large number of manifestations of HIV infection lesions occupy a special place. Skin lesions may have important diagnostic value for the diagnosis of acute stage of the disease, and to identify the stages of secondary diseases.
Заболеваемость ВИЧ-инфекцией (ВИЧ — вирус иммунодефицита человека) сохраняет тенденцию к неуклонному росту. Существенно увеличилось число больных с поздними стадиями ВИЧ-инфекции и наличием различных оппортунистических заболеваний, в частности поражений кожного покрова. Диагностика этих изменений нередко представляет большие трудности на догоспитальном уровне для врачей общего профиля, а также дерматологов и инфекционистов [1, 2].
Среди множества специфических проявлений ВИЧ-инфекции и оппортунистических заболеваний поражения кожи занимают особое место, т. к. уже с момента манифестации заболевания являются наиболее частым и ранним ее проявлением [1–3]. Вовлечение кожи в патологический процесс обусловлено как иммунодефицитом в целом, так и тем обстоятельством, что ВИЧ поражает не только Т-лимфоциты-хелперы, но и клетки Лангерганса, играющие важную роль в дермальных иммунных реакциях и, возможно, являющиеся местом первичной репликации ВИЧ в коже.
В 2011–2014 гг. в ИКБ № 2, куда госпитализируется более 80% ВИЧ-инфицированных больных в г. Москве, нами наблюдались 586 пациентов с различными кожными проявлениями, что составило 69% от общего числа госпитализированных (в 4-й стадии ВИЧ-инфекции — 88%). Их можно подразделить на 3 группы: кожные проявления при манифестации ВИЧ-инфекции, заболевания в стадии вторичных проявлений (4-я стадия) и поражения кожи, не связанные с ВИЧ-инфекцией. Поражения кожи могут иметь важное диагностическое значение. Часто на ранних стадиях развития болезни (уже через 3–4 недели после заражения) на коже больного может появиться острая экзантема (3-е место после мононуклеозоподобного синдрома и лимфаденопатии), состоящая из отдельных эритематозных пятен и папул [1, 4]. Пятнисто-папулезная сыпь — своеобразное поражение кожи у ВИЧ-инфицированных, которое до сих пор не получило определенного нозологического статуса. Сыпь имеет распространенный характер, обычно сопровождается легким зудом. Она локализуется в основном на верхней половине туловища, шее и лице; дистальные отделы конечностей поражаются редко. Папулезную сыпь рассматривают как проявление морфологической реакции кожи на инфицирование ВИЧ. Изменения на коже сопровождаются лихорадкой, изменениями на слизистых ротоглотки (чаще кандидоз полости рта). После стихания острой фазы (2–2,5 недели) пятна и папулы подвергаются спонтанному регрессу. Экзантема при острой ВИЧ-инфекции не отличается морфологической спецификой, поэтому в стационар больные чаще всего направляются с диагнозами: острая респираторная вирусная инфекция, токсикоаллергическая реакция, корь, краснуха. Надо отметить, что состояние иммунного статуса у этой категории больных не имеет существенных отклонений от нормы, а исследование крови на ВИЧ методом иммуноферментного анализа имеет сомнительные или отрицательные результаты, т. к. специфические антитела еще отсутствуют. В ранние сроки диагноз ВИЧ-инфекции может быть подтвержден только методом полимеразной цепной реакции. Серологические реакции на ВИЧ у этих больных становятся положительными позже, чаще через 6–12 недель от начала острой фазы болезни.
Экзантема, наблюдаемая в периоде сероконверсии, обусловлена самим вирусом иммунодефицита, все другие изменения кожи связаны с оппортунистическими заболеваниями, развивающимися на фоне иммунодефицита при снижении СД4+ менее 300 клеток. Этиологически можно выделить 3 основные группы кожных проявлений у больных ВИЧ/СПИД: неопластические, инфекционные (вирусные, грибковые, бактериальные, паразитарные) и дерматозы неясной этиологии. Первые две группы относятся к ВИЧ-индикаторным заболеваниям, так как все виды опухолей у больных ВИЧ/СПИД имеют вирусную этиологию и их формирование обусловлено тяжелым иммунодефицитом. Дерматозы неясной этиологии, возможно, обусловлены лекарственно-аутоиммунными поражениями, особенно при длительной антиретровирусной терапии (АРВТ) (в частности — Эпивиром) или специфической терапии оппортунистических заболеваний, не исключено и непосредственное воздействие ВИЧ на кожу. Самыми распространенными у больных СПИДом являются грибковые поражения кожи и слизистых. Наиболее часто наблюдаются кандидоз, руброфития, разноцветный лишай (81%) [5, 6]. Другие микозы встречаются значительно реже. Особенностями грибковых заболеваний при ВИЧ-инфекции являются: поражение лиц молодого возраста, особенно мужчин; быстрая генерализация с формированием обширных очагов, расположенных по всему кожному покрову; упорное течение; резистентность к проводимой терапии. Характерно сочетание поражения кожи и слизистых оболочек (полость рта, гениталии). Второе место среди поражений кожи занимает себорейный дерматит (68%). Как правило, у этих больных он протекает остро и тяжело. Вначале процесс локализуется только на лице (брови, усы, область рта), волосистой части головы и на разгибателях верхних конечностей. При развитии процесса на волосистой части головы можно обнаружить довольно сильное шелушение, напоминающее перхоть. Иногда при ВИЧ процесс может распространиться по всему кожному покрову в виде зудящих экзематозных бляшек. Такое распространение дерматита говорит о резко пониженном иммунитете и является плохим прогностическим признаком. Третье место по частоте занимают герпетические инфекции, в частности вирусы простого герпеса 1-го и 2-го типов и varicella zoster (28%) [7, 8]. Герпетические высыпания могут появиться на любом участке кожи и слизистых оболочек, но чаще они возникают на губах, половых органах или в перианальной области. Высыпания часто трансформируются в крупные, болезненные, долго не заживающие язвы. Нередко клинические проявления герпеса напоминают ветряную оспу или импетиго. Помимо поражения кожи и слизистых оболочек, при ВИЧ-инфекции у больных часто развивается герпетический проктит, который проявляется в виде болезненной отечной эритемы в перианальной области. Опоясывающий лишай при условии возникновения его у лиц молодого возраста из группы риска, отсутствии провоцирующих заболеваний и иммуносупрессивной терапии служит индикатором ВИЧ-инфекции. Пузырьковые высыпания сопровождаются сильными болями, оставляют рубцы, рецидивируют, что не наблюдается у лиц без иммунного дефицита. Наиболее характерным дерматологическим неопластическим проявлением ВИЧ-инфекции остается саркома Капоши, вызванная вирусом простого герпеса 6-го типа [9, 10]. Надо отметить, что ее частота снизилась с 40% у мужчин со СПИДом в 1980–90 гг. до 9% начиная с 2000 г. Основными клиническими особенностями саркомы Капоши является то, что у большинства больных заболевание развивается в возрасте до 35 лет; очаги поражения на коже носят распространенный характер; склонность к быстрой генерализации процесса (в первую очередь поражаются легкие, желудочно-кишечный тракт, лимфоузлы и слизистая оболочка полости рта); высокая смертность в течение короткого времени без лечения. Появление на коже различных пятен синюшного или розового цвета, бляшек или папул у лиц молодого возраста обязательно должно насторожить лечащего врача в отношении ВИЧ-инфекции и требует обязательного проведения гистологического исследования биоптата кожи для исключения саркомы Капоши. В поздних стадиях болезни кожные элементы (розеолы, папулы, пятна) становятся многочисленными, инфильтрируются, могут изъязвляться. Обильные кожные проявления практически всегда сопровождаются выраженным лимфостазом, поражением суставов, с развитием контрактур. Примером прямой зависимости поражения кожи от ВИЧ-инфекции может служить папилломавирусная инфекция кожи и слизистых оболочек (10%) [11, 12]. У ВИЧ-инфицированных больных изменения на коже имеют необычный вид, поражают нетипичные места, многочисленные, имеют участки распада в центре папул, сливаются и после хирургического удаления практически всегда рецидивируют. Эти элементы появляются преимущественно на лице, а также в области гениталий и могут быть крупными (гигантский моллюск), напоминать рак кожи, остроконечные кондиломы, обычные вульгарные бородавки и кератоакантомы.
У трети ВИЧ-инфицированных в течение нескольких недель от начала лечения различных оппортунистических инфекций этиотропными препаратами, а также АРВТ появлялась распространенная зудящая сыпь в виде эритематозных пятен и папул, что расценивалось как медикаментозная токсикоаллергическая реакция. Нами наблюдались и более тяжелые медикаментозные реакции, в частности синдром Стивенса–Джонсона и токсический эпидермальный некролиз.
Учитывая все вышеизложенное, больным ВИЧ-инфекцией с поражениями кожи и слизистых оболочек необходимо постоянное наблюдение врача-дерматолога. Для достижения положительного эффекта от проводимого лечения необходимы более продолжительные курсы терапии кожных заболеваний и максимальные дозы используемых препаратов, а после излечения — прием показанных препаратов профилактически. Помимо терапии кожных заболеваний больным ВИЧ-инфекцией показано назначение АРВТ. Диагностика кожных проявлений имеет важное практическое значение, так как способствует более раннему установлению диагноза ВИЧ-инфекции, своевременному назначению АРВТ, улучшению качества и продолжительности жизни пациента.
Литература
М. В. Нагибина* , 1 , кандидат медицинских наук
Н. Н. Мартынова**, кандидат медицинских наук
О. А. Преснякова**
Е. Т. Вдовина**
Б. М. Груздев***, кандидат медицинских наук
* ГБОУ ВПО МГМСУ им. А. И. Евдокимова МЗ РФ, Москва
** ГБУЗ ИКБ № 2, Москва
*** МГЦ СПИД, Москва
Oдним из первых препаратов, использованных для лечения ВИЧ-инфекции, был азидотимидин (АЗТ). У нас он выпускался под названием тимозид, на Западе известен как ретровир, зидовудин (ЗДВ). Суточная доза определяется стадией инфекции и переносимостью препара
Oдним из первых препаратов, использованных для лечения ВИЧ-инфекции, был азидотимидин (АЗТ). У нас он выпускался под названием тимозид, на Западе известен как ретровир, зидовудин (ЗДВ). Суточная доза определяется стадией инфекции и переносимостью препарата. Препарат относится к ингибиторам обратной траскриптазы.
Препаратами второго поколения являются дидеоксииназин (ДДИ), дидеоксицитидин (ДДС). В настоящее время спектр препаратов этой группы значительно расширился (ставудин-ДДТ, хивид, фосфозид и другие).
Эта группа лекарственных средств (ЛС) имеет ряд существенных недостатков. Указанные ЛС не подавляют полностью репликацию вируса, который может быть выделен у большинства больных во время терапии.
Как показали исследования, к ЗДВ достаточно быстро развивается устойчивость, в особенности на поздних стадиях болезни с усиленной репликацией ВИЧ, когда, по-видимому, возникает резистентность и к другим аналогам нуклеозидов.
Обычный фактор, существенно ограничивающий применение ЛС этой группы, — их токсичность. Для ЗДВ характерно главным образом токсическое действие на костный мозг, тогда как ДДИ и ДДС обладают нейротоксическим действием. Кроме того, ДДИ может вызывать тяжелый острый геморрагический панкреатит.
Установлена тесная связь между клинической неэффективностью ЗДВ и резистентностью к нему in vitro.
Вторая группа препаратов, открытая сравнительно недавно и уже широко используемая, — это ингибиторы протеаз: индиновир (криксиван), инвираза (саквиновир), вирасепт (нельфиновир) и другие.
В настоящее время речь не идет уже о монотерапии антиретровирусными средствами, а только о ди-, три- и даже тетратерапии. Такие методики позволяют снижать концентрацию вируса до величин, не определяемых с помощью современных тест-систем (< 200 копий/1 мл).
Предпочтительность комбинированной терапии обосновывается следующими положениями (В. В. Покровский).
- Использование многих этиотропных агентов более эффективно подавляет жизнедеятельность вируса, воздействуя на различные болевые точки или синергически воздействуя на одну из них.
- Это позволяет снизить дозы препаратов, что уменьшает частоту и выраженность побочных эффектов.
- Различные лекарства имеют различную способность проникать в ткани (головной мозг и т. д.).
- Комбинация лекарств затрудняет формирование устойчивости, или она появляется позднее.
Все описанные выше подходы к терапии ВИЧ-инфекции предполагали непосредственное воздействие на репликацию вируса. Другая возможная методика лечения ВИЧ-инфекции состоит в усилении защитных сил макроорганизма. Некоторые варианты такого подхода в большинстве случаев неспецифические, изредка специфические и могут воздействовать на защитные свойства клетки-хозяина.
Интерфероны, как природные, так и рекомбинантные, имеют ряд недостатков: антигенность, необходимость многократного введения для поддержания достаточной концентрации в организме, большое количество побочных эффектов и т. д.
Этих недостатков лишены многие индукторы эндогенного интерферона, некоторые из них способны включаться в синтез ИФН в некоторых популяциях клеток, что в ряде случаев имеет определенное преимущество перед поликлональной стимуляцией иммуноцитов интерфероном.
Специфическая активность циклоферона при ВИЧ-инфекции изучена в 1997 году в Институте гриппа РАМН
- Выявлена выраженная ингибирующая активность циклоферона на репродукцию ВИЧ в культуре клеток моноцитов.
- По показателям ингибирующей активности циклоферон значительно превосходит азидотимидин.
- Представленные экспериментальные данные обосновывают клиническое использование циклоферона для лечения больных ВИЧ-инфекцией.
Пятилетний опыт применения циклоферона у ВИЧ-инфицированных позволяет оценить результаты этой работы.
В период 1992 – 1997 годы в Санкт-петербургском городском центре по профилактике и борьбе со СПИД циклоферон получили 40 пациентов с разными стадиями ВИЧ-инфекции. Следует отметить, что 11 больных прошли два курса терапии циклофероном, в связи с чем общее число лиц, получивших один курс лечения циклофероном, составило 29 человек. В основном это были молодые люди в возрасте до 40 лет (20 человек), в том числе трое детей до 14 лет.
Все больные отмечали хорошую переносимость циклоферона, отсутствие пирогенных реакций после его введения.
Пациенты также констатировали улучшение общего состояния, сна и аппетита, повышение жизненного тонуса, работоспособности. 30% из числа получавших препарат и перенесших в осенне-зимний период грипп или ОРВИ отметили, что заболевание протекало непривычно легко и выздоровление наступило быстрее обычного.
Из клинической практики
После курса циклоферона отмечалось существенное снижение вирусной нагрузки (в 3,6 раза). Число CD4+ возросло на 62%. Монотерапия циклофероном оказала положительное стабильное влияние на изученные показатели у пациентов.
Определенный интерес представляют результаты многолетнего наблюдения больных ВИЧ-инфекцией, которые получали длительно циклоферон в своеобразном профилактическом режиме с целью стабилизации процесса и профилактики прогрессирования заболеваний.
В 1998 году на базе Российского научно-методического Центра по профилактике и борьбе со СПИД (руководитель член-корр. АМН В. В. Покровский) была изучена динамика суррогатных маркеров ВИЧ-инфекций (уровень CD4+) и вирусная нагрузка у больных ВИЧ-инфекцией при лечении циклофероном.
Оценка достоверности полученных результатов проводилась с помощью непараметрических критериев (критерий знаков, максимум-критерий, критерий Вилкоксона для сопряженных совокупностей).
В испытуемую группу вошли 10 взрослых больных ВИЧ-инфекцией в стадии первичных проявлений по Российской классификации ВИЧ-инфекции (В. И. Покровский, 1989 г.). Результаты исследования уровня CD4-лимфоцитов представлены в таблице и на рисунке, из которых видно, что после первых четырех недель исследования наметилась тенденция к повышению среднего уровня CD4-лимфоцитов, которое к 12-й неделе стало статистически достоверным. Это повышение сохранилось до конца исследования, несмотря на
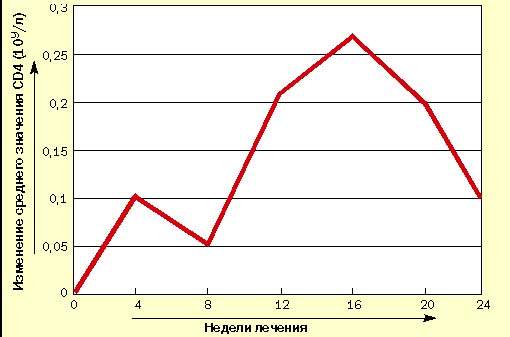 |
| Рисунок 1. Изменение уровня CD4-лимфоцитов у больных ВИЧ-инфекцией при лечении циклофероном (в сравнении с исходным уровнем) |
 |
| Рисунок 2. Средние значения изменения концентрации РНК ВИЧ (log10/мл) |
Таким образом, применение циклоферона в терапии ВИЧ-инфекций сопровождается стабилизацией клинических проявлений заболевания, улучшением состояния, а также гематологических и иммунологических показателей больных.
Циклоферон как монопрепарат оказывает иммуномодулирующее и противовирусное действие при лечении ВИЧ-инфицированных (стадии А1 3Б) в тех случаях, когда нет значительного снижения числа CD4+ клеток (<200). Хорошо зарекомендовало себя назначение циклоферона по следующей схеме.
- По 4 мл препарата в 1, 2, 4, 6, 8, 10, 13, 16, 19 и 22-й дни лечения (у детей по 2 мл). Первые две инъекции могут вводиться внутривенно, остальные внутримышечно. Повторные курсы циклоферона рекомендуется проводить через 6 месяцев под иммунологическим контролем.
- Циклоферон хорошо сочетается со всеми основными лекарственными средствами, его рекомендуется использовать в случае, когда имеются признаки активной репликации ВИЧ (высокие показатели вирусной нагрузки), у больных с обострениями различных оппортунистических заболеваний.
Исчезновение у некоторых больных иммунологических и вирусологических показаний для проведения противоретровирусной терапии может иметь важное значение для разработки новых подходов к проведению лечения больных ВИЧ-инфекцией, для снижения стоимости терапии и отсрочки развития резистентности к ней или преодолению последней.
Циклоферон может оказаться перспективным профилактическим средством при сомнительных контактах и контактах с заведомо ВИЧ-инфицированными партнерами.
Читайте также:

