Как проявляется почечная интоксикация
Обновлено: 23.04.2024
Алкогольная нефропатия – это хроническое поражение почек воспалительного характера, в основе которого лежат аутоиммунные механизмы, индуцированные воздействием на организм этилового спирта и его метаболитов. Выраженность симптомов зависит от типа патологии, преобладает бессимптомное течение до момента развития признаков хронической почечной недостаточности, при некоторых формах наблюдается прогрессирующая гематурия и гипертензия. Диагностика алкогольной нефропатии производится на основании данных физикального осмотра, лабораторных и функциональных исследований. Лечение включает в себя запрет на прием алкогольных напитков и симптоматическую терапию.
МКБ-10
Общие сведения

Причины
Существует несколько основных теорий развития алкогольной нефропатии, достоверных и однозначных данных в пользу какой-либо из них пока нет. Причины отсутствия консенсуса заключаются в разнообразных клинических и морфологических проявлениях алкогольной нефропатии, что дает основание предполагать наличие нескольких механизмов поражения мочевыделительной системы. Диапазон мнений относительно характера заболевания довольно широкий – от утверждений, что нефропатия является частью алкогольной болезни до предложений разделить АН на несколько сходных по течению патологий с различной этиологией. Наиболее признанными теориями развития данного состояния в современной урологии считаются следующие:
- Иммунологические причины. Существует ряд иммунологических механизмов повреждения тканей почек, которые могут быть связаны с алкогольной интоксикацией. В первую очередь это сенсибилизация к антигенам алкогольного гиалина с выделением иммуноглобулинов А, способных повреждать мембраны нефронов. Похожий механизм – прямое цитотоксическое воздействие этанола и продуктов его метаболизма посредством стимуляции выделения цитокинов.
- Инфекционные причины. Некоторые исследователи полагают, что алкоголь снижает уровень защиты организма от инфекций, включая вирус гепатита С и некоторые бактерии (кишечную палочку). В результате этого наряду с прямым воздействием инфекционных агентов на различные органы-мишени возникает косвенное поражение почек.
- Системные причины. Этанол является системным ядом, при продолжительном употреблении провоцирует повышение артериального давления, поражение печени, ЖКТ, поджелудочной железы, метаболические нарушения (аномалии пуринового обмена). Существует мнение, что эти факторы играют определяющую роль в патогенезе алкогольной нефропатии.
Современные исследователи склоняются к мнению, что развитие АХГН имеет многофакторную природу, в патогенезе большей или меньшей степени участвуют все вышеперечисленные процессы. Неизвестна роль генетической предрасположенности, хотя наличие широкого спектра индивидуальных особенностей заболевания указывает на ее наличие. Факторами риска могут выступать ранее перенесенные патологии почек, сахарный диабет, артериальная гипертензия, однако в подобных случаях дифференцировать алкогольный гломерулонефрит от форм вторичной нефропатии иного типа крайне сложно.
Патогенез
Механизм развития алкогольной нефропатии очень сложен из-за многочисленности патогенетических факторов, влияние каждого из которых сильно различается у разных больных. Именно это дает некоторым исследователям основание полагать, что АХГН – лишь составная часть симптомокомплекса алкогольной болезни. Практически у всех пациентов обнаруживаются антитела IgA против компонентов нефрона, что говорит об аутоиммунном механизме патогенеза. При приеме больших доз этанола последний может прямо стимулировать выделение цитокинов в почках, что приводит к разрушению нефронов.
При систематическом употреблении спиртного метаболиты этанола вызывают повреждение печени, нервной системы, поджелудочной железы, сосудов микроциркуляторного русла. Это косвенно усиливает поражение органов мочевыделительной системы. Увеличение АД, типичное для хронического алкоголизма, само по себе способно привести к вторичной нефропатии. Метаболические сбои, в особенности обмен пуринов, повышают нагрузку на органы выделения и также ведут к нарушению их функций вплоть до хронической недостаточности. Выраженность и скорость развития проявлений АХГН зависит от объемов потребляемого алкоголя – критичной дозировкой считается цифра свыше 35 мл в сутки.
Классификация
Выделяют несколько форм алкогольной нефропатии, разница между ними заключается в клиническом течении, наличии или отсутствии сопутствующих заболеваний. Некоторые типы состояния довольно легко спутать с другими видами вторичной нефропатии из-за схожих проявлений и механизмов патогенеза. Отличительной особенностью АХГН является то обстоятельство, что первопричиной всех патологических изменений в организме, прямо или косвенно ухудшающих работу почек, является злоупотребление алкоголем. Общепризнано существование следующих типов заболевания:
- Латентная форма. Является наиболее распространенной и трудно поддающейся диагностике из-за практически полного отсутствия субъективных симптомов. Возникает не только у людей, постоянно употребляющих спиртные напитки, но и у тех, кто делает это с определенной периодичностью (1-2 раза в неделю). Характерны обострения вскоре после последнего приема алкоголя, проявляющиеся уменьшением функциональной активности почек, что подтверждается лабораторными исследованиями. В патогенезе преобладает роль прямого нефротоксического воздействия этанола.
- Гипертензивная форма. Более редкий тип патологии, в основном возникающий у лиц, страдающих алкоголизмом, ожирением и артериальной гипертензией. Последнее обстоятельство обуславливает трудности различения АХГН этого типа и вторичной гипертензивной нефропатии. Повреждение нефронов происходит при развитии гемодинамических и метаболических нарушений, канальцевого ацидоза.
- Нефротическая форма. Крайне редкая и наиболее тяжелая форма хронической алкогольной нефропатии. Сопровождается прогрессирующим диффузным гломерулонефритом, достаточно быстро приводящим к ХПН. Основное звено патогенеза – резкая сенсибилизация организма и аутоиммунное поражение тканей иммуноглобулинами А.
Некоторые авторы причисляют к алкогольной нефропатии острые состояния, например, острую почечную недостаточность при отравлении спиртными напитками. Несмотря на то, что при этом наиболее ярко проявляется прямая нефротоксическая активность этанола, ОПН при алкогольной интоксикации различается по своему механизму развития от других повреждений почек на фоне АХГН. Поэтому большинство специалистов не рассматривают такое состояние как классическую нефропатию.
Симптомы алкогольной нефропатии
В большинстве случаев болезнь протекает практически бессимптомно, проявления патологии регистрируются случайно при выполнении лабораторных исследований по иному поводу. Это особенно характерно для латентной формы – нередко бессимптомное течение может длиться на протяжении многих лет. Обострения, возникающие на 1-3 сутки после употребления этанола, могут проявляться только жалобами на снижение объема мочи (олигурией) и крайне редко – слабыми тянущими болями в пояснице. При длительном течении на первый план выступают проявления алкогольной болезни: эритема ладоней, гинекомастия у мужчин, симптомы поражения поджелудочной железы и печени (боли в подреберье и животе, желтуха).
Гипертензивный вариант алкогольной нефропатии на начальных этапах развития также характеризуется слабой выраженностью собственно нефрогенных симптомов. Пациент жалуется на головные боли, приливы крови к лицу, неприятные ощущения в области сердца и другие следствия повышенного давления крови. Нередко этот тип заболевания сопровождается ожирением. Для нефротической формы АХГН типично достаточно быстрое течение – обычно после эксцесса возникает олигурия, видимая гематурия, ухудшение общего состояния. Обязательно присутствуют экстраренальные проявления хронической интоксикации этанолом.
При отсутствии лечебных мер и продолжающемся поступлении этилового спирта в организм алкогольная нефропатия неизменно сводится к возникновению ХПН. Ее признаками являются усталость, разбитое состояние, головная боль, усиливающиеся после приема этилового спирта. Затем появляется аммиачный запах изо рта, сильная жажда, рвота, сухость кожи, воспаление слизистых оболочек. Количество выделяемой мочи резко снижается, на поверхности кожных покровов образуется беловатый налет из выделяемой потовыми железами мочевины.
Осложнения
Не всегда удается строго дифференцировать осложнения собственно алкогольной нефропатии и интоксикации этиловым спиртом. При АХГН намного легче возникает алкогольное отравление, сопровождающееся острой почечной недостаточностью с анурией, головной болью, рвотой, отеками и другими признаками уремии. Учитывая прогрессирующий характер состояния, к острому отравлению могут привести ранее привычные дозировки алкоголя, что повышает риск развития осложнения. Грозным и неблагоприятным осложнением может выступать уремическая кома, обусловленная интоксикацией не выведенными через почки продуктами обмена веществ.
Диагностика
Для диагностики алкогольной нефропатии используют методы физикального осмотра, ряд лабораторных анализов и инструментальных исследований. Необходима консультация врача-нефролога, иногда к определению состояния могут подключать нарколога. Обычно алгоритм диагностики АХГН включает следующие этапы:
В редких и спорных случаях производят биопсию печени и почек для гистологического изучения данных органов. При алкогольной нефропатии в печени будут определяться признаки гиалиново-капельной дистрофии, в почках – мезангиопролиферативного нефрита диффузного или очагового характера. Рентгеноконтрастные методы исследования (например, урографию) назначают с осторожностью из-за нефротоксичности большинства контрастных препаратов. Дифференциальный диагноз осуществляют с иными типами первичных и вторичных нефропатий, определяющим фактором часто становится факт наличия длительного злоупотребления алкоголем.
Лечение алкогольной нефропатии
Главным и основополагающим назначением является полный запрет употребления алкогольных напитков. Только при отказе от спиртного более чем у половины больных латентной формой алкогольной нефропатии наблюдается стойкое улучшение лабораторных показателей мочи и почти полная ремиссия. Несоблюдение этого предписания даже при выполнении других рекомендаций и терапевтических мер лишь несколько замедляет прогрессирование состояния. При запущенных случаях АХГН и наличии сопутствующих патологий помимо отказа от спиртных напитков назначают ряд вспомогательных терапевтических мер:
- Антигипертензивная терапия. Снижение артериального давления благотворно влияет на прогноз по причине устранения гемодинамических нарушений в почках. Особенно важен этот компонент лечения при гипертензивных формах нефропатии. При нарушениях работы выделительной системы для снижения давления используют ингибиторы АПФ, блокаторы кальциевых каналов и рецепторов к ангиотензину 2.
- Нормализация метаболизма. Последствием алкогольной интоксикации часто становятся нарушения обмена веществ: пуринов, углеводов, жиров. Посредством специальных диет нужно нормализовать метаболизм и снизить нагрузку на выделительную систему. Особенно пагубно на почки действует нарушение выделения пуринов, поэтому при недостаточной эффективности диетического питания могут назначаться антиподагрические препараты (аллопуринол).
- Противовоспалительные средства. При быстром прогрессировании состояния (нефротическая форма) используют кортикостероидные и цитостатические препараты. Цель их применения – снизить активность воспалительных процессов для уменьшения степени повреждения почек. На сегодняшний день их эффективность критикуется рядом исследователей.
При диагностировании ХПН рекомендуется проведение гемодиализа, частота которого зависит от степени поражения выделительной системы. Вспомогательную роль в лечении алкогольной нефропатии может играть врач-нарколог – с его помощью больному легче избавится от зависимости. Использование фармакологических средств в борьбе с алкоголизмом следует производить с учетом пониженной скорости клубочковой фильтрации.
Прогноз и профилактика
В случае строгого соблюдения запрета на прием алкоголя и раннего выявления патологического состояния прогноз алкогольной нефропатии практически всегда благоприятный – функции выделительной системы восстанавливаются почти в полном объеме. При наличии сопутствующих нарушений, вызванных злоупотреблением спиртосодержащей продукцией, исход патологии зависит от их качественного лечения. При ХПН восстановление нормальной работы почек почти всегда невозможно, но поддерживающее лечение способно сохранить приемлемое качество жизни больного еще на многие годы. Самым неблагоприятным прогнозом обладает сочетание АХГН и тяжелых проявлений алкогольной болезни: цирроза печени, алкогольного панкреатита, кардиомиопатии. Но и в этом случае длительное комплексное лечение может значительно улучшить состояние больного.
1. Морфологические аспекты нефротоксического действия крепких алкогольных напитков/ Бабаханян Р.В., Сафрай А.Е., Шевчук М.К., Ягмуров О.Д.// нефрология.- 1998.
2. Морфофункциональные изменения в мочеполовой системе женщин при алкогольной интоксикации/ Шелудько В.В.// Астраханский медицинский журнал. - 2013.
3. Морфология острых экзогенных нефротоксических воздействий/ Ягмуров О.Д., Петров Л.В.// Нефрология. - 2011.
Токсическая нефропатия — это повреждение гломерулярного аппарата и почечных канальцев, вызванное действием экзо- и эндотоксинов, гемодинамическими и метаболическими нарушениями при отравлениях. Проявляется болями в пояснице, астеническим синдромом, отечностью, олигоанурией, которая впоследствии сменяется полиурией, полиорганными нарушениями. Диагностируется при помощи общего, биохимического анализов крови и мочи, проб Реберга, Зимницкого, УЗИ и томографии почек, УЗДГ почечных сосудов, химико-токсикологических исследований. Лечение включает проведение дезинтоксикационной терапии, инфузионной коррекции нарушений метаболизма, ЗПТ.
МКБ-10
Общие сведения
Токсическая нефропатия — собирательное понятие, объединяющее ряд нефрологических заболеваний со сходным этиопатогенезом и клинической картиной. Распространенность патологии достигает 0,04%, что составляет до 20% всех регистрируемых случаев ОПН. Рост заболеваемости связан со все более широким применением химических веществ на различных производствах и в быту: по наблюдениям, ежегодно до 10 млн. человек постоянно контактирует с нефротоксичными химикатами. Кроме того, обратной стороной успехов фармацевтической отрасли стало появление новых лекарственных средств, оказывающих влияние на почки. Актуальность своевременного выявления токсической формы нефропатий обусловлена высоким уровнем смертности и тяжелыми исходами при необратимой деструкции ткани почек.

Причины
Поражение почечной паренхимы обусловлено воздействием химических веществ, оказывающих прямой или опосредованный нефротоксический эффект. В большинстве случаев ренальную дисфункцию, а в тяжелых случаях и деструкцию тканей, вызывают экзогенные производственные и бытовые яды, хотя у некоторых пациентов заболевание вызвано эндогенной интоксикацией. Специалисты в сфере урологии и нефрологии выделяют следующих группы причин, которые приводят к развитию нефропатии:
- Прием веществ с нефротоксическим эффектом. При попадании в почки ядов этой группы возникают острая гломерулопатия или тубулярный некроз, вызванный реабсорбцией большого количества токсических веществ. Непосредственным повреждающим эффектом на почечную ткань обладают соли тяжелых металлов (кадмия, свинца, ртути, золота, мышьяка, йода, висмута, хрома и др.), этиленгликоль, щавелевая и борная кислоты, бензин, фенол, толуол, орелланиновые грибные токсины, яды некоторых животных.
- Опосредованное токсическое повреждение почек. Отравления веществами с гемолитическим эффектом (уксусной кислотой, мышьяковистым водородом, медным купоросом, змеиным ядом и др.) осложняются закупоркой нефронов гемоглобином. Аналогичное повреждение вызывают массивное размозжение тканей и синдром длительного сдавления, при которых наблюдается миоглобинурия. При токсическом поражении печени ренальная паренхима вторично повреждается ксенобиотиками и эндогенными токсинами.
- Общие клинические проявления отравления. Ряд химических веществ не оказывают прямого нефротоксического эффекта, однако системные проявления, возникающие при их приеме, приводят к тяжелой ренальной дисфункции. Чаще всего токсические формы нефропатии развиваются на фоне отравлений с клиникой шока, некомпенсированного ацидоза, выраженных метаболических расстройств. Такая же ситуация возникает под влиянием эндо- и экзотоксинов патогенной и условно-патогенной микрофлоры.
Постоянное расширение ассортимента медикаментозных препаратов, в первую очередь антибактериальных и противоопухолевых средств, привело к увеличению количества случаев токсической лекарственной нефропатии. По результатам исследований, более чем у 30% пациентов неолигурическая почечная недостаточность связана с приемом фармацевтических препаратов.
Нефротоксичные медикаменты могут прямо повреждать почечные канальцы (аминогликозиды, амфотерицины, иммуноглобулины, НПВС и др.), вызывать их закупорку (сульфаниламиды, циклоспорины, производные пуриновых нуклеозидов), системно нарушать ренальную гемодинамику (β-адреноблокаторы, некоторые диуретики) или оказывать сочетанное действие. Развитие токсической ятрогенной нефропатии также возможно при проведении лучевой терапии.
Патогенез
Механизм развития токсической нефропатии определяется причинами, спровоцировавшими почечную дисфункцию. Патогенез расстройств, вызванных нефротоксинами прямого действия, основан на нарушении биохимических процессов в нефронах, эпителиоцитах проксимальных и дистальных канальцев. После фильтрации клубочками токсическое вещество попадает в канальцевую систему, где вследствие реабсорбции воды его уровень возрастает почти в 100 раз. Возникающий градиент концентрации способствует поступлению и накоплению ксенобиотика в канальцевом эпителии до определенного критического уровня.
В зависимости от типа экзотоксина в эпителиоцитах происходят процессы деструкции клеточных и митохондриальных мембран, лизосом, компонентов цитоплазмы, гладкого эндоплазматического ретикулума, рибосом и т. п. с развитием в наиболее тяжелых случаях острого тубулярного некроза. Некоторые нефротоксины за счет инициации гипериммунных процессов разрушают гломерулярный аппарат коркового слоя. Осаждение в клубочковых структурах иммунных комплексов или образование в мембранах комплексных антигенов с последующей атакой антител провоцируют начало острого гломерулонефрита или интерстициального нефрита без повреждения канальцевых эпителиоцитов. Важным фактором прямой нефротоксичности является способность некоторых веществ стимулировать образование свободных радикалов.
Патогенез опосредованного повреждения почек при закупорке канальцев основан на развитии в их клетках некротических процессов, нарушении реабсорбционной способности. Внутриренальный застой мочи сопровождается ретроградным током гломерулярного фильтрата и последующим повреждением нефронов. При нефропатиях, возникших на фоне общих отравлений, основой патоморфологических изменений обычно становится ишемия клеток и нарушение биохимических процессов за счет кислотно-щелочного и водно-электролитного дисбаланса. На начальном этапе возникает дисфункция эпителиоцитов, которая впоследствии может осложниться токсической дегенерацией и некрозом канальцевого эпителия, деструкцией гломерулярных базальных мембран, интерстициальным отеком.
Классификация
Систематизация форм токсической нефропатии проводится с учетом особенностей этиопатогенеза заболевания и тяжести симптоматики. Такой подход позволяет выработать оптимальную тактику ведения пациента, а в ряде случаев предупредить развитие необратимой деструкции тканей. С учетом этиологического фактора и механизма повреждения почек различают следующие формы заболевания:
- Токсическая специфическая нефропатия. Развивается под влиянием экзогенных и эндогенных веществ с прямыми и опосредованным нефротоксическим эффектом. Отличается быстрым развитием тканевой деструкции, которая у части пациентов является необратимой. Чаще требует раннего начала заместительной почечной терапии.
- Токсическая неспецифическая нефропатия. Осложняет течение отравлений и заболеваний с выраженным интоксикационным синдромом, при которых ведущими становятся гемодинамические и метаболические расстройства. На начальных этапах нарушения носят функциональный характер и лишь позднее начинается разрушение тканей.
При легком течении нефропатия выявляется лабораторно: в клиническом анализе мочи определяется повышенное содержание белка, лейкоцитов, эритроцитов, появляются цилиндры. Средняя степень характеризуется уменьшением количества мочи и нарушением фильтрационной функции с увеличением уровня мочевины, креатинина, калия в сыворотке крови. Для тяжелого течения характерна клиника ОПН, вплоть до наступления уремической комы.
Симптомы токсической нефропатии
Возникают тошнота, рвота, понос. Кожные покровы и видимые слизистые становятся сухими, желтушными. Нарастание почечной недостаточности сопровождается практически полным прекращением мочевыделения, усилением отечности, ее нисходящим распространением на другие отделы тела, появлением петехиальной сыпи. При тяжелых поражениях развивается мозговая симптоматика — вялость, заторможенность, оглушенность, слуховые, зрительные, тактильные галлюцинации, судорожный синдром. Признаки выраженной ренальной дисфункции обычно сохраняются в течение 7-14 суток.
На следующем этапе развития заболевания, длящемся от 10-15 до 30 дней, олигоанурия сменяется постепенным усилением диуреза. Больной выделяет за сутки от 1,8 до 5-8 л и более мочи. Сохраняются слабость, утомляемость, мучительная жажда, уменьшается масса тела. Длительность периода реконвалесценции при интоксикационной нефропатии зависит от объема и характера поражения. Обычно для восстановления функциональной состоятельности органа требуется от 6 месяцев до 2 лет.
Осложнения
В 20-70% случаев токсическая нефропатия завершается летальным исходом из-за массивной необратимой деструкции ренальной паренхимы. Снижение фильтрационной функции у пациентов с ОПН приводит к гиперкалиемии с замедлением сердечного ритма, фибрилляцией и асистолией желудочков. Нарушение работы сердца в сочетании с гипопротеинемией повышает риск развития отека легких.
Длительная уремия сопровождается усиленным выделением азотистых метаболитов через кожу, серозные и слизистые оболочки с развитием уремического перикардита, плеврита, гастрита, энтероколита, ларинготрахеита, токсическим поражением печени, костного мозга. При нарушении секреции компонентов ренин-ангиотензиновой системы возможно развитие артериальной гипертензии. Отдаленными последствиями токсического поражения почек являются хронический тубулоинтерстициальный нефрит, хроническая почечная недостаточность, новообразования органов мочевыделительного тракта.
Диагностика
Постановка диагноза токсической нефропатии обычно не представляет сложности в тех случаях, когда заболевание возникло после отравления химическим веществом. Диагностический поиск направлен на оценку характера, объема возможного повреждения тканей, определение выраженности ренальной дисфункции. Пациентам с нефропатией рекомендованы следующие лабораторно-инструментальные методы исследований:
- Общий анализ мочи. Определяются протеинурия, лейкоцитурия, микрогематурия, цилиндрурия. Относительная плотность мочи в олигоанурической фазе превышает 1030 г/л, в полиурической составляет ниже 1003 г/л. Дополнительное проведение пробы Зимницкого при полиурии выявляет снижение концентрационной функции.
- Биохимический анализ крови. До восстановления объема диуреза повышаются сывороточные уровни креатинина, мочевой кислоты, азота мочевины, калия, кальция, неорганического фосфора. Нарушение фильтрационной способности гломерул также подтверждается результатами нефрологического комплекса и пробы Реберга.
- УЗИ почек. При эхографии нефропатия токсического типа проявляется увеличением размеров почечной паренхимы за счет интерстициального и лимфостатического отека. Участки некроза имеют вид гипоэхогенных полостей или гиперэхогенных включений. УЗДГ ренальных сосудов выявляет гемодинамические нарушения.
- Томография почек. Компьютерная томография почек позволяет получить послойное изображение ренальных тканей и обнаружить даже небольшие участки деструкции. В целях безопасности при токсических поражениях исследование рекомендуется проводить без контраста или заменить его МРТ, хотя в таком случае информативность несколько снижается.
Для подтверждения токсического характера нефрологической патологии по возможности проводятся химико-токсикологические исследования, позволяющие установить химическое вещество, которое вызвало расстройство. Контрастные методы исследований (экскреторная урография, ангиография почек) применяют с осторожностью в связи с риском усугубления клинической ситуации контраст-индуцированными деструктивными процессами. Для контроля за состоянием других органов и систем проводятся биохимические пробы печени, коагулограмма, ЭКГ. Изменения общего анализа крови неспецифичны: могут выявляться анемия, умеренный лейкоцитоз, повышение СОЭ, тромбоцитопения.
Нефропатию токсического происхождения дифференцируют со вторичными нефропатиями другого генеза (контраст-индуцированной, диабетической, дисметаболической и др.), острым гломерулонефритом, ишемическим некрозом почек, травматическими повреждениями почечной паренхимы, атероэмболической болезнью. По назначению уролога-нефролога пациента консультируют токсиколог, анестезиолог-реаниматолог, невролог, терапевт, кардиолог, пульмонолог, гепатолог.
Лечение токсической нефропатии
Больных, почки которых повреждены в результате отравления экзо- или эндотоксинами, госпитализируют в палату интенсивной терапии. Основными терапевтическими задачами являются скорейшая элиминация химического вещества, коррекция метаболических расстройств, предупреждение возможных осложнений. С учетом этапа заболевания пациентам показаны:
- Дезинтоксикационная терапия. Проводится в первые часы и сутки после отравления. Для ускоренного выведения токсина проводят промывание желудка, форсированный диурез с назначением осмотических мочегонных и салуретиков, используют адсорбенты, слабительные средства, специфические антидоты. В сложных случаях эффективны плазмаферез, гемосорбция, гемофильтрация, ультрафильтрация, гемодиализ, перитонеальный диализ. Некоторым пациентам назначают переливание крови и ее компонентов.
- Инфузионная коррекция метаболических нарушений. Начинается сразу после госпитализации и продолжается в олигоанурическом периоде ОПН. Для восстановления электролитного баланса и кислотно-щелочного равновесия применяют антагонисты калия (обычно — препараты кальция), инфузию глюкозы с инсулином, ощелачивающие полиионные растворы. Возможен дальнейший прием энтеросорбентов, связывающих токсические метаболиты. При значительной ренальной дисфункции оправдано проведение ЗПТ.
При утяжелении состояния больного проводится комплексная противошоковая терапия, купируются неотложные состояния (уремическая кома, отек легких, судорожный синдром, гипертонический криз). В полиурической фазе продолжается массивная (до 5-6 л/сут) инфузионная терапия для поддержания ОЦК и физиологической концентрации метаболитов. На этапе восстановления проводится общеукрепляющее лечение и определяется тактика дальнейшего ведения пациента с учетом степени сохранности почечных функций.
Прогноз и профилактика
Токсическая нефропатия — тяжелое, прогностически неблагоприятное расстройство с высокими показателями летальности. Своевременное установление токсина, правильная оценка морфологической сохранности и функциональной состоятельности почечной паренхимы, проведение адекватной интенсивной терапии повышают шансы благоприятного исхода нефропатии. Профилактика заболевания направлена на предупреждение попадания в организм токсических веществ: ограничение времени контакта с нефротоксичными ядами, использование средств индивидуальной защиты (респираторов, защитной одежды), отказ от употребления в пищу незнакомых грибов.
Работникам предприятий с вредными условиями производства рекомендовано прохождение профилактических медосмотров для раннего выявления почечной дисфункции. Для снижения количества случаев гемодинамического и метаболического поражения почечных клеток при системных нарушениях пациентам с отравлениями рекомендован регулярный контроль функциональной состоятельности почек и адекватное купирование острого состояния. С учетом роста распространенности лекарственных нефропатий при назначении нефротоксичных лекарственных средств необходимо тщательное обследование пациента для выявления предпосылок к токсическому повреждению ренальной паренхимы.
2. Патогенез токсических нефропатий/ Гоженко А.И. // Актуальные проблемы транспортной медицины. — 2006 — № 2.
3. Клинико-морфологические изменения при токсической нефропатии, вызванной отравлением некоторыми спиртсодержащими жидкостями: Автореферат диссертации/ Морозов В.И. – 1996.
4. Механизмы хронической токсической нефропатии у рабочих химической промышленности: Автореферат диссертации/ Письменский А.В. – 2006.
Почечная недостаточность - это урологическое заболевание, для которого характерно нарушение или полное угасание функций почек: выделительной, метаболической, эндокринной, фильтрационной. Различают острую и хроническую почечную недостаточность. На раннем этапе симптомы заболевания неспецифические — повышенная утомляемость, ощущение сухости во рту, слабость. Далее присоединяется диарея, рвота, расстройства мочевыделения, отеки. Диагноз подтверждают на основании данных биохимического анализа крови и мочи, УЗИ органов мочевыделения, биопсии почек. Лечение преимущественно консервативное. Заболевание представляет опасность для жизни. На его исход влияет возраст пациента, наличие осложнений, степень дисфункции.
Общее понятие
Почки — парные органы мочевыделительной системы, которые поддерживают кислотно-щелочное равновесие, выводят из организма токсические вещества. При снижении функций почек конечные продукты обмена веществ накапливаются в крови, тем самым нарушают равновесие кислот и оснований, разрушают клетки. Возникает риск интоксикации, возможна даже гибель организма.
Деятельность почек также обеспечивает процессы кроветворения, обмена веществ, стимулирует выработку некоторых гормонов. В почках завершается формирование активной формы витамина Д, ответственного за состояние скелетно-мышечной системы. Поэтому, какие-либо изменения в работе почек негативно отражаются на функционировании всего организма, служат фоном для развития различных заболеваний и состояний.
Виды и стадии почечной недостаточности
Различают острую (ОПН) и хроническую почечную недостаточность (ХПН). Для острой формы характерны обратимые нарушения функций органа без утраты нефронов (клеток органа). При хронической форме происходит полное угасание почечных функций, постепенная гибель нефронов. Хроническую почечную недостаточность определяют в случае, если критерии повреждения сохраняются в течение трех и более месяцев.
Справка! Синонимичные названия острой почечной недостаточности — фульминантная, сверхострая или подострая. Все они описывают стремительное прекращение функций ранее здоровой почки.
По причинам и механизму возникновения острую почечную недостаточность условно делят на три категории:
Преренальную. Возникает на фоне нарушения оттока крови, обезвоживания, закупорки легочных артерий, сердечной недостаточности, острой кровопотери, аритмии.
Ренальную (паренхиматозную). В качестве провоцирующих факторов рассматривают токсическое и воспалительное повреждение паренхимы (ткани, в которой расположены нефроны). Причиной могут быть грибы, вирусы, бактерии, противоопухолевые препараты, некоторые антибиотики, контрастные вещества рентгенологического исследования.
Постренальную (обструктивную). Последствие нарушения оттока мочи. Наблюдается при камнях в почках, мочеточниках, опухолях предстательной железы, воспалении мочеиспускательного канала.
Выделяют четыре фазы острой почечной недостаточности:
Начальная. Протекает без выраженных симптомов. Неспецифические проявления — сонливость, слабость, утрата аппетита.
Олигоанурическая. Количество суточной мочи менее 500 мл. В моче повышенная концентрация белка до 150 мг в сутки и выше. Присоединяется тошнота, рвота, влажные хрипы и одышка. Возможно поражение органов пищеварения и сердечно-сосудистой системы. Продолжительность олигоанурической стадии от 10 до 14 дней.
Диуретическая. Суточный объем мочи постепенно увеличивается до 2–5 л. Водно-электролитный баланс восстанавливается на протяжении 5–10 дней.
Стадия выздоровления. Нормализация функций почек длится от 6 месяцев до года.
Хроническая почечная недостаточность в развитии проходит тоже четыре стадии:
Латентная. Клинически не проявляется. Болезнь обнаруживают по результатам анализа крови и мочи. Скорость клубочковой фильтрации снижена до 50–60 мл/мин.
Компенсированная. Предвестники заболевания — сухость во рту, слабость, недомогание. В моче и крови увеличена концентрация креатина и мочевины. Клубочковую фильтрацию определяют на уровне 49–30 мл/мин.
Интермиттирующая. Характерна разнообразная клиническая симптоматика, которая нарастает по мере снижения функций почек. Появляются осложнения со стороны разных органов и систем. Скорость клубочковой фильтрации 29–15 мл/мин. Уровень креатинина стабильно высокий, нарушен кислотно-щелочной баланс в организме (ацидоз).
Терминальная. Характеризуется грубым расстройством кислотно-щелочного и водно-солевого баланса, отечностью. Почка прекращает выделять мочу. Общее состояние утяжеляет формирование сердечной недостаточности, застойные процессы в легких и печени.
С учетом степени дисфункции почек выделяют тотальную почечную недостаточность — полное прекращение всех функций органа, и парциальную — ограничение некоторых функций.
Причины почечной недостаточности
Все причины почечной недостаточности разделяют на преренальные, ренальные, постренальные и врожденные заболевания почек.
Преренальная почечная недостаточность возникает вследствие нарушения оттока крови, уменьшения объема циркулирующей крови или снижения сердечного выброса. Это бывает при закупорке легочной артерии, кровотечениях, сердечной недостаточности, аритмии, гипоксии. Здоровая почка перестает в достаточном объеме выделять мочу, если уменьшается количество внутриклеточной жидкости при обезвоживании, рвоте, диарее, циррозе печени, ожогах.
Ренальная или паренхиматозная почечная недостаточность вызвана ишемическим и токсическим поражением паренхимы почек, реже — воспалением и сосудистыми патологиями. На состоянии и функции почек негативно сказываются контрастные рентгенологические вещества, бесконтрольный прием противоопухолевых и нестероидных противовоспалительных препаратов, некоторых антибиотиков. Риск развития патологии возникает при переливании несовместимой крови, наркотической и алкогольной коме, длительном сдавлении тканей при травме.
Постренальная или обструктивная почечная недостаточность формируется в условиях обструкции (непроходимости) мочевыводящих путей. Нарушения оттока мочи возможны в любом отделе мочевыделительной системы: мочеиспускательном канале, мочеточнике, шейке мочевого пузыря.
Наиболее частая причина почечной недостаточности среди младенческого и раннего детского возраста это врожденные заболевания почек: наследственная непроходимость мочевыводящих путей, дисфункция почечных канальцев. Среди пороков развития преобладает: мегауретер (расширение и удлинение мочеточника), поликистоз, отсутствие или недоразвитие органа.
Благоприятным фоном для формирования почечной недостаточности у взрослых определяют ожирение, курение, несбалансированное питание, злоупотребление алкоголем. В группе риска лица пожилого возраста, с сахарным диабетом и заболеваниями предстательной железы.
Справка! При повсеместном распространении, у лиц молодого и среднего возраста почечная недостаточность встречается в пять раз чаще.
Формированию хронической почечной недостаточности предшествует хронический гломерулонефрит, амилоидоз почки (отложение в почечной ткани гликопротеидного вещества — амилоида, который нарушает функции почек), поликистоз почек (образование в паренхиме органа мелких множественных кист).
Симптомы почечной недостаточности
Клиническая картина зависит от давности и степени нарушения почечной функции. ОПН возникает внезапно, развивается стремительно и проявляется многосимптомным комплексом:
сухостью во рту,
ощущением нехватки воздуха,
глубоким тяжелым дыханием,
Обычно симптомы сохраняются в течение первых трех дней, после чего наступает олигоанурическая фаза. Для нее характерно уменьшение объема мочи от 500 до 50 мл в сутки (анурия), диарея, тошнота, рвота. Возможно развитие перикардита (воспаления сердечной сумки), гастроэнтероколита (воспаления желудка, тонкого и толстого кишечника), сепсиса, пневмонии. Период олигурии длится от нескольких часов до 6–8 недель.
При благоприятном исходе почечные функции постепенно нормализуются, увеличивается количество отделяемой почками мочи, восстанавливается водно-солевой баланс.
При некорректном лечении или его отсутствии болезнь прогрессирует, переходит в хроническую форму. На начальных стадиях наступает мнимое выздоровление, общее состояние стабилизируется. Пациенты с латентной стадией не предъявляют никаких жалоб. Иногда ощущают недомогание, слабость, снижение работоспособности.
По мере нарушения функций почек и гибели нефронов, появляются первые симптомы ХПН:
сухая и бледная кожа,
беспричинное снижение веса,
дрожание кистей и пальцев рук.
Из-за накопления в крови токсических веществ возникает тошнота, рвота, неприятный запах аммиака изо рта, понос. Стул темный со зловонным запахом. Характерна резкая смена психологического состояния, снижение температуры тела ниже 35 градусов, образование эрозий на слизистой оболочки полости рта (стоматит).
Другие признаки хронической почечной недостаточности зависят от сопутствующего заболевания или органа, который был вовлечен в патологический процесс. При прогрессировании почечной дисфункции возможны желудочно-кишечные кровотечения, сердечно-сосудистые проявления (боль в сердце, одышка, синюшность кожи), неврологические нарушения (шум в голове, снижение внимания, онемение языка, зрительные расстройства).
Осложнения почечной недостаточности
Неконтролируемая ОПН приводит к полному необратимому угасанию функций органа, увеличению концентрации калия в крови (гиперкалиемии). Аккумуляция калия в больших дозах может вызвать остановку сердца.
У 50% пациентов острая почечная недостаточность нарушает иммунную защиту, организм становится уязвимым к различного рода инфекциям. Присоединение инфекции утяжеляет течение основной патологии и ухудшает прогноз. Инфекция — одна из наиболее частых причин смерти пациентов с терминальной почечной недостаточностью.
В структуре осложнений ОПН часто определяют сепсис, сердечную недостаточность, воспаление наружной оболочки сердца (перикардит). Страдает также дыхательная и нервная система, ротовая полость. Со стороны опорно-двигательной системы возможно снижение плотности костей. Это проявляется частыми переломами, артритами, ущемлением позвонков, постоянными мышечными и суставными болями.
Полная гибель нефронов при ХПН представляет угрозу жизни, увеличивает риск возникновения осложнений, как отек легких, энцефалопатия (поражение головного мозга), гастроэнтероколит (воспаление желудка), уремическая кома.
Диагностика почечной недостаточности
При подозрении на развитие почечной недостаточности пациенту необходима консультация нефролога. При внешнем осмотре специалист оценивает состояние кожи, наличие аммиачного запаха, дрожание конечностей, собирает анамнез и анализирует жалобы пациента.
Для подтверждения или исключения дисфункции почек проводят ряд исследований:
Общий клинический анализ мочи. Дает информацию о дневном и ночном объеме мочи, ее пенистости, кислотности. Анализ информативен в рамках диагностики сахарного диабета, патологий органов мочевыделительной и половой системы. При почечной недостаточности в моче обнаруживают белок и эритроциты.
Биохимия крови. Определяет снижение фильтрационной и выделительной функции почек, концентрацию мочевой кислоты, калия, кальция, мочевины, креатинина, по содержанию которых можно судить о функциональном состоянии органа.
Проба Зимницкого. Оценивает способность почек к концентрации мочи. Анализ по Нечипоренко исключает воспалительные процессы.
Для выявления структурных изменений органов мочевыделительной системы и новообразований назначают аппаратные методы исследования: УЗИ, рентгенографию, компьютерную и магнитно-резонансную томографию. Чтобы оценить скорость кровотока в почках выполняют ультразвуковое сканирование сосудов. При подозрении на системное заболевание или недостаточной информативности других исследований необходима биопсия почки.
Лечение почечной недостаточности
Тактика лечения зависит от общего состояния пациента, и направлена на устранение причин и заболеваний, которые привели к снижению почечных функций:
при острой кровопотере восполняют объем циркулирующей крови путем переливания;
чтобы уменьшить сердечную нагрузку назначают нитроглицерин, антиаритмические средства;
для коррекции анемии используют препараты эритропоэтина (один из гормонов почек);
витамин D профилактирует почечную остеодистрофию (изменение морфологии костей у пациентов с хронической почечной недостаточностью);
при интоксикации промывают желудок, внутривенно вводят хлорид натрия для восстановления водно-солевого равновесия;
злокачественные новообразования иссекают хирургическим способом, после чего назначают иммунотерапию, лучевую и химиотерапию;
при затруднении оттока мочи удаляют камни из почек и мочеточников;
курсы антибактериальных препаратов необходимы при половых инфекциях, воспалительном поражении органов мочевыделительной системы;
наличие сахарного диабета требует приема инсулина, постоянного контроля уровня глюкозы.
Для уменьшения концентрации в крови токсинов, гормонов, липидов и белков назначают гемосорбцию и плазмаферез. Через периферическую вену забирают кровь, фильтруют от вредных веществ, и потом очищенную кровь вводят обратно пациенту. Количество и частоту процедур определяет нефролог в случае конкретного пациента.
При обильной потере внутриклеточной жидкости во время рвоты, диареи рекомендована диета для восстановления водно-солевого баланса:
ограничить количество поваренной соли до 5 г в сутки;
исключить из рациона копчености, консервы, соленья, жирные сорта мяса, концентрированные бульоны,
противопоказаны продукты, богатые калием — бананы, сухофрукты, виноград, грибы, шоколад;
в достаточном количестве употреблять полиненасыщенные жиры и углеводы.
Если пациент находится в тяжелом состоянии, потребность в энергии и питательных веществах восполняют с помощью растворов глюкозы и специальных препаратов для внутривенного питания.
При тяжелой ХПН, не поддающейся консервативной терапии, необходима трансплантация почки.
Исход острой и хронической почечной недостаточности определяет тяжесть основного заболевания, которое привело к дисфункции органа. При своевременном обращении и грамотной коррекции нарушений у 50% пациентов почечные функции восстанавливаются в полном объеме, у 10–15% — частично, и только 1–5% нуждаются в постоянном очищении крови или трансплантации органа.
Профилактика почечной недостаточности
Профилактика почечной недостаточности заключается в раннем выявлении провоцирующих заболеваний, ограничении факторов риска, укреплении иммунитета, соблюдении норм здорового образа жизни.
Первые проявления заболевания почек остаются часто незамеченными. Время от времени почти каждого человека может беспокоить поясница, наблюдаются скачки артериального давления или возникает головная боль. Обычно эти симптомы проходят самостоятельно. Люди не обращают на них должного внимания, в то время как патологический процесс в почках усугубляется. К врачу обращаются тогда, когда нормальная функциональность органа уже нарушена. Чтобы этого не произошло, нужно знать что такое воспаление почек, симптомы и лечение этого болезненного состояния.
Нефрит: что за болезнь и ее виды
В медицине все воспалительные процессы, которые возникают в почках и охватывают орган полностью или возникают отдельными очагами называют нефрит. Он может быть односторонним (охватывает одну почку) или двухсторонним.
В зависимости от локализации воспаления и его распространения выделяют несколько видов заболеваний:
- Пиелонефрит — наиболее распространенный диагноз. Наблюдается больше у молодых женщин. Причиной являются инфекционные возбудители. Чаще это бактерии и вирусы. Патологический процесс охватывает чашечки, лоханку и паренхиму органа.
- Гломерулонефрит — диагностируется редко. Это состояние опасно осложнениями, так как воспаление распространяется быстро. Поражаются в основном почечные клубочки, иногда — канальцы. Может стать причиной почечной недостаточности. Наблюдается чаще у мальчиков в возрасте до 10 лет.
- Интерстициальная форма — опасная разновидность. Воспаление возникает в промежуточной ткани органа, а также поражает канальцы. Значительно ухудшается работа почек. На начальной стадии легко поддается терапии, при запущенном течение возможна кома и летальный исход.
- Лучевой — причиной является негативное воздействие ионизирующего излучения. Первые симптомы проявляются только спустя 2-3 месяца. Редкая форма.
- Шунтовый — возникает на фоне других системных заболеваний. Это может быть ревматоидный артрит, красная волчанка или аутоиммунные патологии.
По клиническому течению заболевания выделяют острое воспаление почек и хроническое.
Если патология возникает на фоне общего здоровья, то она является первичной. В 80% случаев всех нефритов человек раньше с заболеваниями почек не сталкивался. Вторичное поражение органа происходит из-за уже существующего в организме воспаления в других близлежащих органах.
Проявления воспаления почек
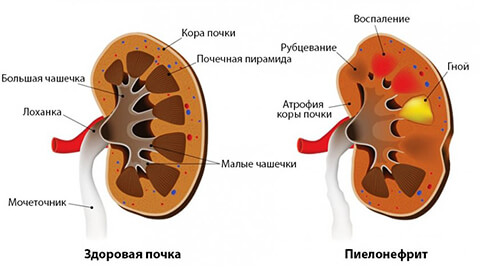
Начало заболевания часто протекает в острой форме. Для этого периода характерны следующие симптомы:
- опоясывающая боль в области поясницы;
- изменение цвета мочи;
- общая усталость и недомогание;
- редкие позывы к мочеиспусканию;
- гипертония;
- отеки лица и тела;
- редкие позывы к мочеиспусканию.
При усугублении состояния может беспокоить жажда, сухость во рту, рези при мочеиспускании. При возникновении воспаления правой почки боли будут ощущаться с правой стороны, чуть ниже поясницы.
Если в этот период не обратиться к специалисту и не начать лечение, то болезнь приобретает хроническое течение. Для него характерны периоды обострений и ремиссии. Симптоматика менее выражена, в период возвращения болезни проявления схожи с острой формой.
Длительное течение заболевания приводит к тому, что почка уменьшается в размере. Она не может работать в полную силу, что приводит к интоксикации. Частым осложнением является уремия. Это тяжелое состояние, при котором из-за почечной недостаточности в организме накапливаются шлаки и токсины.
Частые обострения оказывают негативное влияние на состояние сердечно-сосудистой системы. У женщин часто симптоматика болезни почек может напоминать гинекологические болезни. Здесь важно пройти тщательное обследование, чтобы выявить истинную причину недомогания.
При болезни почек воспаление нередко протекает в скрытой форме. Особенно у детей. Если ребенок стал бояться ходить в туалет, стало возникать самопроизвольное мочеиспускание или в моче появились непонятные примеси — обязательно нужна консультация детского уролога.
Причины воспаления почек
Провокатором воспалительного процесса являются патогенные микроорганизмы. Чаще всего энтерококк, стафилококк, а также кишечные бактерии. В 15-20% наблюдается смешанная инфекция.
Возбудитель в почку может попасть по мочевыводящим путям, через кровь или лимфогенным путем. Активизация патологического процесса запускается из-за общего переохлаждения, перенесенного инфекционного заболевания. Особенно если человек перенес болезнь на ногах.
В группе риска по заболеваниям почек входят люди, у которых имеется:
- Врожденное или приобретенное (в результате травмы) сужение мочевыводящих путей.
- Сахарный диабет, нарушения обмена веществ.
- Были проведены оперативные вмешательства или исследования связанные с проникновением в мочевыводящие каналы. Это установка катетера, введение диагностических инструментов.
Также увеличивает риск длительный прием некоторых медикаментов, действие которых направлено на подавление иммунитета. Например, при трансплантации органов. Чаще всего болезни почек поражают женщин. Это связано с особенностями строения женской мочевыделительной системы.
Причинами вторичного поражения почек являются:
- инфекционно-воспалительный процесс в других органах;
- злоупотребление алкоголем;
- отравление промышленными или бытовыми химикатами; наркомания;
- сильная доза облучения;
- туберкулез.
Диагностика и лечение воспаления почек
При возникновении симптомов нужно обращаться к урологу. Врач назначит обследование, которое включает:
- КТ органов малого таза. При необходимости проводится с контрастом. . и крови.
- Бак посев мочи, который направлен на определение типа возбудителя.
Для уточнения патологии женщине рекомендовано пройти осмотр у гинеколога, чтобы исключить воспаления органов малого таза.
Консервативная терапия
Острая форма или обострение хронического воспаления требуют госпитализации. Обязательно нужно обеспечить пациенту постельный режим и сухое тепло в поясничную область. Только в горизонтальном положении происходит улучшение кровоснабжения сосудов почки, что способствует скорейшему выздоровлению. Физическая активность в остром периоде строго противопоказана.
Врач назначает обезболивающие препараты, спазмолитики, диуретики и антибиотики (при необходимости). Важно при этом соблюдать бессолевую диету. Также следует временно исключить из рациона питания животный белок.
Водный режим устанавливается врачом, исходя из формы и течения заболевания.
Хирургические методы
Если лечение медикаментами не приводит к улучшению состояния больного, а также при тяжелых нарушениях со стороны мочевыделительной системы, целесообразно проведение нефрэктомии. Это операция, в ходе которой удаляется частично или полностью пораженная почка. Этот способ является единственным эффективным методом лечения при обнаружении злокачественных образований на органе или если есть риск развития абсцесса или сепсиса.
После операции пациенту назначается поддерживающая антибактериальная терапия.
В особо тяжелых случаях требуется пожизненное прохождение гемодиализа и последующая пересадка органа.
Народные средства лечения воспаления почек

Во время ремиссии можно поддерживать здоровье почек с помощью растительных препаратов. Это поможет закрепить эффект от лечения. Но выбор следует обязательно делать совместно с лечащим врачом.
При разных формах нефрита рекомендуются следующие травы:
- почки березы;
- шалфей и листья толокнянки;
- ромашка;
- кукурузные рыльца;
- полевой хвощ;
- листья брусники;
- можжевельник.
Фитотерапия не заменит медикаментозное лечение, и не поможет при запущенном течение заболевания. Она может использоваться только в комплексе с терапией, которая назначена урологом.
Профилактика воспаления почек
Чтобы сохранить здоровье почек, и предотвратить возможность развития в них воспаления рекомендуется придерживаться следующих рекомендаций:
- Своевременно пролечивать инфекции половых и мочевыводящих органов.
- Не злоупотреблять алкоголем, особенно пивными напитками.
- Ограничивать употребление соли.
- Не игнорировать боль в пояснице.
- Избегать переохлаждения.
- При ОРВи соблюдать постельный режим.
- Проходить ежегодные профилактические осмотры.
Если проблемы с почками уже есть, то из рациона исключаются пряности и жгучие приправы. Соблюдайте правильный питьевой режим. Следите за иммунной системой.
Читайте также:

