Как терапия от вич влияет на печень
Обновлено: 19.04.2024
Цель исследования. Оценка частоты и выраженности гепатотоксичности у больных, получавших различные схемы антиретровирусной терапии (АРТ), для дальнейшего совершенствования подходов к лечению.
Материалы и методы. Проведен анализ частоты развития гепатотоксичности в первые 48 недель АРТ у 720 взрослых пациентов с ВИЧ-инфекцией. Развитие гепатотоксичности оценивали по международной шкале нежелательных явлений на основании клинической симптоматики, а также динамики уровней АЛТ и АСТ, измеренных до начала лечения, через 1, 3, 6 и 12 месяцев терапии.
Результаты. Наиболее часто повышение уровня ферментов печени происходило через 3–6 месяцев АРТ, независимо от режима лечения. Частота развития выраженной гепатотоксичности (3-й степени) возрастала пропорционально времени приема антиретровирусных препаратов. Использование ИП практически не влияло на частоту повышения уровня трансаминаз, в то время как при применении ННИОТ гепатотоксичность развивалась более чем у половины пациентов к 6 месяцам АРТ. Исходное повышение уровня АЛТ и наличие хронического вирусного гепатита явились наиболее неблагоприятными факторами развития гепатотоксичности в процессе АРТ, особенно у больных, принимающих препараты класса ННИОТ. Женщин с количеством CD4+-лимфоцитов более 250 клеток/мкл и мужчин с этим показателем, превышающим 400 клеток/мкл, необходимо рассматривать как группу риска развития гепатотоксичности при начале приема невирапина.
Заключение. Пациентам, страдающим хроническими вирусными гепатитами или имеющими повышение уровня трансаминаз, в схему АРТ, помимо 2 НИОТ, целесообразно включать ИП. Поскольку в каждом классе есть препараты с большим и меньшим гепатотоксическим эффектом, крайне важно подбирать схемы АРТ строго индивидуально, с учетом всех особенностей пациента.
Повышение уровня трансаминаз – одно из наиболее распространенных нежелательных явлений при лечении ВИЧ-инфицированных пациентов. Эти нарушения могут быть вызваны, с одной стороны, антиретровирусными препаратами (АРВ-препаратами), с другой – влиянием вирусов гепатитов В (ВГВ) и С (ВГС), воздействием токсических субстанций (алкоголя, психоактивных веществ и т. д.), использованием лекарственных препаратов для лечения вторичных и сопутствующих заболеваний, развитием стеатогепатита, связанного с метаболическим синдромом (гиперлипидемией, диабетом, ожирением) [1]. Диагностика гепатотоксичности АРВ-препаратов представляет некоторые сложности. Во-первых, нет четких критериев для постановки диагноза. Во-вторых, пациенты часто принимают несколько препаратов, обладающих гепатотоксическим потенциалом. Наконец, гистологические проявления гепатотоксичности чрезвычайно разнообразны, поэтому биопсия печени имеет ограниченное применение в диагностике. Тем не менее иногда она бывает полезна для исключения других причин повышения уровня ферментов печени [2]. У большинства (70–85%) больных ВИЧ-инфекцией гепатотоксичность не сопровождается клинически выраженными симптомами, а уровень трансаминаз часто возвращается к норме на фоне продолжения приема препарата, вызвавшего это повышение [3]. Однако присоединение таких симптомов, как слабость, тошнота, рвота, желтуха может говорить о более выраженном поражении печени, которое в некоторых случаях может привести к летальному исходу.
Множество рандомизированных контролируемых исследований посвящено изучению связи между развитием гепатотоксичности и АРВ-препаратами [4–7]. Сложность в интерпретации результатов этих исследований заключается в том, что пациенты из групп сравнения неоднородны по своим параметрам (возрасту, полу, алкогольному профилю, исходному количеству CD4+-лимфоцитов, вирусной нагрузке, начальному уровню трансаминаз). Кроме того, в одних исследованиях под гепатотоксичностью понимают повышение уровня ферментов печени, в то время как в других учитываются только клинические проявления (такие как клинически выраженный гепатит) [8]. В настоящее время опираются на критерии, принятые международной клинической исследовательской группой по СПИДу (AIDS Clinical Trials Group), которые основаны на степени повышения уровня трансаминаз [9], а также на клинические симптомы острого гепатита, реакций гиперчувствительности и лактоацидоза.
Существует целый ряд факторов, повышающих риск возникновения гепатотоксичности. К общим факторам риска относят возраст старше 60 лет, повышенный индекс массы тела, наличие тромбоцитопении или инфекции, сочетанной с гепатитами В или С, исходно повышенный уровень АЛТ, а также употребление алкоголя и/или других гепатотоксичных субстанций [4, 7, 10–12].
Разные классы АРВ-препаратов вызывают гепатотоксические реакции с разной частотой и в разные сроки, что зависит от механизма повреждений. Результаты исследований, оценивавшие риск токсичности для печени при использовании конкретных АРВ-препаратов или их классов, противоречивы. Несбалансированные и часто недостаточные выборки в этих исследованиях не позволяют точно определить роль каждого конкретного препарата в развитии печеночной токсичности. Кроме того, использование сочетаний нескольких АРВ-препаратов затрудняет сравнительный анализ. Однако большинство исследователей склоняется к мнению о меньшей (6–10%) гепатотоксичности ингибиторов протеазы ВИЧ (ИП) [13]. Препараты новых классов и следующая генерация препаратов уже существующих классов антиретровирусной терапии (АРТ) – ралтегравир, этравирин, рилпивирин – обладают меньшим токсическим эффектом.
Материалы и методы
Был проведен анализ частоты развития гепатотоксичности в первые 48 недель АРТ у 720 взрослых пациентов с ВИЧ-инфекцией. В составе схемы АРТ 371 больной получал ИП (123 человека – LPV/r, 124 человека – ATV/r или ATV, 38 человек – DRV/r, 25 человек – SQV/r, 61 человек – NFV), а 349 пациентов – ненуклеозидные ингибиторы обратной транскриптазы ВИЧ (ННИОТ): 269 человек – EFV, 80 человек – NVP. В качестве нуклеозидной основы у всех пациентов в состав схемы АРТ включали 2 нуклеозидных ингибитора обратной транскриптазы ВИЧ (НИОТ). Лечение больным было назначено в соответствии с российскими рекомендациями по началу АРТ. Пациентов наблюдали в Федеральном научно-методическом центре по профилактике и борьбе со СПИДом и 17 территориальных центрах по профилактике и борьбе со СПИДом и инфекционными заболеваниями (Республики Башкортостан, Алтайского, Красноярского, Краснодарского и Пермского краев, Волгоградской, Иркутской, Калининградской, Кемеровской, Ленинградской, Нижегородской, Ростовской, Саратовской, Свердловской, Ульяновской и Челябинской областей, г. Тольятти).
До начала лечения всех больных тестировали на наличие ВГВ/ВГС, а также определяли уровень РНК ВИЧ и количество CD4+-лимфоцитов. Применяли общеклинические методы исследования (осмотр пациента, сбор анамнеза, анализ периферической крови и биохимический анализ крови).
Вирусный гепатит С – воспалительное заболевание печени, вызванное соответствующим вирусом. В течение многих лет болезнь может протекать без симптомов, что делает ее особенно опасной: велика вероятность развития последствий – цирроза и рака печени. Именно поэтому так важно своевременно выявить заболевание и начать лечение.
Гепатит С может протекать в острой и хронической формах. Острая форма чаще всего проходит бессимптомно и диагностируется только случайно при обнаружении в крови маркеров острого гепатита С – анти-HCV-IgM, который сохраняется в крови не больше 6 месяцев после заражения вирусом.
После перенесенного острого вирусного гепатита C возможно три варианта развития событий.
Вариант 1.
Примерено у 20% пациентов происходит полное выздоровление.
Вариант 2.
У 20% пациентов развивается неактивный хронический вирусный гепатит С с отсутствием лабораторных маркеров воспалительного процесса в печени.
Вариант 3.
У остальных 60% наблюдается хронический гепатит с клиническими и лабораторными проявлениями поражения печени.
Переход заболевания в хроническую форму происходит незаметно. Повреждение печени с годами нарастает и у пациента формируется фиброз с последующим нарушением функции печени. Болезнь прогрессирует медленно, годами. У пациентов с активным гепатитом риск формирования цирроза в течение 20 лет достигает 20%, из них у 5% развивается рак печени.
Пути передачи гепатита С такие же, как и у гепатита В: через кровь, при половом контакте, от матери к ребенку. Большинство случаев заражения гепатитом С в России приходится на употребление инъекционных наркотиков. Заражение половым путем происходит реже, так же как и передача вируса от матери к ребенку во время беременности. Кормление при заболевании не запрещено, однако следует соблюдать осторожность при появлении крови на сосках.
При бытовых контактах заразиться вирусом гепатита С невозможно. Вирус не передается воздушно-капельным путем, при рукопожатии, объятиях и использовании общей посуды. Больные вирусным гепатитом С не нуждаются в изоляции и не представляют опасности для окружающих. В России они, однако, освобождаются от призыва в армию.
Особенность вируса гепатита С
Но сегодня гепатит С продолжает оставаться одной из главных причин, приводящих к пересадке печени, поэтому его лечение откладывать нельзя.
Кроме того, гепатит С часто является сопутствующим заболеванием при ВИЧ-инфекции, так как оба вируса распространяются через контакт с кровью. Такая коинфекция создает несколько особенных проблем:
- гепатит С делает ВИЧ сильнее (отчасти это связано с повреждениями печени);
- люди, у которых выявлены обе инфекции, более подвержены депрессиям;
- у людей с ВИЧ гепатит С может протекать тяжелее и вызывать серьезные повреждения печени или полный ее отказ;
- пациенты с ВИЧ с большей вероятностью инфицируют других гепатитом С, поскольку их вирусная нагрузка выше;
- препараты для лечения ВИЧ тяжелее переносятся людьми, имеющими гепатит С;
- гепатит С замедляет уровень роста клеток CD4 во время лечения ВИЧ-инфекции.
Качественное и своевременное лечения гепатита С имеет следующие преимущества:
- есть вероятность полного излечения от вируса;
- лечение в большинстве случаев позволяет замедлить патологический процесс в ткани печени и таким образом отдалить наступление необратимых тяжелых осложнений болезни, включая риск развития рака печени;
- лечение снижает вероятность передачи инфекции окружающим, в частности, сексуальным партнерам;
- успешная терапия гепатита С делает невозможной передачу вируса от матери к ребенку (при коинфекции ВИЧ/ВГС риск инфицирования ребенка вирусом гепатита значительно выше, чем при моноинфекции);
- в случае коинфекции ВИЧ/ВГС раннее успешное лечение гепатита С (до начала приема антиретровирусных препаратов) существенно упростит в будущем выбор режима АРВ-терапии и уменьшит риск усугубления токсических эффектов некоторых препаратов на печень;
- лечение гепатита С при достижении устойчивого вирусологического ответа снижает риски печеночных событий, в том числе приводящие к смерти, а также риски развития СПИД-индикаторных заболеваний, не связанных с заболеваниями печени.
Способы защиты от гепатита С:
- не употреблять наркотики;
- использовать только свои предметы личной гигиены (бритва, зубная щетка, маникюрные принадлежности);
- использовать презервативы при каждом половом контакте;
- внимательно следить за соблюдением стерильности инструментария при проведении любых медицинских и косметологических процедур, связанных с повреждением кожных покровов (в тату- и пирсинг-салонах, медучреждениях).
Действующей вакцины от гепатита С на сегодняшний день пока не создано, но ее поиски активно ведутся.
Иммунная система нашего организма представлена органами и клетками, расположенными по всему телу. Лимфоциты, являясь частью иммунной системы и обладая специфичностью, способны создавать и хранить иммунную память о возбудителе инфекционной болезни. Лимфоциты-Т4 (или CD4 Т-клетки) распознают чужеродные вещества или микроорганизмы, проникающие в наш организм, при этом запоминая их. При повторном попадании в наш организм этих чужеродных субстанций, белые клетки крови способны их распознавать, блокируя их разрушительное воздействие и уничтожать.
Тест на ВИЧ проводится методом ИФА и ориентирован на выявление антител и антигена. Отрицательный или негативный результат говорит о том, что антител не обнаружено. При этом ВИЧ очень быстро размножается в организме человека. И риск передать ВИЧ при сексуальном контакте или через кровь очень высокий.
У многих людей в первый год после заражения развивается острое заболевание с повышением температуры, увеличением лимфатических узлов. Иногда острая ВИЧ-инфекция может протекать как бронхит или пневмония, краснуха или в виде высыпаний на коже. Такое состояние у ВИЧ-инфицированного может продолжаться около двух недель, а затем состояние на фоне лечения основных симптомов нормализуется. Но на основании этих признаков нельзя сказать, что человек ВИЧ-инфицированный, т.к. перечисленные симптомы являются общими для многих заболеваний, например - обычной простуды.
Если в этот период не было начато лечение ВИЧ-инфекции, то у человека с ВИЧ наступает период, когда подавленный вирусом иммунитет больше не может выполнять свою защитную функцию. Тогда у ВИЧ-позитивного человека могут развивать заболевания, которые называют вторичными (первичным является ВИЧ-инфекция). Эти заболевания протекают вначале как бактериальные, грибковые и вирусные поражения слизистых оболочек и кожных покровов, позже развивается поражение внутренних органов. Одним из серьезных заболеваний для людей, живущих с ВИЧ является туберкулез. Если лечение так и не начинается, количество CD4 клеток становится менее 200, такое состояние угрожает жизни человека. Могут развиваться поражения нервной системы, онкологические заболевания, в т.ч. саркома Капоши - злокачественная опухоль кожи и сосудов.
Заключительная стадия развития ВИЧ-инфекции - это СПИД или терминальная стадия. Эта стадия была введена в клиническую классификацию ВИЧ-инфекции в 1989г., когда высокоактивной АРТ ещё не существовало и, несмотря на адекватную (по тем временам) терапию, имеющиеся у болеющих вторичные заболевания приобретали необратимый характер, и пациент погибал в течение нескольких месяцев после их развития. В настоящее время даже у пациентов с уровнем CD4, близким к нулю, и тяжёлыми вторичными заболеваниями, лечение ВИЧ-инфекции не является бесперспективным.

Российская клиническая классификация ВИЧ-инфекции
1. Стадия инкубации.
2. Стадия первичных проявлений.
Б. Острая ВИЧ-инфекция без вторичных заболеваний;
В. Острая ВИЧ-инфекция с вторичными заболеваниями.
3. Субклиническая стадия.
4. Стадия вторичных заболеваний.
4А. Потеря массы тела менее 10%, грибковые, вирусные, бактериальные поражения кожи и слизистых, повторные фарингиты, синуситы, опоясывающий лишай.
- прогрессирование на фоне отсутствия АРТ, на фоне АРТ;
- ремиссия (спонтанная, после АРТ, на фоне АРТ).
4Б. Потеря массы тела более 10%, необъяснимая диарея или лихорадка более мес, повторные стойкие вирусные, бактериальные, грибковые, протозойные поражения внутренних
органов, локализованная саркома Капоши, повторный или диссеминированный опоясывающий лишай.
- прогрессирование на фоне отсутствия АРТ, на фоне АРТ;
- ремиссия (спонтанная, после АРТ, на фоне АРТ).
4В. Кахексия. Генерализованные вирусные, бактериальные, микобактериальные, грибковые, протозойные, паразитарные заболевания, в том числе: кандидоз пищевода, бронхов, трахеи, лёгких; пневмоцистная пневмония; злокачественные опухоли; поражения центральной нервной системы.
Отравление лекарствами для лечения ВИЧ, СПИДа и их побочные эффекты
Yarchoan и соавт. обобщили свойства нуклеозидных аналогов и их метаболитов.
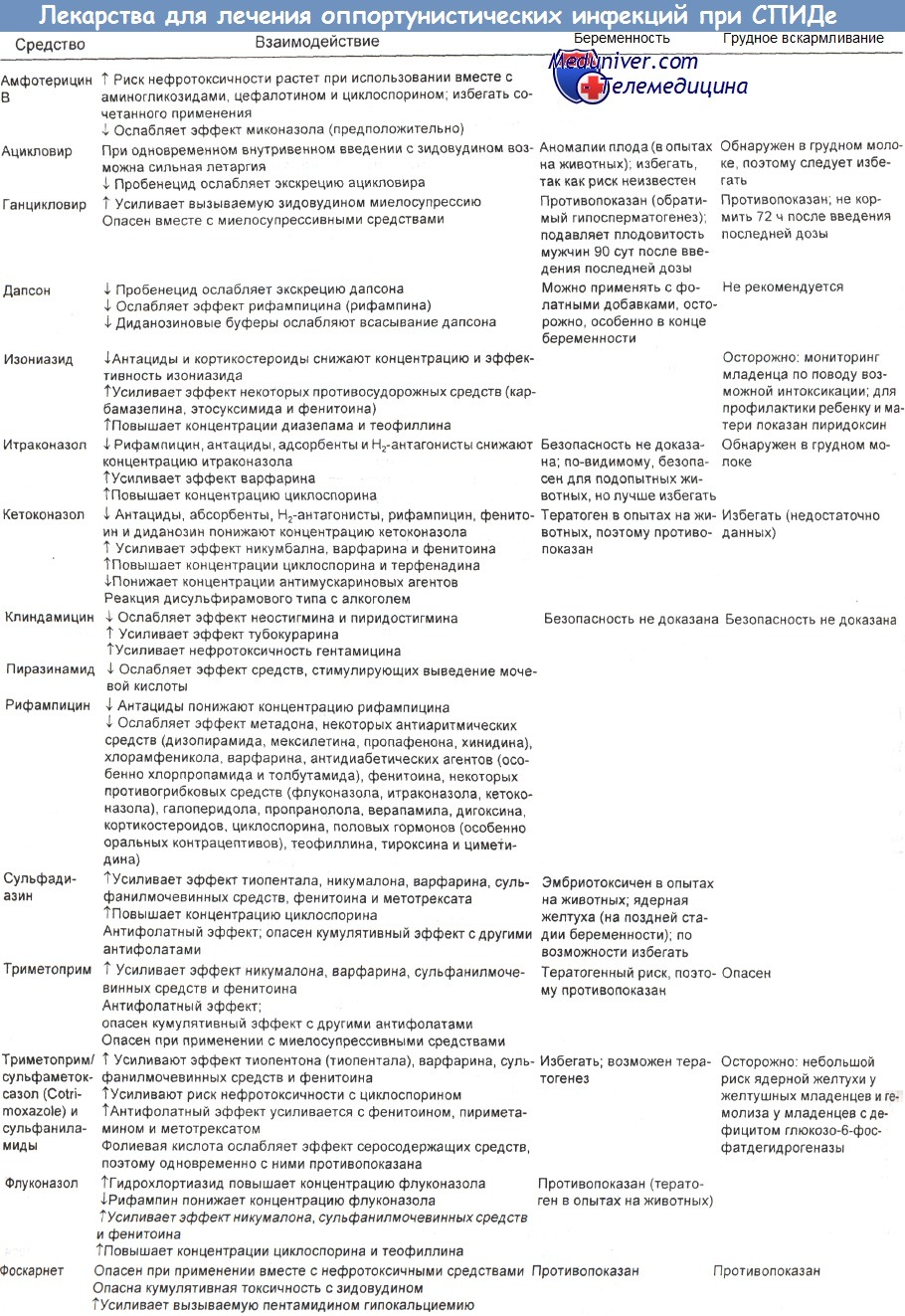
У больных СПИДом часто наблюдаются лекарственные взаимодействия с неблагоприятными побочными эффектами, поскольку этим лицам обычно назначают сразу несколько сильных средств. Краткий обзор таких взаимодействий с указанием риска применения различных агентов при беременности и грудном вскармливании представлен в таблице ниже. Lee и Safrin посвятили этому вопросу всеобъемлющий обзор.
а) Клиническая картина отравления препаратами для лечения ВИЧ и СПИДа:
- Ятрогенные реакции. У ВИЧ-инфицированных лиц высока распространенность ятрогенных реакций (например, сыпи, аллергии, панкреатит), особенно при использовании три-метоприма-сульфаметоксазола, амоксициллина/клавуланата и талидомида. В острой стадии СПИД-ассоциированных заболеваний повышенная частота таких отрицательных реакций, возможно, объясняется нарушением метаболизма лекарств, однако специфические механизмы этого явления не выяснены.
- Кожные реакции. ВИЧ-инфицированные пациенты, получающие сразу несколько лекарств, по-видимому, предрасположены к развитию синдрома Стивенса—Джонсона, токсического эпидермального некролиза и синдрома ошпаренной кожи, особенно если и в анамнезе у них отмечались ятрогенные кожные реакции. Наиболее распространена генерализованная кореподобная экзантема, появляющаяся через 7—10 сут после начала лечения и быстро проходящая при его отмене.
Для более точной оценки факторов риска острого развития нежелательных кожных реакций необходимы долговременные катамнестические исследования.
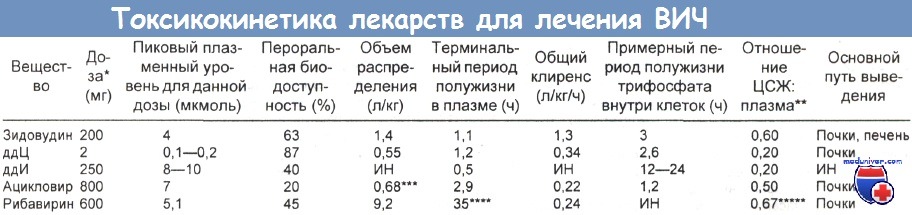
ддЦ — дидезоксицитидин; ддИ — дидезоксиинозин; ИН — информации нет; ЦСЖ — цереброспинальная жидкость.
* Типичная однократная пероральная доза для взрослых. Для ддИ — репрезентативная доза, исследовавшаяся в фазе I испытаний.
Перорально ддИ применяют с антацидами. Дозу ацикловира изучали в сочетании с зидовудином (100 мг), поскольку возможно синергическое антиВИЧ-действие.
** Измерялось через 2—4 ч после приема дозы. *** При стационарной концентрации в плазме.
**** Рибавирин накапливается также в эритроцитах, где может обнаруживаться в течение нескольких недель.
***** Это отношение для рибавирина оценивали через несколько недель лечения. Время (ч), прошедшее между введением дозы и взятием проб жидкостей, неизвестно.
в) Реакции на триметоприм + сульфаметоксазол. Частота тяжелых отрицательных реакций (кожная сыпь, цитопения, гепатотоксичность, рвота, диарея) на применение триметоприма сульфаметоксазола у больных СПИДом гораздо выше (40—80 %), чем у прочих пациентов. Некоторые данные указывают на гидроксиламиновые производные сульфаметоксазола как на реактивные метаболиты, предрасполагающие к таким реакциям. Для ВИЧ-положительных индивидов характерна системная недостаточность глутатиона, что, возможно, ослабляет связывание этих метаболитов и ведет к усилению их воздействия на организм.
г) Панкреатит. Среди причин панкреатита у больных СПИДом называют применение диданозина, пентамидина, триметоприма/сульфаметоксазола, а также ВИЧ-ассоциированные заболевания, например, цитомегаловирусную инфекцию, микобактериоз, криптоспоридиоз и опухоли.

д) Влияние на нервную систему. Психиатрические и неврологические побочные эффекты от лекарств, применяемых при ВИЧ-ассоциированных заболеваниях, перечислены в таблице ниже. Делирий при СПИДе возможен в результате интоксикации (например, снотворными средствами, опиатами, фенциклидином, алкоголем), а также синдрома алкогольной или наркотической абстиненции.
Экстрапирамидные симптомы. Больные СПИДом, принимающие антагонисты дофамина, по-видимому, более предрасположены к развитию экстрапирамидных симптомов, чем психотические пациенты без СПИДа. Нейролептики при СПИДе следует применять осторожно и в дозах ниже стандартных.
е) Патофизиология. Активность цитохрома Р450, тесно связанного с биотрансформацией лекарств, при некоторых вирусных инфекциях человека и животных снижается. Это объясняется продуцированием интерферона и ингибированием синтеза цитохрома Р450 на дотрансляционной стадии.
д) Антидоты и глутатион при ВИЧ-инфекции:
- Диэтилдитиокарбамат (дитиокарб). Одно из контролируемых катамнестических исследований позволяет предположить, что дитиокарб снижает распространенность оппортунистических инфекций у симптоматических ВИЧ-пациентов и ослабляет лимфаденопатию и спленомегалию. Дитиокарб является сильным антиоксидантом.
- N-ацетилцистеин (АЦЦ) и глутатион. Herzenberg и соавт. в Станфордском университетеи Buhl и соавт. продемонстрировали снижение уровня глутатиона в иммунной системе больных СПИДом. По-видимому, глутатион необходим для функционирования натуральных клеток-киллеров и важен для опосредованной лимфоцитами цитотоксичности. Вероятно, он защищает клетки от реактивных кислородсодержащих производных. Дефицит глутатиона и окислительное поражение тканей наблюдаются при отравлении ацетаминофеном, респираторном дистресс-синдроме взрослых, идиопатическом легочном фиброзе и СПИДе. Глутатион служит основным источником плазменного цистеина.
У больных СПИДом в плазме низкие концентрации цистеина и кислоторастворимых тиолов. Глутатион, его сложный эфир и N-ацетилцистеин (АЦЦ) подавляют экспрессию ВИЧ, ослабляют синтез ВИЧ-белков и ВИЧ-РНК. Применение высоких доз ацетаминофена при ВИЧ-инфекции, безусловно, требует серьезного анализа риска.
Кроме тиольных продуктов, на роль анти-ВИЧ-агента претендует пеницилламин, однако соответствующих клинических контролируемых испытаний не проводилось.
Дефицит глутатиона и медленное ацетилирование ряда лекарств чреваты ятрогенной аллергией. Острая стадия ВИЧ-инфекции характеризуется пониженной скоростью ацетилирования триметоприма/сульфаметокса-зола и дапсона. У ВИЧ-положительных пациентов отмечались также гиперреактивность на ужаления насекомых.
е) Внезапная смерть. Следует помнить, что внезапная смерть ВИЧ-положительных наркоманов не обязательно является результатом передозировки. К другим возможным ее причинам относятся, например, пневмонит и энцефалит.

Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Читайте также:

