Как увеличивается печень и селезенка при вич
Обновлено: 25.04.2024
Изучение морфологических изменений органов гемиммунопоэза при воздействии ВИЧ-инфекции имеет первостепенное значение поскольку именно они являются основными органами-мишенями при данной патологии.
Цель исследования - изучение морфологии центральных (костный мозг, тимус) и периферических (селезёнка, лимфатические узлы) органов гемиммунопоэза у больных, погибших на терминальной стадии ВИЧ-инфицирования.
Изучены гистологические препараты секционного материала, окрашенные гематоксилином и эозином, по ван Гизону. ВИЧ-инфекция была подтверждена с помощью иммуноблоттинга, а туберкулёз - бактериоскопическим и бактериологическим методами. Проанализированы результаты 261 вскрытия умерших от туберкулёза. Статистическая обработка данных проводилась с применением критерия Стьюдента.
В результате исследования выявлены следующие изменения в исследуемых органов. В красном костном мозге выявляется миелодисплазия. Отмечается нормальное и несколько увеличенное число ядерных клеток при нормальном соотношении миелоидных и эритроцитарных клеток, умеренный плазмоцитоз и некоторое увеличение ретикулина. Количество лимфоцитов снижено. В пунктате костного мозга находятся гистиоциты, многие из которых поглощены ядерными эритроидными клетками или гранулоцитами. Наблюдается увеличение объёма жировой ткани костного мозга. Эти данные свидетельствуют о том, что при ВИЧ-инфекции структурные изменения костного мозга затрагивают как гемопоэтическую ткань, так и стромальные элементы костного мозга.
Изменения тимуса при СПИДе и врождённом иммунодефиците связаны с поражением Т-системы. В вилочковой железе у умерших при злокачественном течении СПИД отсутствует деление на корковое и мозговое вещество, не выявляются тельца Гассаля и скопления эпителиальных клеток. Ткань тимуса инфильтрирована плазматическими и тучными клетками. Пролиферативная активность лимфоцитов при стимуляции их растворимыми антигенами снижена. При этом уровни иммуноглобулинов (IgM, IgG, IgA) повышены. Происходят изменения периферической картины крови: нейтропения, анемия, тромбоцитопения.
Выявляются очаговые поражения паренхимы селезёнки. Они представлены мелкими и крупными гипоэхогенными очагами, зонами некроза, кальцинатами, кистами, гематомами, метастазами и инфарктом селезёнки. У большей части больных селезёнка увеличена в размерах.
Изменения в лимфоузлах выражаются множественными, часто симметричными аденопатиями, наиболее часто локализующимися в шейной, подмышечной и подчелюстной областях. Особенно типичной является персистирующая генерализованная лимфаденопатия.
а) Терминология:
1. Аббревиатуры:
• Синдром приобретенного иммунного дефицита (СПИД)
• Вирус иммунодефицита человека (ВИЧ)
2. Определения:
• Внутрибрюшные оппортунистические инфекции и опухоли, возникающие на фоне ВИЧ-обусловленного иммунодефицита
б) Визуализация брюшной полости при ВИЧ/СПИД:
1. Общая характеристика:
• Локализация:
о Могут поражаться висцеральные органы, желудочно-кишечный тракт, мочевыделительная система, лимфатические узлы
• Размеры:
о Могут быть различными: от микроабсцесса (
2. Рекомендации по визуализации:
• Лучший метод визуализации:
о КТ с внутривенным контрастным усилением
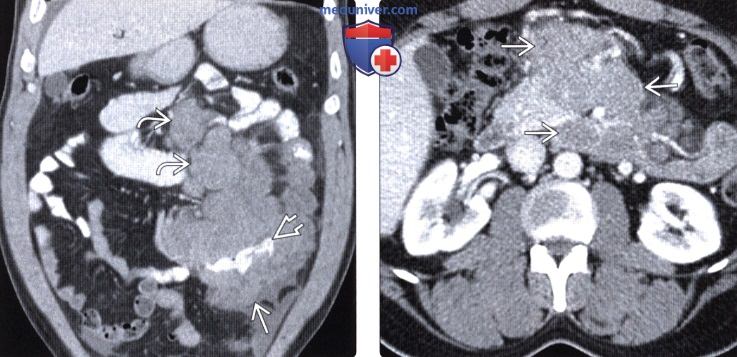
(Слева) На изображении в коро-нальной плоскости при КТ с контрастным усилением определяется диффузное опухолевидное утолщение стенки и расширение тонкого кишечника в левом нижнем квадранте, видно также контрастное вещество в просвете кишки. Чуть выше обратите внимание на выраженную лим фаденопатию. Эти изменения обусловлены подтвержденной биопсией СПИД-детерминированной неходжкинской лимфомой.
(Справа) На аксиальном срезе при КТ с контрастом определяется выраженная мезентериальная лимфаденопатия, обусловленная СПИД-детерминированной неходжкинской лимфомой.
3. КТ брюшной полости при ВИЧ/СПИД:
• Печень:
о В печени могут быть выявлены узловые образования и цирротические изменения, т. к. ВИЧ часто сопровождается хроническими вирусными гепатитами
о Маленькие гиподенсные диффузные очаги в паренхиме печени могут быть обусловлены микроабсцессами (часто при авиум-микобактериальной инфекции, туберкулезе, гистоплазмозе, поражении кандидами, пневмоцистами и др.)
о Могут наблюдаться диффузно-инфильтративные изменения печени, вызванные инфекциями, например авиум-туберкулезом
о Пневмоцисты (реже, чем при авиум-туберкулезе или цитомегаловирусной инфекции) могут приводить к появлению множественных диффузных кальцинатов
- Появление кальцинатов не означает снижение активности заболевания
о у 1/4 пациентов со СПИД-ассоциированной лимфомой печени выявляются гиподенсные узлы различного размера
• Билиарный тракт:
о Холангит, обусловленный оппортунистическими инфекциями:
- Экстра- и интрапеченочные билиарные стриктуры и сосочковый стеноз: желчные протоки могут выглядеть утолщенными и расширенными
- Внешний вид желчных протоков симулирует изменения при первичном склерозирующем холангите
о Акалькулезный холецистит в результате оппортунистических инфекций (цитомегаловирус, криптоспоридии):
- Утолщение и деформация желчного пузыря с наличием жидкости в окружающих тканях
• Селезенка:
о Спленомегалия выявляется у 3/4 пациентов со СПИДом, даже без наличия инфекции или опухоли
о Множественные мелкие гиподенсные очаги (микроабсцессы) обычно обусловлены диссеминированной инфекцией (например, грибками Candida, авиум-микобактериальной инфекцией, кокцидиоидомикозом, пневмоцистами и др.)
о Распространенные гиподенсные поражения могут возникать в результате инфильтративных инфекций, однако нельзя исключать и СПИД-ассоциированную лимфому
о Мелкие кальцинаты, похожие на таковые в печени, при пневмоцистной инфекции
• Желудок, тонкий и толстый кишечник:
о Утолщение стенки кишки, полнокровие слизистой и изменения жировой клетчатки вокруг кишечника всегда подозрительны в плане инфекций (включая оппортунистические)
- Язвообразование в кишечнике на фоне цитамегаловирусной инфекции может привести к перфорации (одна из наиболее частых причин экстренных оперативных вмешательств в брюшной полости у пациентов со СПИДом)
о Многие оппортунистические инфекции могут поражать любой отдел ЖКТ (криптоспоридии, ЦМВ, микобактериальная авиум-инфекция, туберкулез, микромпоридии, Clostridium difficile, амебиаз и др.):
- Предугадать вид возбудителя на основе только его локализации - очень сложная задача, однако некоторые возбудители имеют склонность к определенным отделам ЖКТ:
ЦМВ и туберкулез поражают преимущественно подвздошную кишку
Кандиды, микроспоридии - преимущественно начальные отделы тонкого кишечника
Инфекционные заболевания толстого кишечника чаще всего обусловлены ЦМВ, С. difficle, Campylobacter, амебной инфекцией, сальмонеллами и шигеллами
о Утолщение стенки пищевода говорит об эзофагите, чаще всего обусловленном кандидами, ЦМВ или вирусом простого герпеса
о Проктит у гомосексуалистов, связанный с сексуальной активностью, может быть вызван гонококками Нейссера, хламидиями или вирусом простого герпеса
о Местное утолщение стенки кишки, похожее на объемное образование, подозрительно на злокачественную опухоль (лимфома, саркома Капоши):
- Лимфома, связанная с инвагинацией
• Лимфатические узлы:
о Умеренно выраженная генерализованная лимфаденопатия (размер узла обычно менее 1,5 см) может быть реактивной и означать первую стадию ВИЧ-инфекции:
- Может сохраняться годами при отсутствии каких-либо симптомов (персистирующая генерализованная лимфаденопатия)
о Более выраженная лимфаденопатия (более 1,5 см) характерна для оппортунистических инфекций (авиум-микобактериальная инфекция, туберкулез) или СПИД-ассоциированной лимфомы/саркомы Капоши:
- Некроз мезентериальных лимфоузлов вследствие авиум-микобактериальной инфекции или туберкулеза
- Значительное увеличение лимфоузлов при саркоме Капоши о СПИД-ассоциированная лимфома может быть связана с дискретными очагами поражения в печени/селезенке или с фокальными объемными образованиями ЖКТ:
- ЖКТ, особенно толстая кишка, подвздошная кишка и желудок - наиболее частая экстранодальная локализация поражений при лимфоме (75%)
• Почки:
о Двухстороннее увеличение почек с утолщением уротелия может быть следствием ВИЧ-нефропатии
о Фокальные гиподенсные очаги поражения могут быть проявлением инфекции (туберкулез, авиум-микобактериоз, грибковые) или СПИД-ассоциированной лимфомы
о Кальцинаты могут обнаруживаться при пневмоцистной инфекции (сходные изменения в печени и в селезенке) или реже при МАИ/ЦМВ
• Поджелудочная железа:
о Оппортунистические инфекции могут стать причиной острого панкреатита и стриктур панкреатического протока (например, ЦМВ, Cryptococcus и др.)
(Слева) На аксиальном срезе при КТ с контрастом визуализируются множественные объемные образования в печени, в т. ч. с кровоизлияниями,, у пациента со СПИДом. Данные очаги обусловлены неходжкинской лимфомой. Не совсем типичной находкой в этом случае является легкая обструкция внутрипеченочных желчных протоков.
(Справа) При УЗИ в продольной плоскости выявлено большое гипоэхогенное объемное образование у пациента со СПИДом. При биопсии была подтверждена СПИД-ассоциированная В-клеточная неходжкинекая лимфома. (Слева) При УЗИ в продольной плоскости визуализируется правая почка обычных размеров с выраженной гиперэхогенностью у пациента с ВИЧ-нефропатией в анамнезе. В отличие от остальных хронических заболеваний, почки при ВИЧ-нефропатии часто имеют нормальные размеры или несколько увеличены.
(Справа) При УЗИ в поперечной плоскости выявлены множественные небольшие кальцинаты в селезенке у ВИЧ-инфицированного пациента. Это проявления первичной пневмоцистной инфекции.
4. УЗИ брюшной полости при ВИЧ/СПИД:
• Желчный пузырь:
о Утолщение стенки желчного пузыря может быть реактивным при гепатите или вторичным при остром акалькулезном холецистите, обусловленном оппортунистической флорой
о Утолщение стенки и расширение внепеченочных и/или внутрипеченочных желчных протоков обусловлено холангиопатией на фоне СПИД
• Печень:
о Оппортунистические инфекции проявляются небольшими гипоэхогенными узелками (микроабсцессы) с диффузным распределением в печени
о Пневмоцистная инфекция дает картину небольших гипоэхогенных узлов/мелких очагов с неизмененной эхогенностью
• Лимфатические узлы:
о Некроз лимфоузлов чаще всего возникает в результате авиум-микобактериальной инфекции или туберкулеза
в) Дифференциальная диагностика поражений брюшной полости при ВИЧ/СПИД:
1. Лимфома, не обусловленная ВИЧ/СПИД:
• Более выраженное поражение лимфоузлов, в отличие от СПИД, при котором преобладают экстранодальные поражения
• СПИД-обусловленная лимфома протекает агрессивно, имеет склонность к метастазированию, в то время как лимфома, не обусловленная СПИД, на ранних стадиях ограничивается поражением лимфоузлов
2. Билиарные гамартомы:
• Множественные мелкие кистозные поражения с диффузным распределением в печени
• Могут симулировать микроабсцессы печени, но у пациентов нет каких-либо симптомов инфекции
3. Саркоидоз:
• Может проявляться множественными мелкими гиподенсными поражениями в печени и селезенке (похожими на микроабсцессы)
• Характерна верхняя внутрибрюшная лимфаденопатия, которая ошибочно может быть принята за лимфаденопатию при ВИЧ
• Медиастинальная и воротная лимфаденопатия, характерное поражение легких и отсутствие симптоматики поможет в дифференциальной диагностике
г) Патология. Общая характеристика:
• Этиология:
о При инфицировании ВИЧ приводит к разрушению CD4(+) Т-лимфоцитов и иммунному дефициту о У ВИЧ-инфицированных пациентов повышается риск развития новообразований, особенно при одновременном инфицировании вирусом Эпштейна-Барр, герпеса или папилломавирусом:
- Частота СПИД-ассоциированных опухолей (неходжкинская лимфома, саркома Капоши) существенно снижается при ВААРТ
- Риск других опухолей, протекающих более агрессивно и появляющихся в нетипично молодом возрасте, намного выше у ВИЧ-инфицированных
- Неходжкинская лимфома:
СПИД-ассоциированное новообразование (обычно при CD4 ниже 100), объединяющее несколько типов лимфом, в т.ч. диффузную В-клеточную лимфому и лимфому Беркитта
Выраженная тенденция к экстранодальному распространению (особенно в ЖКТ), поражению нетипичных мест и появлению при прогрессировании основного заболевания
- Саркома Капоши:
Низкодифференцированная саркома мягких тканей сосудистой природы, ассоциированная с ВПГ-8
о Инфекционные осложнения чаще возникают у ВИЧ-инфицированных пациентов с CD4> 200, в то же время, риск значительно возрастает при снижении уровня CD4:
- Множество различных СПИД-детерминированных инфекций, включая распространенную авиум-микобактериальную инфекцию, туберкулез, пневмоцистную инфекцию, рецидивирующие бактериальные пневмонии, персистирующую криптоспоридиальную инфекцию, хроническую герпес-вирусную инфекцию (ВПГ):
Большая часть инфекций возникают при CD4
д) Клинические особенности:
1. Проявления поражений брюшной полости при ВИЧ/СПИД:
• Самые частые признаки/симптомы:
о Острая ВИЧ-инфекция может напоминать мононукпеоз, проявляясь лихорадкой, головными болями и болями во всем теле
о У пациентов с хронической ВИЧ-инфекцией нет клинической симптоматики на фоне эффективной ВААРТ:
- Кожные проявления и легкая общая симптоматика возможны даже без иммуносупрессии
о Пациенты с выраженным СПИДом на фоне ВИЧ и с иммуносупрессией могут иметь симптоматику, обусловленную оппортунистическими инфекционными агентами (диарея, кашель/одышка, боли в животе и др.):
- У некоторых пациентов может возникать синдром кахексии со значительной потерей веса и постоянной диареей
• Другие признаки/симптомы:
о Для пациентов с низким уровнем CD4 характерна панцитопения (анемия, тромбоцитопения, лимфопения)
о Генерализованная лимфаденопатия и спленомегалия могут быть даже при отсутствии активной инфекции
• Клинический профиль:
о Клинический профиль варьирует в зависимости от страны проживания:
- ВИЧ в развивающихся странах распространяется преимущественно при вагинальных половых контактах (другие пути-при введении наркотиков и перинатальный-распространены значительно меньше)
- ВИЧ в США передается преимущественно при внутривенном применении наркотиков и при гомосексуальных половых контактах
2. Демография:
• Возраст:
о Преимущественно взрослое население, однако возможен и перинатальный путь заражения
• Пол:
о По мировой статистике большинство случаев у гетеросексуальных пар, Ж>М
• Эпидемиология:
о Больше 35 млн инфицированных по всему миру
3. Течение и прогноз:
• Разнообразные оппортунистические инфекции и СПИД-обусловленные опухоли без ВААРТ с целью подавления ВИЧ
• СПИД определяется при CD4
4. Лечение поражений брюшной полости при ВИЧ/СПИД:
• Антиретровирусные препараты для поддержания иммунного статуса
• Антибиотики при бактериальных инфекциях и антивирусные препараты при ЦМВ-инфекции
е) Список использованной литературы:
1. Tonolini М et al: Mesenterial, omental, and peritoneal disorders in antiretroviral-treated HIV/AIDS patients: spectrum of cross-sectional imaging findings. Clin Imaging. 37(3):427-39, 2013
В настоящее время исследования по проблеме патологии печени у больных в абсолютном большинстве случаев посвящены изучению вирусных гепатитов В, С, D в данной группе лиц [1, 2, 3]. Вместе с тем, учитывая все возрастающее количество больных имеющих глубокую иммуносупрессию и страдающих различными оппортунистическими заболеваниями, особый интерес представляют поражения печени у этих пациентов, не связанные с вирусами гепатитов.
Целью данной работы
служило определение спектра и частоты поражения печени, а также клинических, лабораторных, инструментальных и морфологических особенностей печеночной патологии при вторичных заболеваниях у больных
Материалы и методы
В период с января 1991 г. по март 2002 г. под нашим наблюдением находились 59 больных на стадии вторичных заболеваний, 3В (СПИД), у которых имело место поражение печени, обусловленное оппортунистическими инфекциями и опухолями. При неоднократном исследовании сыворотки крови данных пациентов иммуноферментным методом и методом ПЦР маркеры вирусных гепатитов В, С, D обнаружены не были. Во всех случаях инфицирование ВИЧ произошло при сексуальных контактах. Возраст пациентов колебался от 21 до 54 лет (средний возраст составил 35,8 + 1,5 лет), мужчин было 57, женщин — 2.
В 57 случаях заболевание закончилось летальным исходом, и характер поражения печени был подтвержден гистологическими исследованиями с окраской препаратов гематоксилином и эозином,
Результаты исследования и обсуждение
Наибольшую группу больных имевших поражение печени, составили пациенты, страдавшие генерализованным туберкулезом (25 человек, 42.4% от общего количества больных с печеночной патологией). Среди всех умерших больных туберкулезом поражение печени имело место в 26.3% случаев, в том числе, при генерализованной форме заболевания — 80.6% случаев. У большинства больных имели место милиарные поражения печени, с наличием мелких просовидных бугорков (гранулем). В двух случаях туберкулеза при наличии глубокой иммуносупрессии, были выявлены крупноочаговые изменения в органе, причем не в виде гранулем, а в форме обширных очагов казеозного некроза со скоплением большого количества возбудителя в них. В семи случаях мы наблюдали острейший туберкулезный сепсис, который был представлен многочисленными мелкими очагами некроза в печени с большим количеством микобактерий в них.
Туберкулез печени морфологически характеризовался значительным объемом поражения паренхимы, выраженной эксудативно-альтеративной реакцией, слабой пролиферативной реакцией и казеозом регионарных лимфатических узлов в области ворот печени. Масса печени была в пределах от 1450 до 1600 г.
Клинические проявления, обусловленные собственно поражением печени, при туберкулезе были скудны. Наряду с характерными для туберкулезной инфекции симптомами интоксикации (повышение температуры до 39.0 — 39.5, потливость, ознобы) имело место увеличение печени в пределах 2 — 6 см ниже края правой реберной дуги, у ряда пациентов — увеличение селезенки. Желтуха была лишь у двух больных.
При проведении УЗИ органов брюшной полости у всех больных отмечали увеличение печени с диффузными изменениями в паренхиме различной степени. В двух случаях на этом фоне определяли очаговые изменения: у одного пациента — единичный очаг повышенной эхогенности с ровным контуром, у второго — множественные очаги пониженной эхогенности размерами от 6 до 9 мм в диаметре. Селезенка у большинства больных была увеличена с диффузными изменениями в паренхиме. У двух пациентов имели место множественные, мелкие очаги пониженной эхогенности, у одного — множественные кальцинаты до 3 — 4 мм в диаметре.
Средние уровни активности АсАТ и АлАТ у больных туберкулезом составили соответственно (у здоровых лиц до 40 МЕ/л), уровни ЩФ и ГГТ — соответственно (контроль ЩФ 76.5 и ГГТ — 9.8). Максимальные цифры билирубина составили 72 мкмоль/л — связанная фракция и 48 мкмоль/л — свободная. В ряде случаев выявляли гиперглобулинемию, отражающей наличие хронической инфекции и печеночных гранулем [4].
Среднее количество в данной группе больных было 117+38 кл/мм 3 (у здоровых лиц —
Цитомегаловирусное поражение печени имело место у 10 пациентов (16.9%). Среди умерших больных, страдавших манифестной поражение печени было установлено в 10.8% случаев. При морфологическом исследовании печени выявляли гигантоклеточный метаморфоз гепатоцитов, купферовских клеток, синусоидальных клеток эндотелия артериол и эпителиоцитов желчных протоков, а также — распространенные очаги некрозов и разрастания соединительной ткани. В ряде случаев отмечали лимфогистиоцитарную инфильтрацию портальных трактов, формирование гранулем вокруг погибших гигантских клеток, наличие цитомегалоклеток в эндотелии развлетвлений воротной вены и развитие гранулематозного гепатита. Масса печени не была существенно увеличена и составляла от 1500 до 1600 г.
У больных СПИДом достаточно часто осложняется склерозирующим холангитом, папиллярным стенозом, стриктурой общего желчного протока и некалькулезным холециститом [5, 6]. В нашем исследовании в двух случаях цитомегаловирусного гепатита мы диагностировали поражение желчевыводящих путей.
Печеночная патология у наблюдаемых нами больных всегда была лишь одной из форм генерализованной Факт поражения печени в большинстве случаев устанавливали лишь при посмертном исследовании. Клинические проявления собственно гепатита у большинства больных были неяркими. Желтуху отмечали лишь в двух случаях. При пальпации живота выявляли умеренное увеличение печени, в 2/3 случаях — увеличение селезенки. У трех человек имели место носовые кровотечения.
По данным УЗИ у всех пациентов отмечали увеличение печени с диффузными изменениями в паренхиме, у трети из них в области ворот печени по ходу сосудов и желчного протока имели место крупные одиночные очаги повышенной эхогенности с неровным контуром, размерами в диаметре (рис. 1). В одном случае были выявлены многочисленные очаги пониженной эхогенности с зоной повышения эхогенности в центре, с неровными, но четкими контурами, размерами в диаметре. У половины пациентов зафиксировано увеличение селезенки, причем, в двух случаях имела место выраженная спленомегалия с диффузными изменениями в паренхиме.
Средние уровни активности АсАТ и АлАТ у больных ЦМВИ были равны соответственно, а уровни ЩФ и ГГТ — Максимальные цифры билирубина составили 139.2 мкмоль/л — связанная фракция и 62.4 мкмоль/л — свободная.
При сочетанном поражении цитомегаловирусом паренхимы печени и желчевыводящих путей, имела место стойкая умеренно выраженная желтуха, приступообразные боли в верхней части живота, тошнота, диарея. Печень была значительно увеличена (до + 7 см от правого края реберной дуги), уплотнена, чувствительная при пальпации. В этих случаях уровни активности ЩФ и ГГТ достигали максимальных значений: 2160 МЕ/л и 1827 МЕ/л, соответственно.
Количество у больных ЦМВИ было крайне низким и в среднем составило
У четырех пациентов (6.8%) поражение печени имело токсоплазменную этиологию. Среди больных токсоплазмозом патология печени была выявлена в 17.4% случаев. При морфологических исследованиях обращало на себя внимание большое количество токсоплазменных цист в синусоидах и паренхиме печени среди фокусов коагуляционных некрозов (рис. 2). При токсоплазменном гепатите могли формироваться гранулемы. Все случаи поражения печени нами установлены посмертно. При жизни больных лишь у одного отмечали иктеричность склер, увеличение печени было небольшим, нарушения функции органа отсутствовали или оставались не резко выраженными. Максимальные цифры активности АсАТ — 320 МЕ/л, АлАТ — 230 МЕ/л, ЩФ — 540 МЕ/л, ГГТ — 230 МЕ/л. Повышения уровня билирубина в крови не отмечали. У больных при УЗИ выявляли увеличение печени с диффузными изменениями в паренхиме. В одном случае имели место множественные очаги повышенной эхогеннности с ровными четкими контурами, размерами от 1.5 до 5.5 см в диаметре (рис. 3).
Количество в крови пациентов находилось в пределах от 10 до 50 кл/мм 3.
Поражение печени грибами представляет собой одно из проявлений генерализованного микоза. У двух наблюдаемых нами пациентов (3.4%) патология печени была связана с криптококкозом и характеризовалась большой площадью поражения органа, наличием множества молодых форм криптококка и слабо выраженной воспалительной реакцией. В одном наблюдении (1.7%) имела место генерализованная кандидозная инфекция с гранулематозом и микроабсцессами печени.
Количество у пациентов грибковым поражением печени колебалось в пределах Уровни АсАТ и АлАТ у пациентов были повышены умеренно Уровень билирубина в крови находился в пределах нормы.
Патология печени, обусловленная атипичным микобактериозом, была выявлена у двух больных (3.4%). При гистологических исследованиях в портальных трактах печени выявляли скопления гистиоцитов, в цитоплазме которых при окраске по методу определяли большое количество микобактерий. Количество у больных было менее 50 кл/мм 3 .
Среди патологий, приводящих к поражению печени, нередко встречаются онкологические заболевания [7]. Данную группу составили 11 пациентов (18.6%). У четырех из них была диагностирована висцеральная форма саркомы Капоши с поражением обеих долей печени. Кроме того, имели место холангиоцеллюлярный рак печени с прорастанием стенки желчного пузыря и метастазами в лимфоузлы ворот печени (1 случай), гепатоцеллюлярная карцинома (1), недифференцированный рак печени (1), рак желудка с метастазами в печень (1), рак легкого с метастазами в печень (1), лимфоцитарная лимфосаркома с метастазами в печень (1), лимфогранулематоз с очаговыми и диффузными поражениями печени (1). У одного пациента наблюдали одновременное метастатическое и цитомегаловирусное поражение органа. На аутопсии при раке печени обращало на себя внимание резкое увеличение ее массы, которая находилась в пределах от 2 до 3.5 кг. Клиническая картина, обусловленная поражением печени, у больных онкологическими заболеваниями была более яркой, по сравнению с пациентами иных групп. Имели место желтуха, значительное увеличение и уплотнение печени, болезненность ее при пальпации, носовые кровотечения. Данные симптомы сочетались с лабораторными признаками нарушения печеночных функций (синтеза белков, факторов свертывания крови). У двух больных с раком печени развилась печеночная недостаточность. В тоже время, средние уровни АсАТ и АлАТ у онкологических больных были ниже, чем у пациентов с вторичными инфекциями соответственно, среди патологий, приводящих к поражению печени, нередко встречаются онкологические заболевания [7]. Данную группу составили 11 пациентов (18.6%). У четырех из них была диагностирована висцеральная форма саркомы Капоши с поражением обеих долей печени. Кроме того, имели место холангиоцеллюлярный рак печени с прорастанием стенки желчного пузыря и метастазами в лимфоузлы ворот печени (1 случай), гепатоцеллюлярная карцинома (1), недифференцированный рак печени (1), рак желудка с метастазами в печень (1), рак легкого с метастазами в печень (1), лимфоцитарная лимфосаркома с метастазами в печень (1), лимфогранулематоз с очаговыми и диффузными поражениями печени (1). У одного пациента наблюдали одновременное метастатическое и цитомегаловирусное поражение органа. На аутопсии при раке печени обращало на себя внимание резкое увеличение ее массы, которая находилась в пределах от 2 до 3.5 кг. Клиническая картина, обусловленная поражением печени, у больных онкологическими заболеваниями была более яркой, по сравнению с пациентами иных групп. Имели место желтуха, значительное увеличение и уплотнение печени, болезненность ее при пальпации, носовые кровотечения. Данные симптомы сочетались с лабораторными признаками нарушения печеночных функций (синтеза белков, факторов свертывания крови). У двух больных с раком печени развилась печеночная недостаточность. В тоже время, средние уровни АсАТ и АлАТ у онкологических больных были ниже, чем у пациентов с вторичными инфекциями соответственно, p 3 .
Литература
1. Блохина Н. П. Клинические аспекты гепатита С Вирусные гепатиты, инф. бюллетень, 2001. №2 (12).
2. Канестри В. Г. Комбинированная противовирусная терапия хронического гепатита С у больных Дис. …канд. мед. наук. М.: 2001.
3. Munoz S., Castilio J., Tellez M. et al. Mortality due to hepatopathy in HIV patients European Conference on clinical aspects and treatment of Athens 2001. Book of Abstracts, Abs. p. 275, page 175.
4. Шерлок Ш., Дули Дж. Заболевания печени и желчных путей: Практич. Рук.: Пер. с англ. / Под ред. З. Г. Апросиной, Н. А. Мухина. — М.: Гэотар Медицина, 1999.
5. Dieterich D., Poles M., Lew E. Ganciclovir treatment of gastrointestinal infection caused by CMV in patients with AIDS // Rev. Infect. Dis. 1996. V. 10.
6. Dieterich D., Poles M., Lew E. et al. Results of 452 liver biopsises in patients seropositive for HIV // Hepatology. 1992. V. 98.
7. Кравченко А. В., Рослый И. М., Сереброская Л. В. и др. Этиологическая структура и особенности поражений печени у больных Тер. архив, 1997. Т. 69, №11.
8. Шахгильдян В. И., Шипулина О. Ю., Каражас Н. В. и др. Лабораторная диагностика цитомегаловирусной инфекции пациентов // Эпид. и инф. болезни, 2001. №1.
Резюме
Цель исследования. Определение спектра и частоты поражения печени, клинических, лабораторных и морфологических особенностей печеночной патологии при вторичных заболеваниях у больных
Материалы и методы. С 1991 по 2002 гг. наблюдали 59 больных имевших поражение печени, обусловленное оппортунистическими инфекциями и опухолями. Проводили биохимический анализ крови пациентов, определяли показатели системы иммунитета, исследовали кровь, биопсийные и аутопсийные материалы для выявления ДНК CMV, T. gondii, M. tuberculosis (ПЦР). Проводили пункционную биопсию печени, УЗИ органов брюшной полости. В 57 случаях заболевание закончилось летальным исходом, и характер поражения печени был подтвержден морфологическими исследованиями.
Результаты. Среди всех больных с поражением печени туберкулезная этиология процесса выявлена в 42.4%, ЦМВ — 16.9%, токсоплазменная — 6.8% случаев. У трех пациентов печеночная патология была связана с грибковой инфекцией. Злокачественные опухоли в печени имели место в 18.6% случаев. Клиническая картина, обусловленная патологией печени, у большинства пациентов была стертая и не соответствовала масштабу морфологических изменений в органе, часто обширных, с явлениями фиброза и некроза. Выявляемые при УЗИ очаги в печени наиболее часто имели место у больных ЦМВИ, токсоплазмозом и при наличии злокачественных опухолей в органе. Изменение уровней биохимических параметров крови пациентов было умеренным. У лиц с отмечено значительное повышение активности ГГТ и ЩФ.
Заключение. У больных помимо вирусных гепатитов В, С, D, наиболее часто поражение печени обусловлено туберкулезом, ЦМВИ, токсоплазмозом. Значительная доля в этиологической структуре поражения печени принадлежит онкологическим заболеваниям. Развитие у больного гепатита, не связанного с вирусами В, С, D или приемом лекарственных средств, является критерием генерализованного патологического процесса, свидетельствующего о наличии у пациента поздней стадии со снижением количества менее 100 кл/мм 3 .
Для больных ВИЧ-инфекцией, имеющих глубокие иммунологические нарушения, характерно развитие различных вторичных и оппортунистических заболеваний, которые протекают в генерализованной форме, не имеют в подавляющем большинстве случаев патогномоничных симптомов и нередко сочетаются между собой. Дополнительные методы диагностики, в том числе ультразвуковое исследование (УЗИ), часто являются необходимыми для своевременного установления диагноза заболевания. Проведение УЗИ особенно важно при патологии тех внутренних органов, поражение которых проявляется стертой клинической симптоматикой. При заболеваниях селезенки УЗИ относится к первоочередным методам исследования [1].
Увеличение селезенки без изменения структуры и эхогенности ее паренхимы встречается довольно часто при различных инфекциях, системных заболеваниях, интоксикациях, портальной гипертензии, гемобластозах и не является определяющим симптомом [2, 3]. Напротив, наличие очагов в паренхиме селезенки, определяемое при проведении УЗИ, имеет важное диагностическое значение. Характер очаговых изменений играет большую роль в дифференциальной диагностике инфекционных и онкологических заболеваний.
Цель работы состояла в определении частоты патологических изменений в селезенке, выявленных при сонографическом исследовании, их ультразвуковой характеристики, установлении связи между ними и вторичными заболеваниями у больных
Материалы и методы
Результаты и обсуждение
При проведении ультразвуковых исследований у 731 больного (43% случаев) определяли увеличение селезенки в длину до 12 20 см, ширину 6 10 см, толщину 4 8 см. Корреляции между увеличением размеров органа и стадией а также наличием оппортунистических заболеваний установлено не было.
Помимо увеличения селезенки у большинства больных определяли структурные изменения паренхимы в виде диффузных и очаговых поражений. Диффузные изменения были выявлены у 1190 больных (70% случаев), среди которых 254 человека имели диагноз 3В СПИД (21.3%). Диффузное поражение паренхимы селезенки диагностировали как при увеличении селезенки, так и при ее нормальных размерах. Подобно спленомегалии, данные изменения у ВИЧ-инфицированных пациентов не были специфичны для какой-либо вторичной патологии.
Очаговые поражения паренхимы селезенки были выявлены у 122 больных (7.2% случаев). Пациенты находились в возрасте 15 79 лет (средний возраст составил 32.6 + 4.5 года). Среди больных с очаговыми изменениями в селезенке у 64 человек (52.5% случаев) был поставлен диагноз СПИДа. Очаговые изменения были представлены мелкими и крупными гипоэхогенными очагами, зонами некроза, кальцинатами, кистами, гематомами, метастазами и инфарктом селезенки.
Мелкие гипоэхогенные очаги в паренхиме селезенки были выявлены в 58 случаях, что составило 47.5% от всех очаговых изменений. Подавляющее большинство пациентов (82.8%) находились на стадии СПИДа. Очаги были как единичными, так и множественными. Их контур в большинстве случаев был нечеткий, размеры составляли от 3 до 12 мм. У большей части больных селезенка была увеличена в размерах.
Из 58 больных с мелкими гипоэхогеными очагами в паренхиме селезенки в 37 случаях (63.8%) был диагностирован генерализованный туберкулез (рис. 1). При патоморфолигическом исследовании селезенки данные изменения представляли собой туберкулезные бугорки, очаги казеозного некроза [4]. Выявление патологии селезенки у больного с микобактериальным поражением легких свидетельствовало о генерализации процесса. У подавляющего большинства больных с генерализованным туберкулезом, помимо поражения селезенки, выявляли и увеличение мезентериальных лимфатических узлов, часто со структурными изменениями в виде мелких очагов или гнойно-некротических процессов. Исчезновение соответствующих изменений в селезенке, лимфатических узлах при проведении противотуберкулезной терапии служило свидетельством правильного выбора и эффективности этиотропного лечения.
Вторую группу с мелкоочаговыми изменениями селезенки составили 7 (12.1%) пациентов со злокачествеными лимфомами: лимфогранулематозом (4 человека) и лимфосаркомой (3) (рис.2). Во всех случаях диагноз был подтвержден посмертно. В данной группе больных, как и при туберкулезе, патология селезенки сочеталась с поражением лимфатических узлов. При этом патология касалась, прежде всего, забрюшинных лимфоузлов (чаще парааортальных и подвздошных), которые имели вид крупных конгломератов с измененной структурой, свойственной опухолевому поражению. При дифференциальном диагнозе с микобактериальной инфекцией и проведении противотуберкулезной терапии ex juvantibus данные изменения обратному развитию не подвергались.
В дифференциальном диагностическом ряду больных с мелкоочаговым поражением селезенки существенное место занимает группа пациентов с генерализованной бактериальной инфекцией. Данную группу составили 4 (6.9%) больных с сепсисом, развитие которого было связано с применением внутривенных наркотических препаратов. Все больные страдали в стадии первичных проявлений (2Б 2В). В отличие от предыдущих двух групп существенные изменения со стороны внутрибрюшных лимфоузлов отсутствовали. При эхокардиографии выявляли признаки септического эндокардита.
Последние два года характеризуются существенным увеличением частоты токсоплазмоза у больных в г. Москве [4]. По данным секционных исследований токсоплазмоз входит в тройку (наряду с туберкулезом и цитомегаловирусной инфекцией) наиболее частых вторичных заболеваний, приводящих к летальному исходу у больных Особенностью токсоплазмоза пациентов является генерализованный характер заболевания с поражением не только головного мозга, но и внутренних органов, вовлечение которых в патологический процесс выявляется при инструментальных методах диагностики, прежде всего при проведении УЗИ. В 5 случаях (8.6%) очаговые изменения в селезенки оказались связанными с токсоплазмозом. У четырех больных данной группы заболевание закончилось летальным исходом, и этиология поражения органа была подтверждена патоморфологическими исследованиями. При токсоплазменном поражении селезенки в начале заболевания патологические изменения определяли как единичные мелкие (2 3 мм) гипоэхогенные очаги по периферии селезенки, а в дальнейшем как крупные зоны пониженной эхогенности без четких контуров с мелколинейной эхогенной исчерченностью. На фоне этиотропной терапии изменения в паренхиме органа постепенно исчезали.
В единичных случаях причинами формирования мелких очагов в селезенке больных служили цитомегаловирусная инфекция, саркома Капоши, сифилис, саркоидоз, пневмоцистоз.
Сравнительный анализ размеров, количества, степени эхогенности очагов при различных оппортунистических и вторичных заболеваниях существенных отличий не выявил, но обращало на себя внимание более мелкие размеры очагов и их низкая эхогенность (вплоть до анэхогенных) при поражении селезенки у больных сепсисом. При лимфопролиферативных заболеваниях очаги отличались более крупными размерами.
Среди 122 больных с очагами в селезенки отдельную группу составили 10 случаев (8.2%) крупноочаговых изменений паренхимы селезенки. Данные структурные изменения были выявлены у 7 больных сепсисом и представляли собой участки разрежения структуры пониженной эхогенности с размытыми контурами. При динамическом наблюдении они трансформировались в зоны некроза (размерами 1.5 3.5 см) в виде участков неоднородной структуры с чередованием анэхогеных зон с более эхогенной периферией. В дальнейшем эти участки подверглись обратному развитию и на их месте формировались зоны уплотнения или кальцинаты. Зоны локального некроза в виде крупных очагов неоднородной структуры размерами 2 4 см были выявлены в двух случаях генерализованного туберкулеза. У одного пациента они сочетались с некрозами паренхимы печени и на фоне противотуберкулезной терапии подверглись обратному развитию с формированием мелких кальцинатов. Во втором случае сформировался крупный абсцесс селезенки, что послужило причиной спленэктомии. В одном случае очаг некроза был выявлен у больного сифилисом.
Значительная группа очаговых изменений селезенки была представлена кальцинатами, которые были выявлены у 45 из 122 больных (36.9%). Кальцинаты визуализировались в виде единичных или множественных мелких (3 5 мм) гиперэхогенных образований, иногда с акустической тенью (рис.3). Лишь 7 пациентов этой группы находились на стадии СПИДа (четверо страдали два туберкулезом, один висцеральным кандидозом), остальные больные имели более ранние стадии Корреляции между наличием кальцинатов в селезенке вторичным заболеванием установлено не было.
Кроме выше перечисленного, в группу очаговых изменений в паренхиме селезенки вошли кистозные образования 5 случаев (4.1%). У 3 больных это были типичные кисты и определялись как образование округлой или овальной формы с тонким ободком и анэхогенным содержимым. У двух больных кисты имели приобретенный постравматический генез и характеризовались утолщенными гиперэхогенными стенками, наличием большого количества кальцинатов. Гематомы (2 пациента, 1.6% случаев) были связаны с предшествуюшей травмой и выглядели как эхонегативное образование в самой ткани селезенки и субкапсульно. В 1 случае (0.8%) определяли рубец в зоне инфаркта селезенки, как очаг повышения эхогенности треугольной формы с втяжением в этом месте контура селезенки, в 1 случае (0.8%) метастаз рака желудка в виде гипоэхогенного образования округлой формы с четким контуром.
Выводы
1. По данным ультразвукового исследования изменения селезенки в подавляющем большинстве случаев были представлены увеличением размеров органа и диффузными изменениями паренхимы, имеющими место в 70% случаев среди обследованных больных на разных стадиях
2. Очаговые изменения в паренхиме селезенки были выявлены значительно реже (7.2% случаев), но половина больных имела стадию 3В (СПИД). В подавляющем большинстве случаев (82.8%) структурные изменения в селезенке у больных СПИДом были представлены мелкими гипоэхогенными очагами.
3. Основную группу больных с мелкоочаговыми изменениями в паренхиме селезенки составили пациенты с генерализованным туберкулезом (63.8% случаев). Данная патология также была диагностирована у больных лимфопролиферативными заболеваниями и сепсисом, соответственно, в 12.1% и 6.9% случаев.
4. У ВИЧ-инфицированных больных, страдающих токсоплазмозом, имело место поражение не только головного мозга, но и внутренних органов, в том числе селезенки. При этом ультразвуковая картина была представлена мелкими гипоэхогенными очагами с тенденцией к слиянию по мере развития заболевания.
5. Большую группу очаговых изменений селезенки составили кальцинаты, встречающиеся у больных на разных стадиях Среди больных на стадии СПИДа кальцинаты были выявлены преимущественно у больных манифестной цитомегаловирусной инфекцией и туберкулезом.
Литература
1. Борсуков А. В. // SonoAce International -2001.- №9.
2. Руководство по медицине. Диагностика и терапия / Т. 1.: Пер. с англ./Под ред. Р. Беркоу, Э. Флетчера М.: Мир, 1997. 1045 с.
3. Стручкова Т. Я., Соколов А. И. // Клиническое руководство по ультразвуковой диагностике / Под ред. В. В. Митькова. М.: Видар. 1996. Т.1,
4. Пархоменко Ю. Г., Тишкевич О. А., Шахгильдян В. И. // Архив патологии 2003. №3.
Резюме
Дополнительные методы диагностики, в том числе ультразвуковое исследование, часто являются необходимыми для своевременного установления диагноза заболевания. При патологии селезенки УЗИ относится к первоочередным методам исследования. Цель работы состояла в определении при сонографическом исследовании частоты патологических изменений в селезенке, их ультразвуковой характеристики, установлении связи между ними и вторичными заболеваниями у больных
С 1989 по 2003 гг. были проведены 3320 ультразвуковых исследования органов брюшной полости у 1700 больных, 318 из которых имели стадию 3В (СПИД). Увеличение селезенки было диагностировано у 731 больного (43% случаев). Диффузные изменения в паренхиме имели место у 1190 больных (70% случаев). Корреляции между спленомегалией, диффузными изменениями в селезенке и стадией а также наличием оппортунистических заболеваний установлено не было. Очаговые изменения в паренхиме селезенки были выявлены у 7.2% обследованных больных, половина из них имела стадию 3В (СПИД). В подавляющем большинстве случаев (82.8%) структурные изменения в селезенке у больных СПИДом были представлены мелкими и средними гипоэхогенными очагами. У 63.8% больных с мелкими очагами в паренхиме селезенки был диагностирован генерализованный туберкулез, 12.1% злокачественые лимфомы, 6.9% бактериальный сепсис. В 5 случаях (8.6%) очаговые изменения в селезенке были связанны с токсоплазмозом, что свидетельствовало о генерализованном характере заболевания. Отдельную группу составили 10 случаев крупноочаговых изменений паренхимы органа в виде участков некрозов. Данные структурные изменения были выявлены у 7 больных сепсисом, 2 туберкулезом, 1 сифилисом. Очаговые изменения селезенки в 36.9% случаев были представлены кальцинатами. Среди больных на стадии СПИДа кальцинаты были выявлены преимущественно у больных манифестной цитомегаловирусной инфекцией и туберкулезом. В группу очаговых изменений в паренхиме селезенки также вошли кистозные образования 4.1% случаев, гематомы 1.6%, инфаркт селезенки (0.8%) и метастаз рака желудка 0.8% случаев.
ВИЧ (VIH), или вирус иммунодефицита человека, поражает различные органы организма человека (пищеварительной, нервной и других систем), но преимущественно воздействует на иммунную систему. В результате развития ВИЧ-инфекции иммунная система теряет способность реагировать даже на самые безобидные инфекции, с которыми легко справляется здоровый организм. Формируется синдром приобретенного иммунодефицита, или СПИД (AIDS). По сути, СПИД является терминальной (завершающей) стадией развития ВИЧ-инфекции, как правило, с летальным исходом. При этом смертельно опасным является не сам СПИД или начальное звено в развитии СПИДа, то есть ВИЧ-инфекция, а заболевания, которые развиваются на фоне измененного иммунного статуса, — так называемые оппортунистические заболевания. К ним относятся различные инфекционные, онкологические или аутоиммунные заболевания (заболевания, при которых иммунная система человека воспринимает собственные клетки организма как чужеродные и повреждает их).
Симптомы ВИЧ-инфекции/СПИДа
Первые симптомы ВИЧ-инфекции могут появиться в конце инкубационного периода (через 2 недели — 6 месяцев после заражения) или чуть позже.
У многих людей данный период протекает бессимптомно, или симптомы могут пройти самостоятельно, даже при отсутствии терапии; заболевание в дальнейшем может никак не проявлять себя в течение нескольких лет.
Для острой фазы заболевания характерны:
- повышенная температура тела;
- увеличенные лимфатические узлы (различных групп: паховые, шейные, подмышечные и др.);
- эритрематозная сыпь (покраснение, вызванное расширением капилляров) и макулопаппулезная сыпь (сыпь в виде плотных выпуклых элементов размером до 10 мм — от телесного до фиолетового оттенков) на лице, туловище, конечностях;
- боли в мышцах и суставах;
- возможны диарея (понос), тошнота, рвота;
- возможно увеличение печени и селезенки.
Далее развивается бессимптомная стадия.
Бессимптомная стадия может протекать как при отсутствии клинических симптомов, так и с развитием персистирующей лимфаденопатии (множественного увеличения лимфатических узлов).В исключительных случаях болезнь минует бессимптомную фазу, прогрессирует вплоть до развития терминальной стадии, СПИДа. Бессимптомный период может длиться до нескольких лет.
Для персистирующей лимфаденопатии характерно:
- увеличение, как минимум, двух групп лимфатических узлов (от 1 см ) в течение 3-х месяцев;
- наиболее часто увеличены шейные, затылочные, подмышечные лимфатические узлы;
- увеличение печени, селезенки.
За бессимптомным периодом следует симптоматическая хроническая фаза ВИЧ-инфекции, характеризующаяся развитием различных вирусных, бактериальных, грибковых заболеваний.
Данная фаза является переходной между бессимптомным периодом развития заболевания и СПИДом, в среднем ее длительность составляет 3-7 лет и более.
- повышенная температура тела;
- повышенное потоотделение в ночное время;
- диарея (понос);
- потеря веса.
Как правило, заболевание на данном этапе сопровождается частыми заболеваниями верхних дыхательных путей и ЛОР-инфекциями:
- отитами (воспаление среднего уха);
- синуситами (воспалением носовых пазух);
- трахеитами (воспалением трахеи);
- тонзиллитами (ангинами).
О переходе ВИЧ-инфекции в терминальную (завершающую) стадию, то есть СПИД (синдром приобретенного иммунодефицита), указывает появление заболеваний у больного человека, которые в норме у здоровых людей встречаются достаточно редко. К ним относятся следующие заболевания.
Грибковые поражения легких:
- воспаление легких, вызванное вирусами герпеса или грибками, чаще рода Сandida;
- пневмоцистная пневмония (вызываемая возбудителем Pneumocystis jirovecii). Заболевание часто наблюдается у ВИЧ-инфицированных и остается одним из первых признаков, по которым ставится подозрение на СПИД (наличие ВИЧ-инфекции).
Поверхностные поражения кожи и слизистых.
- Частые эпизоды опоясывающего лишая.
- Различные грибковые заболевания кожи (в основном вызванные грибами рода Candida – отсюда название кандидоз).
Сопровождается образованием белого налета на видимых частях тела и слизистых оболочках, зудом.
На фоне ВИЧ-инфекции грибок часто поражает внутренние органы (пищевод, легкие и даже головной мозг).
Снаружи грибковое поражение имеет нетипичную локализацию (глаза, сфинктер прямой кишки).
Опухолевые процессы, редко встречающиеся у здоровых людей.
Поражения нервной системы.
- Токсоплазменное поражение головного мозга (вызывается одноклеточным паразитом Toxoplasma gondii, который может инфицировать головной мозг, стать причиной развития энцефалита (воспалительного процесса в веществе головного мозга)).
- Криптококковый менингит — инфекционное заболевание, поражающее мозговые оболочки, вызываемое грибом Cryptococcus neoformans. Сопровождается высокой температурой тела, головной болью, усталостью, тошнотой, рвотой, припадками.
- Прогрессивная мультифокальная лейкоэнцефалопатия — заболевание, при котором постепенно разрушается миелиновый слой, покрывающий длинные отростки нервных клеток (аксоны), в результате нарушается проведение нервных импульсов, что может стать причиной развития параличей, нарушения функции слуха, зрения и других тяжелых неврологических нарушений.
Причиной болезни является полиомавирус. Вирус присутствует в организме большинства абсолютно здоровых людей и никак не проявляет себя. Активация вируса происходит на фоне сниженного иммунитета. Человек умирает в течение нескольких месяцев после появления первых симптомов.
Диагностика
Ранняя диагностика ВИЧ-инфекции осложняется тем, что первоначальные симптомы встречаются и при других различных заболеваниях и не являются характерными непосредственно для ВИЧ-инфекции. Тем не менее подозрение на ВИЧ ставится при следующей симптоматике:
Подозрение на ВИЧ-инфекцию возникает при следующих состояниях:
- пневмоцистная пневмония (воспаление легких грибкового характера), грибковое поражение нервной системы и внутренних органов;
- подтвержденная саркома Капоши у лиц моложе 60 лет;
- токсоплазмоз мозга (инфекция мозга, вызванная токсоплазмой);
- опоясывающий герпес у лиц моложе 50 лет.
Лабораторная диагностика.
На начальных этапах болезни антитела к ВИЧ, как правило, не обнаруживаются, потому основным диагностическим методом является ПЦР (полимеразно-цепная реакция) — метод обнаружения РНК вируса.
ИФА (иммуноферментный анализ) на определение антител к ВИЧ. Антитела, как правило, определяются через 3 месяца с момента заражения.
Иммуноблоттинг (метод применяется после положительного результата ИФА). Суть заключается в определении специфических антител к 3-м основным антигенам оболочки вируса.
Осложнения и последствия
По сути, осложнения и последствия ВИЧ-инфекции являются ничем иным, как признаками развития СПИДа.
Читайте также:

