Как вылечить кишечную инфекцию у ребенка без антибиотиков
Обновлено: 24.04.2024
Острые кишечные инфекции (ОКИ) — это большая группа инфекционных заболеваний человека с энтеральным механизмом заражения, вызываемых патогенными и условно-патогенными бактериями, вирусами или простейшими
Острые кишечные инфекции (ОКИ) — это большая группа инфекционных заболеваний человека с энтеральным (фекально-оральным) механизмом заражения, вызываемых патогенными (шигеллы, сальмонеллы и др.) и условно-патогенными бактериями (протеи, клебсиеллы, клостридии и др.), вирусами (рота-, астро-, адено-, калицивирусы) или простейшими (амеба дизентерийная, криптоспоридии, балантидия коли и др.).
Ведущим компонентом терапии ОКИ является рациональное лечебное питание, адаптированное к возрасту ребенка, характеру предшествующего заболевания и вскармливания.
Цель диетотерапии — уменьшение воспалительных изменений в желудочно-кишечном тракте, нормализация функциональной активности и процессов пищеварения, максимальное щажение слизистой оболочки кишечника.
Основные требования к диете при ОКИ:
включение в диеты низко- и безлактозных продуктов и кисломолочных продуктов, обогащенных бифидо- и лактобактериями;
снижение объема пищи в первые дни болезни на 15–20% (при тяжелых формах до 50%) от физиологической потребности;
Из диеты исключаются стимуляторы перистальтики кишечника, продукты и блюда, усиливающие процессы брожения и гниения в кишечнике: сырые, кислые ягоды и фрукты, соки, сырые овощи, сливочное и растительные масла (в чистом виде), сладости, свежая выпечка. Не следует давать бобовые, свеклу, огурцы, квашеную капусту, редис, апельсины, груши, мандарины, сливы, виноград. Не рекомендуется овсяная крупа, так как она усиливает бродильные процессы. Должны быть исключены из питания жирные сорта мясных и рыбных продуктов (свинина, баранина, гусь, утка, лосось и др.).
Цельное молоко в остром периоде кишечных инфекций назначать не следует, так как оно усиливает перистальтику кишечника и бродильные процессы в результате нарушения расщепления молочного сахара (лактозы), что сопровождается усилением водянистой диареи и вздутием живота.
В первые дни заболевания исключается также черный хлеб, способствующий усилению перистальтики кишечника и учащению стула.
При уменьшении проявлений интоксикации, прекращении рвоты и улучшении аппетита вводится творог, мясо (говядина, телятина, индейка, кролик в виде котлет, фрикаделек, кнелей), рыба нежирных сортов, яичный желток и паровой омлет. Разрешаются тонко нарезанные сухари из белого хлеба, каши на воде (кроме пшенной и перловой), супы слизистые, крупяные с разваренной вермишелью на слабом мясном бульоне.
В остром периоде заболевания рекомендуется использовать молочнокислые продукты (кефир, ацидофильные смеси и др.). Молочнокислые продукты за счет активного действия содержащихся в них лактобактерий, бифидобактерий, конечных продуктов протеолиза казеина (аминокислот и пептидов, глутаминовой кислоты, треонина и др.), увеличенного количества витаминов В, С и др. способствуют улучшению процессов пищеварения и усвоению пищи, оказывают стимулирующее влияние на секреторную и моторную функции кишечника, улучшают усвоение азота, солей кальция и жира. Кроме того, кефир обладает антитоксическим и бактерицидным действием на патогенную и условно-патогенную флору за счет наличия молочной кислоты и лактобактерий. Однако длительное применение только кефира или других молочнокислых смесей нецелесообразно, поскольку эти продукты бедны белками и жирами. Лечебным кисломолочным продуктом является Лактофидус — низколактозный продукт, обогащенный бифидобактериями.
При лечении детей с ОКИ в периоде выздоровления необходимо широко использовать плодово-овощные продукты (яблоки, морковь, картофель и др.), так как они содержат большое количество пектина. Пектин — коллоид, обладающий способностью связывать воду и набухать, образуя пенистую массу, которая, проходя по кишечному тракту, адсорбирует остатки пищевых веществ, бактерий, токсических продуктов. В кислой среде от пектина легко отщепляется кальций, оказывая противовоспалительное действие на слизистую оболочку кишечника. Фрукты и овощи содержат органические кислоты, обладающие бактерицидным действием, а также большое количество витаминов, глюкозу, фруктозу, каротин и др. Применение вареных овощей и печеных фруктов уже в остром периоде кишечных инфекций способствует более быстрому исчезновению интоксикации, нормализации стула и выздоровлению.
Питание детей грудного возраста
В последнее время в клинике кишечных инфекций предпочтение отдается назначению детям, находящимся на искусственном вскармливании, низко- и безлактозных смесей (Низколактозный Нутрилон, Фрисопеп, Хумана ЛП+СЦТ, соевые смеси). При тяжелых формах ОКИ и развитии гипотрофии широко используются гидролизованные смеси (Нутрилон Пепти ТСЦ, Нутримиген, Алфаре, Прегестимил и др.), способствующие быстрому восстановлению процессов секреции и всасывания в кишечнике и усвоению белков, жиров и углеводов, что предупреждает развитие ферментопатии в исходе кишечной инфекции (табл).
По нашим данным, в результате клинико-лабораторной оценки влияния низколактозных смесей на клиническую картину и состояние микробиоценоза кишечника при вирусных диареях у детей раннего возраста был получен положительный эффект стимуляции функциональной активности нормальной и, в первую очередь, сахаролитической микрофлоры (по стабилизации показателей уксусной, масляной и пропионовой кислот), а также регулирующее влияние на процессы метаболизма углеводов и жиров в острый период заболевания. Клинический эффект заключался в быстром и стойком купировании основных проявлений болезни: рвоты, диареи, абдоминального синдрома и эксикоза, что наряду с хорошей переносимостью позволило рекомендовать низколактозные смеси для использования в качестве лечебного питания у детей раннего возраста в острый период кишечных инфекций вирусной этиологии.
При разгрузке в питании ежедневно объем пищи увеличивается на 20–30 мл на одно кормление и соответственно изменяется кратность кормлений, то есть увеличивается интервал между кормлениями. При положительной динамике заболеваний и улучшении аппетита необходимо довести суточный объем пищи до физиологической потребности не позднее 3–5 дня от начала лечения.
Детям 5–6 месяцев при улучшении состояния и положительной динамике со стороны желудочно-кишечного тракта назначается прикорм кашей, приготовленной из рисовой, манной, гречневой круп на половинном молоке (или воде при ротавирусной инфекции). Кашу назначают в количестве 50–100–150 г в зависимости от возраста ребенка и способа вскармливания до заболевания. Через несколько дней добавляют к этому прикорму 10–20 г творога, приготовленного из кипяченого молока, а затем — овощные пюре, ягодный или фруктовый кисель в количестве 50–100–150 мл, соки.
Питание детей 7–8 месяцев должно быть более разнообразным. При улучшении состояния им назначают не только каши, творог и кисели, но и овощные пюре, желток куриного яйца на 1/2 или 1/4 части, затем бульоны, овощной суп и мясной фарш. В каши и овощное пюре разрешается добавлять сливочное масло. Желток (яйцо должно быть сварено вкрутую) можно давать отдельно или добавлять его в кашу, овощное пюре, суп.
Питание детей старше года строится по такому же принципу, как и у детей грудного возраста. Увеличивается лишь разовый объем пищи и быстрее включаются в рацион продукты, рекомендуемые для питания здоровых детей этого возраста. В остром периоде болезни, особенно при наличии частой рвоты, следует провести разгрузку в питании. В первый день ребенку назначают кефир по 100–150–200 мл (в зависимости от возраста) через 3–3,5 часа. Затем переходят на питание, соответствующее возрасту, но с исключением запрещенных продуктов. В остром периоде заболевания всю пищу дают в протертом виде, применяется паровое приготовление вторых блюд. Крупу для приготовления каши и гарнира, овощи разваривают до мягкости. Набор продуктов должен быть разнообразным и содержать кисломолочные смеси, кефир, творог, сливки, сливочное масло, супы, мясо, рыбу, яйца, картофель, свежие овощи и фрукты. Можно пользоваться овощными и фруктовыми консервами для детского питания. Из рациона исключают продукты, богатые клетчаткой и вызывающие метеоризм (бобовые, свекла, репа, ржаной хлеб, огурцы и др.). Рекомендуются арбузы, черника, лимоны, кисели из различных ягод, желе, компоты, муссы, в которые желательно добавлять свежевыделенный сок из клюквы, лимона.
Правильно организованное питание ребенка с кишечной инфекцией с первых дней заболевания является одним из основных условий гладкого течения заболевания и быстрого выздоровления. Неадекватное питание и погрешности в диете могут ухудшить состояние ребенка, равно как и длительные ограничения в питании. Важно помнить, что на всех этапах лечения ОКИ необходимо стремиться к полноценному физиологическому питанию с учетом возраста и функционального состояния желудочно-кишечного тракта ребенка.
Значительные трудности в диетотерапии возникают у детей с развитием постинфекционной ферментопатии, которая развивается в разные сроки заболевания и характеризуется нарушением переваривания и всасывания пищи вследствие недостатка ферментов.
При ОКИ, особенно при сальмонеллезе, кампилобактериозе, протекающих с реактивным панкреатитом, наблюдается нарушение всасывания жира и появление стеатореи — стул обильный с блеском, светло-серый с неприятным запахом. Диетотерапия при стеаторее проводится с ограничением жира в рационе, но не более 3–4 мг/кг массы тела в сутки для детей первого года жизни. Это достигается путем замены части молочных продуктов специализированными низкожировыми продуктами (Ацидолакт) и смесями зарубежного производства, в состав которых в качестве жирового компонента входят среднецепочечные триглицериды, практически не нуждающиеся в панкреатической липазе для усвоения (Нутрилон Пепти ТСЦ, Хумана ЛП+СЦТ, Алфаре, Прегестимил, Фрисопеп и др.). При появлении признаков острого панкреатита из рациона исключают свежие фрукты, ягоды, овощи, концентрированные фруктовые соки на срок до 1 мес.
При лактазной недостаточности рекомендуется использование адаптированных низколактозных смесей (Низколактозный Нутрилон, Фрисопеп, Хумана ЛП+СЦТ и др.) или соевых смесей (Нутрилон Соя, Фрисосой, Хумана СЛ, Симилак Изомил, Энфамил Соя и др.). При их отсутствии — 3-суточный кефир; детям первых трех месяцев жизни можно давать смесь типа В-кефир, состоящую из 1/3 рисового отвара и 2/3 3-суточного кефира с добавлением 5% сахара (глюкозы, фруктозы), 10% каши на воде, овощных отварах.
В качестве прикорма этим больным дают безмолочные каши и овощные пюре на воде с растительным или сливочным маслом, отмытый от сыворотки творог, мясное пюре, печеное яблоко. Схемы введения прикормов могут быть индивидуализированы, следует обратить внимание на раннее назначение мясного (суточная доза в 3–4 приема). Избегают применения сладких фруктовых соков, продуктов, повышающих газообразование в кишечнике и усиливающих перистальтику (ржаной хлеб, белокочанная капуста, свекла и другие овощи с грубой клетчаткой, кожура фруктов, чернослив, сухофрукты). Длительность соблюдения низколактозной диеты индивидуальна — от 1,5–2 до 6 месяцев.
После тяжелых кишечных инфекций может возникнуть непереносимость не только лактозы, но и других дисахаридов, реже — полная углеводная интолерантность (глюкозо-галактозная мальабсорбция), при которой у больных отмечается выраженная диарея, усиливающаяся при применении смесей и продуктов, содержащих дисахариды, моносахариды и крахмал (молочные и соевые смеси, крупы и практически все фрукты и овощи). Это чрезвычайно тяжелое состояние, приводящее к обезвоживанию и прогрессирующей дистрофии, требует строгого безуглеводного питания и парентерального введения глюкозы или полного парентерального питания. В отдельных случаях возможно пероральное введение фруктозы. При индивидуальной переносимости в диете сохраняются белок и жиросодержащие продукты: нежирное мясо — индейка, конина, говядина, кролик, растительное масло, ограниченный ассортимент овощей с низким содержанием сахарозы и глюкозы — цветная и брюссельская капуста, шпинат, стручковая фасоль, салат.
Дефицит белка возникает за счет нарушения утилизации, всасывания либо за счет потери эндогенного белка, особенно у детей с исходной гипотрофией. Коррекция потерь белка проводится путем назначения гидролизованных смесей (Нутрилон Пепти ТСЦ, Нутримиген, Алфаре, Прегестимил, Фрисопеп и др.).
При длительных постинфекционных диареях, особенно у детей, получавших повторные курсы антибактериальных препаратов, возможно развитие вторичной пищевой аллергии, сопровождающейся сенсибилизацией к белкам коровьего молока, реже — к яичному протеину, белкам злаковых культур. Такие нарушения могут возникать не только у детей с аллергическим диатезом, но и у больных без отягощенного преморбидного фона. Клинически постинфекционная пищевая аллергия проявляется гиперчувствительностью к ранее хорошо переносимым продуктам — молочным смесям, молочным кашам, творогу и др. У детей отмечаются боли в животе, вздутие после кормления, срыгивания, жидкий стул с мутной стекловидной слизью, иногда с прожилками крови, при копрологическом исследовании в кале обнаруживаются эозинофилы. Характерна остановка прибавки массы тела, вплоть до развития гипотрофии.
При выявлении аллергии к белкам коровьего молока в питании детей первого года жизни используются смеси на соевой основе (Нутрилак Соя, Нутрилон Соя, Фрисосой, Хумана СЛ, Энфамил Соя и др.) и на основе гидролизатов белка (Нутрилон Пепти ТСЦ, Нутримиген, Прегестимил, Фрисопеп и др.).
Отсутствие специализированных продуктов не является непреодолимым препятствием в организации безмолочного рациона. Элиминационная диета в этом случае составляется на основе безмолочных протертых каш (рисовой, гречневой, кукурузной), фруктовых и овощных пюре, картофеля, кабачков, цветной капусты, тыквы, из печеного яблока, банана, растительного и сливочного масла, мясного пюре. При этом необходимо учитывать физиологические потребности ребенка в основных пищевых веществах и энергии. Мясное пюре, как основной источник белка, при отсутствии специализированных смесей можно назначать с 2–3-месячного возраста. Предпочтительно использовать конину, мясо кролика, птицы, постную свинину, а также диетические мясные консервы — Конек-Горбунок, Чебурашка, Петушок, Пюре из свинины и др.
У детей старше года принцип составления рациона тот же. При назначении безмолочной диеты необходимо полностью компенсировать недостающее количество животного белка протеинами мяса, соевых смесей, а также исключить из диеты продукты, обладающие повышенной сенсибилизирующей активностью (шоколад, рыба, цитрусовые, морковь, свекла, красные яблоки, абрикосы и другие плоды оранжевой или красной окраски, орехи, мед). При постинфекционной пищевой аллергии срок соблюдения указанной диеты составляет не менее 3 месяцев, а чаще — от 6 до 12 месяцев. Эффект от элиминационной диеты оценивается по исчезновению симптомов заболевания, прибавке массы тела, нормализации стула.
Л. Н. Мазанкова, доктор медицинских наук, профессор Н. О. Ильина, кандидат медицинских наук Л. В. Бегиашвили РМАПО, Москва
Острая кишечная инфекция (ОКИ) — это инфекционное воспаление желудка и кишечника, которое проявляется диареей (жидкий стул более 3 раз в сутки), иногда тошнотой, рвотой и повышением температуры тела. Примерно в 80% случаев кишечная инфекция вызывается вирусами (очень часто это ротавирус), то есть применение антибиотиков не будет иметь никакого эффекта.
Чего нужно бояться при кишечной инфекции и как не попасть в больницу
Самое опасное для ребенка с поносом и рвотой — обезвоживание. Именно из-за него приходится госпитализировать ребенка, если родители не смогли его отпоить. Как этого не допустить, мы с вами очень подробно разберем ниже.
Что мне делать, если мой ребенок заболел ОКИ?
Чаще всего нетяжелые кишечные инфекции можно лечить в домашних условиях. При появлении симптомов заболевания желательно связаться со своим врачом и предупредить его, что ваш ребенок заболел, и подробно описать всю ситуацию. Диарея и рвота (плюс еще и повышение температуры) — это потеря воды и солей, а значит, первое и основное, что должны сделать родители — восполнить уже имеющиеся потери и постоянно компенсировать то, что будет теряться дальше.
Сколько давать жидкости?
В среднем для отпаивания ребенка при острой кишечной инфекции нужно примерно 100 мл на каждый килограмм массы тела (1000 мл для малыша весом 10 кг), но может понадобиться и больше. Чтобы было более удобно, вам нужно следить за тем, чтобы у ребенка была влажная кожа и писал он примерно раз в три часа. Если писаете реже – значит, недоработали, давайте больше пить, пока мочеиспускания не участятся.
Чем отпаивать?
Чем кормить?
Пока у ребенка рвота, ему вообще нет смысла давать еду — только жидкость. Когда рвота прекратится, то параллельно с отпаиванием вы можете предлагать уже и еду, но строго по аппетиту! Не нужно кормить насильно — это только вызовет рвоту и усилит понос. Дети на грудном вскармливании прекрасно обходятся грудным молоком + солевые растворы или компот при необходимости. Более старшие дети могут начинать с легко усваиваемых продуктов: фруктовые кисели, сухари с чаем, галетное печенье, рисовая каша (с компотом, например), супы не на бульоне.
Основное правило — давайте часто, но понемногу. Через день-два уже можно возвращаться к прежним продуктам (тому, что ел до болезни), исключив на некоторое время жареное, жирное и острое.
Какое еще лечение эффективно при кишечной инфекции?
Всемирная организация здравоохранения и другие крупные медицинские организации рекомендуют помимо восполнения жидкости и продолжения кормления принимать препараты цинка. Многочисленные исследования показали, что прием препаратов цинка (10–20 мг в сутки вплоть до прекращения диареи) существенно снижает тяжесть и продолжительность диареи у детей младше 5 лет. В настоящее время на основании проведенных исследований рекомендуется вводить цинк (10–20 мг/день) в рацион всех детей с диареей в течение 10–14 дней.
Также вы много слышали о пробиотиках. Доказано, что пробиотики снижают длительность диареи у детей на фоне кишечной инфекции в среднем на 24 часа. Это все, на что вы можете рассчитывать.
Можно ли детям назначать противодиарейный препарат лоперамид?
Нет. Это лекарство запрещено для применения детям в связи с риском развития угрожающих жизни побочных эффектов.
Если почти 80 % всех кишечных инфекций вызываются вирусами, значит, будут очень полезны противовирусные препараты?
А когда нужно давать антибиотики?
Антибиотики при острых кишечных инфекциях показаны довольно редко, в основном это так называемые инвазивные диареи, когда в кале появляется кровь. Еще их применяют в случае заболевания холерой, а также внекишечными бактериальными инфекциями, которые приводят к развитию диареи (пневмония, средний отит и т. д.). Как вы уже поняли, примерно в 80 % всех случаев кишечных инфекций антибиотики назначаются зря. И это как минимум.
Я не хочу, чтобы мой ребенок заболел. Как предотвратить это?
Как все запутано! А можно на примере объяснить, как же все-таки правильно лечить острую кишечную инфекцию?
А если у ребенка поднимается температура?
Вы можете дать жаропонижающий препарат для облегчения состояния — ибупрофен или парацетамол в обычной дозировке. Подробнее о лихорадке и методах борьбы с ней можете почитать Правда и мифы о лихорадке.
Малыш отказывается пить. Как поступить?
Сколько будет длиться этот понос?
В большинстве случаев самая острая фаза диареи прекращается за 5–7, реже — 9 дней. После этого у ребенка может оставаться на некоторое время жидковатый неоформленный стул, пока не восстановится кишечник, но это уже не профузный понос 10–20 раз за сутки.
Когда нужно немедленно обращаться к врачу?
По большому счету, в двух ситуациях:
1) если у ребенка в кале появилась кровь. Появление крови в кале говорит о поражении толстого кишечника, что чаще всего бывает при бактериальных кишечных инфекциях, — в таком случае может понадобиться антибиотик;
2) если вы не справились с отпаиванием, то есть, вопреки всем вашим стараниям, у ребенка кожа стала сухой и он не писал в течение 6 часов (у грудных детей памперс сухой на протяжении 6 часов), вам нужно обратиться за медицинской помощью, поскольку, скорее всего, понадобится внутривенное восполнение жидкости.
опубликовано 02/05/2016 16:26
обновлено 03/03/2019
— Инфекционные болезни
Тем не менее человека, ни разу не болевшего кишечной инфекцией, просто не существует. Не существует хотя бы потому, что имеется множество способов нейтрализации всех многочисленных защитных сил — глотать, не пережевывая, чтобы слюна не успела до микробов добраться, переедать, нейтрализовать щелочными напитками кислый желудочный сок, убивать собственных микробов антибиотиками и т. д.
Но наиглавнейшей причиной кишечных инфекций было, есть и будет несоблюдение элементарных гигиенических норм — неправильное хранение пищевых продуктов, немытые руки, снующие между обеденным столом и туалетом мухи. В конце концов, какими бы замечательными защитными силами человеческий организм ни обладал, всегда найдется такое количество микробов, нейтрализовать которое просто невозможно.
Возбудителями кишечных инфекций могут быть бактерии (дизентерийная палочка, сальмонелла, стафилококк, палочка брюшного тифа, вибрион холеры) и некоторые вирусы.
Конкретное имя конкретного возбудителя конкретной кишечной инфекции интересует, прежде всего, медицинских работников. Объем, направленность и интенсивность противоэпидемических мероприятий во многом определяется именно видом возбудителя.
Одни бактерии распространяются через воду, другие — через продукты питания, причем продукты эти не какие угодно, а совершенно определенные. В одном случае — овощи, в другом — яйца, в третьем — молочные продукты и т. д.
Одни бактерии очень(!) заразны (например возбудитель холеры), другие — поменьше.
В одном случае заболевание развивается стремительно и представляет собой реальную угрозу человеческой жизни, в другом — симптомы развиваются медленно, а сама болезнь не особенно опасна.
Микробы, возбудители кишечных инфекций, могут (как правило, так оно и происходит) поражать не весь желудочно-кишечный тракт, а определенные его отделы. Воспалительный процесс в каждом таком отделе имеет свое медицинское название: воспаление желудка — ГАСТРИТ, двенадцатиперстной кишки — ДУОДЕНИТ, тонкого кишечника — ЭНТЕРИТ, толстого кишечника — КОЛИТ.
После проникновения в человеческий организм возбудители кишечных инфекций начинают активно размножаться, что приводит, во-первых, к нарушениям процесса пищеварения и, во-вторых, к воспалению клеток слизистой оболочки кишечника. Типичным и наиболее характерным следствием двух указанных процессов является основной симптом любой кишечной инфекции — понос[1]. Другие признаки болезни — тошнота, рвота, боли в животе, повышение температуры тела, отсутствие аппетита, общая слабость — встречаются часто, но обязательными спутниками кишечной инфекции не являются.
Кстати, следует отметить, что на бытовом и на медицинском уровне понятия кишечной инфекции весьма разнятся. Для обычного человека ясно: раз есть понос, значит, и кишечная инфекция есть, а для врача главное не симптомы, а путь заражения. С медицинских позиций, любая болезнь, передающаяся через рот (с пищей, водой, немытыми руками — так называемый фекально-оральный путь инфицирования), является типичной кишечной инфекцией. Наиболее показательный пример — вирусный гепатит А (болезнь Боткина). Заражение вирусом всегда происходит при его попадании в желудочно-кишечный тракт, но поражается печень, а никакого поноса в большинстве случаев нет.
Пути профилактики кишечных инфекций достаточно очевидны и сводятся к соблюдению элементарных гигиенических норм: мытью рук, особенно тщательно после посещения туалета, термической обработке пищи и воды, выполнению правил хранения пищевых продуктов, изоляции больных и, как минимум, обязательному выделению им отдельной посуды.
Всегда следует помнить, что наиболее страшным и опасным последствием любого поноса является потеря организмом жидкости и солей. Без пищи человеческий организм более или менее благополучно может просуществовать пару недель, но без адекватного обеспечения водой и солями калия, натрия, кальция человек жить не может: в этом случае счет идет на часы.
Запасы воды и солей особенно невелики в организме ребенка, и именно для детей кишечные инфекции представляют собой реальную угрозу здоровью и жизни.
Таким образом, истинная тяжесть кишечной инфекции зачастую определяется не частотой стула, не запахом и цветом испражнений, а именно степенью обезвоживания. Определить тяжесть кишечной инфекции может только врач, но вероятность того, что по поводу каждого поноса люди будут обращаться за медицинской помощью, очень невелика. Поэтому подчеркнем, что вне зависимости от того, как называется конкретная кишечная инфекция, существуют совершенно определенные правила поведения больного и его родственников.
- Всегда следует задуматься над тем, что это вы такое съели или чем накормили ребенка. Полбеды, если это ваш личный кулинарный шедевр, но если это пирожное из близлежащего магазина, то следует проявить сознательность и подумать о тех, кто может пойти по вашим следам. Узнать телефон районной санитарной станции совсем не трудно.
- Кишечная инфекция у любого члена семьи — сигнал тревоги для всех остальных. Больному — отдельная посуда, всем остальным — организовать идеальную чистоту, тщательно мыть руки, убрать от греха подальше подозрительные продукты, всю посуду перекипятить, не жалеть дезинфицирующих средств.
- И понос, и рвота являются способами защиты организма. В упрощенном варианте это выглядит так: в желудочно-кишечный тракт попало что-то не то, и организм всеми возможными способами пытается эту гадость удалить. Поэтому в первые часы кишечной инфекции мы вовсе не заинтересованы в том, чтобы понос и рвота прекратились. Наоборот, в обоих направлениях организму следует помогать — пить и рвать (а если не хочется — сознательно вызывать рвоту, промывая тем самым желудок), очистить толстый кишечник с помощью клизмы. Для клизмы используется обычная кипяченая вода, ни в коем случае не теплая (оптимальная температура около 20 °С), обязательно следить за тем, чтобы вышла вся введенная жидкость.
- Главный принцип помощи — восполнение потерь жидкости и солей. Для этой цели идеально подходят лекарственные средства, имеющиеся в любой аптеке и представляющие собой заранее приготовленную смесь различных солей, которую перед употреблением разводят кипяченой водой. Если же аптека далеко, вполне подойдут минеральные воды, отвары изюма, трав, шиповника, компот из сухофруктов, можно чай, лучше зеленый, чем черный. В конце концов, лучше пить то, что есть под рукой, чем не пить ничего.
- Температура напитков ориентировочно должна быть равна температуре тела — при этом всасывание жидкости из желудка в кровь будет максимально быстрым.
- При упорно повторяющейся рвоте помните, чтонадо пить чаще, но малыми порциями, чтобы не растягивался желудок, а использование любых противорвотных препаратов всегда согласовывать с врачом.
- По большому счету, существует лишь два абсолютно безопасных способа самостоятельного лечения кишечных инфекций — голод и обильное питье. Любые лекарственные препараты могут привести к самым неожиданным последствиям, ну разве что кишечные сорбенты[2] целесообразны и показаны практически всегда.
- Интенсивность ваших волнений должна быть теснейшим образом связана с общим состоянием ребенка, а не с тем, сколько раз он запачкал пеленки (попросился на горшок, сбегал в туалет). Следите за цветом мочи: если она светлая — дефицита жидкости нет.
- Обращение к врачу обязательно при поносе у детей первого года жизни и, вне зависимости от возраста, при отсутствии тенденции к улучшению в течение суток.
10. Немедленно обращайтесь за медицинской помощью, если:
- наиболее волнующим симптомом кишечной инфекции является боль в животе;
- из-за упорной рвоты вы не можете ребенка напоить;
- более 6 часов нет мочи;
- сухой язык,запавшие глаза, кожа приобрела сероватый оттенок;
- в кале имеется примесь крови;
- понос прекратился, но при этом усилилась рвота, и (или) резко поднялась температура тела, и (или) появились боли в животе.
11. При улучшении состояния не торопитесь скармливать детенышу все подряд. Чай с нежирным творожком, рисовая и овсяная кашки — пусть потерпит-поголодает сутки-двое, здоровее будет.
Следует отметить: современная терапия кишечных инфекций вовсе не предусматривает глотание всеми любимых фталазола и левомицетина хотя бы потому, что причиной каждого второго поноса являются вирусы[3], на которых упомянутые антибактериальные препараты не действуют вообще. Но даже если это бактерия, отношение к использованию антибактериальных препаратов неоднозначно. Так, при дизентерии антибиотики используются практически всегда, а при сальмонеллезе — значительно реже.
Парадоксальность лечения кишечных инфекций состоит прежде всего в том, что строгая диета, восполнение потерь жидкости и солей да плюс время и терпение — это почти всегда достаточные условия для выздоровления (соблюдение при этом правил гигиены подразумевается).
Тем не менее с грустью приходится признавать, что, несмотря на теоретическую логичность и привлекательность, практическое применение и эубиотиков, и бактериофагов вовсе не приводит к выздоровлению быстрее, нежели все те же диета да питье.
Неудивительно, что в подавляющем большинстве стран мира эти лекарственные средства не применяются (и не выпускаются, и не регистрируются), поскольку доказать их эффективность медицинская наука пока еще не в состоянии[4].
В стационаре основным способом оказания неотложной помощи при кишечных инфекциях является инфузионная терапия, т. е. внутривенное введение жидкости и солей для быстрого возмещения потерь.
При самой опасной кишечной инфекции — холере — инфузионная терапия вообще является наиглавнейшей. Возбудитель холеры вырабатывает экзотоксин (он называется холероген), который находится в просвете кишечника, и его в этой связи не удается нейтрализовать сывороткой. Под действием холерогена клетки слизистой оболочки кишечника как бы сморщиваются и теряют жидкость литрами! Вот и приходится в огромных количествах вводить препараты внутривенно и проводить очень активное лечение до тех пор, пока в организме не появятся антитела к токсину.
[2] Кишечные сорбенты — многочисленная группа лекарственных препаратов, способных связывать (сорбировать) и обезвреживать яды (токсины), находящиеся в просвете кишечника. Самым известным кишечным сорбентом является знаменитый активированный уголь, хотя есть и другие препараты, в десятки и сотни раз более активные.
[3] Самым известным вирусом, вызывающим у детей тяжелейшие кишечные инфекции, является так называемый ротавирус, чаще всего поражающий малышей первых двух лет жизни. Неудивительно в этой связи, что вакцинация от ротавирусной инфекции присутствует в календаре прививок многих стран мира.
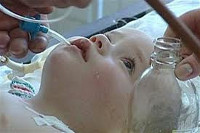
Кишечная инфекция у детей – группа инфекционных заболеваний различной этиологии, протекающих с преимущественным поражением пищеварительного тракта, токсической реакцией и обезвоживанием организма. У детей кишечная инфекция проявляется повышением температуры тела, вялостью, отсутствием аппетита, болями в животе, рвотой, диареей. Диагностика кишечной инфекции у детей основана на клинико-лабораторных данных (анамнезе, симптоматике, выделении возбудителя в испражнениях, обнаружении специфических антител в крови). При кишечной инфекции у детей назначаются антимикробные препараты, бактериофаги, энтеросорбенты; в период лечения важно соблюдение диеты и проведение регидратации.
Общие сведения
Кишечная инфекция у детей – острые бактериальные и вирусные инфекционные заболевания, сопровождающиеся кишечным синдромом, интоксикацией и дегидратацией. В структуре инфекционной заболеваемости в педиатрии кишечные инфекции у детей занимают второе место после ОРВИ. Восприимчивость к кишечной инфекции у детей в 2,5-3 раза выше, чем у взрослых. Около половины случаев кишечной инфекции у детей приходится на ранний возраст (до 3 лет). Кишечная инфекция у ребенка раннего возраста протекает тяжелее, может сопровождаться гипотрофией, развитием дисбактериоза и ферментативной недостаточности, снижением иммунитета. Частое повторение эпизодов инфекции вызывает нарушение физического и нервно-психического развития детей.

Причины
Спектр возбудителей кишечных инфекций у детей крайне широк. Наиболее часто патогенами выступают грамотрицательные энтеробактерии (шигеллы, сальмонеллы, кампилобактеры, эшерихии, иерсинии) и условно-патогенная флора (клебсиеллы, клостридии, протей, стафилококки и др.). Кроме этого, встречаются кишечные инфекции, вызываемые вирусными возбудителями (ротавирусами, энтеровирусами, аденовирусами), простейшими (лямблиями, амебами, кокцидиями), грибами. Общими свойствами всех возбудителей, обусловливающих развитие клинических проявлений, являются энтеропатогенность, способность к синтезу эндо- и экзотоксинов.
Заражение детей кишечными инфекциями происходит посредством фекально-орального механизма алиментарным (через пищу), водным, контактно-бытовым путями (через посуду, грязные руки, игрушки, предметы обихода и т. д.). У ослабленных детей с низкой иммунологической реактивностью возможно эндогенное инфицирование условно-патогенными бактериями. Источником ОКИ может выступать носитель, больной со стертой или манифестной формой заболевания, домашние животные. В развитии кишечной инфекции у детей большую роль играет нарушение правил приготовления и хранения пищи, допуск на детские кухни лиц-носителей инфекции, больных тонзиллитом, фурункулезом, стрептодермией и пр.
Наиболее часто регистрируются спорадические случаи кишечной инфекции у детей, хотя при пищевом или водном пути инфицирования возможны групповые и даже эпидемические вспышки. Подъем заболеваемости некоторыми кишечными инфекциями у детей имеет сезонную зависимость: так, дизентерия чаще возникает летом и осенью, ротавирусная инфекция - зимой.
Распространенность кишечных инфекций среди детей обусловлена эпидемиологическими особенностями (высокой распространенностью и контагиозностью возбудителей, их высокой устойчивостью к факторам внешней среды), анатомо-физиологическими особенностями пищеварительной системы ребенка (низкой кислотностью желудочного сока), несовершенством защитных механизмов (низкой концентрацией IgA). Заболеваемости детей острой кишечной инфекцией способствует нарушение нормальной микробиоты кишечника, несоблюдение правил личной гигиены, плохие санитарно-гигиенические условия жизни.
Классификация
По клинико-этиологическому принципу среди кишечных инфекций, наиболее часто регистрируемых в детской популяции, выделяют шигеллез (дизентерию), сальмонеллез, коли-инфекцию (эшерихиозы), иерсиниоз, кампилобактериоз, криптоспоридиоз, ротавирусную инфекцию, стафилококковую кишечную инфекцию и др.
По тяжести и особенностям симптоматики течение кишечной инфекции у детей может быть типичным (легким, средней тяжести, тяжелым) и атипичным (стертым, гипертоксическим). Выраженность клиники оценивается по степени поражения ЖКТ, обезвоживания и интоксикации.
Характер местных проявлений при кишечной инфекции у детей зависит от поражения того или иного отдела ЖКТ, в связи с чем выделяют гастриты, энтериты, колиты, гастроэнтериты, гастроэнтероколиты, энтероколиты. Кроме локализованных форм, у грудных и ослабленных детей могут развиваться генерализованные формы инфекции с распространением возбудителя за пределы пищеварительного тракта.
В течении кишечной инфекции у детей выделяют острую (до 1,5 месяцев), затяжную (свыше 1,5 месяцев) и хроническую (свыше 5-6 месяцев) фазы.
Симптомы у детей
Дизентерия у детей
После непродолжительного инкубационного периода (1-7 суток) остро повышается температура (до 39-40° C), нарастает слабость и разбитость, снижается аппетит, возможна рвота. На фоне лихорадки отмечается головная боль, ознобы, иногда – бред, судороги, потеря сознания. Кишечная инфекция у детей сопровождается схваткообразными болями в животе с локализацией в левой подвздошной области, явлениями дистального колита (болезненностью и спазмом сигмовидной кишки, тенезмами с выпадением прямой кишки), симптомами сфинктерита. Частота дефекации может варьировать от 4-6 до 15-20 раз за сутки. При дизентерии стул жидкий, содержащий примеси мутной слизи и крови. При тяжелых формах дизентерии возможно развитие геморрагического синдрома, вплоть до кишечного кровотечения.
У детей раннего возраста при кишечной инфекции общая интоксикация преобладает над колитическим синдромом, чаще возникают нарушения гемодинамики, электролитного и белкового обмена. Наиболее легко у детей протекает кишечная инфекция, вызванная шигеллами Зоне; тяжелее - шигеллами Флекснера и Григорьеза-Шига.
Сальмонеллез у детей
Гриппоподобная (респираторная) форма кишечной инфекции встречается у 4-5% детей. При данной форме сальмонеллы обнаруживаются в посеве материала из зева. Ее течение характеризуется фебрильной температурой, головной болью, артралгией и миалгией, явлениями ринита, фарингита, конъюнктивита. Со стороны сердечно-сосудистой системы отмечаются тахикардия и артериальная гипотония.
На тифоподобную форму сальмонеллеза у детей приходится 2% клинических случаев. Она протекает с длительным периодом лихорадки (до 3-4-х недель), выраженной интоксикацией, нарушением функции сердечно-сосудистой системы (тахикардией, брадикардией).
Септическая форма кишечной инфекции обычно развивается у детей первых месяцев жизни, имеющих неблагоприятный преморбидный фон. На ее долю приходится около 2-3% случаев сальмонеллеза у детей. Заболевание протекает крайне тяжело, сопровождается септицемией или септикопиемией, нарушением всех видов обмена, развитием тяжелых осложнений (пневмонии, паренхиматозного гепатита, отоантрита, менингита, остеомиелита).
Эшерихиозы у детей
Данная группа кишечных инфекций у детей крайне обширна и включает коли-инфекци, вызываемые энтеропатогенными, энтеротоксигенными, энтероинвазивными, энтерогеморрагическими эшерихиями.
Кишечная инфекция у детей, вызванная эшерихиями, протекает с субфебрильной или фебрильной температурой, слабостью, вялостью, снижением аппетита, упорной рвотой или срыгиваниями, метеоризмом. Характерна водянистая диарея (обильный, брызжущий стул желтого цвета с примесью слизи), быстро приводящая к дегидратации и развитию эксикоза. При эшерихиозе, вызываемом энтерогеморрагическими эшерихиями, диарея носит кровавый характер.
Вследствие обезвоживания у ребенка возникает сухость кожи и слизистых оболочек, снижается тургор и эластичность тканей, западает большой родничок и глазные яблоки, снижается диурез по типу олигурии или анурии.
Ротавирусная инфекция у детей
Обычно протекает по типу острого гастроэнтерита или энтерита. Инкубационный период в среднем длится 1-3 дня. Все симптомы кишечной инфекции у детей разворачиваются в течение одних суток, при этом поражение ЖКТ сочетается с катаральными явлениями.
Респираторный синдром характеризуется гиперемией зева, ринитом, першением в горле, покашливанием. Одновременно с поражением носоглотки развиваются признаки гастроэнтерита: жидкий (водянистый, пенистый) стул с частотой дефекаций от 4-5 до 15 раз в сутки, рвотой, температурной реакцией, общей интоксикацией. Длительность течения кишечной инфекции у детей – 4-7 дней.
Стафилококковая кишечная инфекция у детей
Различают первичную стафилококковую кишечную инфекцию у детей, связанную с употреблением пищи, обсемененной стафилококком, и вторичную, обусловленную распространением возбудителя из других очагов.
Течение кишечной инфекции у детей характеризуется тяжелым эксикозом и токсикозом, рвотой, учащением стула до 10-15 раз в день. Стул жидкий, водянистый, зеленоватого цвета, с небольшой примесью слизи. При вторичной стафилококковой инфекции у детей кишечные симптомы развиваются на фоне ведущего заболевания: гнойного отита, пневмонии, стафилодермии, ангины и пр. В этом случае заболевание может принимать длительное волнообразное течение.
Диагностика
На основании осмотра, эпидемиологических и клинических данных педиатр (детский инфекционист) может лишь предположить вероятность кишечной инфекции у детей, однако этиологическая расшифровка возможна только на основании лабораторных данных.
Главную роль в подтверждении диагноза кишечной инфекции у детей играет бактериологическое исследование испражнений, которое следует проводить как можно ранее, до начала этиотропной терапии. При генерализованной форме кишечной инфекции у детей проводится посев крови на стерильность, бактериологическое исследование мочи, ликвора.
Определенную диагностическую ценность представляют серологические методы (РПГА, ИФА, РСК), позволяющие выявлять наличие Ат к возбудителю в крови больного с 5-х суток от начала болезни. Исследование копрограммы позволяет уточнить локализацию процесса в ЖКТ.
При кишечной инфекции у детей требуется исключить острый аппендицит, панкреатит, лактазную недостаточность, дискинезию желчевыводящих путей и др. патологию. С этой целью проводятся консультации детского хирурга и детского гастроэнтеролога.
Лечение кишечной инфекции у детей
Комплексное лечение кишечных инфекций у детей предполагает организацию лечебного питания; проведение оральной регидратации, этиотропной, патогенетической и симптоматической терапии.
Диета детей с кишечной инфекцией требует уменьшения объема питания, увеличения кратности кормлений, использования смесей, обогащенных защитными факторами, употребление протертой легкоусвояемой пищи. Важной составляющей терапии кишечных инфекций у детей является оральная регидратация глюкозо-солевыми растворами, обильное питье. Она проводится до прекращения потерь жидкости. При невозможности перорального питания и употребления жидкости назначается инфузионая терапия: внутривенно вводятся растворы глюкозы, Рингера, альбумина и др.
Этиотропная терапия кишечных инфекций у детей проводится антибиотиками и кишечными антисептиками (канамицин, гентамицин, полимиксин, фуразолидон, налидиксовая кислота), энтеросорбентами. Показан прием специфических бактериофагов и лактоглобулинов (сальмонеллезного, дизентерийного, колипротейного, клебсиеллезного и др.), а также иммуноглобулинов (антиротавирусного и др.). Патогенетическая терапия предполагает назначение ферментов, антигистаминных препаратов; симптоматическое лечение включает прием жаропонижающих, спазмолитиков. В период реконвалесценции необходима коррекция дисбактериоза, прием витаминов и адаптогенов.
Прогноз и профилактика
Раннее выявление и адекватная терапия обеспечивают полное выздоровление детей после кишечной инфекции. Иммунитет после ОКИ нестойкий. При тяжелых формах кишечной инфекции у детей возможно развитие гиповолемического шока, ДВС-синдрома, отека легких, острой почечной недостаточности, острой сердечной недостаточности, инфекционно-токсического шока.
В основе профилактики кишечных инфекций у детей – соблюдение санитарно-гигиенических норм: правильное хранение и термическая обработка продуктов, защита воды от загрязнения, изоляция больных, проведение дезинфекции игрушек и посуды в детских учреждениях, привитие детям навыков личной гигиены. При уходе за грудным ребенком мама не должна пренебрегать обработкой молочных желез перед кормлением, обработкой сосок и бутылочек, мытьем рук после пеленания и подмывания ребенка.
Дети, контактировавшие с больным кишечной инфекцией, подлежат бактериологическому обследованию и наблюдению в течение 7 дней.
Изучены частота, характер и продолжительность внекишечных проявлений в зависимости от проводимой терапии у детей с норовирусной инфекцией. Установлено, что при норовирусной инфекции у детей, помимо гастроинтестинальных симптомов, нередко отмечаются и друг
Features of the clinical course and approaches to the therapy of norovirus infection in children R. V. Popova, T. A. Ruzhentsova
The frequency, nature and duration of extra-intestinal manifestations depending on the therapy in children with norovirus infection were studied. It was found that in norovirus infection in children, in addition to gastrointestinal symptoms, there are often other symptoms that affect the upper respiratory tract, pancreas, hepatobiliary and urinary systems and heart. An effective drug that relieves the symptoms of norovirus infection, prevents the development of extra-intestinal manifestations and complications, is colloidal silicon dioxide.
Острые кишечные инфекции (ОКИ) продолжают занимать одно из ведущих мест по распространенности среди других заболеваний. В последние десятилетия анализ их этиологической структуры и характера свидетельствует о существенных изменениях, происходящих как за счет появления новых лабораторных методов диагностики, так и за счет модификации возбудителей. Важную роль играет и трансформация иммунного ответа организма человека под влиянием неблагоприятной экологической обстановки, резкого снижения количества натуральных продуктов питания с увеличением употребления консервантов и стабилизаторов.
По данным исследователей, в настоящее время во многих странах, несмотря на достижения здравоохранения, отмечается рост числа вирусных ОКИ [1–6].
Ведущими возбудителями по-прежнему остаются ротавирусы. Наряду с ними в последние годы отмечается значительный рост частоты регистрации норовирусной инфекции с 2–5% из всех случаев секреторных диарей до 10–26,5% от всех выявленных эпизодов ОКИ [1, 7–10]. Пик заболеваемости, по данным различных авторов, приходится на период с января по апрель [1, 2, 9]. Болеют преимущественно дети в возрасте от рождения до 3 лет, среди которых чаще регистрируются среднетяжелые формы заболевания [1].
Наиболее вероятно, что частота норовирусной инфекции существенно выше, поскольку многие взрослые и подростки к врачам не обращаются из-за нетяжелого течения с преобладанием легких форм. В то же время, по результатам исследований проб питьевой воды, норовирусы нередко опережают ротавирусы по частоте их выявления, выходя на второе место после аденовирусов [11].
Активизации эпидемического процесса норовирусной инфекции может способствовать и длительный период выделения вируса после купирования симптомов ОКИ, составляющий в среднем 28 суток и достигающий 182 дня у иммуноскомпрометированных пациентов [12]. В связи с этим, в соответствии с действующими на сегодняшний день рекомендациями, при отсутствии клинической симптоматики дети могут посещать организованные коллективы вне зависимости от результатов лабораторной диагностики, что сопровождается неуточненным в настоящее время риском распространения инфекции. В то же время норовирусная инфекция отличается высокой контагиозностью: всего 10 частиц вируса достаточно для передачи ее от больного к восприимчивому организму [13]. Возбудитель сохраняет свою жизнеспособность в окружающей среде, на различных поверхностях до 4 недель, устойчив к физическим и химическим воздействиям. Как показали исследования, среди пациентов с подтвержденной норовирусной этиологией ОКИ преобладают дети из организованных коллективов (61%) с моноинфекцией — 93% [1]. Помимо того, в ходе изучения особенностей возбудителя была доказана высокая скорость молекулярной эволюции норовирусов, приводящая к частому возникновению и быстрому глобальному распространению его новых эпидемических вариантов [14]. Все это диктует необходимость своевременного выявления и адекватного лечения больных.
При лабораторном исследовании в копрограмме может быть непереваренная клетчатка, нейтральный жир, зерна крахмала, лейкоциты [1]. В анализе крови у большинства пациентов отмечается лимфоцитоз при нормальном количестве лейкоцитов, при выраженной клинической симптоматике возможны нейтрофильный лейкоцитоз, увеличение скорости оседания эритроцитов и повышение концентрации мочевины. Проявления ОКИ нередко не ограничиваются желудочно-кишечным трактом. Помимо гастроэнтеритического синдрома, почти у всех пациентов отмечается интоксикация, проявляющаяся вялостью, слабостью, адинамией, снижением аппетита, бледностью кожных покровов [1].
Лечение норовирусной инфекции проводится по принятым в Российской Федерации стандартам терапии ОКИ, включающим регидратационные растворы, энтеросорбенты, пробиотики, при необходимости жаропонижающие [15, 17]. Отечественными авторами рекомендуется назначение противовирусной терапии, хотя этот вопрос по-прежнему, учитывая зарубежные данные, остается дискутабельным. В опубликованных ранее работах было показано возможное появление катаральных изменений верхних дыхательных путей: насморка, кашля, признаков ринофарингита при норовирусной инфекции [5, 15, 16].
В литературе есть единичные указания на возможность развития у пациентов, больных норовирусной инфекцией, пневмоний, отитов, цистита, кардиомиопатии, менингита [17–19]. Зарубежные авторы отмечают, что при норовирусной этиологии чаще, чем при ротавирусной, отмечается судорожный синдром [18]. Однако подробного анализа распространенности, факторов риска развития, особенностей течения, характера и длительности внекишечных проявлений и связанных с этим осложнений не проводилось. Не было оценено влияние различных подходов к терапии норовирусной инфекции на формирование той или иной симптоматики у пациентов.
Целью данного исследования было изучить частоту, характер и продолжительность внекишечных проявлений в зависимости от проводимой терапии у детей с норовирусной инфекцией.
Материалы и методы исследования
В исследование включили 80 детей в возрасте от 8 месяцев до 6 лет, госпитализированных в инфекционное отделение для детей ГБУЗ МО МГКБ г. Мытищи. У всех пациентов норовирусная этиология ОКИ была подтверждена лабораторно методом полимеразно-цепной реакции. Преобладали дети в возрасте от одного года до трех лет (42 ребенка — 52%), 27 пациентов (34%) относились к возрастной группе от трех до 6 лет и 11 (14%) — от 8 месяцев до одного года. Большинство пациентов (94%) имели среднетяжелую форму ОКИ. Продолжительность заболевания от момента начала до включения в исследование составила от 1 до 3 суток включительно. Выявление какой-либо другой этиологии относилось к критериям исключения.
При поступлении в стационар, помимо клинического осмотра, всем детям были проведены лабораторные и инструментальные обследования для уточнения состояния органов брюшной полости, сердечно-сосудистой и мочевыделительной систем. Оценивали выраженность гастроэнтерологических, респираторных и интоксикационных проявлений, результаты клинического анализа крови, общего анализа мочи, уровни МВ-креатинкиназы, лактатдегидрогеназы, аспарагиновой трансаминазы, аланиновой трансаминазы в сыворотке крови. Детям проводили электрокардиографию (ЭКГ), а также ультразвуковое исследование (УЗИ) органов брюшной полости и почек. Этиологию ОКИ определяли при помощи полимеразно-цепной реакции.
Пациентов с наличием в анамнезе заболеваний сердечно-сосудистой, мочевыделительной и панкреатогепатобилиарной систем в исследование не включали.
Повторные клинические осмотры до купирования симптомов осуществляли ежедневно и, при необходимости, чаще, оценивали длительность каждого из проявлений. При наличии отклонений по результатам лабораторного и/или инструментального обследования или выявлении показаний в последующие дни нахождения в стационаре через 3–5 дней оценивали показатели повторно, а при отсутствии нормализации — еще раз, на 18–25 день от начала заболевания.
Все пациенты получали стандартную, рекомендуемую при ОКИ, безлактозную диету. Детям первого года жизни, находящимся на грудном вскармливании, его рекомендовали продолжить. Базисная терапия состояла из регидратационных глюкозосолевых растворов, назначенных только перорально — в 39%, парентерально — в 25% и парентерально, а затем перорально — в 36%. Энтеросорбенты получали 81% детей, пробиотики — 89%, жаропонижающие (ибупрофен и/или парацетамол) при температуре более 38–39 °C — 64%.
В зависимости от особенностей стартовой терапии, которая в большинстве случаев начиналась на дому, пациенты были распределены на три группы. В 1?ю группу было отнесено 24 ребенка, получавших с первого дня проявлений заболевания энтеросорбенты и регидратационную терапию, во 2?ю группу вошел 41 больной, которым комплексная терапия была назначена позднее, на вторые или третьи сутки, в 3?ю было включено 15 пациентов, не принимавших энтеросорбенты. Эти препараты не были назначены врачами в большинстве случаев из-за отсутствия диареи, иногда — из-за отказа или негативной реакции у детей.
Статистическая обработка всех полученных данных осуществлялась на персональном компьютере с использованием программы Statistica, версия 6.1 (StatSoft Inc., США). Различия между рассчитанными показателями в группах оценивали по двустороннему Z-критерию, статистически значимыми считали при вероятности > 95% (p < 0,05).
Результаты и обсуждение
Среди основных клинических симптомов у всех пациентов были выделены: рвота от 1 до 25 раз в сутки, отсутствие аппетита, вялость, бледность и повышение температуры тела. Диарея наблюдалась у 81% детей, чаще с конца первых или на вторые сутки. На боли в животе жаловались 48% (13 детей) пациентов из возрастной группы от 3 до 6 лет. У детей более раннего возраста болевой синдром не оценивали из-за высокой вероятности неправильного определения.
У наблюдавшихся пациентов регистрировали разнообразные внекишечные проявления, представленные на рис. Из них лечащие врачи в первую очередь отмечали признаки ринита с заложенностью носа, умеренными водянистыми выделениями, гиперемией и отечностью носовых ходов в сочетании с незначительно или умеренно выраженным фарингитом (у 34% — 27 детей).
По данным дополнительных исследований, среди детей с норовирусной инфекцией в 71,25% (у 57 детей) были выявлены те или иные отклонения на ЭКГ: нарушения реполяризации (у 54% — 43 детей), снижение вольтажа (у 20% — 16 детей), суправентрикулярная или вентрикулярная экстрасистолия (у 7,5% — 6 детей). У 8 детей было отмечено сочетание изменений. Повышение уровней активности МВ?креатинкиназы изолированно или одновременно с увеличением значений лактатдегидрогеназы и/или соотношения аспарагиновой и аланиновой трансаминаз регистрировали у 36% детей.
По результатам УЗИ органов брюшной полости, изменения печени и/или поджелудочной железы были выявлены у 42 детей (53%). Нарушения структуры почек, чаще — уплотнения стенок чашечно-лоханочной системы, было выявлено у 30 детей (38%).
Основные симптомы ОКИ у всех пациентов были купированы в течение 2–4 суток от момента начала адекватной терапии.
Отклонения, выявленные по данным ЭКГ и лабораторного обследования, у 64% при повторной оценке показателей, через 3–5 дней, не выявлялись. Однако у 7,5% пациентов сохранялись нарушения реполяризации, снижение вольтажа и повышение МВ?креатинкиназы сохранялись, несмотря на отсутствие основных симптомов ОКИ, что позволило подозревать вероятный миокардит у этих детей. Через 18–25 дней отклонения сохранялись у 2 пациентов (3,5% из группы детей с выявленными нарушениями на ЭКГ).
По данным УЗИ, через 3 недели купировались изменения поджелудочной железы у 81% (34 детей), печени — у 74% (у 31 ребенка), почек — в 100%. Симптомы инфекции мочевыводящих путей также не отмечались ни в одном случае.
Анализ результатов лабораторного и инструментального обследования в группах, различавшихся по особенностям терапии энтеросорбентами, показал, что в 1?й группе, у детей, получавших с первых суток Полисорб МП, не было случаев сохранения симптоматики внекишечных проявлений более 3 недель. Нарушения на ЭКГ, полностью купировавшиеся к моменту повторного обследования через 3–5 суток, были выявлены у 2 детей (8%). У 3 пациентов (12,5%) были выявлены изменения поджелудочной железы и у 2 из них — печени. Инфекций мочевыводящих путей и уплотнений чашечно-лоханочной системы, по данным УЗИ, в этой группе пациентов не выявляли. У 2 детей (8%) была отмечена анемия легкой степени.
Как видно из табл., частота длительно сохраняющихся внекишечных изменений была выше в группе, не получавшей энтеросорбенты. Очевидно, что отсутствие диареи во многих случаях было связано как с преимущественным поражением верхних отделов желудочно-кишечного тракта, так и, возможно, с обезвоживанием, что также усугубляло внекишечную симптоматику и не могло служить поводом для отказа от энтеросорбирующей терапии. Назначение энтеросорбентов на 2–3 сутки от начала заболевания приводило к снижению частоты внекишечных проявлений по сравнению с группой, которым энтеросорбирующие препараты назначены не были.
Анализ терапии показал, что применение диоксида кремния коллоидного (Полисорб МП) с первых суток у 12 детей прерывало симптомы ОКИ. На фоне терапии диарея ограничивалась неоформленным стулом 2–5 раз в течение одного дня или не проявлялась вовсе, температура тела снижалась до нормальных значений. Изменения поджелудочной железы, выявленные у 1 ребенка, были незначительны и купировались вместе с основными проявлениями ОКИ. Случаев отказа от терапии диоксидом кремния коллоидным из-за органолептических свойств, индивидуальной непереносимости или нежелательных явлений не было.
Выбор данного препарата обусловлен его доказанной безопасностью, а также высокой эффективностью (с высокой удельной поверхностью сорбции частиц более 300 м 2 /г), а также отличными протеонектическими свойствами, всеми прочими свойствами современных энтеросорбентов и длительным постклиническим опытом применения (более 20 лет). Протеонектическими свойствами Полисорба МП объясняется его способность связывать значительные количества микроорганизмов — до 10 млрд микробных тел на 1 г препарата и более, независимо от видовой принадлежности, а также различные эндо и экзотоксины [20].
Таким образом, полученные результаты подчеркивают разнообразие проявлений ОКИ, не ограничивающихся только желудочно-кишечным трактом. Выявленные изменения печени, поджелудочной железы, мочевыделительной системы, сердца у некоторых пациентов сохраняются длительно, более 3 недель с момента появления первых симптомов норовирусной инфекции.
Выводы
- При норовирусной инфекции у детей помимо гастроинтестинальных симптомов нередко отмечаются и другие, затрагивающие верхние дыхательные пути, поджелудочную железу, гепатобилиарную и мочевыделительную систему, сердце.
- Комплексная терапия, соответствующая стандартам лечения ОКИ вирусной этиологии, должна проводиться с первого дня заболевания.
- Эффективным лекарственным препаратом, купирующим симптомы норовирусной инфекции, препятствующим развитию внекишечных проявлений и осложнений, является Полисорб МП.
Литература
Р. В. Попова
Т. А. Руженцова 1 , доктор медицинских наук
ФБУН ЦНИИЭ Роспотребнадзора, Москва
Особенности течения и подходы к терапии норовирусной инфекции у детей/ Р. В. Попова, Т. А. Руженцова
Для цитирования: Лечащий врач № 11/2018; Номера страниц в выпуске: 44-48
Теги: вирусная инфекция, дети, внекишечные проявления
Читайте также:

