Какие инфекции могут поражать сосуды
Обновлено: 13.05.2024
В статье представлен обзор научной литературы, содержащий данные о патогенезе, диагностике и лечении сердечно-сосудистых последствий перенесенной новой коронавирусной инфекции. Поражение сердца наблюдается у 7-28% госпитализированных пациентов с COVID-19.
Резюме. В статье представлен обзор научной литературы, содержащий данные о патогенезе, диагностике и лечении сердечно-сосудистых последствий перенесенной новой коронавирусной инфекции. Поражение сердца наблюдается у 7-28% госпитализированных пациентов с COVID-19. Поражение миокарда при воздействии коронавирусной инфекции может быть реализовано посредством двух патологических механизмов: прямое повреждение миокарда вследствие взаимодействия SARS-CoV-2 с миокардиальными рецепторами ангиотензинпревращающего фермента 2, а также косвенное повреждение миокарда, которое может быть вызвано цитокинами и другими провоспалительными факторами, нарушением микроциркуляции, гипоксическими изменениями кардиомиоцитов. Частыми аритмическими осложнениями COVID-19 бывают фибрилляция предсердий и желудочковая экстрасистолия. Несмотря на многочисленные публикации о поражении сердца в острой фазе этого заболевания, данные о сохраняющихся после выздоровления нарушениях недостаточны, клинические рекомендации по ведению таких пациентов отсутствуют. На основе приведенного клинического случая описаны механизмы комбинированной терапии бисопрололом и амлодипином частой желудочковой экстрасистолии, возникшей после перенесенного СОVID-19.
Пандемия COVID-19, вызванная коронавирусом SARS-CoV-2, продемонстрировала широкий спектр его проявлений, включая сердечно-сосудистые. Встречаемость поражения сердца при этом колеблется от 7% до 28% госпитализированных пациентов, что зависит от тяжести заболевания анализируемого контингента 1. В зависимости от особенностей повреждения миокарда, включая инфаркт миокарда 1-го или 2-го типа, миокардит, васкулит, лекарственное воздействие или другие механизмы, у выздоровевших пациентов могут длительное время наблюдаться субклинические или явные сердечно-сосудистые нарушения. Последствиями тяжелого острого респираторного синдрома могут быть сердечная недостаточность, аритмии, боли в груди, одышка [6]. Так, в исследовании Yvonne M. J. Goërtz и соавт., основанном на анкетировании 2113 больных, перенесших COVID-19, показано, что через 79 дней от начала болезни у 44% лиц сохранялись жалобы на стеснение в груди, у 32% – на сердцебиение [7].
Порой сложно дифференцировать изменения, обусловленные инфекцией, и обострение хронического сердечно-сосудистого заболевания (ССЗ), предшествовавшего ей. Известно, что наличие коморбидных ССЗ, например, артериальной гипертензии, увеличивает риск тяжелого течения COVID-19 и влияет на его прогноз [8]. В настоящее время нет систематизированных данных, описывающих динамику состояния у пациентов, перенесших сердечно-сосудистые осложнения после COVID-19. Национальным институтом здравоохранения и медицинского обслуживания Соединенного королевства (NICE) выделен постковидный синдром, характеризующийся признаками и симптомами, которые развиваются во время или после COVID-19, продолжаются более 12 недель и не объясняются альтернативным диагнозом. Среди сердечно-сосудистых проявлений постковидного синдрома наиболее часто регистрируются кардиалгии, в том числе ощущения сдавления в груди, и учащенное сердцебиение [9].
Вопросы клинической оценки сердечно-сосудистых проявлений постковидного синдрома и тактики его лечения неизбежно встают перед врачами общей практики, терапевтами, кардиологами. Назначение лекарственных препаратов должно быть пересмотрено с учетом особенностей патогенеза заболевания.
Механизмы сердечно-сосудистого поражения при COVID-19
Поражение миокарда при воздействии коронавирусной инфекции может быть реализовано посредством двух патологических механизмов [10]. Во-первых, это прямое повреждение миокарда вследствие взаимодействия SARS-CoV-2 с миокардиальными рецепторами ангиотензинпревращающего фермента 2 (АПФ2). Во-вторых, косвенное повреждение миокарда может быть вызвано цитокинами и другими провоспалительными факторами, нарушением микроциркуляции, гипоксическими изменениями кардиомиоцитов [11, 12]. Помимо перечисленного, нельзя не упомянуть и о лекарственном воздействии препаратов, применяемых при COVID-19, которые удлиняют интервал QT и могут иметь проаритмическую предрасположенность [13].
.jpg)
Исследования показали, что при проникновении SARS-CoV-2 в клетку большую роль играют ионы кальция. Предполагается, что вирусу необходимо два иона Ca 2+ для слияния с клеткой на этапе входа (рис. 1). Некоторые блокаторы кальциевых каналов, такие как нимодипин, мемантин, уменьшают проникновение вируса в клетку [14].
SARS-CoV-2 вызывает ряд патофизиологических процессов, включающих гиперсимпатикотонию, гиперкоагуляцию, системное воспаление, эндотелиальную дисфункцию [15, 16]. Гиперактивация симпатической нервной системы неизбежно развивается у больных COVID-19 за счет многих факторов: гиперактивации иммунной системы, выделения огромного количества цитокинов, интерлейкина-6, факторов некроза опухоли альфа, гипоксии, что, в свою очередь, способствует повреждению миокарда и более тяжелому течению заболевания. Частыми осложнениями COVID-19 бывают фибрилляция предсердий, желудочковая экстрасистолия [17]. Магнитно-резонансное исследование сердца пациентов, излечившихся от COVID-19, обнаруживает отек миокарда, фиброз и нарушение функции левого и правого желудочков [18, 19], что может быть морфологическим субстратом сердечно-сосудистых проявлений перенесенной коронавирусной инфекции.
Лечение сердечно-сосудистых осложнений, связанных с COVID-19
Лечение острого воспаления и повреждения сердца при COVID-19 достаточно широко исследуется и описано в литературе. Так, опуб-ликованное научное заявление Американской кардиологической ассоциации рекомендует применять начальный протокол лечения кардиогенного шока у пациентов с фульминантным миокардитом, включающий введение инотропов и/или вазопрессоров и механическую вентиляцию легких [20]. Лечение долгосрочных проявлений поражений сердца, обусловленных COVID-19, изучено недостаточно и преимущественно заключается в симптоматической терапии [21].
Клинический случай
Больная Д., 43 года, обратилась впервые к кардиологу 15 апреля 2021 г. с жалобами на колющие, ноющие, иногда жгучие боли в области сердца и в межлопаточной области, не связанные с какими-либо провоцирующими факторами, продолжительностью от нескольких минут до 1-2 часов, купирующиеся самостоятельно; чувство учащенного сердцебиения, лабильность артериального давления (АД), перебои в сердце. Подобные симптомы появились с конца октября 2020 г. и усилились в течение последних 2 недель. Ранее жалоб со стороны сердечно-сосудистой системы не было, считала себя практически здоровой, отмечала высокую толерантность к физическим нагрузкам, при ежегодных медицинских осмотрах патологии не выявляли.
При осмотре состояние удовлетворительное. Сознание ясное, ориентирована. Кожные покровы чистые, отеков нет. ИМТ 36 кг/м 2 . В легких перкуторно над всеми полями ясный легочный звук, дыхание везикулярное, хрипы не выслушиваются. Часто-та дыхательных движений в покое 18 в 1 минуту. При перкуссии левая граница смещена до срединно-ключичной линии. Тоны сердца приглушены, ритмичные. Частота сердечных сокращений (ЧСС) – 90 в 1 минуту. Пульс – 80 в 1 минуту. Артериальное давление – 150/90 мм рт. ст. Язык чистый, влажный. Живот симмет-ричный, в акте дыхания участвует, при пальпации мягкий, безболезненный. Печень не увеличена. Мочеиспускание свободное, безболезненное.
Анализы крови и мочи – без особенностей. Кровь на тропонины – 0,001 нг/мл. Кровь на IgG к SARS-CoV-2 (ИФА) – положительный, коэффициент позитивности (КП) – 15,9.
.jpg)
.jpg)
Больной было назначено лечение: рациональная диета с ограничением соли, селективные β-адрено-блокаторы и дигидропиридиновые блокаторы кальциевых каналов с титрацией и последующим переводом на фиксированную комбинацию – Конкор АМ, метаболические препараты, иглорефлексотерапия, физиотерапия, массаж шейно-воротниковой зоны. На фоне проводимого лечения отмечалась положительная динамика, АД в пределах нормы – 130/80 мм рт. ст. По данным суточного мониторирования ЭКГ в динамике: средняя ЧСС – 64 уд./мин, одиночных желудочковых экстрасистол – 68 в сут.
Лечение сердечно-сосудистых проявлений после перенесенного COVID-19 представляет собой непростую задачу. В настоящее время клинические рекомендации по лечению постковидного синдрома не разработаны. Большинство доступных отчетов о наблюдениях за больными с аритмией содержат сведения о развитии осложнения в острой фазе коронавирусной инфекции [22], поэтому значение COVID-19 в патофизиологии нарушений ритма у выздоровевших пациентов неизвестно.
В представленном клиническом случае у пациентки, ранее не наблюдавшейся по поводу ССЗ, сразу после перенесенного COVID-19 появились жалобы на частые перебои в работе сердца и впервые возникла артериальная гипертензия. При обследовании выявлена частая желудочковая экстрасистолия. Известно проаритмическое действие некоторых препаратов, применяющихся для лечения коронавирусной инфекции. В анализируемом случае для лечения двусторонней пневмонии применялся курс антибиотикотерапии, включавший цефалоспорины и фторхинолоны. Токсическое влияние фторхинолонов на сердце проявляется в появлении аритмий на фоне удлинения интервала QT, что встречается также при применении макролидов, гидроксихлорохина. Механизм данного нарушения был описан в работе J. Kang и соавт. [23]. Доказано индуцирование фторхинолонами мутаций в гене, названном human ether-a-go-go-related, или HERG, который контролирует одну из субъединиц калиевых каналов, участвующую в переносе ионов ионизированного калия в кардиомиоцит. Мутация приводит к нарушению проникновения калия внутрь клетки и увеличению периода реполяризации, удлинению интервала QT на электрокардиограмме, а клинически может приводить к желудочковой аритмии. Для азитромицина также описано влияние на калиевые и магниевые каналы, изменяющее содержание ионов в эукариотических клетках миокарда [24].
Несмотря на то, что в момент обследования у пациентки интервал QT не был удлинен, необходимо было назначать препараты, которые, обладая антиаритмическим действием, не увеличивают период реполяризации. Известно, что эффективными средствами лечения желудочковых нарушений ритма сердца у больных с приобретенными формами синдрома удлинения интервала QT являются бета-блокаторы в сочетании с препаратами магния [25]. Кроме того, в описываемом случае не исключается многофакторное влияние перенесенной инфекции на патогенез наблюдаемых нарушений ритма. Так, в исследовании S. T. Lau и соавт. описывалось, что у пациентов, выздоравливающих после инфекции, вызванной вирусами группы SARS, отмечалось сердцебиение в виде тахикардии в покое или при легкой физической нагрузке. Возможными причинами, по мнению авторов, были нарушение функции легких и сердца, дисфункция щитовидной железы, анемия, вегетативная дисфункция и состояние тревоги [26].
Применение бета-адреноблокаторов у пациентов с артериальной гипертензией и желудочковой экстрасистолией обусловлено их следующими эффектами: уменьшением сердечного выброса в результате ослабления сократительной способности миокарда левого желудочка и урежением ЧСС, торможением секреции ренина, увеличением высвобождения вазодилатирующих веществ, уменьшением общего периферического сосудистого сопротивления и влиянием на сосудо-двигательные центры продолговатого мозга. Эта группа препаратов оказывает положительное влияние на ренин-ангиотензин-альдостероновую систему наряду со способностью подавлять активность симпатоадреналовой системы [27], что обусловливает их эффективность при сердечно-сосудистых проявлениях постковидного синдрома. Так, по наблюдениям P. Gao у критически тяжелых больных, госпитализированных по поводу COVID-19, желудочковые тахиаритмии ассоциировались с 3-кратным увеличением риска летальности, в то время как прием бета-адреноблокаторов снижал ее на 80% [28]. Важным является использование кардиоселективных препаратов, не оказывающих негативного влияния на гладкую мускулатуру бронхов. Например, одним из самых высокоселективных бета-блокаторов является бисопролол, селективность которого к β1-адренорецепторам более чем в 3 раза превосходит таковую у метопролола.
Учитывая возможные метаболические нарушения в кардиомиоцитах вследствие гипоксии, обусловленной COVID-19, целесообразным было назначение кардиотропных препаратов и препаратов с антиангинальным эффектом. В этом отношении стоило обратить внимание на группу дигид-ропиридиновых блокаторов кальциевых каналов, ярким представителем которых является амлодипин. Он в незначительной степени влияет на сократимость миокарда и не влияет на функцию синусового узла и атриовентрикулярную проводимость, что наряду с его антигипертензивным и антиангинальным действием оказывает благоприятный эффект на состояние миокарда после повреждения [29]. В исследовании Chi Peng, включающем 4569 пациентов, госпитализированных по поводу COVID-19, процент смертности у больных, принимавших блокаторы кальциевых каналов, был в 3 раза меньше в сравнении с теми, кто их не принимал [30].
Частым проявлением постковидного синдрома являются нарушения, обусловленные прямым действием коронавируса на симпатическую нервную систему [31], симптомы чего наблюдались у нашей пациентки. На фоне лечения мы наблюдали уменьшение жалоб на головную боль, головокружение, раздражительность, эмоциональную лабильность. Целесообразность указанной терапии подтверждается исследованием И. Л. Запесочной и соавт. [32], которые описали положительный эффект комбинированного назначения кардиоселективного бета-адреноблокатора бисопролола и дигидропиридинового блокатора кальциевых каналов амлодипина на параметры церебрального кровотока, проявляющегося улучшении допплерографических показателей.
Таким образом, у пациентов с кардиологическими проявлениями постковидного синдрома оптимальным решением является применение фиксированной комбинации амлодипина и бисопролола, которая представляется на сегодняшний день наиболее эффективной и безопасной в силу особенностей препаратов, ее составляющих. Влияя на различающиеся механизмы проникновения вируса в клетку, эта комбинация препаратов приводит к снижению инфекционности SARS-CoV-2, положительно влияет на исходы заболевания и уменьшает сердечно-сосудистые проявления постковидного синдрома.
Вывод
Лечение сердечно-сосудистых проявлений перенесенной новой коронавирусной инфекции COVID-19 должно быть основано на патофизио-логических механизмах выявленных нарушений. Применение комбинированного сочетания селективных бета-блокаторов и дигидропиридиновых блокаторов кальциевых каналов при желудочковых нарушениях ритма и артериальной гипертензии существенно расширяет возможности терапии постковидного синдрома.
КОНФЛИКТ ИНТЕРЕСОВ. Авторы статьи подтвердили отсутствие конфликта интересов, о котором необходимо сообщить.
CONFLICT OF INTERESTS. Not declared.
Литература/References
Л. В. Мельникова* , 1 , доктор медицинских наук, профессор
Т. В. Лохина**, доктор медицинских наук
Н. В. Беренштейн**, кандидат медицинских наук
М. Г. Иванчукова**
* ФГБОУ ДПО РМАНПО Минздрава России, Москва, Россия
** ПИУВ – филиал ФГБОУ ДПО РМАНПО Минздрава России, Пенза, Россия
Для многих не секрет, что употребление продуктов, богатых холестерином, негативно сказывается на здоровье. В этой статье мы рассказываем, почему это так, и как холестерин становится причиной ишемической болезни сердца и инфаркта.
Что такое атеросклероз
Атеросклероз — распространенное заболеваний артерий, при котором сосуды теряют эластичность, а на их стенках откладываются липидные фракции (холестериновые бляшки). По мере прогрессирования заболевания размер бляшек увеличивается, структура этих бляшек может меняться, а просвет сосуда становится меньше. Это приводит к нарушению кровотока, а в дальнейшем — инфаркту органа, который снабжается кровью.
Атеросклероз характерен для всех типов артерий, в том числе — аорты, коронарных артерий, сонных, а также артерий конечностей и других. Наиболее распространенные последствия атеросклероза — это ишемическая болезнь сердца и инфаркт миокарда. На фоне атеросклеротического поражения сосудов также могут развиваться: почечная недостаточность, инсульты, гангрена конечностей и другие патологии.
Различают несколько разновидностей атеросклероза в зависимости от происхождения и локализации. По первому параметру атеросклероз бывает:
- Гемодинамический — развивается на фоне сосудистых патологий, в том числе и артериальной гипертензии. Воспалительные процессы на стенках сосудов притягивают клетки иммунной системы и жировые фракции. Так образуются бляшки, которые со временем увеличиваются в размерах.
- Метаболический — возникает при нарушениях метаболизма, когда в крови циркулирует избыточное количество ЛПНП. Точные механизмы появления атеросклеротических бляшек на фоне метаболических нарушений пока неизвестны. Неблагоприятными факторами в данном случае являются ожирение, сахарный диабет, чрезмерное употребление простых углеводов и гиподинамия.
- Смешанный — развивается на фоне гемодинамических и метаболических нарушений. Установлено, что в большинстве случаев у пациентов речь идет именно о смешанном атеросклерозе, когда метаболические изменения приводят к гемодинамическим, а те в свою очередь еще сильнее ухудшают обменные процессы.
В зависимости от локализации атеросклероз бывает следующих видов:
- аорты;
- коронарных сосудов;
- сосудов нижних конечностей;
- сосудов головного мозга;
- сосудов почек, печени, поджелудочной железы;
- других сосудов.
Существует еще одна классификация заболевания — по степени развития патологии. Здесь выделяют четыре этапа:
I этап — бессимптомный или доклинический. Выявить атеросклеротические изменения можно только при помощи специальных диагностических инструментов.
II этап — ишемический. Просвет артерий сужается, из-за чего органы, снабжаемые кровью, недополучают питательные вещества и кислород. Наиболее заметны ишемические проявления при атеросклерозе коронарных артерий и артерий головного мозга.
III этап — тромбонекротический. В местах скопления холестериновых бляшек образуются сгустки крови — тромбы. Опасность тромба в том, что он может оторваться от стенки артерии, а затем с током крови закупорить сосуды с меньшим диаметром. Полная закупорка сосуда приводит к некротическим изменениям, что требует немедленного медицинского вмешательства.
IV этап — склеротический. Это терминальный период атеросклероза, на котором пораженная область сосуда заменяется рубцом. Артерия теряет эластичность и не в состоянии выполнять свои функции по обеспечению равномерного тока крови.
Кто в группе риска
Атеросклеротическим изменениям сосудов в той или иной степени подвержены все люди. Все зависит от того, когда атеросклероз приведет к серьезным осложнениям — в 40 лет или в 80. Рассмотрим основные группы людей, которые рискуют встретиться с этой проблемой раньше остальных:
- Люди с артериальной гипертензией. Повышенное давление — повреждающий фактор для сосудов. При повреждении развивается воспалительный процесс, являющийся основным триггером для появления холестериновых бляшек.
- Люди с заболеваниями обмена веществ. Нарушения липидного обмена, сахарный диабет, а также гормональные нарушения являются факторами риска развития атеросклероза.
- Люди, страдающие от ожирения. Этот фактор в совокупности с неправильным питанием — один из основных в развитии атеросклероза.
- Люди, ведущие малоподвижный образ жизни. Гиподинамия ухудшает ток крови, а также способствует развитию застойных явлений.
- Другие факторы. Развитию атеросклероза также способствуют инфекционные заболевания (источники воспаления), неправильное питание, стрессы, наследственные факторы, а также повышенная вязкость крови.
Важно: атеросклероз и холестерин. До конца прошлого века врачи полагали, что между употреблением животной пищи (в которой содержится холестерин) и атеросклерозом существует прямая связь. Считалось, что чем больше употреблять холестерина, тем выше вероятность болезни. Однако для развития атеросклероза одного лишь холестерина недостаточно. Если стенки артерий не повреждены, то сколько бы холестерина не циркулировало в крови, атеросклероза не будет. Кроме того, основное количество холестерина синтезируется в печени, поэтому привнесенный извне холестерин практически не оказывает негативного влияния.
Причины атеросклероза
До сих пор точные причины развития атеросклероза неизвестны. Накопленные на сегодняшний день сведения о заболевании показывают, что главная причина атеросклероза — это повреждение внутренней стенки сосуда, например, при высоком давлении. Косвенным подтверждением этой теории является тот факт, что чаще всего атеросклеротические изменения затрагивают места разветвления артерий, куда приходится максимальное давление крови.
При повреждении стенок сосудов развивается воспалительный процесс. Кроме того, усиленный поток крови при повышенном давлении способствует продукции в стенках сосудов молекул адгезии. Они притягивают на себя иммунные клетки, в частности, макрофаги. Со временем макрофаги накапливают в себе окисленные липопротеины и образуют пенистые клетки. Так формируются жировые полоски на стенке артерии, которые затем трансформируются в бляшки.
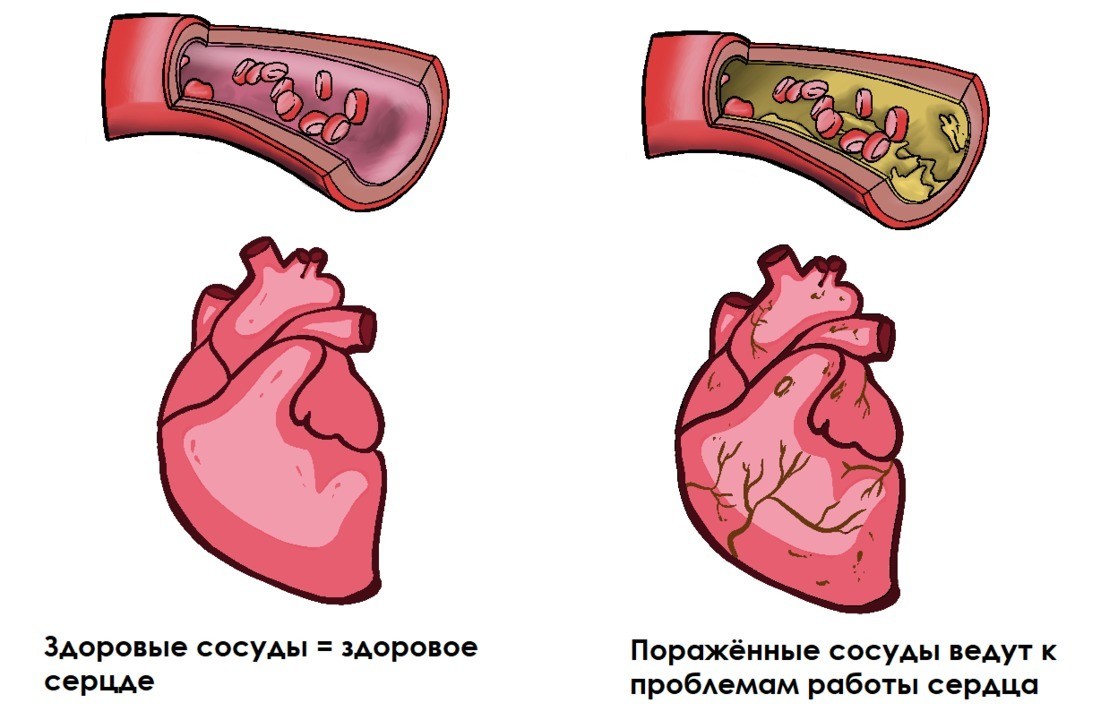
Рисунок 1. Как состояние сосудов отражается на здоровье сердца. Источник: МедПортал
Поэтому одним из наиболее серьезных факторов развития атеросклероза является артериальная гипертензия. При наличии нарушения липидного обмена, это почти всегда приводит к атеросклерозу.
Важно: атеросклероз и мясо. Казалось бы, с понимаем того, что экзогенный холестерин не несет опасности сосудам, мясная пища должна быть реабилитирована. Но не все так просто. Если посмотреть на статистику, то вегетарианцы болезнями сердца и сосудов болеют значительно реже. Согласно последним исследованиям, причина этого может крыться в ТМАО. Такой аббревиатурой называют вещество триметиламиноксид. Причем тут мясо? В мясе содержится много карнитина, который очень нравится кишечным бактериям. В бактериях карнитин превращается в триметиламин (ТМА), который уже в печени окисляется до триметиламиноксида (ТМАО). В настоящее время ТМАО рассматривается как один из факторов развития атеросклероза, инсульта и других сердечно-сосудистых заболеваний. При этом точный механизм развития атеросклероза под воздействием ТМАО пока остается непонятным.
Механизм развития болезни
Рассмотрим подробнее механизмы и три этапа развития атеросклероза, с чего все начинается и чем заканчивается.
Первый этап
Изначально на внутренних стенках артерий образуются жировые полоски и пятна. Из-за воспалительного процесса артериальная стенка отекает, становится рыхлой и притягивает все больше липидных фракций.
Второй этап
Из соединительной ткани и липидов образуются атеросклеротические бляшки. На этом этапе бляшки еще мягкие, поэтому при сильном токе крови они могут разрываться и закупоривать более мелкие сосуды.
Третий этап
На последнем этапе в бляшках скапливается кальций, что делает их тверже.
До сих пор, относительно механизмов развития атеросклероза ведутся дискуссии. Предполагается, что появление атеросклеротических бляшек также связано и с некоторыми инфекциями. Также рассматривают и роль мутаций, при которых стенки артерий становятся более уязвимыми перед повреждающими факторами.
Симптомы атеросклероза
Поскольку атеросклероз поражает различные артерии, то и симптоматика зависит от локализации поражения. При поражении сосудов, питающих сердце, развивается ишемическая болезнь сердца; при атеросклерозе почечных сосудов — почечная недостаточность и так далее. Рассмотрим подробнее симптомы атеросклероза разных артерий.
Атеросклероз сосудов сердца
При поражении атеросклерозом аорты и коронарных артерий на начальных этапах заболевания симптомов у больного нет. Со временем возникают проявления, напоминающие стенокардию. Для атеросклероза сердца характерны боль и ощущение сдавливания в области груди. Боль может распространяться на левую руку и в область под левой лопаткой. Приступ стенокардии в большинстве случаев длится недолго, но в данной случае такие боли могут беспокоить больного часами.
У человека может быть увеличен размер левого желудочка сердца. Это связано с тем, что при атеросклеротическом поражении сердечных сосудов затрудняется ток крови в сердце. Это приводит к переполнению левого желудочка. В таких условиях стенки желудочка начинают растягиваться и утолщаться, поскольку им приходится выполнять дополнительную работу по прокачке крови. Подобные изменения на начальных стадиях хорошо поддаются терапии, поэтому крайне важно как можно раньше обратиться к врачу и начать лечение.
Атеросклероз брюшных артерий
Брюшные артерии питают кровью внутренние органы, располагающиеся в этой области, главным образом, органы ЖКТ. Поэтому при атеросклеротическом поражении сосудов брюшной области у больного возникают жалобы на нарушение пищеварения.
Одним из первых симптомов при атеросклерозе брюшных артерий является боль в животе, тошнота и рвота. Как правило, это затяжные боли, которые могут беспокоить человека о по несколько часов. Как правило, болевые ощущения затрагивают область пупка и верхних отделов живота.
Ухудшение кровоснабжения органов пищеварительного тракта также приводят к вздутию, запорам или диарее. На поздних стадиях атеросклероза брюшных артерий больного часто беспокоит рвота с остатками непереваренной пищи. В тяжелых случаях терминальных стадий атеросклероза возникают некротические изменения тканей кишечника.
Атеросклероз сосудов нижних конечностей
Как и атеросклероз сердечных артерий, атеросклероз сосудов нижних конечностей — достаточно распространенное явление. Эта болезнь может не проявляться годами, а при прогрессировании патологии у человека появляется боль в ногах. На первых этапах боль возникает при прохождении длительных расстояний. Однако, чем больше закупориваются сосуды ног, тем меньшее расстояние может пройти больной без передышки.
Еще одним косвенным признаком атеросклеротического изменения сосудов нижних конечностей является частичная потеря волосяного покрова на ногах. Происходит это из-за ухудшения кровоснабжения. Также возникают и проблемы с ногтями и кожей.
Опасность атеросклероза нижних конечностей, прежде всего, в трофических нарушениях конечности. Если болезнь не лечить, то со временем возрастает риск появления трофических язв и некротических изменений. В запущенных случаях при атеросклерозе нижних конечностей развивается гангрена, при которой показана ампутация.
Атеросклероз сосудов головного мозга
При атеросклеротическом поражении сосудов, питающих головной мозг, у больного на первом этапе возникают симптомы кислородного голодания мозга. В первую очередь беспокоят головные боли и головокружения. Кроме того, ухудшается концентрация внимания и память. Человек становится более рассеянным и вялым.
При прогрессировании болезни часто начинает беспокоить тошнота, иногда рвота. Из-за нехватки кислорода в головном мозге возможно чувство онемения конечностей. При дальнейшей закупорке сосуда возрастает риск ишемического инсульта, при котором отмирает часть ткани мозга.
Когда обратиться к врачу
При подозрении на атеросклероз из-за наличия в семейном анамнезе сердечно-сосудистых заболеваний, лучше всего будет записаться к врачу, чтобы проверить уровень холестерина.
Врач захочет узнать, был ли в семейном анамнезе люди с повышенным уровнем холестерина, высоким давлением или другими заболеваниями сердца. Также важно сообщить врачу об образе жизни, пищевых привычках, употреблении табака. Помимо этого врачу понадобится информация о том, проходил ли человек тест на холестерин раньше.
Осложнения атеросклероза
В зависимости от пораженных атеросклерозом сосудов у пациента могут развиться следующие осложнения:
- ишемическая болезнь сердца и инфаркт миокарда;
- ишемический инсульт;
- сбои в работе ЖКТ;
- образование тромба;
- аневризма аорты;
- нарушение в работе почек;
- трофические язвы и гангрена конечности;
- другие осложнения.
Диагностика
Диагностика при атеросклерозе включает проведение ряда процедур:
- Осмотр пациента и сбор анамнеза. На первом этапе врач изучает жалобы человека, осматривает кожу (при атеросклерозе она, как правило, бледная), а также прослушивает сердце и измеряет артериальное давление.
- Анализы крови (общий и биохимический). При атеросклерозе у больного может быть повышен сахар, белок, холестерин и некоторые другие показатели. По анализу крови также можно предположить, какие именно артерии поражены атеросклерозом.
- Анализы мочи. Изменения состава мочи особенно заметны при атеросклерозе почечных сосудов.
- Инструментальная диагностика. В зависимости от локализации атеросклеротического поражения, пациенту могут проводить электрокардиограмму, эхокардиографию (УЗИ сердца), фонокардиограмму, ангиографию сосудов нижних конечностей, магнитно-резонансную томографию и другие виды исследований.
После проведения исследований лечащий врач устанавливает точный диагноз и составляет схему лечения.
Особенности лечения
Атеросклероз — болезнь, лечение которой не ограничивается одним лишь медицинским вмешательством. Важное значение в лечении заболевания занимает модификация образа жизни. Пациенты должны придерживаться принципов правильного питания и отказаться от вредных привычек. Неотъемлемой частью жизни должны стать ь регулярные физические нагрузки. Их уровень подбирает врач исходя из возраста пациента и общего состояния здоровья. Как правило, это прогулки с постепенным увеличением времени и интенсивности ходьбы.
Для замедления патологического процесса пациенту при атеросклерозе назначают следующие виды лекарств:
- Статины — препараты, снижающие уровень холестерина в крови.
- Секвестранты желчных кислот — препараты, угнетающие выработку желчных кислот. При нехватке желчных кислот намного быстрее утилизируется холестерин.
- Фибраты — препараты, уменьшающие продукцию жиров.
- Сосудорасширяющие препараты. К таким относятся, например, производные никотиновой кислоты. При расширении сосудов кровь легче продвигается по пораженным атеросклерозом сосудам.
В большинстве случаев изменения образа жизни и медикаментозной терапии достаточно для улучшения состояния больного и остановки патологического процесса. Однако в запущенных случаях, при слишком тяжелых изменениях в сосудах и органах, которые они снабжают кровью, пациенту показано хирургическое вмешательство. Основные виды операций при атеросклерозе:
- Шунтирование — создание дополнительных сосудов (шунтов) для обеспечения нормального тока крови.
- Ангиопластика — малоинвазивная операция, при которой в артерию вводится катетер с баллоном на конце. При достижении пораженного участка баллон открывают, что позволяет расширить участок артерии. Затем на это место устанавливают стент — металлическую сетчатую трубку, которая позволяет беспрепятственно продвигаться крови по сосуду.
В лечении атеросклероза крайне важно и лечение сопутствующих заболеваний, так как сахарный диабет, артериальная гипертензия, болезни почек и других.
Диета при атеросклерозе
Диета при атеросклерозе должна удовлетворять следующие принципы:
- Ограничение насыщенных жиров. Человеку рекомендуется уменьшить количество потребляемых животных жиров. Лучше отказаться от жареного мяса, поскольку при жарке происходит изомеризация жиров. Из-за этого в жареном мясе увеличивается доля трансжиров, а от них желательно полностью отказаться.
- Больше овощей и фруктов. Ешьте больше растительной пищи, поскольку в ней содержится клетчатка, которая нормализует уровень сахара и липидов в крови, а также улучшит пищеварение.
- Ограничение соли и сахара. Чрезмерное потребление простых углеводов (сахар, сладости, сладкие напитки, в том числе и натуральный сок) способствует ожирению и нарушению обмена веществ. А слишком большое количество соли в рационе увеличивает риск возникновения сердечно-сосудистых заболеваний в целом.
Крайне важно соблюдать правила пищевого поведения. Никогда не переедайте, ешьте медленно и тщательно пережевывайте пищу. Относительно количества приемов пищи — проконсультируйтесь со своим врачом. Для некоторых пациентов достаточно 2-3 приема пищи в день, а некоторым нужно дробное питание — до 4-6 раз маленькими порциями.
Прогнозы при атеросклерозе
В настоящее время полностью избавиться от атеросклероза невозможно. Пока еще не разработаны такие препараты, которые бы позволили полностью избавиться от бляшек, а самое главное — восстановить стенки сосудов. Поэтому прогнозы при атеросклерозе зависят от того, на какой стадии заболевания пациент обратился к врачу. Если это ранние стадии, то прогноз благоприятный при соблюдении всех рекомендаций врача, особенно касающихся изменения образа жизни.
Профилактика атеросклероза
Профилактические мероприятия в отношении атеросклероза сводятся к соблюдению следующих рекомендаций:
- Соблюдение принципов здорового и сбалансированного питания. Отказ от чрезмерного употребление сахара, соли и жирной пищи.
- Физическая активность минимум 150 минут в неделю.
- Нормализация веса.
- Отказ от вредных привычек (курения, злоупотребления спиртными напитками).
- Контроль психического здоровья и избегание стрессов.
Заключение
Атеросклероз намного легче предупредить, чем лечить. Если с раннего возраста вести здоровый образ жизни, то вероятность атеросклероза и сопутствующих проблем существенно снижается. Так можно защитить свой организм от целого ряда заболеваний, поскольку работы всех органов и систем во многом зависит от состояния сосудов.
Кровеносные сосуды — главные транспортные магистрали нашего тела. Что происходит, если на автотрассе образуются дефекты покрытия или возникает затор? Снижается скорость движения транспорта, запаздывает доставка грузов, создается аварийно-опасная ситуация.
То же самое случается, если из строя выходит кровеносный сосуд: нарушается обмен веществ, органы и ткани испытывают нехватку кислорода и не могут освободиться от продуктов метаболизма, а в тяжелых случаях — теряют способность выполнять свои функции. Поэтому диагностике сосудистых проблем доктора клиники WikiMed придают особое значение.

Часто эта проблема возникает на фоне других заболеваний — ревматизма, системной красной волчанки, вирусного гепатита, сифилиса, онкологической патологии — и приводит к нарушению работы свертывающей системы крови и усиленному образованию тромбов. Наличие тромбов в кровеносных сосудах, в свою очередь, создает опасность развития осложнений и поражения жизненно важных органов.
Нарушение работы свертывающей системы крови может быть обусловлено и другими причинами, которые порой закладываются на генном уровне. Повышен риск развития этой патологии при наличии сопутствующего сахарного диабета, атеросклероза и гипертонической болезни.
Крупный тромб может полностью блокировать ток крови и вызвать ишемию и даже инфаркт (омертвление) участка органа. В зависимости от того, где локализуется тромб, может развиваться ишемический инсульт головного мозга, острая недостаточность сосудов сердца, тромбоэмболия (закупорка тромбом) легочной и бедренной артерии и другие серьезные осложнения. Избежать их позволяет своевременная и качественная диагностика.
На страже здоровья
Для получения полного представления о состоянии кровеносных сосудов у нас используются эффективные инструментальные методы — такие, как:
- УЗИ артерий и вен нижних конечностей;
- УЗИ брахиоцефальных (сосудов шеи, питающих головной мозг) и транскраниальных сосудов (сосудов головного мозга).

На следующем этапе диагностируются нарушения в работе свертывающей системы крови. С этой целью проводится коагулологическое исследование, которое может носить характер скрининга или развернутого анализа.
При необходимости, исследуются гены свертывающей системы на предмет наличия мутаций.
Своевременная диагностика позволяет подобрать лечение, которое предупредит развитие осложнений. А регулярное посещение сосудистого хирурга в дальнейшем позволит вовремя скорректировать схему приема препаратов и отрегулировать работу свертывающей системы крови. Под таким четким контролем в движении крови никогда не возникает помех.
Эта акция - для наших друзей в "Одноклассниках", "ВКонтакте", "Яндекс.Дзене", YouTube и Telegram! Если вы являетесь другом или подписчиком стр.
Для жителей районов Савеловский, Беговой, Аэропорт, Хорошевский
Гуляев Сергей Викторович
Врач-ревматолог, терапевт, нефролог
Кандидат медицинских наук
Мы в Telegram и "Одноклассниках"
Васкулит (ангиит, артериит) – общее название для группы заболеваний, связанных с воспалением и разрушением стенок кровеносных сосудов. Воспаление сосудов может произойти в любом органе.
Заболевание васкулитом приводит к тому, что сосуды перестают правильно выполнять свою функцию (снабжение кровью тканей и выведение продуктов обмена), поэтому поражаются примыкающие к ним органы.
Васкулиты имеют разные классификации, могут различаться локализацией, этиологией и тяжестью клинической картины. При одних васкулитах поражается только кожа, при других – жизненно важные органы.
Оставленный без лечения васкулит может обернуться серьезными осложнениями. Кишечные и легочные кровотечения, тромбозы, почечная недостаточность, печеночная недостаточность, инфаркт – далеко не полный список опасных последствий заболевания. Васкулит способен привести больного к инвалидности и даже летальному исходу.
Виды и классификация васкулитов
Васкулит сосудов является одним из серьезнейших заболеваний. Воспалительным процессом могут быть охвачены как мелкие сосуды кровеносной системы (капилляры, артериолы и венулы), так и крупные (аорта и ее крупные ветви). Пораженные кровеносные сосуды могут располагаться неглубоко под кожей, в самих внутренних органах и любых полостях.
В зависимости от причины болезни, выделяют 2 вида системного васкулита:
- первичный васкулит (выделяется как самостоятельное заболевание, при котором воспаляются сами сосуды);
- вторичный васкулит (появляется вследствие других заболеваний или является реакцией организма на появление инфекции).
Согласно общепринятой классификации, первичный васкулит может подразделяться на три группы, в зависимости от размеров воспаленных сосудов:
- воспаление мелких сосудов (геморрагический васкулит (пурпура Шенлейна-Геноха), гранулематоз (васкулит) Вегенера, микроскопический полиангиит, криоглобулинемический васкулит, синдром-Чардж-Стросса);
- воспаление средних сосудов (узелковый периартериит, болезнь Кавасаки);
- воспаление крупных сосудов (гигантоклеточный артериит (или височный артериит, болезнь Хортона), болезнь Такаясу);
- (гиперчувствительный аллергический васкулит, геморрагический васкулит Шенлейна-Геноха;
- узловатая эритема, узловатый васкулит, узелковый периартериит).
Также васкулит может поражать различные органы человека:
васкулит мозга, васкулит легких, васкулит нижних конечностей, васкулит глаз. Глаза при васкулите могут очень сильно пострадать (воспаление артерий сетчатки способно привести к кровоизлияниям и частичной потере зрения).
Обычно люди, впервые столкнувшиеся с этим заболеванием, интересуются, заразен ли васкулит. Первичный васкулит не заразен и не опасен для окружающих, однако вторичный (инфекционный) васкулит, появившийся на фоне инфекционных заболеваний, например менингита, может представлять эпидемическую опасность.
Васкулит при беременности может не только спровоцировать задержку развития плода, но и привести к выкидышу.
Симптомы и признаки васкулита
Симптомы васкулита различны. Они зависят от характера поражения, вида васкулита, локализации воспалительного процесса, а также от степени выраженности основного заболевания.
Несмотря на разнообразие вариантов, у многих больных имеются некоторые одинаковые проявления: лихорадка, геморрагическая сыпь на коже, слабость, истощение, боли в суставах и мышечная слабость, отсутствие аппетита, потеря веса, онемение отдельных частей тела.
Облитерирующий тромбангиит (или болезнь Бюргера) связан, в первую очередь, с поражением кровеносных сосудов конечностей, проявляется болью в ногах и появлением больших язв на коже (кожный васкулит на ногах).
Болезнь Кавасаки поражает главным образом детей в возрасте до пяти лет и имеет типичные признаки васкулита (покраснение кожи, лихорадка, возможно воспаление глаз).
Узелковый периартериит в основном поражает средние кровеносные сосуды в различных частях тела, включая почки, кишечник, сердце, нервную и мышечную систему, кожу. Кожные покровы отличаются бледностью, сыпь при васкулите данного типа имеет пурпурный цвет.
Микроскопический полиангиит затрагивает в основном мелкие сосуды на коже, легких и почках. Это приводит к патологическим изменениям в органах, к нарушениям их функций. Болезнь характеризуется значительными поражениями кожи, лихорадкой и потерей веса у больных, появлением гломерулонефрита (иммунного поражения клубочков почек) и кровохарканья (легочный васкулит)
Церебральный васкулит (или васкулит мозга) – тяжелое заболевание, выражающееся воспалением стенок сосудов головного мозга. Может привести к кровоизлиянию, некрозу тканей. Причины появления этого вида сосудистого васкулита еще выясняются.
Болезнь Такаясу поражает крупные артерии тела, в том числе аорту. В группе риска - молодые женщины. Признаки данного вида - слабость и боль в руках, слабый пульс, головные боли и проблемы со зрением.
Гигантоклеточный артериит (болезнь Хортона). Процесс охватывает преимущественно артерии головы. Характерны приступы головной боли, гиперчувствительность кожи головы, боли в мышцах челюсти при жевании, нарушения зрения вплоть до слепоты.
Васкулит Шелейна-Геноха (геморрагический васкулит) - это заболевание, поражающее в основном детей, но встречается также и у взрослых. Первые признаки геморрагического васкулита могут появиться через 1-4 недели после перенесенных инфекционных заболеваний, таких как скарлатина, ОРВИ, ангина и т.д. Приводит к воспалению кровеносных сосудов кожи, суставов, кишечника и почек. Характеризуется болью в суставах и животе, появлением крови в моче, покраснением кожи на ягодицах, ногах и ступнях.
Криоглобулинемический васкулит может быть связан с инфицированностью гепатитом С. Больной чувствует общую слабость, у него развивается артрит, на ногах - пятна пурпурного цвета.
Гранулематоз Вегенера вызывает воспаление кровеносных сосудов в носу, носовых пазухах, легких и почках. Типичные симптомы болезни - заложенность носа, а также частые носовые кровотечения, инфекции среднего уха, гломерулонефрит и воспаление легких.
Причины васкулита
Врачи еще не могут до конца определить причины первичного васкулита. Есть мнение, что это заболевание носит наследственный характер и связано с аутоиммунными нарушениями (аутоиммунный васкулит), плюс играют свою роль негативные внешние факторы и инфицирование золотистым стафилококком.
Причиной развития вторичного (инфекционно-аллергическоговаскулита) у взрослых является перенесенная инфекция.
Рассмотрены первичные и вторичные системные васкулиты у детей, клинические проявления, частота встречаемости, подходы к лечению. Приведен клинический пример.
Primary and secondary systemic vasculitis in children were considered, as well as clinical manifestations, frequency and approaches to treatment. A clinical case was given.
Ангиит или васкулит у детей — первичное или вторичное воспаление стенок кровеносных сосудов.
Первичные системные васкулиты — группа заболеваний, характеризующихся поражением стенки сосудов различного калибра (от микроциркуляторного русла до аорты и ее ветвей) по типу очагового воспаления и некроза с последующим вовлечением в патологический процесс органов и тканей в зоне сосудистого повреждения.
Вторичные васкулиты развиваются при инфекционных, аутоиммунных, ревматических, онкогематологических и других заболеваниях [1, 2].
Этиология большинства первичных васкулитов неизвестна. Полагают, что их возникновению у ребенка могут способствовать частые острые инфекционные болезни, очаги хронической инфекции, лекарственная аллергия, наследственная предрасположенность к сосудистым или ревматическим заболеваниям. Бактериальные или вирусные инфекции (стрептококковая, герпесвирусная, парвовирусная, гепатит В или С), с одной стороны, аллергия или отягощенный аллергологический анамнез. с другой стороны, по мнению специалистов, служат двумя равновеликими факторами, формирующими фон для гиперсенсибилизации организма или выступающими как триггерные, провоцирующие факторы.
В настоящее время установлено, что вирусная инфекция Эпштейна–Барр (ЭБВ) и инфекция герпеса человека 6-го типа ассоциированы с целым рядом аутоиммунных заболеваний (классические ревматические болезни, васкулиты, неспецифический язвенный колит и др.). Известно, что вирус герпеса человека 6-го типа у детей при первичном инфицировании и при его реактивации вызывает инфекционную эритему с симптомами васкулита, который наблюдается в 3 раза чаще, чем при ЭБВ и цитомегаловирусной инфекции (ЦМВ) [3–5].
Эти вирусы могут вызывать хронические манифестные и стертые формы заболевания, протекающие по типу хронического мононуклеоза. При этом развитие аутоиммунного заболевания может манифестировать через большой промежуток времени после инфицирования.
Герпетическая инфекция гистологически манифестирует отложением фибрина в микрососудах, при этом меняется поверхностная конформация эндотелия; на инфицированном эндотелии в 2–3 раза повышается уровень выработки тромбина, уменьшается тканевая экспрессия тромбомодулина и активация белка С (G. M. Vercelotti, 1990).
Изменения в области поврежденного участка сосуда разнообразны — от ишемии до кровоизлияния, некроза, инфаркта. Степень сосудистых расстройств зависит от калибра пораженных артерий и состояния коллатерального кровообращения [2].
Большое значение в развитии васкулитов имеют формирование, циркуляция и осаждение на стенках сосудов иммунных комплексов, антинейтрофильных цитоплазматических антител, иммунное пролиферативно-деструктивное воспаление стенки артерий различного калибра, повреждение эндотелия сосудов, повышение сосудистой проницаемости, гиперкоагуляция с нарушением кровотока, ишемия в зоне повреждения сосудов.
В начальный период васкулитов наблюдают общие проявления неспецифического воспалительного синдрома: субфебрильная или фебрильная лихорадка, артралгии, похудание, симптомы периферических и висцеральных сосудистых расстройств, умеренная анемия, лейкоцитоз в периферической крови, увеличение СОЭ, признаки гиперкоагуляции, диспротеинемия, повышение уровня С-реактивного белка, IgA, циркулирующих иммунных комплексов и криоглобулинов [2].
Своеобразие клинических проявлений обусловлено локализацией васкулита, калибром пораженных сосудов, распространенностью патологического процесса, особенностями морфологических изменений (преобладание деструктивных или пролиферативных процессов), степенью расстройств гемодинамики и ишемии органов и тканей.
Доказан сосудистый генез массивных кровоизлияний и некрозов при герпесвирусных энцефалитах. Ярким свидетельством морфологических изменений сосудов, которые удается прижизненно визуализировать при этих инфекциях, являются данные зарубежных и отечественных исследователей, указывающие на развитие коронарита после острой и чаще на фоне хронически текущей ЭБВ-инфекции, а также системного васкулита (синдрома Кавасаки). Коронарные повреждения обнаружены у 55% детей, перенесших ЭБВ-инфекционный мононуклеоз c длительностью лихорадки свыше 5 дней.
Известно, что при герпесвирусной инфекции имеет важное значение способность вирусов к цитопатическому эффекту, проявляющих тропизм к кровеносным сосудам. Поражение сосудов при ЭБВ регистрируется в 7–30%, а при ЦМВ — у 8% [4, 6–8].
Вирус герпеса человека 6-го типа у детей при первичном инфицировании и при его реактивации вызывает инфекционную эритему с симптомами васкулита, который наблюдается в 3 раза чаще, чем при ЭБВ- и ЦМВ-инфекции.
В течение нескольких лет авторами изучалась частота встречаемости и клинических проявлений синдрома васкулита у детей при различных вариантах течения герпесвирусных инфекций. Исследования проводились у 202 больных в возрасте от одного года до 14 лет, из них — 160 детей с инфекционным мононуклеозом (ИМ) и 42 — с синдромом васкулита без признаков инфаркта миокарда, находившихся в соматических и инфекционных отделениях Морозовской городской детской клинической больницы г. Москвы.
Кроме того, при УЗДГ-исследовании оценивалось состояние комплекса интима-медиа и состояния сосудов головы и шейной области у 20 детей в возрасте от 6 мес до 14 лет с активно персистирующими герпесвирусными инфекциями (ЭБВ, ЦМВ и ВГЧ 6-го типа без признаков ИМ) в условиях многопрофильной клиники Vessel Clinic.
В клинико-лабораторном мониторинге наблюдения за больными проводились исследования:
- общих анализов периферической крови, мочи, биохимии крови, коагулограммы;
- бактериологические исследования микробиоценоза ротоглотки, кишечника, паразитарных инфекций, гельминтов;
- серологические исследования осуществлялись методами: реакция иммунофлуоресценции (РИФ) на респираторные вирусы и РИФ с моноклональными антителами к белкам ЦМВ pp 65, рр 72;
- непрямая реакция иммунофлуоресценции (НРИФ) на антигены герпесвирусов в клетках крови и иммуноферментный анализ (ИФА) на герпесвирусы 1-го, 2-го, 4-го, 5-го и 6-го типов; микоплазмы, хламидии, парвовирус 19-го типа и др.;
- полимеразная цепная реакция (ПЦР) на ДНК ЭБВ, ЦМВ, ВПГ 1-го типа, ВПГ 2-го типа; ВГЧ 6-го типа в крови, слюне и моче.
Проявления васкулита имели место при всех этиологических вариантах ИМ в виде пятнисто-папулезной или пятнисто-папулезной с геморрагическим компонентом сыпи, которая чаще расценивалась как токсико-аллергическая у больных, получавших антибиотики аминопенициллинового ряда и реже у не получавших подобных препаратов (рис. 1, 2).
Проявления васкулита в виде геморрагической сыпи, по типу кожной пурпуры, с признаками тромбоваскулита отмечались у большинства больных, страдающих герпесвирусной активно персистирующей инфекцией без признаков инфекционного мононуклеоза, при этом сыпь не имела характерной для геморрагического васкулита (по типу Шенлейна–Геноха) локализации, элементы которой появлялись на различных участках кожи: в области груди, живота, спины, подмышечной впадины, голенях, которые распространялись на фоне лихорадки, а затем стихали. В местах сыпи у некоторых больных появлялась пигментация.
При дуплексном сканировании сосудов головы и шеи при активно персистирующих герпесвирусных инфекциях выявлялись ЭХО-признаки затруднения венозного оттока или ангиоспазма артерий Виллизиева круга, при явном уплотнении комплекса интима-медиа (КИМ) сосудов, что косвенно указывало на эндотелиальную дисфункцию, развившуюся, вероятнее всего, в результате длительного цитопатического воздействия на сосудистый эндотелий непосредственно активно персистирующих герпесвирусов.
.jpg)
В качестве клинического примера представлена история болезни ребенка Елизаветы С., 2 г. 11 мес (28.10.2010 г. рождения).
Состояние при поступлении тяжелое. Температура тела — 37,2? С. Кожные покровы бледные, на коже нижних конечностей пятнисто-папулезная сыпь с геморрагическим пропитыванием, элементы разных размеров, склонные к слиянию на стопах, несколько элементов на верхних конечностях, в области локтей.
Ангионевротические отеки левой стопы, правой кисти, движения в правом голеностопном суставе затруднены.
Зев гиперемирован, миндалины — налетов нет. Передне- и заднешейные, подчелюстные лимфоузлы до 2 см, безболезненные, не спаянные с окружающими тканями.
По остальным органам без видимой патологии.
УЗИ органов брюшной полости, почек, селезенки от 24.10.2013: ЭХО-признаки умеренной гепатомегалии, мезаденита.
По другим органам без выраженных структурных изменений и патологических включений.
Осмотр ЛОР-врача от 24.10.2013 — диагноз: левосторонний острый средний катаральный отит.
Результаты анализов крови представлены в таблицах 1–3.
За время пребывания в отделении отмечалось три волны высыпаний с крупными геморрагическими сливными элементами в бедренных и подколенных областях обеих конечностей и ангионевротическими отеками (рис. 3).
Клинический диагноз: геморрагический васкулит, смешанная форма (кожно-суставной синдром), протекающий на фоне реактивации смешанной персистирующей герпесвирусной инфекции ЭБВ, ВГЧ 6-го типа и бактериальной инфекции.
.jpg)
Рекомендовано включить в лечение глюкокортикоиды и Виферон по 1 млн в суппозиториях.
- Режим боксовый.
- Стол 15.
- Цефтриаксон 550 мл 2 раза в день в/в капельно 25.10.2013–30.10.2013 г.
- Супрастин 0,3 2 раза в день на физрастворе в/в.
- Бифидумбактерин 5 доз 3 раза в день в рот.
- Преднизолон 25 мг в/в в 10:00 с 25.10.2013–28.10.2013 г.
- Преднизолон 3 раза в день, в рот после завтрака — 10 мг, после обеда — 7,5 мг, после ужина — 5 мг с 31.10.2013 г.
- Гепарин 0,3 подкожно 6:00, 14:00, 22:00 с 25.10.2013–11.2013 г.
- Курантил 25 мг в таблетках 3 раза в день в рот с 25.10.2013–11.2013 г.
- Орошение зева Мирамистином 3 раза в день.
- Туалет носа физраствором 3 раза в день.
- Нафтизин 0,05% 1 капля 3 раза в день в нос.
- Отипакс 3 капли 3 раза в день в левое ухо.
- Мукалтин 1 таблетка 3 раза в день в рот.
- Свечи Виферон 500 000 1 раз в день ректально.
- Лосек 5 мг 2 раза в день, в рот за 30 мин до еды, на ночь с 31.10.2013–11.2013 г.
- Инфузионная терапия.
Состояние ребенка при выписке удовлетворительное. Не лихорадит. Катаральные явления купированы. Кожа чистая. Зев рыхлый. В легких дыхание пуэрильное, хрипов нет. Тоны сердца умеренной громкости, ритмичные. Живот мягкий, безболезненный. Стул и диурез в норме. Менингеальных знаков нет. Ребенок выписан домой с улучшением под наблюдение участкового педиатра.
Таким образом, в практической деятельности врача педиатра инфекциониста, семейного врача необходимо определять маркеры активной репликации герпетических вирусов 4-го, 5-го и 6-го типов не только у больных с типичными клиническими проявлениями инфекционного мононуклеоза, у длительно лихорадящих, часто болеющих; у детей с лимфаденопатиями, но и с синдромом васкулита с целью уточнения триггерных факторов его развития, а также предупреждения часто неоправданного и длительного назначения антибиотиков при ИМ и обоснования адекватной противовирусной терапии.
Лечение назначают с учетом нозологического диагноза, фазы болезни и ее клинических особенностей.
Выбор методов лечения васкулита предполагает воздействие на возможную причину и основные механизмы развития болезни. Воздействие на триггерный инфекционный агент, подавление иммунного воспаления путем назначения препаратов противовоспалительного и иммунодепрессивного действия: глюкокортикоидов (преднизолон, метилпреднизолон), цитостатиков (циклофосфамид, метотрексат).
Удаление антигенов и циркулирующих иммунных комплексов с использованием внутривенного введения антител, плазмафереза синхронно с пульс-терапией глюкокортикоидами и/или цитостатиками. Коррекция гемостаза: назначение антикоагулянтов, антиагрегантов. Симптоматическая терапия.
Эффект лечения оценивают по динамике клинических синдромов и лабораторных показателей. Лечение в острую фазу заболевания проводят в стационаре, затем продолжают амбулаторно при обязательном диспансерном наблюдении и контроле.
Литература
- Лыскина Г. А. Системные васкулиты. В кн.: Детская ревматология. Руководство для врачей / Под ред. А. А. Баранова, Л. К. Баженовой. М.: Медицина, 2002. С. 221–270.
- Vanhoutte P. M., Mombouli J. V. Vascular endothelium: vasoactive mediators // Prog. Cardiovasc. Dis. 1996. V. 39. Р. 229–238.
- Yamashita S., Murakami C., Izumi Y. Severe chronic active Epstein- Barr virus infection accompanied by virus-associated hemophagocytic syndrome, cerebellar ataxia and encephalitis // Psychiatry Clin. Neurosci. 1998. Aug; 52 (4): 449–452.
- Kragsbjerg P. Chronic active mononucleosis // Scand. J. Infect. Dis. 1997. 29 (5): 517–518.
- Okano M. Epstein-Barr virus infecion and its role in the expanding spectrum of human diseases // Acta Paediatr. 1998. Jan; 87 (1): 11–18.
- Толстикова Т. В., Брегель Л. В., Киклевич В. Т., Субботин В. М. Коронариты у детей // Сиб. мед. журн. 2009. № 2. С. 67–69.
- Nakagawa A., Ito M., Iwaki T. et al. Chronic active Epstein-Barr virus infection with giant coronary aneurysms // Am. J. Clin. Pathol. 1996. Vol. 105. N6. P. 733–736.
- Егорова О. Н., Балабанова Р. М., Чувиров Г. Н. Значение антител к герпетическим вирусам, определяемых у больных с ревматическими заболеваниями // Терапевтический архив. 1998. № 70 (5). С. 41–45.
Ф. С. Харламова* , 1 , доктор медицинских наук, профессор
Н. Ю. Егорова*, кандидат медицинских наук
О. В. Шамшева*, доктор медицинских наук, профессор
Н. Л. Вальтц**
А. В. Денисова***
* ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
** ГБУЗ Морозовская ДГКБ ДЗМ, Москва
*** Многопрофильная клиника Vessel Clinic, Москва
Читайте также:

