Какие инфекционные заболевания могут быть у грудничка
Обновлено: 22.04.2024
Врожденные инфекции у плода и новорожденного ребенка: виды, возбудители, клиника, диагностика
Передача врождённых и перинатальных инфекций плоду происходит через плаценту (внутриутробные инфекции), во время родов или при контакте с физиологическими жидкостями матери. Длительное разрушение плодных оболочек также способствует развитию внутриутробных заболеваний. Кроме того, заражение может произойти и после рождения (при контакте с матерью и другими людьми).
Врожденная краснуха
Первый признак врождённой краснухи — желтуха, как следствие развития гепатита. Часто возникает гемолиз и тромбоцитопеническая пурпура, а также слабовыраженные клинические проявления менингоэнцефалита. У некоторых новорождённых обнаруживают признаки метафизарной дисплазии. Инфицированные дети при рождении обычно имеют сниженную массу тела и отстают в физическом развитии.
В тяжёлых случаях болезнь обычно заканчивается летальным исходом. Наиболее грозные осложнения — незаращение артериального протока, катаракта, глухота, ретинопатия.
Тест на антитела к краснухе (IgM), которые можно обнаружить в крови детей до 3-го мес жизни, даёт положительный результат. При заболевании матери в I триместре вероятность развития патологии у ребёнка составляет 60%, поэтому некоторые женщины предпочитают прерывать беременность. В дальнейшем риск заметно снижается (2% после 20-й нед), в связи с чем выбор между рождением ребенка с вероятными нарушениями в развитии и прерыванием беременности необходимо делать крайне осторожно.
Цитомегаловирус у плода и новорожденного
Инфекция проявляется примерно в 1% случаев, при этом тяжёлая форма заболевания развивается только у 1% инфицированных. Наиболее высокий риск заражения плода отмечают на сроке гестации, соответствующем I триместру беременности. Симптомы заболевания у новорождённых — сниженная масса тела, гепатомегалия, спленомегалия, тромбоцитопения, продолжительная желтуха, повышенная возбудимость, судорожный синдром, аномальный мышечный тонус и двигательные расстройства.
Наиболее частые осложнения — микроцефалия, нейросенсорная глухота. Нередко обнаруживают кальцификацию головного мозга, гемиплегию (паралич мышц одной стороны тела), замедление психомоторных реакций, хориоретинит и миопатию. Диагностика основана на обнаружении антител к цитомегаловирусу (IgM) или определении экскреции вируса в течение первых двадцати дней жизни.
Возбудитель ЦМВ инфекции
Врожденная инфекция вируса простого герпеса
Первичная инфекция, вызванная вирусом простого герпеса, сопровождается виремией. При этом может произойти трансплацентарное заражение плода. При врождённом инфицировании дети рождаются с тяжёлыми отклонениями (пневмония, менингоэнцефалит, гепатоспленомегалия, цитопения), но лишь у некоторых из них присутствуют герпетические очаги на коже и слизистых оболочках. Лечение ацикловиром позволяет снизить смертность с 80—90% до 10—15%.
Терапию следует начинать до получения результатов лабораторного анализа. Первичная инфекция также возникает при заражении от матери, страдающей генитальным герпесом. При этом в первые дни жизни ребёнка возникают очаги на коже, конъюнктиве, слизистой оболочке рта и половых органов, а в 50% случаев наблюдают генерализованное течение инфекции. Лечение: внутривенное введение ацикловира.
Ветряная оспа плода
Инфицирование плода ветряной оспой возникает при заражении беременной в I—II триместре беременности, при этом вероятность передачи инфекции плоду составляет 3%. Заболевание характеризуется развитием рубцовой контрактуры в области лимбических структур головного мозга, микроцефалии или офтальмомикрии. Непривитые беременные в течение десяти дней после возможного заражения (контакта) должны пройти профилактический курс введения иммуноглобулина (содержащим антитела к вирусу ветряной оспы).
Ветряная оспа новорождённых возникает при заболевании матери в течение одной недели до родов. Смертность составляет 40%, поэтому в первые 48 ч жизни ребёнку необходимо ввести специфический иммуноглобулин. При ухудшении состояния следует незамедлительно начать лечение ацикловиром. Применение нормального иммуноглобулина человека не защищает новорождённого от заражения. В некоторых странах применяется вакцина.
Врожденный листериоз
Трансплацентарная передача Listeria monocytogenes происходит при заражении матери инфекцией, протекающей бессимптомно. Заболевание матери на ранних стадиях беременности обычно приводит к смерти плода, а на более поздних — к преждевременным родам. Инфекцию новорождённых обычно осложняет бактериемия, гепатоспленомегалия, менингоэнцефалит, тромбоцитопения и пневмония. При интранатальном заражении инфекция развивается в течение первых двух недель жизни ребенка и сопровождается менингитом и бактериемией.
Для выделения возбудителя на анализ отбирают кровь, спинномозговую жидкость, плацентарную ткань и послеродовую жидкость из матки. Инфицированную мать и ребёнка помещают в отдельную палату, так как они могут стать причиной вспышки заболевания в родильном отделении. Препарат выбора — ампициллин (иногда в комплексе с гентамицином); длительность лечения 2—6 нед.
Врожденный сифилис
Благодаря эффективным пренатальным исследованиям случаи врождённого сифилиса в настоящее время достаточно редки. У заражённых детей обнаруживают лихорадку, а также симптомы, свойственные вторичному сифилису, сыпь, кондиломы и трещины на слизистых оболочках. При развитии остеохондритов возникает выраженный болевой синдром. Очень часто отмечают постоянный насморк (сопение, гнусавость).
Для подтверждения диагноза применяют темнопольную микроскопию образцов поражённой кожи и слизистых оболочек. Специфические IgM или другие антитела персистируют в организме свыше 6 мес после перенесённой инфекции. Поздние симптомы (глухота, атрофия зрительного нерва, паретический нейросифилис) наблюдают в возрасте 12—20 лет. Нередко возникают бугристые образования на лобных костях, хронический большеберцовый периостит, перфорация передних зубов, деформация первых постоянных коренных зубов и высокий изгиб нёба. Препарат выбора — пенициллин.
Врожденный токсоплазмоз
Вероятность врождённого токсоплазмоза варьирует в разных регионах. Например, в Великобритании его регистрируют достаточно редко, а во Франции — часто. При заражении беременной трансплацентарную передачу инфекции плоду наблюдают в каждом третьем случае. Наиболее высок риск развития патологии плода (мертворождение, смерть после рождения, кальцификация головного мозга, церебральный паралич и эпилепсия) при заражении женщины в I и II триместре беременности.
Хориоретинит может возникать только спустя некоторое время после рождения и быть единственным симптомом болезни. Токсоплазмоз у матери подтверждают при обнаружении специфических антител (IgM) или сероконверсии. IgM также обнаруживают у инфицированных новорождённых. Применение спирамицина позволяет снизить риск трансплацентарного заражения, но не влияет на исход заболевания у новорождённых.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Грудные дети, у которых только начинается формирование крепкого иммунитета, являются беззащитными перед различными вирусными заболеваниями. На самом деле с этим утверждением можно как поспорить, так и согласиться с ним. С одной стороны ребенка защищают материнские антитела, которые поступают через молозиво, в начале грудного вскармливания, а ранее они поступали через плаценту. С другой стороны, у грудничков наблюдается снижение показателей иммунного ответа, именно поэтому они традиционно входят в группу риска развития осложнений и тяжелого течения ОРВИ, например.
Организм ребенка старается не допустить ситуации, когда иммунитет реагирует чрезмерно бурно на любые инфекции, что может привести к развитию сильного болевого синдрома и лихорадки. Но заболеть грудничок все равно может. Каким же образом можно защитить грудного ребенка от вирусов и что делать, как лечить и что принимать, если малыш уже заболел?
Правильное становление и развитие иммунной системы – это главное условие для того, чтобы человек жил долго и по возможности счастливо. От состояния иммунитета зависит, будет ли человек устойчив к патогенам или же он будет постоянно болеть, сталкиваясь с заболеваниями бактериальной, вирусной и грибковой природы, а также с различными иммунодефицитными состояниями.
Не все знают, что процесс созревания главного щита организма – иммунной системы – длится многие годы. При этом иммунологическую память мы не получаем по наследству от родителей, а приобретаем ее в процессе развития.
Первый этап формирования иммунной системы у будущего младенца начинается еще во время внутриутробного периода, во время становления сложных связей между его организмом и организмом матери. Процесс протекает весьма успешно – уже на 10-12-й неделе беременности у плода начинается синтез собственных иммуноглобулинов М. Постепенно их становится все больше. Потом подключаются Т-лимфоциты, и особенно резко их число вырастает на шестые сутки после родов. Но все же, как уже упоминалось, иммунная система младенца находится в состоянии физиологического угнетения. Мудрая природа позаботилась о том, чтобы у новорожденного, который после рождения сталкивается с большим количеством антигенов, не было слишком бурных иммунных реакций, которые могут навредить ему же.
Сразу после рождения малыша защищают материнские антитела, которые находятся у него в крови. Далее начинается поэтапное развитие иммунной системы, которая всю жизнь будет защищать ребенка от вирусных и других заболеваний. i
Критические периоды в формировании иммунной системы ребенка

Первый период длится до двадцати восьми дней, когда ребенок является новорожденным и только-только начинает познавать этот мир. Его защищают материнские антитела, но они не способны быть надежным щитом от болезней, поэтому новорожденные очень восприимчивы к вирусным инфекциям и даже влиянию собственных условно-патогенных микроорганизмов. При бактериальных инфекциях возможно их распространение по всему организму малыша, повышая риск развития хронических болезней в дальнейшем.
Третий период длится с трех до пяти лет жизни ребенка, четвертый период приходится на шесть-семь лет. Пятый критический период развития иммунной системы период у девочек наблюдается в двенадцать-тринадцать лет, а у мальчиков – в четырнадцать-пятнадцать. И во время всех этих периодов дети подвержены множеству заболеваний, их иммунитет не совершенен.
Но, безусловно, один из самых сложных периодов становления иммунной системы – это период до года, когда ребенок только учится справляться с невзгодами окружающего мира и инфекциями, которые подстерегают его на каждом шагу.
ОРВИ у грудного ребенка: что делать?
Простуда и грипп у новорожденных встречаются достаточно редко. Ближе к полугоду, когда действие антител матери постепенно становится более слабым, вероятность развития простуды у ребенка возрастает. Малыш вполне может заразиться от близких людей, в поликлинике или на улице. У детей, находящихся на искусственном вскармливании, риск заболеть выше.
Основная проблема при ОРВИ у младенца состоит в том, что это часто встречаемое заболевание весьма непросто у него распознать. Взрослый человек при простуде и гриппе обычно жалуется на повышенную температуру тела, слабость, ломоту в мышцах, боль в горле, кашель и насморк. Грудной ребенок в силу своего возраста не способен пожаловаться на симптомы, более того, у него еще не сформированы некоторые рефлексы. Он еще не научился сморкаться и откашливаться. Это приводит к тому, что слизь скапливается в области дыхательных путей, где служит питательной средой для бактерий. В результате в дополнение к простуде у ребенка может развиться отит, бронхит, который может стать хроническим, или даже пневмония, что требует немедленной помощи педиатров. В эпоху COVID-19 также могут потребоваться соответствующая дополнительная диагностика и лечение.
Когда нос заложен, ребенок может отказываться от пищи даже когда голоден. А лихорадки у него может и не быть. Чтобы вовремя заметить начало развития болезни, родителям необходимо быть внимательными к грудничку и вовремя приступать к лечению. В большинстве случаев рекомендуется применять специфическую противовирусную терапию. Ее надо начинать сразу же после обнаружения первых признаков болезни. Уже в первые сутки необходимо принимать противовирусные препараты.
Перед тем, как дать ребенку лекарство, обязательно читайте инструкцию. Дело в том, что препаратов, чье применение разрешено для детей до года, совсем немного. Недопустимо лечить грудничка препаратами, которые используются для лечения взрослых или более старших детей.
Что принимать при вирусной инфекции у грудного ребенка?
Один из препаратов, который может применяться для лечения самых маленьких детей, в том числе новорожденных и недоношенных детей с гестационным возрастом менее 34 недель – это противовирусный препарат ВИФЕРОН.
ВИФЕРОН обладает широким спектром противовирусной активности. Альфа-2b интерферон, который входит в состав препарата, создан на основе современных технологий. П ротивовирусные свойства позволяют ему блокировать размножение вируса, а иммуномодулирующий эффект способствует восстановлению иммунитета. Препарат разработан в результате фундаментальных исследований в области иммунологии, доказавших, что в присутствии антиоксидантов (витамины С, Е и другие) усиливается противовирусное действие интерферона.
Для лечения детей до года применяется препарат ВИФЕРОН в форме свечей и геля. Мазь используется для лечения детей старше 1 года.
Детям до 7 лет, в т.ч. новорожденным и недоношенным с гестационным возрастом более 34 недель, назначают ВИФЕРОН Свечи (суппозитории) 150 000 ME по 1 суппозиторию 2 раза/сут через 12 ч ежедневно в течение 5 суток. По клиническим показаниям терапия может быть продолжена. Перерыв между курсами составляет 5 суток.
Недоношенным новорожденным детям с гестационным возрастом менее 34 недель рекомендовано применение препарата ВИФЕРОН 150 000 МЕ по 1 суппозиторию 3 раза в сутки через 8 ч ежедневно в течение 5 суток.
В зависимости от рекомендаций педиатра для лечения ОРВИ необходимо 3-5 раз в день в течение 5 дней наносить полоску ВИФЕРОН Гель длиной примерно 0,5 см на слизистую оболочку носа. До этого слизистую лучше промыть солевым раствором. Для того, чтобы уберечь ребенка от ОРВИ, необходимо 2 раза в день в качестве профилактики наносить полоску геля длиной примерно 0,5 см на слизистую оболочку носа. Длительность курса – 2-4 недели.
Аденовирусная инфекция у младенцев: лечение и профилактика
Аденовирусная инфекция – это разновидность ОРВИ. Заболевание способно поразить как верхние, так и нижние дыхательные пути, а также стать причиной развития таких заболеваний, как бронхит, трахеит, фарингит и воспаление легких. Заболеть ребенок может в любое время года, но чаще всего аденовирусная инфекция встречается в зимне-весенний период. На долю аденовирусов приходится примерно 17% всех случаев ОРВИ. iii
Попав в организм ребенка, вирус начинает размножаться с огромной скоростью. Он способен легко проникать в кровь и распространяться дальше не только по кровеносным сосудам, но и по лимфатическим. Вирус, содержащий молекулу ДНК, может заразить лимфоидную ткань, ЖКТ и даже конъюнктиву глаза, а также привести к развитию так называемого кишечного гриппа.
Среди симптомов, которые появляются у ребенка при аденовирусной инфекции, – слизистые выделения из носа, покраснение полости рта, снижение аппетита, вялость и слабость, покраснение глаз и конъюнктивит, диарея.
Для диагностики заболевания могут применять лабораторные методы исследования, когда на анализ берется кровь. При подозрении на аденовирусную инфекцию врач может рекомендовать провести микроскопические исследования содержимого носа и ротоглотки. Это необходимо сделать в целях исключения бактериальной инфекции.
Чем лечить инфекцию?
Терапия при аденовирусной инфекции показана симптоматическая, а также с применением противовирусных препаратов, в том числе препарата ВИФЕРОН. Для профилактики ребенку необходимо полноценное и здоровое питание, активность по возрасту, поддержание здорового веса, регулярные прогулки на свежем воздухе, проветривание помещений и поддержание достаточного уровня влажности, особенно в сезон отопления.
Цитомегаловирусная инфекция у грудничков
Цитомегаловирусная инфекция (ЦМВ) относится к широко распространенным инфекциям и характеризуется многообразием проявлений от отсутствия каких-либо симптомов до развития тяжелых генерализованных форм с поражением внутренних органов и центральной нервной системы. Инфекция относится к персистирующим – она способна практически незаметно локализоваться в железистой ткани.
ЦМВ у детей до года может протекать в различных клинических формах, требующих проведения дифференцированной терапии. Если ранее у беременной женщины была выявлена ЦМВ, ребенка необходимо обязательно обследовать по причине того, что это инфекционное заболевание может существенно влиять на развитие малыша и качество его жизни.
Пока не существует методов, при помощи которых можно элиминировать вирус, т.е. полностью избавиться от вируса в организме, но при применении ряда препаратов, в том числе противовирусного препарата ВИФЕРОН, можно добиться переведения активно размножающегося вируса в латентное состояние, при котором он будет персистировать в клетках и никак себя не проявлять. iv
Причины инфекции у новорожденных. Определяемся
Проводится рентгенография грудной полости наряду со скринингом сепсиса, включающим полный анализ крови для выявления нейтропении и культур крови. Белки острой фазы (С-реактивный белок — СРБ) полезны, однако для их увеличения требуется 12-24 ч, поэтому один положительный результат не исключает инфекцию, однако два последовательных нормальных значения достоверно подтверждают отсутствие инфекции.
Антибиотики назначают сразу же, не дожидаясь результатов посева культуры. Антибиотики против стрептококков группы В, Listeria monocytogenes и других грамположительных микроорганизмов (обычно бензилпенициллин или амоксициллин) вводятся внутривенно в сочетании с антибиотиками против грамотрицательных бактерий (обычно аминогликозидами, например гентамицином). Если результат посева культур и ЦРП отрицательный и младенец клинически выздоравливает, через 48 ч прекращается введение антибиотиков.
Если результат посева культур положительный и если имеются какие-либо неврологические признаки, необходимо провести обследование и посев СМЖ.

Инфекции новорожденных с поздним началом (>72 ч)
Спустя 72 ч после рождения источником инфекции становится обстановка, окружающая ребёнка. Проявления инфекции обычно неспецифичные.
Клинические особенности неонатального сепсиса:
- Жар, или нестабильность температуры, или гипотермия.
- Плохое питание.
- Рвота.
- Апноэ и брадикардия.
- РДС.
- Сонливость.
- Желтушность.
- Нейтропения.
- Гипо-/гипергликемия.
- Шок.
- Раздражительность.
- Судороги.
- Вздутие живота.
При менингите у новорожденных наблюдают:
- отведение головы кзади (опистотонус);
- напряжённые или выбухающие роднички.
В неонатальном отделении или послеродовой палате имеется высокий риск инфицирования нозокомиальными инфекциями. Весь персонал должен строго придерживаться правил по эффективной обработке рук для предотвращения перекрёстного инфицирования. При интенсивной терапии другими основными источниками инфицирования являются установленные катетеры для парентерального питания или забора проб крови для анализа газового состава, трахеальные трубки, инвазивные процедуры, нарушающие защитный кожный барьер.
В данной ситуации коагулазонегативный стафилококк (Staph, epidermidis) является наиболее часто встречающимся патогеном, однако спектр микроорганизмов широкий и включает Staph, aureus, Escherichia coli, Pseudomonas species, грибы, например Candida. Цель первоначальной терапии (например, флуклоксациллином или гентамицином) — ирадикация большинства стафилококков и грамотрицательных бактерий. Если микроорганизмы устойчивы к этим антибиотикам или состояние младенца не улучшается, необходимы более мощные антибиотики (например, ванкомицин). Серийные исследования белков острой фазы (СРВ) позволяют проводить мониторинг ответа на терапию.
Менингит в неонатальном периоде встречается редко, однако уровень смертности при нём составляет 20-50%, а у трети выживших младенцев остаются серьёзные последствия. Клинические признаки аналогичны таковым при других формах неонатального сепсиса. Выбухание родничка и гиперэкстензия шеи и спины (опистотонус) являются поздними признаками.
Если подозревается менингит, назначают ампициллин или пенициллин и цефалоспорин III поколения (например, цефотаксим, проникающий в СМЖ).
Осложнения включают абсцесс мозга, вентрикулит, гидроцефалию, нарушения слуха и развития нервной системы.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021

В разделе собраны ссылки на статьи по болезням кожи новорожденного ребенка, их диагностике, лечению. Отдельно собраны статьи по уходу за неонатальной кожей.
3. Папулосквамозные поражения кожи у детей (образования кожи с шелушением)
а) Псориаз
б) Красный волосяной лишай (КВЛ)
в) Фолликулярный кератоз (болезнь Дарье)
г) Ладонно-подошвенная кератодермия
д) Порокератозы
е) Аллергический контактный дерматит
ж) Атопический дерматит
з) Себорейный дерматит
з) Ладонно-подошвенный дерматоз
и) Периоральный дерматит
й) Розовый лишай
к) Парапсориаз
л) Красный плоский лишай
м) Блестящий лишай
н) Полосовидный лишай
о) Грибковые болезни - дерматофитии
4. Везикуло-буллезная сыпь у детей (образования кожи с пузырями)
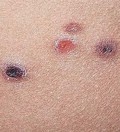
а) Вирусные инфекции кожи
б) Бактериальные инфекции кожи
в) Иммуннные дерматозы
г) Механические пузыри
д) Поражение паразитами: чесотка и педикулез
5. Узлы и опухоли кожи у детей
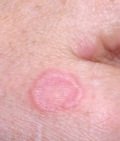
а) Поверхностные узлы и опухоли кожи
Дополнительно рекомендуем раздел сайта по дерматоонкологии (опухолям кожи)
В разделе собраны статьи по эпидемиологии, этиологии, диагностике, лечению рака кожи.
Перейти в раздел опухоли кожи
Перейти в раздел лимфомы кожи
б) Глубокие узлы и опухоли дермы
6. Нарушения пигментации кожи у детей
а) Гиперпигментации - темные пятна на коже
б) Гипопигментации - светлые пятна на коже
в) Дополнительно рекомендуем посетить раздел статей по невусам - родинкам
В разделе собраны ссылки на статьи по невусам всех видов. Невусы в народе также называются родинками.
г) Дополнительно рекомендуем посетить раздел статей по пигментным пятнам кожи - меланозам
В разделе собраны ссылки на статьи по невусам всех видов. Невусы в народе также называются родинками.
Внутриутробные инфекции – группа заболеваний плода и новорожденного, развивающихся вследствие заражения в дородовом периоде или в родах. Внутриутробные инфекции могут приводить к гибели плода, самопроизвольному аборту, задержке внутриутробного развития, преждевременным родам, формированию врожденных пороков, поражению внутренних органов и ЦНС. Методы диагностики внутриутробных инфекций включают микроскопические, культуральные, иммуноферментные, молекулярно-биологические исследования. Лечение внутриутробных инфекций проводится с использованием иммуноглобулинов, иммуномодуляторов, противовирусных, антибактериальных препаратов.

Общие сведения
Внутриутробные инфекции – патологические процессы и заболевания, обусловленные антенатальным и интранатальным инфицированием плода. Истинная распространенность внутриутробных инфекций не установлена, однако, согласно обобщенным данным, с врожденными инфекциями рождается не менее 10% новорожденных. Актуальность проблемы внутриутробных инфекций в педиатрии обусловлена высокими репродуктивными потерями, ранней неонатальной заболеваемостью, приводящей к инвалидизации и постнатальной гибели детей. Вопросы профилактики внутриутробных инфекций лежат в плоскости рассмотрения акушерства и гинекологии, неонатологии, педиатрии.

Причины внутриутробных инфекций
Внутриутробные инфекции развиваются в результате инфицирования плода в дородовом периоде или непосредственно во время родов. Обычно источником внутриутробной инфекции для ребенка выступает мать, т. е. имеет место вертикальный механизм передачи, который в антенатальном периоде реализуется трансплацентарным или восходящим (через инфицированные околоплодные воды) путями, а в интранатальном - аспирационным или контактным путями.
Реже происходит ятрогенное инфицирование плода в период беременности при проведении женщине инвазивной пренатальной диагностики (амниоцентеза, кордоцентеза, биопсии ворсин хориона), введении плоду препаратов крови через сосуды пуповины (плазмы, эритроцитарной массы, иммуноглобулинов) и т. д.
В антенатальном периоде инфицирование плода обычно связано с вирусными агентами (вирусами краснухи, герпеса, цитомегалии, гепатита В и С, Коксаки, ВИЧ) и внутриклеточными возбудителями (токсоплазмоза, микоплазмоза).
В интранатальном периоде чаще происходит микробная контаминация, характер и степень которой зависит от микробного пейзажа родовых путей матери. Среди бактериальных агентов наиболее распространены энтеробактерии, стрептококки группы В, гонококки, синегнойная палочки, протей, клебсиелла и др. Плацентарный барьер непроницаем для большинства бактерий и простейших, однако при повреждении плаценты и развитии фетоплацентарной недостаточности, может произойти антенатальное микробное инфицирование (например, возбудителем сифилиса). Кроме этого, не исключается и интранатальное вирусное заражение.
Факторами возникновения внутриутробных инфекций служат отягощенный акушерско-гинекологический анамнез матери (неспецифические кольпиты, эндоцервициты, ЗППП, сальпингофориты), неблагополучное течение беременности (угроза прерывания, гестозы, преждевременная отслойка плаценты) и инфекционная заболеваемость беременной. Риск развития манифестной формы внутриутробной инфекции существенно выше у недоношенных детей и в том случае, когда женщина инфицируется первично во время беременности.
Известно, что тяжесть проявлений инфекционного процесса у беременной и у плода может не совпадать. Бессимптомное или малосимптомное течение инфекции и у матери может вызвать тяжелые поражения плода, вплоть до его гибели. Это связано с повышенным тропизмом вирусных и микробных возбудителей к эмбриональным тканям, преимущественно ЦНС, сердца, органа зрения.
Классификация
Этиологическая структура внутриутробных инфекций предполагает их деление на:
- вирусные (вирусный гепатит, герпес, краснуха, ОРВИ, цитомегалия, эпидемический паротит, энтеровирусная инфекция)
- бактериальные (туберкулез, сифилис, листериоз, сепсис)
- паразитарные и грибковые (микоплазмоз, токсоплазмоз, хламидиоз, кандидоз и др.)
Для обозначения группы наиболее распространенных внутриутробных инфекций используется аббревиатура TORCH-синдром, объединяющий токсоплазмоз (toxoplasmosis), краснуху (rubella), цитомегалию (cytomegalovirus), герпес (herpes simplex). Буквой О (other) обозначаются другие инфекции, в числе которых - вирусные гепатиты, ВИЧ-инфекция, ветряная оспа, листериоз, микоплазмоз, сифилис, хламидиоз и др.).
Симптомы внутриутробных инфекций
Наличие внутриутробной инфекции у новорожденного может быть заподозрено уже во время родов. В пользу внутриутробного инфицирования может свидетельствовать излитие мутных околоплодных вод, загрязненных меконием и имеющих неприятный запах, состояние плаценты (полнокровие, микротробозы, микронекрозы). Дети с внутриутробной инфекцией часто рождаются в состоянии асфиксии, с пренатальной гипотрофией, увеличенной печенью, пороками развития или стигмами дисэмбриогенеза, микроцефалией, гидроцефалией. С первых дней жизни у них отмечается желтуха, элементы пиодермии, розеолезных или везикулезных высыпаний на коже, лихорадка, судорожный синдром, респиратрные и кардиоваскулярные расстройства.
Ранний неонатальный период при внутриутробных инфекциях нередко отягощается интерстициальной пневмонией, омфалитом, миокардитом или кардитом, анемией, кератоконъюнктивитом, хориоретинитом, геморрагическим синдромом и др. При инструментальном обследовании у новорожденных могут обнаруживаться врожденная катаракта, глаукома, врожденные пороки сердца, кисты и кальцификаты мозга.
В перинатальном периоде у ребенка отмечаются частые и обильные срыгивания, мышечная гипотония, синдром угнетения ЦНС, серый цвет кожных покровов. В поздние сроки при длительном инкубационном периоде внутриутробной инфекции возможно развитие поздних менингитов, энцефалитов, остеомиелита.
Рассмотрим проявления основных внутриутробных инфекций, составляющих TORCH-синдром.
Врождённый токсоплазмоз
Внутриутробное инфицирование одноклеточным протозойным паразитом Toxoplasma Gondii приводит к тяжелым поражениям плода – задержке развития, врожденным порокам развития мозга, глаз, сердца, скелета.
После рождения в остром периоде внутриутробная инфекция проявляется лихорадкой, желтухой, отечным синдромом, экзантемой, геморрагиями, диареей, судорогами, гепатоспленомегалией, миокардитом, нефритом, пневмонией. При подостром течении доминирую признаки менингита или энцефалита. При хронической персистенции развивается гидроцефалия с микроцефалией, иридоциклит, косоглазие, атрофия зрительных нервов. Иногда встречаются моносимптомные и латентные формы внутриутробной инфекции.
К числу поздних осложнений врожденного токсоплазмоза относятся олигофрения, эпилепсия, слепота.
Врождённая краснуха
Внутриутробная инфекция возникает из-за заболевания краснухой при беременности. Вероятность и последствия инфицирования плода зависят от гестационного срока: в первые 8 недель риск достигает 80%; последствиями внутриутробной инфекции могут служить самопроизвольное прерывание беременности, эмбрио- и фетопатии. Во II триместре риск внутриутробного инфицирования составляет 10-20%, в III – 3-8%.
Дети с внутриутробной инфекцией обычно рождаются недоношенными или с низкой массой тела. Для периода новорожденности характерна геморрагическая сыпь, длительная желтуха.
Классические проявления врожденной краснухи представлены триадой Грега: поражением глаз (микрофтальмией, катарактой, глаукомой, хориоретинитом), ВПС (открытым артериальным протоком, ДМПП, ДМЖП, стенозом легочной артерии), поражением слухового нерва (сенсоневральной глухотой). В случае развития внутриутробной инфекции во второй половине беременности у ребенка обычно имеется ретинопатия и глухота.
Кроме основных проявлений врожденной краснухи, у ребенка могут выявляться и другие аномалии: микроцефалия, гидроцефалия, расщелины нёба, гепатит, гепатоспленомегалия, пороки развития мочеполовой системы и скелета. В дальнейшем внутриутробная инфекция напоминает о себе отставанием ребенка в физическом развитии, ЗПР или умственной отсталостью.
Врождённая цитомегалия
Внутриутробное заражение цитомегаловирусной инфекцией может приводить к локальному или генерализованному поражению многих органов, иммунодефициту, гнойно-септическим осложнениям. Врожденные дефекты развития обычно включают микроцефалию, микрогирию, микрофтальмию, ретинопатию, катаракту, ВПС и др. Неонатальный период врожденной цитомегалии осложняется желтухой, геморрагическим синдромом, двусторонней пневмонией, интерстициальным нефритом, анемией.
К отдаленным последствиям внутриутробной инфекции относятся слепота, нейросенсорная глухота, энцефалопатия, цирроз печени, пневмосклероз.
Врождённая герпетическая инфекция
Внутриутробная герпес-инфекция может протекать в генерализованной (50%), неврологической (20%), слизисто-кожной форме (20%).
Генерализованная внутриутробная врожденная герпетическая инфекция протекает с выраженным токсикозом, респираторным дистресс-синдромом, гепатомегалией, желтухой, пневмонией, тромбоцитопенией, геморрагическим синдромом. Неврологическая форма врожденного герпеса клинически проявляется энцефалитом и менингоэнцефалитом. Внутриутробная герпес-инфекция с развитием кожного синдрома сопровождается появлением везикулярной сыпи на кожных покровах и слизистых оболочках, в т. ч. внутренних органов. При наслоении бактериальной инфекции развивается сепсис новорожденных.
Внутриутробная герпес-инфекция у ребенка может приводить к формированию пороков развития - микроцефалии, ретинопатии, гипоплазии конечностей (кортикальной карликовости). В числе поздних осложнений врожденного герпеса - энцефалопатия, глухота, слепота, задержка психомоторного развития.
Диагностика
В настоящее время актуальной задачей является пренатальная диагностика внутриутробных инфекций. С этой целью на ранних сроках беременности проводится микроскопия мазка, бактериологический посев из влагалища на флору, ПЦР-исследование соскоба, обследование на TORCH-комплекс. Беременным из группы высокого риска по развитию внутриутробной инфекции показана инвазивная пренатальная диагностика (аспирация ворсин хориона, амниоцентез с исследованием амниотической жидкости, кордоцентез с исследованием пуповинной крови).
Возможно выявление эхографических маркеров внутриутробных инфекций с помощью акушерского УЗИ. К косвенным эхографическим признакам внутриутробного инфицирования относятся маловодие или многоводие; наличие гиперэхогенной взвеси в околоплодных водах или амниотических тяжей; гипоплазия ворсин хориона, плацентит; преждевременное старение плаценты; отечный синдром плода (асцит, перикардит, плеврит), гепатоспленомегалия, кальцификаты и пороки развития внутренних органов и др. В процессе допплерографического исследования кровотока выявляются нарушения плодово-плацентарного кровотока. Кардиотокография обнаруживает признаки гипоксии плода.
После рождения ребенка с целью достоверной верификации этиологии внутриутробной инфекции используются микробиологические (вирусологические, бактериологические), молекулярно-биологические (ДНК-гибридизация, ПЦР), серологические (ИФА) методики обследования. Важное диагностическое значение имеет гистологическое исследование плаценты.
По показаниям новорожденные с внутриутробными инфекциями в первые сутки жизни должны быть осмотрены детским неврологом, детским кардиологом, детским офтальмологом и др. специалистами. Целесообразно провести ЭхоКГ, нейросонографию, офтальмоскопию, исследование слуха методом вызванной отоакустической эмиссии.
Лечение внутриутробных инфекций
Общие принципы лечения внутриутробных инфекций предполагают проведение иммунотерапии, противовирусной, антибактериальной и посиндромной терапии.
Иммунотерапия включает применение поливалентных и специфических иммуноглобулинов, иммуномодуляторов (интерферонов). Противовирусная терапия направленного действия осуществляется, главным образом, ацикловиром. Для противомикробной терапии бактериальных внутриутробных инфекций используются антибиотики широкого спектра действия (цефалоспорины, аминогликозиды, карбапенемы), при микоплазменной и хламидийной инфекциях – макролиды.
Посиндромная терапия внутриутробных инфекций направлена на купирование отдельных проявлений перинатального поражения ЦНС, геморрагического синдрома, гепатита, миокардита, пневмонии и т. д.
Прогноз и профилактика
При генерализованных формах внутриутробных инфекций летальность в неонатальном периоде достигает 80%. При локальных формах возникают серьезные поражения внутренних органов (кардиомиопатии, ХОБЛ, интерстициальный нефрит, хронический гепатит, цирроз и т. д.). Практически во всех случаях внутриутробные инфекции приводят к поражению ЦНС.
Профилактика внутриутробных инфекций заключается в проведении предгравидарной подготовки, лечении ЗППП до наступления беременности, исключении контактов беременной с инфекционными больными, коррекции программы ведения беременности у женщин групп риска. Женщины, ранее не болевшие краснухой и не получавшие прививки против краснухи, должны быть вакцинированы не позднее, чем за 3 месяца до предполагаемой беременности. В ряде случаев внутриутробные инфекции могут являться основанием для искусственного прерывания беременности.
Читайте также:

