Какие могут быть побочные эффекты после лечения туберкулеза
Обновлено: 26.04.2024
Какие возможны варианты туберкулеза легких по отношению к лекарственному лечению? Какова роль фторхинолонов в лечении туберкулеза легких?
Какие возможны варианты туберкулеза легких по отношению к лекарственному лечению?
Какова роль фторхинолонов в лечении туберкулеза легких?
Таблица. Стандартные концентрации ПТП, используемые для выявления лекарственной устойчивости МБТ
Первый этап характеризуется проведением интенсивной насыщенной химиотерапии четырьмя-пятью ПТП в течение 2-3 месяцев, что ведет к подавлению размножающейся микобактериальной популяции, уменьшению ее количества и предотвращению развития лекарственной резистентности. На первом этапе используется комбинация препаратов, состоящая из изониазида, рифампицина, пиразинамида, стрептомицина и/или этамбутола.
Второй этап — менее интенсивной химиотерапии — проводится, как правило, двумя-тремя ПТП. Цель второго этапа — воздействие на оставшуюся бактериальную популяцию, в большинстве своем находящуюся внутриклеточно в виде персистирующих форм микобактерий. Здесь главной задачей является предупреждение размножения оставшихся микобактерий, а также стимуляция репаративных процессов в легких с помощью различных патогенетических средств и методов лечения.
Такой методический подход к лечению ЛЧТЛ позволяет к концу первого этапа комбинированной химиотерапии под непосредственным медицинским наблюдением абациллировать 100%, а к завершению всего курса лечения — закрыть каверны в легких у более чем 80% больных с впервые выявленным и рецидивным туберкулезом легких [5].
Намного сложнее вопрос о проведении этиотропного лечения второго варианта, к которому мы относим ЛУТЛ, вызванный лекарственно резистентными (ЛР) МБТ к одному и более ПТП и/или их сочетанию. Особенно тяжело протекает ЛУТЛ у больных с множественной ЛР МБТ к изониазиду и рифампицину, то есть к основным и самым эффективным ПТП. Поэтому поиск новых концептуальных путей повышения эффективности лечения ЛУТЛ и разработка современной методологии специфического воздействия на ЛР МБТ является одним из важнейших и приоритетных направлений современной фтизиатрии.
Развитие ЛР у МБТ к ПТП — одна из главных причин недостаточно эффективной этиотропной химиотерапии. Больные туберкулезом, выделяющие ЛР-штаммы МБТ, длительное время остаются бактериовыделителями и могут заражать окружающих ЛР-возбудителем. Чем больше число больных, выделяющих ЛР МБТ, тем выше риск распространения инфекции среди здоровых лиц и появления новых случаев заболевания туберкулезом с первичной резистентностью не только к основным, но и к резервным ПТП.
Феномен ЛР МБТ имеет важное клиническое значение. Существует тесная взаимосвязь количественных изменений микобактериальной популяции и изменения ряда биологических свойств МБТ, одним из которых является ЛР. В активно размножающейся бактериальной популяции всегда имеется небольшое количество ЛР-мутантов, которые практического значения не имеют, но по мере уменьшения бактериальной популяции под влиянием химиотерапии изменяется соотношение между количеством ЛР и устойчивых МБТ [5]. В этих условиях происходит размножение главным образом устойчивых МБТ, эта часть бактериальной популяции увеличивается. Следовательно, в клинической практике необходимо исследовать ЛР МБТ и результаты этого исследования сопоставлять с динамикой туберкулезного процесса в легких [5].
По определению экспертов ВОЗ [3], ЛУТЛ — это случай туберкулеза легких с выделением МБТ, резистентных к одному и более ПТП. По данным Центрального НИИ туберкулеза РАМН, у каждого второго впервые выявленного и ранее не леченного противотуберкулезными препаратами больного в мокроте выявлялись ЛР к ПТП МБТ, при этом у 27,7% из них наблюдалась устойчивость к двум основным противотуберкулезным препаратам — изониазиду и рифампицину. При хроническом фиброзно-кавернозном туберкулезе частота вторичной ЛР МБТ возрастает до 95,5%.
По нашему мнению, и это составляет основу нашей концепции, для повышения эффективности лечения туберкулеза, вызванного ЛР МБТ, необходимо в первую очередь использовать ускоренные методы выявления ЛР МБТ, что позволяет своевременно изменять режим химиотерапии.
Исследование лекарственной устойчивости МБТ в настоящее время возможно по прямому и непрямому методам.
Непрямой метод определения лекарственной чувствительности МБТ требует от 30 до 60, а иногда до 90 суток, ввиду того что вначале производится посев мокроты на твердые питательные среды и только после получения культуры МБТ производят ее пересев уже на среды с добавлением ПТП. При этом коррекция химиотерапии носит отсроченный характер, как правило, уже на конечном этапе интенсивной фазы химиотерапии.
В последнее время для ускоренного определения лекарственной устойчивости нами применялся радиометрический метод с использованием автоматической системы ВАСТЕС-460 ТВ (Becton Dickinson Diagnostic Systems, Sparks, MD), которая позволяет выявлять лекарственную резистентность МБТ на жидкой среде Middlebrook 7H10 через 6-8 дней.
Не менее важно правильное лечение впервые выявленных больных туберкулезом легких и применение современных режимов химиотерапии с использованием в начале лечения комбинации из четырех-пяти основных противотуберкулезных препаратов до получения результатов лекарственной устойчивости МБТ [2]. В этих случаях существенно повышается вероятность того, что даже при наличии первичной ЛР МБТ бактериостатическое действие окажут два или три химиопрепарата, к которым чувствительность сохранена. Именно несоблюдение фтизиатрами научно обоснованных комбинированных режимов химиотерапии при лечении впервые выявленных и рецидивных больных и назначение ими только трех ПТП является грубой врачебной ошибкой, что в конечном счете ведет к формированию наиболее трудно поддающейся лечению вторичной ЛР МБТ.
Наличие у больного туберкулезом легких ЛР МБТ существенно снижает эффективность лечения, приводит к появлению хронических и неизлечимых форм, а в ряде случаев и летальных исходов. Особенно тяжело протекают специфические поражения легких у больных с полирезистентными МБТ, которые обладают множественной ЛР, как минимум к изониазиду и рифампицину, т. е. к основным и самым активным противотуберкулезным препаратам. ЛР МБТ имеет не только чисто клиническое и эпидемиологическое, но и экономическое значение, так как лечение таких больных резервными ПТП обходится намного дороже, чем больных с чувствительными МБТ к основным химиопрепаратам.
В этих условиях расширение списка резервных ПТП, воздействующих на ЛР МБТ, является актуальным и крайне важным для повышения эффективности лечения больных с ЛУТЛ. Кроме того, присоединение к ЛУТЛ неспецифической бронхолегочной инфекции существенным образом утяжеляет течение специфического процесса в легких, требуя назначения дополнительных антибиотиков широкого спектра. В этом плане применение антибиотиков, воздействующих как на МБТ, так и на неспецифическую патогенную бронхолегочную микрофлору, является научнообоснованным и целесообразным.
В этом плане хорошо себя зарекомендовал в России такой препарат из группы фторхинолонов, как офлоксацин (таривид) [3]. Мы же свой выбор остановили на ломефлоксацине, как препарате, который еще не столь широко применяется при лечении туберкулеза и у которого, судя по имеющимся данным, практически не выявляются побочные эффекты и крайне редко формируется ЛР возбудителей инфекционных заболеваний [2].
Ломефлоксацин (максаквин) — антибактериальный препарат из группы фторхинолонов. Как и все представители производных оксихинолонкарбоновой кислоты, максаквин обладает высокой активностью против грамположительных (включая метициллин-устойчивые штаммы Staphylococcus aureus и Staphylococcus epidermidis) и грамотрицательных (включая Pseudomonas) микроорганизмов, в том числе по отношению к различным типам Micobacterium tuberculosis).
Механизм действия максаквина заключается в ингибировании хромосомной и плазмидной ДНК-гиразы, фермента, ответственного за стабильность пространственной структуры микробной ДНК. Вызывая деспирилизацию ДНК микробной клетки, максаквин ведет к гибели последней.
Максаквин обладает иным механизмом действия, нежели другие антибактериальные средства, поэтому к нему не существует перекрестной устойчивости с другими антибиотиками и химиотерапевтическими препаратами [2].
Основной целью настоящего исследования явилось изучение клинической и микробиологической эффективности максаквина при комплексном лечении больных деструктивным ЛУТЛ, выделяющих ЛР МБТ к изониазиду, рифампицину и другим ПТП, а также при сочетании туберкулеза с неспецифической бронхолегочной инфекцией.
Под наблюдением находилось 50 больных деструктивным ЛУТЛ, выделяющих с мокротой ЛР МБТ к изониазиду, рифампицину и ряду других ПТП. Эти люди в возрасте от 20 до 60 лет составили основную группу.
В контрольную группу вошли также 50 больных деструктивным ЛУТЛ легких в той же возрастной группе, выделяющие ЛР МБТ к изониазиду, рифампицину и другим ПТП. Эти пациенты лечились только протионамидом, амикацином, пиразинамидом и этамбутолом.
У 47 больных основной группы и 49 контрольной в мокроте микробиологическими методами были выявлены различные возбудители неспецифической бронхолегочной инфекции.
Среди больных основной группы диссеминированный туберкулез был установлен у 5 человек, инфильтративный — у 12, казеозная пневмония — у 7, кавернозный — у 7 и фиброзно-кавернозный туберкулез — у 17 человек. Большинство больных (45 пациентов) имели распространенный туберкулез легких с поражением более двух долей, у 34 больных был двусторонний процесс. У всех больных основной группы в мокроте были обнаружены МБТ, как методом микроскопии по Цилю — Нильсену, так и методом посева на питательные среды. При этом у них МБТ были устойчивы как минимум к изониазиду и рифампицину. Необходимо отметить, что все пациенты уже ранее неоднократно и неэффективно лечились основными ПТП, и специфический процесс у них приобрел рецидивирующий и хронический характер.
В клинической картине преобладали симптомы интоксикации с высокой температурой тела, потливостью, адинамией, изменениями в крови воспалительного характера, лимфопенией, увеличенной СОЭ до 40-50 мм в час. Следует отметить наличие грудных проявлений болезни — кашель с выделением мокроты, подчас значительного количества, слизисто-гнойной, а у половины больных — гнойной, с неприятным запахом. В легких выслушивались обильные катаральные явления по типу мелко-, средне-, а подчас и крупнопузырчатых влажных хрипов.
У большинства больных преобладали клинические проявления, которые скорее укладывались в картину неспецифического бронхолегочного поражения (бронхита, острой пневмонии, абсцедирования) с частыми и практически не стихающими обострениями.
Основным возбудителем неспецифической инфекции был Streptococcus hemoliticus — у 15,3% и Staphilococcus aureus — у 15% больных. Среди грамотрицательной микрофлоры преобладал Enterobacter cloacae в 7,6% случаев. Следует отметить высокую частоту ассоциации возбудителей неспецифической бронхолегочной инфекции.
МБТ были обнаружены у всех 50 больных. У 42 человек определялось обильное бактериовыделение. У всех пациентов выделенные штаммы МБТ были устойчивы к изониазиду и рифампицину. При этом у 31 больного лекарственная устойчивость МБТ к изониазиду и рифампицину сочеталась с другими ПТП.
Определение минимальной ингибирующей концентрации (МИК) максаквина проводили на лабораторных штаммах H37Rv и Academia, а также клинических штаммах (изолятах), выделенных от 30 больных, из которых 12 изолятов были чувствительны ко всем основным химиопрепаратам и 8 обладали резистентностью к изониазиду, рифампицину и стрептомицину. В опытах in vitro подавление роста лабораторных штаммов МБТ наблюдалось в зоне 57,6±0,04 до 61,8±0,02 мкн/мл, что почти в семь раз больше, чем показатели, характерные для остальных ПТП .
Таким образом, в ходе микробиологических исследований было установлено выраженное бактериологическое действие максаквина на МБТ, при этом более выраженный эффект наблюдался при его воздействии на лекарственно чувствительные штаммы и изоляты. Однако при повышенных концентрациях максаквина эффект также заметен при воздействии на полирезистентные МБТ, устойчивые к основным ППТ.
Лечение максаквином проводилось у всех 50 больных основной группы в разработанной нами комбинации с другими резервными препаратами: протионамидом, амикацином, пиразинамидом и этамбутолом.
Максаквин назначали в дозе 800 мг в сутки перорально однократно в утренние часы сразу вместе с другими противотуберкулезными препаратами для создания максимальной суммарной бактериостатической концентрации в крови и очагах поражения. Доза максаквина выбрана с учетом микробиологических исследований и соответствовала МИК, при которой отмечалось существенное подавление роста МБТ. Терапевтический эффект определяли через месяц — для оценки воздействия его на неспецифическую патогенную бронхолегочную микрофлору и через два месяца — для оценки воздействия на полирезистентные МБТ. Длительность курса лечения резервными химиопрепаратами в сочетании с максаквином составляла два месяца.
Через месяц комплексного лечения было отмечено значительное улучшение состояния больных основной группы, что проявлялось в уменьшении количества мокроты, кашля и катаральных явлений в легких, снижении температуры тела, при этом более чем у двух третей больных — до нормальных цифр.
У всех больных к этому сроку в мокроте перестал определяться рост вторичной патогенной бронхолегочной микрофлоры. К тому же у 34 больных значительно уменьшилась массивность выделения микобактерий туберкулеза. Практически у всех больных нормализовались анализы крови.
Следует отметить, что у 28 пациентов рентгенологически через месяц лечения максаквином в сочетании с протионамидом, амикацином, пиразинамидом и этамбутолом отмечалось частичное рассасывание специфических инфильтративных изменений в легких, а также существенное уменьшение перикавитарной воспалительной реакции. Это позволило применить на данном этапе искусственный пневмоторакс, который является обязательным методом в лечении ЛУТЛ и составляет вторую и не менее важную часть нашей концепции повышения эффективности лечения больных деструктивным туберкулезом легких, выделяющих полилекарственнорезистентные МБТ.
При анализе эффективности специфического действия комбинации резервных противотуберкулезных препаратов в сочетании с максаквином на полирезистентные МБТ при лечении 50 больных основной группы мы делали основной акцент на показатель прекращения бактериовыделения, как по микроскопии мокроты по Цилю — Нильсену, так и по посеву на питательные среды через два месяца после химиотерапии.
Анализ частоты прекращения бактериовыделения у больных основной и контрольной группы через два месяца лечения показал, что у пациентов, получавших максаквин в сочетании с протионамидом, амикацином, пиразинамидом и этамбутолом, прекращение бактериовыделения было достигнуто в 56% случаях. В контрольной группе больных, не получавших максаквина, — только в 30% случаев.
Следует отметить, что у остальных больных основной группы за этот период времени существенно уменьшилась массивность выделения МБТ.
Инволюция локальных изменений в легких у 50 больных контрольной группы также шла более замедленными темпами, и только у 25 больных к концу второго месяца удалось достичь частичного рассасывания перикавитарной инфильтрации и применить к ним искусственный пневмоторакс. К 39 из 50 пациентов основной группы был применен искусственный пневмоторакс в течение 1,5-2 месяцев, и 17 из них удалось достигнуть закрытия каверн в легких. 11 оставшихся больных, имеющих противопоказания к проведению искусственного пневмоторакса, в этот период были подготовлены к плановому оперативному вмешательству.
При определении лекарственной устойчивости МБТ к максаквину через два месяца лечения у больных основной группы только в 4% случаев была получена вторичная лекарственная устойчивость, сформировавшаяся в процессе двухмесячной химиотерапии, что в конечном итоге потребовало его отмены и замены на другой химиопрепарат, к которому МБТ сохранили свою чувствительность.
К концу второго месяца у 4% больных отмечались явления непереносимости максаквина — в виде диспепсических явлений и диареи, связанной с дисбактериозом, аллергических кожных проявлений и эозинофилии до 32%, что привело к полной отмене препарата. Во всех остальных случаях при двухмесячном ежедневном применении максаквина в суточной дозе 800 мг побочных явлений не отмечалось.
Проведенная после окончания курса лечения максаквином комбинированная химиотерапия резервными препаратами и динамическое наблюдение за этими же больными показали, что достигнутый ко второму месяцу положительный результат в абациллировании мокроты оказал положительное влияние и на конечный результат излечения больных с ЛУТЛ.
Таким образом, применение максаквина в дозе 800 мг в сутки в сочетании с протионамидом, амикацином, пиразинамидом и этамбутолом у больных деструктивным ЛУТЛ с сопутствующей неспецифической бронхолегочной инфекцией показало его достаточную эффективность как антибиотика широкого спектра, воздействующего на грамотрицательную и грамположительную микрофлору, и препарата, действующего на туберкулезное воспаление.
Максаквин с полной уверенностью может быть отнесен к группе резервных ПТП. Он эффективно действует не только на МБТ, чувствительные ко всем ПТП, но и на ЛУ МБТ к изониазиду и рифампицину, что и обусловливает целесообразность его назначения таким больным. Тем не менее максаквин не следует рассматривать как основной препарат в схемах лечения больных с впервые выявленным туберкулезом легких, он должен оставаться в резерве и применяться только при ЛУТЛ и сопутствующей неспецифической бронхолегочной инфекции.
Для изониазида это составляет 1 мкг/мл, для рифампицина — 40 мкг/мл, стрептомицина — 10 мкг/мл, этамбутола — 2 мкг/мл, канамицина — 30 мкг/мл, амикацина — 8 мкг/мл, протионамида (этионамида) — 30 мкг/мл, офлоксацина (таривида) — 5 мкг/мл, циклосерина — 30 мкг/мл и для пиразинамида — 100 мкг/мл.
Литература
1. Лечение туберкулеза. Рекомендации для национальных программ. ВОЗ. 1998. 77 с.
2. Мишин. В. Ю., Степанян И. Э. Фторхинолоны в лечении туберкулеза органов дыхания // Русский медицинский журнал. 1999. № 5. С. 234-236.
3. Рекомендации по лечению резистентных форм туберкулеза. ВОЗ. 1998. 47 с.
4. Хоменко А. Г., Мишин В. Ю., Чуканов В. И. и др. Эффективность применения офлоксацина в комплексном лечении больных туберкулезом легких, осложненным неспецифической бронхолегочной инфекцией // Новые лекарственные препараты. 1995. Вып. 11. С. 13-20.
5. Хоменко А. Г. Современная химиотерапия туберкулеза // Клиническая фармакология и терапия. 1998. № 4. С. 16-20.
Все противотуберкулезные препараты обладают побочным действием, которое особенно выражено при их комплексном применении.
Побочное действие или реакция это отрицательное влияние лекарственного препарата на органы и системы человека, приводящие к нарушению их деятельности (Н.А.Шмелев, Э.С. Степанян 1977г.).
Побочное действие лекарственных препаратов проявляется в двух формах:токсической и аллергической, иногда выделяют токсико-аллергическую. Разделение это носит условный характер, но достаточно удобно для определения методов профилактики и лечения. Отдельным пунктом выделяют дисбактериоз и его последствия.
Токсический эффект обусловлен избирательным влиянием препаратов на функцию различных органов и систем организма. Наиболее часто поражаемый орган - печень, так как в ней осуществляется инактивация всех противотуберкулезных лекарств.
Помимо общего токсического действия, многие противотуберкулезные препараты обладают специфическими эффектами. Так группа аминогликозидов (стрептомицин, канамицин, амикацин, капреомицин.) вызывает поражение слухового нерва (VIII пара), этамбутол иногда ухудшает функцию зрительного анализатора, пара-аминсалициловая кислота (ПАСК) - выраженное раздражение слизистой желудка и кишечника, изолированные эозинофилии, пиразинамид вызывает гипереурикэмию и нарушение тромбоцитарного ростка кроветворения.
Кроме того, побочные эффекты делятся на устранимые и неустранимые, т.е. последствия которых устранить практически невозможно (потеря зрения, слуха и т.д.).
Вот более подробный список препаратов и вызываемых ими побочных эффектов:
Пусть Вас не пугает этот долгий перечень, вовсе не обязательно, что Вы столкнетесь даже с одним из перечисленных ниже эффектов. Но знать о них надо, чтобы предупредить нежелательные последствия. К примеру, аллергические реакции при приеме изониазида возникают у 3 человек из 1000 (0, 3%).
Изониазид
Метаболизируется в печени до неактивных продуктов. Экскреция почками.
Побочные эффекты: Головная боль, раздражительность, эйфория, бессонница, парестезии, онемение конечностей, полиневрит, психозы, судорожный синдром, эпилептиформные припадки, ощущение сердцебиения, стенокардия, повышение АД, токсический гепатит, аллергические реакции, меноррагия.
Противопоказания: гиперчувствительность, эпилепсия, судорожный синдром, бронхиальная астма, псориаз, печеночная недостаточность, гепатит, цирроз печени, флебит.
Рифампицин
Побочные эффекты: тошнота, рвота, диарея, анарексия, эрозивный гастрит, псевдомембранозный энтероколит, повышение активности печеночных трансаминаз в сыворотке крови, гипербилирубинэмия, аллергические реакции (крапивница, эозинофилия, отек Квинке, бронхоспазм, артралгия, лихорадка), лейкопения, дисменорея, головная боль, нарушение координации движений, гепатит, индукция порфирии, нефронекроз, интерстициальный нефрит, нарушение зрения, атаксия, дезоприентация, мышечная слабость, герпес,
При интермиттирующей или нерегулярной терапии или при возобновлении лечения после перерыва возможны гриппоподобный синдром (лихорадка, головная боль, головокружение, миалгия), кожные реакции, лихорадка, гемолитическая анемия, тромбоцитопеническая пурпура, острая печеночная недостаточность.
Препарат отменяют при развитии тромбоцитопении, гемолитической анемии, бронхоспазма, одышки, шока и почечной недостаточности.
Этамбутол
Побочные эффекты: тошнота, анорексия, рвота, головокружение, депрессия, аллергические реакции (кожная сыпь), уменьшение центральных и переферических полей зрения, нарушение светового восприятия (в основном зеленого и красного цветов), нарушение функции печени.
В начале лечения возможно усиления кашля, увеличение количества мокроты.
Пиразинамид
(действует на внутриклеточно расположенные микобактерии)
Побочные эффекты: тошнота, рвота, диарея, нарушение функции печени (анорексия, болезненность печени, гепатомегалия, желтуха, желтая атрофия), спленомегалия, анемия, артралгия, дизурия, лихорадка, обострение пептической язвы, аллергические реакции, фотосенсибилизация, гиперурикемия, обострение подагры, интерстициальный нефрит, повышение концентрации сывороточного железа.
Протионамид
Побочные эффекты: аллергические реакции, бессонница, возбуждение, тошнота, рвота, диарея, нарушение функции печени, головокружение, тахикардия, слабость, парестезии.
Этионамид
(Угнетает рост и размножение микобактерий туберкулеза при вне- и внутриклеточном расположении. Усиливает фагоцитоз в очаге туберкулезного воспаления).
Побочные эффекты: тошнота, рвота, диарея, гастралгия, метеоризм, желтуха, анорексия, стоматит, аллергические реакции (кожная сыпь), периферический неврит, неврит зрительного нерва, ортостатическая гипотензия, тромбоцитопения, дефицит пиридоксина, психические нарушения.
При одновременном приеме с циклосерином повышает риск возникновения нейротоксических побочных эффектов.
Лучше с пиридоксином
Стрептомицин
Побочные эффекты: нефротоксичность, ототоксичность, глухота, вестибулярные и лабиринтные нарушения, аллергические реакции, диарея, головная боль, головокружение, тахикардия.
Амикацин
Канамицин
Побочные эффекты: нефротоксичность, ототоксичность, глухота, аллергические реакции, тошнота, рвота, диарея, парастезии, нарушение функции печени, цилиндрурия, микрогеметурия, альбуминурия.
Офлоксацин(таривид)
Ципрофлоксацин
Побочные эффекты: перечислить все возможные реакции не представляется возможным, в целях экономии места отмечу их сходство с побочными действиями офлоксацина.
Левофлоксацин (Таваник)
Циклосерин
Побочные эффекты: Головная боль, головокружение, бессонница, сонливость, беспокойство, раздражительность, снижение памяти, парестезии, периферический неврит, тремор, эйфория, депрессия, суицидальная настроенность, психоз, эпилептиформные судороги, тошнота, изжога, лихорадка, усиление кашля. Опасными последствиями грозит прием алкоголя в сочетании с циклосерином.
ПАСК
Как Вы видите многие схожие побочные эффекты имеются у различных препаратов. И в связи с этим, найти причину их возникновения нелегко. Перечисленные здесь эффекты приводятся производителями и, конечно, список далеко не полный. Так если Вы начнете принимать какой- либо препарат и вдруг на следующий день Ваше состояние резко изменяется: повышается температура, появляются заложенность носа, головные боли и миалгии, а в инструкции подобных явлений не указано, вовсе не обязательно что Вы подхватили грипп или простуду, просто это был Ваш индивидуальный ответ на введенное средство. Прекратив прием препарата Вы быстро придете в норму, и очень жаль, что при туберкулезе подобные отмены могут стоить слишком дорого.
Туберкулез легких – это инфекционная патология, вызываемая бациллой Коха, характеризующаяся различными в клинико-морфологическом отношении вариантами поражения легочной ткани. Многообразие форм туберкулеза легких обусловливает вариабельность симптоматики. Наиболее типичны для туберкулеза легких респираторные нарушения (кашель, кровохарканье, одышка) и симптомы интоксикации (длительный субфебрилитет, потливость, слабость). Для подтверждения диагноза используются лучевые, лабораторные исследования, туберкулинодиагностика. Химиотерапия туберкулеза легких проводится специальными туберкулостатическими препаратами; при деструктивных формах показано хирургическое лечение.
МКБ-10

Общие сведения
На сегодняшний день туберкулез легких представляет не только медико-биологическую, но и серьезную социально-экономическую проблему. По данным ВОЗ, туберкулезом инфицирован каждый третий житель планеты, смертность от инфекции превышает 3 млн. человек в год. Легочный туберкулез является самой частой формой туберкулезной инфекции. Удельный вес туберкулеза других локализаций (суставов, костей и позвоночника, гениталий, кишечника, серозных оболочек, ЦНС, глаз, кожи) в структуре заболеваемости значительно ниже.

Причины
Характеристика возбудителя
Отличительной чертой МБТ является их высокая устойчивость к внешним воздействиям (высоким и низким температурам, влажности, воздействию кислот, щелочей, дезинфектантов). Наименьшую стойкость возбудители туберкулеза легких демонстрируют к солнечному свету. Для человека опасность представляют туберкулезные бактерии человеческого и бычьего типа; случаи инфицирования птичьим типом микобактерий крайне редки.
Пути заражения
Основной путь заражения при первичном туберкулезе легких – аэрогенный: от больного открытой формой человека микобактерии распространяются с частичками слизи, выделяемыми в окружающую среду при разговоре, чихании, кашле; могут высыхать и разноситься с пылью на значительные расстояния. В дыхательные пути здорового человека инфекция чаще попадает воздушно-капельным или пылевым путем.
Меньшую роль в инфицировании играют алиментарный (при употреблении зараженных продуктов), контактный (при использовании общих предметов гигиены и посуды) и трансплацентарный (внутриутробный) пути. Причиной вторичного туберкулеза легких выступает повторная активация ранее перенесенной инфекции либо повторное заражение.
Факторы риска
Однако попадание МБТ в организм не всегда приводит к заболеванию. Факторами, на фоне которых туберкулез легких развивается особенно часто, считаются:
- неблагоприятные социально-бытовые условия
- курение и другие химические зависимости
- недостаточное питание
- иммуносупрессия (ВИЧ-инфекция, прием глюкокортикоидов, состояние после трансплантации органов)
- онкологические заболевания и др.
В группе риска по развитию туберкулеза легких находятся мигранты, заключенные, лица, страдающие наркотической и алкогольной зависимостью. Также имеет значение вирулентность инфекции и длительность контакта с больным человеком.
Патогенез
При снижении местных и общих факторов защиты микобактерии беспрепятственно проникают в бронхиолы, а затем в альвеолы, вызывая специфическое воспаление в виде отдельных или множественных туберкулезных бугорков или очагов творожистого некроза. В этот период появляется положительная реакция на туберкулин - вираж туберкулиновой пробы. Клинические проявления туберкулеза легких на этой стадии часто остаются нераспознанными. Небольшие очажки могут самостоятельно рассасываться, рубцеваться или обызвествляться, однако МБТ в них длительно сохраняются.
Классификация
Первичный туберкулез легких - это впервые развившаяся инфильтрация легочной ткани у лиц, не имеющих специфического иммунитета. Диагностируется преимущественно в детском и подростковом возрасте; реже возникает у лиц старшего и пожилого возраста, которые в прошлом перенесли первичную инфекцию, закончившуюся полным излечением. Первичный туберкулез легких может принимать форму:
- первичного туберкулезного комплекса (ПТК)
- туберкулеза внутригрудных лимфоузлов (ВГЛУ)
- хронически текущего туберкулеза.
Вторичный туберкулез легких развивается при повторном контакте с МБТ или в результате реактивации инфекции в первичном очаге. Основные вторичные клинические формы представлены:
Отдельно различают кониотуберкулез (туберкулез, развивающийся на фоне пневмокониозов), туберкулез верхних дыхательных путей, трахеи, бронхов; туберкулезный плеврит. При выделении больным МБТ в окружающую среду с мокротой говорят об открытой форме (ВК+) туберкулеза легких; при отсутствии бацилловыделения – о закрытой форме (ВК–). Также возможно периодическое бацилловыделение (ВК±).
Течение туберкулеза легких характеризуется последовательной сменной фаз развития:
- 1) инфильтративной
- 2) распада и обсеменения
- 3) рассасывания очага
- 4) уплотнения и обызвествления.
Симптомы туберкулеза легких
Первичный туберкулезный комплекс
Первичный туберкулезный комплекс сочетает в себе признаки специфического воспаления в легком и регионарный бронхоаденит. Может протекать бессимптомно или под маской простудных заболеваний, поэтому выявлению первичного туберкулеза легких способствуют массовые скрининги детей (проба Манту) и взрослых (профилактическая флюорография).
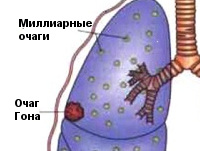
Чаще возникает подостро: больного беспокоит сухой кашель, субфебрилитет, утомляемость, потливость. При острой манифестации клиника напоминает неспецифическую пневмонию (высокая лихорадка, кашель, боль в груди, одышка). В результате лечения происходит рассасывание или обызвествление ПТК (очаг Гона). В неблагоприятных случаях может осложняться казеозной пневмонией, образованием каверн, туберкулезным плевритом, милиарным туберкулезом, диссеминацией микобактерий с поражением почек, костей, мозговых оболочек.
Туберкулез внутригрудных лимфоузлов
Признаки туберкулезной интоксикации включают отсутствие аппетита, снижение массы тела, утомляемость, бледность кожи, темные круги под глазами. На венозный застой в грудной полости может указывать расширение венозной сети на коже грудной клетки. Данная форма нередко осложняется туберкулезом бронхов, сегментарными или долевыми ателектазами легких, хронической пневмонией, экссудативным плевритом. При прорыве казеозных масс из лимфоузлов через стенку бронхов могут формироваться легочные очаги туберкулеза.
Очаговый туберкулез легких
Клиническая картина очагового туберкулеза малосимптомна. Кашель отсутствует или возникает редко, иногда сопровождается выделением скудной мокроты, болями в боку. В редких случаях отмечается кровохарканье. Чаще больные обращают внимание на симптомы интоксикации: непостоянный субфебрилитет, недомогание, апатию, пониженную работоспособность. В зависимости от давности туберкулезного процесса различают свежий и хронический очаговый туберкулез легких.
Течение очагового туберкулеза легких относительно доброкачественное. У больных с нарушенной иммунной реактивностью заболевание может прогрессировать в деструктивные формы туберкулеза легких.
Инфильтративный туберкулез легких
Клиническая картина инфильтративного туберкулеза легких зависит от величины инфильтрата и может варьировать от нерезко выраженных симптомов до острого лихорадочного состояния, напоминающего грипп или пневмонию. В последнем случае отмечается выраженная высокая температура тела, ознобы, ночная потливость, общая слабость. Со стороны органов дыхания беспокоит кашель с мокротой и прожилками крови.
В воспалительный процесс при инфильтративной форме туберкулеза легких часто вовлекается плевра, что обусловливает появление болей в боку, плеврального выпота, отставание пораженной половины грудной клетки при дыхании. Осложнениями инфильтративного туберкулеза легких могут стать казеозная пневмония, ателектаз легкого, легочное кровотечение и др.
Диссеминированный туберкулез легких
Может манифестировать в острой (милиарной), подострой и хронической форме. Тифоидная форма милиарного туберкулеза легких отличается преобладанием интоксикационного синдрома над бронхолегочной симптоматикой. Начинается остро, с нарастания температуры до 39-40 °С, головной боли, диспепсических расстройств, резкой слабости, тахикардии. При усилении токсикоза может возникать нарушение сознания, бред.
При легочной форме милиарного туберкулеза легких с самого начала более выражены дыхательные нарушения, включающие сухой кашель, одышку, цианоз. В тяжелых случаях развивается острая сердечно-легочная недостаточность. Менингеальной форме соответствуют симптомы поражения мозговых оболочек.
Подострое течение диссеминированного туберкулеза легких сопровождается умеренной слабостью, понижением работоспособности, ухудшением аппетита, похуданием. Эпизодически возникают подъемы температуры. Кашель продуктивный, не сильно беспокоит больного. Иногда первым признаком заболевания становится легочное кровотечение.
Хронический диссеминированный туберкулез легких при отсутствии обострения бессимптомен. Во время вспышки процесса клиническая картина близка к подострой форме. Диссеминированный туберкулеза легких опасен развитием внелегочного туберкулеза, спонтанного пневмоторакса, тяжелых легочных кровотечений, амилоидоза внутренних органов.
Кавернозный и фиброзно-кавернозный туберкулез легких
Характер течения кавернозного туберкулезного процесса волнообразный. В фазу распада нарастают интоксикационные симптомы, гипертермия, усиливается кашель и увеличивается количество мокроты, возникает кровохарканье. Часто присоединяется туберкулез бронхов и неспецифический бронхит.
Фиброзно-кавернозный туберкулез легких отличается формированием каверн с выраженным фиброзным слоем и фиброзными изменениями легочной ткани вокруг каверны. Протекает длительно, с периодическими обострениями общеинфекционной симптоматики. При частых вспышках развивается дыхательная недостаточность II-III степени.
Осложнениями, связанными с деструкцией легочной ткани, являются профузное легочное кровотечение, бронхоплевральный свищ, гнойный плеврит. Прогрессирование кавернозного туберкулеза легких сопровождается эндокринными расстройствами, кахексией, амилоидозом почек, туберкулезным менингитом, сердечно-легочной недостаточностью – в этом случае прогноз становится неблагоприятным.
Цирротический туберкулез легких
Является исходом различных форм туберкулеза легких при неполной инволюции специфического процесса и развитии на его месте фиброзно-склеротических изменений. При пневмоциррозе бронхи деформированы, легкое резко уменьшено в размерах, плевра утолщена и нередко обызвествлена.
Изменения, происходящие при цирротическом туберкулезе легких, обусловливают ведущие симптомы: выраженную одышку, тянущую боль в груди, кашель с гнойной мокротой, кровохарканье. При обострении присоединятся признаки туберкулезной интоксикации и бацилловыделение. Характерным внешним признаком пневмоцирроза служит уплощение грудной клетки на стороне поражения, сужение и втянутость межреберных промежутков. При прогрессирующем течении постепенно развивается легочное сердце. Цирротические изменения в легких необратимы.
Туберкулома легкого
Представляет собой инкапсулированный казеозный очаг, сформировавшийся в исходе инфильтративного, очагового или диссеминированного процесса. При стабильном течении симптомы не возникают, образование выявляется при рентгенографии легких случайно. В случае прогрессирующей туберкуломы легкого нарастает интоксикация, появляется субфебрилитет, боль в груди, кашель с отделением мокроты, возможно кровохарканье. При распаде очага туберкулома может трансформироваться в кавернозный или фиброзно-кавернозный туберкулез легких. Реже отмечается регрессирующее течение туберкуломы.
Диагностика
Диагноз той или иной формы туберкулеза легких выставляется врачом-фтизиатром на основании совокупности клинических, лучевых, лабораторных и иммунологических данных. Для распознавания вторичного туберкулеза большое значение имеет подробный сбор анамнеза. Для подтверждения диагноза проводится:
- Лучевая диагностика.Рентгенография легких является обязательным диагностической процедурой, позволяющей выявить характер изменений в легочной ткани (инфильтративный, очаговый, кавернозный, диссеминированный и т. д.), определить локализацию и распространенность патологического процесса. Выявление кальцинированных очагов указывает на ранее перенесенный туберкулезный процесс и требует уточнения данных с помощью КТ или МРТ легких.
- Анализы. Обнаружение МБТ достигается неоднократным исследованием мокроты (в т. ч. с помощью ПЦР), промывных вод бронхов, плеврального экссудата. Но сам по себе факт отсутствия бацилловыделения не является основанием для исключения туберкулеза легких. Современные иммунологические тесты позволяют выявить туберкулезную инфекцию почти со 100%-ной вероятностью. К ним относятся QuantiFERON и Т-спот. ТБ.
- Туберкулинодиагностика. К методам туберкулинодиагностики относятся диаскин-тест, пробы Пирке и Манту, однако сами по себе данные методы могут давать ложные результаты. Иногда для подтверждения туберкулеза легких приходится прибегать к пробному лечению противотуберкулезными препаратами с оценкой динамики рентгенологической картины.
По результатам проведенной диагностики туберкулез легких дифференцируют с пневмонией, саркоидозом легких, периферическим раком легкого, доброкачественными и метастатическими опухолями, пневмомикозами, кистами легких, абсцессом, силикозом, аномалиями развития легких и сосудов. Дополнительные методы диагностического поиска могут включать бронхоскопию, плевральную пункцию, биопсию легкого.

Лечение туберкулеза легких
Во фтизиатрической практике сформировался комплексный подход к лечению туберкулеза легких, включающий медикаментозную терапию, при необходимости - хирургическое вмешательство и реабилитационные мероприятия. Лечение проводится поэтапно: сначала в тубстационаре, затем в санаториях и, наконец, амбулаторно. Режимные моменты требуют организации лечебного питания, физического и эмоционального покоя.
- Противотуберкулезная терапия. Ведущая роль отводится специфической химиотерапии с помощью препаратов с противотуберкулезной активностью. Для терапии различных форм туберкулеза легких разработаны и применяются 3-х, 4-х и 5-тикомпонентные схемы (в зависимости от количества используемых препаратов). К туберкулостатикам первой линии (обязательным) относятся изониазид и его производные, пиразинамид, стрептомицин, рифампицин, этамбутол; средствами второго ряда (дополнительными) служат аминогликозиды, фторхинолоны, циклосерин, этионамид и др. Способы введения препаратов различны: перорально, внутримышечно, внутривенно, эндобронхиально, внутриплеврально, ингаляторно. Курсы противотуберкулезной терапии проводят длительно (в среднем 1 год и дольше).
- Патогенетическая терапия. При туберкулезе легких включает прием противовоспалительных средств, витаминов, гепатопротекторов, инфузионную терапию и пр. В случае лекарственной резистентности, непереносимости противотуберкулезных средств, при легочных кровотечениях используется коллапсотерапия.
- Хирургическое лечение. При соответствующих показаниях (деструктивных формах туберкулеза легких, эмпиеме, циррозе и ряде др.) применяются различные оперативные вмешательства: кавернотомию, торакопластику, плеврэктомию, резекцию легких.
Профилактика
Профилактика туберкулеза легких является важнейшей социальной проблемой и приоритетной государственной задачей. Первым шагом на этом пути является обязательная вакцинация новорожденных, детей и подростков. При массовых обследованиях в дошкольных и школьных учреждениях используется постановка внутрикожных туберкулиновых проб Манту. Скрининг взрослого населения осуществляется путем проведения профилактической флюорографии.
Побочные реакции на противотуберкулёзные препараты – одна из главных причин недостаточной эффективности химиотерапии. На современном уровне знаний патогенеза побочного действия противотуберкулёзных препаратов классифицируются следующие виды побочных реакций.
1. Токсические побочные реакции:
- токсико-метаболические (общие реакции организма);
- токсико-органные (поражения печени, почек, нервной, сердечно-сосудистой и других систем).
2. Аллергические побочные реакции:
- немедленного типа, связанные с образованием антител (анафилактический шок, отёк Квинке, крапивница);
- замедленного типа, связанные с цитотоксическими лимфоцитами (поражение кожи и слизистых оболочек – синдром Лайела, гепатит, гломерулонефрит и другие)
4. Дисбиотические нарушения кишечника (дисбактериоз):
Все побочные реакции могут носить устранимый и неустранимый характер. В случаях устранимых побочных реакций рациональная патогенетическая терапия позволяет продолжить назначенный режим химиотерапии, тогда как в случаях неустранимых побочных реакций, таких как лекарственный гепатит, лекарственный гломерулонефрит, необходима отмена лекарства, вызвавшего нежелательный эффект и переход на индивидуализированное лечение.
В диагностике отрицательных реакций от химиотерапии ведущее значение имеет клиническая картина.
Токсическое действие обусловливает ухудшение общего состояния и самочувствия больного, но на этом фоне чаще всего выявляются симптомы органной патологии, наиболее характерной для каждого препарата. Примерами этого являются поражения почек, слуха и вестибулярного аппарата от стрептомицина, канамицина, капреомицина; нейрооптикопатия, периферические невриты и психоневрологические расстройства – от изониазида, циклосерина, протионамида; поражения печени – от рифампицина, изониазида, этионамида, пиразинамида; сердечно-сосудистых нарушений – от стрептомицина, канамицина, капреомицина ,изониазида, циклосерина; изменений в гемограмме – лейкоцитоз или лейкопения, моноцитоз , сдвиг лейкограммы влево, анемия, тромбоцитопения – от разных препаратов.
Аллергические реакции характеризуются стереотипностью, независимостью от химической структуры, иногда и дозы препарата. Классические симптомы: сыпь, зуд, подъёмы температуры, эозинофилия в крови, ринит, бронхоспазм, отёк Квинке. Эти симптомы могут быть самостоятельными или сопровождаются недомоганием, вегетативными реакциями (тахикардия, головокружение, головная боль), снижением аппетита, тошнотой.
Токсико-аллергические реакции отличаются разнообразием и многосимптомностью: одновременно аллергических проявлений и нарушений, характерных для фармакологических свойств препаратов. Наиболее типичными клиническими вариантами таких осложнений проявляются токсико-аллергические – гепатит, нефрит, миокардит, различные невриты, гематологические сдвиги, диспепсии, сочетающиеся с аллергическими симптомами. Токсико-аллергическое побочное действие чаще приобретает затяжное течение и труднее поддаётся корригирующей терапии.
Клинические проявления и устранение побочных реакций на противотуберкулёзные препараты
Изониазид. Клинические проявления побочного действия изониазида и его аналогов отличаются разнообразием симптомов: головокружение, боли в области сердца, головная боль, нарушения сна и настроения (в редких случаях с развитием психозов), парестезии, периферические невриты, довольно часто – гепатиты. Выше указанные симптомы нередко сочетаются с аллергическими реакциями: зуд, эритематозные высыпания, эозинофилия. Необходим систематический контроль за лабораторными показателями функций печени, гемограммой и ЭКГ (2 раза в месяц).
Рифампицин. Наиболее часто наблюдается гепатотропный эффект от рифампицина. Как правило, на практике гепатологические осложнения развиваются при сочетании рифампицина с изониазидом и пиразинамидом, что объясняется метаболическими особенностями их взаимодействия в организме. Своеобразие побочного действия рифампицина состоит также в особенностях его иммуно-аллергических реакций. Клиническое проявление такого побочного действия – псевдогриппозный синдром – повышение температуры, ринит, миалгии, артралгии, диспепсия, редко – бронхиальная обструкция и эритема. При лечении рифампицином необходим регулярный контроль биохимических показателей функции печени, почек и гемограмма.
Стрептомицин, канамицин, капреомицин. Эти препараты оказывают значительное аллергизирующее влияние на организм. Клиническая картина: эозинофилия, повышение температуры, высыпания на коже ,отёк Квинке, бронхоспазм, повышение уровня аланиновой аминотрансферазы в сыворотке крови. Могут наблюдаться парестезии, головные боли, бессонница. Следует отметить тропность стрептомицина к вестибулярному аппарату, а канамицина и капреомицина к слуховой ветви VIII пары черепно-мозговых нервов. При первых симптомах поражения слухового нерва – шум или звон в ушах, понижение слуха, а также при вестибулярных расстройства – головокружение, тошнота, усиливающаяся при изменении положения тела и поворотах головы, нарушение координации – необходима отмена препаратов. Из-за поздней отмены их нарушения могут сохраняться и даже прогрессировать. При начальных вестибулярных нарушениях или других нейротоксических реакциях после отмены препаратов можно перейти на интермиттирующий их приём. В период лечения указанными препаратами обязательны осмотр невролога и отоларинголога (1 раз в месяц) лабораторный контроль показателей функции почек, уровня эозинофилов в гемограмме, ЭКГ.
Пиразинамид. Среди осложнений от пиразинамида отмечена патология со стороны печени и желудочно-кишечного тракта. Лечение пиразинамидом проводится при обязательном контроле за функцией печени (1 раз в месяц).
Протионамид (Этионамид). нежелательные реакции от протионамида связаны преимущественно с раздражающим действием этих препаратов на слизистую оболочку желудочно-кишечного тракта и проявляются ухудшением аппетита, металлическим привкусом во рту, тошнотой, диспепсическими расстройствами, потерей массы тела. Возможны симптомы нарушения функции печени, центральной нервной системы, эозинофилия, высыпания по типу крапивницы. При использовании протионамида необходим ежемесячный лабораторный контроль функции печени. При неудовлетворительной переносимости переход на интермиттирующий приём.
ПАСК. Наиболее частые нежелательные реакции от ПАСК диспепсические расстройства. Необходимо принимать препарат после еды, запивая молоком или щелочной водой. Аллергические реакции могут проявляться дерматитом, подъёмом температуры. Редко наблюдаются токсико-аллергические поражения печени и почек ,преимущественно у пациентов с предшествующими заболеваниями этих органов; известны случаи анемии. В зависимости от выраженности осложнений ПАСК отменяют временно или полностью, при этом назначают витамины В1, В6, В12 с фолиевой кислотой, антигистаминные препараты. Лечение ПАСК требует регулярного контроля за анализом мочи, функции почек и печени, за лейкограммой.
Фторхинолоны (обладают противотуберкулёзной активностью: офлоксацин, ципрофлоксацин, ломефлоксацин, левофлоксацин, спарфлоксацин и моксифлоксацин). Побочное действие от этих препаратов чаще всего отмечается со стороны желудочно-кишечного тракта (отсутствие аппетита, тошнота, рвота ,диарея и дисбактериоз и кандидоз) и ЦНС (нарушение сна, головокружение, головная боль, перепады настроения, судорожный синдром). Известны случаи аритмий, транзиторной артериальной гипотонии.
Количество применяемых основных противотуберкулёзных препаратов существенно не влияет на частоту побочных реакций. Тенденция к увеличению частоты побочных реакций имеет место в основном в режимах химиотерапии с применением стрептомицина и у больных с сопутствующей патологией (хронический алкоголизм, хронический персистирующий гепатит, сахарный диабет, патология ССС, заболевания ЖКТ, ЦНС и др.). При этом, побочные реакции проявляются, как правило, в первый месяц химиотерапии и, крайне редко в дальнейшем продолжении комплексного лечения после временной отмены и адекватном патогенетическом сопровождении.
Анафилактический шок может быть вызван любым противотуберкулёзным препаратом, чаще при парентеральном введении. В комплекс срочных мер входит немедленное прекращение введения лекарства, вызвавшего шок. Внутримышечно назначают один из антигистаминных препаратов – димедрол, супрастин, пипольфен по 1 – 3 мл, одно из спазмолитических средств – но-шпа, папаверин по 2 мл, гормональные препараты – растворы гидрокортизона для инъекций 100 мг или преднизолона для инъекций 30 мг. При резком падении артериального давления внутривенно струйно вводят преднизолон 30 – 90 мг и полиглюкин 200 – 400 мл.
При возбуждении больного и судорогах вводят внутримышечно седуксен, реланиум по 2 мл; при мышечных, загрудинных, кардиальных болях – промедол, омнопон по 1 мл. Подкожно при дыхательных расстройствах и сосудистом коллапсе показан кордиамин 2 – 4 мл. Одновременно необходимо согреть пациента грелками, дать горячее питьё. Если вышеуказанные мероприятия не приводят к устранению шоковых реакций, необходима реанимационная помощь.
Регресс побочных реакций наступает тем быстрее, чем раньше отменён препарат. Обязательно назначение корригирующих и симптоматических лекарственных средств. Возобновление лечения возможно после нормализации клинического состояния и лабораторных показателей, путём последовательного включения каждого препарата. При неустранимости лекарственных осложнений с помощью патогенетической и симптоматической терапии использование препаратов немедленно прекращается и в дальнейшем их применение противопоказано; необходим подбор других более щадящих сочетаний.
У больных с рецидивирующим характером лекарственных осложнений неаллергического характера целесообразно заменять непрерывную терапию интермиттирующим методом даже в начале лечения.
Исходя из патогенетических основ большинства лекарственных осложнений и современных терапевтических возможностей, наибольшее применение в их ликвидации имеют витамины группы В (В1, В6, В2, В12) и аскорбиновая кислота. Курсы витаминов используют весь период лечения противотуберкулёзными препаратами с первых дней, лучше парентерально по 3 – 6 недель с перерывами по 2 – 3 недели. Аналогичны действию витаминов гепатопротекторы (эссенциале, карсил, липамид) и желчегонные средства (желчегонный фитосбор, аллохол, кукурузные рыльца). При любых проявлениях аллергических и токсико-аллергических реакций всегда необходимо назначение антигистаминных средств (димедрол, супрастин, пипольфен).
Читайте также:

