Какой стафилококк вызывает рожу
Обновлено: 24.04.2024
История применения антибактериальных препаратов переживает определенную цикличность. В доантибиотиковую эру среди возбудителей тяжелых инфекций преобладали Гр(+) возбудители, потом пришли антибиотики, и во время второй мировой основными возбудителями стали Гр(-) возбудители (по принципу «свято место пусто не бывает), но тут Гр(+) опять подняли голову, т.к. выяснилось, что свыше 80% штаммов стафилококков продуцируют пенициллиназу и разрушают бензилпенициллин и аминопенициллины.
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: врач – клинический фармаколог Трубачева Е.С.
Staphylococcus aureus делится на две группы – мецитиллинчувствительные (MSSA) и мецитиллинрезистентные (MRSA):
1. MSSA вырабатывают беталактамазы – пенициллиназы, которые разрушают незащищенные пенициллины, но сохраняют высокую чувствительность к оксациллину и цефазолину. Кроме того они обладают лейкоцидином Пантона-Валентайна, который вызывает распад тканей практически в любом очаге, что служит косвенным подтверждением стафилококковой инфекции еще до получения микробиологического анализа.
2. MRSA в свою очередь подразделяются на госпитальные, которые характеризуются тем, что:
- являются полирезистентными, т.е. нечувствительные ко всему классу бета-лактамов, включая карбапенемы;
- у них отсутствует лейкоцидин Пантона-Валентайна, поэтому реже возникают деструктивные процессы (пациенты просто тихо и долго гниют, в отличие от инфекций, вызванных дикими штаммами)
- вызывают нозокомиальные пневмонии, инфекции кожи, ран, сепсис, бак эндокардит протезированных клапанов, инфекции имплантов.
и внебольничные MRSA, характеризующиеся:
- полирезистентностью;
- наличием лейкоцидина Пантона-Валентайна, благодаря которому они более агрессивны и вызывают некротизирующие заболевания кожи, сосудов и легких (особенно четко роль лейкоцидина Пантона-Валентайна видна в развитии некротизирующей пневмонии);
- в основном характерны для наркоманов и лиц без определенного места жительства.
Факторами риска MRSA инфекций являются
- назофарингеальная колонизация MRSA;
- лечение бета-лактамами (выбивается чувствительная флора и ее место занимает MRSA;
- нахождение в ОРИТ;
- повреждение кожи при длительной госпитализации более 2-х недель (п/о раны, ожоги, язвы);
- внутрисосудистые катетеры и импланты;
- мед. работники и члены их семей (соседи – реаниматологи или хирурги, если семьи между собой общаются)
Для чего мы все это вспоминаем? Дело в том, что основные проблемы, связанные со стафилококковой инфекцией, это:
- Широкое распространение в медицине и как следствие недооценка проблемы.
- Назначение эмпирической терапии без учета риска MRSA, и как следствие – отсрочка адекватной терапии, что в случае золотистого стафилококка в прямом смысле смерти подобно.
- Клиническая эффективность антибиотика in vitro не всегда тоже самое что in vivo (мы все таки отличаемся от чашки Петри).
- Неадекватное дозирование и длительность терапии (недостаточные дозы и короткие курсы) – отсюда осложнения и рецидивы.
- Высокая летальность при неадекватной терапии
Проводить антистафилококковую терапию меньше 3-х, а то и 4-х недель нельзя, так как для этого возбудителя характерно развитие метастатических очагов и весь процесс пойдет по новому, только с учетом еще и того, что возбудитель окажется резистентным к ранее проводимой терапии.
Когда можно лечить 2 недели стафилококковую инфекцию?
- В/в катетер или другой источник инфекции удален (хорошо если катетер, а если речь об импланте – его же не удалишь).
- Инфекционный эндокардит исключен по данным чрезпищеводной ЭХО-КГ.
- Отсутствуют импланты (протезированный клапан, кардиостимулятор, А-В фистула).
- Нормализация температуры и отрицательная гемокультура в течение 72 ч после удаления источника инфекции.
- Нет признаков метастатических очагов на других органах и тканях.
Во всех остальных случаях лечим 21-28 дней. А что происходит у нас? Максимум 10-14 дней пролечили и отпустили.
Антистафилококковые препараты мы обязаны назначить сразу как только получили положительную гемокультуру на стафилококк однократно! И только потом проводим повторную проверку, так как максимально раннее начало антибактериальной терапии в 2-3 раза снижает летальность.
Итак, как уже стало понятно, основную проблему представляют устойчивые формы S.aureus. Для их эрадикации были синтезированы и предлагаются к использованию следующие препараты
- Гликопептиды – Ванкомицин (1958 год) – категория доказательств IА
- Стрептогранины – Синерцид (в РФ отсут)
- Оксазолиндиноны – Линезолид – категория доказательств IА
- Липопептиды – Даптомицин – категория доказательств IА – Тигециклин – категория доказательств IIВ
1. Ванкомицин
Внедрен в практику в 1958 году, а первый устойчивый штамм стафилококка поймали только в 1996 году. Проблема с ванкомицинустойчивыми штамма стафилококка в том, что до сих пор нет отработанных схем преодоления этой самой устойчивости. Помимо прочего у возбудителей непрерывно нарастает МПК (минимальная подавляющая концентрация) к ванкомицину и сейчас при МПК 2 мы говорим о резистентном штамме.
Еще одна проблема – это плохо очищенные формы препарата. Если ванкомицин плохо очищен, то риск токсических нефропатий достигает 20%. К сожалению надо констатировать тот факт, что Ванкомицин отечественного разлива относится к плохо очищенным формам.
Основным и самым грозным осложнением является развитие острой почечной недостаточности, а она развивается у 40% пациентов, если дозировка препарата составляет более 4 гр/сут. А потому вводить данный препарат можно только под контролем клиренса креатинина (КК). То есть первый анализ мы проводим до введения препарата, второй через 2-3 дня и смотрим, если имеет место падение КК: если он падает на 25% – это говорит о нефротоксичном действии препарата, если на 50%, то препарат следует немедленно отменить.
Ванкомицин является бактериостатическим антибиотиком, эффективность действия мы оцениваем не ранее чем через 72 часа, а то и на 5-е сутки от начала терапии. Доза должна подбираться в соответствии с МПК возбудителя и под постоянным контролем клиренса креатинина. То есть для использования этого препарата нам необходимы хорошая клиническая и микробиологическая лаборатории.
Современные рекомендации по дозированию препарата выглядят следующим образом:
У Вас есть возможность это делать? У меня такой возможности не было и нет до сих пор, а потому мы до сих пор используем этот препарат как саперы на минном поле, где ошибиться можно только один раз.
Активность против MSSA у Ванкомицина сопоставима с плацебо, а значит применять его можно только при верифицированной MRSA, либо комбинировать с препаратами, активными против MSSA (цефазолином, например)
Следует так же помнить о том, что Ванкомицин, в виду строения его молекулы, а особенно ее размера, плохо проникает в ткани и проблемными его локализациями будут дыхательные пути, ЦНС, клапаны сердца и кости. А потому быстрого действия там не дождешься и терапия требуется очень и очень длительная.
В заключении хотелось бы сказать, что препарат хорош, но будет лучше, если вы его не будете назначать в самостоятельном режиме, а вызовете врача – клинического фармаколога, ибо назначение и дозировка таких вот препаратов входит в его непосредственные обязанности.
Что делать если клин. фарма нет, а пациент есть. И что надо соблюсти, чтобы безопасно применять ванкомицин?
- Использовать хроматографически очищенные препараты – Ванкоцин, Эдицин (в настоящих условиях это практически невозможно, торги они не выигрывают)
- Требуется коррекция гиповолемии, сердечной недостаточности (перфузия почек должна быть нормальное, иначе усугубим нефротоксический эффект)
- Избегать комбинаций с нефро- или ототоксичными препаратами (аминогликозидами, НПВС и т.д.)
- Коррекция режима дозирования по клиренсу креатинина. Если в течение 2-3-х дней он снизился вдвое от изначального, а данных за то, что он мог рухнуть не только от Ванко нет – это проявление нефротоксичности препарата.
2. Линезолид
Является чистым бактериостатиком. Производителем неоднократно заявлялось, что препарат эффективнее Ванкомицина, однако проведенные независимые метаанализы клинических исследований хорошего качества рандомизированных и с двойным слепым контролем показали, что единственное, где Линезолид имеет преимущество – это вентилятор-ассоциированный пневмонии, вызванные MRSA. В других случаях, в т.ч. и стафилококковой пневмонии, преимуществ нет никаких. Зато стоимость лечения повышается в разы.
Еще один момент, о котором умалчивается – это безопасность применения Линезолида. Да, нефротоксичности нет, но по данным того же метаанализа частота возникновения тромбоцитопений при его использовании в 11,72 раза выше чем в группе плацебо.
Таким образом, Линезолид является препаратом выбора при нозокомиальной вентилятор-ассоциированной MRSA пневмонии, где при его использовании летальность ощутимо ниже, чем при использовании ванкомицина.
3. Тигециклин (или тайгециклин)
Давайте разберемся и с ним, тем более к вам будут часто приходить и рассказывать про него как про самый препаратистый антибиотик в мире.
- Препарат позиционируется как новый класс антибиотиков, на деле это производный тетерациклина со всеми исходящими отсюда последствиями.
- Он является бактериостатиком, как все тетрациклины
- Имеет хорошую тканевую фармакокинетику, но при этом крайне низкие концентрации в плазме крови (ангиогенные инфекции из его показаний выпадают сразу)
А теперь о том, куда его следует применять:
- В качестве средства целенаправленной этиотропной терапии НИ, вызванных полирезистентными бактериями:
- БРЛС: альтернатива карбопенемам
- Ацинетобактер – альтернатива сульбактаму
- Клебсиела и E.coli – устойчивые к карбопенемам
- Stenotrophomonas maltophilia
Повторюсь еще раз, место его применения это ЦЕЛЕНАПРАВЛЕННАЯ ЭТИОТРОПНАЯ ТЕРАПИЯ, т.е. когда микроб четко установлен в результате бактериологического исследования вместе с чувствительностью к антибиотикам.
Повторюсь еще раз – место этого препарата в лечении грам-отрицательной инфекции, но никак не стафилококков. Да и вообще это препарат крайне глубокого резерва, как по характеристикам, так и по цене, т.к. в ближайшие 10 лет не будет ни одного нового препарата с Гр(-) активностью, так как их просто нет даже в проекте (медицина традиционно не успевает за возбудителями, а только пытается их догонять, о чем мы в самом начале и говорили, прослеживая эволюцию возбудителей)
4. Даптомицин.
Препарат появился у нас недавно, хотя во всем мире применяется уже очень давно (в Штатах с 2003 года)
Препарат относится к классу липопептидов и от всех имеющихся на данный момент антиMRSA препаратов отличается тем, что является бактерицидным. И этот самый эффект развивается у него очень быстро и нам не надо ждать нескольких дней. То есть антибактериальный эффект мы можем оценивать как и у всех бактерицидных препаратов через 48 часов от начала применения, а это очень важно у больных в тяжелом состоянии. Еще одним несомненным плюсом является то, что не происходит лизиса клеток и не увеличивается интоксикация.
Основными показаниями к применению являются:
- Эндокардит,
- Менингит,
- Остеомиелит,
- Инфекции у больных с нейтропенией,
- Сепсис стафилококковой этиологии
Также препарат может использоваться в эмпирической терапии (кстати, единственный из всех имеющихся на данный момент) Гр(+)инфекций, так как активность против MSSA и MRSA одинаковая.
Кроме того, препарат проявляет активность против MRSA в биопленках, а значит нет необходимости в удалении протезов и имплантов. А значит Даптомицин показан при ангиогенных инфекциях (бактериемиях), остеомиелите, бактериальном эндокардите.
- Препарат откровенно дорог
- В связи с крупным размером молекулы имеются проблемы с тканевой кинетикой, а потому пневмонии и инфекции ЦНС на данный момент мы им не лечим.
- Побочные эффекты – миалгии, производитель говорит о необходимости следить за КФК и обращать пристальное внимание на пациентов уже имеющих подобные проблемы.
- Описано несколько случаев эозинофильных пневмоний, а потому и на это следует обращать внимание, так как при своевременной диагностике и вовремя назначенной терапии, данный вид пневмонии проходит без следа.
Итак, сводя все к общему знаменателю:
Ванкомицин мы используем тогда, когда у нас верифицирован MRSA стафилококк, имеется хорошая микробиологическая лаборатория, которая нам даст его МПК и это МПК не будет больше 2 (иначе он уже резистентен), в наличие есть клинический фармаколог, который посчитает дозу, будет ее контролировать и корригировать согласно изменениям клиренса креатинина. Но при этом мы помним о том, что препарат не работает на MSSA. И конечно же мы продолжаем помнить о его высокой нефротоксичности, если не имеем возможности пользоваться высокоочищенными формами.
Тигециклину нечего делать антистафилококковой терапии, этот препарат предназначен только для этиотропной терапии Гр(-)инфекции.
В связи с высокой активностью против MRSA и MSSA, быстрым бактерицидным эффектом является препаратом выбора при ангиогенных инфекциях, сепсисе и инфекционном эндокардите, а также препаратом выбора при эмпирической терапии MRSA+MSSA. Не использовать при лечении нозокомиальных пневмоний и инфекций ЦНС.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Сепсис: причины появления, симптомы, диагностика и способы лечения.
Определение
Сепсис – это патологический процесс, в основе которого лежит реакция организма в виде генерализованного воспаления на инфекцию различной природы. При сепсисе бактерии преодолевают иммунную защиту человека и распространяются из очага воспаления по всему организму. Местное воспаление, сепсис, тяжелый сепсис и септический шок – это различные формы выраженности воспалительной реакции организма на инфекционный процесс.
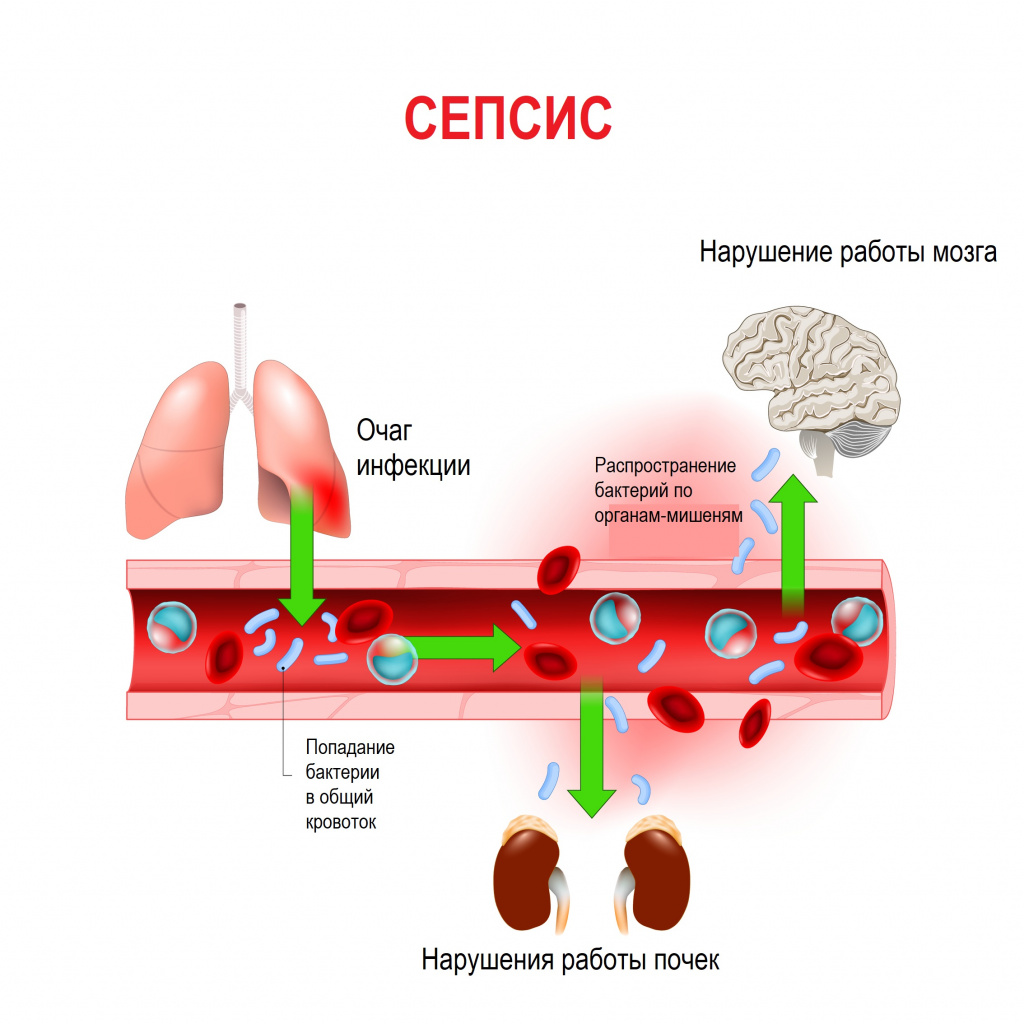
Истинная частота возникновения случаев сепсиса остается неизвестной, однако по оценкам исследователей, во всем мире сепсис является лидирующей причиной летальности у пациентов в критическом состоянии. Согласно результатам большого европейского исследования SOAP, включившего 3147 пациентов из 198 европейских медицинских центров, сепсис развился в 37,4% случаев, а госпитальная летальность от него колебалась от 14% случаев в Швейцарии до 41% в Португалии, в среднем составив 24,1%. Данные другого крупного исследования PROGRES (12 881 больной тяжелым сепсисом в 37 странах) показали, что госпитальная летальность в среднем составила 49,6%.
Причины возникновения сепсиса
Возбудителями сепсиса могут быть бактерии, вирусы или грибы. Но чаще сепсис имеет бактериальную природу - его причиной становятся стафилококки, стрептококки, пневмококки, менингококки, сальмонеллы, синегнойная палочка и др.
В большинстве случаев патологический процесс вызывают условно-патогенные микроорганизмы, которые присутствуют на коже, слизистых оболочках дыхательного и пищеварительного трактов, мочевыводящих путей и половых органов. Иногда при сепсисе выделяют сразу 2-3 микроорганизма.
Причиной сепсиса могут стать гнойно-воспалительные заболевания кожи (абсцессы, фурункулы, флегмоны), обширные травмы, ожоги, инфекционно-воспалительные заболевания мочевыводящей системы (пиелонефрит), живота (например, гнойно-некротический деструктивный панкреатит), тяжелая ангина, гнойный отит, пневмония, инфицирование во время родов или абортов и др.
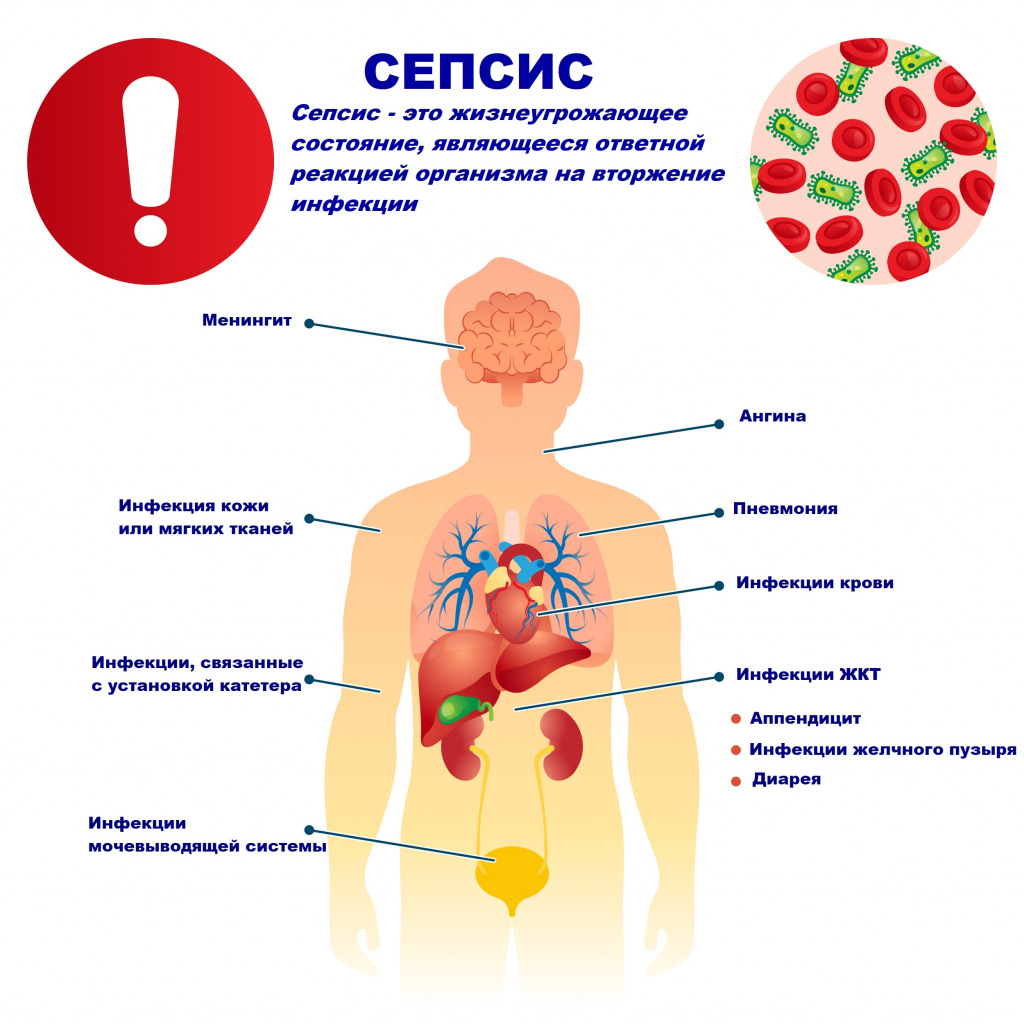
Возможность возникновения сепсиса зависит не только от свойств возбудителя, но и от состояния иммунной системы человека - нарушения в ее работе предрасполагают к распространению инфекции. Причинами таких нарушений могут быть врожденные дефекты иммунитета, хронические инфекционные болезни (ВИЧ, гнойные процессы), эндокринные заболевания (сахарный диабет), онкологические болезни, хронические интоксикации (алкоголизм, наркомания), проникающая радиация, прием иммуносупрессоров (кортикостероидов, цитостатиков) и др.
В ответ на внедрение возбудителя вырабатываются цитокины – особые белковые молекулы, которые выполняют защитные функции сначала на местном уровне, а затем, попадая в системный кровоток, продолжают работать уже на уровне всего организма. Цитокины бывают провоспалительными и противовоспалительными. В самом начале инфекционного процесса их количество находится в равновесии. Если регулирующие системы организма не способны поддерживать это равновесие, то цитокины накапливаются в кровотоке в сверхвысоких объемах, начинают доминировать их деструктивные, разрушающие эффекты, в результате повреждается сосудистая стенка, запускается синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром) и полиорганная дисфункция. Вследствие полиорганной дисфункции печени, почек, кишечника появляются новые повреждающие факторы (лактат, мочевина, билирубин и др.), которые усиливают деструктивные процессы. При ДВС-синдроме в сосудах микроциркуляторного русла образуются множественные тромбы в сочетании с несвёртываемостью крови, приводящей к множественным кровоизлияниям.
Классификация заболевания
В зависимости от локализации входных ворот и первичного очага сепсис подразделяют на:
- перкутанный (чрескожный) – развивается при попадании возбудителя в организм через поврежденный кожный покров (ранки, царапины, фурункулы и др.);
- акушерско-гинекологический – развивается после родов и абортов;
- оральный (одонтогенный и тонзиллогенный) – развивается в результате первичной инфекции в полости рта;
- оториногенный – развивается в результате распространения инфекции из полости уха и/или носа;
- пневмогенный – при наличии инфекционного очага в нижних дыхательных путях;
- хирургический;
- урологический;
- пупочный – развивается у новорожденных вследствие проникновения инфекционных агентов в кровь через пупочную ранку;
- криптогенный (идиопатический, эссенциальный, генуинный) – сепсис неизвестного происхождения: первичный очаг гнойного воспаления неизвестен.
- молниеносный сепсис,
- острый сепсис,
- подострый сепсис,
- хронический сепсис (хрониосепсис).
По клиническим признакам:
1. Синдром системного воспалительного ответа (ССВО) – системная реакция организма на воздействие различных сильных раздражителей (инфекции, травмы, операции и др.) характеризуется двумя или более признаками:
- температура тела ≥ 38°С или ≤ 36°С;
- частота сердечных сокращений (ЧСС) ≥ 90 ударов в минуту;
- частота дыхания (ЧД) > 20 в минуту или гипервентиляция (РаСО2 ≤ 32 мм рт. ст.);
- лейкоциты крови > 12х109 /л или < 4х109 /л, или незрелых форм >10%.
По виду и характеру возбудителя:
- аэробный сепсис,
- анаэробный сепсис,
- смешанный сепсис,
- грибковый сепсис,
- вирусный сепсис.
Клинические проявления сепсиса могут варьировать от незначительных до критических. При молниеносном течении патологическое состояние развивается бурно - за несколько часов или суток. При остром сепсисе симптомы развиваются за несколько дней. Для хрониосепсиса характерно вялое течение и наличие малозаметных изменений, формирующихся месяцами. Рецидивирующий сепсис протекает с эпизодами обострений и затуханий.
Инкубационный период после выявления ворот инфекции или первичного очага составляет от 1 до 3-5 суток. Начало сепсиса, как правило, острое, хотя иногда может быть подострым или постепенным. Интоксикация проявляется резкой слабостью, адинамией, анорексией, нарушением сна, головной болью, расстройством сознания, менингеальным синдромом (поражением оболочек головного и спинного мозга), тахикардией, артериальной гипотензией. Температура тела держится высокой, со скачками утром и вечером. Признаки интоксикации особенно выражены на высоте лихорадки. На коже у трети больных появляется геморрагическая сыпь.
Со стороны дыхательной системы наблюдаются одышка и хрипы в легких. При нарушении функции почек снижается количество выделяемой мочи (олигурия) вплоть до полного прекращения мочеиспускания (анурия), в моче появляются следы крови, гноя. Наблюдается ухудшение функции печени с развитием желтухи и явлениями гепатита, увеличивается селезенка. Повреждение органов ЖКТ проявляется нарушением пищеварения, отсутствием аппетита, язык сухой, обложенный, нередко наблюдаются упорные септические поносы, тошнота и рвота. Метастазирование возбудителя из первичного очага с образованием вторичных очагов инфекции может приводить к инфаркту легкого, гангрене легкого, гнойному плевриту, эндокардиту (поражению внутренней оболочки сердца), воспалению сердечной мышцы (миокардиту), воспалению околосердечной сумки (перикардиту), гнойному циститу, абсцессам мозга и воспалению оболочек мозга (гнойному менингиту), гнойным артритам, флегмонам и абсцессам в мышцах.
Недостаточность функции одного органа длительностью более суток сопровождается летальностью до 35%, при недостаточности двух органов – 55%, при недостаточности функции трех и более органов летальность к четвертому дню возрастает до 85%.
Производят посевы крови, мочи, ликвора, мокроты, гнойного экссудата из элементов сыпи, абсцессов, пунктатов плевры, суставов и других септических очагов. Посевы делают многократно, чтобы определить чувствительность к максимальному количеству антибиотиков. Используется также обнаружение антигенов в крови методом ИФА и определение генома возбудителя методом ПЦР.
Одним из наиболее специфичных и чувствительных маркеров бактериальной инфекции служит прокальцитониновый тест. Прокальцитонин – один из основных маркёров системного воспаления, вызванного бактериями.
Синонимы: Анализ крови на прокальцитонин; ПКТ. Procalcitonin; PCT. Краткая характеристика определяемого вещества Прокальцитонин Прокальцитонин является прогормоном кальцитонина, состоящим из 116 аминокислот с молекулярной массой 14,5 кDa. Биосинтез прокальцитонина в физиологических условиях прои.
Как наилучшим образом вести пациента со стафилококковой инфекцией кожи? Как врач общей практики может диагностировать и лечить рожистое воспаление? Какое лечение эффективно при эритразме? B норме кожа человека заселена огромным
Как наилучшим образом вести пациента со стафилококковой инфекцией кожи?
Как врач общей практики может диагностировать и лечить рожистое воспаление?
Какое лечение эффективно при эритразме?
B норме кожа человека заселена огромным количеством бактерий, мирно сосуществующих на ее поверхности или в волосяных фолликулах.
Однако кожа обладает определенными свойствами, защищающими ее от инфицирования патогенами. К ним относятся плотный и сухой ороговевающий слой, практически непроницаемый для микроорганизмов, и клейкое межклеточное вещество — сложная смесь липидов, плотно соединяющая клетки мальпигиевого слоя и также защищающая кожу, закупоривая вход в волосяные фолликулы.
Другие факторы, останавливающие проникновение патогенных микроорганизмов, включают постоянное обновление клеток кожи, кислое значение pH, наличие иммуноглобулинов в составе пота и различные виды кожной флоры.
Кожные инфекции, как правило, развиваются только тогда, когда травма, избыточная гидратация или воспалительные заболевания кожи нарушают эти защитные свойства. Организмы, вызывающие кожные инфекции, могут быть частью постоянной кожной флоры или ближайших слизистых оболочек или происходить из внешних источников, таких как другой человек, окружающая среда или зараженные объекты.
Импетиго — наиболее поверхностная кожная инфекция, вызываемая S. aulreuls и S. pyogenes. Различают два основных клинических варианта: буллезное импетиго, считающееся стафилокковым заболеванием, и небуллезное импетиго, вызываемое S. aulreuls или S. pyogenes либо обоими организмами.
Заболевание встречается у детей гораздо чаще, чем у взрослых, развиваясь на открытых частях тела, лице и конечностях, в местах царапин, ссадин и укусов насекомых.
Вначале появляются красные пятна, которые превращаются в пузырьки и гнойнички, легко вскрывающиеся и образующие толстые, слипшиеся желтовато-коричневые чешуйки на эритематозном основании (см. рис. 1). Они часто многочисленны, могут вызывать зуд, но, как правило, безболезненны.
 |
| Рисунок 1. Толстые желтые корки в основании эритемы и поверхностных эрозий у пациента со стрептококковым импетиго |
При буллезной форме могут развиваться большие пузырьки и волдыри диаметром 1-2 см. Они вскрываются медленнее и сохраняются в течение двух-трех дней. Возбудители, как правило, определяются культивированием, но в клинически очевидных случаях в этом нет необходимости.
Наиболее серьезным осложнением импетиго является постстрептококковый острый гломерулонефрит, общая заболеваемость которым в последние годы снизилась.
Буллезное импетиго обусловлено исключительно S. aulreuls, который выделяет токсин эксфолиатин, вызывающий расщепление межклеточного вещества в поверхностных слоях эпидермиса. Абсорбируясь в большом количестве в кровоток, этот токсин вызывает стафилококковый синдром обожженной кожи, который в 5% случаев заканчивается летально.
При инфекциях средней тяжести и локализованных формах используют местный антибиотик, например мупироцин или фузидовую кислоту, эффективно также местное применение неомицина и бацитрацина. Очень действенно использование ликацин-геля.
При тяжелых и распространенных формах назначают системный антибиотик. Обычно достаточно эритромицина или цефалоспорина первого поколения, например цефалексина.
Эктима относится к инфекциям, напоминающим импетиго, но затрагивающим более глубокие слои кожи. Она характеризуется формированием толстых слипшихся чешуек (см. рис. 2), покрывающих области изъязвлений кожи, которым предшествует образование гнойничков и пузырьков. Чаще всего поражаются ягодицы, бедра и ноги. Заболевание распространено в тропиках, где его развитию способствуют плохие гигиенические условия и недостаточное питание. Возбудителями могут быть S aulreuls или S pyogenes либо оба микроорганизма, но вызываемые ими изъязвления достигают дермы и заживают рубцеванием, что не свойственно импетиго. Лечение — системные антибиотики, воздействующие на S. aulreuls и S. pyogenes.
Поверхностный фолликулит, фурункулы и карбункулы. Фолликулит (воспаление эпителия волосяных фолликулов) — распространенное дерматологическое заболевание, не всегда первично только инфекционной природы. Физическая или химическая травма, а также связанное с профессиональным занятием воздействие продуктов смолы, применяемых также в лечебных целях, — все это вызывает фолликулит.
При проникновении стафилококков в более глубокие слои волосяных фолликулов воспаление захватывает дерму, вызывая образование фурункулов и карбункулов. Развивается воспалительный пузырек с гнойной головкой (фурункул) или инфекция охватывает несколько близлежащих волосяных фолликулов и образуется воспалительный конгломерат, из которого высвобождается гной (карбункул).
Фурункулы чаще всего встречаются на лице и ногах, а типичная локализация карбункулов — задняя часть шеи; как правило, они сопутствуют сахарному диабету. Крупные фурункулы и карбункулы вскрывают и дренируют, назначая пенициллиназо-устойчивый антибиотик.
Рецидивирующие стафилококковые инфекции кожи. Некоторые пациенты подвержены рецидивам стафилококковых инфекций кожи.
Предрасполагающими факторами здесь служат сахарный диабет, хроническая почечная недостаточность и некоторые иммуннодефицитные состояния, но у большинства пациентов перечисленные выше заболевания отсутствуют: вероятно, эти больные являются хроническими носителями стафилококков, и при мельчайшей травме кожи патогены вызывают инфекцию.
Рецидивы таких инфекций пытаются предотвратить различными способами: путем омывания кожи различными антисептиками, лечения других членов семьи антистафилококковыми антибиотиками и пролонгированной терапии другими местными или системными антибактериальными препаратами. Все эти методы направлены на уничтожение стафилококкового “шлейфа”.
К сожалению, эти меры, как правило, неспецифичны и малоэффективны, так как бактерии появляются вновь вскоре после отмены антимикробного препарата. Поэтому предпочтительнее длительное использование местных антисептиков.
Рожа и целлюлит — это острые, быстро распространяющиеся инфекции кожи и подлежащих тканей.
Отличительной чертой рожистого воспаления является четко очерченный, приподнятый край, отражающий вовлечение более поверхностных (дермальных) слоев (см. рис. 3). Однако целлюлит может располагаться поверхностно, а рожа глубже, так что во многих случаях эти два процесса сосуществуют и различить их практически невозможно.
Считается, что рожистое воспаление вызывается стрептококками, как правило, группы A и иногда — группами G и C. При целлюлите высевается либо только S. aulreuls, либо совместно со стрептококком. H. influlenzae типа b — важный этиологический фактор лицевого целлюлита у детей младше двух лет.
Рожа, в типичном случае поражающая лицо, — болезнь пожилых, развивающаяся без видимых причин или иногда после травмы лица.
Целлюлит поражает нижние конечности, в особенности область икр. Ему часто предшествует травма, язва или другое повреждение кожи, откуда и исходит инфекция.
Как и при рожистом воспалении, целлюлит может сопровождаться или предваряться лихорадкой и ознобом, но у многих пациентов температура не повышается, и они не выглядят серьезно больными.
Кожа красная, горячая и отечная, края воспаленного участка неровные, на поверхности могут развиваться пузырьки и волдыри (см. рис. 4). В редких случаях обнаруживается лимфангит и региональный лимфаденит.
Без лечения могут развиваться такие осложнения, как фасциит, миозит, подкожный абсцесс и септикопиемия. Периорбитальный целлюлит, вызванный обычно травмой, может осложняться тромбозом пещеристого синуса, формированием орбитального, субпериостального или церебрального абсцессов или менингитом.
Пациентов с этими состояниями необходимо госпитализировать.
Описанные здесь стафилококковые и стрептококковые пиодермии составляют большую часть кожных бактериальных инфекций. Нужно уметь различать инфекционные процессы, присущие трем клиническим ситуациям:
- инфекция не укладывается в рамки типичной клинической картины пиодермии или не поддается полностью стандартной терапии;
- организм пациента ослаблен и не может выдержать борьбу с инфекцией;
- в эпидемиологическом анамнезе есть возможность контакта с необычными кожными патогенными микроорганизмами.
- Инфекции, вызываемые резидентными коринебактериями
Для эритразмы характерны красно-коричневые шелушащиеся участки кожи, расположенные в паху, в подмышечных впадинах и межпальцевых промежутках (см. рис. 5).
Corynebacteriulm minultissimulm считается этиологическим фактором этого заболевания, протекающего бессимптомно и развивающегося, как правило, у диабетиков, тучных и пожилых людей, а также у тех, кто проживает в тропическом климате.
Благодаря тому что данные микроорганизмы продуцируют порфирины, в ультрафиолетовом свете лампы Вуда пораженные участки флюоресцируют от кораллово-розового до оранжево-красного оттенка, что подтверждает диагноз. Как правило, культивирования не требуется.
Иногда для излечения достаточно интенсивного мытья с мылом. Другой подход — местное лечение эритромицином и клиндамицином или местными азолями, например клотримазолом, которые активны в отношении некоторых грам-положительных бактерий и грибов. При обширных поражениях наиболее эффективен, вероятно, эритромицин.
Оспенный кератолиз — это поверхностная кожная инфекция, очевидно вызываемая штаммами Corynebacteriulm и характеризующаяся наличием оспинок диаметром 1-7 мм на подошвах стоп. Оспинки, сливаясь, могут образовывать поверхностные эрозии.
Заболевание обычно протекает бессимптомно, но иногда пациенты жалуются на зудящую, как от ожога, боль или сырный запах.
Похоже, оспенный кератолиз связан с избыточным увлажнением ног из-за тесной обуви, частых контактов с водой или повышенной потливости.
Лечение гипергидроза вкупе с методами, описанными для эритразмы, как правило, эффективно.
Подмышечный трихомикоз проявляется восковыми узелками, формирующимися в волосах подмышки. Желтые, красные или черные, они образуются большими колониями коринеформных бактерий, покрывающих кутикулу волоса.
Прежде всего заболевание поражает пациентов, которые мало внимания уделяют личной гигиене и страдают избыточным потоотделением.
Для успешного лечения, как правило, достаточно брить волосы и пользоваться дезодорантами для подмышек. Эффективно также местное применение эритромицина и клиндамицина.
Литература
1. Noble W. C. Microbal Skin Disease: its Epidemiology. Arnold, London, 1983.
2. Hoor E. W., Hooton T. M., Horton C. A. et al. Mircroscopic evalulation of cultaneouls cellulitis in adults // Arch. Intern. Med. 1986; 146: 295-297.
Что такое рожа (или рожистое воспаление)?
Рожа или рожистое воспаление – серьезное инфекционное заболевание, внешними проявлениями которого является прогрессирующие поражение (воспаление) кожного покрова.
Слово рожа произошло от французского слова rouge, что в переводе означает – красный.
По распространенности в современной структуре инфекционной патологии рожа занимает 4-е место - после острых респираторных и кишечных инфекций, вирусных гепатитов, особенно часто регистрируется в старших возрастных группах. От 20 до 30 лет рожей страдают в основном мужчины, чья профессиональная деятельность связана с частой микротравматизацией и загрязнением кожи, а также с резкими сменами температуры. Это водители, грузчики, строители, военные и т. д. В старшей возрастной группе большая часть больных – женщины. Рожистое воспаление обычно появляется на ногах и руках, реже – на лице, еще реже – на туловище, в промежности и на половых органах. Все эти воспаления хорошо заметны окружающим и вызывают у больного чувство острого психологического дискомфорта.
Причина заболевания
Причина заболевания – проникновение стрептококка через поврежденную царапинами, ссадинами, потертостями, опрелостью и т.п. кожу.
Около 15% людей могут являться носителями этой бактерии, но при этом не болеют. Потому что для развития недуга необходимо, чтобы в жизни больного присутствовали также определенные факторы риска или предрасполагающие заболевания.
- нарушения целостности кожи (ссадины, царапины, уколы, потертости, расчесы, опрелость, трещины);
- резкая смена температуры (как переохлаждение, так и перегрев);
- стрессы;
- инсоляция (загар);
- ушибы, травмы.
Очень часто рожа возникает на фоне предрасполагающих заболеваний: грибка стопы, сахарного диабета, алкоголизм, ожирения, варикозной болезни вен, лимфостаза (проблемы с лимфатическими сосудами), очагов хронической стрептококковой инфекции (при роже лица – тонзиллит, отит, синусит, кариес, пародонтит; при роже конечностей – тромбофлебит, трофические язвы), хронических соматических заболеваний, снижающих общий иммунитет (чаще в пожилом возрасте).
Стрептококки широко распространены в природе, относительно устойчивы к условиям внешней среды. Спорадический рост заболеваемости наблюдается в летне-осенний период.
Источником инфекции при этом являются как больные, так и здоровые носители.
Признаки, характерные для рожистого воспаления
Клиническая классификация рожи основана на характере местных изменений (эритематозная, эритематозно-буллезная, эритематозно-геморрагическая, буллезно-геморрагическая), на тяжести проявлений (легкая, среднетяжелая и тяжелая), на кратности возникновения заболевания (первичная, рецидивирующая и повторная) и на распространенности местных поражений организма (локализованная - ограниченная, распространенная).
Заболевание начинается остро с появления озноба, общей слабости, головной боли, мышечных болей, в ряде случаев - тошноты и рвоты, учащения сердцебиения, а также повышения температуры тела до 39,0-40,00С, в тяжелых случаях могут быть судороги, бред, раздражение мозговых оболочек. Через 12-24 ч с момента заболевания присоединяются местные проявления заболевания - боль, покраснение, отек, жжение и чувство напряжения пораженного участка кожи. Местный процесс при роже может располагаться на коже лица, туловища, конечностей и в отдельных случаях - на слизистых оболочках.
При эритематозной форме рожи пораженный участок кожи характеризуется участком покраснения (эритемой), отеком и болезненностью. Эритема имеет равномерно яркую окраску, четкие границы, склонность к периферическому распространению и возвышается над кожей. Ее края неправильной формы (в виде зазубрин, "языков пламени" или другой конфигурации). В последующем на месте эритемы может появляться шелушение кожи.
Эритематозно-буллезная форма заболевания начинается так же, как и эритематозная. Однако спустя 1-3 сут с момента заболевания на месте эритемы происходит отслойка верхнего слоя кожи и образуются различных размеров пузыри, заполненные прозрачным содержимым. В дальнейшем пузыри лопаются и на их месте образуются коричневого цвета корки. После их отторжения видна молодая нежная кожа. В отдельных случаях на месте пузырей появляются эрозии, способные трансформироваться в трофические язвы.
Эритематозно-геморрагическая форма рожи протекает с теми же проявлениями, что и эритематозная. Однако в этих случаях на фоне эритемы появляются кровоизлияния в пораженные участки кожи.
Буллезно-геморрагическая рожа имеет практически те же проявления, что и эритематозно-буллезная форма заболевания. Отличия состоят только в том, что образующиеся в процессе заболевания на месте эритемы пузыри заполнены не прозрачным, а геморрагическим (кровянистым) содержимым.
Легкая форма рожи характеризуется кратковременной (в течение 1-3 сут), сравнительно невысокой (до 39,0оС) температурой тела, умеренно выраженной интоксикацией (слабость, вялость) и эритематозным поражением кожи одной области. Среднетяжелая форма рожи протекает с относительно продолжительной (4-5 сут) и высокой (до 40,0оС) температурой тела, выраженной интоксикацией (резкая общая слабость, сильная головная боль, анорексия, тошнота, рвота и др.) с обширным эритематозным, эритематозно-буллезным, эритематозно-геморрагическим поражением больших участков кожи. Тяжелая форма рожи сопровождается продолжительной (более 5 сут), очень высокой (40,0оС и выше) температурой тела, резкой интоксикацией с нарушением психического статуса больных (спутанность сознания, делириозное состояние - галлюцинации), эритематозно-буллезным, буллезно-геморрагическим поражением обширных участков кожи, часто осложняющимся распространенными инфекционными поражениями (сепсисом, пневмонией, инфекционно-токсическим шоком и др.).
Рецидивирующей считается рожа, возникшая на протяжении 2 лет после первичного заболевания на прежнем участке поражения. Повторная рожа развивается более чем через 2 года после предыдущего заболевания.
Рецидивирующая рожа формируется после перенесенной первичной рожи вследствие неполноценного лечения, наличия неблагоприятных сопутствующих заболеваний (варикозная болезнь вен, микозы, сахарный диабет, хронические тонзиллиты, синуситы и др.), развития иммуной недостаточности.
Осложнения
Прогноз
Прогноз благоприятный. При часто рецидивирующей роже может возникнуть слоновость, нарушающая трудоспособность.
Профилактика рожистого воспаления
Предупреждение травм и потертостей ног, лечение заболеваний, причиной которых является стрептококк.
Частые рецидивы (более 3 в год) в 90% случаев оказываются следствием сопутствующего заболевания. Поэтому лучшей профилактикой второго и последующих пришествий рожи является лечение основного заболевания.
Но также существует и медикаментозная профилактика. Для больных, которых рожистое воспаление мучает регулярно, существуют специальные антибиотики пролонгированного (медленного) действия, мешающие стрептококку размножаться в организме. Эти лекарства надо принимать длительное время – от 1 месяца до года. Но принять решение о необходимости такого лечения может только врач.
Что может сделать Ваш врач?
Лечат рожу, как и любое другое инфекционное заболевание, антибиотиками. Легкую форму – амбулаторно, средние и тяжелые – в стационаре. Помимо препаратов применяется физиотерапия: УФО (местное ультрафиолетовое облучение), УВЧ (ток высокой частоты), терапия лазерами, работающими в инфракрасном световом диапазоне, воздействие слабыми разрядами электротока.
Объем лечения определяет только врач.
Что можете сделать Вы?
При появлении первых же признаков нужно обратиться к врачу. Нельзя затягивать с лечением, чтобы избежать серьезных осложнений.
Р-р д/местн. и наружн. прим. масляный 20%: 5 мл, 10 мл, 15 мл, 20 мл, 30 мл или 50 мл фл., 15 мл, 20 мл или 25 мл фл.-капельн.
Читайте также:

