Кандидоз ступней и ладоней
Обновлено: 25.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Кандидоз: причины появления, симптомы, диагностика и способы лечения.
Кандидоз – инфекционное заболевание, вызываемое дрожжеподобными грибками рода Candida. Оно обусловлено активным размножением грибка на слизистых оболочках полости рта, половых и внутренних органов и на коже.
Все представители рода Candida относятся к условно-патогенным микроорганизмам, то есть они постоянно присутствуют в составе нормальной микрофлоры. Но при снижении иммунитета, изменении гормонального фона и по ряду других причин эти грибки могут начать активно колонизировать слизистые оболочки и кожу.
Наиболее распространенные представители рода – Candida albicans и C. tropicalis. В 90-95% случаев урогенитального кандидоза именно C. albicans является доминирующим возбудителем.
![shutterstock_714362212 [преобразованный].jpg](https://www.invitro.ru/upload/medialibrary/d29/d29b49ccfe770f215bf7b01b406a2d2f.jpg)
Первый контакт с грибками рода Candida происходит во время прохождения ребенка по родовым путям. Однако в медицинской литературе описаны случаи обнаружения этих микроорганизмов в околоплодных водах, что свидетельствует о возможности вертикального (трансплацентарного) пути передачи. Также встречается передача грибка рода Candida при грудном вскармливании, кожном контакте ребенка с матерью, бытовым и пищевым путями.
Эти микроорганизмы вырабатывают эндотоксины и ферменты, вызывающие гибель клеток и некроз тканей, что способствует усилению адгезивной (прикрепление к клеткам слизистых оболочек или кожи) способности грибка и обеспечивает проникновение в ткани.
Гиперпродукция этих и ряда других веществ обуславливает патогенность представителей семейства Candida.
Причины возникновения кандидоза
- Экзогенные (внешние) факторы, способствующие проникновению грибков в организм:
- профессиональные вредности, приводящие к частым повреждениям кожи;
- длительное пребывание в теплой и влажной среде;
- нарушение целостности слизистых оболочек.
- Факторы, приводящие к снижению сопротивляемости организма:
- наличие хронических заболеваний;
- длительный прием препаратов, способствующих нарушению естественной микрофлоры;
- несбалансированное питание;
- частые стрессы, нарушения режима сна и отдыха.
- Нарушения обмена веществ (гиповитаминозы), заболевания иммунной системы (ВИЧ-инфекция), эндокринные патологии (сахарный диабет и пр.).
- Длительный прием некоторых препаратов: гормональных контрацептивов, системных глюкокортикостероидов, антибиотиков широкого спектра действия, цитостатиков.
- Длительное пребывание или проживание в местности с повышенной влажностью и температурой, комфортными для циркуляции спор грибков в окружающей среде.
По локализации процесса выделяют:
- Урогенитальный кандидоз.
- Кандидоз слизистой оболочки полости рта.
- Поверхностный кандидоз.
- Межпальцевый кандидоз.
- Кандидоз околоногтевых валиков и ногтей.
- Кандидоз желудочно-кишечного тракта.
Урогенитальный кандидоз (УГК) – широко распространенное заболевание: по данным медицинской статистики, около 75% женщин репродуктивного возраста хотя бы единожды регистрировали у себя симптомы УГК.
Выделяют острую и хроническую форму урогенитального кандидоза, кандидоз вульвы, вагины и других урогенитальных локализаций. В ряде случаев при диагностике используют уточнение: осложненный или неосложненный УГК, что отражает количество обострений в год и степень выраженности заболевания.
Симптомы женского урогенитального кандидоза
- Появление бело-желтых творожистых или сливкообразных выделений из половых путей. Интенсивность выделений может усиливаться перед менструацией, что связано с изменением гормонального фона.
- Неприятные ощущения, зуд в области гениталий, зачастую усиливающиеся при половом контакте или мочеиспускании.
- Покраснение и отечность слизистой вульвы и влагалища, наличие повреждений на коже половых органов (трещины, микротравмы).
- При хроническом течении УГК развивается сухость слизистых оболочек половых путей.
- Покраснение, отечность, неприятные ощущения в области половых органов.
- Беловатые выделения творожистой структуры из половых путей.
- Боль и жжение при половом контакте и при мочеиспускании.
Межпальцевый кандидоз локализуется в пространстве между пальцами. При этом отмечается покраснение участков кожи с последующим появлением пузырьков в прозрачным содержимым. Заболевание быстро распространяется в тесных коллективах (в детских садах, школах и т. д.).
Кандидоз слизистой оболочки полости рта (КСОПР)
Кандидоз полости рта вызывает неприятные ощущения, особенно при приеме пищи – жжение, боль, сухость. В зависимости от локализации процесса выделяют несколько форм кандидоза полости рта.
Часто КСОПР и желудочно-кишечного тракта сопровождает иммунодефицитные состояния: ВИЧ-инфекцию, синдром приобретенного иммунодефицита человека (СПИД) или врожденный иммунодефицит (например, при патологии Т-лимфоцитов). При наличии этих заболеваний кандидоз протекает с максимально выраженными симптомами, с трудом поддается лечению, носит агрессивный характер.
Самое частое проявление КСОПР – кандидозный стоматит, поражающий в основном грудных детей и взрослых с ослабленным иммунитетом.
При этой патологии слизистая оболочка полости рта краснеет, отекает, на ней появляются белесоватые пленки, имеющие творожистую консистенцию. На начальных стадиях болезни налет легко снимается. С течением заболевания пленки становятся плотнее, отделяются с трудом, при снятии обнажается кровоточащая слизистая оболочка.
При кандидозном стоматите возможно поражение языка, что проявляется покраснением спинки языка, появлением налета и слущиванием эпителия. Эти симптомы сопровождаются сильными болевыми ощущениями пораженной области при разговоре, приеме пищи и при пальпации (прощупывании) языка.
У курильщиков чаще других видов КСОПР развивается хронический гиперпластический кандидоз, сопровождаемый образованием белых, сливающихся между собой бляшек, которые возвышаются над поверхностью гиперемированной слизистой.
При этой патологии изменяется консистенция слюны: она становится вязкой и пенящейся; появляются неприятный запах изо рта, налет на слизистой серого или белого цвета. В 10-40% случаев эта клиническая форма кандидоза малигнизируется (т. е. приобретает злокачественный характер).
У пожилых людей чаще всего развивается хроническая атрофическая форма кандидоза полости рта. Слизистая оболочка при этом краснеет и отекает. Поражение часто локализуется под зубными протезами, что вызывает болевые ощущения.
Кандидозный хейлит и кандидоз углов рта в основном встречаются у детей и пожилых. Поражение обычно двустороннее, при этом образуются красные болезненные трещины в углах рта, покрытые легко снимающимся белым налетом или чешуйками. При длительном течении заболевания возможно присоединение бактериальной инфекции.
Диагностика кандидоза
Алгоритм диагностического поиска при кандидозе любой локализации включает в себя взятие материала с пораженной области с последующей его микроскопией, посевом для определения вида грибка и его чувствительности к антимикотическим (противогрибковым) препаратам.
В целях диагностики состояний, приведших к снижению иммунитета, используется общий анализ крови;
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Трудности в лечении и реабилитации больных микробной экземой (МЭ) определяются сложностью купирования рецидивов заболевания традиционными методами лечения.
Трудности в лечении и реабилитации больных микробной экземой (МЭ) определяются сложностью купирования рецидивов заболевания традиционными методами лечения. Нередко обострения МЭ возникают на фоне, казалось бы, адекватной терапии, при простудных заболеваниях, обострении очагов хронической инфекции, стрессах и т.п. Ведущую роль впатогенезе МЭ играет бактериальная сенсибилизация. Она связана с наличием и персистенцией очагов хронической инфекции на фоне изменения нейроэндокринной и иммунной систем. Выделяют несколько разновидностей МЭ — паратравматическая, нуммулярная, варикозная, сикозиформная, экзема сосков и пигментного кружка у женщин.
В настоящее время в патогенезе дерматозов аллергического генеза большая роль отводится триггерным факторам. Это бактериальные, микогенные, герпетическая и цитомегаловирусная инфекции, а также дисбиоз кишечника, с повышенной пролиферацией патогенной и условно патогенной флоры. Кроме того, присутствие в кишечнике Helicobacter pylori, паразитирование гельминтов, лямблий могут способствовать развитию заболевания. У больных МЭ установлено изменение кожной реактивности к Staphylococcus aureus, Streptococcus hemolythicus (бета-гемолитический), Candida albicans. Сенсибилизация к указанным аллергенам характеризуется возрастанием частоты и размеров гиперэргической реакции немедленного типа (ГНТ) и снижением этих показателей гиперэргической реакции замедленного типа (ГЗТ).
Кандидозная инфекция из года в год становится значимой междисциплинарной проблемой, что обусловлено ее широким распространением среди населения. Грибы Candida spp. по встречаемости у человека оставляют позади все остальные грибы, вместе взятые. Они выявляются на коже и слизистых оболочках более чем у половины всего населения, являются оппортунистической инфекцией, персистируя у иммунокомпроментированных лиц.
Широкое использование антибиотиков, кортикостероидов, гормональных контрацептивов способствовало трактовке кандидоза как одного из серьезных инфекционных осложнений медикаментозной терапии. Поводы для назначения антибиотиков больным МЭ многочисленны. Это, в первую очередь, традиционные схемы лечения с обязательным назначением антибиотиков, использование последних при обострении очагов бактериальной инфекции, присоединении вторичной пиодермии как следствие нарушения целостности кожи при ее расчесывании. Системные кортикостероиды при лечении МЭ применяются реже. Они показаны при тяжелом течении заболевания и возникновении аллергических реакций на введение медикаментов.
Назначая больному МЭ антибиотики, задумываемся ли мы над рядом вопросов. Какова реальность возникновения кандидоза в каждом конкретном случае? Как колонизация организма больного МЭ грибами Candida spp. может отразиться на течении основного заболевания? Как правильно клинически и лабораторно диагностировать кандидоз? Как выбрать эффективный антимикотик, учитывая их значительное количество на фармацевтическом рынке? Каким антимикотикам отдать предпочтение — системным или топическим? Как после проведенной терапии предотвратить рецидив заболевания, учитывая оппортунистический характер кандидоза? Проводя наши исследования, мы попытались ответить на часть из этих вопросов.
Целью настоящего исследования явилось изучение особенностей течения МЭ, осложненной поверхностным кандидозом кожи (КК) и/или слизистых оболочек (КСО) и совершенствование на этой основе тактики ведения больных.
Материалы и методы исследования. Работа выполнялась на базе научно-исследовательского института вакцин и сывороток им. И. И. Мечникова. Встречаемость больных МЭ среди больных с дерматологической патологией составила 8%. Под наблюдением было 74 больных МЭ в возрасте от 7 до 48 лет, мужчин 34 (46%), женщин 40 (54%). Средний возраст пациентов составил 17,4±11,2 лет. Длительность заболевания сроком до 2 месяцев имели только 12,2% больных. Остальные пациенты болели значительно дольше, в том числе 1/3 — от 6 месяцев до года, а 40,5% более года. Практически все больные МЭ имели очаги хронической инфекции: преобладали заболевания ЛОР-органов (3/4 пациентов), воспалительные заболевания органов малого таза (почти 1/2 женщин), заболевания верхних дыхательных путей (1/3). Важно отметить полиорганность воспалительных заболеваний у больных МЭ. Только на одну систему предъявляли жалобы 16,2% больных. Две системы были вовлечены в процесс у 1/3 (31,1% или 23), три — у 1/3 (33,8% или 24), четыре — у 1/5 (18,9% или 14). Иными словами, у пациентов имела место персистирующая микробная сенсибилизация. Преобладали больные нуммулярной МЭ (78,3%), реже наблюдалась микотическая экзема кистей (18,9%). Сикозиформную экзему (1,4%) и экзему пигментного соска и пигментного кружка (1,4%) имели только один мужчина и одна женщина. Большинство пациентов (86%) до обращения к нам получали лечение, в том числе достаточно интенсивное, по месту жительства или в другом лечебном учреждении.
Учитывая, что культуральная диагностика не позволяет дифференцировать носительство и кандидоз как заболевание, использована окраска мазков по Романовскому–Гимзе, дающая возможность идентифицировать псевдомицелий как ключевой механизм патогенеза. Материалом для культуральной диагностики служило отделяемое зева, носа и половых органов. Посев материала осуществляли на среду Сабуро и питательные селективные среды. При бактериологическом исследовании учитывался только обильный рост колоний. Для оценки состояния микробиоценоза кишечника всем больным проведены исследования микрофлоры толстой кишки по общепринятой методике Р.В.Эпштейн-Литвак иФ.Л.Вильшанской (1970).
Результаты исследования. Клинически и лабораторно поверхностный кандидоз кожи диагностирован у 48 (65%) больных МЭ, а дрожжеподобные грибы рода Candida spp. в данной группе во всех случаях выявлены в зеве (100%), более половины (56%)— в носу и у 1/3 (33%)— в области половых органов. При посеве кала на дисбактериоз они обнаружены только в 10,4% случаев. Не исключено, что отсутствие Candida spp. в культуре при исследовании кала на дисбактериоз связано с нарушением методики забора материала. Из 2 более очагов дрожжеподобные грибы выявлены в 80% случаев, преобладали штаммы C.albicans (92%).
Аналогичная ситуация при МЭ была типична для микробиоценоза носа. В целом по выборке преобладали стафилококки (79,7%), сочетавшиеся с Candida spp. у большинства больных (77,1%). Стафилококки у больных МЭ, ассоциированной с КК и/или КСО и без него, из отделяемого носа высевались практически одинаково часто (77,1% и 84,6%). В то же время в первом случае из отделяемого носа они вырастали в 1,5 раза чаще, чем из отделяемого зева (84,6% против 57,7%). В носу также существенно преобладал S. aureus (86,4%). St.еpidermidis, в отличие от зева, верифицировался только в отделяемом из носа, но в единичных случаях (13,6%). Подтвержден вторично факт антагонизма между стрептококками и Candida spp. Стрептококки из отделяемого носа вырастали только у больных МЭ при отсутствии C.albicans. В отделяемом носа они выявлялись в 1,6 раза реже, чем в отделяемом зева (26,9% против 42,3%). В носу St. hemolyticus (бета-гемолитический) встречался в 1,9 раза чаще (71,4% против 36,4%), чем в зеве. В отличие от зева другая микробная флора у больных МЭ, ассоциированной с КК и/или СО и без него, выявлялась одинаково часто (14,6% и 11,5%). У больных МЭ, ассоциированной с КК и/или КСО, преобладали C.albicans (91,6%). C.tropicalis (4,2%) и C.krusei (4,2%) выявлены у единичных больных.
Клинические манифестации поверхностного кандидоза преобладали на слизистых оболочках. Их осмотр проводился при соответствующем освещении. Большинство больных МЭ имели кандидозный глоссит (85,4%) и тонзиллит (77,1%), 2/3— хейлит (66,7%) и заеды (64,6%), более половины женщин— вульвовагинит (56%), около половины кандидозные паронихии (47,9%) и онихии (41,6%) в пределах 1/5— межпальцевую кандидозную эрозию (20,8%), единичные больные— перианальный кандидоз (6,3%) и мужчины— баланопостит (6,3%). Локализация клинических проявлений КК и/или КСО должна учитываться при назначении специфической топической терапии.
Анамнестически проанализирована роль лекарственных препаратов (системных антибиотиков и кортикостероидов) как возможная причина КК и/или КСО. Опытную группу составили больные МЭ(48 больных или 65%), ассоциированной с КК и/или КСО, контрольную— больные МЭ (26 больных или 35%) без кандидоза. Установлено, что два и более курсов антибиотикотерапии в год получали 85% пациентов опытной группы и только 15%— контрольной. Полученные различия статистически достоверны (р<0,05). Поводом для назначения антибиотиков при МЭ служили традиционные схемы терапии (92%) и санация очагов хронической инфекции (54%), чаще лор-органов (тонзилит, отит, гайморит, ринит). Полученные данные позволяют считать КК и/или КСО инфекционным осложнением антибиотикотерапии при МЭ. Системные кортикостероиды получали только 10% больных опытной и 8% контрольной групп (р>0,05). Для снятия остроты процесса назначали всего 1–2 инъекции Дипроспана или 1–2 процедуры внутривенного капельного введения преднизолона в дозе 30–60мг.Иными словами,системные кортикостероиды не являются причиной возникновения КК и/или КСО при МЭ.
Проведено сопоставление результатов бактериологического исследования с данными иммунологического обследования больных. С этой целью у больных опытной (МЭ+КК и/или КСО) и контрольной (МЭ без КК и КСО) групп проводилось определение в сыворотке крови специфических IgM и IgG к C. albicans. В опытной группе положительные IgM и IgG выявлены у 38% больных, только IgG— у 29%, только IgM— у 14%. Специфические антитела IgM- и IgG-классов отсутствовали у 19% больных даже при обильном росте C. albicans в зеве. В то же время в контрольной группе у 5 (19,2%) больных идентифицированы специфические IgG, а у 1 (3,8%)— IgM. Отрицательные результаты имели место в 84,6% случаев. Полученные данные свидетельствуют, что у 1/5 больных МЭ, ассоциированной с клинически и бактериологически верифицированным КК и/или КСО, отсутствует гуморальный ответ на грибковую колонизацию организма. У 1/4 больных МЭ без КК и/или КСО имеются специфические кандидозные антитела. Иными словами, диагностика КК и/или КСО только по определению специфических антител не всегда свидетельствует о колонизации организма дрожжеподобными грибами рода Candida spp., однако процент совпадения результатов бактериологического и иммунологического обследования достаточно высок.
Для оценки тяжести клинического течения МЭ нами разработан авторский вариант индекса оценки тяжести микробной экземы (ИОТМЭ). В его основу положены 6 клинических проявлений заболевания— эритема, мокнутие, инфильтрация, ипетигинизация, увеличение лимфатических узлов и площадь очагов поражения. ИОТМЭ равнялся сумме баллов, оценивающих каждый из шести клинических проявлений заболевания, и колебался от 3 до 36 баллов. В соответствии с предложенным индексом условно выделены три степени тяжести МЭ: легкая (до 15 баллов), средняя (от 16 до 25) и тяжелая (более 25).
Были представлены варианты клинического течения МЭ, ассоциированной с КК и/или СО. Для заболевания были характерны крупные очаги поражения, значительное мокнутие и ипетигинизация. В процесс нередко вовлекались лимфатические узлы, что возможно связано с синергизмом бактериальной и микотической инфекции. Нередко (23%) наблюдались аллергические высыпания— кандидамикиды, протекающие с симптомами интоксикации (температура, небольшой озноб, головная боль, потливость).
Какова же форма кандидоза у больных микробной экземой? Ответ на этот вопрос был получен при исследовании сыворотки крови всех больных МЭ, ассоциированной с грибами Сandida spp., на наличие антигена-маннана— основного белка клеточной стенки грибов C.albicans. Результат оказался отрицательным во всех случаях.
На рис.4 представлен алгоритм определения вида антимикотической терапии после завершения обследования больного МЭ.
Этиотропное лечение проводилось при наличии поверхностного кандидоза. Существенно, что положительные результаты бактериологического обследования на Candida spp. подтверждались наличием клинических проявлений КК и/или КСО у 89,2% больных, положительным антительным ответом (специфические IgМ и IgG)— у 81,2% и положительными результатами внутрикожного тестирования аллергеном C.аlbicans— у 2/3 пациентов.
Противорецидивную терапию назначали после этиотропной. Ее задача — предотвратить рецидив заболевания и реколонизацию организма грибами Candida spp., пока действует предрасполагающий фактор. Поводами для ее применения были использование системных антибиотиков по различным показаниям, погрешности в диете (чрезмерное употребление углеводов, продуктов с бродильным эффектом), обострение очагов хронической инфекции, различные вирусные и бактериальные инфекции.
Профилактическое лечение проводили с целью предупреждения гиперколонизации организма больного дрожжами рода Candida spp. при действии предрасполагающих факторов. При отсутствии клинических проявлений КК и/или КСО Candida spp. высевали в 10,8% случаев, специфические IgМ и IgG верифицировались в 23% случаев, ГНТ к C.albicans имела место у 57,7% больных, ГЗТ— у 61,6%. Таким образом антимикотическая терапия с профилактической целью показана и больным МЭ при отрицательных результатах обследования на дрожжи.
Тактика ведения больных МЭ (рис.5) заключалась в назначении общей и местной терапии при ведущей роли топических антимикотических и антибактериальных препаратов. Общая терапия включала применение антигистаминных препаратов (Супрастин, Парлазин, Тавегил) в течение 2–3 недель, пробиотиков в зависимости от выявленных нарушений микробиоценоза кишечника (Бифидумбактерин, Колибактерин, Лактобактерин) до месяца. Антибиотики (Флемоксина Солютаб, Флемоклава Солютаб) назначали при тяжелом течении заболевания в течение 7–10 дней. Провоцирующими факторами являлись нарушения общего состояния (температура, озноб, недомогание), обнаружение избыточного роста патогенной флоры в кишечнике (Clostridium perfringens, Proteus spp., Bacteroides spp., Staphylococcus aureus, Pseudomonas aeruginosa и др.), обострение имеющихся очагов хронической инфекции, наличие лимфаденопатии.
Оценка эффективности терапии МЭ проводилась с использованием следующих клинических критериев: выздоровление, значительное улучшение, улучшение, без эффекта. Под выздоровлением понимали полное разрешение очагов МЭ. На месте высыпаний могли оставаться гипо- (реже) и гиперпигментированные пятна. Значительным улучшением считали стойкую положительную динамику процесса, характеризующуюся уменьшением ИОТМЭ в 4 раза. Под улучшением понимали медленную, но положительную динамику процесса, характеризующуюся уменьшением ИОТМЭ в 2 раза. Фиксировались переносимость лечения и медикаментозные осложнения.
Существенным условием профилактики обострений и рецидивов МЭ, ассоциированной с КК и/или КСО, было соблюдение ряда условий. Ограничение в пищевом рационе углеводов и продуктов, содержащих продукты брожения, 1–2-кратный прием Пимафуцина внутрь до и после застолья, связанного с обильным употреблением углеводов. При острой инфекции или обострении очагов хронической инфекции в носоглотке— топическое применение Бетадина. При использовании антибиотиков по любым показаниям 5–7-дневный курс описанной выше терапии.
Кандидозная сенсибилизация организма может развиваться не только при инфекционном процессе, но и при кандидоносительстве различной локализации, а также при попадании метаболитов клеток гриба через дыхательные пути. Рост числа Candida spp. у 1/3 здоровых лиц в посеве из ротовой полости косвенно нашел отражение в наших исследованиях в виде положительных результатов ГНТ у 1/3 здоровых лиц контрольной группы. В то же время нельзя не учитывать и тот факт, что даже при выделении в кале различных грибов рода Candida серологические тесты на специфические антитела были в пределах нормы.
Отсутствие Candida spp. при обследовании только кала на дисбактериоз не должно ограничивать клиническое мышление в плане отсутствия кандидозной гиперколонизации. Отмечено, что слизистая оболочка кишечника поражается дрожжевыми грибами рода Candida spp. только после ее повреждения другими патогенами, например вирусами или бактериями. Механизм патогенного действия грибов рода Candida на организм человека разнопланов— интоксикация, иммунопатология и сенсибилизации.
Наличие у больных МЭ поверхностного КК и/или КСО с большой долей вероятности указывает на целесообразность назначения топических, а не системных антимикотиков. Обоснован выбор препаратов, обладающих одновременно антимикотическим и антибактериальным действием. Таковыми являются Залаин, Бетадин и Пимафукорт. В то же время нельзя допускать развитие у больного другой симптоматики, известной как микофибия.
Заключение
Резюмируя вышеизложенный материал, можно заключить, что МЭ достаточно часто (2/3 случаев) осложняется поверхностным кандидозом кожи и слизистых оболочек, который можно считать инфекционным осложнением антибиотикотерапии. Грибы рода Candida достаточно часто верифицируются в носоглотке. Специфические IgM и IgG к антигену С.аlbicans выявляются в 81% при положительном результате бакпосева на дрожжеподобные грибы и лишь в 15,8% случаев— при отрицательном. Сопутствующий кандидоз значительно ухудшает течение МЭ. Исследование сыворотки крови всех больных МЭ, ассоциированной с грибами Сandida spp., на наличие антигена-маннана во всех случаях было отрицательным, что свидетельствует о наличии неивазивного (поверхностного) кандидоза и определяет тактику лечения. Опыт применения только топической антимикотической терапии, санирующей очаги хронической инфекции в носоглотке, кишечнике, половых органах, показал высокий терапевтический эффект при отсутствии медикаментозных осложнений.
Для цитирования: Бурова С.А. Системный и локализованный кандидоз у больных сахарным диабетом. РМЖ. 2003;17:969.
Национальная академия микологии, Центр глубоких микозов, ГКБ № 81, Москва
О собенности обменных процессов в организме больного сахарным диабетом (СД) требуют индивидуального подхода к лечению инфекционных и неинфекционных заболеваний у этих пациентов. Общей чертой разнообразных состояний при СД является гипергликемия, возникающая вследствие либо нарушения способности поджелудочной железы вырабатывать необходимое количество инсулина, либо изменения чувствительности периферических тканей к инсулину, либо сочетания того и другого.
По типу выделяют: СД 1 типа и СД 2 типа; по тяжести течения: легкой, средней и тяжелой степени.
У больных СД отмечаются гормональный дисбаланс, гиперкалиемия, нарушение липидного обмена, ожирение, снижение функции гранулоцитов, гликолиз различных белков, тканевая гипоксия, расстройство системы гемостаза, иммунные нарушения (в том числе аутоиммунные процессы), а также макрососудистые и микрососудистые осложнения, такие, как атеросклероз, ишемическая болезнь сердца, артериальная гипертония, гангрена нижних конечностей и др. [2,3].
В связи с этими факторами СД нередко осложняется присоединением различных инфекций, которые имеют свои особенности. Наиболее часто у этих пациентов поражаются мочевыводящие пути, при этом в моче выделяют грамотрицательные бактерии, стафилококки, энтерококки и, наконец, грибы, которые в структуре возбудителей у больных СД составляют, по нашим данным, 32,5%. Это объясняется также и тем, что в условиях гиперкалиемии грибы активно используют глюкозу для своих метаболических процессов и усиленно размножаются, вызывая болезнь. В большинстве случаев возбудителем являются дрожжеподобные грибы Candida аlbicans.
Клинические формы грибкового поражения мочевыводящих путей у больных СД от бессимптомной кандидурии до кандидозных уретрита, цистита, пиелонефрита, простатита, эпидидимита и баланопостита, проявляются различными по степени дизурическими явлениями, болями в поясничной и области мочевого пузыря, положительным симптомом Пастернацкого, жжением в уретре, раздражением и покраснением головки полового члена, синдромом нейрогенного мочевого пузыря, недержанием мочи и др.
Кандидозный бронхит и пневмония часто осложняют течение СД. Они приобретают, как правило, хроническое рецидивирующее течение, трудно поддаются излечению и характеризуются одышкой, продуктивным кашлем, болями в грудной клетке, изменением на рентгенограмме и др. симптомами [1].
Кандидозные эзофагит, синусит, ангина встречаются редко. Кандидозные и криптококковые перитонит, остеомиелит, сепсис и менингит при СД описаны в литературе недостаточно, но следует помнить об этих осложнениях у больных СД, особенно в отделениях реанимации и палатах интенсивной терапии [4,5,6].
Известно также, что при СД нарушение микроциркуляции в сосудах нижних конечностей наблюдается в 20 раз чаще, чем у лиц без эндокринной патологии. Это способствует развитию синдрома диабетической стопы, трофических язв, присоединению кандидозной инфекции [3].
В 81–й Городской клинической больнице за последние 3 года в стационаре и амбулаторно наблюдали 76 больных с системными и локализованными микозами на фоне СД, верифицированными по данным микробиологических исследований (табл. 1). Из них 27 мужчин и 49 женщин.
Кандидозный (к) стоматит выявлен у 5 больных, к. глоссит – у 4, к. фарингит – у 5, к. эзофагит – у 3, к. бронхит – у 4, к. бронхопневмония – у 2, к. пневмония – у 1, к. цистит – у 19, к. уретрит – у 11, к. острый вульвовагинит – у 18, к. баланопостит – у 2. У всех больных диагноз микоза был впервые установлен в нашей клинике.
Лечение было комплексным: соблюдение строгой диеты, применение сахароснижающих препаратов, лечение сопутствующих заболеваний, прием общеукрепляющих средств, физиотерапевтических процедур, и наконец, проведение противогрибковой этиотропной терапии.
Лечение кандидозной инфекции у больных СД имеет некоторые особенности:
- при нарушении обменных процессов, осложнениях СД и наличии многочисленных сопутствующих заболеваний у большинства больных, особенно у лиц пожилого возраста, предпочтителен толерантный противогрибковый препарат, высокоэффективный и без токсических побочных действий;
- при длительном хроническом течении заболевания и, как правило, вялотекущем процессе, требуется применять продолжительную схему лечения в адекватных разовых и курсовых дозах;
- после проведения основного курса лечения больной должен оставаться на диспансерном учете, при этом не исключаются профилактические курсы лечения системными и местными антимикотиками.
В многочисленных научных исследованиях и в практике доказано, что для лечения микозов у описанной категории больных, как впрочем, и для всех больных кандидозом, оптимальным является системный противогрибковый препарат, современный триазол – флуконазол [1,7,8].
Есть исследования, доказывающие, что именно у больных СД флуконазол резко уменьшает продукцию фосфолипазы грибами Candida albicans, тем самым уменьшая адгезивную способность этих инфектантов [9].
Приводим схемы лечения кандидоза на фоне СД системным антимикотиком флуконазолом (Медофлюконом) (табл. 2).
Применяли различный режим приема Медофлюкона в капсулах по 200 мг – 1 раз в день, 2 раза в день или через день.
Эффективность лечения определяли по исчезновению клинических симптомов болезни, рентгенологической и эндоскопической динамике и эрадикации возбудителя (табл. 3).
Таким образом, течение системных и локализованных микозов у больных СД имеет определенные особенности, что требует комплексной терапии и эффективного, нетоксичного антимикотика, более длительных курсов лечения и последующего диспансерного наблюдения. Применение Медофлюкона, как этиотропного противогрибкового средства, показало высокую эффективность: выздоровление в 67,1% случаев, улучшение в 30,3% случаев. Низкий процент побочных действий, даже у больных СД, еще раз подтвердил превосходство флуконазола (Медофлюкона) перед другими препаратами при лечении кандидоза.
1. Бурова С.А. Проблемы грибковых заболеваний человека. // Российский журнал кожных и венерологических болезней –1998–№1–с.39–41.
2. Бурова С.А., Талалаева С.М. Отдаленные результаты лечения онихомикозов у больных сахарным диабетом. // Российский журнал кожных и венерических болезней. – 2000 – №5. – с.31–33.
3. Руководство по клинической эндокринологии. /Под ред. В.Г.Баранова. – Л., 1977.
5. Magee L.T. et al. Pyrolesis typing of isolates from a recurrence of systemic cryptococcosis.// J.Med. Microbiol. – 1994 – №40(3).–p.165–169.
6. Morris B.A. et al. Cryptococcal peritonitis in CAPD patient. // J. Med. Vet. Mycal. –1992–№30(4)–p.309–315.
7. Penk A., Pittrow L. Therapeutic experience with fluconazole in the treatment of fungal infections in diabetic patients.// Mycoses. –1999–№42 Suppl.2–p.97–100.
8. Sobel J.D., et al. Candiduria a randomized d.–b. study of treatment with fluconazole and placebo.// Clin. Infect. Dis. –2000 –№30.–p.19–24.
9. Willis A.M., et al. The influence of antifungal drugs on virulence properties of Candida alb. in patient with diabetes mellitus.// Oral Surg. Med. –2001–№91(3).–p.317–321.
Ежедневно к врачу дерматовенерологу обращается большое количество людей с изменениями ногтевых пластинок. Врач делит заболевания на 2 группы: грибкового и негрибкового характера. Здоровая ногтевая пластинка розового цвета с гладкой поверхностью с природным блеском. Любые изменения ногтевых пластинок-повод обратиться к врачу за консультацией и постановкой правильного диагноза. Зачастую, люди пытаются самостоятельно поставить себе диагноз и назначают самостоятельно лечение, что может привести к ухудшению состояния. Только врач, обладая необходимыми знаниями и опытом, используя дополнительные методы диагностики, может поставить правильный диагноз с назначением эффективного лечения.
Что относится к заболеваниям негрибкового характера:
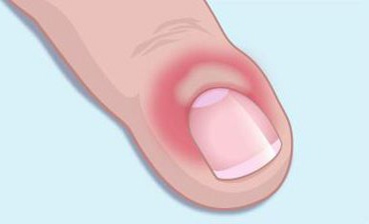
I.Инфекционные заболевания — паронихия (воспаление околоногтевого валика по причине присоединения инфекции)
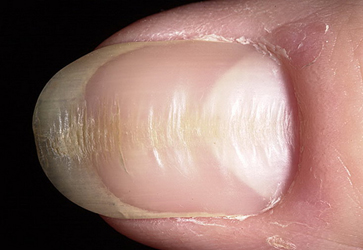
II. Неинфекционные – — дистрофия ногтей (ногти становятся плоскими или вогнутыми, появляются бороздки на поверхности. Чаще причина — эндокринные заболевания и несбалансированное питание.
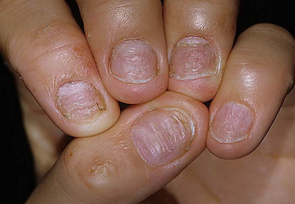
III. Другие- изменения ногтевых пластинок при недостаточности щитовидной железы (тонкость, ломкость, расcлоенность, ногти в виде ‘барабанных палочек’ при заболеваниях легких, cердечно — сосудистых изменениях, ВИЧ- инфекции, изменения ногтей при кожных заболеваниях таких как псориаз, красный плоский лишай.
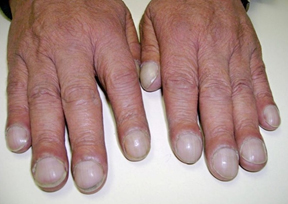
— онихолизис (отделение ногтевой пластинки от мягких тканей пальца)
— онихокриптоз (вросший ноготь) вследствие травмы, ношения тесной обуви, наследственности, неправильной обработки ногтей.
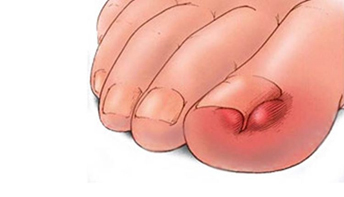
— онихошизм (поперечное расслоение ногтя) Ногтевая пластинка истончается и разделяется на несколько слоев. Причинами могут быть неправильное питание, травма, недостаток железа, и кальция в крови, сахарный диабет, использование некачественных лаков.
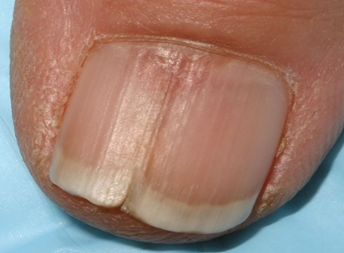
— меланонихия – почернения ногтя или образование полосы бурого цвета вследствие травмы, кровоизлияния в окружающие ткани.

Остановимся на таком серьезном изменении как меланонихия. Она заслуживает серьезного отношения , вследствие того, что является признаком такого серьезного заболевания как меланома ногтевой пластинки. Учитывая, что достаточно долгое время никаких серьезных признаков кроме как появление темных полос не вызывает, люди обращаются достаточно поздно.
Меланонихия начинается с появления бурых пятен или полос от коричневого до черного цвета. К меланонихии может привести:
- хроническая травматизация ногтя (например обувью, чаще 1,5 пальцы)
- поражение ногтей грибковой инфекцией ( некоторые виды грибов дают темный окрас)
- прием некоторых медикаментов, таких как линкомицин, химиотерапевтические препараты, противомалярийные.
- редко, но при такой патологии как амилоидоз, псориаз, ограниченная склеродермия.
- бактериальные инфекции
- Геморрагия в ногтевом ложе. Отличительной особенностью от меланомы является то, что гематома не достигает свободного края. НО! Наличие крови под ногтем не исключает злокачественности.
Лишь врач может провести дифференциальную диагностику с установкой правильного диагноза.
Следует не забывать, что существует ряд факторов, указывающих на наличие подногтевой меланомы:
- локализация на большом пальце руки или ноги
- локализация на одном краю
- возраст старше 60 лет, но не всегда
- внезапное появление на ранее нормальной ногтевой пластинке и быстро распространяющееся потемнение с нечеткими краями
- потемнение без предшествующей травмы
- появление без предшествующей травмы
- появление у людей с диспластическими невусами в анамнезе или семейном анамнезе
При любых изменениях ногтей следует немедленно обращаться к врачу.
10% меланом характеризуются нетипичной локализацией — на коже ладоней, подошв, коже пальцев и ногтевого ложа. Данный вид меланом называется акральная лентиго-меланома. Данный вид меланом опасен тем, что развивается медленно, и ее обнаруживают достаточно поздно.
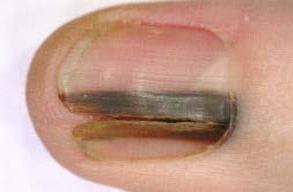
Чаще всего страдают люди более возрастной группы, но, в последнее время, наблюдается и у более молодой возрастной группы.
Инсоляция является одним из провоцирующих факторов возникновения, не менее важным является механическая травма.
Излюбленным местом патологии ногтевых пластинок являются ногти 1 и 5 пальцев, так как данные пальцы чаще других подвергаются травме. Первый признак данного вида меланом – это появление полоски или пятна от коричневого до черного цвета, начиная от ногтевого валика до свободного края ногтя, также пигментация на околоногтевом валике. В дальнейшем происходит утолщение ногтевой пластинки с последующим разрушением и изъязвлением ногтевого ложа.
На коже ладоней и подошв акральную лентиго-меланому часто расценивают как бородавку, костную мозоль, cтержневую мозоль. На ногтевой пластинке расценивают как грибковое поражение, подногтевую гематому, невус, вросший ноготь, кератоакантому. Поэтому людям с уже имеющимися родинками на стопах и ладонях следует бережно к ним относится и проходить ежегодный осмотр, а людям с вновь образованными родинками своевременно обращаться к врачу.
Читайте также:

