Кишечная инфекция при инсульте
Обновлено: 15.04.2024
Сосудистые заболевания головного мозга и кишечные инфекции. ОНМК и кишечные инфекции
Иногда приходится дифференцировать острые кишечные инфекции от некоторых сосудистых заболеваний головного мозга — субарахноидального кровоизлияния, ОНМК или ПНМК в вертебробазилярной области. В литературе имеются указания на сложность диагностики в этих ситуациях.
Нами наблюдались больные, направленные в инфекционную больницу с диагнозом пищевой токсикоинфекции, у 12 из которых было диагностировано субарахноидальное кровоизлияние, у 15 — ОНМК и у 12 — ПНМК. К группе сосудистых заболеваний головного мозга надо отнести и кризовое течение гипертонической болезни (ГБ). Нами наблюдались 106 больных с гипертоническими кризами (ГК), в том числе 89 — с ГК 1-го типа и 17 — с ГК 2-го типа.
При люмбальной пункции у всех пациентов была выявлена кровь в цереброспинальной жидкости, диагностировано субарахноидальное кровоизлияние. Эти больные были переведены в нейрохирургический стационар.
OHMК в вертебробазилярном бассейне было выявлено у 15, ПНМК —у 12 больных. Возраст наблюдаемых пациентов (5 мужчин и 22 женщины) колебался от 40 до 75 лет. Больные чаще всего поступали на 2—4-й день болезни в тяжелом состоянии. Начало заболевания у 22 больных было острым, у 5 — постепенным. При ОНМК в вертебробазилярном бассейне отмечались головная боль, тошнота и повторная рвота, слабость, нарушение зрения, дыхания и сердечной деятельности, нередко — артериальная гипотензия. Диарея беспокоила 3 больных, стул был не более 5 раз в сутки.
Диагноз острой кишечной инфекции не подтвердился, результаты бактериологических исследований кала были отрицательными.
При ПНМК в вертебробазилярной области отмечались головная боль, тошнота, повторная рвота, ощущение слабости и недостатка воздуха, вазомоторные реакции, нарушения конвергенции и кратковременные расстройства сознания. Все указанные проявления болезни прошли в течение 1 сут. Диарея продолжительностью 2 сут беспокоила лишь 2 больных (стул был не более 5 раз в сутки). Бактериологические исследования кала у этих пациентов были отрицательными.
К группе ПНМК многие исследователи относят гипертонические кризы ГК. Нами наблюдались 106 пациенток, направленных в стационар с диагнозом пищевой токсикоинфекции, у которых был также ГК (в возрасте 40—50 лет — 8, 51 год — 60 лет — 20, 61 год — 70 лет — 48, свыше 70 лет — 30). Во всех случаях регистрировалось острое начало болезни. Основные симптомы: головная боль (у 106 больных, из них у 39 — разлитая, у 67 — локализованная в затылочной или заднешейной области), тошнота (у 105 больных), рвота (у 104 больных, из них у 21 — однократная, у 83 — многократная), диарея (у 18 больных) — не более 5 раз в сутки.
У подавляющего большинства кал имел консистенцию жидкой каши; боль в области живота (у 5), озноб (у 92 больных), повышение температуры тела до 37,5 °С (у 24), головокружения (у 93 — в 88 случаях Усиливались при перемене положения головы), нарушения координационных проб (у 33), статическая атаксия (у 33), шум в ушах (у 14), нистагм (преимущественно горизонтальный) — у 15 больных. На боль в области сердца сжимающего характера жаловались 5 пациентов, у 35 систолическое АД было выше 200 мм рт.ст., у 19 больных пульсовое АД превышало 100 мм рт.ст., у 21 было менее 60 мм рт.ст. ГК 1-го типа был диагностирован у 69 больных (65,1 %) и 2-го типа — у 32 (30,2 %). У 5 пациентов (4,7 %) отмечался гипертонический кардиальный криз, что подтверждалось динамикой клинической картины болезни и изменениями на ЭКГ.
Бактериологические исследования кала во всех случаях были отрицательными. Успешное проведение дифференциальной диагностики между сосудистыми заболеваниями головного мозга и пищевыми токсикоинфекциями позволяет провести в указанных жизнеопасных состояниях своевременную рациональную терапию. Надо иметь в виду, что пищевые токсикоинфекции могут быть фактором риска возникновения ГК при гипертонической болезни.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Инфаркт кишечника – это некроз кишечной стенки, связанный с острым прекращением кровотока по мезентериальным сосудам вследствие их эмболии или тромбоза. Характерным признаком является интенсивная боль в животе при полном отсутствии каких-либо объективных данных во время обследования пациента (живот мягкий, малоболезненный). Для уточнения диагноза проводится УЗИ и обзорная рентгенография ОБП, дуплексное сканирование и ангиография мезентериальных сосудов, лапароскопия. Консервативная терапия неокклюзионных форм патологии возможна только в первые часы заболевания, поздние стадии и остальные формы требуют хирургического лечения.

Общие сведения
Инфаркт кишечника – острое нарушение мезентериального кровообращения с последующим некрозом кишки и развитием перитонита. Данная патология является одной из серьезных проблем абдоминальной хирургии. Чаще всего эмболия, тромбоз, атеросклероз и неокклюзионная ишемия сосудов кишечника возникают на фоне тяжелой патологии сердца. В связи с увеличением процента пожилого населения и омоложением сердечно-сосудистой патологии инфаркт кишечника встречается все чаще (0,63% сравнительно с единичными случаями в конце прошлого века). Средний возраст пациентов – 70 лет, преобладают женщины (более 60%). Учитывая солидный возраст больных и массу фоновых заболеваний, решить вопрос о хирургической тактике лечения бывает достаточно сложно.
Еще одной проблемой является то, что поставить диагноз достаточно сложно, а подтвердить его без проведения ангиографии до операции практически невозможно. Вследствие ошибочной диагностики затягивается предоперационная подготовка; за это время происходят необратимые изменения в кишке, приводящие к смерти пациента. Ситуация усугубляется тем, что в последние годы инфаркт кишечника значительно омолодился (каждый десятый пациент моложе 30 лет), а радикальная резекция кишечника в поздней стадии заболевания приводит стойкой инвалидизации.

Причины
Все причинные факторы, приводящие к инфаркту кишечника, можно разделить на три группы: тромботические, эмболические и неокклюзионные. Тромботический вариант патологии характеризуется тромбозом мезентериальных артерий (реже вен) в их проксимальных отделах. Чаще всего тромб локализуется в устье верхней брыжеечной артерии. К тромбозу висцеральных ветвей аорты может приводить повышенная свертываемость крови, полицитемия, сердечная недостаточность, панкреатит, травмы, опухоли, прием гормональных контрацептивов.
Эмболический вариант заболевания развивается при закупорке брыжеечных сосудов тромбоэмболами, мигрировавшими из проксимальных отделов сосудистого русла. Причиной этого чаще всего служат мерцательная аритмия, формирование пристеночных тромбов на фоне инфаркта миокарда, аневризмы аорты, выраженные нарушения коагуляции. После обтурации сосуда эмбол может смещаться в дистальные отделы и ветви сосуда, вызывая прерывистую, мигрирующую ишемию.
Неокклюзионный вид инфаркта кишки связан не с обтурацией висцеральных сосудов, а со снижением притока крови по ним. Причинами ограничения висцерального кровотока могут быть мезентериальный тромбоз, снижение фракции сердечного выброса, выраженная аритмия, спазм сосудов брыжейки, гиповолемия при шоке, сепсисе, обезвоживании. Факторы из перечисленных трех групп нередко комбинируются.
Классификация
Заболевание может протекать с компенсацией, субкомпенсацией и декомпенсацией кровотока. Кроме того, выделяют три последовательные стадии инфаркта кишечника: ишемии, инфаркта и перитонита. В первой стадии изменения в кишечнике еще обратимы, а клинические проявления в основном связаны с рефлекторными реакциями организма.
В инфарктной стадии происходит некроз кишечника, деструктивные изменения продолжаются даже после восстановления кровотока. Защитные свойства кишечной стенки постепенно ослабевают, бактерии начинают проникать сквозь все ее слои в брюшную полость. В стадии перитонита происходит распад тканей кишечной стенки, геморрагическое пропотевание с развитием тяжелейшего воспаления брюшины.
Симптомы инфаркта кишечника
Первая стадия патологии (ишемическая) обычно длится не более шести часов. В этот период пациента беспокоят сильные боли в животе, вначале схваткообразные, затем постоянные. Локализация боли зависит от того, какой отдел кишечника поражен: при ишемии тонкой кишки беспокоит боль в околопупочной области, восходящей и слепой кишки – в правой половине живота, поперечно-ободочной и нисходящей – в левой половине.
Боль очень сильная, однако не соответствует полученным при осмотре пациента объективным данным. При пальпации живот мягкий, малоболезненный. Для данного заболевания характерно острое появление болевого синдрома, однако возможно и постепенное, иногда двухэтапное начало заболевания. Кроме болей в животе, больной может жаловаться на тошноту, рвоту, диарею. Аускультация живота в начальной стадии выявляет повышенную перистальтику, которая постепенно ослабевает в течение нескольких часов.
В стадиях инфаркта и перитонита состояние больного прогрессивно ухудшается. Кожные покровы бледные, сухие. Боль постепенно ослабевает, а при полном некрозе стенки кишечника полностью исчезает, что является плохим прогностическим признаком. Язык сухой, с налетом. Живот вздутый, но поскольку для патологии характерно позднее появление симптомов раздражения брюшины, живот долгое время остается мягким.
Патогномоничен симптом Кадьяна-Мондора: при пальпации в брюшной полости определяется цилиндрическое плотно-эластичное образование, малосмещаемое и болезненное - отекший участок кишки и брыжейки. При аускультации брюшной полости участки тимпанита (звонкого звука над перераздутыми петлями кишечника) чередуются с участками притупления звука (над некротизированными петлями). Выпот в брюшной полости (асцит) может формироваться уже через несколько часов от начала заболевания.
Если заболевание прогрессирует, явления интоксикации и обезвоживания нарастают, больной становится безучастным, апатичным. Даже если начать оказание помощи пациенту на этой стадии, состояние может прогрессивно ухудшаться, наступает кома, начинаются судороги. На заключительном этапе болезни смертность достигает практически 100%.
Диагностика
Низкая информированность врачей догоспитального этапа об инфаркте кишечника значительно затрудняет своевременную диагностику. Позднему выявлению данной патологии способствует недостаточная оснащенность стационаров диагностическим оборудованием (ангиограф, компьютерный томограф). Однако заподозрить инфаркт кишечника можно и с помощью другим методов исследования. На УЗИ органов брюшной полости выявляется утолщенная стенка кишечника, наличие свободной жидкости в брюшной полости. Дуплексное цветное ультразвуковое сканирование является единственным достоверным УЗ-методом диагностики тромбоза мезентериальных сосудов.
Обзорная рентгенография органов брюшной полости информативна на более поздних стадиях, когда становятся видны чаши Клойбера, кишечные арки. Проведение контрастной рентгенографии не рекомендуется, так как она не предоставляет каких-либо ценных для постановки диагноза данных, но значительно затягивает этап диагностики. МСКТ органов брюшной полости позволяет провести более точное исследование петель кишечника (дает возможность обнаружить газ в брыжейке и стенке кишки), а МРТ мезентериальных сосудов – оценить состояние сосудистого русла, обнаружить тромбы и эмболы.
Наиболее точным методом исследования является ангиография мезентериальных сосудов. Данное исследование рекомендуют проводить в двух проекциях – прямой и боковой. Такая методика позволяет вычислить точную локализацию патологического процесса, выявить пораженные ветви висцеральных сосудов, определить тактику и объем оперативного вмешательства. Помогает в диагностике и определении лечебной тактики и консультация врача-эндоскописта.
Диагностическая лапароскопия дает возможность визуально оценить состояние петель кишечника, выявить некоторые патогномоничные для инфаркта кишечника признаки. К ним относят изменение цвета кишечной стенки, отсутствие пульсации краевых сосудов, изменение сосудистого рисунка (продольный вместо поперечного). Выявление данных признаков позволяет выставить показания к ургентной операции даже при невозможности проведения ангиографии. Противопоказаниями к лапароскопии являются выраженное вздутие кишечника, наличие обширных лапаротомий в анамнезе, крайне тяжелое состояние пациента.
Специфических лабораторных признаков патологии, особенно в начальных стадиях заболевания, не существует. В общем анализе крови по мере развития заболевания нарастает лейкоцитоз, сдвиг лейкоформулы влево. Анализ кала на скрытую кровь также становится положительным на стадии некроза кишечника. Некоторые авторы указывают на повышение уровня лактата в крови как на специфичный признак инфаркта кишечника.
Лечение инфаркта кишечника
Цель лечения – устранение всех патогенетических звеньев заболевания. Один из основополагающих принципов терапии тромбоза мезентериальных сосудов – раннее начало фибринолиза. Однако начало патогенетического лечения на догоспитальном этапе возможно только теоретически, потому что этот диагноз практически никогда не ставится до госпитализации пациента и обследования с участием абдоминального хирурга.
Сразу после госпитализации начинают коррекцию патологии, которая привела к развитию инфаркта кишечника, одновременно с инфузионной терапией. Инфузия кристаллоидных и коллоидных растворов призвана возместить недостающий объем циркулирующей крови, восстановить перфузию ишемизированных участков кишки. Начиная кардиотропную терапию, следует отказаться от использования вазопрессоров, так как они вызывают спазм сосудов брыжейки и усугубляют ишемию. При неокклюзионной ишемии показано введение спазмолитиков для улучшения висцерального кровотока.
Консервативная терапия оправдана только при отсутствии у пациента признаков перитонита. Наибольшая эффективность достигается при терапии, начатой в первые два-три часа от появления симптоматики. Чем дольше будет длиться этап консервативного лечения, тем меньше шансов на благоприятный исход, поэтому этап нехирургической терапии должен быть максимально кратким. При отсутствии быстрого эффекта проводится ургентная операция. То же касается и предоперационной подготовки – чем она короче, тем выше шансы на выздоровление.
Радикальными считаются лишь оперативные вмешательства на сосудистом русле (при наличии показаний - в сочетании с резекцией кишечника). Изолированная резекция некротизированной кишечной петли без удаления тромба из сосуда не устраняет основной патогенетический механизм возникновения инфаркта кишечника, а значит – не приводит к улучшению состояния пациента. Если оперативное вмешательство произведено в сроки более 24 часов от начала заболевания, лапаротомия в 95% случаев лишь констатирует необратимые изменения в большей части кишечника. Радикальная резекция пораженной кишки в такой ситуации не предотвращает смерти больного.
Если была произведена обширная резекция кишечника, в послеоперационном периоде пациенту может потребоваться консультация гастроэнтеролога для определения тактики энтерального и парентерального питания. Иногда такие пациенты требуют пожизненного частичного или полного парентерального питания с помощью внутривенного введения углеводов, белковых и жировых фракций.
Прогноз и профилактика
Прогноз неблагоприятный, так как заболевание редко своевременно диагностируется, а на поздних стадиях оперативное лечение часто бывает неэффективным. Несмотря на усовершенствование диагностических и лечебных мероприятий, смертность при различных формах патологии достигает 50-100%. Профилактика инфаркта кишечника заключается в своевременном лечении приводящих к нему заболеваний (аортальные и митральные пороки сердца, аритмии, атеросклероз, тромбофилии).
Инсульт — это острое нарушение мозгового кровообращения, которое без неотложной медицинской помощи приводит к смерти. Догадаться о начале приступа можно по первым признакам, которые мы рассмотрим в статье.

Что происходит при инсульте?
Инсульт бывает двух видов:
- геморрагическим — вызван разрывом мозговой артерии;
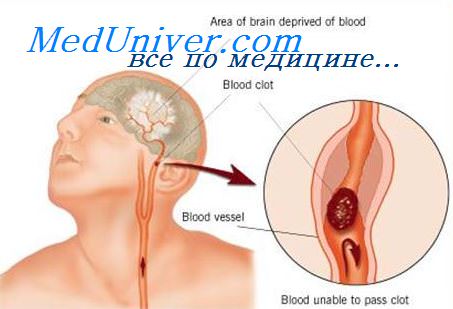
- ишемическим — прекращение или ухудшение мозгового кровообращения вследствие сужения артерии или ее закупорки тромбом.
Независимо от вида заболевания, происходит гибель клеток мозга, что приводит к тяжелым последствиям.
Ишемический инсульт развивается постепенно, чаще возникает рано утром или поздней ночью. Геморрагический наоборот характеризуется молниеносным течением, его симптомы возникают в период бодрствования, например, на фоне физического или психологического перенапряжения.
Клиническая картина зависит от степени нарушения мозгового кровообращения, от локализации кровоизлияния (в желудочки, в таламус или другие участки), от выраженности отека мозга.
Перед началом приступа появляются первые признак нарушения кровообращения головного мозга. К ним относится головная боль, головокружение, слабость, тошнота и рвота. Однако есть более специфические симптомы:
- Если попросить человека улыбнуться, он не сможет этого сделать. Уголок рта опущен вниз.
- Больной не может показать язык, он падает на одну сторону, поскольку отсутствует мышечный тонус.
- Возникает слабость с одной стороны тела. Пациент не может одновременно поднять обе руки.
- Нарушается дикция, речь становится заторможенной. Человек не в состоянии повторить простую фразу и даже разборчиво произнести свое имя.
При появлении таких признаков нужно немедленно вызывать скорую помощь.
Примечание! При инсульте важно, как можно быстрее восстановить кровообращение и нормальное питание нейронов. Чем раньше остановить гибель мозговых клеток, тем ниже риски возникновения тяжелых последствий и выше шансы на успешную реабилитацию.
Как оказать первую помощь?
Если вы заметили предвестники инсульта у человека, который находится рядом, нужно оказать ему первую помощь:
- Вызвать скорую помощь.
- Не паниковать. Уложить человека на горизонтальную поверхность, на спину или набок, можно слегка приподнять голову и верхнюю часть туловища.
- До приезда медиков обеспечить больному полный покой, как физический, так и психоэмоциональный, а также приток свежего воздуха.
- Контролировать состояние человека, следить за его пульсом и дыханием. В случае отсутствия сердцебиения делать непрямой массаж сердца, дыхания — искусственное дыхание.
Если есть возможность быстрее доставить пострадавшего в больницу, чем приедет бригада скорой помощи, то нужно ею воспользоваться.
Медики оценивают сердечную и дыхательную деятельность, оказывают первичную неотложную медицинскую помощь. После поступления в больницу пациента госпитализируют в нейрореанимационное отделение.
Медикаментозную терапию выбирают в зависимости от вида инсульта, тяжести состояния пациента. В острой фазе важно восстановить мозговое кровообращение, нормализовать артериальное давление, работу сердца и функцию дыхания.
В случае обширных гематом, нарастающем отеке мозга, отсутствии эффекта от консервативной терапии проводят хирургическое вмешательство.
Признаки ишемического инсульта
У мужчин и женщин симптомы нарушения мозгового кровообращения по ишемическому типу схожие. К ним относится:
- внезапная сильная головная боль, которая может возникнуть как после какой-либо деятельности, так и в состоянии покоя;
- головокружение;
- нарушение координации движения, удержания равновесия;
- ухудшение зрения: размытость картинки, сужение зрительных полей, косоглазие;
- оглушенность;
- мышечная слабость, как правило, односторонняя;
- снижение чувствительности в теле, конечностях;
- тошнота, рвота;
- потеря способности говорить, воспроизводить услышанную информацию;
- спутанность или потеря сознания.
Вышеперечисленные признаки могут плавно нарастать. Патологические нарушения зависят от того, какая часть мозга поражена.
Признаки геморрагического инсульта
Острое нарушение мозгового кровообращения по геморрагическому типу всегда начинается внезапно, сопровождается такими признаками:
- резкая сильная головная боль, которую можно сравнить с ударом кинжала;
- тошнота, рвота;
- покраснение лица;
- нарушение дыхания;
- непроизвольные движения глазами;
- судороги;
- потеря сознания.
Чем опасен инсульт?
При возникновении приступа нарушения мозгового кровообращения каждая минута на счету. От скорости предоставленной медицинской помощи зависит жизнь и работоспособность человека.
- нарушение движения: паралич или парез;
- психические расстройства: депрессия, тревожность, агрессия;
- речевые нарушения;
- ухудшение или провалы в памяти;
- нарушение координации движений;
- расстройства чувствительности некоторых участков тела;
- потеря или ухудшение слуха, зрения.
В первый месяц после перенесенного инсульта до 25% пациентов умирает от его последствий. Причиной смерти чаще становится отек мозга, инфаркт миокарда, эмболия легочной артерии, сепсис, почечная недостаточность. Около 50% пациентов, перенесших инсульт, имеют неврологические нарушения, которые приводят к инвалидности.
Реабилитация после инсульта
Больше всего шансов на полное восстановление после инсульта у пациентов, которые к концу первого месяца реабилитации имеют минимальные неврологические расстройства. Устранить последствия острого нарушения мозгового кровообращения можно только общими стараниями реабилитологов и больного.
Реабилитационные мероприятия разрабатываются командой профильных специалистов. К методам реабилитации относится:
- массаж конечностей, языка;
- лечебная физкультура для восстановления двигательной активности;
- специальные упражнения для развития мелкой моторики, разработки лицевых мышц;
- восстановление тазовых функций, дыхания, бытовых навыков;
- физиотерапевтические процедуры, в том числе водные;
- психологическая поддержка;
- устранение когнитивных нарушений;
- работа с логопедом.
Период восстановления может длиться до 3 лет, значительные улучшения можно наблюдать уже в течение первых трех месяцев. Необходимо выполнять все рекомендации специалистов, лишь в этом случае удастся вернуться к нормальной жизни.
Как предупредить инсульт?
К факторам риска инсульта относятся:
- вредные привычки;
- неправильное питание: злоупотребление жирной, жареной пищей, копченостями, фастфудом;
- малоподвижный образ жизни;
- лишний вес;
- сахарный диабет;
- гипертония, атеросклероз и другие заболевания сосудов;
- болезни сердца;
- нарушение свертывания крови, склонность к формированию тромбов;
- инфекционно-воспалительные или дегенеративные поражения мозговых отделов;
- перенесенные черепно-мозговые травмы;
- регулярные стрессы;
- гипоксия;
- тяжелая интоксикация;
- наследственная предрасположенность, преклонный возраст.
Для профилактики инсульта важно ограничить влияние провоцирующих факторов, пациентам из группы риска наблюдаться у кардиолога и невролога.
С-реактивный белок (СРБ) – компонент крови, чувствительный к острым и хроническим воспалениям в организме. Его быстрое увеличение связано с высокой активностью воспалительного процесса и степенью повреждения тканей. Концентрация СРБ повышается при достаточно тяжелых заболеваниях, прогрессирование которых можно предотвратить, если вовремя пройти диагностику и начать лечение.

Что такое С-реактивный белок?
Второе его название гликопротеин. Он вырабатывается клетками печени, является маркером значительного повреждения тканей.
Это белок острой фазы воспалительного процесса. Он более чувствителен к воспалению, нежели скорость оседания эритроцитов (СОЭ). Его концентрация моментально повышается уже в течение первых часов развития патологического процесса в организме, который сопровождается распадом клеток и некрозом тканей.
Особенность СРБ в том, что показатели приходят в норму так же быстро, как и происходит рост. Его концентрация снижается раньше, чем изменяется СОЭ. Повышение С-реактивного белка предшествует возникновению болезненной симптоматики: лихорадки, головной боли, повышенного потоотделения, других признаков инфекционной болезни.

Норма С-реактивного белка в крови
Чтобы оценить концентрацию гликопротеина, необходимо сдать анализ крови на С-реактивный белок. Нормой является значение 0-1 мг/л. В острую фазу болезни показатели могут возрастать в 20-100 раз.
Чтобы точно понять причину повышения С-реактивного белка, результаты лабораторного исследования нужно интерпретировать с учетом других показателей крови, данных, полученных в ходе инструментальной диагностики.
Высокий уровень белка может свидетельствовать об огромном количестве заболеваний. Причины его повышения:
- бактериальные, вирусные или грибковые инфекции;
- заболевания поджелудочной железы, включая панкреатит, панкреонекроз, сахарный диабет;
- онкологические заболевания, метастазы;
- массивные ожоги, обморожения, травмы;
- аутоиммунные и ревматические патологии – ревматоидный артрит и полиартрит, васкулит, системная красная волчанка;
- артрит, артроз;
- туберкулез;
- инфекционный эндокардит;
- острый инфаркт миокарда или инсульт;
- сепсис, перитонит;
- хронические воспалительные процессы в организме, например, хронический тонзиллит;
- оперативные вмешательства, послеоперационный период.
Небольшое увеличение присуще пациентам с избыточным весом, нарушением гормонального фона.
К факторам, провоцирующим повышение С-реактивного белка также относится беременность, прием пероральных контрацептивов, продолжительная гормональная терапия, чрезмерные физические нагрузки. А вот применение нестероидных противовоспалительных препаратов и некоторых других лекарств наоборот снижает концентрацию СРБ.

Воспалительные процессы и инфекционные заболевания
С-реактивный белок повышается при острых воспалениях, рецидивах хронических воспалительных заболеваний, повреждении тканей во время хирургических вмешательств. Уровень может достигать 40-100 мг/л.
Если после операции СРБ остается патологически высоким, то это указывает на развитие послеоперационных осложнений: пневмония, абсцесс, тромбофлебит.
Что касается инфекционных болезней, то самые высокие значения СРБ при бактериальной инфекции, могут достигать 100 мг/л. При вирусных заболевания концентрация не превышает 20 мг/л.
Повышение уровня СРБ сопряжено с риском развития болезней сердца и сосудов. Концентрация выше 3 мг/л может указывать на воспалительные процессы в стенках сосудов, гипертонию, развитие инфаркта миокарда, инсульта, прогрессирование атеросклероза.
Белок повышается в первые сутки после развития инфаркта, постепенно снижается в течение месяца. При рецидивах его уровень снова возрастает.
В группе риска сердечно-сосудистых патологий находятся пациенты с высоким уровнем СРБ и воздействием следующих провоцирующих факторов:
- ожирение;
- высокая концентрация глюкозы в крови;
- курение;
- малоподвижный образ жизни;
- высокий уровень холестерина, триглицеридов в крови.

Рак легкого, желудка, яичников, предстательной, поджелудочной железы, печени и других органов сопровождается некрозом тканей, поэтому при метастазах и раковых клетках в организме происходит рост уровня СРБ.
Анализ на С-реактивный белок используют для оценки прогрессирования опухоли и эффективности противоопухолевой терапии, выявления рецидива болезни.
Подготовка к исследованию
Чтобы получить достоверные результаты обследования, нужно готовиться к процедуре. Важно исключить воздействие факторов, которые могут вызвать повышение белка. Для этого необходимо:
- за 12 ч. до исследования отказаться от приема пищи;
- за полчаса до процедуры не курить, избегать физических и психоэмоциональных нагрузок.
Для анализа делается забор венозной крови.

Когда требуется обследование?
Анализ назначают в таких случаях:
- для дифференциальной диагностики вирусной и бактериальной инфекции;
- чтобы выявить наличие очагов воспаления в организме, в том числе скрытых, отследить эффективность лечения;
- при подозрении на злокачественные опухоли;
- для контроля состояния пациента в послеоперационном периоде;
- чтобы оценить риск возникновения заболеваний сердца и сосудов;
- для контроля течения хронических болезней.
Для повышения информативности, исследование на СРБ дополняют клиническим анализом крови, коагулограммой, анализом на ревматоидный фактор, онкомаркеры.

Чем опасен повышенный С-реактивный белок?
Опасность представляют болезни, которые сопровождаются ростом СРБ. Запредельно высокий уровень диагностируют не только при бактериальной инфекции, но также при панкреонекрозе, ожоге, сепсисе, перитоните. Концентрация может достигать 300 мг/л.
Как снизить высокий уровень С-реактивного белка?
Расшифровкой анализов, как и назначением лечения должен заниматься профильный специалист – инфекционист, ревматолог, кардиолог, онколог, терапевт. При правильной терапии СРБ начинает снижаться на 6-10 сутки, в то время, как СОЭ – на 14-28 день.
Чтобы снизить концентрацию С-реактивного белка назначают медикаменты. Эффективны сатины и ацетилсалициловая кислота. Они уменьшают воспалительные процессы в стенках сосудов и проявления атеросклероза. При инфекционно-воспалительных заболеваниях снижению СРБ в крови способствуют нестероидные противовоспалительные средства.

Не менее важен здоровый образ жизни и правильное питание. Необходимо отказаться от курения и употребления алкоголя. Нормализация веса при ожирении сопровождается снижением С-реактивного белка, поэтому стоит заниматься спортом, придерживаться диеты с низким уровнем холестерина.
Регулярные физические нагрузки, здоровый образ жизни и сбалансированное питание – залог крепкого иммунитета, лучшая профилактика сердечно-сосудистых, онкологических и инфекционных заболеваний, которые чаще всего становится причиной высокого СРБ.
Читайте также:

