Кишечная палочка коли протейная
Обновлено: 19.04.2024
Бактерии широко распространяются, новые госпитальные штаммы регулярно формируются из-за широкого применения антибиотиков и высокой резистентности протея к большинству этих препаратов. Протеи в отделениях для грудничков могут вызвать экзогенную нозокомиальную инфекцию.
Инфекцию распространяют больные люди разных возрастов и бактериовыделители без ярко выраженной симптоматики. Самое большое количество возбудителей протеоза выделяют с испражнениями больные с кишечной протейной инфекцией. В 1 г фекалий содержится до 10 7 —10 8 бактерий. Также большое количество возбудителя попадает во внешнюю среду при гнойно-воспалительных процессах: нагноении ожоговых поверхностей, операционных ран, отите, остеомиелите, флегмонах и т. д. То же касается и болезней мочевых путей, вызванных Proteus.
Данному заболеванию подвержены в том числе новорожденные, груднички и дети дошкольного возраста, лица, имеющие аномалии и поражения мочевых путей, а также ослабленные хирургическими вмешательствами и/или разными болезнями.
Пути передачи протейной инфекции:
- контактный
- пищевой (творог, рыба, мясо, фруктово-овощные смеси)
- медаппаратура, инструменты
- предметы ухода за больными взрослыми и детьми.
Заболевания протеозами фиксируют на протяжении всех пор года, в основном заболеваемость спорадическая (без эпидемических вспышек).
Что провоцирует / Причины Протейной инфекции у детей:
Существует пять видов рода протеев:
- P. mirabilis
- P. vulgaris
- P. retgeri
- P. morganii
- P. inconstans (providencia).
Разница между видами заключается в антигенной структуре. Протеи на данный момент считаются условно-патогенными микроорганизмами, возбудителями нозокомиапьных инфекций по типу пиелонефрита, острого гастроэнтерита, омфалита и т.д.
Патогенез (что происходит?) во время Протейной инфекции у детей:
Протеи вырабатывают уреазу – фермент, который расщепляет мочевину. Это грозит ощелачиванием мочи, нарушением целостности эпителия мочевых путей и снижением его резистентности. Таким образом возбудитель болезни колонизирует мочевые пути.
Протеи в тонком кишечнике приводят к развитию энтероколита, энтерита. Формирование того или иного симптома зависит от состояния макроорганизма, дозы и вирулентности штамма возбудителя. Почти сразу после заражения какая-то доза бактерий попадает в стенку кишки и в органы, где и сохраняется. Предположительно, там он и размножается несколько суток. Если есть соответствующие условия, появляются вторичные очаги, которые в условиях снижения резистентности организма ребенка могут приводить к локальным инфекционным процессам или вторичной бактериемии.
Таким образом, протеи при экзогенном заражении могут спровоцировать не только кишечную инфекцию, но и сделать кишечник источником потенциальной эндогенной инфекции различной локализации (месторасположения).
Симптомы Протейной инфекции у детей:

Среди основных симптомов протеозов:
- гнойно-воспалительные процессы на коже
- поражения мочевых путей
- гнойно-воспалительные процессы в костной ткани
- поражения ЖКТ
- поражения мозговых оболочек
- поражения уха
- поражения придаточных пазух
- поражения легких и т. д.
В детском организме поражается прежде всего желудочно-кишечный тракт, а также мочевая система. При кишечной инфекции заражение происходит во время контакта с заболевшим диереей человеком или во время употребления зараженной протеем еды. От 2-3 часов до 2 суток колеблется инкубационный период. Болезнь имеет острое начало, проявляются общеинфекционные симптомы, нарушается функция ЖКТ.
Стул больного водянистый, желто-зеленый, имеет очень неприятный запах. В стуле можно заметить непереваренные комочки пищи, может быть присемь слизи. Дефекация происходит 5-10 раз в сутки. В 1/3 случаев среди симптомов – метеоризм и боли в животе. В ½ случаев фиксируют увеличение печени, а в 1/3 случаев – селезенка.
У детей до 12-ти месяцев при заражении протейной инфекцией начинается кишечный токсикоз с эксикозом I—II степени. Фиксируют потерю массы тела, сухость слизистых оболочек и кожи, снижение эластичности кожи и тургора мягких тканей. Происходят нарушения сердечно-сосудистой системы: относительная тахикардия, приглушение тонов сердца, в некоторых случаях – систолический шум.
Патологические изменения легких проявляются такими симптомами:
- токсическая одышка
- развитие пневмонии.
В пик болезни фиксируют олигурию с умеренным количеством белка в моче. Под олигурией понимают уменьшение количества отделяемой почками мочи. Анализ крови показывает у ½ больных детей нейтрофилез, лейкоцитоз, палочкоядерный сдвиг, умеренно повышенную СОЭ.
Кишечная инфекция длится 5-10 дней. Самый длительный симптом – дисфункция кишечника с вторичными нарушениями пищеварения. Морфологические изменения в кишечнике представляют собой острый серозный энтерит. Гистологические методы исследования показывают отек стенок кишок, полнокровие, поверхностные дефекты. Лимфогистиоцитарные инфильтратыобнаруживаются обнаруживают в слизистой оболочке и подслизистом слое кишки. Дистрофические процессы наблюдаются в других внутренних органах. Есть вероятность развития пневмонии. Затяжной энтероколит может привести к возникновению глубоких множественных язв, диаметр которых от 0,2 до 0,5 мм. Язвы имеют приподнятые края. Редко они находятся в области единичных лимфатических фолликулов.
У детей с аномалией развития почек и органов мочевой системы может быть поражение мочевых путей. Частое поражение мочевых путей объясняется выработкой протеями фермента уреазы, которая способствует нарушению целостности эпителия мочевых путей и внедрению возбудителя в эти ткани. После попадания в мочевую систему возбудитель закрепляется в паренхиме почек, что приводит к развитию пиелонефрита.
Симптоматика протейных пиелонефритов:
- тупые боли в области поясницы
- повышенная утомляемость
- субфебрильная температура тела
- транзиторная гипертензия (не всегда).
Особенности протейной инфекции у новорожденных и детей до 12-ти месяцев. Нередкими являются вспышки протеозов в отделениях для новорожденных. Заражение может произойти через аппаратуру. Протейная инфекция может локазалироваться по-разному у новорожденных. Протейная диарея имеет острое начало, температура тела поднимается до уровня 37,5—38 ˚С. Проявляются такие симптомы как рвота и жидкий стул со слизью и зеленью, болезненность живота, вздутие, урчание по ходу расположения кишечника.
На протяжении 2-3 первых дней развивается дегидратация на фоне общеинфекционного токсикоза. Дети начинают плохо питаться (отталкивают грудь), наблюдается вялость, появляется токсическая одышка.
Есть вероятность инфекции пупочной ранки — омфалита в сочетании с инфекцией пупочных сосудов в виде септического артериита и флебита, захватывающего пупочную и портальную вены.
Протейная инфекция у новорожденных иногда развивается как острый гнойный менингит с септицемией. Болезнь имеет внезапное начало, температура тела поднимается до уровня 38 ˚С, малыш проявляет беспокойство, нарушается ритм дыхания, появляется цианоз. У младенцев наблюдается резкое ослабление сосательного рефлекса, возникновение спастических судорог в ручках и ножках, гемипарезы. Ребенок начинает пронзительно кричать. В крови отмечается лейкоцитоз более 10 9 , в спинномозговой жидкости — плеоцитоз с преобладанием нейтро-филов (до 70—90%). Если не случается летального исхода, происходит отставание в психомоторном развитии и судорожные припадки.
Диагностика Протейной инфекции у детей:
Для постановки диагноза нужны бактериологические исследования такого биологического материала как испражнения, рвотные массы, моча, кровь, отделяемое из воспалительных очагов на коже. Иногда исследуют на присутствие бактерий воду, пищевые продукты, смывы с предметов, которые использовал больной, с медаппаратуры, а также лекарственные растворы.
В диагностике важны показания серологических исследований. Антитела к аутоштамму протея начинают выявляться в РА с 5— 6-го дня болезни в титрах 1:200 и 1:400 с максимумом к 9—15-му дню от начала заболевания (1:400— 1:1600). Применяют также РСК и РПГА.
Болезни мочевых путей с с протейной бактериурией сопровождаются появлением антипротейных антител в титрах от 1:160 до 1:640. При пиелонефритах и септических состояниях диагностическое значение придается титрам антипротейных антител 1:320 и выше.
Лечение Протейной инфекции у детей:
Терапия кишечных инфекций базируется на тех же принципах, что и лечение других кишечных инфекций бактериальной природы. Для лечения легких форм используется колипротейный бактериофаг. Для лечения тяжелых форм протейной инфекции у детей применяют антибактериальные препараты, например, защищенные пенипиллины, гентамицин, цефалоспорины III поколения.
Нормализацию микрофлоры кишечника в периоде реконвалесценции проводят с помощью полибактерина, бифидумбактерина, линекса, бификола, энтерола и пр.
Если произошло поражение мочевыводящих путей и почечной паренхимы, необходимо восстановить нормальный пассаж мочи. Антибактериальную терапию в данных случаях проводят при бактериурии и признаках пиелонефрита. Уроштаммы протея устойчивы к пенициллину, эритромицину, полимиксину и сохраняют высокую чувствительность к препаратам налидиксовой кислоты.
Чтобы усилить эффективность противопротейных препаратов, их сочетают с другими. К примеру, фурадонин сочетается с эритромицином, невиграмон с левомниетином, ампициллин с геитамицином.
Вялотекущие процессы лечатся комплексной терапией, с включением иммуномодуляторов, к примеру, нуклеината натрия, метилурацила, а также вакцины из бактерий рода Proteus или аутовакцины. При тяжелых формах болезни врачи иногда прописывают колипротейную плазму и антипротейную иммунную сыворотку.
Прогноз
Неблагоприятным исходам грозят случаи генерализированных заболеваний у новорожденных недоношенных детей. Острые кишечные инфекции, вызванные протеями, оканчиваются в большинстве случаев выздоровлением ребенка. Течение протейной инфекции бывает упорным, с рецидивами. В последние годы часто формируется вялотекущий пиелонефрит, трудно поддающийся лечению.
Профилактика Протейной инфекции у детей:
Специфических профилактических мер протеозов пока что нет. Для предупреждения протеозов важно соблюдать санитарно-гигиенические правила. Большие трудности представляет борьба с нозокомиальной протейной инфекцией, особенно в палатах для новорожденных и в урологических стационарах. Для снижения риска инфицирования протеем в указанных медицинских учреждениях необходимо наряду с применением дезинфекции и антисептических средств orpaничивать инвазивные манипуляции до минимума.
К каким докторам следует обращаться если у Вас Протейная инфекция у детей:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Протейной инфекции у детей, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .

В последние годы инфекционисты отмечают рост заболеваний, обусловленных нетрадиционными микроорганизмами. Особое место занимает протейная инфекция. Ее кишечная форма, вызванная бакетриями рода Протей — P. vulgaris протекает тяжелее у детей раннего возраста. Не менее опасны гнойно-воспалительные заболевания мочевыводящей системы, вызываемые P. mirabilis, P. rettgeri и P. morganii.
В греческой мифологии Протей – божество, способное менять облик. Отсюда название полиморфных, мелких, нитевидных палочек, отличающихся активной подвижностью. Размеры клеток составляют 0,5 — 3 мкм. P. morganii, P. rettgeri — менее полиморфны и малоподвижны.
Протейная инфекция: причины, развитие, опасность для организма
Возбудителями протейной инфекции являются грамотрицательные условно-патогенные микроорганизмы семейства энтеробактерий, которые присутствуют в нормальной микрофлоре кишечника, а также повсеместно распространены в воздухе, почве и воде. Бактерии рода Proteus в течение долгого времени не причислялись к возбудителям серьезных инфекционно-воспалительных заболеваний. Однако в связи с последними достижениями в области диагностики было обнаружено, что эти микроорганизмы способны вызывать трудно поддающиеся лечению патологии (протеозы), поражающие преимущественно ЖКТ и мочеполовую систему.
Протей – факультативный анаэроб, палочковидная, неспороносная, подвижная, грамотрицательная бактерия. В микробиологическом анализе кала протей встречается в комплексе с другими условно-патогенными бактериями семейства энтеробактерий. Кроме протея, в составе нормальной микрофлоры кишечника человека определяются: клебсиелла, энтеробактер, гафния, серратия, морганелла, провиденция, цитробактер. В 1 г кала должно быть меньше 10 4 общего количества этих бактерий. Большее количество перечисленных бактерий является признаком дисбактериоза.
В природе бактерии рода Proteus обнаруживаются: в сточных водах, в земле, в водоемах, на овощах, в разлагающихся органических веществах. Эти микроорганизмы — сапрофиты, они живут на слизистых оболочках, на коже, в кишечнике человека и животных. Протеи устойчивы во внешней среде и сохраняют жизнедеятельность в слабых растворах фенола и других средств. Выявлена также резистентность ко многим антибиотикам.
Причины протейной инфекции
Протейная палочка, присутствующая в кишечной микрофлоре в небольших количествах, не причиняет организму никакого вреда. При определенных обстоятельствах (снижение иммунитета, неправильное питание, длительный прием антибиотиков) она может активизироваться и начать интенсивно размножаться. Также инфицирующее количество этих бактерий способно проникнуть в организм из внешней среды.
Основными путями передачи инфекции являются пищевой и контактно-бытовой. Чаще всего заражение происходит при употреблении белковых продуктов (мяса, рыбы, молока, колбасы), которые хранились с нарушением надлежащих сроков и условий. Значительно реже инфицирование осуществляется через немытые руки, во время купания или при употреблении зараженной воды.
Инфицирование протеем может произойти через полуфабрикаты, сырые продукты или готовые блюда из мяса, рыбы, молока, колбасы, студня. В них происходит быстрое размножение бактерий с образованием токсинов. Реже отмечают водный путь передачи: при купании в загрязненных водоемах или употреблении инфицированной воды. Возможен и контактный путь передачи на инфицированных руках зараженного человека.
Развитие патологии
При непосредственном попадании протея в ЖКТ вместе с продуктами питания инфекционное заболевание развивается очень стремительно. Первые симптомы ярко выражены, а общая клиническая картина совпадает с проявлениями сильного пищевого отравления. При контактно-бытовом способе заражения развитие признаков инфекции обычно происходит медленнее.
Если инфекционный процесс протекает в легкой форме, больной испытывает слабость, у него отмечаются повышение температуры, рвота, боль в животе, частый водянистый стул, в котором могут обнаруживаться слизь и зеленые включения. При тяжелом течении заболевания приступы рвоты случаются около 10 раз за сутки и более, а температура обычно поднимается до 40°С.
При условии своевременного и адекватного лечения вся острая симптоматика протеоза легкой или средней степени тяжести исчезает спустя несколько дней, после чего больной быстро идет на поправку.
Протеи выделяют токсические вещества — эндотоксины с гемолитическими свойствами и с различной степенью биохимической активности. У штаммов P. vulgaris обнаружена лецитиназная активность. Протеи обладают способностью адгезии к уротелию при помощи ресничек. Отмечают, что резистентность к антибиотикам связана с адгезивной способностью уропатогенных протеев.
Острой кишечной протейной инфекцией, протекающей по типу гастроэнтерита, гастрита и колиэнтерита часто болеют дети раннего возраста с пониженным иммунитетом и после бесконтрольного назначения антибиотиков. Заболевание сопровождается симптомами токсикоза — повышением температуры, рвотой, метеоризмом, схваткообразными болями в животе, нарушением аппетита, кратковременными судорогами, появлением водянистого, зловонного, учащенного стула.
В тяжелых случаях могут развиться осложнения: гемолитико-уремический синдром, а также симптомы острой гемолитической тромбопении, анемии или острой почечной недостаточности.
Клинические проявления внутрибольничной инфекции протейной этиологии весьма разнообразны: поражения мочевыводящей системы, отиты, холециститы, нагноения ран и септические состояния. Попадание протеев в пупочную ранку новорожденного может привести к бактериемии или развитию менингита.
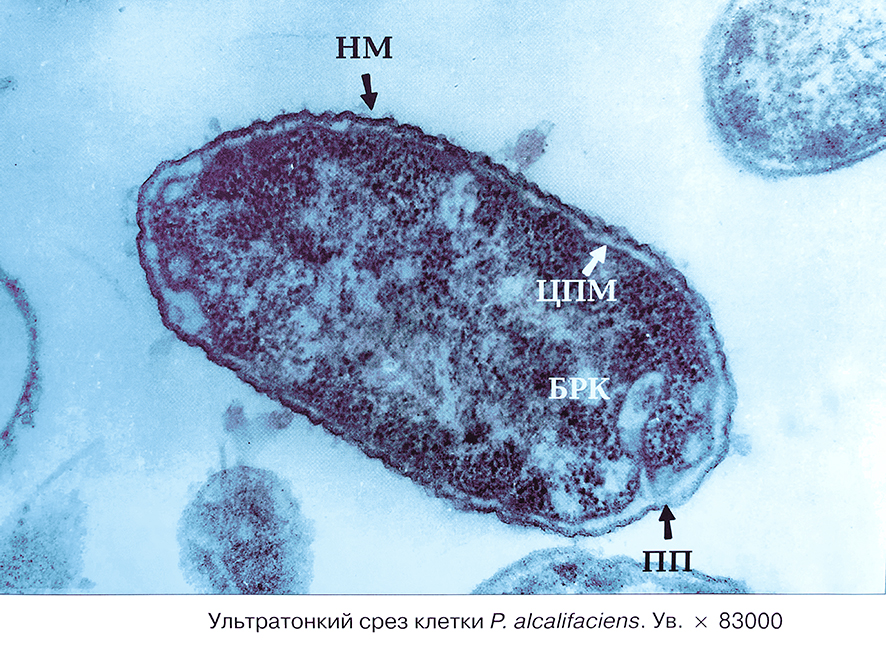
Данные заболевания могут развиться: при передаче возбудителя контактно-бытовым или воздушно-капельным путями, при заносе с катетером, другими урологическими инструментами.
Ультратонкий срез клетки Proteus alcalifaciens. Увеличение *83000
Если в мазках исследуемого материала (участки ожоговой ткани, гной, раневое отделяемое, испражнения) обнаруживаются грамотрицательные палочки, то бактериоскопический метод позволяет сделать предварительное заключение. Бактериологическим методом на средах определяют колонии протея в виде тонкого стелющегося налета. Активно размножаются протеи на белковой питательной среде вызывают гниение мяса, рыбы, других белковых продуктов.
Важнейшие профилактические меры — это соблюдение санитарного режима в детских учреждениях и стационарах, проведение общесанитарных мероприятий. Для профилактики протея каждому необходимо соблюдать правила личной гигиены, исключить потребление подозрительных продуктов в питании, избегать контактов с больными детьми и взрослыми.
При лечении протейной инфекции следует придерживаться лечебной щадящей диеты с исключением жареных, острых блюд, белковых продуктов. В острый период протейного инфицирования, при поражении желудочно-кишечного тракта — необходимо обеспечить восполнение потерянной жидкости. Полезно употреблять отвары трав – тысячелистника, алтея, зверобоя, ромашки, календулы; морсы, компоты с клюквой, черной смородиной, абрикосами, черникой, яблоками. Применять антибиотики можно только по назначению врача, в соответствии с данными анализов чувствительности бактерии протея к ним.
Обязательно нужно принимать препараты – пробиотики, пребиотики, синбиотики для восстановления нормальной флоры кишечника.
Синбиотические комплексы Нормофлорины, содержащий живые активные лакто- и бифидобактерии, секретирующие молочную, уксусную, масляную, пропионовую кислоты, оказывающие защитное, антисептическое, противовоспалительное, сорбционное действие – уменьшает интоксикацию, улучшает моторику кишечника, функцию печени, повышает иммунную реактивность. Это помогает в борьбе с протейной инфекцией, восстанавливает работу желудочно-кишечного тракта, общее самочувствие, повышает иммунитет.
Схема (возрастные дозировки для детей или взрослых): (взрослый) нормофлорин Л – 20 мл (при диарее) – 40 (при запорах) мл утром перед едой, Д — 40 мл вечером за 20 мин до еды, Б – 20-30 мл на ночь в клизме. При диарее в обед можно добавить Д – 30-40 мл, при запорах в обед + Л – 30-40 мл.
Курс приема нормофлоринов — 1 — 1,5 месяца, для выведения токсинов, патогенной микрофлоры, восстановления полезных собственных бактерий. Уникальный состав нормофлоринов, не содержащих белков коровьего молока, молочного сахара, консервантов позволяет при протейной инфекции успешно применять его у детей с первых дней жизни, беременных, кормящих, больных сахарным диабетом, аллергическими заболеваниями, т.е. у взрослых при любой сопутствующей патологии.
Опасность протейной инфекции

Протейная инфекция
Тяжелые формы патологии могут осложняться состояниями, требующими срочной госпитализации больного, такими как сильное обезвоживание, судороги, инфекционно-токсический шок.
protey_mirabilis
Помимо острых инфекций пищеварительной системы бактерии Proteus способны поражать другие органы, распространяясь через кровь или по лимфатическим сосудам. Очаг воспаления может локализоваться в мочеполовой системе, глазах, ушах, легких и даже в костной ткани или мозговых оболочках. Данные патологии достаточно часто переходят в хроническую форму с упорным рецидивирующим течением, которая тяжело поддается терапии.
Если протейная инфекция заносится на незажившие поверхности кожи и слизистых оболочек (послеоперационные раны, ожоги), вызванный ею воспалительный процесс значительно замедляет регенерацию тканей и снижает эффективность лечебных мероприятий.
Следует отметить, что даже незначительное превышение нормального количества протейной палочки в кишечной микрофлоре может негативно отразиться на состоянии здоровья. Так, если у человека имеются аутоиммунные болезни, существует высокий риск их обострения из-за возросшей активности протейной палочки. Атопический дерматит, астма, аллергические заболевания и другие иммунозависимые патологии могут впервые развиться или обостриться под воздействием бактерий Proteus.

Протейная инфекция: причины, развитие, опасность для организма
Возбудителями протейной инфекции являются грамотрицательные условно-патогенные микроорганизмы семейства энтеробактерий, которые присутствуют в нормальной микрофлоре кишечника, а также повсеместно распространены в воздухе, почве и воде. Бактерии рода Proteus в течение долгого времени не причислялись к возбудителям серьезных инфекционно-воспалительных заболеваний. Однако в связи с последними достижениями в области диагностики было обнаружено, что эти микроорганизмы способны вызывать трудно поддающиеся лечению патологии (протеозы), поражающие преимущественно ЖКТ и мочеполовую систему.
Причины протейной инфекции
Протейная палочка, присутствующая в кишечной микрофлоре в небольших количествах, не причиняет организму никакого вреда. При определенных обстоятельствах (снижение иммунитета, неправильное питание, длительный прием антибиотиков) она может активизироваться и начать интенсивно размножаться. Также инфицирующее количество этих бактерий способно проникнуть в организм из внешней среды.
Основными путями передачи инфекции являются пищевой и контактно-бытовой. Чаще всего заражение происходит при употреблении белковых продуктов (мяса, рыбы, молока, колбасы), которые хранились с нарушением надлежащих сроков и условий. Значительно реже инфицирование осуществляется через немытые руки, во время купания или при употреблении зараженной воды.
Развитие патологии
При непосредственном попадании протея в ЖКТ вместе с продуктами питания инфекционное заболевание развивается очень стремительно. Первые симптомы ярко выражены, а общая клиническая картина совпадает с проявлениями сильного пищевого отравления. При контактно-бытовом способе заражения развитие признаков инфекции обычно происходит медленнее.
Если инфекционный процесс протекает в легкой форме, больной испытывает слабость, у него отмечаются повышение температуры, рвота, боль в животе, частый водянистый стул, в котором могут обнаруживаться слизь и зеленые включения. При тяжелом течении заболевания приступы рвоты случаются около 10 раз за сутки и более, а температура обычно поднимается до 40°С.
При условии своевременного и адекватного лечения вся острая симптоматика протеоза легкой или средней степени тяжести исчезает спустя несколько дней, после чего больной быстро идет на поправку.
Опасность протейной инфекции
Тяжелые формы патологии могут осложняться состояниями, требующими срочной госпитализации больного, такими как сильное обезвоживание, судороги, инфекционно-токсический шок.
Помимо острых инфекций пищеварительной системы бактерии Proteus способны поражать другие органы, распространяясь через кровь или по лимфатическим сосудам. Очаг воспаления может локализоваться в мочеполовой системе, глазах, ушах, легких и даже в костной ткани или мозговых оболочках. Данные патологии достаточно часто переходят в хроническую форму с упорным рецидивирующим течением, которая тяжело поддается терапии.
Если протейная инфекция заносится на незажившие поверхности кожи и слизистых оболочек (послеоперационные раны, ожоги), вызванный ею воспалительный процесс значительно замедляет регенерацию тканей и снижает эффективность лечебных мероприятий.
Следует отметить, что даже незначительное превышение нормального количества протейной палочки в кишечной микрофлоре может негативно отразиться на состоянии здоровья. Так, если у человека имеются аутоиммунные болезни, существует высокий риск их обострения из-за возросшей активности протейной палочки. Атопический дерматит, астма, аллергические заболевания и другие иммунозависимые патологии могут впервые развиться или обостриться под воздействием бактерий Proteus.
Кишечная палочка представляет собой палочковидную бактерию, населяющую нижнюю часть кишечника теплокровных организмов. Справедливо отметить, что в умеренном количестве определенные разновидности кишечных палочек населяют и человеческий организм. Они не только безвредны, но и приносят определенную пользу хозяину - участвуют в синтезе витамина К и витаминов группы В, поддерживают нормальную микрофлору в ЖКТ, создавая условия для жизнедеятельности бифидо- и лактобактерий. Однако при определенных обстоятельствах и в определенной среде склонны к активному размножению патогенные разновидности кишечной палочки. Более того, безвредная для человека кишечная палочка остается безвредной лишь в пределах кишечника. Попадая в другие системы организма, например, во влагалище, предстательную железу, брюшную полость она может стать причиной, соответственно, вагинита, простатита, перитонита.
Некоторые штаммы кишечной палочки (обитающие преимущественно во внешней среде) могут стать причиной желудочно-кишечных расстройств, менингита и различных инфекционных воспалительных процессов (пневмония, сепсис и т.д.). Более подвержены заражению дети и пожилые люди по причине неокрепшего или ослабленного иммунитета. Тем не менее, осторожными нужно быть и взрослым людям, отличающимся крепким здоровьем.
Источниками патогенных штаммов кишечной палочки являются:
- пища, приготовленная с несоблюдением санитарных норм;
- загрязнение продуктов навозом, полив урожая загрязнённой водой или сточными водами; употребление такого урожая невымытым;
- употреблением для питья воды, загрязнённой сточными водами;
- купание в инфицированных водоемах и случайное заглатывание такой воды.
Симптомы заражения проявляются следующим образом:
- расстройство стула (понос или запор);
- тошнота и рвота;
- вздутие, дискомфорт, боль в животе, метеоризм;
- изменение запаха каловых масс, возникновение запаха изо рта;
- общее недомогание - слабость, сонливость, отсутствие аппетита;
- возможно повышение температуры тела.
Диагностика наличия патогенных штаммов кишечной палочки происходит на основании анализа каловых или рвотных масс, гноя, отделяемого со слизистой оболочки зева и носа, при подозрениях на сепсис на анализ берется кровь.
Лечение кишечной палочки предполагает терапию антибиотиками, однако подбирать их надо с учетом результатов бактериологического посева, на который направляется содержимое кишечника. Чаще всего назначаются антибиотики из группы аминогликозидов. При лечении антибиотиками всегда необходимо учитывать вероятность развития дисбактериоза, а потому профилактика данного нарушения также предполагается и должна быть прописана лечащим врачом.
Эшехериозы – группа заболеваний, вызванных возбудителем кишечной инфекции. Энтеропатогенный эшерихиоз – болезнь, которой подвержены в основном новорожденные и дети раннего возраста.
Эпидемиология
Энтеропатогенным эшерихиозом часто болеют дети от 3 месцев до 1 года жизни, в особенности те, у кого неблагоприятный преморбидный фон, ослабленность интеркуррентными заболеваниями, а также находящиеся на искусственном вскармливании. Эшерихиозу данного типа подвержены и недоношенные дети. Болезнь встречается в виде спорадических случаев и эпидемических вспышек, которые возникают в основном в родильных домах, соматических стационарах, ясельных группах детского сада, отделениях для новорожденных и домах ребенка.
Инфекцию распространяют дети в пик проявления симптомов заболевания, поскольку в этом периоде болезни ребенок выделяет в окружающую среду очень большое количество возбудителя энтеропатогенного эшерихиоза. Данный возбудитель может от 2 до 5 месяцев сохраняться на посуде, белье, игрушках, предметах обихода, с которыми имел контакт больной человек. Взрослые люди являются переносчиками инфекции в случаях, если не соблюдают правила личной гигиены и противоэпидемического режима в детских учреждениях.
Основной путь заражения эшерихиозом – экзогенный, в основном контактно-бытовой. Также порой фиксируют пищевой путь заражения – через продукты детского питания (молочные смеси, соки и т. д.). Такие случаи вызывают эпидемии, приводят к тяжелым формам заболевания. Есть возможность заразиться данным заболеванием воздушно-пылевым путем. Может случиться заражение через воду и при проведении различных медицинских манипуляций. Если беременная мать является бессимптомным носителем эшерихиоза у детей, новорожденный может заразиться в процессе родов.
Заболевание встречается в виде спорадических случаев на протяжении всего года, вне зависимости от температурного режима. Доказана высокая контагиозность возбудителя, распространяется он быстро.
У детей на естественном вскармливании минимальные шансы заразиться. У малыша формируется иммунитет благодаря молоку матери, в котором содержатся секреторные IgA и факторы неспецифической защиты.
Что провоцирует / Причины Энтеропатогенного эшерихиоза у детей:
Заболевание вызывают эшерихии, которые представляют собой подвижные грамотрицательные палочки, аэробы. Они относятся к виду Еscherichia (Е.) coli, роду Escherichia, семейству Enterobacteriaceae.

Патогенез (что происходит?) во время Энтеропатогенного эшерихиоза у детей:
Инфекция попадает в организм человека через ЖКТ. Через рот они не умирая преодолевают желудок, попадая в тонкую кишку. ЭПЭ колонизируют слизистую оболочку тонкой кишки, вызывая повреждение и отторжение участков апикальной цитоплазмы, слущивание отдельных эпителиоцитов и их групп с развитием эрозий и умеренного воспаления.
Наиболее эпидемические штаммы могут транспортироваться фагосомоподобными вакуолями через эпителиальную клетку в подлежащую, приводя к транзиторной бактериемии и даже сепсису.
Местный воспалительный процесс развивается под действием возбудителя эшерихиоза, который размножается на поверхности эпителия, их эндотоксинов, токсичных соединений, гистамина, ингибиторов холинэстеразы, ферментов и пр. В итоге возникает диарейный синдром. Он приводит, в свою очередь, к обезвоживанию организма.
Патоморфология
Иммунитет
После того, как ребенок перенес энтеропатогенный эшерихиоз, у него формируется иммунитет к тому серовару эшерихий, который вызвал заболевание. Они действуют всего несколько месяцев. В кишечнике продуцируются лактоферрин, секреторные IgA, лизоцим, лимфоциты, которые имеют значение среди других факторов иммунитета.
Симптомы Энтеропатогенного эшерихиоза у детей:
От 5 до 8 суток длится инкубационный период при заражении данной формой эшерихиоза. При массивном инфицировании и у ослабленных, а также новорожденных детей инкубационный период может быть минимальным – 1-2 суток.
Болезнь может начинаться остро или постепенно (сначала проявляются явления энтерита). Испражнения чаще всего водянистые (желтые или оранжевые), среди примесей – прозрачная слизь в небольшом количестве. Когда вода из испражнений младенца впитывается в пеленку, стул может казаться нормальным, слизь не видна. Испражнения могут быть кашецеобразной консистенции, пенистыми. Могут наблюдаться включения в виде зелени – незначительные.
Наиболее постоянным симптомом является рвота, которая случается 1 или 2 раза в сутки. Также могут быть упорные срыгивания – с самых первых суток заболевания. Все симптомы часто проявляются постепенно, достигая максимума на 5-7 день после начала заболевания. Состояние ребенка ухудшается, адинамия усиливается, аппетит значительно снижен, частота срыгиваний увеличена.
Температура может быть фебрильной или субфебрильной на протяжении 1-2 недель. Стул случается 10-15 раз в сутки, и даже больше. Обезвоживание всё более заметно. У большинства детей развивается токсикоз с эксикозом.
Внешний осмотр фиксирует метеоризм (вздутие живота), урчание по ходу тонкой кишки, бледность кожного покрова. Печень и селезенка в подавляющем большинстве случаев не увеличены. Тяжелые формы заболевания могут привести к летальному исходу.
Течение и исход
Энтеропатогенный эшерихиоз протекает в острой форме. Симптомы проявляются несколько дней (как минимум) или 2-3 недели (как максимум), в очень редких случаях – дольше. Обострения и повторные волны возникают из-за другой вирусной кишечной или бактериальной инфекции или же из-за наслоения интеркуррентных заболеваний, к примеру, ОРВИ.
У ослабленных, часто болеющих детей, страдающих гипотрофией и иммунной недостаточностью, бывает затяжное течение (суперинфекции нет). Затяжное течение фиксируют, когда заболевание протекает больше 1 месяца.
Если болезнь имеет тяжелое течение (в особенности у младенцев), есть вероятность генерализации патологического процесса. Из кишечника он может распространяться на другие органы, приводя к тяжелым последствиям, даже к сепсису. Смерть вызывает тяжелый токсикоз с эксикозом, нарушение межуточного обмена и весьма часто — наслоение другой кишечной или вирусной инфекции.
Эшерихиозные менингиты имеют тяжелое течение, высокий процент смертей, большое количество остаточных явлений вплоть до гидроцефалии. Септические и токсико-сетпические формы эшерихиоза проявляются частой рвотой или срыгиваниями, высокой лихорадкой с большими размахами температуры тела в течение суток, частым стулом с обильными испражнениями с небольшой примесью слизи.
Диагностика Энтеропатогенного эшерихиоза у детей:
Для диагностики необходимы клинико-эпидемиологические данные, требуется лабораторное подтверждение. Диагностика позволяет сразу заподозрить энтеропатогенный эшерихиоз у детей только при типичных формах болезни. На болезнь в данном случае указывает постепенно нарастающий токсикоз с эксикозом, выраженная бледность кожных покровов, упорная нечастая рвота, метеоризм, частый водянистый стул (обильный, с примесью слизи прозрачного оттенка), испражнения желтого или оранжевого цвета.
Стертые, легкие и среднетяжелые формы диагностировать не просто, необходима лабораторная диагностика. Ведущий метод – бактериологический. Исследование проводится с забором испражнений больного ребенка, иногда – рвотных масс или ротоглоточной слизи, промывных вод желудка. Люминесцентный метод исследования позволяет получить ориентировочный результат уже через несколько часов.
Лечение Энтеропатогенного эшерихиоза у детей:
Лечение больных эшерихиозом базируется на тех же основах, что и при других острых кишечных инфекциях. Больные с тяжелой или среднетяжелой формой (при потребности в инфузионной терапии) подлежат госпитализации в обязательном порядке. Легкие формы лечат, не прибегая к госпитализации. В больницу кладут также детей по эпидпоказаниям, новорожденных и имеющих тяжелые сопутствующие заболевания или осложнения.
Диета должна учитывать возраст ребенка, тяжесть и период инфекционного процесса, его вскармливание до заражения. Энтеропатогенный эшерихиоз у детей поражает в основном тонкую кишку, потому ребенку тяжело переваривать пищевые продукты. Тем не менее и при энтеропатогенном эшерихиозе следует достаточно энергично увеличивать объем питания (после соответствующей разгрузки) и вводить в рацион новые продукты питания, но по мере восстановления функционального состояния желудочно-кишечного тракта, не приводя к срыву пищеварения.
При патогенетической терапии необходима срочная детоксикация с применением таких препаратов как смекта, энтеродез или энтеросгель (по назначению лечащего врача). При длительной энтеросорбции желательно использовать гидрофобный селективный энтеросорбент, который не повреждает кишечный барьер. Если мероприятия будут проведены своевременно, увеличиваются шансы ребенка на скорейшее выздоровление без осложнений заболевания.
Регидратационную терапию проводят, учитывая вид токсикоза и то, насколько обезвожен организм ребенка. Регидратация может быть оральной или внутривенной. В большинстве случаев применяют первый названный путь.
При тяжелых формах заболевания назначают проведение инфузионной терапии (цели: регидратация, интоксикация). Лечащий врач может назначить при тяжелой форме болезни преднизалон. Доза рассчитывается так: 2—3 мг/ кг тела в сутки. Также возможно лечение гидрокортизоном, доза которого составляет 5— 10 мг/ кг тела в сутки. курс лечения 3-5 суток.
Может быть необходима также посиндромная терапия, назначение витаминов, антигистаминных препаратов, сердечно-сосудистых средств и т. д. Если есть осложнения бактериальной природы, применяют антибиотики или химиопрепараты. Чтобы предотвратить генерализацию процесса у новорожденных и детей первых месяцев жизни, назначают также терапию антибиотиками. В легких случаях назначают рациональное питание, оральную регидратацию, ферментные препараты, бактериальные и симптоматические средства, энтеросорбенты. Если после 5-7-дневного курса терапии анитбактериальными препаратами сохраняется дисфункция кишечника, применяют эубиотики для восстановления нормальной кишечной флоры. Такая же терапия нужна в случае подтвержденного дисбактериоза кишечника. Курс лечения составляет 1-2 недели.
Для диагностики необходимы клинико-эпидемиологические данные, требуется лабораторное подтверждение. Диагностика позволяет сразу заподозрить энтеропатогенный эшерихиоз у детей только при типичных формах болезни. На болезнь в данном случае указывает постепенно нарастающий токсикоз с эксикозом, выраженная бледность кожных покровов, упорная нечастая рвота, метеоризм, частый водянистый стул (обильный, с примесью слизи прозрачного оттенка), испражнения желтого или оранжевого цвета.
Стертые, легкие и среднетяжелые формы диагностировать не просто, необходима лабораторная диагностика. Ведущий метод – бактериологический. Исследование проводится с забором испражнений больного ребенка, иногда – рвотных масс или ротоглоточной слизи, промывных вод желудка. Люминесцентный метод исследования позволяет получить ориентировочный результат уже через несколько часов.
Профилактика Энтеропатогенного эшерихиоза у детей:
- Профилактика должна быть направлена на строжайшее соблюдение санитарно-гигиенического и противоэпидемического режима в отделениях для новорожденных и недоношенных детей, родильных домах, в домах ребенка, ясельных группах детского сада.
- Необходимо применять одноразовое белье при уходе за новорожденными и детьми до 12-ти месяцев жизни.
- Рекомендуют естественное вскармливание детей до 6-ти месяцев жизни.
- Соблюдение технологических и санитарно-гигиенических требований при изготовлении продуктов детского питания.
- Бактериологическое исследование испражнений детей первых 2 лет жизни с дисфункцией кишечника.
- Важное значение имеет своевременное выявление источника инфекции, его изоляция и санирование.
- Текущая и заключительная дезинфекция в очаге инфекции, наблюдение на протяжении 1 недели.
- Мер специфической профилактики нет.
К каким докторам следует обращаться если у Вас Энтеропатогенный эшерихиоз у детей:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Энтеропатогенного эшерихиоза у детей, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Читайте также:

