Клацид при половых инфекциях
Обновлено: 15.04.2024
Уреаплазменную инфекцию лишь условно можно отнести к инфекциям, передаваемым половым путем. Дело в том, что возбудителем при этом является Ureaplasma urealyticum из семейства микоплазм, которые действительно могут обитать в половых путях и передават
Уреаплазменную инфекцию лишь условно можно отнести к инфекциям, передаваемым половым путем. Дело в том, что возбудителем при этом является Ureaplasma urealyticum из семейства микоплазм, которые действительно могут обитать в половых путях и передаваться при половых контактах. Однако роль уреаплазм, как и других микоплазм, за исключением M. genitalium, в возникновении воспалительной реакции достаточно неоднозначна, вследствие чего этот возбудитель большинство авторов, особенно за рубежом, относят к условно-патогенным. И в МКБ-10, международно признанном списке болезней, такого заболевания, как уреаплазмоз или уреаплазменная инфекция, не приведено. Между тем ряд исследователей приводят достаточно убедительные доказательства, свидетельствующие в пользу патогенности этой инфекции. Не так давно в Москве даже была защищена докторская диссертация, автор которой отстаивал именно эту точку зрения.
В 1954 г. Шепард впервые обнаружил U. urealyticum в выделениях, полученных от больного уретритом, и назвал их Т-микоплазмами (от английского слова tiny - крошечный). По своим размерам уреаплазмы являются одними из самых мелких представителей бактериальной флоры, выявляемой у человека, а по виду своей жизнедеятельности относятся к внутриклеточным паразитам.
Известны два биовара уреаплазм - Parvo и Т960, которые разделены на 14 сероваров. Последние достижения молекулярной биологии в исследовании ДНК и рибосомальной РНК уреаплазм позволили некоторым авторам (F. Kong et al., 2000) отказаться от классической классификации и разделить все уреаплазмы на два вида - Ureaplasma urealyticum (бывший биовар Т960) и Ureaplasma parvum (бывший биовар Parvo).
Как уже говорилось выше, вопрос о роли уреаплазм в этиологии и патогенезе заболеваний урогенитального тракта до сих пор не решен. Слишком уж широко они распространены, и слишком часто эти микроорганизмы выявляются у лиц, не имеющих клинической симптоматики. Авторы, относящие уреаплазмы к облигатным патогенам, считают, что они вызывают уретриты, цервициты, простатиты, послеродовые эндометриты, пиелонефриты, бесплодие, различную патологию беременности (хориоамниониты) и плода (легочную патологию). Другие исследователи полагают, что уреаплазмы являются частью условно-патогенной флоры урогенитального тракта и способны вызывать инфекционно-воспалительные заболевания мочеполовых органов только при определенных условиях (в частности, при недостаточности иммунитета) или при соответствующих микробных ассоциациях.
Показатели инфицированности урогенитального тракта уреаплазмами среди сексуально активного населения варьируют от 10 до 80%. Уреаплазмы, как правило, обнаруживают у людей, ведущих активную половую жизнь, а наиболее часто эти микроорганизмы выявляются у лиц, имеющих три и более половых партнеров. По данным F. Kong et al., у 81-87% больных выявляется Ureaplasma parvum и у 13-19% - Ureaplasma urealyticum. Клиническая картина воспалительного процесса, при котором обнаруживаются уреаплазмы, не имеет патогномоничных симптомов.
Авторы некоторых работ утверждают, что именно уреаплазмы зачастую являются причиной неблагоприятных исходов беременности, усугубляют риск преждевременных родов и летального исхода при рождении детей с очень низкой массой тела.
Вопрос о влиянии уреаплазм на репродуктивную функцию человека остается открытым. Между тем женское бесплодие может быть связано с воспалительными процессами в области половых органов, индуцированными уреаплазмами, приводящими к нарушению прохождения яйцеклетки в полость матки. Мужское бесплодие может быть обусловлено, во-первых, воспалительными процессами, а во-вторых - влиянием уреаплазм на сперматогенез. Адсорбция уреаплазм на поверхности сперматозоидов способна изменять их подвижность, морфологию и хромосомный аппарат.
Как и для большинства представителей условно-патогенной флоры, для уреаплазм выделяют ряд факторов, способствующих развитию инфекционно-воспалительных процессов. Наиболее важными из них являются иммунные нарушения, изменения гормонального статуса, массивность колонизации, ассоциации с другими бактериями. Все эти аспекты следует учитывать при выборе тактики ведения таких больных.
Методы диагностики
- Культуральное исследование на селективных средах. Такое исследование позволяет в течение 3 дней выделить культуру возбудителя и отделить уреаплазмы от других микоплазм. Материалами для исследования служат соскобы из урогенитального тракта и моча пациента. Метод позволяет определить чувствительность выделенных возбудителей к различным антибиотикам, что очень важно с учетом нередкой сегодня антибиотикорезистентности. Специфичность метода составляет 100%. Этот метод используется для одновременного выявления Mycoplasma hominis и Ureaplasma urealyticum.
- Обнаружение ДНК возбудителей методом ПЦР. Исследование позволяет в течение суток выявить возбудителя в соскобе из урогенитального тракта и определить его видовую принадлежность.
- Серологические тесты. Позволяют определять присутствие антигенов и специфических антител к ним в крови. Могут быть полезны при рецидивирующем течении болезни, при развитии осложнений и бесплодии.
Как и проблема патогенности уреаплазм, вопрос о необходимости элиминации этих возбудителей из урогенитального тракта также остается открытым. Чаще всего авторы предлагают принимать меры по элиминации этих микроорганизмов при наличии у человека инфекционно-воспалительного процесса в месте их обнаружения (уретрите, простатите, цервиците, вагините), а также при бесплодии, невынашивании беременности, воспалительных заболеваниях органов малого таза, хориоамнионите, послеродовых лихорадочных состояниях при наличии уреаплазм в мочеполовом тракте.
Этиотропное лечение уреаплазменной инфекции основывается на применении антибактериальных препаратов различных групп. Активность препаратов в отношении любой инфекции определяется по минимальной подавляющей концентрации (МПК) в исследованиях in vitro. Показатели МПК, как правило, коррелируют с результатами клинического излечения. Казалось бы, оптимальными препаратами должны являться антибиотики с наименьшей МПК, но при этом нельзя сбрасывать со счетов важность таких параметров, как биодоступность, способность к созданию высоких внутритканевых и внутриклеточных концентраций, переносимость и комплаентность лечения.
Уреаплазмы устойчивы к β-лактамным антибиотикам (пенициллинам и цефалоспоринам), из-за того что у них отсутствует клеточная стенка, и сульфаниламидам, так как эти микроорганизмы не синтезируют кислоту. При лечении уреаплазменной инфекции могут быть эффективны те антибактериальные агенты, которые воздействуют на синтез белка и ДНК, т. е. обладающие бактериостатическим действием. Это препараты тетрациклинового ряда, макролиды, фторхинолоны, аминогликозиды, левомицетин и некоторые другие (см. табл. 1).
Как видно из таблицы, доксициклин и кларитромицин отличаются наилучшими показателями МПК, кроме того, они высокоактивны в отношении уреаплазм. Другие препараты обладают избирательной активностью и их выбор определяется в зависимости от результатов микробиологических исследований.
Тетрациклины
Согласно методическим рекомендациям 1998 г. и Федеральному руководству по использованию лекарственных средств, при уреаплазменной инфекции рекомендуется назначение доксициклина (юнидокс солютаб, вибрамицин, медомицин). Препарат назначают по 100 мг 2 раза в день в течение 7-14 дней. Обычно при первом приеме антибиотика дозу удваивают. По рекомендациям Американского центра по контролю и профилактике заболеваний (CDC), доксициклин, наравне с эритромицином и офлоксацином, является препаратом выбора при лечении негонококковых уретритов (НГУ). Менее удобен для пациента курс тетрациклина, который применяют по 500 мг 4 раза в день в течение 7-10 дней.
Доксициклин используют в виде двух солей, в зависимости от того, применяют антибиотик в капсулах или в виде порошка. В капсулах используют доксициклина гидрохлорид или хиклат. Порошок для приготовления других пероральных форм представляет собой моногидрат доксициклина. Использование соли моногидрата вместо гидрохлорида исключает возникновение эзофагитов. Наиболее удобной в применении является лекарственная форма солютаб.
Благодаря своим особым фармакокинетическим свойствам, доксициклин переносится гораздо лучше, чем тетрациклин.
Хорошие результаты были получены при назначении доксициклина женщинам, инфицированным различными микоплазмами (в том числе уреаплазмами) и страдающим бесплодием или привычным невынашиванием беременности. После санации от микоплазм в ряде случаев наступала беременность, которая заканчивалась нормальными родами в срок и без осложнений.
Необходимо, однако, отметить, что от 2 до 33% штаммов уреаплазм могут быть устойчивы к тетрациклину. К другим существенным недостаткам препаратов тетрациклинового ряда можно отнести противопоказания к их назначению беременным и детям до 8 лет, высокую частоту побочных реакций со стороны желудочно-кишечного тракта, а также фотосенсибилизацию кожи во время их применения.
Макролиды, линкозамины, стрептограмины
Из препаратов группы макролидов, азалидов, линкозаминов и стрептограминов наиболее предпочтительны кларитромицин, джозамицин, азитромицин, мидекамицин и эритромицин.
Как уже упоминалось выше, наилучшие показатели МПК из всех макролидных антибиотиков имеет кларитромицин, обладающий всеми преимуществами современных антибиотиков, относящихся к этому классу: хорошей переносимостью, небольшой частотой побочных реакций и высоким комплайенсом.
Кларитромицин (клабакс, клацид) назначают по 250 мг 2 раза в сутки, а в пролонгированной форме СР по 500 мг 1 раз в сутки, в течение 7-14 дней.
Джозамицин (вильпрафен) по 500 мг 3 раза в сутки в течение 7-14 дней.
Азитромицин (азитрал, сумамед, хемомицин) назначают по 250 мг 1 раз в сутки в течение 6 дней или по 1 г однократно.
Мидекамицин (макроен)- по 400 мг 3 раза в сутки в течение 7-14 дней.
Эритромицин (эритромицин, эрифлюид) по 500 мг 4 раза в сутки 7-14 дней.
Рокситромицин (роксид, рокситромицин, рулид) по 150 мг 2 раза в сутки 7-14 дней.
Во время беременности нежелательно назначать азитромицин, рокситромицин, кларитромицин и мидекамицин. Для лечения беременных женщин с уреаплазменной инфекцией рекомендовано применять эритромицин внутрь по 500 мг каждые 6 ч в течение 7-10 дней. Показано, что после такого лечения уменьшаются угроза прерывания беременности, частота самопроизвольных абортов и явления многоводия.
Для лечения беременных рекомендован также джозамицин. Он обладает высокой эффективностью, не вызывая побочных реакций со стороны печени, не влияет на метаболизм других препаратов. При этом действие джозамицина на естественную бактериальную флору невелико.
При рождении детей, внутриутробно инфицированных уреаплазмами, также проводят терапию эритромицином. Предпочтительно внутривенное, капельное назначение препарата из расчета 20-40 мг на 1 кг массы тела.
Фторхинолоны
Все виды микоплазм высоко чувствительны к новым фторхинолонам, особенно офлоксацину. Его лидирующее положение в этой группе обусловлено широким антибактериальным спектром воздействия, высокой бактерицидной активностью, хорошими фармакокинетическими характеристиками (быстротой всасывания, высокими концентрациями препарата в тканях, клетках, биологических жидкостях), низкой токсичностью.
Офлоксацин (заноцин, офло, тарицин) назначают по 200 мг 2 раза в сутки в течение 7-10 дней, пефлоксацин - по 600 мг 1 раз в сутки в течение 7-10 дней, моксифлоксацин (авелокс) по 400 мг 1 раз в сутки в течение 10 дней.
Следует отметить, что исследования антибиотикочувствительности уреаплазм показывают частую их резистентность в клинической практике к офлоксацину и другим фторхинолонам.
Как и в случае с тетрациклинами, препараты этой группы нежелательно применять у беременных, они также вызывают фотосенсибилизацию.
Уреаплазмы среднечувствительны к аминогликозидам и левомицетину. Из аминогликозидов наиболее эффективен гентамицин, который назначают парентерально по 40 мг каждые 8 ч в течение 5 дней. Стрептомицин и канамицин при уреаплазменной инфекции практически неэффективны.
В последние годы как в нашей стране, так и за рубежом участились случаи выявления микоплазм, генетически резистентных к тетрациклину (до 40%), эритромицину, спирамицину (до 30%) и ципрофлоксацину.
Для выбора схемы адекватной терапии в конкретных случаях рекомендуется лабораторное определение чувствительности выделенных культур уреаплазм к различным антибиотикам. Однако многие авторы отмечают способность уреаплазм быстро приобретать устойчивость к антибактериальным препаратам при их пассировании in vitro. Следовательно, необходимо тестирование свежевыделенных от больных штаммов. Другая сложность состоит в том, что чувствительность к антибиотикам in vitro не обязательно коррелирует с положительным эффектом in vivo. Это может быть связано с фармакокинетикой препаратов. Анализ исследований, посвященных лечению уреаплазменной инфекции, показывает чрезвычайно большой разброс показателей эффективности различных антибиотиков - от 40 до 100%. В независимых исследованиях критерий эффективности того или иного антибиотика при уреаплазменной инфекции редко превышает 80%.
В ряде случаев этиотропная терапия может являться частью комбинированной терапии, в частности иммунотропной. В работе Hadson MMT et al. (1998) сообщается о важности иммунологического статуса больного при уреаплазменной инфекции. Так как антибиотики, активные в отношении уреаплазм, обладают бактериостатическим, а не бактерицидным действием, определяющую роль играет иммунный ответ больного. Использование иммунотропной терапии может быть особенно актуальным при неэффективности хотя бы одного курса противомикробного лечения.
Наши собственные исследования показали, что при выборе иммунотропной терапии особенно высокую эффективность демонстрировал препарат иммуномакс.
Этот препарат относится к группе иммуномодуляторов и показан для коррекции ослабленного иммунитета, лечения и профилактики вирусных и бактериальных инфекций.
Суммируя вышеизложенное, можно констатировать, что при лечении больных уреаплазменной инфекцией из всех антибиотиков следует отдавать предпочтение доксициклину из группы тетрациклинов, кларитромицину из группы макролидов, джозамицину - при беременности.
Наиболее удачной комбинацией при резистентных к стандартной этиотропной терапии случаях уреаплазменной инфекции, а также при рецидивирующем течении этой инфекции является применение антибиотиков в сочетании с иммунотропным лечением, что позволяет добиться элиминации возбудителя и избежать рецидивов инфекции.
М. А. Гомберг, доктор медицинских наук
А. М. Соловьев, кандидат медицинских наук
ЦИКВИ, МГМСУ, Москва
В 1954 г. Шепард впервые обнаружил U.urealyticum в выделениях, полученных от больного уретритом, и назвал их Т-микоплазмами (от английского слова tiny –крошечный). По своим размерам уреаплазмы являются одними из самых мелких представителей бактериальной флоры, выявляемой у человека, а по виду своей жизнедеятельности относятся к внутриклеточным паразитам.
Известны 2 биовара уреаплазм – Parvo и Т960, которые разделены на 14 сероваров. Последние достижения молекулярной биологии в исследовании ДНК и рибосомальной РНК уреаплазм позволили некоторым авторам (F. Kong et al., 2000) отказаться от классической классификации и разделить все уреаплазмы на 2 вида – Ureaplasma urealyticum (бывший биовар Т960) и Ureaplasma parvum (бывший биовар Parvo).
Как уже говорилось выше, вопрос о роли уреаплазм в этиологии и патогенезе заболеваний урогенитального тракта до сих пор не решен. Слишком уж широко они распространены, и слишком часто эти микроорганизмы выявляются у лиц, не имеющих клинической симптоматики. Авторы, относящие уреаплазмы к облигатным патогенам, считают, что они вызывают уретриты, цервициты, простатиты, послеродовые эндометриты, пиелонефриты, бесплодие, различную патологию беременности (хориоамниониты) и плода (легочную патологию). Другие исследователи полагают, что уреаплазмы являются частью условно-патогенной флоры урогенитального тракта, и способны вызывать инфекционно-воспалительные заболевания мочеполовых органов только при определенных условиях (в частности, при недостаточности иммунитета) или при соответствующих микробных ассоциациях.
Показатели инфицированности урогенитального тракта уреаплазмами среди сексуально активного населения варьируют от 10 до 80%. Уреаплазмы, как правило, обнаруживают у людей, ведущих активную половую жизнь, а наиболее часто эти микроорганизмы выявляются у лиц, имеющих три и более половых партнеров. По данным F. Kong et al., у 81-87% больных выявляется Ureaplasma parvum и у 13-19% - Ureaplasma urealyticum. Клиническая картина воспалительного процесса, при котором обнаруживаются уреаплазмы, не имеет патогномоничных симптомов.
Авторы некоторых работ утверждают, что именно уреаплазмы зачастую являются причиной неблагоприятных исходов беременности, усугубляют риск преждевременных родов и летального исхода при рождении детей с очень низкой массой тела.
Вопрос о влиянии уреаплазм на репродуктивную функцию человека остается открытым. Между тем женское бесплодие может быть связано с воспалительными процессами в области половых органов, индуцированными уреаплазмами, приводящими к нарушению прохождения яйцеклетки в полость матки. Мужское бесплодие может быть обусловлено, во-первых, воспалительными процессами, а во-вторых, – влиянием уреаплазм на сперматогенез. Адсорбция уреаплазм на поверхности сперматозоидов способна изменять их подвижность, морфологию и хромосомный аппарат.
Как и для большинства представителей условно-патогенной флоры, для уреаплазм выделяют ряд способствующих развитию инфекционно-воспалительных процессов факторов. Наиболее важными из них являются иммунные нарушения, изменения гормонального статуса, массивность колонизации, ассоциации с другими бактериями. Все эти аспекты следует учитывать при выборе тактики ведения таких больных.
Методы диагностики
1. Культуральное исследование на селективных средах. Такое исследование позволяет в течение 3-х дней выделить культуру возбудителя, и отделить уреаплазмы от других микоплазм. Материалами для исследования служат соскобы из урогенитального тракта и моча пациента. Метод позволяет определить чувствительность выделенных возбудителей к различным антибиотикам, что очень важно с учетом не редкой сегодня антибиотикорезистентности. Специфичность метода составляет 100%. Этот метод используется для одновременного выявления Mycoplasma hominis и Ureaplasma urealyticum
2. Обнаружение ДНК возбудителей методом ПЦР. Исследование позволяет в течение суток выявить возбудителя в соскобе из урогенитального тракта и определить его видовую принадлежность.
3. Серологические тесты. Позволяют определять присутствие антигенов и специфических антител к ним в крови. Могут быть полезны при рецидивирующем течении болезни, при развитии осложнений и бесплодии.
Как и проблема патогенности уреаплазм, вопрос о необходимости элиминации этих возбудителей из урогенитального тракта также остается открытым. Чаще всего авторы предлагают принимать меры по элиминации этих микроорганизмов при наличии у человека инфекционно-воспалительного процесса в месте их обнаружения (уретрите, простатите, цервиците, вагините), а также при бесплодии, невынашивании беременности, воспалительных заболеваниях органов малого таза, хориоамнионите, послеродовых лихорадочных состояниях при наличии уреаплазм в мочеполовом тракте.
Этиотропное лечение уреаплазменной инфекции основывается на применении антибактериальных препаратов различных групп. Активность препаратов в отношении любой инфекции определяется по минимальной подавляющей концентрации (МПК) в исследованиях in vitro. Показатели МПК, как правило, коррелируют с результатами клинического излечения. Казалось бы, оптимальными препаратами должны являться антибиотики с наименьшей МПК, но при этом нельзя сбрасывать со счетов важность таких параметров, как биодоступность, способность к созданию высоких внутритканевых и внутриклеточных концентраций, переносимость и комплаентность лечения.
Уреаплазмы устойчивы к беталактамным антибиотикам (пенициллинам и цефалоспоринам) из-за того, что у них отсутствует клеточная стенка, и сульфаниламидам, так как эти микроорганизмы не синтезируют кислоту. При лечении уреаплазменной инфекции, в принципе, могут быть эффективны те антибактериальные агенты, которые воздействуют на синтез белка и ДНК, то есть обладающие бактериостатическим действием. Это препараты тетрациклинового ряда, макролиды, фторхинолоны, аминогликозиды, левомицетин и некоторые другие (см. Таб. 1).
Таблица 1.
Чувствительность урепалазм к различным антибактериальным агентам (МПК в мкг/мл)
Урогенитальный хламидиоз - инфекционное заболевание, передаваемое половым путем Возбудитель – Сhlamydia trachomatis В странах Европы урогенитальная инфекция, вызванная C.trachomatis является самой распространенной ИППП*
* Европейское руководство по ИППП, 2004
Классификация урогенитального хламидиоза
- A56.0 Хламидийные инфекции нижних отделов мочеполового тракта
- A56.1 Хламидийные инфекции органов малого таза и других органов УГ системы
- A56.2 Хламидийная инфекция мочеполового тракта неуточненная
- A56.3 Хламидийная инфекция аноректальной области
- А56.4 Хламидийный фарингит
- A56.8 Хламидийные инфекции, передаваемые половым путем, другой локализации
- А74.9 Хламидийная инфекция неуточненная Эпидемиология урогенитального хламидиоза
В США ежегодно регистрируется свыше 600 000 больных урогенитальным хламидиозом.
В Великобритании распространенность хламидийной инфекции наиболее высока у 15-19 – летних женщин (800\100 тыс. населения),
В Швеции-1000\100 тыс. населения C.trachomatis выделяются у 12-60% женщин с воспалительными процессами слизистой оболочки шейки матки;
У 5-10% - при наличии симптомов уретрита;
У 20-70% при наличии ВЗОМТ.
Хламидии: репродуктивный цикл
Элементарные тельца (внеклеточная форма)
Ретикулярные тельца (внутриклеточная форма)
Клинические проявления урогенитального хламидиоза у женщин*
до 80% случаев протекают бессимптомно; приблизительно в 30% случаев отмечаются:
- Слизисто-гнойный цервицит
- Гнойные выделения из влагалища
- Боль внизу живота
- Кровоточивость после полового акта или между менструациями
- Дизурия Признаки ВЗОМТ, хронические тазовые боли
* Европейское руководство по ИППП
Этиология ВЗОМТ
с преобладанием возбудителей, передаваемых половым путем
- N.gonorrhoeae…………………(25-50%)
- C.trachomatis…………………..(25-47%)
- Анаэробно-аэробные ассоциации:
Bacteroides spp.,
Peptostreptococcus spp.,
G.vaginalis, Str.spp., E.coli ………. (25-60%) - M.hominis?, U.urealyticum ?
Клинические особенности хламидийной инфекции у женщин
- Одновременное (последовательное) инфицирование различных отделов УГТ
- Частое сочетание C.trachomatis с другими возбудителями: N.gonorrhoeae, ВПГ, ВПЧ, генитальными микоплазмами, БВ-ассоциированными микроорганизмами, грибами Candida.
Клинические проявления урогенитального хламидиоза у мужчин*
редко протекает бессимптомно – в 75% случаев отмечаются:
- Выделения из уретры
- Дизурия
- Диспареуния
- Признаки эпидидимита и/или простатита
Методы лабораторной идентификации C.trachomatis и их эффективность
| Культура клеток | 40-85% |
| Прямая иммунофлуоресценция (ПИФ) с использованием моноклональных антител | 50-90% |
| Полимеразная (лигазная) цепная реакция (ПЦР) | 98% |
| Иммуноферментый анализ (ИФА) | 20-85% |
| РНК-ДНК-гибридизация | 70-85% |
| Методы амплификации нуклеиновых кислот (МАНК) | 70-95% |
Кратность исследований
- До назначения лечения
- Через 4 недели после лечения
- Далее – по показаниям
Дополнительные исследования:
- Обследование на другие ИППП
- Определение антител ВИЧ, гепатиту В и С
- Клинический анализ крови и мочи
- Биохимический анализ крови и мочи
- УЗИ органов малого таза
- Консультации соответствующих специалистов
- Иммунный статус
- Кольпоскопия
- Цитологическое исследование слизистой оболочки шейки матки
- Уретроскопия
Предполагается значение генитальных микоплазм (данные литературы)
| возбудитель | Нозология |
| U.urealyticum M.hominis M.genitalium | ВЗОМТ; спонтанные аборты; пиелонефрит; послеродовый и послеабортный сепсис; бесплодие; рождение детей с низкой массой тела; хронические заболевания легких, пороки развития, перитонит, септический артрит, менингит, менингоэнцефалит, абсцесс мозга. |
Установлено клиническое значение генитальных микоплазм
| Возбудитель | Нозология |
| U.urealyticum | Цистит - женщины, Уретрит- мужчины |
| M.hominis | Бактериальный вагиноз |
| M.genitalium | Уретрит-мужчины |
Лабораторная идентификация
| C.trachomatis | Генитальные микоплазмы |
| ПИФ Культуральный метод Молекулярно-биологические (ДНК,PCR, LCR) | Методы, позволяющие осуществить видовую идентификацию и оценку количественного содержания |
| Real-time PCR | Real-time PCR |
| ИФА (IgJ, IgA,IgM) |
Урогенитальный хламидиоз. Критерии назначения терапии
- Подтвержденная лабораторно инфекция, вызванная (генитальная, экстрагенитальная – конъюнктивит, проктит, фарингит)
- Инфекция, вызванная C.trachomatis у полового партнера
- Отсутствие возможности провести лабораторное исследование на C.trachomatis у пациента с подтвержденной инфекцией, вызванной Neiseria gonorrhoeae
- Отсутствие возможности провести лабораторное исследование на C.trachomatis у пациента с клиническими признаками хламидийной инфекции
Урогенитальный хламидиоз: критерии эмпирической терапии.
- Наличие симптомов хламидийной инфекции
- В анамнезе половой контакт с больным хламидийной инфекцией
- Наличие уретрита или эпидидимита у мужчин
- Диагноз цервицита или воспалительных заболеваний органов малого таза (ВЗОМТ) у женщин
- Наличие у сексуального партнера цервицита, ВЗОМТ, уретрита, эпидидимита, хламидийной или гонококковой инфекции
- Сексуальное насилие
- Выявление гонококкового уретрита, цервицита или проктита (в популяциях с высокой частотой хламидийной инфекции)
Текущие рекомендации
- Рекомендации ВОЗ
- Рекомендации CDC (Center for Disease Control and Prevention, США)
- Европейское руководство по ИППП
Текущие рекомендации выделяют схемы терапии
| Рекомендуемые | Альтернативные |
| Обеспечение наилучшего соотношения между необходимой эффективностью и доказанной безопасностью применения | Обеспечение приемлемых результатов лечения при отсутствии возможности использования рекомендуемых схем в силу различных обстоятельств |
Лечение урогенитального хламидиоза
| ВОЗ | СДС | Европейские рекомендации |
| Доксициклин - по 100 мг перорально 2 раза в день - 7 дней; азитромицин - 1 г перорально однократно; Амоксициллин по 500 мг 3 раза в день - 7 дней; Эритромицин по 500 мг перорально 4 раза в день - 7 дней | Азитромицин 1 г перорально однократно; Доксициклин по 100 мг, 2 раза в день - 7 дней; Эритромицин - основание по 500 мг 4 раза в день -7дней; Эритромицин – этилсукцинат по 800 мг перорально 4 раза в день - 7 дней; Офлоксацин по 300 мг 2 раза в день – 7 дней; Левофлоксацин по 400 мг 1 раз в день - 7 дней | Азитромицин - 1 г перорально, однократно; Доксициклин по 100 мг, 2 раза в день внутрь - 7 дней; Эритромицин-основание по 500 мг 4 раза в день-7дней; Кларитромицин по 250 мг перорально, 2 раза в день - 7 дней Офлоксацин по 300 мг, 2 раза в день – 7 дней; Рокситромицин по 150 мг перорально, 2 раза в день - 7 дней; |
Терапия урогенитального хламидиоза
- Рекомендуемые схемы:
- Доксициклин - по 100 мг внутрь 2 раза в день в течение 7 дней
- Азитромицин - 1,0 внутрь однократно
- Кларитромицин - 250 мг 2 раза в сутки в течение 7 дней
- Эритромицин основание - 500 мг внутрь 4 раза в сутки в течение 7 дней
- Рокситромицин - 150 мг внутрь 2 раза в сутки в течение 7 дней
- Офлоксацин - 200 мг внутрь 2 раза в сутки в течение 7 дней
Макролиды
Макролиды (оказываемые эффекты)
Макролиды (механизм действия)
Блокада синтеза белка в рибосоме микробной клетки (М - точка приложения действия макролидов)
Сравнительная активность антибиотиков-макролидов in vitro, МИК 90, мкг/л1
| Штамм | джозамицин | азитромицин | кларитромицин | рокситромицин |
| Chlamydia trachomatis | 0.015 | 0.125 | 0.007 | 0.03 |
| Ureaplasma urealyticum | 1 | 1 | 1 | 1 |
Сравнительное изучение эффективности кларитромицина и доксициклина при лечении больных негонококковым уретритом/слизисто-гнойным цервицитом
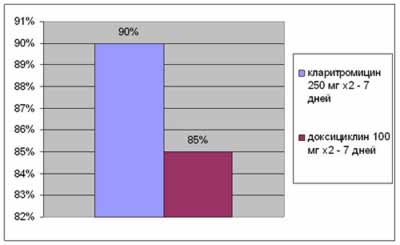
Сравнительный анализ эффективности азитромицина и кларитромицина при лечении больных хроническим простатитом у больных урогенитальным хламидиозом (n = 123)
| Микробиологическая эффективность | Клиническая эффективность | ||||
| Результат | Азитромицин 4,5 г3 недели | Кларитромицин 500 мг х2 – 15 дней | Результат | Азитромицин 4,5 г3 недели | Кларитромицин 500 мг х2 – 15 дней |
| Эрадикация | 68,75 | 66,77 | Излечение | 69,57 | 71,11 |
| Рецидив | 31,25 | 33,33 | Неуспех лечения | 30,43 | 28,85 |
Сравнительная чувствительность штаммов C.trachomatis к антибиотикам макролидам*
Препарат % чувствительных штаммов
Клацид - быстрый противовоспалительный эффект
Клацид блокирует процесс распространения инфекции уже в первые 2-4 часа после приема препарата, что обусловлено - быстрым захватом кларитромицина моноцитарными клетками с последующей активацией медиаторов моноцитов, вызывающих гибель бактерий (антибактериальный эффект in-vitro наступает только через 24 часа)
Клацид: иммуномодулирующий эффект
- Кларитромицин повышает активность клеток Т-киллеров
- Кларитромицин повышает количество Т-клеток, продуцирующих гамма-интерферон и интерлейкин 4
- Кларитромицин повышает количество Т-хелперов при иммуносупрессии вследствие химиотерапии опухолей в эксперименте, (является перспективным препаратом при адьювантной химиотерапии рака)
Это новая, уникальная упаковка, специально разработанная для лечения урогенитального хламидиоза обоих партнеров

500 мг х 1 раз в сутки – 7 дней
500 мг х 1 раз в сутки – 7 дней
Действующее вещество кларитромицин пролонгированного действия
Лекарственная форма таблетки 500 мг
Способ применения один раз в сутки
Количество таблеток в упаковке 2 х 7=14
Ведение половых партнеров
- Все партнеры, находившиеся в половом контакте с больным в течение 60 дней до установления диагноза подлежат обязательному обследованию и лечению
- Не рекомендуются сексуальные отношения в период лечения, а также диспансерного наблюдения (до установления контроля излеченности)
- Показано использование презерватива
Клацид® СР (кларитромицин) - Досье препарата
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем и подготовлено для печатного издания справочника Видаль 2021 года.
Владелец регистрационного удостоверения:
Произведено:
Контакты для обращений:
Лекарственные формы
Форма выпуска, упаковка и состав препарата Клацид ®
Таблетки, покрытые пленочной оболочкой желтого цвета, овальные, двояковыпуклые.
| 1 таб. | |
| кларитромицин | 250 мг |
Вспомогательные вещества: кроскармеллоза натрия - 35 мг, целлюлоза микрокристаллическая - 85 мг, крахмал прежелатинизированный - 65 мг, кремния диоксид - 7.2 мг, повидон (K29-32) - 20 мг, стеариновая кислота - 12.5 мг, магния стеарат - 7.5 мг, тальк - 17.5 мг, краситель хинолиновый желтый (E104) - 0.3 мг.
Состав пленочной оболочки: гипромеллоза - 13 мг, гипролоза (гидроксипропилцеллюлоза) - 1 мг, пропиленгликоль - 8.6 мг, сорбитана олеат - 1 мг, титана диоксид - 3 мг, сорбиновая кислота - 0.55 мг, ванилин - 0.55 мг, краситель хинолиновый желтый (E104) - 0.8 мг.
10 шт. - блистеры (1) - пачки картонные.
14 шт. - блистеры (1) - пачки картонные.
20 шт. - блистеры (1) - пачки картонные.
Таблетки, покрытые пленочной оболочкой светло-желтого цвета, овальные, двояковыпуклые.
| 1 таб. | |
| кларитромицин | 500 мг |
Вспомогательные вещества: кроскармеллоза натрия - 65.6 мг, целлюлоза микрокристаллическая - 183.9 мг, кремния диоксид - 12 мг, повидон (K29-32) - 25.5 мг, стеариновая кислота - 21 мг, магния стеарат - 12.6 мг, тальк - 29.4 мг.
Состав пленочной оболочки: гипромеллоза (гидроксипропилметилцеллюлоза) - 22.1 мг, гипролоза - 1.7 мг, пропиленгликоль - 14.62 мг, сорбитана олеат - 1.7 мг, титана диоксид - 5.1 мг, сорбиновая кислота - 0.94 мг, ванилин - 0.94 мг, краситель хинолиновый желтый (E104) - 0.07 мг.
7 шт. - блистеры (1) - пачки картонные.
7 шт. - блистеры (2) - пачки картонные.
7 шт. - блистеры (3) - пачки картонные.
10 шт. - блистеры (1) - пачки картонные.
10 шт. - блистеры (2) - пачки картонные.
10 шт. - блистеры (3) - пачки картонные.
14 шт. - блистеры (1) - пачки картонные.
14 шт. - блистеры (2) - пачки картонные.
14 шт. - блистеры (3) - пачки картонные.
Фармакологическое действие
Полусинтетический антибиотик группы макролидов. Оказывает антибактериальное действие, взаимодействуя с 50S рибосомальной субъединицей и подавляя синтез белка бактерий, чувствительных к нему.
Кларитромицин продемонстрировал высокую активность in vitro в отношении как стандартных лабораторных штаммов бактерий, так и выделенных у больных в ходе клинической практики. Проявляет высокую активность в отношении многих аэробных и анаэробных грамположительных и грамотрицательных микроорганизмов. Минимальные подавляющие концентрации (МПК) кларитромицина для большинства возбудителей меньше, чем МПК эритромицина в среднем на одно log 2 разведение.
Кларитромицин in vitro высоко активен в отношении Legionella pneumophila, Mycoplasma pneumoniae. Оказывает бактерицидное действие в отношении Helicobacter pylori; данная активность кларитромицина выше при нейтральном рН, чем при кислом.
Кроме того, данные in vitro и in vivo указывают на то, что кларитромицин действует на клинически значимые виды микобактерий. Enterobacteriaceae и Pseudomonas spp., также как и другие не ферментирующие лактозу грамотрицательные бактерии, не чувствительны к кларитромицину.
Активность кларитромицина в отношении большинства штаммов перечисленных ниже микроорганизмов доказана как in vitro, так и в клинической практике при заболеваниях, перечисленных в разделе "Показания".
Аэробные грамположительные микроорганизмы: Staphylococcus aureus, Streptococcus pneumoniae, Streptococcus pyogenes, Listeria monocytogenes; аэробные грамотрицательные микроорганизмы: Haemophilus influenzae, Haemophilus parainfluenzae, Moraxella catarrhalis, Neisseria gonorrhoeae, Legionella pneumophila; другие микроорганизмы: Mycoplasma pneumoniae, Chlamydia pneumoniae (TWAR), микобактерии: Mycobacterium leprae, Mycobacterium kansasii, Mycobacterium chelonae, Mycobacterium fortuitum, Mycobacterium avium complex (MAC) - комплекс, включающий Mycobacterium avium, Mycobacterium intracellulare.
Продукция β-лактамазы не оказывает влияния на активность кларитромицина.
Большинство штаммов стафилококков, резистентных к метициллину и оксациллину, обладают устойчивостью и к кларитромицину.
Чувствительность Helicobacter pylori к кларитромицину изучалась на изолятах Helicobacter pylori, выделенных от 104 пациентов, до начала терапии препаратом. У 4 пациентов были выделены резистентные к кларитромицину штаммы Helicobacter pylori, у 2 - штаммы с умеренной резистентностью, у остальных 98 пациентов изоляты Helicobacter pylori были чувствительны к кларитромицину.
Кларитромицин оказывает действие in vitro в отношении большинства штаммов перечисленных ниже микроорганизмов (однако безопасность и эффективность использования кларитромицина в клинической практике не подтверждена клиническими исследованиями, и практическое значение остается неясным).
Аэробные грамположительные микроорганизмы: Streptococcus agalactiae, стрептококки (группы C, F, G), стрептококки группы Viridans; аэробные грамотрицательные микроорганизмы: Bordetella pertussis, Pasteurella multocida; анаэробные грамположительные микроорганизмы: Clostridium perfringens, Peptococcus niger, Propionibacterium acnes; анаэробные грамотрицательные микроорганизмы: Bacteroides melaninogenicus; спирохеты: Borrelia burgdorferi, Treponema pallidum; кампилобактерии: Campylobacter jejuni.
Основным метаболитом кларитромицина в организме человека является микробиологически активный метаболит 14-гидроксикларитромицин (14-ОН-кларитромицин). Микробиологическая активность метаболита такая же, как у исходного вещества, или в 1-2 раза слабее в отношении большинства микроорганизмов. Исключение составляет Нaemophilus influenzae, в отношении которого эффективность метаболита в 2 раза выше. Исходное вещество и его основной метаболит оказывают либо аддитивный, либо синергический эффект в отношении Нaemophilus influenzae в условиях in vitro и in vivo в зависимости от штамма бактерий.
Тест на чувствительность
Количественные методы, требующие измерения диаметра зоны подавления роста, дают наиболее точные оценки чувствительности бактерий к антимикробным препаратам. Одна из рекомендуемых методик для определения чувствительности использует диски, импрегнированные 15 мкг кларитромицина (диско-диффузионный метод Кирби-Бауэра); при интерпретации теста диаметры зон подавления роста коррелируют со значениями МПК кларитромицина. Значения МПК определяются методом разведения в бульоне или в агаре.
При использовании этих методик, отчет из лаборатории о том, что штамм является "чувствительным", указывает на то, что возбудитель инфекции, вероятно, ответит на лечение. Ответ "резистентный" указывает на то, что возбудитель, возможно, не ответит на лечение. Ответ "промежуточная чувствительность" предполагает, что терапевтический эффект препарата может быть неоднозначен или микроорганизм может оказаться чувствительным при использовании более высоких доз препарата ("промежуточная чувствительность" также называется "умеренной чувствительностью").
Фармакокинетика
Препарат легко и быстро всасывается из ЖКТ. Абсолютная биодоступность составляет около 50%. При многократном приеме препарата кумуляции практически не обнаружено, и характер метаболизма в организме человека не изменялся. Прием пищи непосредственно перед приемом препарата увеличивал биодоступность препарата в среднем на 25%. В целом, это повышение незначительно и должно иметь небольшую клиническую значимость при рекомендуемых режимах дозирования. Таким образом, кларитромицин может применяться независимо от приема пищи.
Распределение , метаболизм, выведение
In vitro. Исследования in vitro показали, что кларитромицин связывается с белками плазмы крови на 70% в концентрации от 0.45 до 4.5 мкг/мл. При концентрации 45 мкг/мл связывание снижается до 41%, вероятно в результате насыщения мест связывания. Это наблюдается только при концентрациях, многократно превышающих терапевтическую.
In vivo. Исследования in vivo на животных показали, что кларитромицин присутствует во всех тканях, за исключением ЦНС, в концентрациях, в несколько раз превышающих плазменные. Наиболее высокие концентрации (в 10-20 раз выше плазменных) обнаруживались в печени и легких.
Здоровые. При назначении кларитромицина в дозе 250 мг 2 раза/сут максимальная равновесная концентрация (C max ) кларитромицина и 14-OH-кларитромицина в плазме достигались через 2-3 дня и составляли 1 мкг/мл и 0.6 мкг/мл соответственно. T 1/2 исходного препарата и его основного метаболита составляли соответственно 3-4 ч и 5-6 ч соответственно.
C max 14-OH-кларитромицина не увеличивалась пропорционально дозе кларитромицина, в то время как T 1/2 как кларитромицина, так и его гидроксилированного метаболита имел тенденцию к увеличению с повышением дозы. Такая нелинейная фармакокинетика кларитромицина в сочетании с уменьшением образования 14-гидроксилированных и N-деметилированных продуктов при применении в высоких дозах указывает на нелинейный метаболизм кларитромицина, который становится более выраженным при высоких дозах.
Почками выводится около 37.9% после перорального приема кларитромицина в дозе 250 мг и 46% после приема кларитромицина в дозе 1200 мг; кишечником выводится около 40.2% и 29.1% (включая испытуемого лишь с одной пробой кала, содержащей 14.1%) соответственно.
Пациенты. Кларитромицин и его метаболит 14-ОН-кларитромицин быстро проникают в ткани и жидкости организма. Имеются ограниченные данные, свидетельствующие о том, что концентрация кларитромицина в цереброспинальной жидкости при пероральном приеме незначительна (т.е. только 1-2% от концентрации в сыворотке крови при нормальной проницаемости гематоэнцефалического барьера (ГЭБ)). Концентрация в тканях обычно в несколько раз выше, чем в сыворотке крови.
В таблице приведены примеры тканевых и сывороточных концентраций:
| Концентрации (250 мг каждые 12 ч) | ||
| Вид ткани | Тканевая концентрация (мкг/г) | Сывороточная концентрация (мкг/мл) |
| Миндалины | 1.6 | 0.8 |
| Легкие | 8.8 | 1.7 |
Фармакокинетика в особых клинических случаях
Нарушения функции печени. У пациентов со средней и тяжелой степенью нарушения функции печени, но с сохраненной функцией почек коррекция дозы кларитромицина не требуется. Равновесная концентрация (C ss ) в плазме крови и системный клиренс кларитромицина не отличаются у пациентов данной группы и здоровых лиц. C ss 14-ОН-кларитромицина у людей с нарушениями функции печени ниже, чем у здоровых.
Нарушение функции почек. При нарушении функции почек увеличиваются C max и минимальная концентрация (C min ) кларитромицина в плазме крови, Т 1/2 , площадь под фармакокинетической кривой "концентрация-время" (AUC) кларитромицина и его метаболита 14-ОН-кларитромицина. Константа элиминации и выведение почками уменьшаются. Степень изменений этих параметров зависит от степени нарушения функции почек.
Пациенты пожилого возраста. У пациентов пожилого возраста концентрация кларитромицина и его метаболита 14-ОН- кларитромицина в крови была выше, а выведение медленнее, чем у группы молодых людей. Однако после коррекции с учетом почечного клиренса креатинина (КК) не было отличий в обеих группах. Таким образом, основное влияние на фармакокинетические параметры кларитромицина оказывает функция почек, а не возраст.
Пациенты с микобактериальными инфекциями. C ss кларитромицина и 14-ОН-кларитромицина у больных с ВИЧ-инфекцией, получавших кларитромицин в обычных дозах (500 мг 2 раза/сут), были сходными с таковыми у здоровых людей. Однако при применении кларитромицина в более высоких дозах, которые могут потребоваться для лечения микобактериальных инфекций, концентрации антибиотика могут значительно превышать обычные. У больных с ВИЧ-инфекцией, принимавших кларитромицин в дозе 1000 мг/сут или 2000 мг/сут в два приема, равновесные значения С max обычно составляли 2-4 мкг/мл и 5-10 мкг/мл соответственно. При применении препарата в более высоких дозах отмечалось удлинение Т 1/2 по сравнению с таковым у здоровых людей, получавших кларитромицин в обычных дозах. Повышение концентрации в плазме и удлинение Т 1/2 при применении кларитромицина в более высоких дозах связано с нелинейной фармакокинетикой препарата.
Комбинированное лечение с омепразолом. Кларитромицин, по 500 мг 3 раза/сут, в комбинации с омепразолом в дозе 40 мг/сут способствует увеличению Т 1/2 и AUC 0-24 омепразола. У всех пациентов, получавших комбинированную терапию, в сравнении с получавшими один омепразол, наблюдалось повышение на 89% AUC 0-24 и на 34% Т 1/2 омепразола. У кларитромицина С max , C min и AUC 0-8 увеличивались, соответственно, на 10%, 27% и 15% по сравнению с данными, когда применялся только кларитромицин без омепразола. В равновесном состоянии концентрации кларитромицина в слизистой желудка через 6 ч после приема в группе, получавшей комбинацию, в 25 раз превосходили таковые по сравнению с получавшими один кларитромицин. Концентрации кларитромицина в тканях желудка через 6 ч после приема двух препаратов в 2 раза превышали данные, полученные в группе пациентов, получавших один кларитромицин.
Показания препарата Клацид ®
Инфекционно-воспалительные заболевания, вызванные чувствительными к кларитромицину микроорганизмами, у взрослых и детей старше 12 лет:
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем и подготовлено для печатного издания справочника Видаль 2021 года.
Владелец регистрационного удостоверения:
Произведено:
Контакты для обращений:
Лекарственные формы
Гранулы д/пригот. сусп. д/приема внутрь 125 мг/5 мл: фл. 42.3 г или 70.7 г в компл. с дозир. ложкой или шприцем
Гранулы д/пригот. сусп. д/приема внутрь 250 мг/5 мл: фл. 49.5 г или 70.7 г в компл. с дозир. ложкой или шприцем
Форма выпуска, упаковка и состав препарата Клацид ®
Гранулы для приготовления суспензии для приема внутрь в виде гранулированного порошка от белого до светло-желтого цвета, с фруктовым ароматом; при встряхивании с водой образуется непрозрачная суспензия от белого до светло-желтого цвета, с фруктовым ароматом.
| 5 мл готовой сусп. | |
| кларитромицин | 125 мг |
Вспомогательные вещества: карбомер (карбопол 974P) - 75 мг, повидон К90 - 17.5 мг, кремния диоксид - 5 мг, мальтодекстрин - 285.7 мг, сахароза - 2748.3 мг, титана диоксид - 35.7 мг, камедь ксантановая - 3.8 мг, ароматизатор фруктовый - 35.7 мг, калия сорбат - 20 мг, лимонная кислота безводная - 4.2 мг, гипромеллозы фталат - 152.1 мг, масло касторовое - 16.1 мг.
42.3 г - флаконы пластиковые объемом 60 мл (1) с нанесенной меткой в виде линии, в комплекте с дозировочной ложкой или дозирующим шприцем - пачки картонные.
70.7 г - флаконы пластиковые объемом 100 мл (1) с нанесенной меткой в виде линии, в комплекте с дозировочной ложкой или дозирующим шприцем - пачки картонные.
Гранулы для приготовления суспензии для приема внутрь в виде гранулированного порошка от белого до светло-желтого цвета, с фруктовым ароматом; при встряхивании с водой образуется непрозрачная суспензия от белого до светло-желтого цвета, с фруктовым ароматом.
| 5 мл готовой сусп. | |
| кларитромицин | 250 мг |
Вспомогательные вещества: карбомер (карбопол 974P) - 150 мг, повидон К90 - 35 мг, кремния диоксид - 10 мг, мальтодекстрин - 238.1 мг, сахароза - 2276.2 мг, титана диоксид - 35.7 мг, камедь ксантановая - 3.8 мг, ароматизатор фруктовый - 35.7 мг, калия сорбат - 20 мг, лимонная кислота - 4.24 мг, гипромеллозы фталат - 304.2 мг, масло касторовое - 32.1 мг.
49.5 г - флаконы пластиковые объемом 70 мл (1) с нанесенной меткой в виде линии, в комплекте с дозировочной ложкой или дозирующим шприцем - пачки картонные.
70.7 г - флаконы пластиковые объемом 100 мл (1) с нанесенной меткой в виде линии, в комплекте с дозировочной ложкой или дозирующим шприцем - пачки картонные.
Фармакологическое действие
Полусинтетический антибиотик группы макролидов. Оказывает антибактериальное действие, взаимодействуя с 50S рибосомальной субъединицей бактерий и подавляя синтез белка, чувствительных к нему бактерий.
Кларитромицин продемонстрировал высокую активность in vitro в отношении как стандартных лабораторных штаммов бактерий, так и выделенных у больных в ходе клинической практики. Проявляет высокую активность в отношении многих аэробных и анаэробных грамположительных и грамотрицательных микроорганизмов. Минимальные подавляющие концентрации (МПК) кларитромицина для большинства возбудителей меньше, чем МПК эритромицина в среднем на одно log 2 разведение.
Кларитромицин in vitro высоко активен в отношении Legionella pneumophila и Mycoplasma pneumoniae. Оказывает бактерицидное действие в отношении Helicobacter pylori; данная активность кларитромицина выше при нейтральном рН, чем при кислом. Кроме того, данные in vitro и in vivo указывают на то, что кларитромицин действует на клинически значимые виды микобактерий. Enterobacteriaceae и Pseudomonas spp., также как и другие не ферментирующие лактозу грамотрицательные бактерии, не чувствительны к кларитромицину.
Активность кларитромицина в отношении большинства штаммов перечисленных ниже микроорганизмов доказана как in vitro, так и в клинической практике при заболеваниях, перечисленных в разделе "Показания".
Аэробные грамположительные микроорганизмы: Staphylococcus aureus, Streptococcus pneumoniae, Streptococcus pyogenes, Listeria monocytogenes; аэробные грамотрицательные микроорганизмы: Haemophilus influenzae, Haemophilus parainfluenzae, Moraxella catarrhalis, Neisseria gonorrhoeae, Legionella pneumophila; другие микроорганизмы: Mycoplasma pneumoniae, Chlamydia pneumoniae (TWAR), микобактерии: Mycobacterium leprae, Mycobacterium kansasii, Mycobacterium chelonae, Mycobacterium fortuitum, Mycobacterium avium complex (MAC) - комплекс, включающий Mycobacterium avium, Mycobacterium intracellulare.
Продукция β-лактамазы не оказывает влияния на активность кларитромицина.
Большинство штаммов стафилококков, резистентных к метициллину и оксациллину, обладают устойчивостью и к кларитромицину.
Чувствительность Helicobacter pylori к кларитромицину изучалась на изолятах Helicobacter pylori, выделенных от 104 пациентов, до начала терапии препаратом. У 4 пациентов были выделены резистентные к кларитромицину штаммы Helicobacter pylori, у 2 - штаммы с умеренной резистентностью, у остальных 98 пациентов изоляты Helicobacter pylori были чувствительны к кларитромицину.
Кларитромицин оказывает действие in vitro в отношении большинства штаммов перечисленных ниже микроорганизмов, однако безопасность и эффективность использования кларитромицина в клинической практике не подтверждена клиническими исследованиями, и практическое значение остается неясным.
Аэробные грамположительные микроорганизмы: Streptococcus agalactiae, стрептококки (группы C, F, G), стрептококки группы Viridans; аэробные грамотрицательные микроорганизмы: Bordetella pertussis, Pasteurella multocida; анаэробные грамположительные микроорганизмы: Clostridium perfringens, Peptococcus niger, Propionibacterium acnes; анаэробные грамотрицательные микроорганизмы: Bacteroides melaninogenicus; спирохеты: Borrelia burgdorferi, Treponema pallidum; кампилобактерии: Campylobacter jejuni.
Основным метаболитом кларитромицина в организме человека является микробиологически активный метаболит 14-гидроксикларитромицин (14-ОН-кларитромицин). Микробиологическая активность метаболита такая же, как у исходного вещества, или в 1-2 раза слабее в отношении большинства микроорганизмов. Исключение составляет Нaemophilus influenzae, в отношении которого эффективность метаболита в 2 раза выше. Исходное соединение и его основной метаболит оказывают либо аддитивный, либо синергический эффект в отношении Нaemophilus influenzae в условиях in vitro и in vivo в зависимости от штамма бактерий.
Тест на чувствительность
Количественные методы, требующие измерения диаметра зоны подавления роста, дают наиболее точные оценки чувствительности бактерий к антимикробным препаратам. Одна из рекомендуемых методик для определения чувствительности использует диски, импрегнированные 15 мкг кларитромицина (диско-диффузионный метод Кирби-Бауэра); при интерпретации теста диаметры зон подавления роста коррелируют со значениями МПК кларитромицина. Значения МПК определяются методом разведения в бульоне или в агаре.
При использовании этих методик, отчет из лаборатории о том, что штамм является "чувствительным", указывает на то, что возбудитель инфекции, вероятно, ответит на лечение. Ответ "резистентный" указывает на то, что возбудитель, возможно, не ответит на лечение. Ответ "промежуточная резистентность" предполагает, что терапевтический эффект препарата может быть неоднозначен или микроорганизм может оказаться чувствительным при использовании более высоких доз препарата ("промежуточная резистентность" также называется "умеренной резистентностью").
Фармакокинетика
Первые данные по фармакокинетике были получены при изучении таблеток кларитромицина. Препарат быстро всасывается из ЖКТ. Абсолютная биодоступность таблеток кларитромицина по 250 мг составляет примерно 50%. Пища несколько задерживала начало всасывания и образование активного метаболита 14-ОН-кларитромицина, однако не влияла на биодоступность препарата.
Распределение, метаболизм и выведение
В исследованиях in vitro связывание кларитромицина с белками плазмы составляло в среднем около 70% при клинически значимых концентрациях от 0.45 до 4.5 мкг/мл.
Здоровые. Биодоступность и фармакокинетику суспензии кларитромицина изучали у здоровых взрослых и детей. При однократном приеме у взрослых общая биодоступность суспензии была эквивалентной таковой для таблеток (в обоих случаях доза составляла 250 мг) или несколько превышала ее. Как и в случае таблеток, пища несколько задерживала всасывание суспензии кларитромицина, но не влияла на общую биодоступность препарата. Максимальная концентрация (C max ), площадь под кривой "концентрация-время" (AUC) и период полувыведения (T 1/2 ) кларитромицина при приеме детской суспензии (после еды) составляли 0.95 мкг/мл, 6.5 мкг×ч/мл и 3.7 ч соответственно, а при приеме таблетки 250 мг (натощак) - 1.10 мкг/мл, 6.3 мкг×ч/мл и 3.3 ч соответственно.
При приеме суспензии кларитромицина в дозе 250 мг каждые 12 ч у взрослых равновесные концентрации (C ss ) в крови достигались к приему пятой дозы. При этом параметры фармакокинетики были следующими: C max - 1.98 мкг/мл, AUC - 11.5 мкг×ч/мл, время достижения максимальной концентрации (T max ) - 2.8 ч и T 1/2 - 3.2 ч для кларитромицина и, соответственно, 0.67, 5.33, 2.9 и 4.9 для 14-ОН-кларитромицина.
У здоровых людей сывороточные концентрации достигали максимума в течение 2 ч после приема внутрь натощак. При приеме препарата в форме таблеток в дозе 250 мг каждые 12 ч пиковые равновесные концентрации кларитромицина в сыворотке крови достигались в течение 2-3 дней и составляли приблизительно 1 мкг/мл. Соответствующие пиковые концентрации для дозы 500 мг каждые 12 ч составляли от 2 мкг/мл до 3 мкг/мл.
Т 1/2 кларитромицина составлял 3-4 ч при приеме таблеток 250 мг каждые 12 ч, но возрастал до 5-7 ч после приема 500 мг каждые 12 ч. Равновесная C max основного метаболита, 14-ОН-кларитромицина, составляет около 0.6 мкг/мл, а Т 1/2 при приеме препарата в дозе 250 мг каждые 12 ч равен 5-6 ч. При приеме кларитромицина в дозе 500 мг каждые 12 ч равновесная C max 14-ОН-кларитромицина несколько выше (до 1 мкг/мл), а Т 1/2 составляет около 7 ч. При применении обеих доз равновесные концентрации метаболита обычно достигаются в течение 2-3 дней.
При применении кларитромицина в дозе 250 мг каждые 12 ч примерно 20% дозы выводится почками в неизмененном виде. При приеме кларитромицина в дозе 500 мг каждые 12 ч почками в неизмененном виде выводится примерно 30% дозы. Почечный клиренс кларитромицина существенно не зависит от дозы и примерно равен нормальной скорости клубочковой фильтрации. Основным метаболитом, определяемым в моче, является 14-ОН-кларитромицин, доля которого составляет 10-15% от дозы (250 или 500 мг каждые 12 ч).
Пациенты. Кларитромицин и его метаболит 14-ОН-кларитромицин быстро проникают в ткани и жидкости организма. Тканевые концентрации обычно в несколько раз выше сывороточных.
В таблице приведены примеры тканевых и сывороточных концентраций:
| Концентрации (250 мг каждые 12 ч) | ||
| Вид ткани | Тканевые (мкг/г) | Сывороточные (мкг/мл) |
| Миндалины | 1.6 | 0.8 |
| Легкие | 8.8 | 1.7 |
У детей, нуждавшихся в пероральном лечении антибиотиками, кларитромицин демонстрировал высокую биодоступность, при этом профиль его фармакокинетики был сходным с таковым у взрослых, принимавших ту же лекарственную форму. Препарат быстро и хорошо всасывается у детей. Пища несколько задерживает всасывание кларитромицина, однако не оказывает существенного влияния на его биодоступность или фармакокинетические свойства. Равновесные параметры фармакокинетики кларитромицина, достигнутые через 5 дней (девятая доза), были следующими: C max - 4.60 мкг/мл, AUC - 15.7 мкг×ч/мл и T max - 2.8 ч; соответствующие значения для метаболита 14-ОН-кларитромицина равнялись 1.64 мкг/мл, 6.69 мкг×ч/мл и 2.7 ч соответственно. Расчетные Т 1/2 кларитромицина и его метаболита равняются 2.2 и 4.3 ч соответственно.
У больных средним отитом через 2.5 ч после приема пятой дозы (7.5 мг/кг 2 раза/сут) средние концентрации кларитромицина и его метаболита в жидкости среднего уха составили 2.53 и 1.27 мкг/г. Концентрации препарата и его метаболита в 2 раза превосходили сывороточные концентрации.
Фармакокинетика в особых клинических случаях
Нарушение функции печени. C ss кларитромицина у пациентов с нарушением функции печени не отличаются от таковых у здоровых людей, в то время как концентрации 14-ОН-кларитромицина были ниже. Снижение образования 14-ОН-кларитромицина у пациентов с нарушением функции печени по крайней мере частично нивелировалось увеличением почечного клиренса кларитромицина по сравнению с таковым у здоровых людей.
Нарушение функции почек. Фармакокинетика кларитромицина изменялась также у пациентов с нарушением функции почек, получавших препарат в повторных дозах по 500 мг. У таких больных концентрации в плазме, Т 1/2 , C max , C min и AUC кларитромицина и его метаболита были выше, чем у здоровых людей. Отклонения этих параметров коррелировали со степенью почечной недостаточности: при более выраженном нарушении функции почек различия были более значительными.
Пациенты пожилого возраста. У пациентов пожилого возраста концентрация кларитромицина и его метаболита 14-ОН-кларитромицина в крови была выше, а выведение медленнее, чем у группы молодых людей (при приеме кларитромицина в повторных дозах по 500 мг). Однако после коррекции результатов с учетом почечного клиренса креатинина (KK) не было отличий в обеих группах. Таким образом, основное влияние на фармакокинетические параметры кларитромицина оказывает функция почек, а не возраст.
Пациенты с микобактериальными инфекциями. C ss кларитромицина и 14-ОН-кларитромицина у больных с ВИЧ-инфекцией, получавших кларитромицин в обычных дозах (таблетки для взрослых, суспензия для детей), были сходными с таковыми у здоровых людей. Однако при приеме кларитромицина в более высоких дозах, которые могут потребоваться для лечения микобактериальных инфекций, концентрации антибиотика могут значительно превышать обычные.
У детей с ВИЧ-инфекцией, принимавших кларитромицин в дозе 15-30 мг/кг/сут в два приема, равновесные значения C max обычно составляли от 8 до 20 мкг/мл. Однако у детей с ВИЧ-инфекцией, получавших суспензию кларитромицина в дозе 30 мг/кг/сут в два приема, C max достигала 23 мкг/мл. При приеме препарата в более высоких дозах отмечалось удлинение Т 1/2 по сравнению с таковым у здоровых людей, получавших кларитромицин в обычных дозах. Повышение концентрации в плазме и удлинение Т 1/2 при применении кларитромицина в более высоких дозах связано с нелинейной фармакокинетикой препарата.
Показания препарата Клацид ®
Инфекционно-воспалительные заболевания, вызванные чувствительными к кларитромицину микроорганизмами:
Читайте также:

