Классификация лепры по ридли
Обновлено: 23.04.2024
• Этиология лепры
• Эпидемиология лепры
• Классификация лепры
• Лепроматозный тип лепры
• Туберкулоидный тип лепры
• Недифференцированный тип лепры
• Диагностика лепры
• Лечение лепры
• Профилактика лепры
Лепра (lepra) - хроническое
инфекционное заболевание,
вызываемое микобактериями лепры,
характеризующееся гранулематозным
поражением кожи, слизистых верхних
дыхательных путей и периферической
нервной системы, а при
несвоевременной диагностике –
вовлечением в процесс костномышечного аппарата, органов зрения и
внутренних органов.
4. Распространение лепры в мире
5. Распространение лепры а мире
Наиболее распространена лепра в странах
Азии, Африки и Южной Америки (Индия,
Нигерия, Бразилия, Индонезия, Вьетнам,
Бангладеш ). В США и странах Европы
спородические случаи лепры выявляются у
иммигрантов из эндемичных районов. В России
и Странах СНГ эндемические очаги лепры
существуют в Каракалпакии, Казахстане,
Нижнем Поволжье, на Северном Кавказе,
Дальнем Востоке, в Прибалтике.
6. Этиология
Возбудителем лепры является бацилла,
открытая в 1871 г. норвежским врачом G.
Hansen семейства Mycobacteriacea,
названная Mycobacterium Leprae hominis.
Бацилла лепры представляет собой
граммположительную спирто- и
кислотоустойчивую палочку,
окрашивающуюся по Цилю-Нильсену,
Эрлиху и анилиновыми красителями
7. Микобактерии лепры в слизистой оболочке носа
8. Классификация
По современной классификации
(классификация Ридли-Джоплинга, 1966)
выделяют следующие клинические формы
лепры:
ТТп – полярный туберкулоидный тип лепры;
ТТс – субполярная туберкулоидная форма;
ПТ – погранично-туберкулоидная форма;
ПП – пограничная форма;
ПЛ – погранично-лепроматозная форма;
ЛЛс – субполярная лепроматозная форма;
ЛЛп – полярный лепроматозный тип лепры;
Н – недифференцированная форма лепры.
В практической деятельности разделяют
три типа лепры:
•Лепроматозный
•Туберкулоидный
•Недифференцированный (пограничный)
В течении каждого из типов лепры
возможны 4 стадии: прогрессирующая,
стационарная, регрессивная и остаточных
явлений
10. Лепроматозный тип лепры
При лепроматозном типе лепры вначале на коже
появляются нерезко очерченные, малозаметные
красноватые пятна с фиолетовым или вишневым
оттенком. Чувствительность (болевая, температурная,
тактильная) в области этих пятен вначале не
нарушается. Постепенно пятна становятся плотными.
Часто образуются мощные инфильтраты. В процесс
наряду с собственно кожей вовлекается и подкожная
жировая клетчатка, образуются узлы (лепромы). Такие
инфильтраты и узлы чаще всего располагаются на
разгибательной поверхности конечностей, на лице в
области лба, надбровных дуг, щек, носа. Мимика лица
нарушается, либо обезображивается, принимая
"свирепое" выражение ("морда льва" - fades leonina).
11. Лепроматозный тип лепры. Лепромы на коже лица
12. Лепроматозный тип лепры. Лепромы на коже лица
13. Лепроматозный тип лепры. Лепромы на коже уха.
14. Лепроматозный тип лепры
15. Лепроматозный тип лепры
16. Лепроматозный тип лепры. Лепромы на коже конечности
17. Лепроматозный тип лепры. Лепромы на коже конечности
18. Лепроматозный тип лепры. Контрактура пальцев кисти и мутиляция пальцев.
21. Лепроматозный тип лепры. Мутиляция пальцев стоп
22. Лепроматозный тип лепры.Огромные инфильтраты кожи (активная стадия).
23. Туберкулоидный тип лепры
Туберкулоидный тип лепры характеризуется
значительно более доброкачественным течением.
Главным образом поражены кожные покровы,
периферические нервы. На коже появляются резко
очерченные депигментированные витилигоподобные
пятна или яркие, с четкими границами красноватозастойного цвета с центральным побледнением пятна,
по периферии которых в виде своеобразного бордюра
располагаются напоминающие красный плоский лишай
полигональные, плоские и плотные папулы с
фиолетвым оттенком. Сливающиеся папулы образуют
красновао-фиолетового или красновато-бурого цвета,
различные по величине плоские бляшки, местами
имеющие кольцевидную конфигурацию. В центральной
части таких бляшек постепенно развиваются
депигментация и атрофия.
24. Ранний туберкулоидный элемент с приподнятым краем(бордюром).
25. Пятно с регрессом в центре и с отсутствием чувствительности.
26. Крупный туберкулоидный элемент с чётко выраженным бордюром.
27. Крупный туберкулоидный элемент с чётко выраженным бордюром.
28. Туберкулоидный тип лепры. Поражение кожи.
29. Туберкулоидный тип лепры. Поражение кожи.
30. Туберкулоидный тип лепры
31. Туберкулоидный тип лепры
32. Туберкулоидный тип лепры
33. Туберкулоидный тип лепры
34. Недифференцированный тип лепры.
Недифференцированный тип лепры характеризуется
отсутствием типичных высыпаний.
Небольшое число неярких пятен с нерезкими
границами, различной величины и очертаний
затрудняет диагностику. Выявить палочку Ганзена у
таких больных удается редко. Патологическая картина
проявляется банальным неспецифическим
инфильтратом, подобным тому, который может быть
при различных хронических дерматозах. Лепрозные
палочки в таком инфильтрате чаще всего не
обнаруживаются. Эти больные малоконтагиозны, их
общее состояние и самочувствие, как правило,
хорошие.
35. Недифференцированная лепра. Поражение лица.
36. Недифференцированная форма лепры. Диффузная инфильтрация кожи лица и ушной раковины.
37. Диагностика
К основным признакам, определяющим лепру,
относятся следующие:
•Характерные проявления на кожном покрове;
•Утолщение пораженных периферических
нервов;
•Нарушение различных видов
чувствительности кожи;
•Наличие кислоустойчивых микобактерий
в
мазках
из
скарификатов кожи и соскобов слизистой
носа, а также в
тканевых срезах биоптата кожных поражений.
38. Скопления микробактерий лепры в виде шаров в носовой слизи.
39. Единичные микробактерии лепры и их скопления в виде сигарных палочек в тканевом соке.
40. Микробактерии лепры в слизистой оболочке носа.
41. Лепроминовая реакция (реакция Митсуда)
Для получения этой реакции в сгибательную
поверхность предплечья внутрикожно вводят 0,1 мл
лепромина ( антиген, представляющий собой взвесь
убитых автоклавированием микобактерий лепры в
физиологическом растворе с добавлением 0,5%
фенола) Реакция может быть ранней, если через 24-48
ч после внутрикожного введения лепромина появляется
гиперемия и отечность. Поздняя, или замедленная,
положительная реакция характеризуется образованием
на месте введенного лепромина через 2-4 нед. бугорка
размером до 1-1,5, склонного к изъязвлению. Поздняя
положительная реакция имеет хорошее
прогностическое значение. Ранняя и особенно
отрицательная реакция на лепромин имеют
неблагоприятное прогностическое значение, так как
отражают состояние анергии и слабость
иммунобиологических, защитных сил организма.
42. Лепроминовая реакция при различных типах лепры
• Лепроматозный тип – отрицательная
лепроминовая реакция
• Туберкулоидный тип – положительная,
замедленная лепроминовая реакция
• Недифференцированный тип – при
отрицательной лепроминовой реакции
возможна трансформация в
лепроматозную форму лепры. При
положительной лепроминовой реакции
– в туберкулоидную форму.
43. Дифференциальная диагностика лепры
44. Витилиго
45. Микоз гладкой кожи
46. Лейшманиоз
47. Красный плоский лишай
48. Лечение лепры
Лечение проводится комплексным хроническим
перемежающимся методом. Выбор того или иного
препарата и определение его дозы осуществляется
индивидуально. Основными противолепрозными
средствами как у нас в стране, так и за рубежом
являются сульфоновые препараты : ДДС
(диаминодифенилсульфон), авлосульфон, сульфатин
(сульфон-3), сульфетрон (солюсульфон), дапсон,
диуцифон, димоцифон, лепросан и др. В дополнение к
ним используют производные тиомочевины - Сиба-1906
(тиокарбонилид), рифампицин, клофазимин В-633,
лампрен, протионамид, этионамид. Возможно
назначение следующей комбинации препаратов: дапсон
+ рифампицин + лампрен в течение 6-24 месяцев.
49. Профилактика лепры
Согласно существующему в РФ законодательству, при
выявлении больного лепрой срочно заполняется
"экстренное извещение" (форма № 58), которое врач
отсылает в местные органы санитарной службы,
обеспечивающие и контролирующие госпитализацию
больного и первичное обследование всех лиц,
находящихся с ним в контакте. Все члены семьи
обследуются не реже 1 раза в год. Новорожденные
немедленно отделяются от больных матерей и
переводятся на искусственное вскармливание, а более
взрослые дети допускаются к учебе в общих школах
при условии их клинико-лабораторного обследования
не реже 2 раз в год. В местах, эндемичных по лепре,
проводят массовое обследование населения. Лицам,
находившимся в контакте с больными, проводят
лепроминовую пробу – внутрикожное введение
лепроминоавтоклавированной взвеси микобактерий
лепры.
Лицам, имеющим отрицательный результат
лепроминовой пробы проводится обследование
и активная иммунопрофилактика путем
повторного введения вакцины БЦЖ.
Иммунопрофилактика (иммунизация) населения
вакциной БЦЖ показана в местности с
относительно частой заболеваемостью лепрой.
Члены семьи больного подвергаются
превентивному лечению с учетом результатов
лепроминовой пробы. Превентивное лечение
назначается членам семьи, где выявлен
больной лепроматозным и диморфным типом
лепры, если у больного в соскобах со слизистой
носа или в скарификатах высыпаний на коже
были обнаружены микобактерии лепры.
Химиопрофилактика ограничивается одним курсом
сульфонотерапии (6 мес) препаратами ДДС,
авлосульфон, сульфетрон) если больной был
своевременно выявлен и изолирован, т.е. контакт
был кратковременным. Если же контакт был
длительным, то проводится 2 курса превентивного
лечения, во время которого ежемесячно
проводится лабораторный контроль.
Периодические врачебные осмотры и при
необходимости лабораторные исследования лиц,
длительно находившихся в тесном контакте с
больным лепрой проводятся на протяжении 20 лет
после госпитализации больных. Первые 10 лет – не
реже 1 раза в год, последние 10 лет – 1 раз в 2
года.
Больным лепрой не разрешается работать в
пищевой промышленности и детских
учреждениях. Согласно
международному соглашению, запрещен
переезд больных лепрой из одной страны
в другую. Личная профилактика лепры у
лиц, по роду своей деятельности
контактирующих с больными,
заключается в строгом соблюдении
элементарных санитарно-гигиеничесикх
правил (частое мытье рук мылом,
обязятельная санация микротравм.
Лепра представляет собой хроническое генерализованное инфекционное заболевание, при котором поражаются преимущественно производные эктодермы (кожа, слизистые оболочки и периферическая нервная система), лимфатические узлы, печень, селезенка, кости, эндокринные железы (при лепроматозном типе). На земном шаре насчитывается около 15 млн. больных лепрой. Основные ее очаги находятся в юго-восточной Азии (Индия, Бирма, Таиланд и др.), Африке, на островах Океании (Сулавеси, Филиппинские, Гавайские острова и др.), в Индонезии, Центральной и Южной Америке. В Европе лепра встречается в Португалии, Испании, Греции, Италии, Франции и т. д. Небольшие очаги ее имеются в Средней Азии, на Дальнем Востоке, в низовьях Волги (Астраханская область), Дона, в Закавказье. В прошлом лепра как единичные казуистические случаи иногда выявлялась в прибалтийских республиках и в Беларуси. В нашей стране она не представляет ни социальную, ни медицинскую проблему.
Возбудителем лепры является кислото- и спиртоустойчивая палочка Mycobacterium leprae, описанная норвежским ученым Г. Хансеном в 1874 г. и впоследствии названная его именем. Однако культура ее до сих пор не получена.
Единственным источником заражения служит больной человек. Особенно восприимчивы к лепре дети. Предполагается, что в результате длительного контакта с больным лепрой у здорового человека постепенно происходит сенсибилизация к бациллам Хансена вследствие их многократного проникновения в организм. Вместе с тем следует отметить, что человек обладает естественной резистентностью к лепре. Однако ею можно заразиться при снижении защитных сил организма, что могут обусловить плохие социально-экономические условия, низкий санитарно-гигиенический уровень, высокая температура и влажность воздуха, простудные заболевания, гиповитаминозы, алкоголизм, беременность, роды, повреждения кожи, слизистых оболочек и т. д. В таком случае при длительном контакте с больным возможно заражение лепрой. Оно происходит в основном аэрогенно-капельным путем, через верхние дыхательные пути или через поврежденную кожу. Существует мнение, что лепра может распространяться и кровососущими насекомыми. Имеются данные, что микобактерии лепры могут проникать в слизистую ребенка с молоком больной кормящей матери. Установлено, что микобактерии лепры могут длительное время сохранять жизнеспособность, находясь вне организма человека. Это в определенной мере проясняет проблему эпидемиологии ряда случаев заболевания лепрой.
Степень передачи инфекции (заразительность) значительно выше уровня регистрируемой заболеваемости (интенсивность передачи возбудителя), т. е. эффективная заражаемость, или инфицированность, намного выше уровня клинической заболеваемости и болезненности, что объясняется высокой резистентностью человека к лепрозной инфекции.
Больные в субклинической стадии заболевания (в ряде случаев лепра длительно протекает в форме скрытой инфекции, без проявления клинических симптомов) могут быть бациллоносителями и служить источником заражения.
Некоторые успехи в области эпидемиологии, патогенеза и терапии лепры были достигнуты, когда экспериментально удалось добиться локального размножения микобактерии лепры после их введения в мякоть подошвы лапки мышей (S. Shepard, 1960) и заразить лепрой (путем внутривенного введения ее возбудителей) девятипоясного (W. Kirchheimer, E. Storrs, 1971) и восьми-поясного (Convit et al., 1978) броненосцев.
Согласно классификации Ридли — Джоплинга (1966), заболевание лепрой рассматривается как непрерывный иммунологический процесс. При этом туберкулоидный (ТТ) и лепроматозный (LL) типы лепры относятся к полярным группам и выделяются три промежуточные (пограничные) группы: погранично-туберкулоидная (ВТ); пограничная (ВВ) и погранично-лепроматозная (BL). Кроме того, выделяются две дополнительные группы: субполярный лепроматоз (LLS), недифференцированная лепра (I). В данную классификацию не укладываются стертые и атипичные разновидности (формы) лепроматозного типа лепры: лепра Лусио и гистоидная лепра.
В СНГ различают три типа лепры: лепроматозный, туберкулоидный и недифференцированный.
Комитет экспертов ВОЗ (1967) рекомендует медицинскому персоналу при работе в полевых условиях все случаи заболевания лепрой относить к лепроматозному, туберкулоидному или недифференцированному типу. Причем к первому (лепроматозному) типу следует относить заболевания, при которых бактериоскопические исследования дают положительные результаты, а также пограничную форму (недифференцированный тип); ко второму (туберкулоидному) типу — заболевания, при которых возбудитель не выявляется.
При определении типа лепры учитывают ее клинические проявления, результаты лепроминовой пробы, клеточную структуру очагов поражения, плотность популяций микобактерии в гистологических препаратах, количество лимфоцитов в гранулеме и их расположение, а также расположение последней по отношению к эпидермису, состояние периферических нервов кожи.
Инкубационный период лепры длится от 3—5 до 30 лет и более. Ее клиническая картина определяется степенью естественной резистентности организма, которая может быть установлена с помощью лепроминовой пробы (реакция Мицуды). Различают четыре стадии развития заболевания — прогрессирующую, стационарную, регрессирующую и резидуальную.
Диагностика.
Важное место в диагностике занимает микроскопия билптатов из патологического очага.
Заболевание лепроматозного типа развивается при резком снижении защитных сил организма. Его характерным признаком является специфическая гранулема с многочисленными бациллами Хансена, упакованными наподобие сигарет в пачке в пенистой цитоплазме крупных лепрозных клеток. Реакция Мицуды при лепроматозном типе всегда отрицательная.
Туберкулоидпый тип лепры развивается при более высокой резистентности организма. Его характерным признаком является типичная, но не специфическая туберкулоидная гранулема. Бациллы Хансена в небольшом количестве могут быть обнаружены в высыпаниях только в период обострения процесса. При туберкулоидном типе лепроминовая проба дает положительный результат.
При недифференцированном типе лепры развивается неспецифическое хроническое воспаление. Бацилл Хансена в инфильтрате очень мало, и обнаруживаются они крайне редко. Лепроминовая проба положительна примерно в 50 % случаев.
Гистопатологическими исследованиями очагов поражения лепроматозного типа обнаруживаются специфические гранулемы. В них располагаются крупные лепрозные клетки, отличающиеся пенистой цитоплазмой, которая содержит много микобактерий и липоидных включений. Инфильтрат лепромы отделяется от эпидермиса зоной неизмененной соединительной ткани, состоит из гистиоцитов, эпителиоидных клеток, лимфоцитов, единичных плазматических клеток и включает большое количество микобактерий.
При туберкулоидном типе лепры гранулема состоит из большого числа эпителиоидных клеток, сосредоточивающихся в ее центральной части. Они окружены по периферии валиком из лимфоцитов. В гранулеме обнаруживаются и гигантские многоядерные клетки типа клеток Лангханса, единичные плазматические и тучные клетки, фиброциты, немногочисленные микобактерий.
Морфологическая картина очагов поражения недифференцированного типа лепры характеризуется наличием банального хронического воспаления верхней трети дермы. Инфильтрат при этом обычно располагается периневрально и состоит из лимфоцитов, фибробластов и гистиоцитов. Микобактерий Хансена в нем очень мало, и обнаруживаются они исключительно редко (только в пораженных нервах).
Для постановки диагноза лепры важно установить факт пребывания обследуемого в эндемичном очаге и выявить характерные для нее клинические проявления. Большое значение имеют дополнительные исследования подозрительных высыпаний (определение их температурной, болевой, тактильной чувствительности), а также результаты фармакодинамических проб с гистамином, морфином или дионином. С этой целью по одной капле 0,1 % водного раствора гистамина (либо 1 % раствора морфина или 2 % раствора дионина) наносят на исследуемый подозрительный в отношении лепры участок кожи и на внешне непораженную кожу. Через капли делают поверхностный укол или лег- кую царапину. У здоровых людей на месте укола ограниченная эритема через 1—2 мин сменяется рефлекторной эритемой диаметром в несколько сантиметров, а еще через несколько минут в ее центре возникает волдырь (триада Льюиса). Рефлекторная эритема на поражениях лепрозной этиологии не развивается или выражена очень слабо.
Значительную диагностическую ценность для распознавания высыпаний при лепре имеет проба с горчичником. При наличии гипопигментных пятен на них накладывают по обычной методике горчичник, захватывая и здоровый участок кожи. На пятне лепрозной этиологии эритема в таких случаях не возникает или бывает весьма слабее, чем на непораженной коже.
Проба Минора: исследуемый участок кожи смазывают 2— 5 % раствором йода и после его высыхания посыпают крахмалом; стимулируют потоотделение (обследуемого помещают в суховоздушную ванну или дают ему выпить несколько стаканов горячего чаю). В результате кожа с неугнетенным потоотделением окрашивается в синий цвет, на лепрозных поражениях синяя окраска не появляется (сохраняется желтый цвет кожи, окрашенной раствором йода).
Для подтверждения диагноза лепры рекомендуется обязательно исследовать мазки соскобов слизистой оболочки обеих сторон перегородки носа, а также соскобов поверхностей неглубокого надреза лепромы, мазки из скарификатов надбровных дуг, мочек ушных раковин, подбородка, кончиков пальцев (на наличие микобактерий Хансена; окраска методом Циля — Нильсена)
Для диагностических целей проводится также гистологическое исследование биоптатов явных лепром и подозреваемых на лепрозное поражение участков кожи. При этом часть срезов также окрашивают по Цилю — Нильсену.
Лепра (1ерга) — хроническое инфекционное заболевание, характеризующееся длительным инкубационным периодом, торпидным, затяжным течением с периодическими обострениями (лепролгыс реакции). Болезнь представляет собой системный процесс с поражением кожи, слизистых оболочек, нервно-эндокринной системы и внутренних органов.
Если этиология лепры известна, то патогенез болезни, ее эпидемиология, условия заражения и распространения изучены далеко не полностью.
Эпидемиология. Основное значение имеют социально-экономические факторы, чем и объясняется особенно широкое распространение заболевания среди беднейшего населения стран Азии.
Человек заражается от больного в результате длительного контакта, которому должна сопутствовать сенсибилизация, прогрессирующая повторных инокуляциях. Особенно велика опасность инфицирования детском возрасте, большую степень риска имеют дети, склонные к аллергическим заболеваниям. Микобактерии лепры, выделяются из организма больного через слизистые оболочки дыхательных путей или из изъязвившихся лепром. Много микобактерий лепры содержится в носовой слизи и отделяемом слизистых оболочек глотки, гортани. Один больной даже при спокойном разговоре за 10 мин. может рассеять огромное количество лепрозн. палочек в радиусе 1—1,5 м. Содержатся в слезах, моче, сперме, выделениях из уретры, грудном молоке даже крови в периоды реактивации лепрозного процесса.
Отсутствуют данные о внутриутробном заражении плода.
По отношению к лепрозной инфекции имеется высокая естественная резистентность. Этим объясняется, что не все лица, имеющие даже длительный контакт с лепрозными больными, заболевают, а у отдельных людей лепра протекает в форме скрытой инфекции. При этом у лиц, имевших длительный контакт с лепрозными больными, можно обнаружить микобактерии лепры в пунктате лимфатических узлов или даже повторно находить их в соскобе со слизистой оболочки полости носа при отсутствии каких-либо признаков заболевания. Но в то же время разнообразные факторы, ослабляющие сопротивляемость организма (недостаточное и неполноценное питание, алкоголизм, простуды, тяжелые физические нагрузки), способствуют заражению или переходу процесса из латентной в активную форму. Учитывая возможность более частого травмирования кожи нижних конечностей, полагают, что инфицирование в основном происходит через кожные покровы нижних конечностей. Это предположение основывается на частом обнаружении микобактерии лепры в увеличенных бедренных лимфатических узлах в начальном периоде болезни. В этом случае патогенетическое значение придается нарушению микроциркуляции, варикозному синдрому и микозам стоп — особенно эпидермофитии и кандидозам.
Инкубационный период в среднем длится от 4 до 6 лет. Однако достаточно достоверно установлена возможность инкубации как в течение 2—3 мес., так и от 10 - 20 до 50 лет. Следовательно, для лепры характерны длительность и значительные колебания сроков инкубационного периода.
Лепру считают малоконтагиозным заболеванием, она менее заразна, чем туберкулез. Дети намного чувствительнее, чем взрослые, и в условиях длительного контакта у них быстрее и значительно чаще наступает заражение лепрой.
Клиника: жалобы больных на недомогание, сильные невралгические боли, болезненность в суставах, нарастающую слабость, желудочно-кишечные расстройства. Иногда отмечают парестезии, гиперестезии, лихорадку. Уже в этот период на слизистой оболочке перегородки носа можно обнаружить палочки Ганзена. В дальнейшем развиваются клинические симптомы болезни, в зависимости от морфологических проявлений которой различают три типа заболевания.
Классификация. По принятой в 1953 г. мадридской классификации выделяют 2 полярных типа лепры: лепраматозный и туберкулоидный и 2 промежуточные группы: недифференцированная и пограничная (диморфная). Современная классификация, развивающая по сути мадридскую, отражает иммунологическую реактивность и данные иммунобиологических, гистопатологических, бактериоскопнческих исследований. В практической деятельности различают следующие 3 типа лепры; лепроматозный, туберкулоидный, недифференцированный или пограничный. В течении каждого из этих типов лепры возможны 4 стадии: прогрессирующая, стационарная, регрессивная и остаточных явлений. В прогрессирующей и стационарной стадиях даже при проведении рациональной терапии наблюдаются лепрозные реакции, проявляющиеся обострением основных очагов болезни и полиморфными вторичными аллергическими высыпаниями. Формирование типа лепры зависит от степени иммунобиологической резистентности организма больного. У лиц с явлениями астенизации, иммунодефицита, сопровождающимися отрицательной лепроминовой пробой, чаще всего развивается наиболее контагиозный тип лепры — лепроматозный. У лиц с высокой иммунологической реактивностью, проявляющейся положительной лепроминовой пробой, наблюдается сравнительно благоприятный тип — туберкулоидный. Между этими двумя противоположными типами нередко выявляется своеобразная промежуточная форма — недифференцированный тип лепры. Такой вариант формирования болезни вероятен у лиц с еще не определившимся характером иммунобиологической реактивности. Поэтому недифференцированный тип лепры в дальнейшем может трансформироваться или в туберкулоидный (при благоприятном течении), или в лепроматозный.
Лечение лепры проводится сульфоновыми препаратами, в частности диафенилсульфоном - ДДС (дапсон, авлосульфон), солюсулъфоном (сулъфетрон), диуцифоном, димоцифо-ном. Эффективны рифампицин (бенемицин, рифадин, римактан), этионамид, протионамид, лампрен и др. В комплексе терапии необходимо применять стимулирующие неспецифические препараты (пирогеная, иммуноглобулин, тимозан, левамизол, пиридоксин, тиаминхлорид, никотинамид, или никотиновая кислота; витамин В12, АТФ). При проявлении признаков обострения лечение противолепрозными препаратами прекращают, больного переводят на постельный режим и назначают симптоматическую терапию по поводу лихорадки, болей: жаропонижающими, гипосенсибилизирующими, обезболивающими средствами. Если же эти меры не дают эффекта, целесообразно использовать противомалярийные и даже кортикостероидные препараты.
Вначале лечение проводится в лепрозории, затем - амбулаторно под наблюдением специально выделенного врача кожно-венерологического диспансера. Общая продолжительность лечения больных лепроматозным типом - не менее 5-10 лет (3-5 лет в лепрозории), а больных туберкулоидным и недифференцированным типами лепры - не менее 3-5 лет (в лепрозории - 6-18 месяцев). Большинство больных лепроматозным типом нуждаются в лечении на протяжении всей жизни, чтобы избежать рецидива заболевания. В последнее время лечение проводится более эффективными комбинациями препаратов, включающими и отечественные (диуцифон и димоцифон). К примеру, Е. Б. .Хромова (1984) для предупреждения рецидивов рекомендует димоцифон сочетать с изониазидом, протионамидом и рифампицином или с лампреном и рифампицином; диуцифон - с димоцифоном и тубазидом; изопродиан (ДДС, тубазид, протионамид) - с диуцифоном и рифампицином. Причем больным, резистентным к терапии сульфонами, назначают комбинации диуцифона с тубазидом и рифампицином либо с лампреном, тубазидом, рифампицином, тимолином или левамизолом.
В статье отражены современные представления о лепре, представлены современные данные литературы, посвященные вопросам эпидемиологии заболевания, особенностям клинической картины, диагностики, дифференциальной диагностики и лечения дерматоза.
The article summarizes information about the disease leprosy. Data of the literature on epidemiology of the disease, the features of the clinical picture, diagnosis, differential diagnosis and treatment of the dermatosis are presented.
Лепра (проказа, болезнь Хансена) — хроническое инфекционное заболевание из группы микобактериозов, характеризующееся продолжительным инкубационным периодом и рецидивирующим течением. Заболевание носит системный характер и поражает производные эктодермы — кожные покровы, слизистые оболочки и периферическую нервную систему. В настоящее время, несмотря на применение эффективной схемы антибиотикотерапии и устранение угрозы эпидемии лепры, по всему миру продолжают ежегодно выявляться новые случаи заболевания, поэтому перспектива полной ликвидации болезни ставится под сомнение [1–3].
Распространенность лепры в мире стабильно снижается из года в год. Согласно данным ВОЗ, количество новых случаев, каждый год выявляемых во всем мире, уменьшилось с 763 000 в 2001 г. до 249 000 в 2008 г. [1]. В 2013 г. было выявлено 215 656 новых случаев заболевания, в 2014 г. — 213 899, в 2015 г. — 211 973 [2, 3].
Глобальная статистика свидетельствует о том, что 96% (203 600 человек) новых случаев заражения лепрой были выявлены в 22 государствах (таких как Индия, Бразилия, Ангола, Конго, Судан, Эфиопия и др.). На долю других стран приходятся оставшиеся 4% [3].
Одной из шести стран мира с наиболее высокой распространенностью лепры является Бразилия, где ежегодно диагностируется более 30 000 новых случаев заболевания. В 2014 г. распространенность лепры в Бразилии составила 1,27 случая на 10 000 жителей. Уровень распространенности дерматоза по стране неравномерен: помимо эндемичных по лепре регионов существуют и такие, в которых отмечается низкий уровень распространенности лепры [4].
В России эндемичным регионом по лепре является Астраханская область. За последние десятилетия больные лепрой были выявлены и в других субъектах Российской Федерации: в Сибири, на Северном Кавказе и Дальнем Востоке [9, 10]. Однако стоит отметить, что, благодаря внедрению в практику целого комплекса противолепрозных мероприятий, заболеваемость лепрой в России носит устойчивый спорадический характер. В 2015 г. на учете состояло 240 больных, из них в Астраханской области — 135 [10].
Возбудителями лепры являются Mycobacterium leprae (M. leprae) и Mycobacterium lepromatosis (M. lepromatosis). M. leprae была впервые открыта норвежским врачом Герхардом Хансеном в 1873 г. [11]. Данный микроорганизм относится к семейству Mycobacteriaceae и является кислото- и спиртоустойчивой бактерией, которая представляет из себя грамположительную прямую или изогнутую палочку длиной 1–7 мкм и диаметром 0,2–0,5 мкм [12]. M. leprae может длительное время сохранять жизнеспособность при низких температурах и высушивании. Данному микроорганизму свойственен крайне медленный рост, который зачастую не характерен для бактерий (одно деление продолжается приблизительно 12 суток) [12]. Возбудитель заболевания является облигатным внутриклеточным паразитом. M. leprae способна продолжительно персистировать в макрофагах человека, что обеспечивается взаимодействием различных механизмов (антигенная изменчивость и пр.). Именно поэтому пациенты, выписанные из лепрозориев на амбулаторное лечение с персистирующими формами лепры, могут быть источником заражения [9].
В 2008 г. был открыт второй возбудитель лепры — M. lepromatosis, который, в отличие от M. leprae, является некислотоустойчивой бактерией и вызывает преимущественно тяжелый диффузный лепроматозный тип лепры [13, 14].
От других инфекционных заболеваний лепру отличает длительный инкубационный период, который варьирует от 2–3 месяцев до 50 лет (в среднем составляя 4–6 лет) [11].
Общепризнан воздушно-капельный путь передачи инфекционных агентов, однако не исключаются другие пути заражения — через укусы кровососущих насекомых и поврежденные кожные покровы. Лепра является малоконтагиозным заболеванием. Заражение микобактериями лепры происходит в результате длительного тесного общения с больным, не получающим лечения, вследствие сенсибилизации, нарастающей при повторяющихся контактах, снижения сопротивляемости организма (в результате неполноценного питания, тяжелых физических нагрузок, частых простудных заболеваний, алкоголизма и других интоксикаций) и иммуногенетической восприимчивости [11].
На восприимчивость к лепре оказывают влияние различные наборы генов, в том числе системы антигена лейкоцитов человека (HLA). В настоящее время изучаются изменения в генах-кандидатах, участвующих в ответной реакции организма хозяина на инфекционный агент. Исследования геномного сканирования выявили связывающие пики для лепры в областях хромосом 6p21, 17q22, 20p13 и 10p13 [15, 17].
Устойчивость к заражению M. leprae обеспечивается, с одной стороны, низкой вирулентностью M. leprae, с другой — индивидуальными особенностями врожденного иммунитета. Важную роль в поддержании врожденного иммунитета играет целостность эпителия, секрет желез и поверхностный иммуноглобулин A (IgA). Кроме того, уничтожать микобактерии, независимо от активации адаптивного иммунитета, могут NK-клетки, цитотоксические Т-лимфоциты и активированные макрофаги. При заражении регулирование воспалительных цитокинов и хемокинов приводит к пролиферации либо Т-хелперов 1-го типа (Th1), либо Т-хелперов 2-го (Th2) типа, что способствует активации клеточного или гуморального звена иммунитета, что определяет клиническую форму заболевания [16, 17].
Клеточный иммунитет неэффективен в отношении предотвращения развития заболевания у лиц с туберкулоидной формой лепры. Гуморальный иммунитет у лиц с лепроматозной формой заболевания, ответственный за продуцирование IgM против PGL-1 (фенольный гликолипид-1), не обеспечивает защиту и не предотвращает диссеминацию бактерий [17].
Высокий уровень ФНО-α в сыворотке крови у пациентов с туберкулоидной формой лепры свидетельствует об участии данного цитокина в деструкции M. leprae и образовании гранулемы. ФНО-α участвует в иммунной защите посредством активации макрофагов, однако гиперпродукция ФНО-α и его взаимодействие с ИФН-γ способствуют повреждению тканей и формированию узловатой лепрозной эритемы (ENL) [17].
При лепроматозной форме лепры наблюдается повышенный уровень трансформирующего фактора роста бета (ТФР-β), отсутствующего при туберкулоидной форме и проявляющегося в небольшом количестве при пограничной форме лепры. ТФР-β подавляет активацию макрофагов, что ингибирует продуцирование ФНО-α и ИФН-γ, способствуя персистенции инфекции [17].
О механизмах трансмиссии лепры известно, что микобактерии проникают в клетки эндотелия и оседают в Шванновских клетках нервов кожи, к которым имеют тропизм, где в дальнейшем происходит долговременный период их адаптации и размножения. Остается неизвестным, как колонизация Шванновских клеток микобактериями лепры приводит к распространению инфекции в другие ткани [18]. Нейронный тропизм M. leprae обусловлен его связыванием с областью G на мостике молекулы ламинина альфа-2, а альфа-дистрогликан служит рецептором для M. leprae на Шванновских клетках [18].
В работе Masaki и соавт. (2013), в исследовании in vitro и in vivo с использованием мышей, определялось взаимодействие M. leprae со Шванновскими клетками. Исследование показало, что M. leprae изменяют дифференцировку Шванновских клеток до клеток-предшественников [19]. Клеточная перестройка приводит к снижению регуляции Шванновской клеточной линии Sox10 [19]. Таким образом, M. leprae способствуют распространению инфекционного процесса через два механизма: прямая дифференцировка Шванновских клеток в мезенхимальные ткани и образование гранулемаподобных структур, которые выделяют бактерионесущие макрофаги [19]. Исследование расширяет понимание о пластичности зрелых клеток и демонстрирует свойства M. leprae, приводящих к перестройке взрослых клеток в стволовые [18]. Распространение инфекции путем дифференцировки Шванновских клеток возможно при их инфицировании большим количеством M. leprae. Методология, используемая на мышах, у которых нет Т-клеток, упрощает воспалительное микроокружение в преимущественно макрофаги [19]. Данная работа описывает перспективную in vitro модель для объяснения патогенеза M. leprae, но необходимы подробные исследования, прежде чем экстраполировать выводы на течение инфекционного процесса в организме человека [18].
Существует две классификации лепры: мадридская классификация, принятая в 1953 г., а также ее последующая модификация, предложенная Д. С. Ридли и В. Джоплингом в 1973 г. [11].
Согласно мадридской классификации выделяют два полярных типа лепры: туберкулоидный и лепроматозный и два промежуточных типа: недифференцированный и пограничный (диморфный) [11].
В классификации Ридли–Джоплинга выделяют три типа лепры — недифференцированный (I — Indeterminate), туберкулоидный (Tuberculoidtype — TT) и лепроматозный (Lepromatoustype — LL). Лепроматозный и туберкулоидный типы являются полярными. Кроме того, различают субполярные и пограничные группы заболевания. Классификация Ридли–Джоплинга не нашла широкого применения ввиду сложности, поэтому в практической деятельности различают лепроматозный и туберкулоидный тип лепры, а также пограничный тип, который в дальнейшем может трансформироваться в одну из первых двух форм [20].
При лепроматозном типе лепры поражается как периферическая, так и центральная нервная система с развитием невротических расстройств, реже — психозов и поражений по типу невритов и полиневритов. В большинстве случаев поражаются лучевые, малоберцовые и большие ушные нервы: они утолщаются и становятся доступными для пальпации. В последующем развиваются двигательные и трофические расстройства, а также нарушения чувствительности. Больным свойственны невралгии, гиперестезии, парестезии, неадекватное или замедленное реагирование на раздражение, аналгезия. На фоне трофических нарушений развивается процесс мутиляции кистей и стоп. Поражение внутренних органов характеризуется неспецифическими изменениями в печени, легких, селезенке и нарушением функции некоторых желез внутренней секреции [11].
При недифференцированной форме лепры специфические высыпания отсутствуют. Для данной формы характерно появление небольшого количества бледных пятен различной величины с нечеткими границами, а также поражение периферической нервной системы по типу полиневрита. Как правило, выявить возбудителя у этой категории лиц удается крайне редко [11].
При развитии обострений лепрозного процесса форма заболевания может меняться. Несмотря на множество клинических проявлений лепры, окончательная постановка диагноза не всегда является простой задачей, так как отсутствуют патогномоничные клинические признаки заболевания [25].
При диагностике лепры учитывают данные эпидемиологического анамнеза (пребывание в эндемичном регионе, контакты с больными лепрой), объективного осмотра (обращают внимание на характер и длительность существования высыпаний, наличие признаков нарушений периферической иннервации).
Общепринятым лабораторным методом диагностики лепры считается бактериоскопическое исследование. Соскобы для исследования берут с очагов поражения на коже и слизистой оболочке носа путем легкого поскабливания. Мазок помещают на предметное стекло и окрашивают по Цилю–Нильсену. Также исследуют пунктат из бедренных или паховых лимфатических узлов. Однако бактериоскопическое исследование имеет очень низкую чувствительность, особенно у больных с промежуточной или туберкулоидной формой поражения [26].
Лепроминовая реакция (проба Митсуды) является показателем способности хозяина поддерживать в своем организме клеточный иммунитет к M. leprae. Проба Митсуды не всегда является достоверной, так как у 10% здоровых по лепре людей может наблюдаться отрицательная реакция. Ограничивают применение лепроминового теста и технические трудности, связанные с получением лепромина и его внутрикожным введением [11].
Наиболее чувствительным методом диагностики, позволяющим определять M. leprae, является полимеразная цепная реакция (ПЦР). ПЦР на данный момент считается наиболее перспективной из прямых диагностических методик и применяется для диагностики любого типа лепры [10, 18]. Преимуществом ПЦР являются неинвазивность и простота получения клинического материала, что предоставляет возможность проведения скрининга большого количества образцов при обследовании пациентов в высокоэндемичных по этому заболеванию регионах. Применение ПЦР позволяет усовершенствовать диагностику лепры и выявлять заболевание на ранней стадии [26].
Используемые в настоящее время традиционные методы диагностики, такие как лепроминовая проба и бактериоскопическое исследование, не всегда позволяют подтвердить диагноз лепры на ранних стадиях заболевания. При этом эффективность лечебных и профилактических мероприятий определяется возможностью ранней диагностики заболевания. В мире постоянно регистрируются новые случаи лепры, поэтому актуальным вопросом остается разработка и внедрение новых, более точных, методов диагностики, которые стали бы доступными для широкого использования и позволили с высокой степенью достоверности диагностировать лепру на ранних стадиях развития заболевания.
Лечение заболевания стандартизовано ВОЗ в 1981 г. [28]. Комбинированная лекарственная терапия включает в себя использование трех основных препаратов: дапсон, рифампицин и клофазимин [28].
Дапсон — бактериостатический препарат, действующий как конкурентный ингибитор ферментов дигидрофолатсинтетазы и дигидрофолатредуктазы, которые являются ключевыми ферментами путей биосинтеза фолатов в микобактериях лепры [28].
Рифампицин — оказывает в отношении M. leprae бактерицидное действие. Является селективным ингибитором ДНК-зависимой РНК-полимеразы и блокирует синтез РНК [29].
Клофазимин — жирорастворимый кристаллический краситель красноватого цвета с бактериостатическим и противовоспалительным свойствами. Механизм антибактериального действия клофазимина изучен недостаточно. Вероятно, он связан с блокировкой матричной функции ДНК, повышением фагоцитарной активности макрофагов и синтеза лизосомальных ферментов [28]. Клофазимин и рифампицин обладают эффективностью в отношении дапсонрезистентных микроорганизмов.
В 1997 г. ВОЗ была установлена продолжительность курса лечения: 6 месяцев для мультибациллярных форм лепры и 12 месяцев для олигобациллярных. Дапсон назначается в дозировке 100 мг для взрослых один раз в день, рифампицин в дозировке 600 мг один раз в месяц, клофазимин в дозировке 300 мг один раз в месяц. Для лечения детей применяются более низкие дозы препаратов [28]. В случае невозможности применения одного или двух препаратов из вышеперечисленных существуют схемы лечения с применением фторхинолонов, которые также показали свою эффективность в отношении M. leprae [30].
Своевременная диагностика лепры, профилактика распространения лепры беженцами и вынужденными переселенцами, особенно из высокоэндемичных государств (Бангладеш, Филиппинские острова, Индия, Ангола, Бразилия, Шри-Ланка и др.), являются серьезной и актуальной проблемой для мирового здравоохранения, одной из приоритетных задач при осуществлении контроля над здоровьем иностранных граждан и лиц без гражданства, въезжающих на территорию страны. В Российской Федерации, в соответствии с существующим порядком, установленным на законодательном уровне, для контроля над распространением заболеваний среди населения, нерезидентам Российской Федерации необходимо пройти медицинское освидетельствование в медицинских организациях. Однако данная процедура освидетельствования осложнена отсутствием комплексной методологической платформы.
Таким образом, несмотря на снижение распространенности лепры, представляется актуальным усиление контроля за обязательным обследованием на лепру прибывающих в страну иностранных граждан, разработка отечественных аналогов лекарственных препаратов и поиск новых схем лечения больных лепрой.
Литература
А. А. Кубанов*, доктор медицинских наук, профессор, член-корреспондент РАН
Т. В. Абрамова**, кандидат медицинских наук
Е. К. Мураховская* , 1 , кандидат медицинских наук
В. А. Ласачко*
* ФГБОУ ДПО РМАНПО МЗ РФ, Москва
** ФГБУ ГНЦДК МЗ РФ, Москва
Кожные болезни:
Популярные разделы сайта:
Лепра у детей - диагностика, лечение
Лепра - хроническое инфекционное заболевание, вызываемое Mycobacterium leprae, палочкой, имеющей тропность к нервной ткани и коже. Клинические проявления, течение и прогноз лепры зависят от иммунитета к М. leprae.
Синоним: болезнь Ганзена.
Классификация лепры
1. Туберкулоидный тип: высокая резистентность Т-клеток (Тh), от одного до 5 очагов поражения кожи, отсутствие палочек.
2. Пограничный туберкулоидный тип: более 5 обширных очагов поражения кожи, вовлечение в процесс периферических нервов.
3. Пограничный тип: отмечаются как туберкулоидные, так и лепроматозные многочисленные поражения кожи, большое количество палочек.
4. Пограничный лепроматозный тип: многочисленные кожные поражения, facies leonina, поздние поражения нервной ткани.
5. Лепроматозный тип: отсутствие Т-клеток (Th2), генерализованное поражение, большие лепромы.
Эпидемиология лепры
Патофизиология лепры
Лепра вызывается М. leprae, которые проникают через носовую, ротовую полости или раневую поверхность. Передается от инфицированного человека через слизистую носовой полости, открытые раны или контаминированные иглы. Несмотря на то, что люди являются основным резервуаром инфекции, микроорганизм был обнаружен у броненосцев (штат Луизиана), низших обезьян, шимпанзе и мышей.
М. leprae - облигатный внутриклеточный паразит, который поражает макрофаги и шванновские клетки в относительно холодных (менее 35°С) областях тела (периферические нервы, кожа, нос, слизистые оболочки, кости, висцеральные органы), которые необходимые ему для роста. В зависимости от уровня клеточно-опосредованного иммунитета (лепроминовая проба), заболевание может прогрессировать (Th2-ответ, интерлейкин-4, интерлейкин-10), находится в стационарной стадии или спонтанно регрессировать (Th1-ответ, интерлейкин-2, интерферон-гамма).
Клиника лепры
Тип высыпаний: от пятен (при туберкулоидной форме) до папул, узлов, инфильтрированных бляшек (при лепроматозной форме).
Цвет: красный или гипопигментированный. Размер: от нескольких миллиметров до нескольких сантиметров.
Форма: кольцевидная, овальная, круглая Пальпация: инфильтрированные бляшки, с отсутствием или снижением чувствительности.
Локализация: лицо - facies leonina, ягодицы, нижние конечности.
Слизистые оболочки: язык (узлы, бляшки, трещины).
Волосы: отсутствуют на пораженной коже.
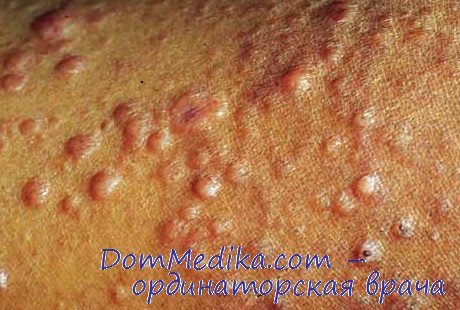
Общие проявления лепры
Нервная система: утолщение периферических нервов (лицевого, большого ушного, локтевого, лучевого, срединного, общего малоберцового или заднего большеберцового), отсутствие чувствительности в зоне поражений, нейропатические изменения (мышечная атрофия), вазомоторные реакции или нарушения секреции.
Органы зрения: сухость глаз. Вовлечение в патологический процесс передней камеры глаза ведет к развитию глаукомы или катаракты (при лепроматозной форме).
Яички: при лепроматозной форме может развиться гипогонадизм.
Дифференциальная диагностика лепры
Лепру следует дифференцировать с широким спектром заболеваний: грибковым поражением, отрубевидным лишаем, себорейным дерматитом, васкулитами, панникулитами, красным плоским лишаем, склеродермией, целлюлитом, витилиго, ограниченной склеродермией, кольцевидной гранулемой, аллергическими реакциями на лекарственные препараты, саркоидозом, лейшманиозом, сифилисом, красной волчанкой, кольцевидной эритемой, Т-клеточной лимфомой кожи или туберкулезом кожи.
Лабораторная диагностика лепры
Исследование мазка с кожи: после небольшого разреза кожи выполняется соскоб, микроорганизмы визуализируются с помощью окраски по Цилю-Нильсену, Граму, Файту-Вэйду, Суданом III, Суданом IV или гексаметилентетрамином серебра. При лепроматозной форме микроорганизмы обнаруживаются в 100% случаев, при пограничных формах в 75% случаев, при туберкулоидной форме - только в 5% случаев. Лепроминовая проба (реакция Мицуды): при туберкулоидной и пограничной туберкулоидной формах внутридермальное введение убитых M.leprae вызывает положительную реакцию (образование узелковых форм в месте введения через 3-4 недели).
Течение и прогноз лепры
Лепра - калечащее, социально дезадаптирующее заболевание, лечение которого осложняется реактивными процессами, вызванными приемом антибактериальных препаратов, беременностью, другими инфекциями или даже психическими расстройствами.
1. Реакции первого типа при лепре: в результате развития реакции гиперчувствительности замедленного типа наблюдаются воспалительные и болезненные поражения кожи, сопровождающиеся выраженным отеком кистей, стоп и лица. Препаратом выбора является преднизон.
2. Реакции второго типа при лепре (лепрозная узловатая эритема): появляются болезненные красные узелки на лице и конечностях, при этом в результате образования иммунных комплексов формируются абсцессы или язвенные поверхности, а также васкулит мелких сосудов, в том числе и кожи. Препаратом выбора является талидомид.
3. Реакция Лусио: отмечаются эритематозные бляшки неправильной формы, которые могут изъязвляться или некротизироваться на фоне сопутствующего тромбоза сосудов кожи.
После завершения курса лечения основными осложнениями являются неврологические: контрактуры кистей и стоп.
Лечение лепры
ВОЗ рекомендует многокомпонентную терапию в зависимости от возраста пациента и обнаруженных возбудителей. Детям в возрасте от 5 до 14 лет, у которых в области лепрозных поражений выявлена олигобациллярность, необходимо назначение только однократной дозы рифампина, офлоксацина и миноциклина.
При большом количестве возбудителей у детей младше 14 лет назначаются препараты сульфонового ряда (дапсон) применяемые в течение 12-18 месяцев, если нет дефицита G6PD. Из-за устойчивости к дапсону, в сочетании с ним для лечения туберкулоидной и пограничной туберкулоидной форм лепры следует применять рифампин в течение 6 месяцев. При пограничной лепроматоз-ной и лепроматозной формах необходимо назначение клофазимина, курс лечение которым должен продолжаться по крайней мере два года до получения отрицательных результатов бактериологического исследования.
Уже после первых доз препаратов пациент перестает быть заразным для окружающих, а после проведения полноценного курса сожжет считаться вылеченным. Рецидивы редки, у переболевших могут обнаруживаться возбудители, однако они нежизнеспособны.
Читайте также:

