Кластерное серебро при лечении вич
Обновлено: 24.04.2024
В середине 1980-х ученые идентифицировали вирус иммунодефицита человека и сразу же стали искать лекарство. История антиретровирусной терапии началась в 1987 году, когда для лечения ВИЧ-инфекции стали использовать препарат зидовудин. Но его эффективность была невысокой, а побочные эффекты слишком сильными. Первая высокоэффективная терапия появилась только через десять лет — в 1996 году. Эта комбинация из нескольких лекарств блокирует размножение попавшего в организм вируса сразу на нескольких этапах его цикла. С тех пор ВИЧ-инфекция — не смертельное, а хроническое заболевание, которое можно контролировать при должном лечении.
Антиретровирусные препараты (АРВ) подавляют размножение ВИЧ, но неспособны полностью удалить вирус из организма, именно поэтому их нужно принимать постоянно в течение всей жизни. Как только концентрация препарата в крови падает ниже порогового значения, вирус снова начинает размножаться. Это особенно опасно, ведь если вирус размножается в присутствии небольшого количества лекарства, то он вырабатывает устойчивость к этому препарату.
Пить таблетки на протяжении всей жизни с точностью до минут — не самая простая задача. Этому мешают и банальная забывчивость, и разные случайные обстоятельства. А чем чаще человек нарушает время приема терапии, тем выше риск развития у вируса устойчивости. Именно поэтому врачи стараются назначать схемы с приемом лекарств один раз в день и с минимальным числом таблеток — чем реже и меньше нужно принимать лекарств, тем проще соблюдать режим. Правильное соблюдение режима приема терапии называют высокой приверженностью лечению.
Сейчас лучшими схемами считаются те, при которых пациенту нужно принимать одну таблетку один раз в день, да еще и независимо от приема пищи. Но настоящим прорывом в АРВТ станет разработка схем, при которых лекарство достаточно будет принимать всего один или несколько раз в месяц, — пролонгированных схем терапии. Хотя в настоящее время неизвестно, как поведут себя пролонгированные режимы в рутинной практике. Будет ли к ним сохраняться высокая приверженность — как это показывают исследования?
по теме

Общество
Грудное молоко VS смеси при ВИЧ: что говорят эксперты в 2020 году?
Основной недостаток таких таблеток — срок их действия ограничено временем нахождения таблетки в кишечнике и не превышает 12—24 часов. В случае же диареи таблетка может покинуть организм гораздо быстрее, а значит, уменьшится концентрация лекарства в крови, что может быть опасно. Для антиретровирусных препаратов создание таблеток или капсул с замедленным высвобождением лекарственного вещества не очень перспективно — современные схемы уже позволяют принимать терапию один раз в день. То есть удобство применения терапии такие таблетки не повысят.
Если нужно добиться продления эффекта препарата на дни и недели, а лекарство всасываться через кожу упорно не хочет, приходится прибегать к парентеральным пролонгированным формам. Можно зашить под кожу специальную стерильную таблетку, которая будет медленно растворяться и выделять лекарственное вещество: на коже делается небольшой разрез, в него вводят таблетку и зашивают рану.
Помимо таблеток, под кожу можно вводить специальные полимерные импланты, содержащие нужное лекарство. Преимущество имплантов — они могут выделять лекарственное вещество очень долго, до нескольких лет. Чаще всего такие импланты используют для гормональной контрацепции. Так как гормоны действуют в очень маленьких дозах, даже в небольшой по размерам имплант можно сразу поместить запас препарата на несколько лет. Например, противозачаточный препарат Имплантон, который вводится под кожу, продолжает действовать три года. Если действие препарата нужно прекратить — достаточно просто извлечь имплант.
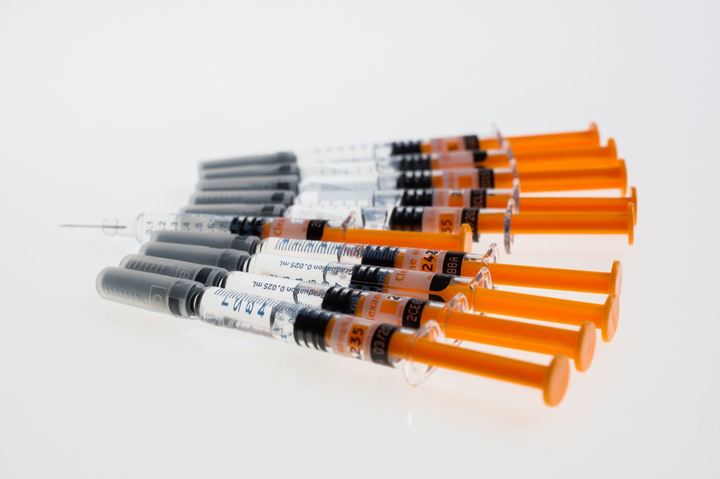
Более простой вариант — ввести в мышцу взвесь маленьких крупинок лекарства в подходящем растворителе. Выглядит это как обычный укол, при этом крупинки лекарства задерживаются в мышце, медленно растворяются и попадают в кровь. Такие способы введения лекарства особенно удобны в случаях, когда пациент может часто пропускать прием препарата, или забывать, принял ли он лекарство. Например, в случае лечения психических заболеваний. Но есть и недостатки: вводить такой препарат должен медицинский работник, а в случае непереносимости или выраженных побочных эффектов лекарство очень трудно быстро удалить из организма.
Что уже доступно на рынке?
Многие фармацевтические компании проводят исследования пролонгированных АРВ-препаратов, но разработка одного такого препарата сама по себе очень большой пользы не принесет — ведь для лечения ВИЧ-инфекции необходимо сочетание нескольких препаратов, то есть нужна комбинированная пролонгированная схема.
Такую схему, разработанную ViiV Healthcare совместно с Janssen, одобрили в марте 2020 года в Канаде — первый пролонгированный комбинированный АРВ-препарат Cabenuva. Схема показала высокую эффективность и безопасность в клинических исследованиях LATTE-2, FLAIR, ATLAS с участием более тысячи пациентов. В состав Cabenuva входят каботегравир и рилпивирин, то есть это двухкомпонентная схема. Препарат вводят один раз в месяц внутримышечно.
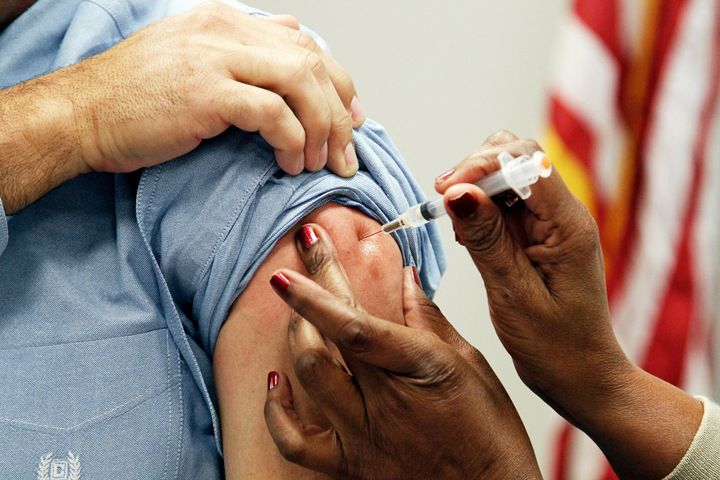
Перед началом применения Cabenuva пациент не менее месяца принимает каботегравир в таблетках (называется Vocabria) в комбинации с Эдюрантом — таблетками рилпивирина. Это необходимо, чтобы проверить переносимость такой схемы у конкретного пациента и оценить побочные эффекты. Если схема переносится хорошо, пациенту вводят первую нагрузочную дозу Cabenuva — 3 миллилитра суспензии, содержащей 600 миллиграммов каботегравира, и 3 миллилитра суспензии, содержащей 900 миллиграммов рилпивирина. Суспензии вводятся в разные участки ягодичной мышцы, то есть делают два укола. После этого поддерживающие дозы вводят ежемесячно: 2 мл (400 мг) каботегравира и 2 мл (600 мг) рилпивирина. Если по каким-то причинам введение очередной ежемесячной поддерживающей дозы невозможно, пациент до момента следующей инъекции может принимать пероральную схему (Vocabria + Эдюрант). Пролонгированная форма каботегравира также имеет большие перспективы для использования в качестве доконтактной профилактики ВИЧ-инфекции.
Еще один препарат, который уже применяется в клинической практике, — ибализумаб (Трогарзо) — можно назвать пролонгированным с несколькими оговорками. По химической природе ибализумаб — моноклональное антитело, то есть близок к человеческим иммуноглобулинам. Ибализумаб связывается с некоторыми белками на поверхности вируса и мешает проникновению ВИЧ в клетки. Препарат вводят внутривенно один раз в две недели и часто сочетают с другими АРВ-препаратами. Такая схема — не самый удобный вариант, поэтому сейчас ибализумаб используется только для лечения ВИЧ с множественной лекарственной устойчивостью, когда другие схемы оказываются неэффективными. Поэтому ибализумаб правильнее будет отнести к нишевым препаратам.
К сожалению, на этом и заканчивается не очень длинный перечень пролонгированных АРВ-препаратов, которые уже применяются на практике. Дальше пойдет речь о препаратах, находящихся на разных стадиях исследований.
Что сейчас находится в разработке?
PRO 140
С точки зрения места в клинической практике на ибализумаб похоже еще одно моноклональное антитело, находящееся в стадии клинических исследований, — PRO 140. Этот препарат также можно будет использовать для лечения ВИЧ-инфекции, если у пациента не работают другие схемы. А по механизму действия PRO 140 похож на уже существующий на рынке препарат маравирок (Целзентри). Он связывается с CCR-5 рецепторами на поверхности клеток-мишеней и мешает проникновению вируса в клетку. Строение активного центра молекулы PRO 140 отличается от маравирока, поэтому он активен даже в тех случаях, когда вирус выработал устойчивость к маравироку. Как и маравирок, PRO 140 активен только против CCR-5-тропных подтипов ВИЧ, то есть подойдет не всем пациентам. Препарат вводят внутривенно, один раз в неделю.
Нейтрализующие антитела
На разных стадиях клинических исследований находятся несколько перспективных антител, которые связываются с вирусным белком gp120 и нейтрализуют вирус: VRC01, 3BNC117 и 10-1074. Предполагается, что эти препараты достаточно будет вводить раз в месяц или даже реже и их можно будет применять совместно с другими пролонгированными АРВ-препаратами.
Албувиртид
Аналог уже применяющегося на практике энфувиртида (Фузеон). Этот препарат связывается с вирусным белком gp-41 и мешает проникновению вируса в клетку. Основное отличие в том, что Фузеон вводят подкожно два раза в сутки, что очень неудобно, а албувиртид — только один раз в 2—4 недели. Препарат должен применяться совместно с другими АРВ-лекарствами.
Изобретение относится к фармакологии и медицине и может быть использовано для лечения больных, зараженных ВИЧ-инфекцией, а также и другими вирусами, и касается антивирусной композиции, способа активации ее активной компоненты и лечения ВИЧ-инфицированных больных с помощью этой композиции. Сущность изобретения включает антивирусную композицию, содержащую предварительно активированную компоненту атомарного серебра, стабилизатор атомарного серебра, выбранного из ряда синтетических или природных полимеров медицинского назначения, а также димексид, перекись водорода и дистиллированную воду, способ получения активной компоненты, состоящей из атомарного серебра, стабилизатора и дистиллированной воды. Способ лечения инфицированных больных заключается в ректальном введении в нижний отдел прямой кишки лечебной композиции в виде микроклизмы объемом 100 мл, 1 раз в сутки в течение 10 дней, с повторением курсов через 7-10 дней до получения отрицательного анализа крови на ВИЧ-инфекцию. Преимущество изобретения заключается в разработке способа воздействия на ВИЧ-клетки человека, приводящей к инактивации вируса. 3 с. и 1 з.п.ф-лы.
Формула изобретения
4. Способ лечения по п. 3, отличающийся тем, что его проводят на фоне сбалансированного, калорийного питания в комплексе с пероральным приемом поливитаминов и пищевых добавок, содержащих микроэлементы: кремний, калий, магний, кальций, медь, железо, марганец, фосфор, никель, цинк.
Описание изобретения к патенту
Изобретение относится к фармакологии и медицине и может быть использовано для лечения больных, зараженных ВИЧ-инфекцией, а также и другими вирусами.
Известно для лечения ВИЧ-инфицированных больных в стадии 2Б и 2В применение Тимазида в течение 48 недель. Результат: лечение снижает риск клинического прогрессирования ВИЧ-инфекции и замедляет темп снижения уровня CD4-лимфоцитов и только. Но практика показала, что применение отдельных противовирусных препаратов (монотерапия) неэффективна, так как быстро приводит к образованию устойчивых штаммов вируса, как правило более агрессивных, чем "дикий" штамм.
Поэтому более эффективной принято считать тройную комбинированную терапию ТКТ, когда одновременно применяют 3 препарата, включающую 2 ингибитора обратной транскриптазы, например АЗТ (тимазид, ставидин) плюс ингибитор протеазы (вирасепт или инвираза), при суточной дозе каждого по 600-2400 мг/сутки, при весе больного 60 кг и курсе лечения в несколько месяцев [1].
Поэтому жизненно необходим поиск лекарств, лишенных этих недостатков и доступных по стоимости больным ВИЧ даже из малоимущих социальных слоев.
Наиболее близким к заявляемому способу является метод коррекции иммунодефицитных состояний организма посредством введения в организм электроактивированного водного раствора солей, содержащего азотнокислое серебро АgNО 3 в концентрации до 7 г/л или смеси солей NaCl, KCl, CaCl 2 и MgCl 2 с суммарным содержанием 10 г/л, причем в виде разделенных на 2 вида: с+и - редокс-потенциалами растворов. В комплексе с имплантацией не менее 3-х штаммов кишечной микрофлоры (бактерий эубиотиков), раздельно; культуру лактобактерий, культуру бифидобактерий и культуру колибактерий, не менее 20 мл каждой жидкой культуры в разные отделы кишечника [2] (прототип).
Недостатки: [2] (прототип) - сложная технология лечения, сложная технология получения лекарственной композиции, весьма трудоемкая требующая специального лабораторного оборудования, высококвалифицированного персонала, а также участка выращивания бактерий эубиотиков. Как следует из задачи, решаемой прототипом - профилактика и лечение больных осуществляются за счет интенсивной нейтрализации и очищения организма от шлаков и восстановления микробиоценоза организма.
Для лечения больного, зараженного ВИЧ-инфекцией, необходима, в первую очередь, непосредственная борьба с этим вирусом, замедление его репродуцирования, а также уничтожение уже внедренных в клетки вирусов, безусловно, при одновременном укреплении жизненных сил организма. Трудность борьбы с ВИЧ-инфекцией связана со специфическими особенностями строения и поведения самих вирусов в организме человека [4].
Установлено [5] , что внедрившиеся в клетки организма вирусы обладают собственным генетическим аппаратом, который кодирует синтез вирусных веществ из биохимических предшественников, находящихся в клетке хозяине, при этом используются биосинтетические и энергетические системы клетки хозяина. Сборка вирусных частиц происходит внутри клеток организма больного в результате агрегации, т.е. суммирования, присоединения, объединения однородных показателей (величин) макромолекул вирусных нуклеиновых кислот, наработанных клеткой-хозяином. Макромолекулы вирусных нуклеиновых кислот скапливаются в определенных частях клетки хозяина (микрогетерогенность), поэтому необходим такой активный реагент, который проникал бы в эти части клеток и при непосредственном контакте с макромолекулами вирусных нуклеиновых кислот разрушал бы последние.
Применение такого высокореактивного соединения, как азотнокислое серебро, такую функцию обеспечить не может, поскольку при внутривенном введении в кровеносное русло ионы серебра очень быстро реагируют с белковыми компонентами крови, превращаясь в полимерные альбуминаты серебра. Альбуминаты серебра не способны диффундировать через клеточные мембраны внутрь пораженных вирусом ВИЧ-клеток организма и быстро выводятся из последнего почками и печенью [6].
Решается задача разработки эффективного лечебного средства, в частности антивирусной композиции, способной к трансмембранному переносу внутрь пораженной ВИЧ-клетки активнодействующей лекарственной субстанции, инактивирующей генетический аппарат ВИЧ. Экспериментально установлено, что подобными вирулицидными свойствами обладает, в частности, ультрадисперсное металлическое серебро Аg o с размерами частиц и для получения максимального терапевтического эффекта при лечении необходимо добиваться, чтобы до 80% от массы частицы серебра имели размеры порядка . С поверхности кластеров такого малого размера легче генерируются атомы серебра, которые при попадании внутрь инфицированной ВИЧ-клетки больного, блокируют генетический аппарат вируса. Таким образом, нанокластеры серебра являются стабильной депонированной формой лекарственной субстанции. Атомы серебра постоянно генерируются с поверхности кластеров серебра по мере их связывания внутри клеток организма с генетическим аппаратом ВИЧ. Присутствие перекиси водорода в композиции активирует генерацию атомов.
Композиция указанного состава обеспечивает:
- окисление атомарного серебра на поверхности кластера перекисью водорода;
- комплексование атомов серебра со специфически сольватирующим растворителем - димексидом (диметилсульфоксидом), который осуществляет трансмембранный перенос комплекса внутрь клетки;
- взаимодействие кластеров серебра с компонентами клетки-хозяина, а также вируса ВИЧ, внедрившегося внутрь клетки, вследствие чего нарушается механизм репликации вируса внутри клетки и что, в конечном счете, ведет к гибели самих вирусов.
Поскольку высокодисперсное кластерное серебро, несмотря на стабилизацию в момент образования в ходе синтеза, в подавляющей массе имеет больший размер частиц, чем необходимо для достаточного вирулицидного фармакологического эффекта, поэтому для получения активной компоненты каждый раз перед составлением антивирусной композиции синтезированный раствор серебра подвергают активации.
Способ получения активной компоненты:
Известен способ получения активированных растворов солей - электролитический [2] (прототип), по которому АgNО 3 или другие соли электроактивируют на мембранном электролизере и получают отдельно электролиты с+и - редокс-потенциалами. Указанным способом получают ионное Аg + для введения больному.
Способ получения активной компоненты, т. е. активированного Аg o со сверхмалыми частицами размером включает физико-химическую обработку исходных компонент, содержащих серебро, отличающийся тем, что исходную смесь, состоящую из атомарного серебра, стабилизатора и воды, подвергают обработке в автоклаве при t o 100-110 o С в течение 45-60 минут.
ПРИМЕР 1. Исходное мелкодисперсное серебро Аg o с добавленным стабилизатором поливинилпирролидоном 7.000-12.000 (а.е.м.) или 20.000-40.000 (а.е.м.) в соотношении 1:12 + дистиллированная вода остальное помещают в автоклав и подвергают обработке в автоклаве паром при t o 105 o С в течение 45 минут. По данным электронной микроскопии полученного коллоидного раствора, до 80% от общей массы частиц в нем, составляют частицы диаметром
ПРИМЕР 2. Исходное мелкодисперсное серебро Аg o с добавленным казеином в качестве стабилизатора в соотношении 1:0,43 + дистиллированная вода остальное помещают в автоклав и подвергают обработке паром в автоклаве при t o 110 o С в течение 60 минут. По данным электронной микроскопии полученного коллоидного раствора, до 80% от общей массы частиц в нем, составляют частицы диаметром
Предлагаемый способ лечения:
Способ лечения [2] (прототип) характеризуется многостадийностью и включает 11 различных, достаточно трудоемких процедур. Необходимо раздельное введение нескольких составляющих средств курса лечения: внутривенное введение по 200 мл в сутки водного раствора АgNО 3 или смеси нескольких солей, предварительно электроактивированных, с отрицательным редокс-потенциалом, затем перорально по 300 мл в сутки в течение 15-20 дней и в количестве 0,5-1,5 литра в виде очистительных клизм 1 раз в сутки. Растворы с положительным редокс-потенциалом вводят в виде аэрозоля через нос и рот 2 раза в сутки и в виде вагинальных спринцеваний по 100-200 мл за одну процедуру 2 раза в сутки. Кроме того, проводят имплантацию бактерий эубиотиков (кишечной микрофлоры) через биопсийный канал, раздельно в разные отделы кишечника, для чего опять же необходимо специальное оборудование. Внутривенное введение растворов требует обязательного пребывания больных в стационаре. При передозировке АgNО 3 более 0,8 м/моль на 1 кг веса больного возможны явления острой интоксикации [3] . Перечисленные недостатки серьезно затрудняют применение данного способа на практике для лечения ВИЧ-инфицированных больных, поскольку большинство из них наркоманы, зачастую неуправляемы и поэтому трудно вводимы в столь сложную схему лечения.
Предлагаемый способ, отличающийся от [2] (прототип) тем, что лечение ВИЧ-инфицированных больных осуществляют путем ректального введения больному в прямую кишку жидкой лекарственной композиции. Выбор прямой кишки в качестве пути введения лекарственной субстанции в организм ВИЧ-инфицированного удобен тем, что обеспечивается большая площадь контакта лечебной композиции с тканями больного организма. Сокращается путь доставки лекарственной субстанции внутрь пораженных вирусом клеток, при этом в прямой кишке отсутствуют кислоты и ферменты, которые могли бы инактивировать лекарственную композицию. То есть ректальный путь введения серебра наиболее эффективный, щадящий и удобный для проведения лечения больного.
Лечение проводят 1 раз в сутки, в вечернее время, путем введения в нижний отдел прямой кишки заявленной композиции, содержащей активную компоненту - высокодисперсное предварительно активированное атомарное серебро со стабилизатором, димексидом и перекисью водорода. Введение микроклизмой в количестве 100 мл, после обычной водной очистительной клизмы объемом 0,5 литра, в течение 10 суток. Через 7-10 дней курс лечения повторяют до отрицательных показаний анализа крови на ВИЧ-инфекцию. Концентрация РНК вируса в плазме крови (вирусная нагрузка) является независимым прогностическим фактором для оценки прогрессирования заболевания и имеет практическое значение для определения состояния инфекционного процесса. Известно, что содержание РНК ВИЧ в плазме крови - показатель, позволяющий наиболее точно предсказать клинический исход для больного [7,8]. Лечение больного проводится на фоне сбалансированного калорийного питания, богатого витаминами и микроэлементами.
ПРИМЕР 3. Больной Б, (20 лет) на учете как ВИЧ-инфицированный с августа 2000г. (предполагаемая дата инфицирования апрель-май 2000г). Причина инфицирования - внутривенное введение наркотиков, перенесенные заболевания - опийная наркомания. 13.11.2000г. поставлен диагноз - ВИЧ-инфекция в стадии 2В (генерализованная лимфоаденопатия). Сопутствующие заболевания: вирусный гепатит С в минимальной стадии активности, пиодермия, хламидиоз.
Лечение начато 18.01.2001 года. При анализе от 13.01.2001г. вирусная нагрузка составляла 10.000 копий в 1 миллилитре крови. После 1 курса лечения заявленной композицией и способом на 29.01.2001 г. вирусная нагрузка снизилась до 5000 копий в 1 миллилитре крови. В течение второго курса на 7.02.2001г. вирусная нагрузка составила 500 копий в 1 миллилитре крови. После 3 курса - на 20.03.2001г. (некоторое повышение РНК и ДНК частиц вируса в крови) вирусная нагрузка возросла до 1000 копий в 1 миллилитре крови. За счет разрушения мембранных клеточных мешочков "везикул", являющихся хранилищами вирусов в пораженных клетках иммунной системы и попадания их в кровь [4].
После 4-го курса лечения на 23.05.2001г. анализ крови больного на наличие маркеров нуклеиновых кислот РНК и ДНК ВИЧ-1 отрицательный. Улучшились показатели крови больного:
количество эритроцитов увеличилось с 3,910 12 до 4,710 12 ;
гемоглобин увеличился со 120 до 145;
лейкоциты уменьшились с 8,510 9 до 5,910 9 ;
СОЭ снизилось с 7 до 5;
билирубин общий снизился с 32,4 до 15,8.
Анализы крови больного проводились в Новосибирском государственном областном центре по профилактике и борьбе со СПИД и инфекционными заболеваниями, а также в клинико-диагностической лаборатории ЗАО "Вектор-Бест" в ГНЦ "Вектор", находящихся в п.г.т. Кольцово Новосибирского района, Новосибирской области. Анализы прилагаются.
Пока пролечено 2 ВИЧ-инфицированных. Курсы лечения проводились амбулаторно и в домашних условиях на базе нормального, калорийного, сбалансированного питания и повышения ослабленных сил организма ежедневным систематическим пероральным приемом поливитаминов и пищевых добавок, содержащих микроэлементы: кремний, калий, магний, кальций, медь, железо, марганец, фосфор, никель, цинк. Заявляемый нами препарат практически не оказал на организм больного никаких токсических осложнений и вредных побочных действий, лечение переносилось совершенно легко при сохранении больным обычного ритма жизни.
Таким образом, заявленная композиция и способ лечения ею ВИЧ-инфицированных больных является нетоксичным, недорогим, приемлемым каждому больному, возможен для осуществления в домашних условиях, так как не требует специальной аппаратуры или в условиях поликлиники, что очень важно, если учитывать специфику психического состояния таких больных (наркозависимость). Приводим примерную расчетную калькуляцию себестоимости 1 дозы (100 мл) заявляемой лекарственной композиции:
Серебро 6 руб. , стабилизатор 10 руб., спирт 2 руб., азот 2 руб., димексид 7 руб., перекись водорода 1,5 руб., дистиллированная вода 1 руб., итого 29,5 руб.
Вспомогательные материалы 3 руб., транспортные расходы 3 руб., амортизация оборудования 2,5 руб., энергозатраты 1 руб., заработная плата 20 руб., налоги 10 руб.,прочие затраты 3 руб., итого 42,5 руб.
Итого совокупные затраты на приготовление одной дозы заявляемой лекарственной композиции составят 29,5 рулей+42,5 рублей=72 рубля.
Количество введений препарата до уменьшения вирусной нагрузки в плазме крови до величины ниже порога чувствительности, имеющихся в настоящее время диагностических систем составляет в среднем 40, на что требуется 2 месяца лечения, таким образом, стоимость полного курса лечения оценивается нами в сумме 72 рубля40 доз=2880 рублей. Это в 12 раз дешевле, чем стоимость одного курса лечения препаратами ТКТ-терапии (1200$ USA).
Таким образом, предлагаемой лечебной композицией и способом лечения решаются следующие задачи:
- разработка простой высокоэффективной технологии лечения ВИЧ-инфицированных больных, доступной для применения в амбулаторных и домашних условиях;
- резкое удешевление лечения ВИЧ-инфицированных больных по сравнению с традиционной технологией лечения;
- снижение токсического воздействия применяемого лекарственного средства на печень и почки по сравнению с официально рекомендуемой медикаментозной терапией.
ИСТОЧНИКИ ИНФОРМАЦИИ:
1. Памятка по проведению антиретровирусной комбинированной терапии ВИЧ-инфекции в Московском городском центре борьбы и профилактики СПИД. Утверждено главным специалистом по СПИДу комитета здравоохранения г. Москвы Горбачевой Э.С. 23.06.1998г.
2. (Прототип) Патент 2149633 РФ; МКИ 7 А 61 К 33/00, 33/14, 33/38; А 61 Р 37/00; БИ 15, 2000 - "Способ лечения иммунодефицитных состояний организма".
3. В. И. Белеванцев, И, В. Бондарчук. Институт неорганической химии СО РАН. Очерк свойств серебра и его соединений./ Применение препаратов серебра в медицине. Препринт 2 /Институт клинической иммунологии, Новосибирск, 1994, с. 89-95/.
4. Роберт Р. Редфилд, Дональд С. Берке. Клиническая картина инфекций вирусом СПИДа /журнал Scientific American, 1988г., с. 60-69, издание на русском языке/.
5. Уильям А. Хэзелтайн, Флосси Воонг-Стааль. Молекулярная биология вируса СПИДа /журнал Scientific American, издание на русском языке, 1988г., с. 20-29/.
6. Durbin P.W. /HIth. Phus, 1960. V.2. P. 225-238/.
7. Stein DS, Korvik JA, Vermund SH. CD4+ lymphocyte cell enumeration for prediction of clinical course of human immunodeficiency virus disease: a review J Infect Dis 1992, 165: 352-63.
8. Mellors JW, Munoz A, Giorgi JV et al. Plasma viral load and CD4+ lymphocytes as prognostic markers of HIV-1 infection, Ann intern Mod 1997,126: 946-54.
Oдним из первых препаратов, использованных для лечения ВИЧ-инфекции, был азидотимидин (АЗТ). У нас он выпускался под названием тимозид, на Западе известен как ретровир, зидовудин (ЗДВ). Суточная доза определяется стадией инфекции и переносимостью препара
Oдним из первых препаратов, использованных для лечения ВИЧ-инфекции, был азидотимидин (АЗТ). У нас он выпускался под названием тимозид, на Западе известен как ретровир, зидовудин (ЗДВ). Суточная доза определяется стадией инфекции и переносимостью препарата. Препарат относится к ингибиторам обратной траскриптазы.
Препаратами второго поколения являются дидеоксииназин (ДДИ), дидеоксицитидин (ДДС). В настоящее время спектр препаратов этой группы значительно расширился (ставудин-ДДТ, хивид, фосфозид и другие).
Эта группа лекарственных средств (ЛС) имеет ряд существенных недостатков. Указанные ЛС не подавляют полностью репликацию вируса, который может быть выделен у большинства больных во время терапии.
Как показали исследования, к ЗДВ достаточно быстро развивается устойчивость, в особенности на поздних стадиях болезни с усиленной репликацией ВИЧ, когда, по-видимому, возникает резистентность и к другим аналогам нуклеозидов.
Обычный фактор, существенно ограничивающий применение ЛС этой группы, — их токсичность. Для ЗДВ характерно главным образом токсическое действие на костный мозг, тогда как ДДИ и ДДС обладают нейротоксическим действием. Кроме того, ДДИ может вызывать тяжелый острый геморрагический панкреатит.
Установлена тесная связь между клинической неэффективностью ЗДВ и резистентностью к нему in vitro.
Вторая группа препаратов, открытая сравнительно недавно и уже широко используемая, — это ингибиторы протеаз: индиновир (криксиван), инвираза (саквиновир), вирасепт (нельфиновир) и другие.
В настоящее время речь не идет уже о монотерапии антиретровирусными средствами, а только о ди-, три- и даже тетратерапии. Такие методики позволяют снижать концентрацию вируса до величин, не определяемых с помощью современных тест-систем (< 200 копий/1 мл).
Предпочтительность комбинированной терапии обосновывается следующими положениями (В. В. Покровский).
- Использование многих этиотропных агентов более эффективно подавляет жизнедеятельность вируса, воздействуя на различные болевые точки или синергически воздействуя на одну из них.
- Это позволяет снизить дозы препаратов, что уменьшает частоту и выраженность побочных эффектов.
- Различные лекарства имеют различную способность проникать в ткани (головной мозг и т. д.).
- Комбинация лекарств затрудняет формирование устойчивости, или она появляется позднее.
Все описанные выше подходы к терапии ВИЧ-инфекции предполагали непосредственное воздействие на репликацию вируса. Другая возможная методика лечения ВИЧ-инфекции состоит в усилении защитных сил макроорганизма. Некоторые варианты такого подхода в большинстве случаев неспецифические, изредка специфические и могут воздействовать на защитные свойства клетки-хозяина.
Интерфероны, как природные, так и рекомбинантные, имеют ряд недостатков: антигенность, необходимость многократного введения для поддержания достаточной концентрации в организме, большое количество побочных эффектов и т. д.
Этих недостатков лишены многие индукторы эндогенного интерферона, некоторые из них способны включаться в синтез ИФН в некоторых популяциях клеток, что в ряде случаев имеет определенное преимущество перед поликлональной стимуляцией иммуноцитов интерфероном.
Специфическая активность циклоферона при ВИЧ-инфекции изучена в 1997 году в Институте гриппа РАМН
- Выявлена выраженная ингибирующая активность циклоферона на репродукцию ВИЧ в культуре клеток моноцитов.
- По показателям ингибирующей активности циклоферон значительно превосходит азидотимидин.
- Представленные экспериментальные данные обосновывают клиническое использование циклоферона для лечения больных ВИЧ-инфекцией.
Пятилетний опыт применения циклоферона у ВИЧ-инфицированных позволяет оценить результаты этой работы.
В период 1992 – 1997 годы в Санкт-петербургском городском центре по профилактике и борьбе со СПИД циклоферон получили 40 пациентов с разными стадиями ВИЧ-инфекции. Следует отметить, что 11 больных прошли два курса терапии циклофероном, в связи с чем общее число лиц, получивших один курс лечения циклофероном, составило 29 человек. В основном это были молодые люди в возрасте до 40 лет (20 человек), в том числе трое детей до 14 лет.
Все больные отмечали хорошую переносимость циклоферона, отсутствие пирогенных реакций после его введения.
Пациенты также констатировали улучшение общего состояния, сна и аппетита, повышение жизненного тонуса, работоспособности. 30% из числа получавших препарат и перенесших в осенне-зимний период грипп или ОРВИ отметили, что заболевание протекало непривычно легко и выздоровление наступило быстрее обычного.
Из клинической практики
После курса циклоферона отмечалось существенное снижение вирусной нагрузки (в 3,6 раза). Число CD4+ возросло на 62%. Монотерапия циклофероном оказала положительное стабильное влияние на изученные показатели у пациентов.
Определенный интерес представляют результаты многолетнего наблюдения больных ВИЧ-инфекцией, которые получали длительно циклоферон в своеобразном профилактическом режиме с целью стабилизации процесса и профилактики прогрессирования заболеваний.
В 1998 году на базе Российского научно-методического Центра по профилактике и борьбе со СПИД (руководитель член-корр. АМН В. В. Покровский) была изучена динамика суррогатных маркеров ВИЧ-инфекций (уровень CD4+) и вирусная нагрузка у больных ВИЧ-инфекцией при лечении циклофероном.
Оценка достоверности полученных результатов проводилась с помощью непараметрических критериев (критерий знаков, максимум-критерий, критерий Вилкоксона для сопряженных совокупностей).
В испытуемую группу вошли 10 взрослых больных ВИЧ-инфекцией в стадии первичных проявлений по Российской классификации ВИЧ-инфекции (В. И. Покровский, 1989 г.). Результаты исследования уровня CD4-лимфоцитов представлены в таблице и на рисунке, из которых видно, что после первых четырех недель исследования наметилась тенденция к повышению среднего уровня CD4-лимфоцитов, которое к 12-й неделе стало статистически достоверным. Это повышение сохранилось до конца исследования, несмотря на
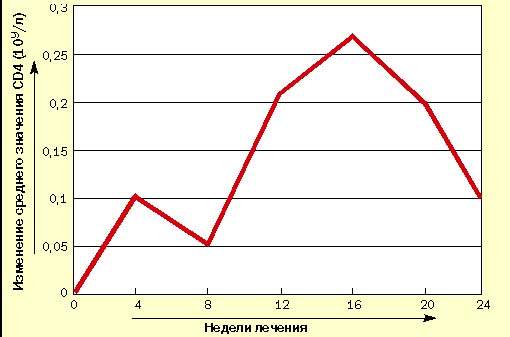 |
| Рисунок 1. Изменение уровня CD4-лимфоцитов у больных ВИЧ-инфекцией при лечении циклофероном (в сравнении с исходным уровнем) |
 |
| Рисунок 2. Средние значения изменения концентрации РНК ВИЧ (log10/мл) |
Таким образом, применение циклоферона в терапии ВИЧ-инфекций сопровождается стабилизацией клинических проявлений заболевания, улучшением состояния, а также гематологических и иммунологических показателей больных.
Циклоферон как монопрепарат оказывает иммуномодулирующее и противовирусное действие при лечении ВИЧ-инфицированных (стадии А1 3Б) в тех случаях, когда нет значительного снижения числа CD4+ клеток (<200). Хорошо зарекомендовало себя назначение циклоферона по следующей схеме.
- По 4 мл препарата в 1, 2, 4, 6, 8, 10, 13, 16, 19 и 22-й дни лечения (у детей по 2 мл). Первые две инъекции могут вводиться внутривенно, остальные внутримышечно. Повторные курсы циклоферона рекомендуется проводить через 6 месяцев под иммунологическим контролем.
- Циклоферон хорошо сочетается со всеми основными лекарственными средствами, его рекомендуется использовать в случае, когда имеются признаки активной репликации ВИЧ (высокие показатели вирусной нагрузки), у больных с обострениями различных оппортунистических заболеваний.
Исчезновение у некоторых больных иммунологических и вирусологических показаний для проведения противоретровирусной терапии может иметь важное значение для разработки новых подходов к проведению лечения больных ВИЧ-инфекцией, для снижения стоимости терапии и отсрочки развития резистентности к ней или преодолению последней.
Циклоферон может оказаться перспективным профилактическим средством при сомнительных контактах и контактах с заведомо ВИЧ-инфицированными партнерами.
Целью исследования явилась оценка эффективности лечения больных острой ВИЧ-инфекцией при раннем назначении антиретровирусной терапии с включением в схему элсульфавирина.
Assessment of efficiency of treatment of patients with acute HIV infection with use in the scheme of antiretroviral therapy elsulfavirin / Ya. S. Ulyanova, D. V. Kapustin, E. I. Krasnova1, V. V. Provorova, N. I. Khokhlova / Novosibirsk state medical university, Novosibirsk, Russia
В доступной литературе мы не нашли данных по использованию эльсульфавирина в комплексном лечении больных острой ВИЧ-инфекцией.
Методы и принципы исследования
Больные находились на лечении в инфекционных отделениях ГБУЗ НСО ГИКБ № 1 г. Новосибирска.
Критерии включения пациентов в исследование:
- возраст 18 лет и старше;
- наличие острой ВИЧ-инфекции, доказанное иммуноферментным анализом (ИФА), иммуноблоттингом (ИБ) и молекулярными методами (ПЦР ДНК ВИЧ);
- подписанное больным добровольное информирование согласие на участие в исследовании.
Критерии исключения пациентов из исследования:
- отказ от обследования;
- нерегулярное наблюдение у врача-инфекциониста в СПИД-центре;
- наличие других заболеваний, приводящих к развитию иммунодефицита (в т. ч. первичные иммунодефициты, длительный прием цитостатических препаратов, аутоиммунные заболевания).
Результаты исследования
Одним из важных факторов, влияющих на приверженность пациентов к АРВТ, является переносимость лекарственных препаратов и развитие нежелательных явлений.
В соответствии с целями и задачами исследования было сформировано 3 группы пациентов. В 1-ю группу вошли 17 человек, которые получали предпочтительную схему первой линии: тенофовир – 300 мг, ламивудин – 300 мг, эфавиренз – 600 мг (TDF + 3TC + EFV). Во 2-ю группу вошли 15 пациентов, получающих альтернативную схему первого ряда: тенофовир – 300 мг, ламивудин – 300 мг, лопинавир/ритонавир – 200 + 50 мг (TDF + 3TC + Lpv/r). В 3-й группе из 25 человек все получали схему, включавшую тенофовир – 300 мг, ламивудин – 300 мг, элсульфавирин – 20 мг (TDF + 3TC + ESV). По уровню исходной вирусной нагрузки РНК ВИЧ-пациенты трех групп были сопоставимы (табл. 1).
Во 2-й группе больных, получавших схему TDF + 3TC + Lpv/r, у 33,3% (5) пациентов вирусная нагрузка не определялась (< 100 копий/мл), у 33,3% (5) – регистрировалась менее 3 log и у 33,4% (5) – регистрировалась в диапазоне 3–5 log.
Учитывая результаты проводимых сравнительных клинических исследований по эффективности элсульфавирина в сравнении с эфавирензом, используемым в клинических исследованиях в качестве эталонного препарата в группе сравнения, доказана аналогичная эфавирензу эффективность элсульфавирина. Полученные нами более эффективные результаты терапии в группе пациентов, принимающих в качестве третьего препарата в АРВТ элсульфавирин, свидетельствуют о низком проценте побочных реакций и, как следствие, высокой приверженности пациентов к лечению, чего не отмечалось в двух других группах и что, возможно, влияло на эффективность терапии.
Анализируя вышесказанное, в качестве стартовой терапии для пациентов с острой ВИЧ-инфекцией мы выбрали наиболее предпочтительную схему АРВТ: тенофовир – 300 мг, ламивудин – 300 мг, элсульфавирин – 20 мг. Прием препаратов – однократный в сутки. На терапию взяты 158 пациентов с острой ВИЧ-инфекцией. Перед началом лечения вирусная нагрузка у 86% (136) пациентов превышала 106 копий/мл и в 14% (22) случаев составляла менее 6 log. После выписки из стационара не дошли до центра СПИДа, т. е. были потеряны, 7 пациентов, что составило 4,4%. Продолжил лечение 151 человек. По результатам 4 недель наблюдения у всех пациентов отмечено снижение вирусной нагрузки более 2 log, при этом в 64,3% случаев (у 97 пациентов) она составила 3 log, а в 22,5% (34) – стала неопределяемой (< 100 копий/мл).
На 12-й неделе выбыли 4 пациента: 1 по причине перевода на схему, содержащую ингибитор интегразы долутегравир, в связи с развившимися нежелательными явлениями на проводимую терапию, и еще 3 пациента были сняты с учета в центре СПИД в связи с переездом в другие регионы. Таким образом, на 12-й неделе терапии обследованы 147 пациентов. Вирусологическая ремиссия, соответствующая неопределяемой вирусной нагрузке (< 100 копий/мл), была достигнута у 67,7% (100) пациентов, у 28,9% (42) – вирусная нагрузка составляла 3 log, у оставшихся 3,4% (5) пациентов вирусная нагрузка не превышала 4 log.
На 24-й неделе терапии вирусологическая ремиссия достигнута в 80,9% (119) случаях, у 13,2% (19) пациентов вирусная нагрузка составляла менее 3 log, у 4% пациентов (6) вирусная нагрузка по-прежнему составляла 4 log, троим из этих больных изменена схема терапии на ингибитор интегразы долутегравир на 24-й неделе и еще троим – в течение последующих 12 недель наблюдения. С 3 пациентами связь была потеряна.
Таким образом, в ходе проводимого наблюдения за эффективностью раннего начала АРВТ у пациентов с острой ВИЧ-инфекцией, в течение 36 недель терапии в 91,8% случаях достигнута вирусологическая ремиссия. Потеряны из-за прекращения посещения центра СПИД и отсутствия с ними связи 6,3% (10 пациентов), 3 человека уехали из Новосибирской области с прикреплением в Центр по профилактике и борьбе со СПИД другого региона.
Заключение
Раннее начало антиретровирусной терапии больным острой ВИЧ-инфекцией с выбором схемы АРВТ, включающей отечественный препарат элсульфавирин с хорошей переносимостью, формирует высокую приверженность к лечению, в короткие сроки купирует высокий уровень виремии, что важно для профилактики распространения заболевания и эффективного лечения.
КОНФЛИКТ ИНТЕРЕСОВ. Авторы статьи подтвердили отсутствие конфликта интересов, о котором необходимо сообщить.
CONFLICT OF INTERESTS. Not declared.
Литература/References
Я. С. Ульянова
Д. В. Капустин
Е. И. Краснова 1 , доктор медицинских наук, профессор
В. В. Проворова, кандидат медицинских наук
Н. И. Хохлова, кандидат медицинских наук
ФГБОУ ВО НГМУ Минздрава России, Новосибирск, Россия
Оценка эффективности лечения больных острой ВИЧ-инфекцией с использованием в схеме антиретровирусной терапии элсульфавирина/ Я. С. Ульянова, Д. В. Капустин, Е. И. Краснова, В. В. Проворова, Н. И. Хохлова
Для цитирования: Ульянова Я. С., Капустин Д. В., Краснова Е. И., Проворова В. В., Хохлова Н. И. Оценка эффективности лечения больных острой ВИЧ-инфекцией с использованием в схеме антиретровирусной терапии элсульфавирина // Лечащий Врач. 2021; 6 (24): 52-55. DOI: 10.51793/OS.2021.24.6.011
Теги: ВИЧ, выбор терапии, комбинированная терапия
У меня ВИЧ. Теперь я должен придерживаться определенной диеты?
Скорее нет. Однако теперь вам придется соблюдать определенные условия, потому что ваше пищеварение может измениться: как от самого заболевания, так и от АРВ-терапии, которую вы принимаете. ВИЧ-позитивные люди часто сталкиваются с такими проблемами как потеря веса, диарея, повышение уровня холестерина.
Каковы основные принципы здорового питания при ВИЧ?
Не существует серьезных различий в принципах здорового питания у ВИЧ-положительных и ВИЧ-отрицательных людей.
Выбирайте нежирную свинину или говядину, куриную грудку, рыбу, цельнозерновые и бобовые продукты. Потребляйте кисломолочные продукты, либо альтернативное молоко (например, соевое), обогащенное кальцием. Выбирайте продукты без добавленного сахара, ограничьте потребление простых углеводов. Не менее 30% ежедневной нормы калорий должно приходиться на жиры, в том числе мононенасыщенные: орехи, авокадо, рыба, оливковое масло.
Какие витамины нужно принимать при ВИЧ-инфекции?
Витамин А и бета-каротин (здоровье кожи и легких): зеленые, желтые, оранжевые или красные овощи и фрукты; печень; яйца; молоко. Помните о том, что витамин А — жирорастворимый, а значит овощные салаты лучше заправлять оливковым маслом.
Витамины группы В (поддержка иммунной и нервной системы): мясо, рыба, курица, орехи, бобы, авокадо, брокколи и зеленые листовые овощи.
Витамин C (защищает от инфекций, что особенно важно на фоне ВИЧ): цитрусовые.
Витамин D (у ВИЧ-позитивных людей критически важен для профилактики развития остеопороза): рыбий жир либо инъекции.
Витамин Е (защищает клетки и помогает бороться с инфекциями): зеленые листовые овощи, арахис и растительные масла.
Железо (борьба с анемией): зеленые листовые овощи, цельнозерновой хлеб, печень, рыба, яйца.
Селен и цинк (важны для иммунной системы): орехи, птица, рыба, яйца и арахис, фасоль, молоко и другие молочные продукты.
Если вам кажется, что вы не получаете достаточно витаминов и микроэлементов с пищей — обсудите с врачом возможность приема поливитаминов.
Что нельзя есть при ВИЧ-инфекции?
На фоне приема Эфавиренца (Стокрин) не рекомендуется есть грейпфруты и помело, пить грейпфрутовый сок и принимать препараты на основе гинкго. Лопиновир (Калетра) не сочетается со зверобоем.
Кроме того, на фоне приема АРВ-терапии следует более внимательно отнестись к препаратам: кальций, железо, магний, алюминий или цинк. Их прием с АРВТ нужно разделять на несколько часов. По этому вопросу лучше проконсультироваться с лечащим врачом.
Может ли диета скорректировать проблемы на фоне приема АРВ-препаратов?
Правильную рекомендацию может дать только врач. Но вот несколько советов, которые точно не сделают хуже.

Если ВИЧ-инфекция и прием АРВ-препаратов сопровождается:
Тошнотой и рвотой
Ешьте небольшими порциями каждые 1-2 часа. Избегайте жирных и острых блюд. Пейте имбирный чай. Следите за тем, чтобы ваша еда была не слишком горячей.
Пейте больше жидкости, чем обычно. Ограничьте прием молочных продукт, свежих овощей и фруктов, сладких напитков или напитков с кофеином. Ешьте медленно. Избегайте жирного.
Попробуйте упражнения (или йогу), которые помогут вам повысить аппетит. Не пейте слишком много прямо перед едой. Настройтесь на прием пищи, ешьте с семьей или друзьями. Пробуйте новые блюда, отнеситесь с фантазией к презентации.
Слишком большой потерей веса
Увеличьте порции. Ешьте сухофрукты, орехи и мороженое. Спросите у врача о возможности принимать белковые добавки. К слишком большой потере веса стоит отнестись серьезно — она может быть связана с присоединением оппортунистических инфекций.
Проблемами с глотанием
Ешьте мягкие продукты: йогурт или картофельное пюре. Не ешьте сырые овощи, отдавайте предпочтение мягким фруктам: бананы или груши. Ограничьте кислое (апельсины, лимоны и помидоры). Посоветуйтесь с врачом: проблемы с глотанием могут быть признаком оппортунистических инфекций.
Липодистрофией (Патологическое состояние, которые характеризуется атрофией или гипертрофией жировой ткани. Чаще встречается у пациентов, которые принимают старые препараты)
Ограничьте жир, особенно насыщенные и трансжиры. Выбирайте “полезные” ненасыщенные жиры и источники омега-3 жирных кислот. Старайтесь меньше потреблять алкоголь и рафинированный сахар. Ешьте больше продуктов, богатых клетчаткой.
Сочетается ли ВИЧ-инфекция с вегетарианством и веганством?
Неопровержимых доказательств обратного пока нет. Но можно отметить, что это тема пока мало изучена.
Если вы собираетесь стать веганом или отказались от животной пищи еще до постановки диагноза, то следует помнить о том, что ВИЧ-инфекцию часто сопровождает потеря веса, а значит вам нужно особенно тщательно подойти к своему рациону и добавкам.
Когда пойдете обсуждать рацион со своим лечащим врачом — вооружитесь. Например, зачитайте ему статью о том, что ВИЧ-позитивный веган стал финалистом конкурса PETA “Самый сексуальный веган по соседству”.
Можно ли пить алкоголь?
Можно, но не усердствуйте! Дело в том, что сегодня люди с ВИЧ живут примерно столько же, сколько и ВИЧ-отрицательные. Но потребление алкоголя может сказаться на долгосрочном качестве жизни. Кроме того, алкоголь может повлиять на способность человека принимать лекарства, а проблемы с приверженностью ведут к последствиям, вплоть до развития лекарственной резистентности.
Также стоит помнить, что алкоголь влияет на печень, что особенно актуально для тех, у кого ВИЧ-инфекция сочетается с гепатитом B или C. Кроме того, недавние исследования показывают, что у ВИЧ-позитивных людей может быть ниже порог “безопасного” потребления этанола.
Читайте также:

