Клиническая картина первичных проявлений инфекции
Обновлено: 19.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Определение
Вирус SARS-CoV-2 распространяется в микроскопических частицах жидкости, выделяемых больным человеком во время кашля, чихания, разговора, пения или тяжелого дыхания и попадает на слизистые носа, рта, либо глаз другого человека.
Кроме того, вирус может также распространяться контактно-бытовым путем, когда частицы с вирусом, находящиеся на поверхностях или предметах, через руки попадают на слизистые респираторного тракта.
Передача инфекции аэрозольным путем происходит в закрытых, переполненных и плохо вентилируемых помещениях.
Симптомы COVID-19 при тяжелой и средней тяжести форме заболевания
Наиболее распространенные симптомы
- Одышка, учащенное дыхание (55%).
- Усиление кашля, появление мокроты (30-35%).
- Кровохарканье (5%).
- Потеря аппетита (20%).
- Спутанность сознания (9%).
- Ощущение сдавления и заложенности в грудной клетке (> 20%).
- Температура тела выше 38°С (80%) более 5 дней.
- Насыщение крови кислородом по данным пульсоксиметрии (SpO2) ≤ 95% (до 20%).
- тахикардия,
- дефицит витамина D,
- раздражительность,
- судороги,
- тревожность,
- угнетенное состояние,
- нарушения сна.
Важно! Симптомы могут не обнаруживаться во время инкубационного периода COVID-19 или проявляться в любой комбинации (например, без температуры). Точный диагноз устанавливает врач по результатам обследований.
У пациентов старше 65 лет может наблюдаться атипичная картина заболевания, которая включают делирий (помутнение сознания), нарушения речи, двигательные расстройства, а также более тяжелые и редкие неврологические осложнения – инсульт, воспалительное поражение мозга и другие.
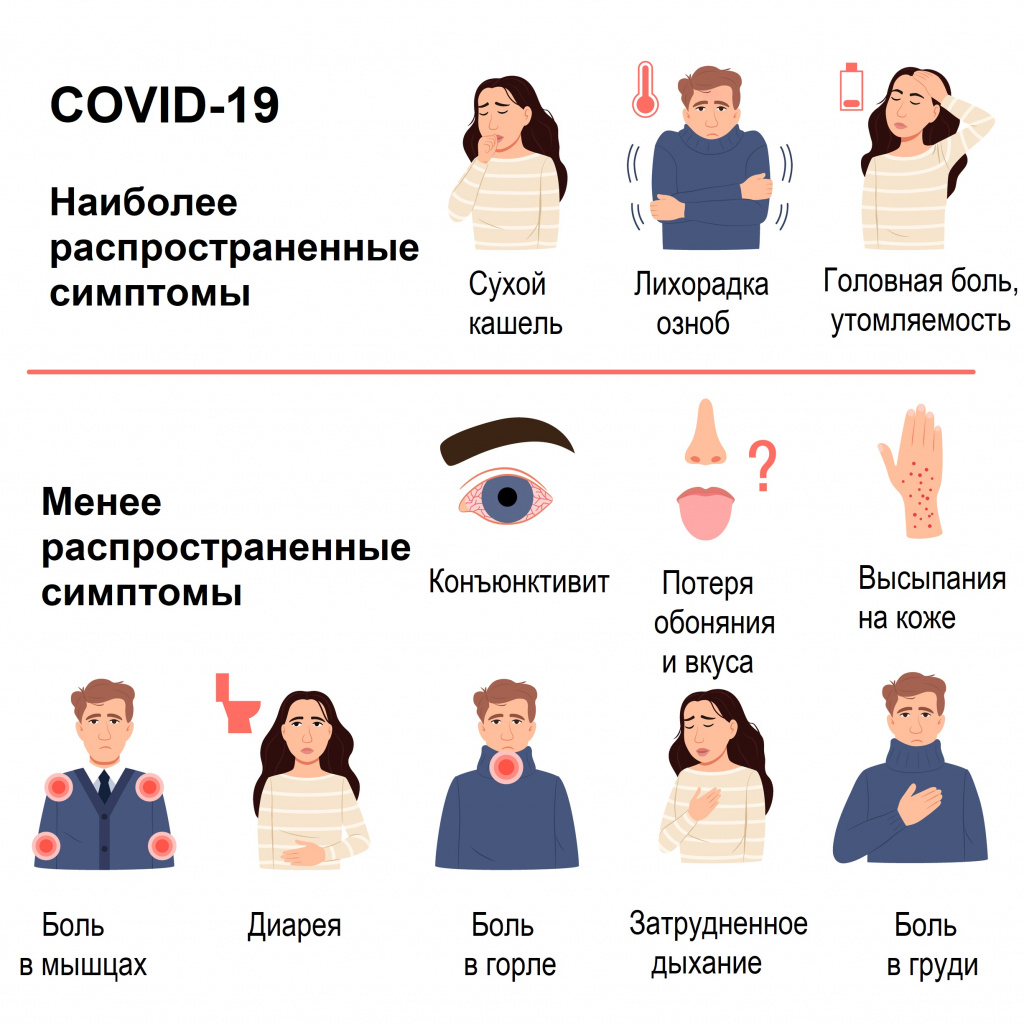
Большинство (около 80%) пациентов, у которых появляются симптомы заболевания, выздоравливают без госпитализации. Примерно у 15% пациентов развивается серьезная форма заболевания, при которой необходима кислородотерапия, а у 5% – крайне тяжелая форма, требующая лечения в условиях отделения интенсивной терапии.
Отличия новой коронавирусной болезни COVID-19 от ОРВИ и гриппа
COVID-19 тоже относится к ОРВИ – острым респираторным вирусным инфекциям, характеризующимся сходными симптомами: кашель, насморк, повышение температуры, головная боль, першение и боли в горле. Наиболее четко выраженную клиническую картину вызывают вирусы гриппа, парагриппа, аденовирусы. Коронавирус может протекать в более тяжелой форме, нежели другие ОРВИ, приводя к осложнениям и даже летальному исходу. Именно поэтому крайне важно отличать новый тип коронавируса от относительно безобидной простуды.
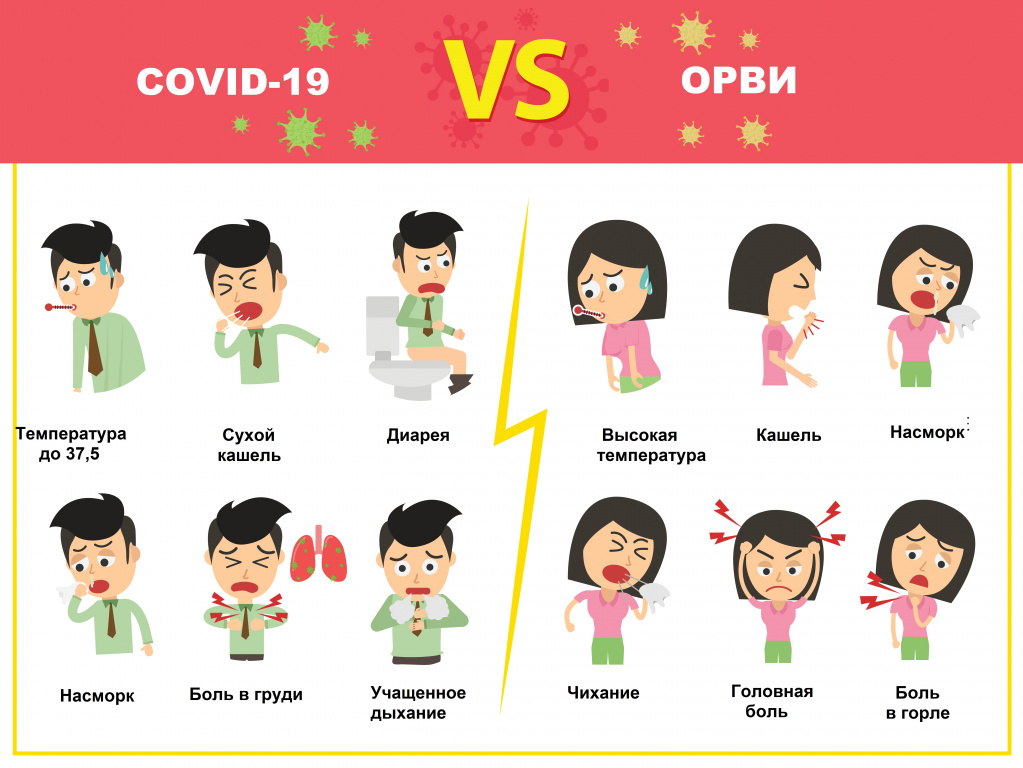
В чем отличие коронавируса от гриппа
Надо отметить, что COVID-19 и грипп имеют много общего:
- передаются воздушно-капельным и контактным путем;
- могут проявляться ломотой в суставах, головной болью, сильной слабостью и общим ощущением разбитости;
- могут возникать кишечные расстройства.
- Грипп начинается остро с повышения температуры сразу до фебрильных значений (39-40⁰С). На первый план выступают симптомы общей интоксикации: головная боль, слабость, боли в мышцах и суставах, слезотечение, боль в глазах.
- Коронавирус развивается постепенно - от общего недомогания в первые дни до выраженных симптомов, включая значимое повышение температуры тела через неделю.
Другие заболевания со схожими симптомами
Пневмонии, в том числе атипичные.
Аллергии. Одышка, проблемы с обонянием и другие симптомы могут возникать в результате воздействия аллергенов. Проблему решают антигистаминные препараты, которые при вирусной инфекции неэффективны.
Бронхиальная астма, которая также дает о себе знать затрудненным дыханием и мучительным кашлем, но имеет неинфекционную природу.
Отличаются ли симптомы у детей и у взрослых?
Дети составляют лишь около 2% от числа всех заболевших COVID-19. При этом они легче переносят коронавирусную инфекцию и часто являются ее бессимптомными носителями.
Протекание COVID-19 у детей разного возраста:
От 1 года до 3 лет
Инфекция обычно проявляется как легкое недомогание. Характерные симптомы COVID-19 не наблюдаются. Иногда присутствует потеря аппетита, которая проходит через 2-3 дня и никак не сказывается на общем самочувствие малыша.
Дети в этом возрасте болеют около семи дней и выздоравливают без осложнений. У них может появиться осиплость голоса и легкая заложенность носа. Кашля нет, не исключены редкие чихания.
У младших школьников и подростков может наблюдаться незначительное повышение температуры тела и легкое недомогание. Возможен сухой кашель, еще реже - головная боль.
По данным Роспотребнадзора, легкая форма заболевания, как правило, обусловлена сильным иммунитетом пациента.
Иммунная система детей и подростков, как правило, хорошо подготовлена к борьбе с вирусами. Они могут заразиться, но заболевание у них протекает в более мягкой форме или вообще бессимптомно.
Этапы развития заболевания с учетом симптомов
Симптомы коронавируса у взрослого человека по дням
1-3-й день. Заболевание начинается с легкого недомогания, незначительного повышения температуры, заложенности носа и боли в мышцах, как при ОРВИ или гриппе.
3-5-й день. Повышается температура тела, возможен несильный, поверхностный кашель. Может пропасть обоняние, а вкусовые ощущения сильно измениться. Возникают пищеварительные расстройства, выражающиеся, в том числе, диареей. Этот период считается кульминацией легкой формы течения COVID-19.
5-10-й день. Важный период для определения тяжести заболевания коронавирусной инфекцией. У 80% заболевших COVID-19 наблюдаются улучшения, которые через несколько дней могут привести к полному выздоровлению. Второй сценарий подразумевает ухудшение состояния, которое проявляется увеличением количества и тяжести симптомов. При таком развитии событий у пациента появляются сильный насморк, изнуряющий кашель, озноб, боль в теле, одышка.
10-12-й день. Этот период характеризуется сильной одышкой, болью в груди, прогрессированием слабости, бледностью, что свидетельствует о развитии пневмонии. Повреждение легких приводит к кислородному голоданию. Требуется госпитализация. Это состояние считается среднетяжелым.
12-14-й день. При COVID-19 75% пациентов с вирусной пневмонией начинают идти на поправку в среднем через 2 недели от начала заболевания. Однако тем, у кого развивается тяжелая форма заболевания, может потребоваться искусственная вентиляция легких.
14-30-й день. На излечение от тяжелой формы пневмонии, вызванной коронавирусом, требуется в среднем до двух недель с момента наступления серьезного осложнения.
Но даже после полного выздоровления может сохраняться одышка в легкой форме, проявляться слабость и недомогание в течение длительного времени (до нескольких месяцев).
- Поражение только верхних отделов дыхательных путей.
- Пневмония без дыхательной недостаточности.
- Острый респираторный дистресс-синдром (пневмония с острой дыхательной недостаточностью).
- Сепсис, септический (инфекционно-токсический) шок.
- Синдром диссеминированного внутрисосудистого свертывания, тромбозы и тромбоэмболии.
- Насыщение крови кислородом менее 88%.
Цитокиновый шторм при COVID-19 - реакция организма на воспалительный процесс, приводящая к тому, что иммунные клетки атакуют не только вирус, но и ткани собственного организма. Следствием этого может стать разрушение тканей и органов, и, как следствие, гибель организма.
Очень важно, что иногда COVID-19 опасен не только пневмонией и ее осложнениями, но и негативным влиянием на сосуды, мозг и сердце, что повышает риск развития инсульта. В таких случаях у пациента наблюдается головокружение, могут случаться обмороки, синеет лицо и немеют мышцы.
Симптомы, свидетельствующие о процессе выздоровления
Внимание! Временные интервалы течения болезни условны, они зависят от индивидуальных особенностей организма. COVID-19 в легкой форме, как правило, протекает не более 14 дней. Но подтвердить окончательное выздоровление может только тест на антитела.
Учитывая тяжесть заболевания, процесс выздоровления может проходить по-разному. Критерий выздоровления – если два последовательно сделанных теста на коронавирус методом ПЦР дали отрицательный результат.
Для проведения исследования в медицинских офисах необходимо предъявить СНИЛС и документ удостоверяющий личность. Запись на исследование В случае получения положительного или сомнительного результата на COVID-19 и при необходимости проведения подтверждающего тестирования обра.
Чума xe "Чума" — зооантропонозная особо опасная карантинная природно-очаговая инфекция, протекающая с выраженной интоксикацией, лихорадкой, поражением лимфатических узлов, лёгких, возможностью септического течения.
Этиология. Возбудитель — неподвижная грамотрицательная бактерия Yersinia pestis семейства Enterobacteriaceae. Устойчива во внешней среде.
Эпидемиология. Основной природный резервуар — различные грызуны (крысы, белки, луговые собачки, сурки и т.д.), определённая роль в передаче возбудителя принадлежит кошкам. В передаче чумы человеку ведущую роль играют взрослые особи крысиных блох (Xenopsylla cheopsis), пожизненно сохраняющие возбудителя. Показано, что человек заражается не столько при укусе, сколько после втирания в кожу масс, срыгиваемых блохой. Передача возбудителя осуществляется также контактным и аспирационным путями.
Патогенез. Возбудитель внедряется в организм в месте укуса блохи; в свою очередь, блохи инфицируются бактериями, питаясь кровью грызунов в период бактериемии, предшествующей гибели животных (трансовариальная передача возбудителя у блох отсутствует, бактерии погибают при попадании в кишечник). При температуре тела блохи 28 °С возбудитель не образует токсичных для человека продуктов. В организме человека клетки, поглощённые нейтрофилами, частично погибают, но выжившие бактерии начинают синтезировать токсические субстанции. Патогенез заболевания до конца не изучен. Ни один Аг или токсин, вырабатываемый возбудителем, в отдельности не в состоянии вызвать болезнь. Механизм развития заболевания включает 3 стадии. • Лимфогенный перенос от места проникновения до лимфатических барьеров • Распространение бактерий из лимфатических узлов в кровоток (бактериемия) • Распространение микробов с появлением вторичных очагов • Примечание. Проникшие возбудители активно поглощают мононуклеарные и полиморфонуклеарные фагоциты, однако фагоцитарные реакции носят незавершённый характер и способствуют дальнейшему распространению возбудителя. Особо важное значение имеют бурное размножение возбудителя, его локализация около капилляров и сосудов, обусловливающая быстрое проникновение в кровоток.
• Бубонная чума. Кардинальный признак — бубон (чаще подмышечный или паховый), ранний признак — ощущение сильной боли в месте будущего развития бубона (часто больной вынужден принимать неестественные позы). Бубон спаян с окружающими тканями. Увеличиваясь до 1–10 см в диаметре, он размягчается, может нагноиться и спонтанно дренироваться. В случае развития геморрагического некроза лимфатического узла и утраты барьерной функции в кровоток поступает большое количество бактерий, что ведёт к вторичной чумной пневмонии и/или генерализованному чумному сепсису. Как осложнение вторичная лёгочная чума составляет 5–10% бубонных поражений и резко утяжеляет состояние больного; иногда регистрируемый (вследствие генерализации) вторичный чумной менингит, как правило, заканчивается смертью больного. Смертность при нелеченой бубонной чуме — 75%. При выздоровлении бубон претерпевает обратное развитие или склерозируется.
• Первично-лёгочная чума — молниеносная и чрезвычайно контагиозная форма; распространяется воздушно-капельным путём и эпидемически наиболее опасна. Проявляется ранним возникновением болей в грудной клетке, кашлем с кровавой мокротой, развитием сердечно-лёгочной недостаточности. Больной выделяет с мокротой большое число возбудителей, при этом объём мокроты может достигать огромных количеств. Показатель смертности в нелеченых случаях близок к 100%. Смерть наступает через 2–6 сут после первичного аэрогенного контакта с инфекцией.
• Кишечная чума проявляется профузной диареей с обильными выделениями крови и слизи, возможны сильные боли в эпигастральной области и чувство общего недомогания, обычно заканчивается смертью больного.
• Первично-септическая чума характеризуется многочисленными геморрагиями на коже и слизистых оболочках; тяжёлые случаи характеризуются массивными кровотечениями из почек, кишечника и примесью крови в рвотных массах. Генерализация процесса возникает без предшествующих явлений местного порядка; типичны исключительно быстрое диссеминирование возбудителя в организме, массивные интоксикация и бактериемия. Заболевание быстро заканчивается смертью больного.
• Вторично-септическая чума — исход (осложнение) других форм болезни, протекает также крайне тяжело, клинически проявляется возникновением вторичных очагов инфекции, бубонов и признаками геморрагической септицемии.
• Вторично-лёгочная форма — осложнение бубонной чумы, клинически сходна с первичной. Течение доброкачественное. Представляет эпидемиологическую опасность.
Методы исследования • Бактериологическое исследование отделяемого бубона (при бубонной форме), содержимого язвы или других кожных поражений (кожная форма), мокроты и слизи из зева (лёгочная форма), крови (все формы), фекалий и ликвора (при поражениях кишечника или мозговых оболочек). Материал следует получить до начала антибиотикотерапии • Возможно проведение ускоренной диагностики чумы с помощью бактериофага Yersinia pestis • Для быстрого обнаружения также применяют АТ, меченые флюоресцеином (позволяет обнаружить Yersinia pestis в течение первых 2 ч исследования), реакцию нейтрализации АТ, реакцию преципитации в стандартных агаровых пластинках и метод ускоренного роста Yersinia pestis на средах обогащения • Вероятность выделения возбудителя увеличивает биологическая проба на лабораторных животных. Разработаны методы, ускоряющие биологическую пробу, например введение заражённым животным ГК или куриного желтка, что ускоряет диагностику чумы в случаях снижения вирулентности или при применении малой заражающей дозы.
Дифференциальную диагностику проводят с другими состояниями, сопровождаемыми бактериемией, с пневмококковой пневмонией и лимфаденитами различной этиологии.
Лечение • Стрептомицин 30 мг/кг/сут в/м в 4 приёма каждые 6 ч в течение 7–10 дней. Предположительно равноэффективен гентамицин. При септической или лёгочной форме лечение следует начинать в первые сутки заболевания • Альтернативный препарат — тетрациклин 25–50 мг/кг в 4 приёма в течение 10 дней • При чумном менингите — хлорамфеникол в начальной дозе 25 мг/кг в/в, затем по 10–15 мг/кг в/в или внутрь 4 р/сут в течение 10 дней.
Осложнения • Прогрессирование бубонной формы до септической и лёгочной форм • Некроз бубона • Перикардит • Респираторный дистресс-синдром взрослых • Менингит.
МКБ-10 • A20 Чума
Код вставки на сайт
Чума xe "Чума" — зооантропонозная особо опасная карантинная природно-очаговая инфекция, протекающая с выраженной интоксикацией, лихорадкой, поражением лимфатических узлов, лёгких, возможностью септического течения.
Этиология. Возбудитель — неподвижная грамотрицательная бактерия Yersinia pestis семейства Enterobacteriaceae. Устойчива во внешней среде.
Эпидемиология. Основной природный резервуар — различные грызуны (крысы, белки, луговые собачки, сурки и т.д.), определённая роль в передаче возбудителя принадлежит кошкам. В передаче чумы человеку ведущую роль играют взрослые особи крысиных блох (Xenopsylla cheopsis), пожизненно сохраняющие возбудителя. Показано, что человек заражается не столько при укусе, сколько после втирания в кожу масс, срыгиваемых блохой. Передача возбудителя осуществляется также контактным и аспирационным путями.
Патогенез. Возбудитель внедряется в организм в месте укуса блохи; в свою очередь, блохи инфицируются бактериями, питаясь кровью грызунов в период бактериемии, предшествующей гибели животных (трансовариальная передача возбудителя у блох отсутствует, бактерии погибают при попадании в кишечник). При температуре тела блохи 28 °С возбудитель не образует токсичных для человека продуктов. В организме человека клетки, поглощённые нейтрофилами, частично погибают, но выжившие бактерии начинают синтезировать токсические субстанции. Патогенез заболевания до конца не изучен. Ни один Аг или токсин, вырабатываемый возбудителем, в отдельности не в состоянии вызвать болезнь. Механизм развития заболевания включает 3 стадии. • Лимфогенный перенос от места проникновения до лимфатических барьеров • Распространение бактерий из лимфатических узлов в кровоток (бактериемия) • Распространение микробов с появлением вторичных очагов • Примечание. Проникшие возбудители активно поглощают мононуклеарные и полиморфонуклеарные фагоциты, однако фагоцитарные реакции носят незавершённый характер и способствуют дальнейшему распространению возбудителя. Особо важное значение имеют бурное размножение возбудителя, его локализация около капилляров и сосудов, обусловливающая быстрое проникновение в кровоток.
• Бубонная чума. Кардинальный признак — бубон (чаще подмышечный или паховый), ранний признак — ощущение сильной боли в месте будущего развития бубона (часто больной вынужден принимать неестественные позы). Бубон спаян с окружающими тканями. Увеличиваясь до 1–10 см в диаметре, он размягчается, может нагноиться и спонтанно дренироваться. В случае развития геморрагического некроза лимфатического узла и утраты барьерной функции в кровоток поступает большое количество бактерий, что ведёт к вторичной чумной пневмонии и/или генерализованному чумному сепсису. Как осложнение вторичная лёгочная чума составляет 5–10% бубонных поражений и резко утяжеляет состояние больного; иногда регистрируемый (вследствие генерализации) вторичный чумной менингит, как правило, заканчивается смертью больного. Смертность при нелеченой бубонной чуме — 75%. При выздоровлении бубон претерпевает обратное развитие или склерозируется.
• Первично-лёгочная чума — молниеносная и чрезвычайно контагиозная форма; распространяется воздушно-капельным путём и эпидемически наиболее опасна. Проявляется ранним возникновением болей в грудной клетке, кашлем с кровавой мокротой, развитием сердечно-лёгочной недостаточности. Больной выделяет с мокротой большое число возбудителей, при этом объём мокроты может достигать огромных количеств. Показатель смертности в нелеченых случаях близок к 100%. Смерть наступает через 2–6 сут после первичного аэрогенного контакта с инфекцией.
• Кишечная чума проявляется профузной диареей с обильными выделениями крови и слизи, возможны сильные боли в эпигастральной области и чувство общего недомогания, обычно заканчивается смертью больного.
• Первично-септическая чума характеризуется многочисленными геморрагиями на коже и слизистых оболочках; тяжёлые случаи характеризуются массивными кровотечениями из почек, кишечника и примесью крови в рвотных массах. Генерализация процесса возникает без предшествующих явлений местного порядка; типичны исключительно быстрое диссеминирование возбудителя в организме, массивные интоксикация и бактериемия. Заболевание быстро заканчивается смертью больного.
• Вторично-септическая чума — исход (осложнение) других форм болезни, протекает также крайне тяжело, клинически проявляется возникновением вторичных очагов инфекции, бубонов и признаками геморрагической септицемии.
• Вторично-лёгочная форма — осложнение бубонной чумы, клинически сходна с первичной. Течение доброкачественное. Представляет эпидемиологическую опасность.
Методы исследования • Бактериологическое исследование отделяемого бубона (при бубонной форме), содержимого язвы или других кожных поражений (кожная форма), мокроты и слизи из зева (лёгочная форма), крови (все формы), фекалий и ликвора (при поражениях кишечника или мозговых оболочек). Материал следует получить до начала антибиотикотерапии • Возможно проведение ускоренной диагностики чумы с помощью бактериофага Yersinia pestis • Для быстрого обнаружения также применяют АТ, меченые флюоресцеином (позволяет обнаружить Yersinia pestis в течение первых 2 ч исследования), реакцию нейтрализации АТ, реакцию преципитации в стандартных агаровых пластинках и метод ускоренного роста Yersinia pestis на средах обогащения • Вероятность выделения возбудителя увеличивает биологическая проба на лабораторных животных. Разработаны методы, ускоряющие биологическую пробу, например введение заражённым животным ГК или куриного желтка, что ускоряет диагностику чумы в случаях снижения вирулентности или при применении малой заражающей дозы.
Дифференциальную диагностику проводят с другими состояниями, сопровождаемыми бактериемией, с пневмококковой пневмонией и лимфаденитами различной этиологии.
Лечение • Стрептомицин 30 мг/кг/сут в/м в 4 приёма каждые 6 ч в течение 7–10 дней. Предположительно равноэффективен гентамицин. При септической или лёгочной форме лечение следует начинать в первые сутки заболевания • Альтернативный препарат — тетрациклин 25–50 мг/кг в 4 приёма в течение 10 дней • При чумном менингите — хлорамфеникол в начальной дозе 25 мг/кг в/в, затем по 10–15 мг/кг в/в или внутрь 4 р/сут в течение 10 дней.
Осложнения • Прогрессирование бубонной формы до септической и лёгочной форм • Некроз бубона • Перикардит • Респираторный дистресс-синдром взрослых • Менингит.
Этиология. Возбудитель — ВИЧ рода Retrovirus подсемейства Lentivirinae семейства Retroviridae. ВИЧ погибают при температуре 56 °С в течение 30 мин, но устойчивы к низким температурам; быстро погибают под действием этанола, эфира, ацетона и обычных дезинфицирующих средств. В крови и других биологических средах при обычных условиях сохраняют жизнеспособность в течение нескольких суток. Известно 2 типа вируса • ВИЧ-1 (HIV-1; ранее известен как HTLV-III или LAV) распространён в Северной и Южной Америке, Европе, Азии, Центральной, Южной и Восточной Африке • ВИЧ-2 (HIV-2) — менее вирулентный вирус; редко вызывает типичные проявления СПИДа; основной возбудитель СПИДа в Западной Африке.
Эпидемиология. Источник инфекции — человек в любой стадии инфекционного процесса. Вирус выделяют из крови, спермы, влагалищного секрета, материнского молока (эти жидкости определяют пути передачи вируса), слюны. Пути передачи — половой, парентеральный, трансплацентарный, через материнское молоко. Группы риска • Гомосексуальные и бисексуальные мужчины (43%) • Наркоманы, вводящие наркотики в/в (31%) • Гетеросексуалы (10%) • Реципиенты крови и её компонентов, трансплантируемых органов (2%) • Больные гемофилией (1%).
Классификация (Покровский В.И., 1989) • I стадия — инкубация • II стадия — первичных проявлений •• Фаза А — острая инфекция (мононуклеозоподобный синдром) •• Фаза Б — бессимптомная (латентная) •• Фаза В — генерализованная лимфаденопатия • III стадия — вторичных заболеваний. Подразделение по фазам на основании клинического симптомокомплекса •• Фаза А — дефицит массы тела до 10% исходной, поверхностные поражения кожи и слизистых оболочек грибковой, бактериальной и/или вирусной этиологии •• Фаза Б — дефицит массы тела более 10%, рецидивирующие или стойкие поражения кожи и слизистых оболочек или внутренних органов грибковой, бактериальной и/или вирусной этиологии, беспричинная диарея и/или лихорадка продолжительностью более 1 мес, рецидивирующий опоясывающий лишай, туберкулёз лёгких, локализованная саркома Капоши •• Фаза В — кахексия, генерализованные инфекции различной этиологии, диссеминированная саркома Капоши, внелёгочный туберкулёз, атипичный микобактериоз, пневмоцистная пневмония, кандидоз пищевода, поражения ЦНС различной этиологии • IV стадия — терминальная.
Патогенез
• Популяции клеток, поражаемые ВИЧ •• ВИЧ поражает СD4 + -клетки (моноциты, макрофаги и родственные клетки, экспрессирующие СD4-подобные молекулы), используя молекулу СD4 в качестве рецептора; эти клетки распознают Аг и выполняют функции Т-хелперов/амплификаторов •• Инфицирование возможно при фагоцитозе иммунных комплексов, содержащих ВИЧ и АТ. Заражение моноцитов и макрофагов не сопровождается цитопатическим эффектом, и клетки становятся персистивной системой для возбудителя.
• Ткани, в которых ВИЧ способен репродуцироваться в организме заражённого индивида •• Основными считают лимфоидные ткани. Возбудитель репродуцируется постоянно, даже на ранних стадиях •• В ЦНС — микроглия •• Эпителий кишечника.
• Ранняя виремическая стадия •• Вирус реплицируется в течение различных промежутков времени в небольших количествах •• Временное уменьшение общего числа СD4 + -клеток и возрастание числа циркулирующих ВИЧ-инфицированных СD4 + -Т-лимфоцитов •• Циркуляцию ВИЧ в крови выявляют в различные сроки; вирусемия достигает пика к 10–20-м суткам после заражения и продолжается до появления специфических АТ (до периода сероконверсии).
• Бессимптомная стадия. В течение различных периодов времени (до 10–15 лет) у ВИЧ-инфицированных симптомы болезни отсутствуют. В этот период защитные системы организма эффективно сдерживают репродукцию возбудителя •• Гуморальные реакции — синтез АТ различных типов, не способных оказывать протективный эффект и не предохраняющих от дальнейшего развития инфекции •• Клеточные иммунные реакции — способны либо блокировать репродукцию возбудителя, либо предотвращать проявления инфекции. Вероятно, цитотоксические реакции доминируют у ВИЧ-инфицированных с длительным отсутствием клинических проявлений.
• Иммунодепрессия •• Уменьшение количества циркулирующих СD4 + -клеток ••• Уменьшение количества циркулирующих СD4 + T-клеток, что существенно для репликации интегрированного ВИЧ. Репликацию интегрированного ВИЧ in vitro активирует митотическая или антигенная стимуляция инфицированных Т-клеток или сопутствующая герпетическая инфекция ••• Возможная причина уменьшения количества Т-клеток — проявление цитопатического эффекта, вызванного репликацией вируса. Заражение Т-клеток in vitro не всегда продуктивно; вирусный геном в интегрированном состоянии может оставаться неэкспрессированным в течение долгого периода времени, в то время как число Т-клеток постоянно уменьшается ••• Появление вирусных гликопротеинов в мембране заражённых Т-клеток — пусковой механизм для запуска иммунных механизмов, направленных против подобных клеток. Механизмы реализации — активация цитотоксических Т-клеток и реакция АТ-зависимой цитотоксичности ••• Аккумуляция неинтегрированной вирусной ДНК в цитоплазме инфицированных клеток обусловливает бурную репликацию ВИЧ и гибель клеток ••• ВИЧ инфицирует клетки-предшественники в тимусе и костном мозге, что приводит к отсутствию регенерации и уменьшению пула СD4 + -лимфоцитов ••• Снижение количества СD4 + -лимфоцитов сопровождается падением активности ТН1-субпопуляции Т-клеток (однако доказательств того, что возрастает активность клеток ТН2, нет). Дисбаланс между субпопуляциями клеток ТН1 и ТН2 предшествует развитию СПИДа. Уменьшается активность цитотоксических Т-клеток и клеток естественных киллеров, что связано с дефицитом CD4 + -лимфоцитов. Ответ В-клеток тоже ослабевает по мере численного сокращения ТН2-субпопуляции ••• Дефекты гуморальных реакций на различные Аг обусловлены дефицитом Т-хелперов. В-лимфоциты находятся в состоянии постоянной поликлональной активации •• Вследствие поликлональной активации и дефекта регуляторных механизмов В-клетки продуцируют АТ к Аг ВИЧ с низкой специфичностью, перекрёстно реагирующие с ядерными, тромбоцитарными и лимфоцитарными аутоантигенами.
• Механизмы, позволяющие ВИЧ избегать действия факторов иммунологического надзора •• Повышенный гуморальный анти-ВИЧ-ответ, ещё более выраженный на фоне СПИДа •• Интеграция генома ВИЧ в ДНК хозяина при минимальной экспрессии вирусных генов •• Мутации ВИЧ в эпитопе gp120. ВИЧ мутирует гораздо чаще, чем большинство других вирусов, т.к. обратная транскриптаза ВИЧ работает с ошибками и лишена корригирующей активности •• Клеточные иммунные реакции.
КЛИНИЧЕСКАЯ КАРТИНА
Инкубационный период продолжается от 2–6 нед до нескольких месяцев (в большинстве случаев) и даже нескольких лет. Характерно бессимптомное течение.
Стадия первичных проявлений (II стадия) — волнообразное развитие клинических проявлений заболевания • Начальная фаза острой инфекции (фаза А) •• В 15% случаев развивается так называемый мононуклеозоподобный синдром (острый ретровирусный синдром): повышение температуры тела до 38–39 °С, распространённая периферическая лимфаденопатия, явления фарингита (боль в горле, катаральные изменения в ротоглотке), экзантема (эритематозная пятнисто-папулёзная сыпь на лице и туловище, иногда на конечностях в области ладоней и подошв) и появление в крови атипичных мононуклеаров •• Одновременно могут развиваться поражения слизистых оболочек — афтозный стоматит, эзофагит, язвы на слизистой оболочке половых органов. Больного могут беспокоить головная боль, миалгии и артралгии, диспептические явления (тошнота, рвота, диарея) •• У части больных возникает молочница, определяется гепатоспленомегалия. В редких случаях в фазу А отмечают снижение массы тела, возникают неврологические нарушения: асептический менингит, менингоэнцефалит, нейро- или радикулопатии, невриты, парезы и т.д. Может развиться тяжёлый острый или подострый энцефалит, вызванный ВИЧ и, как правило, заканчивающийся летально. Длительность фазы А варьирует от нескольких дней до 3–4 нед • При регрессировании и исчезновении клинических проявлений наступает бессимптомная (латентная) фаза (фаза Б), она может длиться нескольких месяцев или лет. В эту фазу ещё нет выраженного иммунодефицита, и диагноз может быть поставлен только лабораторно на основании выявления специфических вирусных Аг или АТ • Генерализованная лимфаденопатия (фаза В) — лимфаденопатия сохраняется во все последующие периоды болезни. Подозрение на ВИЧ-инфекцию при этом возникает в тех случаях, когда поражены лимфатические узлы не менее чем трёх различных областей, расположенных в верхних отделах тела (выше диафрагмы). Диаметр лимфатических узлов у взрослых больных не менее 1 см, а длительность проявлений лимфаденопатии превышает 2 мес • У многих больных первичные клинические проявления отсутствуют; ВИЧ-инфекция протекает латентно вплоть до стадии вторичных заболеваний. Общая продолжительность II стадии заболевания варьирует от 2–3 мес до 8–10 лет.
Терминальная стадия (IV фаза) продолжается вплоть до летального исхода.
Сопутствующие заболевания • Сифилис (у ВИЧ-инфицированных протекает тяжелее) • Туберкулёз. Больных туберкулёзом исследуют на ВИЧ, или, при отсутствии такой возможности, их лечат комплексно, по схеме, применяемой для лечения туберкулёза у ВИЧ-инфицированных.
МЕТОДЫ ИССЛЕДОВАНИЯ. Алгоритм диагностики: ИФА (первичное выделение АТ к ВИЧ), при положительном результате — иммуноблоттинг для подтверждения диагноза. При отрицательном результате иммуноблоттинга целесообразно исследование крови методом ПЦР для выявления реплицирующегося вируса • Твёрдофазный ИФА выявляет АТ к ВИЧ •• АТ, выявляемые ИФА, появляются в крови примерно через 2 мес с момента заражения. У 95% инфицированных они появляются лишь через 5–8 мес •• Антигенемию выявляют модифицированной иммуноферментной пробой, обнаруживающей р24 Аг в сыворотке крови, обработанной кислотой (в результате процедуры разрушаются иммунные комплексы и высвобождаются Аг) • Вестерн-блоттинг (иммуноблоттинг) применяют для подтверждения диагноза ВИЧ-инфекции. Метод обнаруживает специфические АТ в сыворотке крови и является только подтверждающим тестом. Результаты рассматривают как положительные после обнаружения АТ к р24, р31, gp41, gp120 •• Рекомендовано применение реакций с двумя Аг из трёх групп: р24, gp41 и gp120/160. При неопределённых результатах исследование повторяют через 3 и 6 мес •• АТ к р24 Аг появляются через 6 нед после заражения (АТ к gp120 и gp41 обнаруживают раньше). Поскольку АТ во время первичных проявлений инфекции обычно отсутствуют, то серонегативный больной, относящийся к группе повышенного риска, должен пройти повторный тест спустя 6 нед. В редких случаях сероконверсия может развиваться через год или более. Проба на р24 Аг положительная у 85–95% заражённых детей в возрасте 4–6 мес; значительно реже Аг обнаруживают у детей младше 4 мес •• На поздних стадиях ВИЧ-инфекции результаты серологических исследований могут быть ложноотрицательными, что обусловлено снижением титров АТ и уровня образования дочерних популяций возбудителя из-за общего снижения чувствительных иммунокомпетентных клеток •• Методы, выявляющие АТ, не пригодны для диагностики ВИЧ-инфекции у новорождённых, т.к. материнские IgG могут присутствовать в сыворотке ребёнка до года и более • Альтернативные методы исследования •• Виремию выявляют в культуре клеток in vitro и ПЦР с кровью пациента •• Выделение вируса in vitro и выявление генетического материала возбудителя ПЦР. Результаты положительны у 35–55% инфицированных новорождённых в возрасте менее 1 нед и у 90–100% детей в возрасте 3–6 мес • Определение прогрессирующего уменьшения числа СD4 + -лимфоцитов •• Выявление маркёров активации лейкоцитов, например, молекул, выделяемых при активации Т-лимфоцитов ( b 2-микроглобулин, растворимый рецептор ИЛ-2, растворимый СD8), и молекулы, выделяемой при активации моноцитов (неоптерин) •• Постоянное возрастание содержания b 2-микроглобулина и неоптерина характерно для слабого развития симптоматической инфекции. Сочетание уменьшения числа клеток CD4 + и повышения уровня b 2-микроглобулина или неоптерина, либо снижение CD4 + -клеток и обнаружение Аг р24 свидетельствует о более обоснованном прогнозе развития СПИДа, чем просто низкое содержание CD4 + -лимфоцитов • Серологические исследования на токсоплазмоз. У 80% токсоплазмоз развивается после уменьшения количества CD4 + -клеток до 100/мкл и ниже • Исследование биопсийного материала кожи перианальной области у ВИЧ-позитивных женщин, т.к. они более подвержены инфекции ВПЧ.
ЛЕЧЕНИЕ
Тактика ведения • Сбор максимально полной информации о прошлых заболеваниях и результатах их лечения • Тщательный осмотр пациента по органам и системам, обращают внимание на лихорадку неясного генеза, продолжительную диарею, снижение массы тела, аденопатию, язвы в ротовой полости, дисфагию, кашель, учащение дыхания, одышку при нагрузке, кожные высыпания, синуситы • Частоту обследований определяют по клинической картине, психическому статусу больного, необходимости в контроле над функцией иммунной системы и развитием побочных эффектов ЛС • Во время последующих визитов к врачу проводят полное и тщательное физикальное обследование всех систем органов • Определение содержания Т-хелперов проводят в зависимости от стадии заболевания каждые 3–6 мес • Активность репродукции возбудителя определяют качественной ПЦР • У ВИЧ-инфицированных женщин отмечают повышенный риск развития рака шейки матки. Необходимо выполнять мазки по Папаниколау каждые 6 мес или чаще.
Этиотропное лечение • Назначают одновременно не менее 2 препаратов для предупреждения быстрого развития резистентности. Следует учесть вероятность развития множества побочных эффектов ЛС • Ингибиторы обратной транскриптазы ВИЧ •• Зидовудин 500–1 500 мг/сут в 4–6 приёмов. Рекомендован при содержании CD4 + -клеток >500/мкл; беременным ВИЧ-серопозитивным женщинам (между 14 и 34 нед беременности); лицам, заразившимся ВИЧ (например, при уколе иглой); детям до 6 нед, рождённым от ВИЧ-инфицированных матерей. Противопоказан при выраженной нейтропении, значительном снижение концентрации Hb. При лечении рекомендовано проводить исследования крови каждые 2 нед в течение первых 3 мес, затем не реже 1 р/мес •• Залцитабин по 0,75 мг 3 р/сут; рекомендован при поздней стадии заболевания (монотерапия при непереносимости или неэффективности зидовудина или в сочетании с зидовудином). При появлении побочных эффектов (чаще всего анемии и нейтропении) препарат отменяют или корректируют схему лечения. Крайне осторожно следует применять при периферической невропатии, панкреатите и застойной сердечной недостаточности в анамнезе, кардиомиопатии. Во время лечения рекомендовано систематическое исследование общего и биохимического анализа крови •• Диданозин 125–200 мг каждые 12 ч за 30 мин до приёма пищи; наиболее эффективен в сочетании с азидотимидином. Побочные эффекты: панкреатит, тошнота, рвота, боли в животе, диспепсия, периферическая невропатия и др. При появлении признаков панкреатита лечение следует прекратить. С осторожностью назначают при панкреатите в анамнезе, злоупотреблении алкоголем, нарушении функций почек. Антациды, содержащие магний или алюминий, усиливают побочные эффекты. Не рекомендован одновременный приём с тетрациклином • Ингибиторы протеаз (наиболее эффективны в сочетании с ингибиторами обратной транскриптазы) •• Саквиновир по 600 мг 3 р/сут. Противопоказан детям до 13 лет. Побочные эффекты: головные боли, миалгия, сыпь, зуд, изъязвление слизистой оболочки ротовой полости, тошнота, диарея и др. Следует применять с осторожностью при поражении печени и почек. Кетоконазол повышает, а рифампицин снижает концентрацию препарата в плазме •• Индинавир по 800 мг 3 р/сут (при печёночной недостаточности, нефролитиазе, в комбинации с кетоконазолом — по 600 мг 3 р/сут). Противопоказан детям. При приёме препарата рекомендовано выпивать не менее 1,5 л жидкости в сутки. Необходим контроль за появлением признаков нефролитиаза. Совместим с ко-тримоксазолом, флуконазолом, изониазидом, кларитромицином, пероральными контрацептивами. Не рекомендованы комбинации с рифампицином, цисапридом • Ингибиторы сборки и созревания дочерних популяций, например a -ИФН.
Профилактика оппортунистических инфекций. • Пневмонии, вызванной Pneumocystis carinii, — всем пациентам с пневмоцистозами в анамнезе; с содержанием CD4 + -клеток Streptococcus pneumoniae, — пневмококковая вакцина (пневмо 23) каждые 5 лет • Гриппозной инфекции, вызванной вирусами типа А и В, — ежегодная вакцинация против гриппа • Криптококковый менингит — амфотерицин В для лечения активной формы заболевания, флуконазол для первичной профилактики или предотвращения рецидивов • Церебральный токсоплазмоз — пириметамин и сульфадиазин натрия (или клиндамицин); ко-тримоксазол для первичной профилактики • При микобактериальной инфекции •• Инфекция, вызываемая Mycobacterium tuberculosis, — изониазид ежедневно в течение 1 года •• Инфекция, вызванная Mycobacterium avium-intracellulare, — рифампицин (у пациентов с симптомами СПИДа или при снижении содержания CD4 + -клеток
Течение и прогноз. После бессимптомного периода у 80–100% пациентов развивается симптоматическая ВИЧ-инфекция, а около 50–100% обречены на развитие клинически выраженного СПИДа. После перехода ВИЧ-инфекции к СПИДу ожидаемая продолжительность жизни не превышает 2–3 лет. Пока число CD4 + -лимфоцитов не снижается менее 200/мкл, СПИД (включая оппортунистические инфекции) обычно не развивается. При ВИЧ-инфекции число Т-хелперов уменьшается со скоростью 50–80/мкл/год с более быстрым снижением их количества по достижении уровня 200/мкл.
Профилактика • Изменение отношения общества к проблемам внебрачных половых связей, проституции, гомосексуализма • Воспитание у молодёжи нравственности, ответственности и соответствующих гигиенических навыков • Обучение населения правильному сексуальному поведению: ограничение числа половых партнеров и использование презервативов • В медицинских учреждениях необходимо выполнять правила использования и стерилизации шприцев, игл и других инструментов • Борьба с наркоманией. Наркоманы, вводящие наркотики в/в, составляют основную группу вновь выявленных ВИЧ-инфицированных в Российской Федерации.
МКБ-10 • B20 Болезнь, вызванная ВИЧ, проявляющаяся в виде инфекционных и паразитарных болезней • B21 Болезнь, вызванная ВИЧ, проявляющаяся в виде злокачественных новообразований • B22 Болезнь, вызванная ВИЧ, проявляющаяся в виде других уточнённых болезней • B23 Болезнь, вызванная ВИЧ, проявляющаяся в виде других состояний • B24 Болезнь, вызванная ВИЧ, неуточнённая
В повседневной практике педиатру часто приходится сталкиваться с различными изменениями на коже пациентов. По статистике, различные поражения кожи являются причиной почти 30% всех обращений к педиатру. Иногда это только дерматологические проблемы, иногда высыпания являются проявлениями аллергической или соматической патологии, но в последнее время существенно вырос процент дерматологических проявлений инфекционных заболеваний. Иными словами, синдром инфекционной экзантемы прочно входит в нашу практику и требует определенной осведомленности, так как порой он является одним из главных диагностических признаков, позволяющих своевременно поставить диагноз и избежать тяжелых последствий.
Экзантемы являются одним из наиболее ярких и значимых в диагностическом и дифференциально-диагностическом отношении симптомов. Они встречаются при многих инфекционных заболеваниях, которые даже получили название экзантематозных (корь, краснуха, скарлатина, брюшной и сыпной тифы, ветряная оспа, герпетические инфекции). При них сыпь - обязательный компонент клинической картины заболевания, вокруг нее как бы разворачивается диагностический процесс, на нее опирается и дифференциальный диагноз. Существует также группа инфекций, при которых сыпь встречается, но она непостоянна и эфемерна. Такого рода экзантемы возможны при многих вирусных инфекциях (энтеро- и аденовирусных, ЦМВ, ЭБВ и др.). В этих случаях диагностическая ценность экзантем невелика.
Экзантема почти всегда сосуществует с энантемой, причем последняя обычно появляется за несколько часов или 1-2 дня до экзантемы. Например, обнаружение розеол или петехий на небе у больного с симптомами ОРВИ позволит доктору заподозрить герпетическую инфекцию, сыпной тиф или лептоспироз, а пятна Филатова - Коплика являются единственным по-настоящему патогномоничным симптомом кори. Это лишний раз доказывает чрезвычайную важность тщательного осмотра не только кожи, но и слизистых оболочек.
Единой классификации инфекционных экзантем в настоящее время не существует. Наиболее удобно их разделять на генерализованные и локализованные. Классическими называют экзантемы потому, что заболевания, относящиеся к данной группе, всегда протекают с синдромом экзантемы. Атипичные же заболевания сопровождаются высыпаниями часто, но не всегда (рис. 1, 2).
В статье речь пойдет о генерализованных вирусных атипичных экзантемах.
Рис. 1. Классификация экзантем
Рис. 2. Генерализованные экзантемы
Экзантема при парвовирусной инфекции постепенно исчезает в течение 5-9 дней, но при воздействии провоцирующих факторов, таких как солнечное облучение, горячая ванна, холод, физическая нагрузка и стресс, могут персистировать недели и даже месяцы. Исчезает сыпь бесследно.
У части больных на фоне сыпи или после ее исчезновения может отмечаться поражение суставов. Характерно симметричное поражение преимущественно коленных, голеностопных, межфаланговых, пястно-фаланговых суставов. Болевой синдром зависит от тяжести заболевания и может быть слабым или сильным, затрудняющим самостоятельное передвижение, суставы опухшие, болезненные, горячие на ощупь. Течение полиартритов доброкачественное.
В анализе крови в высыпной период выявляется легкая анемия, низкое содержание ретикулоцитов, в ряде случаев - нейтропения, тромбоцитопения, повышенная СОЭ [6]. Для более точной диагностики возможно использовать ПЦР (сыворотка, ликвор, пунктат костного мозга, биоптат кожи и т. д.) для определения ДНК парвовируса. Также применяется метод ИФА с определением в сыворотке крови уровня специфических антител: IgM в сыворотке крови пациента обнаруживаются одновременно с появлением симптомов заболевания (на 12-14-й день после заражения), их уровень достигает максимума на 30-й день, затем снижается в течение 2-3 месяцев. Через 5-7 дней от момента клинических проявлений парвовирусной инфекции появляются IgG, которые сохраняются в течение нескольких лет [7].
Специфической этиотропной терапии парвовирусной инфекции не существует. В зависимости от клинической формы проводится посиндромная терапия.
Внезапная экзантема
Внезапная экзантема (син.: розеола детская, шестая болезнь) - это острая детская инфекция, вызывающаяся вирусом герпеса 6-го типа, реже 7-го типа и сопровождающаяся пятнисто-папулезной экзантемой, возникающей после снижения температуры тела. Вирус герпеса типа 6 был впервые выделен и идентифицирован в 1986 году у больных с лимфопролиферативными заболеваниями, а в 1988 году было доказано, что данный тип вируса является этиологическим агентом внезапной экзантемы. Инфекция, вызванная вирусом герпеса человека типа 6, является актуальной проблемой современной педиатрии, что связано с ее широкой распространенностью: почти все дети инфицируются в возрасте до 3 лет и сохраняют иммунитет на всю жизнь [8, 9]. При данном заболевании четко выражена сезонность - чаще внезапная экзантема регистрируется весной и осенью.
После снижения температуры тела, реже за день до или через сутки после, появляется экзантема. Высыпания вначале появляются на туловище и затем уже распространяются на шею, верхние и нижние конечности, редко - лицо. Представлены округлыми пятнами и папулами до 2-5 мм в диаметре, розового цвета, окруженными белым венчиком, бледнеющими при надавливании. Элементы сыпи редко сливаются и не сопровождаются зудом. Продолжительность высыпаний - от нескольких часов до 3-5 дней, после чего они исчезают бесследно [10, 11]. Особенностью заболевания является то, что, несмотря на болезнь, самочувствие ребенка страдает не сильно, может сохраняться аппетит и активность. В клиническом анализе крови отмечаются лейкопения и нейтропения, лимфоцитоз, могут обнаруживаться атипичные мононуклеары и тромбоцитопения. Течение внезапной экзантемы доброкачественное, склонное к саморазрешению.
Заболевание склонно к саморазрешению и в подавляющем большинстве случаев не требует специфического лечения.
Инфекционный мононуклеоз
Инфекционный мононуклеоз - это острое инфекционное заболевание, вызываемое вирусами группы герпесов, наиболее часто ЭБВ, и характеризующееся лихорадочным состоянием, ангиной, увеличением лимфатических узлов, печени и селезенки, лимфоцитозом, появлением атипичных мононуклеаров в периферической крови [13].
ЭБВ повсеместно распространен среди человеческой популяции, им поражено 80-100% населения земного шара [14, 15]. Большинство детей инфицируется к 3 годам, а все население - к совершеннолетию. Максимальная заболеваемость отмечается в 4-6 лет и подростковом возрасте. Выражена сезонность -с весенним пиком и незначительным подъемом в октябре. Характерны подъемы заболеваемости каждые 6-7 лет.
Инкубационный период составляет от 2 недель до 2 месяцев. Основной симптомокомплекс включает следующие ведущие симптомы:
Заболевание в большинстве случаев начинается остро, с подъема температуры тела до высоких цифр. Обычно весь симптомокомплекс разворачивается к концу первой недели. Наиболее ранними клиническими проявлениями являются: повышение температуры тела; припухание шейных лимфатических узлов; наложения на миндалинах; затруднение носового дыхания. К концу первой недели от начала заболевания у большинства больных уже пальпируются увеличенная печень и селезенка, в крови появляются атипичные мононуклеары.
Помимо основного симптомокомплекса, при инфекционном мононуклеозе часто отмечаются различные изменения кожи и слизистых оболочек, появляющиеся в разгар заболевания и не связанные с приемом лекарственных препаратов. Практически постоянным симптомом является одутловатость лица и отечность век, что связано с лимфостазом, возникающем при поражении носоглотки и лимфатических узлов. Также нередко на слизистой оболочке полости рта появляются энантема и петехии. В разгар заболевания часто наблюдаются различные высыпания на коже. Сыпь может быть точечной (скарлатиноподобной), пятнисто-папулезной (кореподобной), уртикарной, геморрагической. Сыпь появляется на 3-14-й день заболевания, может держаться до 10 дней и разрешается бесследно. Отличительной чертой является ее большая интенсивность на акральных участках, где она обычно сливается и дольше держится. Экзантема не зудит и проходит бесследно.
Нельзя не упомянуть еще об одном очень характерном проявлении инфекционного мононуклеоза - появлении сыпи после назначения антибиотиков пенициллинового ряда [16]. Сыпь возникает, как правило, на 3-4-й день от начала приема антибиотиков, располагается преимущественно на туловище, представлена пятнисто-папулезной сливающейся экзантемой (кореподобный характер). Некоторые элементы сыпи могут быть более интенсивно окрашены в центре. Сыпь разрешается самостоятельно без шелушения и пигментации. Важным моментом является то, что данная экзантема не является проявлением аллергической реакции на лекарственный препарат: пациенты как до, так и после ЭБВ-инфекции могут хорошо переносить антибактериальные препараты пенициллинового ряда. Эта реакция до конца не изучена и на данный момент рассматривается как взаимодействие вируса и лекарственного препарата. Отличительными чертами такой сыпи являются следующие:
Инфекционный мононуклеоз в большинстве случаев протекает гладко, без осложнений. Заболевание заканчивается через 2-4 недели. В некоторых случаях по истечении этого срока сохраняются остаточные проявления болезни.
Этиотропнаятерапия инфекционногомононуклеоза окончательно не разработана. При среднетяжелой и тяжелой формах можно использовать препараты рекомбинантного интерферона (виферон), индукторы интерферона (циклоферон), иммуномодуляторы с противовирусным эффектом (изопринозин) [17, 18]. В основном применяется патогенетическая и симптоматическая терапия [19, 20].
Энтеровирусная экзантема может быть вызвана различными типами энтеровирусов, а в зависимости от этиологии различается и симптоматика. Выделяют три вида энтеровирусных экзантем:
Кореподабная экзантема возникает преимущественно у детей раннего возраста. Заболевание начинается остро, с подъема температуры тела, головной боли, мышечных болей. Практически сразу появляются гиперемия ротоглотки, инъекция склер, нередко в начале болезни бывают рвота, боли в животе, возможен жидкий стул. На 2-3-й день от начала лихорадочного периода одномоментно появляется обильная распространенная экзантема на неизмененном фоне кожи. Сыпь располагается всегда на лице и туловище, реже на руках и ногах, может быть пятнистой, пятнисто-папулезной, реже петехиальной, размеры элементов - до 3 мм. Сыпь сохраняется 1-2 дня и исчезает бесследно. Примерно в это же время снижается температура тела.
Розеолоформная экзантема (бостонская болезнь) начинается также остро, с повышения температуры до фебрильных цифр. Лихорадка сопровождается интоксикацией, першением и болью в горле, хотя при осмотре ротоглотки никаких существенных изменений, кроме усиления сосудистого рисунка, нет. В неосложненных случаях лихорадка держится 1-3 дня и резко падает до нормы. Одновременно с нормализацией температуры появляется экзантема. Она имеет вид округлых розовато-красных пятен размером от 0,5 до 1,5 см и может располагаться по всему телу, но наиболее обильной бывает на лице и груди. На конечностях, особенно на открытых участках, сыпь может отсутствовать. Сыпь сохраняется 1-5 дней и бесследно исчезает [22].
Генерализованная герпетиформная экзантема возникает при наличии иммунодефицита и характеризуется наличием мелкой везикулезной сыпи. Отличием от герпетической инфекции является отсутствие сгруппированности везикул и помутнения их содержимого.
Одним из локальных вариантов энтеровирусной экзантемы является заболевание, протекающее с поражением кожи рук и ног, слизистой оболочки полости рта - так называемая болезнь рук, ног и рта (син.: ящуроподобный синдром, вирусная пузырчатка конечностей и полости рта). Наиболее частыми возбудителями данного заболевания служат вирусы Коксаки А5, А10, А11, А16, В3 и энтеровирус типа 71 [23, 24].
Заболевание встречается повсеместно, болеют преимущественно дети до 10 лет, однако отмечаются случаи заболеваний и среди взрослых, особенно молодых мужчин. Так же как и при других энтеровирусных заболеваниях, встречается чаще летом и осенью.
Инкубационный период короткий, от 1 до 6 дней, продромальный - невыразительный или отсутствует вовсе. Заболевание начинается с незначительного повышения температуры тела, умеренной интоксикации. Возможны боли в животе и симптомы поражения респираторного тракта. Практически сразу на языке, слизистой щек, твердом небе и внутренней поверхности губ появляется энантема в виде немногочисленных болезненных красных пятен, которые быстро превращаются в везикулы с эритематозным венчиком. Везикулы быстро вскрываются с формированием эрозий желтого или серого цвета. Ротоглотка не поражается, что отличает заболевание от герпангины [25]. Вскоре после развития энантемы у 2/3 пациентов появляются аналогичные высыпания на коже ладоней, подошв, боковых поверхностей кистей и стоп, реже - ягодиц, гениталий и лице. Так же как и высыпания во рту, они начинаются как красные пятна, которые превращаются в пузырьки овальной, эллиптической или треугольной формы с венчиком гиперемии. Высыпания могут быть единичными или множественными [26].
Заболевание протекает легко и разрешается самостоятельно без осложнений в течение 7-10 дней. Однако необходимо помнить, что вирус выделяется до 6 недель после выздоровления [27, 28].
Диагностика энтеровирусных экзантем носит комплексный характер и предусматривает оценку клинических симптомов заболевания совместно с данными эпидемиологического анамнеза и обязательного лабораторного подтверждения (выделение энтеровируса из биологических материалов, нарастание титра антител) [29].
Лечение носит в большинстве симптоматический характер. Применение рекомбинантных интерферонов (виферон, реаферон), интерфероногенов (циклоферон, неовир), иммуноглобулинов с высоким титром антител может потребоваться только при лечении больных тяжелыми формами энтеровирусного энцефалита [30].
Таким образом, проблема инфекционных заболеваний, сопровождающихся экзантемами, остается актуальной по сей день. Высокая распространенность данной патологии среди населения требует повышенного внимания от врачей любой специальности.
Читайте также:

