Кокковая инфекция в зеве
Обновлено: 17.04.2024
В структуре инфекционной заболеваемости детей ведущее место занимают респираторные инфекции [1–3]. Известно, что всеобщей закономерностью является повышенная восприимчивость к ним детей раннего и дошкольного возраста [6–8].
В структуре инфекционной заболеваемости детей ведущее место занимают респираторные инфекции [1–3]. Известно, что всеобщей закономерностью является повышенная восприимчивость к ним детей раннего и дошкольного возраста [6–8]. Именно среди детей указанной возрастной группы формируется особо выделяемая категория (15–30%) часто болеющих детей (ЧБД), вопросы лечения и оздоровления которых до сих пор остаются нерешенными и являются трудной задачей для педиатров [5–7]. У 67% ЧБД преимущественно рецидивирующей патологией становятся заболевания ЛОР-органов [9]. Характер воспалительного процесса в ротоглотке во многом зависит от реактивности иммунной системы, факторов местной защиты, в том числе микробиоценоза слизистой ротоглотки. Течение инфекционного процесса в ротоглотке могут обусловить различные микроорганизмы, в том числе и условно-патогенные [4, 6, 8, 10]. Вместе с тем состояние микробиоты ротоглотки изучено еще недостаточно. Отсутствуют однозначные представления о нормобиозе и значимости выделения различных видов микробов.
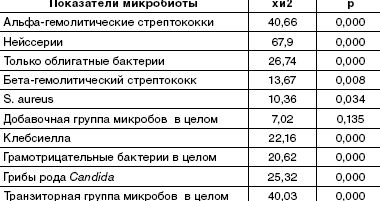
Нами проведено исследование микрофлоры задней стенки глотки у здоровых детей и больных различной респираторной патологией, госпитализированных в стационар. Обследован 351 ребенок в возрасте от 2 месяцев до 15 лет (в том числе: здоровые дети — 98, острый тонзиллит — 58, ОРВИ — 128, пневмония — 20, инфекционный мононуклеоз с гнойно-воспалительным поражением ротоглотки — 47). Использовалась стандартная методика забора мазков с миндалин и задней стенки глотки с проведением качественно-количественного определения состава выделенных микроорганизмов. Анализ полученных результатов был проведен по трем группам микроорганизмов (постоянные, добавочные, транзиторные), подразделенных в соответствии с частотой и количеством их обнаружения у здоровых детей по методу Воропаевой Е. А. [11]. По данным автора постоянная (облигатная) микрофлора данного биотопа в основном представлена альфа- и гамма-гемолитическими стрептококками (105–106 КОЕ/мл) и нейссериями (102–104 КОЕ/мл). Добавочную группу составляют стафилококки, коринебактерии и гемофилы, выделяемые у 26,9–46,2% здоровых детей, в количестве 101–104 КОЕ/мл. К случайным (транзиторным) микроорганизмам отнесены Bacillus, грибы рода Candida, Micrococcus, синегнойная палочка, грамотрицательные энтеробактерии в количестве не выше 101–102 КОЕ/мл, в 1,9–25,0%. Частота выделения различных видов микробов и интенсивность обсеменения ими задней стенки глотки у различных групп детей приведена в табл. 1.
Сравнительный анализ полученных результатов обнаружил достоверные различия в состоянии микроэкологии задней стенки глотки в группах здоровых детей и пациентов с респираторной патологией (табл. 2).
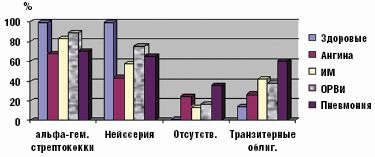
При гнойном или катаральном воспалительном процессе в ротоглотке обнаружено угнетение облигатной ассоциации альфа-гемолитического стрептококка и нейссерий, образующих защитную биопленку. Дисбиоз локуса развивался в 75–100% случаев. Он имел определенные особенности в зависимости от характера инфекционного процесса. Наиболее выраженное угнетение пролиферации облигатных бактерий было обусловлено местным гнойно-воспалительным процессом при ангине и системным поражением при пневмонии (рис. 1).
Именно при данной патологии чаще всего отсутствовали облигатные микробы, выделялись монокультуры или ассоциации микроорганизмов, состоящие только из добавочных и/или транзиторных представителей с высокой вероятностью их этиологической значимости, обнаруживались отрицательные посевы (рис. 2). Наиболее устойчивым компонентом облигатной ассоциации был стрептококк, отсутствие нейссерий либо снижение их количества наблюдалось значительно чаще.
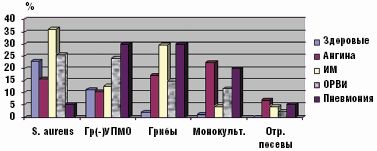
Инициация инфекционного процесса респираторными вирусами способствовала преимущественной пролиферации грамотрицательных бактерий (особенно клебсиеллы) в больших количествах (более 104 КОЕ/мл), а также их ассоциаций (р = 0,000, рис. 2). Синегнойная палочка выделялась только у ЧДБ либо больных пневмонией. Лечение в стационаре способствовало нарастанию частоты обнаружения грамотрицательных микробов в 2–3 раза вне зависимости от этиологии инфекционного процесса. Обнаружение грамотрицательных бактерий у здоровых детей являлось следствием перенесенной ОРВИ (20% против 0, р < 0,001) и сохранялось до двух месяцев. Наиболее часто грамотрицательные бактерии высевались со слизистой ротоглотки у детей первого года жизни (р = 0,002) или часто болеющих (р = 0,004).
Пролиферация грибов рода Candida, особенно в больших количествах (более 102 КОЕ/мл), была характерна для больных инфекционным мононуклеозом, пневмонией, ЧБД — особенно младших возрастных групп (р = 0,000), активировалась на фоне антибактериальной терапии и расценивалась как неблагоприятный фактор, поскольку отсутствовала у здоровых детей из группы эпизодически болеющих.
Наши данные показали, что отсутствие альфа-гемолитических стрептококков и/или нейссерий, обнаружение синегнойной палочки, грибов рода Candida и спорообразующих анаэробов, а также грамотрицательных бактерий нескольких видов или их монокультур является признаком глубокого дисбиоза и требует внимания педиатра. Оценка выраженности дисбиоза ротоглотки у детей, не имеющих признаков острой инфекции на момент обследования, должна проводиться с учетом клинического состояния пациентов их преморбидного состояния и анамнеза. Внимание следует уделять частоте эпизодов ОРВИ в году, срокам и тяжести последнего заболевания, а также наличию хронической патологии ЛОР-органов, поскольку именно наличие этих клинических признаков коррелировало с глубиной дисбиотических нарушений в ротоглотке.
Рассматривая состав микрофлоры слизистой оболочки задней стенки глотки как индикатор инфекционной резистентности детей, мы включали в состав комплексного лечения и реабилитации пациентов иммунотропные средства.
В качестве одного из современных иммуномодуляторов использован препарат Кипферон® суппозитории для вагинального или ректального введения. Кроме того, в терапевтический комплекс включались пробиотики: Полибактерин, Кипацид и Флорин форте.
Кипферон® представляет собой композицию из комплексного иммуноглобулинового препарата (КИП) с высоким содержанием специфических IgG, IgA и IgM и рекомбинантного человеческого интерферона альфа-2b. Содержащийся в препарате рекомбинантный человеческий интерферон альфа-2b обуславливает активацию местного иммунитета, позволяет эффективно устранять очаги воспаления, а КИП — уменьшает количество условно-патогенных микроорганизмов и устойчиво восстанавливает нормальную микрофлору, как минимум на протяжении 2–3 месяцев. У детей с ОРВИ, получавших Кипферон®, после лечения в 3 раза снизилась частота высева S. aureus (от 33,3% до 10%, p < 0,05). Не отмечено угнетение облигатных микроорганизмов. В 2 раза реже регистрировалась транзиторная микрофлора. В группе сравнения, в динамике лечения, возросло число несвойственных для данного биотопа микроорганизмов, в том числе выявлялись ранее отсутствовавшие гемолизирующая кишечная палочка и грибы рода Candida.
У больных тонзиллитом после лечения в 6 раз уменьшилась частота высева S. aureus (от 20% до 3,3%, p < 0,05), реже (6,6% против 24,2%, p < 0,05), чем в контроле, обнаруживались грамотрицательные энтеробактерии.
У больных инфекционным мононуклеозом лечение Кипфероном® способствовало улучшению микробиологических показателей, в том числе снижению числа детей с высоким уровнем (3–6) микробных ассоциантов на слизистой ротоглотки, элиминации S. aureus (от 53,3% до 23,1%), грибов рода Candida, бета-гемолитического стрептококка группы А (от 20% до 0%, p < 0,05).
Микробиологический эффект пробиотиков способствовал высеву исключительно облигатных микробов, отсутствию ассоциаций двух и более транзиторных микробов за счет элиминации микробов добавочной группы, энтеробактерий, синегнойной палочки и грибов рода Candida.
Таким образом, вышеизложенное позволяет считать целесообразным пересмотр значимости выделения отдельных видов микробов со слизистой ротоглотки. Наши исследования свидетельствуют о том, что препараты, действие которых направлено на повышение собственной противоинфекционной резистентности организма ребенка, должны составлять основу реабилитации часто болеющих детей.
По вопросам литературы обращайтесь в редакцию.
Л. В. Феклисова, доктор медицинских наук, профессор
Е. Р. Мескина, кандидат медицинских наук
Л. А. Галкина, кандидат медицинских наук
Е. Е. Целипанова, кандидат медицинских наук
Н. А. Савицкая, кандидат медицинских наук
С. П. Казакова, кандидат медицинских наук
Е. А. Воропаева, кандидат медицинских наук
ГУ МОНИКИ им. М. Ф. Владимирского, Москва
Ключевые слова: микробиота ротоглотки, дети, ОРВИ, инфекционный мононуклеоз, острый тонзиллит, Кипферон ® .
Слизистая оболочка верхних дыхательных путей представляет собой первую линию защиты организма против разнообразных патогенных факторов окружающей среды, таких как бактериальные, грибковые, вирусные, промышленные химические раздражители и загрязнения и обеспечивает противовирусный иммунитет. Повреждение слизистой или сухость облегчают проникновение вируса в организм. После того, как враг попал в организм и начал повреждать клетки, огромное значение играет выработка интерферонов, которые обеспечивают их невосприимчивость к действию вируса.
Противовирусный иммунитет – это очень сложный процесс, в котором участвует множество ресурсов иммунной системы. К сожалению, иммунные реакции не всегда срабатывают так, как об этом пишут в учебниках по биологии. Часто какой-либо процесс может быть нарушен, что приводит к осложнениям и проблемам. Когда снижен иммунный ответ, нужны средства, поднимающие иммунитет. Они могут быть природными, либо купленными в аптеке, главное – это эффективность и безопасность.
Слизистая оболочка верхних дыхательных путей большей частью покрыта тонким специализированным эпителием, создающим восприимчивый (чувствительный) барьер, который постоянно бомбардируется экзогенным живым или мертвым антигенным материалом.
Вдыхаемый воздух содержит значительное количество потенциально вредных веществ (газы, взвешенные корпускулярные частицы, бактерии, вирусы, микоплазмы, грибы, в том числе дрожжи, риккетсии, пыльцу, частицы слущенного эпителия человека и животных и др.). Согласно концепции местного иммунитета, слизистые оболочки и кожа как покровы, обращенные во внешнюю среду, защищают внутреннюю среду организма и сохраняют постоянство внутренней среды путем тесного взаимодействия эволюционно выработанного комплекса неспецифических и специфических механизмов защиты.
Местный иммунитет ЛОР-органов - это барьерная функция слизистых оболочек, включающая лимфоэпителиальные органы глотки, расположенные на пересечении воздухоносных и пищепроводных путей, первыми реагирующие на очередное антигенное раздражение (инфекцию) включением механизмов иммунной защиты, и неспецифические защитные факторы слизистой оболочки (мукоцилиарный транспорт, продукция лизоцима, лактоферрина, интерферона и др.)
А теперь непосредственно о микрофлоре верхних дыхательных путей и полости рта. Важно понимать, что ЛОР-органы не являются исключением в отношении микробной стерильности, т. е. в норме мы можем выявлять определенные микроорганизмы в носу, глотке и наружном ухе. Эти микробы в условиях сохранения иммунной резистентности не только не приносят нам никакого вреда, но и наоборот, оказывают положительное влияние. Они образуют так называемую биопленку (толщиной от 0,1 до 0,5 мм) – полисахаридный каркас которой, состоящий из микробных полисахаридов и муцина, предотвращает заселение организма патогенными микроорганизмами. Благодаря выделению микроорганизмами биопленки различных кислот, спирта, лизоцима (антибактериальное вещество) и стимуляции образования иммуноглобулина А тормозится развитие патогенных микробов. Кроме того, нормальные микроорганизмы препятствуют выделению токсинов патогенными бактериями.

Это лишний раз подтверждает важность сбалансированной микрофлоры для полноценной жизнедеятельности всего организма.
Нормальная микрофлора глотки разнообразна, поскольку здесь смешивается микрофлора полости рта и воздухоносных путей. Представителями резидентной микрофлоры считаются: нейссерии, дифтероиды, и гемолитические стрептококки, энтерококки, микоплазмы, коагулазоотрицательные стафилококки, моракселлы, бактероиды, боррелии, трепонемы, актиномицеты. В верхних дыхательных путях преобладают стрептококки и нейссерии, помимо этого встречаются стафилококки, дифтероиды, гемофильные бактерии, пневмококки, микоплазмы, бактероиды. Слизистая оболочка гортани, трахеи, бронхов в норме стерильна. Следует сказать, что вышеуказанный видовой спектр микроорганизмов не является неизменным. Его состав зависит от многих факторов: сопутствующей патологии, возраста, условий внешней среды, условий труда, питания, перенесенных заболеваний, травм и стрессовых ситуаций и т.д.
Такие состояния, как острые и хронические заболевания всего организма, а особенно уха, горла, носа и полости рта, аллергия, неблагоприятные физические факторы (переохлаждение, инсоляция и т. д.), химические агенты, физическое, интеллектуальное и психоэмоциональное перенапряжение, прием антибактериальных, гормональных и цитостатических препаратов, недостаточное питание, гиповитаминоз, профессиональные вредности, курение, алкоголь провоцируют нарушение нормального микробиологического равновесия в ЛОР-органах и являются причинами нарушения качественного и количественного состава микрофлоры ротоглотки. Существует бактериологическое понятие, которое характеризует изменение соотношения представителей нормальной микрофлоры, снижение числа или исчезновение некоторых видов микроорганизмов за счет увеличения количества других и появления микробов – это дисбактериоз.
Терапия дисбактериоза должна быть строго индивидуальной и направленной в первую очередь на ликвидацию источника проблемы. Например, пока не будет адекватно пролечен аденоидит (консервативно или оперативно), от дисбактериоза вряд ли возможно избавиться. Вопрос о необходимости приема антибиотика определяется исключительно течением основного заболевания: если дисбактериоз глотки вызван наличием у ребенка хронического панкреатита, то антибактериальные средства тут неуместны; если же дисбактериоз связан с запущенной формой хронического синусита или аденоидита – без этой группы лекарственных препаратов, скорее всего, не обойтись. Воспалительные очаги в носо- и ротоглотке должны быть обязательно устранены – кариозные зубы пролечены, аденоидные вегетации, небные миндалины санированы и т.д. Помните, что они могут не только вызывать местные воспалительно-инфекционные процессы и дисбактериоз ротоглотки, но и являться источником аутоинфекции и аутоинтоксикации всего организма. Убедительные данные свидетельствуют, что возникновение ряда заболеваний респираторной, желудочно-кишечной, сердечно-сосудистой систем, опорно-двигательного аппарата обусловлено очаговой инфекцией в ротоглотке. Поэтому санация полости рта и ЛОР-органов – это обязательное условие и первый шаг к выздоровлению при многих патологических процессах.
Не стоит также забывать о мерах профилактики развития инфекционно-воспалительных процессов ротоглотки и ЛОР-органов. Так, стандартными мерами профилактики являются: ежедневные гигиенические мероприятия (туалет носа), регулярное посещение врача, рациональное питание, закаливание, создание оптимального микроклимата (влажность, температура), лечение сопутствующей патологии.
Кроме вышеперечисленных мер профилактики, помочь решить проблему инфекционно-воспалительных заболеваний ЛОР-органов и помочь восстановить нормальный микробиоценоз слизистой оболочки может прием средств растительного происхождения на основе прополиса.
Прополис – это смесь природных смол, вырабатываемых пчёлами из соединений, собираемых с разных частей растений, бутонов и выделений. Современные противомикробные применения прополиса включают рецептуры для лечения синдрома простуды (инфекции верхних дыхательных путей, обычная простуда и гриппоподобные инфекции), для заживления ран, лечения ожогов, акне, простого и генитального герпеса, и нейродермита.

Мазок из зева – это доступный бактериоскопический метод исследования. В результате удается выявить состояние микробиома, выделить возбудителя, например, бактерии, вирусы или простейшие и определить чувствительность микроорганизмов к лекарственным препаратам. Именно при ангине этот метод исследования оказывается основным.
Ангина и ее особенности
Ангина – сложное и опасное инфекционное заболевание, характеризующееся острым воспалением небных миндалин или других лимфоидных образований в ротоглотке.
Спровоцировать воспаление могут грибки, бактерии или вирусы.
В клинической практике принято выделять несколько видов ангин, и классификация основана степени тяжести, состоянии пациента и какие структуры миндалин поражаются.
В рамках статьи интересует вопрос диагностики и причины возникновения воспаления. В 80% случаев причиной ангины является гемолитический стрептококк группы А, и как раз его будут искать при исследовании мазка из зева. В остальных 20% случаев возбудителями могут быть:
- стафилококки;
- аденовирусы;
- грибки.
Лечение назначается в зависимости от причины воспаления. Известно, что антибиотики, столь эффективные в лечении бактериальной пневмонии, не влияют на вирусы, а вот противовирусные не влияют на бактерии.
Когда рекомендовано проведение мазка из зева?
Показаниями для забора материала – мазка из зева, последующего посева на микрофлору будет:
- все виды ангины;
- формирование налета на миндалинах;
- гнойные образования рядом с миндалинами;
- подозрения на мононуклеоз;
- подозрение на коклюш;
- для исключения дифтерии;
- для определения антибиотикочувствительность;
- для оценки течения болезни и результатов лечения.
Как подготовиться к процедуре?
Забору биологического материала должна предшествовать подготовка. Эти простые действия помогут избежать ошибок и получить достоверные результаты.
- Во-первых, рекомендовано рассказать врачу о принимаемых лекарствах, особенно, антибиотиках. В некоторых случаях может быть принято решение об их отмене и прекращении приема. Если исследование проводится с целью оценки эффективности лечения - в отмене препаратов нет необходимости.
- Во-вторых, за 1-3 дня до проведения процедуры запрещено применять ополаскиватели для полости рта с антисептической направленностью. Исключено использование спреев, в составе которых есть антисептики, средства с антимикробной направленностью и тем более антибиотики.
- В-третьих, исследование проводится утром, натощак. Перед процедурой не рекомендовано чистить зубы, завтракать и даже пить воду и нельзя использовать жвачки.
Результаты исследования
Исследование направлено на выявление микроорганизмов и определение их количества. В мазке из зева можно обнаружить следующую патогенную микрофлору:
Эти микроорганизмы могут спровоцировать множество заболеваний и воспалительных процессов: ангины, фарингиты, скарлатину и даже пневмонию. В домашних условиях можно самостоятельно сделать тест на этого возбудителя с помощью стрептатеста.
Может не только вызывать ангину, но и стать причиной системных поражений. Стоит отметить, что эти виды микроорганизмов могут быть неактивными, не представлять опасности для организма, сдерживаться работой иммунитета. Однако, при стечении обстоятельств, например, на фоне снижения иммунитета, может вызвать болезни, в том числе, и ангину.
Это клетки, которые высвобождаются при аллергических реакциях и указывают на неинфекционную природу воспаления.
В мазке могут обнаруживаться и другие микроорганизмы:
- пневмококки;
- стафилококки;
- стрептококки;
- нейсерии;
- вирус простого герпеса;
- грибки рода Candida.
Если содержание этих микроорганизмов не превышает определенного количества, то нет необходимости проводить лечение с целью их полного уничтожения. Такие дисбиотические нарушения могут стать причиной серьезных последствий.
Положительный результат говорит о росте представителя условной или условно-патогенной микрофлоры, которые могу вызвать те или иные болезни и последствия. Отрицательный результат говорит об отсутствии бактериальных возбудителей, и, в таком случае, можно предположить вирусную или грибковую природу болезни.
При выявлении возбудителя среди бактерий, исследование продолжается, и следующий этап – определение чувствительности к антибиотикам.
Мазок из зева на микрофлору – простой, но надежный метод определения возбудителя и его антибиотикочувствительности. Эти данные с высокой точностью выявляют возбудителя, на основе которых составляется план лечения, и можно контролировать его результаты.

Обнаружение коккобациллярной флоры в мазке свидетельствует о нарушениях в женском организме.

| Прием гинеколога с высшей категорией | 1000 руб. |
| Консультативный прием врача по результатам анализов, по результатам УЗИ | 500 руб. |
| Расширенная кольпоскопия | 1500 руб. |
| Амино-тест на бактериальный вагиноз | 300 руб. |
| Медикаментозный аборт (все включено) | 4500 |
В норме микрофлору женского влагалища населяют бифидобактерии, пептострептококки и лактобактерии, на каждые из которых возложена функция защиты от вредоносных микроорганизмов, являющихся возбудителями различных заболеваний. Результатом сбоев в организме и воздействия на него внешними факторами и может начаться развитие коккобациллярной флоры.
Коккобациллярная флора
При распространении кокковых палочек происходит резкое снижение полезной микрофлоры, а подобные изменения могут стать причиной развития кольпита и его осложнений. При длительном игнорировании патологических нарушений может развиться бесплодие. Кокковая флора опасна и тем, что может передаваться от партнера к партнеру, поэтому требует ответственного подхода к лечению.
Мазок на бациллярную флору, как правило, берется при каждом плановом посещении гинеколога. Предпосылками для проведения внепланового исследования могут оказаться жалобы пациентки на болезненность в нижней части живота, появление зуда и жжения в области половых органов, боли при половых актах, нехарактерные выделения, обладающие неприятным запахом.
Что касается бациллярной флоры, здесь речь, как правило, идет о распространении во влагалище бацилл, по форме схожих с палочками. В медицинской практике установлены допустимые нормы присутствия таких бактерий в мазке. Бациллы выполняют важные функции, обеспечивая производство молочной кислоты, обладающей защитными свойствами.
На фоне существенного снижения количества лактобактерий может начаться развитие бактериального вагиноза и других опасных инфекционных недугов. Если же происходит превышение допустимого количества бацилл по тем или иным причинам, среда во влагалище может стать слишком агрессивной, что осложнит процесс оплодотворения.
Что должно быть в норме?
При отсутствии проблем со здоровьем в мазке лактобактерии должны занимать не менее 95%, что и считается нормой. Оптимальной считается грамвариабельная флора, которую определяют в том случае, если в мазке присутствует в допустимых количествах грамположительные и грамотрицательные бактерии.
Если в результатах анализов присутствует такой термин, как полиморфная флора, то в исследуемом материале в больших количествах присутствуют бактерии и вирусы. Установление умеренной или значительной флоры происходит в том случае, если имеют место инфекционные заболевания, для выявления которых требуются дополнительные диагностические мероприятия.
Преобладание коккобациллярных элементов в мазке может свидетельствовать о развитии кольпита, бактериального вагиноза и других заболеваний, передающихся половым путем. При выявлении в мазке отклонений от допустимой нормы кокков и бацилл проводится дополнительная диагностика для выявления патологий.
Развитие нарушения нередко сопровождается возникновением дисбактериоза. В таком случае также могут понадобиться дополнительные анализы и медицинская визуализация.
Особенности лечения болезни
Назначение лечения коккобациллярной флоры невозможно без определения причин, спровоцировавших её развитие. Как уже было отмечено, нередко повышение уровня кокков и бацилл выступает признаком развития дисбактериоза в организме. Коррекция состояния в данном случае может быть достигнута изменениями ежедневного рациона.
Так, питание рекомендуется разнообразить кисломолочными продуктами и приёмами витаминных комплексов. Если же диагностирована тяжелая форма дисбактериоза, может понадобиться лечение пробиотиками, предназначенными для быстрого восстановления природной микрофлоры.
Выявление патологического нарушения может свидетельствовать и о наличии инфекционных заболеваний, передающихся половым путем. Пациенткам с таким диагнозом, как правило, назначают лечение противомикробными лекарственными средствами, антибиотиками и иммуномодуляторами, необходимыми для восстановления ослабленной иммунной системы.
Лечение диагностированных заболеваний, передающихся половым путем, предполагает прохождение назначенной терапии обеими партнерами. Лечение требуется даже в тех случаях, если пациента ничего не беспокоит. Дело в том, что даже без ярко выраженной симптоматики ЗППП могут стать причиной бесплодия и не менее серьёзных осложнений.
Специалисты в назначении схемы подавления коккобациллярной флоры отдают предпочтение комплексному подходу, предполагающему одновременное применение таблетированных препаратов с лекарственными средствами местного использования.
В большинстве случаев пациентам назначают лечение Метронидазолом – препаратом, противодействующим простейшим микроорганизмам и анаэробной флоре. Не меньшую эффективность приписывают и Орнидазолу, и Тенонитрозолу.
Что касается препаратов местного применения, то наиболее популярным в данной категории считается Гиналкин – таблетированное лекарственное средство, отличающееся широким спектром воздействия и предназначенное для введения во влагалище. Согласно многочисленным отзывам, нормализация состояния наблюдается после прохождения двухнедельного курса лечения.
Выявление коккобациллярной флоры в период беременности
Спровоцировать развитие бактерии во влагалище женщины могут и нарушения гормонального фона, с которыми организм сталкивается в период вынашивания ребенка. При выявлении единичных кокков в мазке может быть рекомендовано выделение большего внимания гигиене половых органов, а также использование специальных свечей и других лекарственных средств местного применения.
Если же при исследовании мазка обнаружено недопустимое количество кокков, понадобится прохождение комплексного лечения. В ином случае беременная женщина рискует столкнуться с распространением воспалительных процессов на органы мочеполовой системы, что может отрицательно сказаться на нормальном течении беременности.
Для нормализации коккобациллярной флоры могут использоваться пробиотики и коррекция питания беременной женщины. Немаловажную роль в комплексном лечении патологического изменения флоры в период беременности играют и мероприятия, направленные на укрепление иммунной системы, ведь многие нарушения и заболевания развиваются именно на фоне снижения иммунитета.
Во всех случаях грамотное лечение может назначить только опытный гинеколог. Поэтому не пытайтесь расшифровывать анализы на флору сами — доверьте это специалисту.
Берегите себя и будьте здоровыми!

Коккобациллы являются следствием возникновения у женщины половых инфекций или развития бактериального вагиноза. Также такие бактерии могут присутствовать в кале, что в скором времени приведет к появлению дисбактериоза.

| Прием гинеколога с высшей категорией | 1000 руб. |
| Консультативный прием врача по результатам анализов, по результатам УЗИ | 500 руб. |
| Расширенная кольпоскопия | 1500 руб. |
| Амино-тест на бактериальный вагиноз | 300 руб. |
| Медикаментозный аборт (все включено) | 4500 |
Коккобациллы — что это такое?
Коккобациллярная флора представляет собой наличие определенного рода бактерий, которые объединяются в 2 подвида — это бациллы и кокки. К ним можно отнести хламидии и возбудителей болезни — гарднереллеза.
Нарушение баланса флоры половых органов происходит по причине увеличения количества коккобацилл. Когда это связано с бактериями, которые распространяются половым путем, то развивается бактериальный вагиноз, поражающий сотни миллион женщин на земле.
Кокки до определенного момента являются полезными микроорганизмами, но если полиморфная флора нарушена, увеличена щелочная среда влагалища, то исчезает защита и болезнетворные бактерии начинают активно распространяться по половым органам, ухудшая самочувствие пациентки.
Появление кокков во влагалище женщины может быть спровоцировано различными факторами, представленными:
- половыми инфекционными заболеваниями;
- игнорированием правил личной гигиены;
- ослаблением иммунной системы;
- аллергическими реакциями;
- длительными приемами антибиотиков;
- гормональными нарушениями;
- мастурбация грязными руками и прочее.
Оптимальное соотношение коккобациллярной флоры в женском организме
Контрольный мазок берется при каждом плановом посещении гинеколога, либо же при наличии болезненных симптомов половой системы. Благодаря такому анализу определяется количество палочки кокков в выделениях.
Полученные анализы можно разделить на 3 вида:
- В слабокислой среде показатели рН не превышают 5,0.
- Умеренное значение для нейтральной среды – рН 7,0.
- Щелочная среда характеризуется показателями рН более 7,5.
Если же полученные результаты не соответствуют статистическим данным, то речь идет о возникновении грамположительных кокков, которые разрушают микрофлору влагалища и ведут к ухудшению репродуктивной системы пациентки.
Когда смешанная флора в мазке приближается по показателям к щелочной, тогда можно вести речь о развитии дисбактериоза, по причине запущенного воспаления половых органов.
Внимание: размножение коков часто является распространенной причиной бесплодия, а потому нужно не затягивать поход к гинекологу (при появлении специфических выделений и болей в области яичников).
Кокки при беременности
Женщины в период вынашивания ребенка должны регулярно контролировать уровень микрофлоры, показания рН в щелочной среде. При увеличении палочек кокков могут возникнуть различные нарушения и осложнения, которые чреваты замиранием плода и самопроизвольным выкидышем.
В некоторых случаях воспалительный процесс в запущенной стадии может перейти на прямую кишку, маточную область, вызывая серьезные отклонения в репродуктивной сфере женского организма.
Дополнительная диагностика
При появлении симптомов нарушения функции половой системы (зуд и жжение во влагалище, обильные выделения темного окраса со специфическим запахом, боли в нижней части живота) важно незамедлительно обратиться к гинекологу для осмотра и лечения заболевания.
Первым делом проверяется микрофлора женщины, делается три контрольных мазка:
- свод влагалища;
- канал шейки матки;
- уретра.
Образцы наносятся на специальное стекло и отправляются в лабораторию. Палочки кокковой и бациллярной флоры тщательно изучены, а потому не будет проблем с их идентификацией.
При выявлении коккобациллярной флоры для дополнительных исследований может понадобиться кровь и моча. Только после проведения комплексного исследования удастся определиться с разновидностями кокков и бацилл, населяющих слизистую влагалища, а также установить их количество и наличие сопутствующих болезней.
Применяемые препараты и схемы лечения кокковой и бациллярной флоры
- Спринцевание травяными отварами – ромашка, календула, чистотел. Выполнять процедуру не более 5-7 дней, обязательно перед началом сеанса проконсультироваться с доктором.
- Вагинальные свечи с облепиховым маслом и другими эфирными экстрактами можно приобрести в аптечном пункте, состав продуктов считается безопасным, оказывает положительное влияние на улучшение функциональности репродуктивных органов.
- Лечебные тампоны с маслом облепихи, медом, чистотелом – можно приготовить в домашних условиях, однако, перед их применением важно провести информативную беседу с лечащим врачом.
Во избежания рецидива необходимо тщательнее уделять внимание гигиене половых органов, пересмотреть средства, которые могут вызвать нарушение кислотности микрофлоры.
При половых актах нужно пользоваться презервативами, избегать случайных половых связей, регулярно проходить профилактические осмотры у гинеколога. Нельзя заниматься самолечением во избежания серьезных осложнений в репродуктивной системе женщины.
Коккобациллярная флора далеко не всегда свидетельствует о серьезных заболеваниях и патологических изменениях, поэтому при выявлении каких-либо отклонений от нормы не стоит впадать в панику.
Выводы
Читайте также:

