Кокковые инфекции у ребенка лечение
Обновлено: 23.04.2024
В структуре гинекологических заболеваний детского возраста воспалительные поражения гениталий занимают ведущее место. Клиническое значение указанной патологии определяется не только ее частотой, но и тем, что она может явиться причиной серьезных нарушений репродуктивной системы в дальнейшем.
Сказанное определяется прежде всего физиологическими особенностями и этапностью становления биоценоза половых путей растущей девочки.
Микрофлора вульвы и влагалища девочек в норме в зависимости от возраста
Биоценоз половых путей растущей девочки изучен достаточно хорошо, что дало возможность выработать критерии для оценки его состояния в норме и при патологии. Формирование естественной микрофлоры влагалища у здоровой девочки – сложный многофакторный процесс, в основе которого лежит взаимодействие гормональной системы с иммунологическими особенностями организма. При этом доминирующее значение имеет функциональное состояние яичников, наличие лактофлоры и состояние местного иммунитета.
У новорожденной девочки влагалище стерильно, но уже через 12 часов после рождения слизистая заселяется бактериями, среди которых преобладают лактобациллы (палочка Додерлейна). Последние расщепляют гликоген влагалищного эпителия с образованием молочной кислоты, что формирует кислую реакцию влагалищной среды, которая и защищает слизистую от контаминации экзогенными микроорганизмами.
К 20–му дню жизни материнские гормоны (прогестерон, эстрогены), обеспечивающие пролиферацию вагинального эпителия и его высокую степень насыщения гликогеном, выводятся из организма. Мазок принимает атрофический характер – эпителий истончается, лактобактерии исчезают, реакция среды становится слабо–щелочной или нейтральной. При этом влагалище заселяется кокковой и бациллярной флорой.
Обследование здоровых девочек с 2–х месячного возраста до менархе показало преобладание следующих микроорганизмов:
- эпидермальный стафилококк – 84% случаев;
- дифтероиды (коринебактерии) – 80%;
- бактероиды и пептококки – 76%;
- пептострептококки – 56%;
- эубактерии – 32%;
- гарднерелла вагиналис – 32 % ( в школьном возрасте);
- микоплазма – 9% (в основном до 9 лет) случаев.
После 9 лет повышается эстрогенная секреция и вновь происходят изменения во влагалищном эпителии в виде усиления пролиферации, созревания, накопления гликогена, и к 10 годам начинается заселение лактобациллами, со смещением рН среды в кислую сторону.
К 12 годам в мазке преобладает лактофлора. Повышение эстрогенной стимуляции приводит к дальнейшему созреванию эпителия, размножению лактобацилл и к 13–14 годам рН влагалищной среды становится кислой.
Частота вульвовагинитов после 10 лет снижается до 30–40%, уступая в пубертатном периоде заболеваниям, именуемым расстройствами менструальной функции.
В основу большинства классификаций вульвовагинитов у девочек положен этиологический принцип. Наиболее удобной для использования в практической работе является классификация, приведенная в таблице 1.
- анатомо–физиологические особенности гениталий у девочек;
- экстрагенитальные заболевания различной природы;
- экзогенные патологические факторы.
Имеют значение неблагоприятные социально–бытовые условия, несоблюдение правил личной гигиены.
Однако ведущая роль принадлежит причинному инфекционному фактору. В большинстве случаев (в 72%) у девочек до 10 лет этиологическим фактором вульвовагинитов является бактериальная флора, представленная:
- кишечной палочкой у 60% больных;
- золотистым стафилококком у 21%;
- диплококком у 11%;
- энтерококком у 7%;
- хламидиями у 13%;
- анаэробной флорой – 7%.
В возрасте от 10 до 15 лет среди вульвовагинитов чаще встречаются микотические, что может быть обусловлено кислой реакцией влагалищной среды, благоприятной для грибов, а также наличием взаимосвязи с предшествующей антибактериальной терапией. Согласно литературным данным, наиболее часто встречаются:
- грибы рода Кандида у 46,7% больных;
- кишечная палочка у 37%;
- стафилококки у 14,5%;
- стрептококки у 20 %;
- ассоциации микроорганизмов у 7%.
Следует обратить внимание на возрастание этиологической роли стрептококковой инфекции в развитии вульвовагинитов у девочек–подростков.
Несмотря на различие этиологических факторов вульвовагинитов, клинические проявления в основном идентичны (табл. 2).
Необходимые исследования для установления и подтверждения диагноза включают как общие, так и специальные методы обследования девочек (табл. 3).
При наличии клиники вульвовагинита в мазке:
– лейкоцитов больше 15 в п/зрения;
– слущенного эпителия – много;
– флора – смешанная, кокковая, палочковая, специфическая – в значительном количестве (табл. 4).
Лечение вульвовагинитов у девочек нередко является сложной задачей, требует комплексной терапии и предполагает дифференцированную тактику. При тяжелых проявлениях воспаления, частых рецидивах, кроме соблюдения личной гигиены и проведения местного противовоспалительного лечения, необходима терапия основного заболевания, санация очагов хронической инфекции, повышение защитных сил организма (табл. 5).
Лечение вульвовагинитов у девочек нередко является сложной задачей, требует комплексной терапии и предполагает дифференцированную тактику. При тяжелых проявлениях воспаления, частых рецидивах, кроме соблюдения личной гигиены и проведения местного противовоспалительного лечения, необходима терапия основного заболевания, санация очагов хронической инфекции, повышение защитных сил организма (табл. 5).
Местная антибиотикотерапия применяется при рецидивирующем характере течения и только при идентифицированной патогенной микрофлоре с определением ее чувствительности к антибактериальным препаратам (табл. 6). При тяжелых вульвовагинитах показано парентеральное введение антибактериальных препаратов. Учитывая частоту анаэробов, участвующих в развитии вагинитов, а также тяжесть анаэробной инфекции, многие авторы рекомендуют широкое использование в его лечении метронидазола, эффективного в отношении Trichomonas vaginalis, бактероидов, фузобактерий. При наружном применении препарат обладает также антиоксидантным и противовоспалительным дерматопротективным действием. Метронидазол действует синергически с другими антибиотиками. Внутрь детям старше 15 лет назначают по 250–500 мг 2–3 раза в сут. Детям до 15 лет назначают в дозе 20–40 мг/кг в сут., в 3 приема. Свечи и вагинальные таблетки назначают по 1 шт. (500 мг) на ночь. Внутривенное введение показано при тяжелом течении инфекций, а также при отсутствии возможности приема препарата внутрь. Для детей старше 12 лет разовая доза при внутривенной инфузии составляет 500 мг, интервал между введениями 8 ч. Длительность курсов лечения и частота их проведения определяются индивидуально.
На заключительном этапе этиотропного лечения с целью коррекции вагинальных дисбиотических процессов применяются местно и энтерально такие препараты, как, бифидумбактерии, лактобактерин, биовестин–лакто.
Лечение микотического вульвовагинита у девочек
Микотический вульвовагинит в большинстве случаев является частным проявлением кандидоза, развитию которого способствуют тяжелые соматические и инфекционные заболевания, нарушение обмена, гиповитаминозы, нерациональное использование антибиотиков широкого спектра действия, иммунодефицитные состояния. В связи с этим обязательным условием эффективного лечения кандидоза гениталий является сведение к минимуму или устранение указанных факторов, что достигается:
1) лечением основного заболевания;
2) диетотерапией с ограничением продуктов, богатых углеводами;
3) витаминотерапией и иммунокорригирующими средствами;
4) десенсибилизирующей терапией.
Особенностью кандидозного вульвовагинита является упорное течение, склонность к рецидивированию. Поэтому специфическое лечение, как правило, должно быть длительным, курсовым. Количество курсов – не менее 2–3, перерыв между курсами 7–10 дней.
При микотическом поражении гениталий у девочек нередко возникают ассоциации с бактериями, простейшими. В этих случаях целесообразно применение препаратов, обладающих не только антимикотической активностью, но и проявляющих антибактериальное воздействие на грамположительные и грамотрицательные микроорганизмы, а также имеющих антипаразитарное действие (табл. 7, 8).
К таким препаратам (из указанных выше) относятся:
Изоконазол – активен в отношении дрожжеподобных грибов, грамположительных микробов (стафилококки, микрококки, стрептококки).
– активен в отношении дрожжеподобных грибов, грамположительных микробов (стафилококки, микрококки, стрептококки).
Миконазол – выражена активность в отношении грибов рода Кандида и грамположительной микрофлоры
Сангвиритрин – обладает широким спектром антимикотической и антимикробной активности, действуя на грамположительные и грамотрицательные микроорганизмы. Активен в отношении антибиотикорезистентных штаммов микробов.
В последние годы стали применяться комбинированные препараты для лечения микотических и смешанных вульвовагинитов. Литературные данные свидетельствуют об их высокой эффективности, позволяющей добиться полного клинического и микробиологического выздоровления при отсутствии побочных реакций. В то же время сведений о применении комбинированных препаратов в педиатрической практике фактически нет, имеются лишь отдельные наблюдения.
В перерывах между курсами специфической антимикотической местной терапии проводят неспецифическую терапию широко известными средствами:
- 2% раствором соды;
- 20% раствором буры в глицерине;
- жидкостью Кастеллани;
- 1% раствором йодинола;
- генциан–виолетом 1:5000;
- основным фуксином 1:5000.
Вышеперечисленные средства способствуют удалению мицелия гриба, нарушают процесс прикрепления гриба к слизистым, тормозят его размножение.
Эффективность лечения микотического вульвита увеличивается при сочетанном применении антимикотических средств местно и энтерально. Общее лечение становится обязательным при неэффективности местного, в частности, при рецидивировании процесса и его генерализации.
Кетоконазол – высокоэффективный антимикотический препарат. Однако при лечении возможны серьезные побочные реакции, обладает кумулятивным эффектом. В связи с этим применение препарата ограничено.
Натамицин – малотоксичен, к нему чувствительны большинство патогенных дрожжеподобных грибов, особенно Candida albicans. По данным сотрудников кафедры педиатрии РМАПО, препарат эффективен, хорошо переносится больными, в т.ч. детьми первого года жизни, побочных реакций не отмечено.
С целью восстановления биоценоза влагалища и коррекции местного иммунитета после проведенной комплексной терапии микотического вульвовагинита целесообразно назначение эубиотиков (ацилакт, лактобактерин и др.) в свечах ректально и вагинально.
Исходя из вышеизложенного, тактика лечения вульвовагинитов у девочек должна быть строго дифференцирована и определяться как этиологическим фактором, так и состоянием макроорганизма в целом. Внедрение в практику современных антибактериальных и антимикотических препаратов позволяет не только повысить эффективность терапии воспалительных заболеваний гениталий у девочек, но и снизить число рецидивов, профилактировать хронизацию процесса, избежать отдаленных последствий перенесенного воспаления гениталий.
1. Кохреидзе Н.А., Кравченко М.Е.. Становление вагинальной микрофлоры в возрастном аспекте // Ж. Детская больница, 2002, 3: 45–47.
2. Буданов П.В., Баев О.Р. Диагностика и варианты комплексного нарушения микроценоза влагалища // Вопросы гинекологии, акушерства и перинатологии, 2002; т.1, 2: 73–76.
3. Лебедев В.А., Давыдов А.И. Урогенитальный хламидиоз // Вопросы гинекологии, акушерства и перинатологии, 2002; т.1, 2: 25–30.
4. Коколина В.Ф., Бижанова Д.А. Диагностика и лечение вульвовагинитов // Ж. Педиатрия, 1993№ 6: 57–59.
5. Коколина В.Ф., Зубакова О.В. Диагностика и лечение урогенитальных инфекций в гинекологии детского и подросткового возраста. Методическое пособие. М. 1998.
7. Кулаков В.И., Прилепская В.Н. Практическая гинекология // Москва, 2001, 177–253.
8. Серов В.Н. с соавт. Значение генитальных инфекций в формировании распространенных гинекологичесих заболеваний и их современное лечение // Информационное письмо, Москва, 1997.
Стрептококковая инфекция приводит к таким болезням как скарлатина, ангина, гломерулонефрит, ревматизм, пиодермия, рожа, вызывает генерализованные процессы по типу септицемии и т. д. Стрептококковая инфекция может вызвать осложнение других болезней.
Согласно международной классификации, различают:
- септицемию, вызванную стрептококком группы А;
- септицемию, вызванную стрептококком группы D;
- септицемию, вызванную стрептококком pnevmonine (пневмококковую септицемию);
- стрептококковую септицемию неуточненную;
- другие стрептококковые септицемии.
Заболевания, вызванные стрептококками, случаются по всей планете. Болезни кожи характерные для жарких стран. Скарлатина и ангина чаще встречаются в странах, где преобладает холодный и умеренный климат. Болезни подвержены дети любого возраста, даже новорожденные. Инфекция передается воздушно-капельным и контактно-бытовым путями. Также заражение может произойти через инфицированные продукты питания.
Опасаться стоит больных ангиной, пневмонией, стрептодермией, скарлатиной и другими стрептококковыми заболеваниями, а также бактерионосителей без клинических проявлений.
Формально все болезни, которые вызваны стрептококками, относят к инфекционным болезням. Но при гломерулонефрите, ревматизме и пр. нет заразительности – отличительного признака инфекционных болезней. Потому в группу стрептококковых инфекций следует относить только те, что имеют все признаки инфекционной болезни: заразительность, циклическое развитие клинических симптомов, инкубационный период, формирование специфического иммунитета. Эти признаки характерны для заболеваний, вызываемых Р-гемолитическим стрептококком группы А: ангина, скарлатина, пневмония, бронхит, рожа, фарингит, а также некоторые гнойно-воспалительные заболевания новорожденных, которые вызваны стрептококками других групп: флегмона, стрептодермия, абсцесс и т. д.
Что провоцирует / Причины Стрептококковой инфекции у детей:
Стрептококки — это грамположительные бактерии, диаметр которых от 0,6 до 1 мкм. Имеют шаровидную или овальную форму. Располагаются они парами или цепочками.
Стрептококки делят на 21 группу по углеводным антигенам клеточной стенки. Обозначаются они литерами от А до U. Болезнь у человека возникает в основном от стрептококков группы A. Для новорожденных и грудничков опасны стрептококки групп В, С и D. Они вызывают эндокардит, тяжелый сепсис, остеомиелит, менингит, инфекции мочевых путей и т. д. Стрептококки группы F вызывают глубокие воспалительные процессы ротовой полости и дыхательных путей.
Стрептококки вырабатывают разные ферменты и токсины: эритрогенные токсины (А, В, С), стрептокиназы А и В, стрептолизины О и S, дезоксирибонуклеазы и т. д. Самый токсичный компонент, который вырабатывается стрептококком, это экзотоксин. Он повреждает ткани организма, подавляет функции ретикулоэндотелиальной системы, влияет на проницаемость мембран, вызывает иммуносупрессию и др.

Патогенез (что происходит?) во время Стрептококковой инфекции у детей:
В патогенезе стрептококковых заболеваний большая роль принадлежит токсическому синдрому, который связан в основном с эритрогенным токсином, а также с аллергическим, что обусловлен сенсибилизацией к белковым структурам стрептококка и разрушенным им тканям.
Симптомы Стрептококковой инфекции у детей:
Проявления стрептококковой инфекции зависят от направленности патологического процесса.
Вторичные формы развиваются в результате включения аутоиммунных и токсико-септических механизмов развития воспаления в различных органах и системах. Это такие болезни как стрептококковый васкулит, гломерулонефрит и ревматизм.
К редким клиническим формам стрептококковых инфекций относят энтерит, некротическое воспаление мышц и фасций, очаговые инфекционные поражения органов и тканей, синдром токсического шока. Стрептококкам группы В подвержены в основном (но не только) новорожденные. Младенцы заражаются интранатально. Стрептококки группы В вызывают в основном поражение мочеполовых путей.
Стрептококковые инфекции новорожденных проявляются в виде бактериемии (30% случаев), пневмонии (32-35%) и менингита. В ½ случаев симптомы начинают проявляться в первые 24 часа после рождения. Такие инфекции имеют крайне тяжелое течение, летальный исход наступает в 37 случаях из 100. После проявления бактериемии и менингита погибают около 10-20% заболевших, а у 50% тех, кто выжил, фиксируют нарушения развития.
Стрептококковые инфекции группы В часто служат причиной послеродовых эндометритов, циститов, аднекситов у родильниц и осложнений в послеоперационном периоде при проведении кесарева сечения.
Диагностика Стрептококковой инфекции у детей:
Стрептококковая инфекция слизистой оболочки глотки и кожных покровов требует подтверждения с помощью бактериологических методов, позволяющих выделить и идентифицировать возбудителя. Перед лечением проводят тест на чувствительность к антибиотикам, поскольку на сегодняшний день многие виды стрептококка стали устойчивы к антибиотикам.
Экспресс-диагностика стрептококков группы А дает возможность выявить возбудителя за 15-20 минут, при этом чистую культуру не выделяют. Но выявление стрептококков не во всех случаях означает, что именно они спровоцировали патологический процесс (болезнь). Ребенок может быть просто носителем, а проявляющиеся симптомы спровоцированы другими вирусами/бактериями/организмами.
Ревматизм и гломерулонефрит практически всегда характеризуются повышением титра антител к стрептококкам уже с первые дни обострения. Титр антител к внеклеточным антигенам определяют с помощью реакции нейтрализации.
Если есть необходимость, проводят обследование пораженных стрептококковой инфекцией органов: осмотр отоларинголога, УЗИ мочевого пузыря, рентгенографию легких и т. д.
Лечение Стрептококковой инфекции у детей:
Лечение проводится разными специалистами – в зависимости от формы инфекции – уролог, гинеколог, пульмонолог, дерматолог и т. д. Этиологическое лечение первичных клинических форм стрептококковых инфекций проводится антибиотиками пенициллинового ряда. Если за пять дней антибиотик не доказал свою эффективность, его отменяют.
Тест на чувствительность к антибиотикам включает такие препараты: азитромицин, эритромицин, оксациллин, кларитромицин и т. д. Неэффективными для лечения стрептококковой инфекции у детей считаются гентомицин, препараты тетрациклинового ряда, канамицин.
Также должно применяться симптоматическое и патогенетическое лечение, которые зависят от клинической формы болезни. При вторичных формах стрептококковой инфекции часто возникает необходимость применения длительных курсов антибиотикотерапии, при которых нередко назначают препараты пролонгированного действия.
В последние годы было открыто, что на течение болезни положительно влияени применение иммуностимулирующих средств и иммуноглобулина человека.
Профилактика Стрептококковой инфекции у детей:
Следует соблюдать меры индивидуальной профилактики и личной гигиены, контактируя с теми, кто болен респираторными заболеваниями. Указанные меры подразумевают ношение маски, обработку поверхностей и посуды, мытье рук с мылом.
Должен осуществляться контроль над состоянием здоровья коллективов: осмотры в школах и детских садах, изоляция заболевших детей, необходимые лечебные мероприятия, выявление скрытых форм носительства стрептококковой инфекции и их лечение.
Чтобы полностью очистить организм от возбудителя и излечиться от заболевания, Всемирная организация здравоохранения рекомендует применять пенициллины согласно назначению врача более 10-ти дней.
Важны профилактические меры, препятствующие распространению внутрибольничной стрептококковой инфекции. Потому что в стационарах находятся дети, у которых ослабленное состояние, потому их организмам многократно сложнее противиться заболеванию, и у них вероятнее летальный исход.
Чтобы предупредить заражение рожениц и новорожденных, следует соблюдать санитарно-гигиенические нормы и режим, разработанные для отделений гинекологии и родильных домов.
К каким докторам следует обращаться если у Вас Стрептококковая инфекция у детей:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Стрептококковой инфекции у детей, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Пневмококковые инфекции — группа бактериальных заболеваний, которые проявляются проявляющихся гнойно-воспалительными изменениями в разных органах и системах, чаще всего проходящих в легких по типу крупозной пневмонии и в ЦНС по типу гнойного менингита.
Пневмококки постоянно живут в верхних дыхательных путях взрослых и детей, потому их относят к условно-патогенным микроорганизмам. У большинства здоровых детей пневмококки обнаруживают в посевах слизи из ротоглотки. Носители данного возбудителя это в основном дети раннего возраста и пожилые люди. Предполагают, что во время носительства формируется иммунитет – скорее типоспецифический, чем напряженный. Болезнь в этих случаях может развиться, только если резко снизилась иммунная реактивность организма во время тяжелых форм гриппа и ОРВИ, долговременного применения кортикостероидных гормонов, цитостатиков и т. д.
Эпидемии возникают из-за клонов пневмококков с большей вирулентностью и инвазивностью. Они зарождаются при неблагоприятных условиях внешней среды у ослабленных детей. Этому способствует скученность (например, в детских коллективах), холодное время года, повышенная заболеваемость ОРВИ). Инфекцию всегда переносит человек – как больной, так и носитель. Пути передачи пневмококковой инфекции: воздушно-капельный, контактно-бытовой.
Заболеванию подвержены дети с дефицитом типоспецифических антител. Особенно тяжело протекает болезнь у малышей с серповидно-клеточной анемией или дефицитом С3.
Что провоцирует / Причины Пневмококковой инфекции у детей:
Изначальное название пневмококков – Diphcoccus pneumoniae. На сегодня возбудитель переименован на Streptococcus pneumonia и отнесен к семейству Streptococcaceae, роду Streptococcus.
Пневмококки представляют собой грамположительные овальные или сферические кокки, размер которых от 0,5 до 1,25 мкм. Располагаются они попарно, иногда – короткими цепочками. Ранее кокки назывались ланцетовидными диплококками за свою форму ланцета (дистальный конец каждой пары заостренный). Пневмококки имеют хорошо организованную капсулу. Выделяют более 85 сероваров пневмококков по полисахаридному составу капсулы.
Пневмококки имеют капсульные антигены, а также соматические, которых насчитывается три. Разрушение пневмококков сопровождается высвобождением эндотоксина. Во внешней среде пневмококки устойчивы. Могут сохраняться 1-2 месяца в высушенной мокроте, а на зараженных пеленках около 1-2 недель. Мгновенно погибают при кипячении. Около 10 минут могут жить при температуре среды 50-60 ˚С. Пневмококки имеют высокую чувствительность к распространенным дезинфицирующим средствам.

Патогенез (что происходит?) во время Пневмококковой инфекции у детей:
По лимфе и крови пневмококки распространяются из первичного очага поражения, что приводит к пролонгированной бактериемии. Она может проходить без симптомов или как инфекционно-токсический синдром. Если организм ребенка ослаблен, пневмококки могут преодолеть гематоэнцефалический барьер и вызвать менингит/ менингоэнцефалит.
Распространение инфекции контактным бронхогенным путем может привести к гнойному плевриту, среднему отиту, гаймориту, перикардиту, мастоидиту, эпидуральному абсцессу, эмпитеме. Пневмококковая бактериемия в некоторых случаях может привести к гнойному артриту, остеомиелиту, абсцессу мозга.
Тяжелые формы пневмококковой инфекции свойственны в основном грудничкам. Тяжесть болезни зависит от вирулентности возбудителя и от реактивности макроорганизма. Болезнь проходит особенно тяжело в случае массивной бактериемии. В тяжелых случаях пневмококкые заболевания сопровождаются развитием реологических и гемодинамических нарушений вплоть до возникновения острой надпочечниковой недостаточности, диссеминированного внутрисосудистого свертывания крови, отека и набухания вещества мозга.
Симптомы Пневмококковой инфекции у детей:
Пневмококковую инфекцию у детей классифицируют по критерию очага поражения. Выделяют такие виды:
- крупозная пневмония
- пневмококковый менингит
- эндокардит
- остеомиелит .
Такая форма как крупозная пневмония представляет собой острое воспаление легких с быстрым вовлечением в процесс доли легкого и прилегающего участка плевры. Болезни подвержены в основном дети школьного возраста и подростки. Крайне редко случается крупозная пневмония у грудничков. Морфологические изменения при данном заболевании происходят по стадиям. Патологический процесс, как правило, начинается в задних и заднебоковых отделах правого легкого в виде небольшого фокуса воспалительного отека, который быстро увеличивается, формируя фазу гиперемии и серозной экссудации (стадия прилива) с размножением в экссудате пневмококков. Далее наступает фаза миграции лейкоцитов и выпадения фибрина (стадия гепатизации) с последующим постепенным рассасыванием элементов экссудата — лейкоцитов и фибрина на стадии разрешения.
Крупозная пневмония у детей начинается остро с таких симптомов как озноб и боли в боку, которые становятся сильнее при глубоких вдохах, сухой кашель, слабость, головная боль, повышенная температура (доходит до 39 - 40 °С), разбитость, возбужденность, в некоторых случаях бредовые состояния.
Вскоре появляются такие симптомы:
- гиперемия щек;
- короткий болезненный кашель с выделением небольшого количества вязкой стекловидной мокроты;
- учащенное поверхностное дыхание;
- раздувание крыльев носа;
- герпетические высыпания на крыльях носа;
- герпетические высыпания на губах; губ (в некоторых случаях);
- цианоз кончиков пальцев (в некоторых случаях).
Наблюдается отставание грудной клетки при дыхании на стороне поражения. Если процесс локализирован в нижней доле правого легкого, болит не только грудная клетка, но и живот, потому есть шанс спутать крупозную пневмонию у детей с болезнями брюшной полости, такими как перитонит, аппендицит, панкреатит и прочие. У детей может отмечаться частый жидкий стул, повторная рвота, вздутие живота. Эти симптомы также могут указывать на острую кишечную инфекцию, что утрудняет диагностический процесс.
Когда процесс локализирован в верхней доле правого легкого, могут возникнуть такие менингеальные симптомы как судороги, ригидность мышц затылка, резкая головная боль, частая рвота и проч. В тяжелых состояниях возможен бред.
Изменения в легких претерпевают весьма характерное развитие. В типичных случаях в первые сутки на пораженной стороне отмечают отметить тимианический оттенок перкуторного звука, потом всего за несколько часов звук становится притупленным. Под конец первых суток заболевания на высоте вдоха выслушивают крепитацию и мелкопузырчатые влажные или сухие хрипы.
Пик крупозной пневмонии приходится на 2-3-й день от начала заболевания. На пике притупление в зоне поражения становится резко выраженным и над очагом поражения начинает выслушиваться бронхиальное дыхание, иногда шум трения плевры, голосовое дрожание и бронхофония. При этом кашель становится сильнее, более влажным и болезненным. Мокрота в некоторых случаях становится красновато-коричневого оттенка. Одышка нарастает, а цианоз губ и лица усиливается.
Анализ крови на пике болезни показывает нейтрофильный лейкоцитоз, увеличение содержания палочкоядерных до 10— 30%, может быть сдвиг формулы до юных и миелоцитов. В частых случаях выявляется токсическая зернистость нейтрофилов, типичны анэозинофилия, умеренный моноцитоз, повышение СОЭ.
Рентген показывает основные стадии развития крупозной пневмонии. На стадии прилива видно небольшое прозрачности в зоне пораженного участка, усиление легочного рисунка из-за полнокровия сосудов. Стадия гепатизации отмечается выраженным понижением прозрачности участка пораженного легкого, картина похожа на ателектаз (спадение доли легкого). На стадии разрешения ренгенограмма показывает медленное восстановление прозрачности пораженного участка легкого. В некоторых случаях бывает жидкость в плевральной полости, что называется плевропневмонией. Болезнь длится в общем примерно 3-4 недели (зависит от каждого индивидуального случая). Лихорадочный период (повышенная температура) длится от 7 до 10 суток. Структура и функции легких полностью восстанавливаются спустя 1-1,5 месяца.
Пневмококковый менингит является самой тяжелой формой гнойного менингита у детей. Болезнь характерна для детей от 6 до 12-ти месяцев. До 5-ти месяцев жизни это заболевание встречается крайне редко. У детей старшего возраста пневмококковый менингит обычно возникает после травмы черепа или хронических заболеваний придаточных пазух носа, а также болезнь характерна для детей с нарушениями иммунитета (как врожденными, так и приобретенными). В группе риска – дети с онкологическими заболеваниями или серповидно-клеточной анемией. Поражение мозговых оболочек – вторичное явление, сначала следуют другие проявления инфекции, вызванной пневмококками.
Пневмококковый менингит, как правило, имеет острое начало, температура тела сильно повышена. Но если ребенок ослаблен, температура может достигать субфебрильных значений, а в редких случаях остается в норме. У детей проявляется беспокойство, они срыгивают и кричат. Среди первых симптомов часто отмечают тремор, судороги, выбухание большого родничка, гиперестезию, а в тяжелых случаях и потерю сознания. Менингеальный синдром неярко выраженный и часто неполный. В большинстве случаев болезнь начинается сразу как менингоэнцефалит. В таких случаях с первых суток отмечают нарушение сознания, судороги, тремор конечностей, резкое психомоторное возбуждение, что переходит в сопор и кому.
Спинномозговая жидкость гонойная, мутная, зеленовато-серого оттенка. Отстаивание приводит к выпадению осадка. В жидкости наблюдается нейтрофильный плеоцитоз, высокое содержание белка, пониженное количество сахара и хлоридов.
Анализ крови показывает лейкоцитоз с резким сдвигом влево, моноцитоз, анэозинофилию. Вероятная также умеренная анемия. СОЭ выше нормы.
Пневмококки в ряде случаев выступают возбудителями гнойного артрита, среднего отита, перикардита, остеомиелита, первичного перитонита, эндокардита и пр. Эти болезни могут быть как самостоятельными, так и возникают на фоне пневмонии, трахеита, бронхита. Они характерны в основном для детей раннего возраста. По симптоматике они неотличимы от болезней, вызванных иными гноеродными бактериями.
Диагностика Пневмококковой инфекции у детей:
Диагностика пневмококковой инфекции у детей требует выделения возбудителя из очага поражения или крови больного ребенка. При подозрении на крупозную пневмонию берут мокроту для исследования. При подозрении на сепсис для анализов используют кровь, а при подозрении на другие болезни пневмококковой природы берут воспалительный экссудат или гнойное отделяемое.
Патологический материал отправляют на микроскопическое исследование. Основанием для предварительной диагностики выступает обнаружение грамположительпых диплококков ланцетовидной формы, окруженных капсулой. Далее устанавливают принадлежность обнаруженных кокков к пневмококкам с помощью комбинированных типоспецифических сывороток, содержащих в высоких титрах антитела ко всем серотипам пневмококка. В первые несколько суток от начала пневмококкового менингита есть шанс найти возбудитель в спинномозговой жидкости. В ней он может располагаться внеклеточно или внутриклеточно. Чтобы выделить чистую культуру, делают посев исследуемого материала на кровяной, асцитический или сывороточный агар.
Пневмококк на питательных средах дает рост мелких прозрачных колоний. Чтобы выделить чистую культуру, в некоторых случаях применяют биологическую пробу. Для этой цели заражают белых мышей внутрибрюшинно исследуемым материалом. Если в материале есть патогенные пневмококки, мыши погибают через сутки-двое.
Лечение Пневмококковой инфекции у детей:
Лечение пневмококковой инфекции должно быть комплексным. Выраженные формы требуют лечения антибиотиками.
Легкие и среднетяжелые формы (такие как бронхит, назофарингит и отит) можно лечить фепоксиметилпенициллином (вепикомбином). Доза 50000—100000 ЕД на 1 кг тела в сутки, разделенная на 4 приема (принимают внутрь). Или назначается пенициллин в аналогичной дозе, 3 раза в сутки, вводится внутримышечно. Курс – от 5 до 7 дней. Другой вариант – назначается азитромицин (сумамед) из расчета 10 мг/кг в день, курс 3 суток.
Больных крупозной пневмонией или менингитом лечат цефалоспориновым антибиотиком 3-го и 4-го поколения. В ходе антибиотикотерапии рекомендуется проверять чувствительность выделенных пневмококков к назначенному препарату и при необходимости его заменять. В последние годы часто выделяют штаммы пневмококков, которые устойчивы ко многим антибиотикам.
Тяжелые формы пневмококковой инфекции лечат не только антибиотиками, но и инфузионной, патогенетической, общеукрепляющей и симптоматической терапией по принципам, аналогичным таковым при иных инфекционных заболеваниях.
При пневмококковом менингите летальные исходы составляют 10-20%. При других формах болезни летальные исходы случаются редко. Смертью болезнь может кончиться у детей с врожденным или приобретенным иммунодефицитом, длительно леченных иммуносупрессивными препаратами, у детей с врожденными уродствами.
Профилактика Пневмококковой инфекции у детей:
Ее вводят детям от 2-х лет из группы риска по пневмококковой инфекции: детям с асготенией, иммунодефицитами, хронической патологией почек, серповидно-клеточной анемией, хронической патологией сердца. Вакцина вводится единоразово подкожно или внутримышечно, доза составляет 0,5 мл. Эта вакцина редко вызывает побочные реакции, обладает высокой иммуногенностыо. После вакцинации антитела в крови сохраняются до 5-ти лет. Противопоказанием к введению пневмококковой вакцины является гиперчувствительность к составным компонентам вакцины.
Детям с иммунодефицитным состоянием в случае контакта с больным пневмококковой инфекцией можно вводить гамма-глобулин по 0,2 мл/кг внутримышечно.
К каким докторам следует обращаться если у Вас Пневмококковая инфекция у детей:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Пневмококковой инфекции у детей, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Хотя диагностика и лечение респираторной патологии у детей занимают ведущее место в работе педиатра, антибактериальная терапия требуется практически всего 6–8% больным этой категории — в основном с отитом, синуситом, стрептококковой ангиной, л
Хотя диагностика и лечение респираторной патологии у детей занимают ведущее место в работе педиатра, антибактериальная терапия требуется практически всего 6–8% больным этой категории — в основном с отитом, синуситом, стрептококковой ангиной, лимфаденитом, пневмонией, а также при бронхитах, вызванных только микоплазмой и хламидиями. К сожалению, и у нас, и за рубежом далеко не изжито избыточное применение этих препаратов — их применяют подчас у 30–80% детей с острыми респираторными вирусными инфекциями (ОРВИ). Не принося пользы, такая практика повышает риск развития устойчивости флоры и побочных явлений, дезориентируя к тому же врача: не получив эффекта от антибиотика при вирусной инфекции, врач переходит на резервные препараты, которые также не дают эффекта. Поэтому основной вопрос — показаны ли антибиотики данному больному? — решать положительно следует при только доказанной (или вероятной тяжелой) бактериальной инфекции. И хотя доказать бактериальную природу острых респираторных заболеваний (ОРЗ) удается редко, накопленные данные позволяют врачу с высокой вероятностью не только выявить таких детей, но и очертить круг вероятных возбудителей и их чувствительность к антибиотикам. В табл. 1 представлены формы респираторной патологии, при которых показано и не показано назначение антибиотика, а также симптомокомплекс, позволяющий заподозрить пневмонию в отсутствие четких физикальных данных, и значения маркеров воспаления, при которых введение антибиотика оправдано.
В табл. 2 представлены основные возбудители бактериальных ОРЗ; очевидно, что спектр возбудителей ОРЗ у детей невелик, что облегчает выбор препарата, который действует на вероятных возбудителей конкретного заболевания. Эти данные для антибиотиков, которые следует применять в амбулаторных условиях, приведены в табл. 3.
К счастью, резистентность к пенициллину циркулирующих среди населения России пневмококков (менее 10% штаммов) во много раз ниже, чем, например, в странах Юго-Запада Европы (40–50%). Но следует учитывать, что среди детей в детских дошкольных учреждениях (ДДУ) и особенно в интернатах 50–60% выделенных штаммов пневмококков устойчивы к пенициллину. Пневмококки сохраняют 100-процентную чувствительность к амоксициллину (а также к цефтриаксону), но устойчивы к ко-тримоксазолу, тетрациклину, гентамицину и другим аминогликозидам. Устойчивость пневмококков к пенициллинам не связана с выработкой лактамазы (она обусловлена потерей пенициллин-связывающих белков), поэтому применение ингибитор-защищенных пенициллинов не повышает эффективности лечения. Устойчивость пневмококков к макролидам растет быстрее (до 15–20% штаммов в некоторых регионах), в меньшей степени она растет к 16-членным макролидам: джозамицину, мидекамицину, спирамицину.
Haеmophilus influenzae (как бескапсульные, так и типа b) в России чувствительны к амоксициллину, доксициклину, цефалоспоринам 2 и 3 поколений, всем аминогликозидам. Но эти возбудители не чувствительны к пенициллину, цефалексину, цефазолину, большинству макролидов — кроме азитромицина (его применение при отитах и синуситах ограничено низкой его концентрацией в соответствующих полостях).
Под влиянием лечения H. influenzae вырабатывает лактамазы, инактивирующие лактамные препараты (в т. ч. пенициллин и амоксициллин), поэтому у детей, леченных ранее (а также у детей из ДДУ), применяются с начала лечения амоксициллин/клавуланат или цефуроксим аксетил.
Бета-гемолитический стрептококк группы А (БГСА) чувствителен ко всем антибиотикам, кроме аминогликозидов, однако в ряде регионов частота устойчивых к макролидам штаммов может достигать 15%. Moraxella catarrhalis, способная продуцировать лактамазу, выделяемая обычно у леченых ранее детей, чувствительна к макролидам, цефалоспоринам, аминогликозидам, но резистентна к амоксициллину.
В амбулаторной практике назначают препараты первого выбора, если нет оснований предполагать наличие лекарственной устойчивости (табл. 4). При подавляющем большинстве форм эффективны оральные формы пенициллинов, цефалоспоринов первого-второго поколений и макролидов, их надежнее всего вводить в детской лекарственной форме — гранулах, диспергируемых таблетках Солютаб или сиропе, позволяющей точное дозирование.
С препаратов второго выбора начинают лечение только в случае предшествующей (за последние 2–3 месяца) терапии антибиотиками, а также при внутрибольничной инфекции (у ребенка, заболевшего через 1–3 суток после выписки из стационара). Наиболее используемый препарат — амоксициллин/клавуланат — Амоксиклав, Аугментин, Флемоклав Солютаб), эффективный как против пневмо- и стрептококков, так и гемофильной палочки и моракселл. Цефалоспорины второго поколения (цефуроксим аксетил — Зиннат, который намного активнее цефаклора в отношении пневмо- и стрептококков) также эффективны как препараты второго выбора. Используются возрастные дозировки, однако для амоксициллина/клавуланата и Зинната в ряде инструкций указаны заниженные (20–30 мг/кг/сут) дозы, которые могут оказаться недостаточными (см. наблюдение) — они не должны быть ниже 45–50 мг/кг/сут.
Средства третьего выбора (резервные, обычно парентеральные) применяют только в случаях полирезистентности, обычно в условиях стационара.
Не используют при респираторной патологии ко-тримоксазол и тетрациклин ввиду роста устойчивости к ним пневмотропной флоры, а также оральные цефалоспорины третьего поколения — цефтибутен (Цедекс) и цефиксим (Супракс), которые могут быть недостаточно активными в отношении кокковой флоры, в частности, пневмококков.
Оральные антибиотики не используют при тяжелых острых процессах. К ним относится гнойный синусит (протекает с отеком щеки или окологлазной клетчатки), он часто требует оперативного вмешательства, лимфаденит с признаками гнойного воспаления (спаянность с гиперемированной кожей, флюктуация). У детей с крупом важно исключить эпиглоттит — бактериальное воспаление надгортанника, также вызывающее инспираторный стридор как при вирусном крупе, но с фебрильной температурой, интоксикацией, болями при глотании при отсутствии лающего кашля, дисфонии. Для эпиглоттита характерно усиление диспноэ в положении на спине, нейтрофильный лейкоцитоз, он требует ранней интубации для профилактики асфиксии. Эти заболевания, как и осложненная плевритом и деструкцией пневмония, требуют госпитализации, перед которой следует ввести парентерально препарат широкого спектра — цефтриаксон (80 мг/кг), который должен быть в укладке скорой и неотложной помощи и у каждого участкового врача.
В остальных случаях используются оральные препараты (табл. 4). При подозрении на острый средний отит (или его диагностике при отоскопии) адекватно назначение амоксициллина в дозе 50 мг/кг/сут, или амоксициллина/клавуланата в той же дозе (преодоление устойчивости некапсульного гемофилюса и моракселл), или, у леченного недавно ребенка, в дозе 80–100 мг/кг/сут амоксициллина для преодоления возможной сниженной чувствительности пневмококков в полости среднего уха. В последнем случае желательно использовать Аугментина или Флемоклава Солютаб с соотношением амоксициллина и клавулановой кислоты 7:1. Срок лечения — 10 дней у детей до двух лет и 7 дней — у старших.
Та же лечебная тактика эффективна при негнойном бактериальном синусите, который диагностируют на второй-третьей неделе ОРЗ при сохранении заложенности носа, часто также лихорадки, болей в проекциях пазух.
Большие сложности возникают при лечении острого тонзиллита, который лишь в 30% случаев вызывается БГСА, а в остальных — аденовирусом или вирусом Эпштейна–Барр (инфекционный мононуклеоз). Для них одинаково характерны острое начало, лихорадка с ознобом или без, боль в горле при глотании, гиперемия, отечность миндалин, часто также язычка и мягкого неба, гнойный детрит в лакунах, налеты, увеличение лимфоузлов (без нагноения). Стрептококковый тонзиллит отличается от вирусного отсутствием кашля и катара, конъюнктивита, болезненностью лимфоузлов и падением температуры через 24–48 ч после назначения антибиотика. Аденовирусный тонзиллит отличают конъюнктивит и назофарингит, мононуклеоз — назофарингит, увеличение печени и селезенки, появление в крови широкоплазменных лимфоцитов. Положительный высев делает диагноз БГСА-инфекции бесспорным, как и повышение антистрептолизина-О (АСЛ-О), поэтому во всех случаях острого тонзиллита показаны такие исследования.
При доказанном стрептококковом тонзиллите, как и при неясности этиологического диагноза (особенно у детей старше 6 лет и в весеннее время), назначают один из пенициллинов, цефалексин или макролид, которые приводят к падению температуры через 14–36 часов, подтверждая диагноз стрептококкового тонзиллита; в этих случаях лечение следует продолжить до 10 дней (для азитромицина — в дозе 12 мг/кг/сут — 5 дней). При отсутствии эффекта антибиотик можно отменить, оставив лишь симптоматическое лечение.
При поражении нижних дыхательных путей (его признаки — тахипноэ или диспноэ, наличие хрипов, укорочение перкуторного звука) важно дифференцировать вирусный бронхит от пневмонии, в подавляющем большинстве случаев — бактериальной.
Инфекцию микоплазмой, обусловливающей у детей старше 5 лет около половины всех пневмоний (между пневмонией и бронхитом при неплотном легочном инфильтрате трудно провести грань), следует заподозрить при стойкой (5–10 дней) высокой температуре, обычно с нерезким токсикозом (не вызывающим сильной тревоги родителей), с необильными катаральными симптомами и конъюнктивитом, с обильными, мелкопузырчатыми (как у грудных детей с бронхиолитом) хрипами, но выслушиваемыми асимметрично. Характерный признак — отсутствие эффекта от назначения амоксициллина и других лактамных препаратов; назначение любого макролида в возрастной дозе приводит в течение 1–3 дней к апирексии и уменьшению явлений бронхита.
Для подтверждения или исключения бактериальной инфекции обычно используются так называемые маркеры бактериального воспаления — уровни лейкоцитоза, С-реактивного белка, в последнее время — также прокальцитонина. Нередко приходится видеть ребенка с ОРВИ без видимых бактериальных очагов, который получает антибиотики только потому, что у него выявлен лейкоцитоз порядка 10–15×10 9 /л. У большинства таких больных ОРВИ течет гладко без применения антибиотиков. Доказано, что только лейкоцитоз > 15×10 9 /л, абсолютное число нейтрофилов > 10×10 9 /л и/или палочкоядерных > 1,5×10 9 /л (а также С-реактивный белок (СРБ) > 30 мг/л и прокальцитонин > 2 нг/мл) более или менее надежно указывают на возможность бактериальной инфекции, тогда как более низкие цифры встречаются при вирусных инфекциях достаточно часто. Так, у детей с ОРВИ, бронхитом, крупом лейкоцитоз 10–15×10 9 /л встречается у 1/3, СРБ 15–30 мг/л — у 1/4 больных. При тонзиллитах, вызванных аденовирусами и вирусом Эпштейна–Барр, у 1/3 детей лейкоцитоз лежит в пределах 10–15×10 9 /л, а 1/3 — выше 15×10 9 /л, уровни СРБ 30–60 мг/л выявляются у 1/4 детей, а у 1/3 — выше 60 мг/л.
Следует учитывать и то, что при бактериальных инфекциях лейкоцитоз наблюдается далеко не всегда: так, при гнойном отите и типичной пневмонии у 40% больных лейкоцитоз не превышает 15´109/л, а при катаральном отите и атипичной пневмонии — у 90%.
Литература
В. К. Таточенко, доктор медицинских наук, профессор
НЦЗД РАМН, Москва
Наблюдение
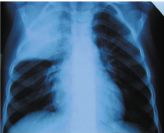

Настя К. 4,5 лет поступила на 4-й день болезни, сопровождавшейся температурой 39 °C, кашлем. Две дозы Флемоклава Солютаба по 15 мг/кг эффекта не дали.
При поступлении: навязчивый кашель, покраснение правой щеки, укорочение над правым легким сверху, хрипов нет. Кровь: Л — 31,6 ´ 109/л, п/я — 29%, с/я 57%, СОЭ 36 мм/час, СРБ 60 мг/л, ПКТ 10 нг/мл.
Доза Флемоклава Солютаба 45 мг/кг привела к падению Т° к концу дня, быстрому улучшению состояния и нормализации картины в легких через 2 недели. Курс лечения — 5 дней.

Коксаки – это кишечный вирус, вернее, довольно большая группа, насчитывающая аж 30 энтеровирусов
Что такое вирус Коксаки?
Коксаки – это кишечный вирус, вернее, довольно большая группа, насчитывающая аж 30 энтеровирусов. Такое название он получил в честь городка Коксаки в США, где он был впервые обнаружен в 1948 году. Тогда Коксаки был выделен из фекальных масс больных полиомиелитом детей. С тех пор эпидемии Коксаки уже бывали не раз, и скорее всего, ждут нас снова. Вирус крайне заразен, причем локализуется он не только в желудочно-кишечном тракте, но может поразить и другие органы. Хорошая новость состоит в том, что раз переболев, больше Коксаки не заразишься: формируется пожизненный иммунитет. Вирус погибает при воздействии высоких температур и дезинфицирующих веществ, а вот в простой водопроводной воде и фекалиях он сохраняется весьма долго.
Кто в группе риска и как можно заразиться?
Чаще всего этим вирусом болеют дети примерно от 3 до 10 лет, что связано с особенностями образа жизни: редким мытьем рук, недостаточной гигиеной. 4-5 лет – самый опасный возраст для заражения данным вирусом. А вот грудничкам Коксаки почти не страшен: во-первых, их иммунитет защищает молоко матери, во-вторых, с гигиеной у них обычно все в полном порядке: в песочницах они не играют и грязные пальцы и предметы в рот до поры до времени не тащат. Заражения чаще всего происходят летом и осенью, особенно на отдыхе у морей. Способов передачи вируса несколько: воздушно-капельный, через немытые руки, грязную сырую пищу, общую посуду.
Каковы проявления заболевания?
От момента заражения до появления первых признаков болезни может пройти до 10 дней. Начинается все довольно резко, взлетает температура до 39 и более градусов, и держится до 3-4 дней, только потом нормализуясь. Жар сопровождается слабостью, головной и мышечной болью. Очень похоже на грипп, однако при этом вирусе добавляется специфическая сыпь и расстройства стула. Сыпь в виде маленьких пузырьков возникает на слизистой рта и горла, на лице вокруг рта, на ладонях, стопах, между пальцами, на ягодицах. Высыпания на слизистой рта сопровождаются сильной болью, при этом дети отказываются есть и пить. Очень важно давать малышу обезболивающее и следить за достаточным потреблением жидкости. Жидкий стул может беспокоить по несколько раз в день, возможна и рвота. У взрослых могут появиться признаки конъюктивита.
Как понять, что это именно Коксаки, а не что-то другое?
Самым правильным будет сдать лабораторные тесты. Для этого берется мазок из носоглотки и анализ кала, а затем образец исследуется ПЦР-методом, что позволяет выявить генотип вируса. Кроме того, можно сдать анализ крови на антитела к вирусу. Какой именно анализ нужно сдать вам (и нужно ли вообще), подскажет врач на основании ваших симптомов и состояния.
Как лечиться?
Во-первых, нужно вызвать врача на дом. Только педиатр или терапевт (в случае, если заболел взрослый человек) на основании осмотра и специального анализа сможет поставить правильный диагноз. Ехать в стационар обычно не нужно, вполне можно лечиться дома. Специальные противовирусные препараты не требуются, нужна только симптоматическая терапия: при высокой температуре выпить жаропонижающее, при зуде кожи или других кожных реакциях на сыпь может понадобиться антисептическое и антигистаминное средство, при интоксикации – прием сорбентов, при боли в горле – антисептики для горла. Если с иммунитетом все в порядке, все проявления вируса пройдут сами за несколько дней без следа. Антибиотики при лечении не применяются, их назначение необходимо только в случае присоединения бактериальной инфекции.
Могут ли возникнуть осложнения?
В большинстве случаев осложнений вируса не возникает. Но изредка возможно развитие крайне опасных ситуаций:
- Серозного менингита. Он характеризуется болями в горле, болью в мышцах, судорогами, лихорадкой, обморочным состоянием и другими признаками. При грамотном и своевременном лечении проходит без последствий.
- Эндокардита, миокардита, то есть поражений сердца. При этом заболевании ребенок все время сонный, давление у него понижено, может появиться аритмия, одышка, судороги. При любых описанных явлениях нужно немедленно вызывать скорую помощь.
- Гепатита. Если вирус поражает печень, то она увеличивается, беспокоит боль в правой стороне живота.
- Обезвоживания. Его признаки – плач без слез у ребенка, очень редкие позывы к мочеиспусканию, все время клонит в сон. Если такое случилось, необходимо лечение в форме капельниц.
- Присоединения вторичной бактериальной инфекции (там, где была сыпь, возникают гнойные выделения, краснота, это место отекает). Лечится такое состояние с помощью антибактериальных мазей.
Чтобы не пропустить осложнения, нужно с самого начала заболевания быть под присмотром врача и по всем вопросам консультироваться с ним, а в экстренных случаях срочно звонить в скорую помощь.
Возможна ли профилактика вируса?
- Во-первых, это постоянное соблюдение гигиены, частое мытье рук, избегание больших скоплений людей без лишней необходимости.
- Во-вторых, это тщательное мытье и приготовление пищи, ведь при термической обработке вирус не выживает. Не стоит пить воду из-под крана, из водоемов и различных ключей, гораздо правильнее будет пить проверенную бутилированную воду.
При соблюдении всех этих нехитрых правил, у вас и ваших детей будет меньше вероятности заразиться Коксаки и другими вирусами.
Запись на прием к врачу педиатру
Читайте также:

