Коли инфекция у новорожденных лечение
Обновлено: 24.04.2024
Эшерихиозы — группа бактериальных антропонозных инфекционных болезней, вызываемых патогенными (диареегенными) штаммами кишечной палочки, протекающих с симптомами общей интоксикации и поражением ЖКТ.
Классификация
Этиология и патогенез
Эшерихии — подвижные грамотрицательные палочки, аэробы, относящиеся к виду Escherichia coli, роду Escherichia, семейству Enterobacteriaceae. Растут на обычных питательных средах, выделяют бактерицидные вещества-колицины. Морфологически серотипы не отличаются друг от друга. Эшерихии содержат соматические (О-Аг — 173 серотипа), капсульные (К-Аг — 80 серотипов) и жгутиковые (Н-Аг — 56 серотипов) антигены. Диареегенные кишечные палочки подразделяются на пять типов:
Факторы патогенности ЭТКП (пили, или фимбриальные факторы) определяют склонность к адгезии и колонизации нижних отделов тонкой кишки, а также к токсинообразованию. Термолабильный и термостабильный энтеротоксины ответственны за повышенную экскрецию жидкости в просвет кишки. Патогенность ЭПКП обусловлена способностью к адгезии. ЭИКП способны, имея плазмиды, проникать в клетки кишечного эпителия и размножаться в них. ЭГКП выделяют цитотоксин, шигоподобные токсины 1-го и 2-го типов, содержат плазмиды, которые облегчают адгезию к энтероцитам. Факторы патогенности энтероадгезивных кишечных палочек изучены недостаточно.
Эшерихии устойчивы в окружающей среде, могут месяцами сохраняться в воде, почве, испражнениях. Сохраняют жизнеспособность в молоке до 34 дней, в детских питательных смесях — до 92 дней, на игрушках — до 3-5 мес. Хорошо переносят высушивание. Обладают способностью размножаться в пищевых продуктах, особенно в молоке. Быстро погибают при воздействии дезинфицирующих средств и при кипячении. У многих штаммов Е. coli отмечают полирезистентность к антибиотикам.
Эшерихии проникают через рот, минуя желудочный барьер, и в зависимости от типовой принадлежности оказывают патогенное действие.
Энтеротоксигенные штаммы способны вырабатывать энтеротоксины и фактор колонизации, посредством которого осуществляются прикрепление к энтероцитам и колонизация тонкой кишки.
Энтеротоксины — термолабильные или термостабильные белки, которые воздействуют на биохимические функции эпителия крипт, не вызывая видимых морфологических изменений. Энтеротоксины усиливают активность аденилатциклазы и гуанилатциклазы. При их участии и в результате стимулирующего действия простагландинов увеличивается образование цАМФ, вследствие чего в просвет кишки секретируется большое количество воды и электролитов, которые не успевают реабсорбироваться в толстой кишке, — развивается водянистая диарея с последующими нарушениями водно-электролитного баланса. Инфицирующая доза ЭТКП — 10х10 10 микробных клеток.
ЭИКП обладают свойством внедряться в клетки эпителия толстой кишки. Проникая в слизистую оболочку, они вызывают развитие воспалительной реакции и образование эрозий кишечной стенки. Из-за повреждения эпителия усиливается всасывание в кровь эндотоксинов. У больных в испражнениях появляются слизь, кровь и полиморфно-ядерные лейкоциты. Инфицирующая доза ЭИКП — 5х10 5 микробных клеток.
Механизм патогенности ЭПКП изучен недостаточно. У штаммов (055,086,0111 и др.) выявлен фактор адгезии к клеткам Нер-2, за счёт которого происходит колонизация тонкого кишечника. У других штаммов (018, 044, 0112 и др.) этот фактор не обнаружен. Инфицирующая доза ЭПКП — 10х10 10 микробных клеток.
ЭГКП выделяют цитотоксин (SLT — shiga-like toxin), который разрушает клетки эндотелия, выстилающего мелкие кровеносные сосуды кишечной стенки проксимальных отделов толстой кишки. Сгустки крови и фибрин препятствуют кровоснабжению кишки — в кале появляется кровь. Развивается ишемия кишечной стенки, вплоть до некроза. У некоторых больных наблюдают осложнения с развитием синдрома диссеминированного внутрисосудистого свёртывания (ДВС), ИТШ и ОПН.
ЭАКП способны к колонизации эпителия тонкой кишки. Вызванные ими заболевания взрослых и детей протекают длительно, но легко. Это связано с тем, что бактерии прочно закрепляются на поверхности эпителиальных клеток.
Эпидемиология
Основной источник эшерихиозов — больные со стёртыми формами заболевания, меньшую роль играют реконвалесценты и носители. Значимость последних возрастает, если они работают на предприятиях по приготовлению и реализации пищевых продуктов. По некоторым данным, источник возбудителя при энтерогеморрагических эшерихиозах (0157) — крупный рогатый скот. Инфицирование людей происходит при употреблении продуктов, которые были недостаточно термически обработаны. Механизм передачи — фекально-оральный, который осуществляется пищевым, реже — водным и бытовым путём. По данным ВОЗ, для энтеротоксигенных и энтероинвазивных эшерихии характерен пищевой, а для энтеропатогенных — бытовой путь.
Из пищевых продуктов чаще фактором передачи служат молочные изделия, готовые мясные продукты, напитки (квас, компот и др.).
В детских коллективах инфекция может распространяться через игрушки, загрязнённые предметы обихода, руки больных матерей и персонала. Реже регистрируют водный путь передачи эшерихиозов. Наиболее опасно загрязнение открытых водоёмов, которое происходит в результате сброса необезвреженных хозяйственно-бытовых сточных вод, особенно из детских учреждений и инфекционных больниц.
Основу профилактики эшерихиозов составляют меры по пресечению путей передачи возбудителя. Особенно важно соблюдать санитарно-гигиенические требования на объектах общественного питания, водоснабжения; предупреждать контактно-бытовой путь заражения в детских учреждениях, родильных домах, стационарах (использование индивидуальных стерильных пелёнок, обработка рук дезинфицирующими растворами после работы с каждым ребёнком, дезинфекция посуды, пастеризация, кипячение молока, молочных смесей). Продукты, готовые к употреблению, и сырые, нужно разделывать на разных досках отдельными ножами. Посуду, в которой транспортируют пищу, необходимо обрабатывать кипятком.
При подозрении на эшерихиоз необходимо обследовать беременных до родов, рожениц, родильниц и новорождённых.
Контактных в очаге заболевания наблюдают 7 дней. Детей, контактных с больным эшерихиозом по месту жительства, допускают в детские учреждения после разобщения с больным и трёхкратных отрицательных результатов бактериологического исследования кала.
При выявлении больных эшерихиозом в детских учреждениях и родильных домах прекращают приём поступающих детей и рожениц. Персонал, матери, дети, бывшие в контакте с больным, а также дети, выписанные домой незадолго до заболевания, обследуются трёхкратно (проводят бактериологическое исследование кала). При выявлении лиц с положительными результатами обследования их изолируют. Больных, перенёсших эшерихиоз, наблюдают в течение 3 мес с ежемесячным клиническим и бактериологическим обследованием в КИЗ. Перед снятием с учёта — двукратное бактериологическое исследование кала с интервалом в 1 день.
Клиническая картина
Cимптомы, течение
Клинические проявления эшерихиозов зависят от типа возбудителя, возраста больного, иммунного статуса.
Заболевание начинается остро, больных беспокоят слабость, головокружение. Температура тела нормальная или субфебрильная. Появляются тошнота, повторная рвота, разлитые схваткообразные боли в животе. Стул частый (до 10-15 раз в сутки), жидкий, обильный, водянистый, нередко напоминающий рисовый отвар. Живот вздут, при пальпации определяют урчание, небольшую разлитую болезненность. Тяжесть течения определяется степенью дегидратации. Возможна молниеносная форма заболевания с быстрым развитием эксикоза. Длительность болезни 5-10 дней.
Особенности эшерихиоза, вызванного энтероадгезивными штаммами, изучены мало. Заболевание регистрируют у пациентов с ослабленной иммунной системой. Чаще выявляют внекишечные формы — поражение мочевыводящих (пиелонефрит, цистит) и желчевыводящих (холецистит, холангит) путей. Возможны септические формы (коли-сепсис, менингит).
Диагностика
Клиническая картина эшерихиозов сходна с клинической картиной других диарейных инфекций. Поэтому диагноз подтверждают на основании бактериологического метода исследования. Материал (испражнения, рвотные массы, промывные воды желудка, кровь, моча, ликвор, жёлчь) следует брать в первые дни болезни до назначения больным этиотропной терапии. Посевы производят на среды Эндо, Левина, Плоскирева, а также на среду обогащения Мюллера.
Используют иммунологические методы исследования РА, РИГА в парных сыворотках, но они не убедительны, так как возможны ложноположительные результаты из-за антигенного сходства с другими энтеробактериями. Эти методы используют для ретроспективной диагностики, особенно во время вспышки.
Перспективным методом диагностики служит ПЦР. Инструментальные методы исследования (ректороманоскопия, колоноскопия) при эшерихиозах малоинформативны.
Дифференциальный диагноз
Дифференциальную диагностику эшерихиозов проводят с другими острыми диарейными инфекциями: холерой, шигеллёзом, сальмонеллёзом, кампилобактериозом, ПТИ стафилококковой этиологии и вирусными диареями: ротавирусной, энтеровирусной, Норволк-вирусной инфекцией и др.
В отличие от эшерихиозов, холера характеризуется отсутствием интоксикации, лихорадки, болевого синдрома, наличием многократной рвоты, быстрым развитием дегидратации III-IV степени. Помогает в постановке диагноза эпидемиологический анамнез — пребывание в эндемичных для холеры регионах.
Сальмонеллёз, в отличие от эшерихиозов, характеризуется более выраженной интоксикацией, разлитыми болями в животе, болезненностью при пальпации в эпигастральной и околопупочной областях, урчанием. Характерен зловонный стул зеленоватого цвета.
Для ПТИ стафилококковой этиологии, в отличие от эшерихиозов, характерны острое, бурное начало заболевания, короткий инкубационный период (30-60 мин), более выражены симптомы интоксикации, рвота неукротимая. Боли в животе режущего характера, с локализацией в эпигастральной и околопупочной областях. Характерны групповой характер заболевания, связь заболевания с пищевым фактором, быстрый регресс болезни.
Осложнения
Чаще эшерихиозы протекают доброкачественно, но возможны осложнения: ИТШ, гиповолемический шок с дегидратацией III-IV степени, ОПН, сепсис, пневмония, пиелоцистит, пиелонефрит, холецистит, холангит, менингит, менингоэнцефалит. Летальный исход в результате ОПН (синдром Гассера) регистрируют у детей до 5 лет в 3-7% случаев. В Москве за последние 10 лет летальных исходов не было.
Лечение
В остром периоде болезни больным рекомендуют щадящую терапию (стол № 4, при нормализации стула — № 2, в период реконвалесценции — № 13).
В лёгких случаях заболевания достаточно назначения оральной регидратационной терапии (регидрон и другие растворы, количество которых должно в 1,5 раза превышать потери воды с испражнениями).
Показаны ферменты (панзинорм-форте, мезим-форте), энтеросорбенты (полисорб, энтеросгель, энтеродез в течение 1-3 дней). При лёгком течении болезни целесообразно использование кишечных антисептиков (интетрикс по две капсулы три раза в день, неоинтестопан после каждого акта дефекации по две таблетки, до 14 в сутки, энтерол по две капсулы два раза в день) в течение 5-7 дней. Лёгкие и стёртые формы эшерихиозов не требуют назначения этиотропных препаратов.
При лечении больных в условиях стационара показан постельный режим в первые 2-3 дня. Назначают этиотропную терапию. С этой целью при среднетяжёлых формах используют один из следующих препаратов: ко-тримоксазол по две таблетки два раза в день или препараты фторхинолонового ряда (ципрофлоксацин по 500 мг два раза в сутки перорально, пефлоксацин по 400 мг два раза в сутки, офлоксацин по 200 мг два раза в сутки), длительность терапии 5-7 дней.
В тяжёлых случаях фторхинолоны применяют вместе с цефалоспоринами 2-го (цефуроксим по 750 мг четыре раза в сутки внутривенно или внутримышечно; цефаклор по 750 мг три раза в сутки внутримышечно; цефтриаксон 1,0 г один раз в сутки внутривенно) и 3-го поколения (цефоперазон по 1,0 г два раза в сутки внутривенно или внутримышечно; цефтазидим по 2,0 г два раза в сутки внутривенно или внутримышечно).
При дегидратации II-III степени назначают регидратационную терапию внутривенно кристаллоидными растворами (хлосоль, ацесоль и пр.), которую проводят по общим правилам.
При выраженных симптомах интоксикации используют коллоидные растворы (декстран и др.) в объёме 400-800 мл/сут.
После приёма антибактериальных препаратов при продолжающейся диарее используют эубиотики для коррекции дисбактериозов (бифидумбактерин-форте, хилак-форте и др.) в течение 7-10 дней. Больных выписывают после полного клинического выздоровления, нормализации стула и температуры тела, а также однократного бактериологического исследования кала, которое проводят не ранее чем через 2 дня после окончания лечения.
При лёгкой форме заболевания 5-7 дней, при среднетяжёлой 12-14 дней, при тяжёлой — 3-4 нед. Диспансеризация не регламентирована.
Госпитализация
Госпитализацию больных с эшерихиозами проводят по клиническим и эпидемиологическим показаниям. Больных при среднетяжёлом и тяжёлом течении заболевания госпитализируют в инфекционные больницы. В лёгких случаях больные могут лечиться амбулаторно при наличии благоприятных бытовых, санитарно-гигиенических условий.
По эпидемиологическим показаниям госпитализации подлежат лица из декретированных групп, больные из организованных коллективов, а также пациенты, проживающие в коммунальных квартирах, общежитиях.
Эшерихиоз (коли-инфекция, колибактериоз) – это острая кишечная инфекция, которую вызывают грамотрицательные бактерии Escherichia coli (E.coli), или кишечная палочка, а точнее, ее патогенные штаммы. Дело в том, что безвредные штаммы E.coli в норме присутствуют в ЖКТ каждого человека и даже несут полезную функцию, помогая организму синтезировать витамин К и бороться с патогенной микрофлорой. В кишечник новорожденного они заселяются уже в первые сутки после его появления на свет и сопровождают его всю жизнь. При эшерихиозе, однако, в дело вступают другие штаммы E.coli, вызывающие отравление.
В зависимости от того, какими именно эшерихиями инфицирован организм ребенка, в детской медицине принято делить эту болезнь на шесть подвидов:
- энтеропатогенный (ЭПЭК) – поражает преимущественно грудничков первого года. У детей старше 3 лет он практически не встречается. Особенно подвержены ему недоношенные и ослабленные дети, груднички с рахитом или анемией, а также находящиеся на искусственном вскармливании. Характеризуется ярко выраженной диареей, рвотой, метеоризмом, и, поскольку у маленьких детей быстро начинается обезвоживание, довольно опасен. А поскольку у детей первого года жизни еще не сформирован пассивный иммунитет, и ЖКТ в силу анатомических особенностей более уязвим, нередко при нем инфекция генерализуется, захватывая весь организм, вплоть до развития коли-сепсиса.
- энтероинвазивный (ЭИЭК) – затрагивает детей всех возрастных групп, в основном, старше 1 года. По своим проявлениям очень схож с шигеллезом (дизентерией), но встречается реже. Заболевание начинается резко, скачком температуры и рвотой. В тяжелой форме у детей старше года практически не встречается.
- энтеротоксигенный (ЭТЭК) – встречается в основном у детей раннего возраста и формирует стойкий иммунитет, поэтому крайне редко диагностируется у взрослых. Передается в основном пищевым путем. В отличие от других вариантов, характеризуется сильной диареей и иногда рвотой при нормальной температуре тела (не выше субфебрильных значений), что роднит его с холерой. Развивается быстрое обезвоживание.
- энтерогемморагический (ЭГЭК) – как правило, диагностируется у дошкольников от 1 года до 5 лет. Часто передается человеку от крупного рогатого скота. В тяжелых формах может вызывать кровотечения и некрозы стенок кишечника.
- энтероаггрегативный и диффузно-адгезивный типы – у детей встречаются очень редко, могут проявляться внекишечными воспалениями, например, циститом, холециститом, пиелонефритом.
Как ребенок может заразиться эшерихиозом?
E.coli передаются обычно пищевым или водным путем, а также воздушно-пылевым и контактно-бытовым, в том числе от человека к человеку. Известны и случаи заражения от домашних животных. На поверхностях предметов комнатной температуры они могут выживать более 100 дней, в молоке – до месяца (причем прекрасно в нем размножаются), в детских смесях для питания – до 3 месяцев. Не погибают при высушивании. При этом у многих штаммов выработалась резистентность ко многим антибиотикам. Гибнут они только при кипячении и при обработке дезинфицирующими средствами.
Сезонный подъем заболеваемости зависит от штамма: у ЭПЭК это зима-весна, у прочих – лето.
Исходя из этого, профилактика колибактериоза сводится к соблюдению общепринятых гигиенических норм: мыть с мылом руки и предметы, которые грудничок может взять в рот, мыть овощи и фрукты, по возможности подвергать продукты термической обработке.
Как понять, что у ребенка эшерихиоз?
Симптомы различаются в зависимости от подвида патогенной бактерии, от возраста ребенка и от тяжести протекания инфекции. Они могут быть схожи с множеством других заболеваний ЖКТ – в диапазоне от диспепсии до сальмонеллеза и холеры. Кроме того, эшерихиоз может вызывать осложнения: отит, цистит, пиелонефрит и даже менингит. Поэтому при любых проявлениях поражения ЖКТ необходимо как можно скорее обратиться к грамотному педиатру, чтобы начать лечение и избежать развития тяжелых форм интоксикации.
Для грудных малышей более характерны энтеропатогенная (ЭПЭ) и энтеротоксигенная (ЭТЭК) формы. Симптоматика при обеих довольно схожая. При пищевом пути передачи болезнь начинается резко, с подъема температуры, рвоты и диареи, при контактном – более сглажено. Испражнения водянистые, желтые или оранжевые, иногда пенистые или кашицеобразные. Рвота сохраняется до 2 раз в сутки. Характерна бледность кожи, вздутие живота, метеоризм, снижение аппетита. Проявления достигают пика на 5-7 день, затем идут на спад.
Остальные подвиды обычно поражают детей старше года. При энтероинвазивном виде повышается температура (обычно умеренно), возникают схваткообразные боли в животе, испражнения скудные, с примесью слизи или крови. Симптомы интоксикации идут на спад после первых двух суток. При энтерогемморагическом варианте температура повышается редко, начинает сильно болеть живот, стул водянистый, позднее в нем появляется примесь крови. Сильно бледнеет кожа, на 3-5 день состояние пациента ухудшается.
Для постановки диагноза инфицирование E.coli должно быть подтверждено лабораторным исследованием. На анализ обычно берут испражнения и/или кровь. Необходимы также общие анализы крови и мочи и биохимический анализ крови.
Как лечат эшерихиоз?
Дети с легким течением болезни обычно лечатся дома, где их посещает педиатр из поликлиники. Госпитализируют пациентов со среднетяжелым и тяжелым течением, а также обычно новорожденных, поскольку их врачи должны наблюдать постоянно.
Обычно педиатр назначает заболевшему регидратационную терапию для восполнения уровня жидкости и электролитов, симптоматическую терапию для облегчения его состояния, пробиотики, энтеросорбенты, ферменты и иногда иммуноглобулины. Антибиотики выписывают детям до года и пациентам в среднетяжелом и тяжелом состоянии.
Как и при любых кишечных расстройствах, очень важно соблюдение диеты. Грудничков необходимо кормить меньшими порциями, но чаще, чем обычно. Постепенно объем каждого кормления увеличивается, как и промежуток между ними.
Стафилококковый энтероколит у детей. Кишечная коли-инфекция
Стафилококковым энтероколитом заболевают преимущественно дети раннего возраста, особенно недоношенные и дети с неблагоприятным преморбидным фоном, у которых снижена специфическая иммунологическая защита против стафилококка и в то же время защитные барьеры (кожа, слизистые оболочки) легко проницаемы для инфекции. Заболеванию особенно подвержены дети с наследственным иммунодефицитным состоянием.
Начало заболевания постепенное. Течение длительное. Различают первичный стафилококковый энтероколит и вторичный.
Первичный энтероколит развивается на фоне полного здоровья после контактов с больными гнойными заболеваниями или пищевым отравлением. Вторичный энтероколит развивается значительно чаще на фоне различных заболеваний (острые респираторные инфекции, пневмония, дизентерия) в результате экзогенной или эндогенной стафилококковой инфекции, как результат дисбактериоза (при длительном течении основного заболевания и применении, антибиотиков), а также при генерализованных формах стафилококковой инфекции (сепсис, пиодермия, стафилококковая пневмония).
В механизме развития вторичных стафилококковых энтероколитов придают значение аллергическим состояниям организма.
Патологоанатомические изменения при энтероколитах могут быть распространенными или ограниченными. Воспаление имеет серозно-десквамативный, фибринозно-гнойный или некротический характер. Некроз слизистой оболочки может распространяться до серозного покрова, при: этом образуются глубокие язвы с гнойной инфильтрацией их. дна и краев с большим количеством колоний микробов. В сосудах брыжейки па фоне нарушения кровообращения могут обнаруживаться тромбы.
В отдельных случаях воспаление имеет распространенный геморрагически-некротический характер с массивной лейкоцитарной инфильтрацией.
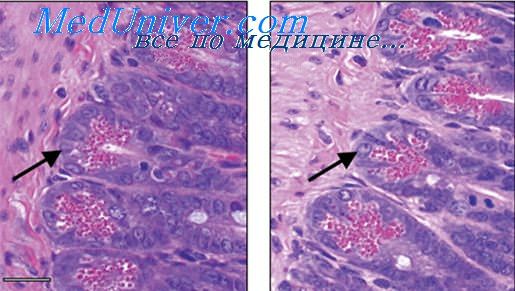
Наблюдаются редкие случаи стафилококкового псевдо-мембранозного энтероколита. Патогенез его не ясен: характеризуется развитием поверхностного некроза слизистой оболочки и образованием мембраны из омертвевшей части слизистой оболочки, пронизанной фибрином, слизью, лейкоцитами и бактериями.
При стафилококковом энтероколите возможны осложнения в виде перфорации стенки кишок, развития фибринозно-гнойно-калового перитонита, развития стафилококкового сепсиса. Смерть наступает от осложнений или токсикоза.
Кишечная коли-инфекция
В этиологии и эпидемиологии кишечной коли-инфекции имеют значение патогенные штаммы кишечной палочки 0III-В4, 055-В5, 026-В6, 0145. Они отличаются от непатогенных штаммов кишечных палочек по антигенному строению (соматический антиген О, поверхностный — К с подгруппами А и В и жгутиковый — В).
Кишечная коли-инфекция — болезнь преимущественно детей 1-го года жизни, особенно новорожденных и недоношенных, у которых отмечается высокая восприимчивость к этой инфекции. Измененные защитные свойства организма ребенка, снижение его резистентности имеют основное значение для развития и тяжести течения кишечной коли-инфекции.
Заражение происходит от больных и реконвалесцентов контактным путем, через воду, молоко.
Возможна аутоинфекция, самозаражение. Патогенез кишечной коли-инфекции недостаточно изучен. Полагают, что основным условием развития заболевания является переселение кишечной палочки в верхние отделы желудочно-кишечного тракта, где в норме она не обитает. У новорожденных, особенно недоношенных, этому благоприятствуют возрастные особенности — сниженная кислотность и бактерицидность желудочного сока, высокая проницаемость эпителиального барьера кишок и эндотелиального барьера капилляров.
В патогенезе заболевания придают большое значение дисбактериозу. В эксперименте отмечают, что при нарушении нормальной флоры кишечника нарушается барьерная функция кишечной стенки. Энтеропатогенные бактерии проникают в стенку по межклеточным промежуткам и через микрососуды в кровь. Е. coli не способны к внутриклеточному паразитированию. Характерные проявления болезни вызывает энтеротоксин. Возникает токсемия с общим токсикозом, резким поражением капилляров и нервной системы.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Врожденные инфекции у плода и новорожденного ребенка: виды, возбудители, клиника, диагностика
Передача врождённых и перинатальных инфекций плоду происходит через плаценту (внутриутробные инфекции), во время родов или при контакте с физиологическими жидкостями матери. Длительное разрушение плодных оболочек также способствует развитию внутриутробных заболеваний. Кроме того, заражение может произойти и после рождения (при контакте с матерью и другими людьми).
Врожденная краснуха
Первый признак врождённой краснухи — желтуха, как следствие развития гепатита. Часто возникает гемолиз и тромбоцитопеническая пурпура, а также слабовыраженные клинические проявления менингоэнцефалита. У некоторых новорождённых обнаруживают признаки метафизарной дисплазии. Инфицированные дети при рождении обычно имеют сниженную массу тела и отстают в физическом развитии.
В тяжёлых случаях болезнь обычно заканчивается летальным исходом. Наиболее грозные осложнения — незаращение артериального протока, катаракта, глухота, ретинопатия.
Тест на антитела к краснухе (IgM), которые можно обнаружить в крови детей до 3-го мес жизни, даёт положительный результат. При заболевании матери в I триместре вероятность развития патологии у ребёнка составляет 60%, поэтому некоторые женщины предпочитают прерывать беременность. В дальнейшем риск заметно снижается (2% после 20-й нед), в связи с чем выбор между рождением ребенка с вероятными нарушениями в развитии и прерыванием беременности необходимо делать крайне осторожно.
Цитомегаловирус у плода и новорожденного
Инфекция проявляется примерно в 1% случаев, при этом тяжёлая форма заболевания развивается только у 1% инфицированных. Наиболее высокий риск заражения плода отмечают на сроке гестации, соответствующем I триместру беременности. Симптомы заболевания у новорождённых — сниженная масса тела, гепатомегалия, спленомегалия, тромбоцитопения, продолжительная желтуха, повышенная возбудимость, судорожный синдром, аномальный мышечный тонус и двигательные расстройства.
Наиболее частые осложнения — микроцефалия, нейросенсорная глухота. Нередко обнаруживают кальцификацию головного мозга, гемиплегию (паралич мышц одной стороны тела), замедление психомоторных реакций, хориоретинит и миопатию. Диагностика основана на обнаружении антител к цитомегаловирусу (IgM) или определении экскреции вируса в течение первых двадцати дней жизни.
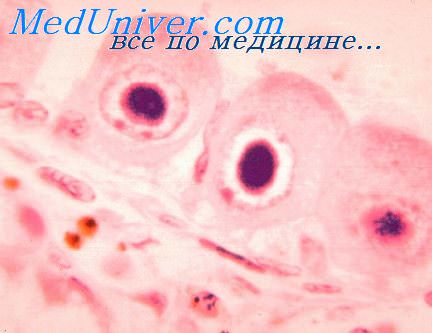
Возбудитель ЦМВ инфекции
Врожденная инфекция вируса простого герпеса
Первичная инфекция, вызванная вирусом простого герпеса, сопровождается виремией. При этом может произойти трансплацентарное заражение плода. При врождённом инфицировании дети рождаются с тяжёлыми отклонениями (пневмония, менингоэнцефалит, гепатоспленомегалия, цитопения), но лишь у некоторых из них присутствуют герпетические очаги на коже и слизистых оболочках. Лечение ацикловиром позволяет снизить смертность с 80—90% до 10—15%.
Терапию следует начинать до получения результатов лабораторного анализа. Первичная инфекция также возникает при заражении от матери, страдающей генитальным герпесом. При этом в первые дни жизни ребёнка возникают очаги на коже, конъюнктиве, слизистой оболочке рта и половых органов, а в 50% случаев наблюдают генерализованное течение инфекции. Лечение: внутривенное введение ацикловира.
Ветряная оспа плода
Инфицирование плода ветряной оспой возникает при заражении беременной в I—II триместре беременности, при этом вероятность передачи инфекции плоду составляет 3%. Заболевание характеризуется развитием рубцовой контрактуры в области лимбических структур головного мозга, микроцефалии или офтальмомикрии. Непривитые беременные в течение десяти дней после возможного заражения (контакта) должны пройти профилактический курс введения иммуноглобулина (содержащим антитела к вирусу ветряной оспы).
Ветряная оспа новорождённых возникает при заболевании матери в течение одной недели до родов. Смертность составляет 40%, поэтому в первые 48 ч жизни ребёнку необходимо ввести специфический иммуноглобулин. При ухудшении состояния следует незамедлительно начать лечение ацикловиром. Применение нормального иммуноглобулина человека не защищает новорождённого от заражения. В некоторых странах применяется вакцина.
Врожденный листериоз
Трансплацентарная передача Listeria monocytogenes происходит при заражении матери инфекцией, протекающей бессимптомно. Заболевание матери на ранних стадиях беременности обычно приводит к смерти плода, а на более поздних — к преждевременным родам. Инфекцию новорождённых обычно осложняет бактериемия, гепатоспленомегалия, менингоэнцефалит, тромбоцитопения и пневмония. При интранатальном заражении инфекция развивается в течение первых двух недель жизни ребенка и сопровождается менингитом и бактериемией.
Для выделения возбудителя на анализ отбирают кровь, спинномозговую жидкость, плацентарную ткань и послеродовую жидкость из матки. Инфицированную мать и ребёнка помещают в отдельную палату, так как они могут стать причиной вспышки заболевания в родильном отделении. Препарат выбора — ампициллин (иногда в комплексе с гентамицином); длительность лечения 2—6 нед.
Врожденный сифилис
Благодаря эффективным пренатальным исследованиям случаи врождённого сифилиса в настоящее время достаточно редки. У заражённых детей обнаруживают лихорадку, а также симптомы, свойственные вторичному сифилису, сыпь, кондиломы и трещины на слизистых оболочках. При развитии остеохондритов возникает выраженный болевой синдром. Очень часто отмечают постоянный насморк (сопение, гнусавость).
Для подтверждения диагноза применяют темнопольную микроскопию образцов поражённой кожи и слизистых оболочек. Специфические IgM или другие антитела персистируют в организме свыше 6 мес после перенесённой инфекции. Поздние симптомы (глухота, атрофия зрительного нерва, паретический нейросифилис) наблюдают в возрасте 12—20 лет. Нередко возникают бугристые образования на лобных костях, хронический большеберцовый периостит, перфорация передних зубов, деформация первых постоянных коренных зубов и высокий изгиб нёба. Препарат выбора — пенициллин.
Врожденный токсоплазмоз
Вероятность врождённого токсоплазмоза варьирует в разных регионах. Например, в Великобритании его регистрируют достаточно редко, а во Франции — часто. При заражении беременной трансплацентарную передачу инфекции плоду наблюдают в каждом третьем случае. Наиболее высок риск развития патологии плода (мертворождение, смерть после рождения, кальцификация головного мозга, церебральный паралич и эпилепсия) при заражении женщины в I и II триместре беременности.
Хориоретинит может возникать только спустя некоторое время после рождения и быть единственным симптомом болезни. Токсоплазмоз у матери подтверждают при обнаружении специфических антител (IgM) или сероконверсии. IgM также обнаруживают у инфицированных новорождённых. Применение спирамицина позволяет снизить риск трансплацентарного заражения, но не влияет на исход заболевания у новорождённых.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Причины инфекции у новорожденных. Определяемся
Проводится рентгенография грудной полости наряду со скринингом сепсиса, включающим полный анализ крови для выявления нейтропении и культур крови. Белки острой фазы (С-реактивный белок — СРБ) полезны, однако для их увеличения требуется 12-24 ч, поэтому один положительный результат не исключает инфекцию, однако два последовательных нормальных значения достоверно подтверждают отсутствие инфекции.
Антибиотики назначают сразу же, не дожидаясь результатов посева культуры. Антибиотики против стрептококков группы В, Listeria monocytogenes и других грамположительных микроорганизмов (обычно бензилпенициллин или амоксициллин) вводятся внутривенно в сочетании с антибиотиками против грамотрицательных бактерий (обычно аминогликозидами, например гентамицином). Если результат посева культур и ЦРП отрицательный и младенец клинически выздоравливает, через 48 ч прекращается введение антибиотиков.
Если результат посева культур положительный и если имеются какие-либо неврологические признаки, необходимо провести обследование и посев СМЖ.

Инфекции новорожденных с поздним началом (>72 ч)
Спустя 72 ч после рождения источником инфекции становится обстановка, окружающая ребёнка. Проявления инфекции обычно неспецифичные.
Клинические особенности неонатального сепсиса:
- Жар, или нестабильность температуры, или гипотермия.
- Плохое питание.
- Рвота.
- Апноэ и брадикардия.
- РДС.
- Сонливость.
- Желтушность.
- Нейтропения.
- Гипо-/гипергликемия.
- Шок.
- Раздражительность.
- Судороги.
- Вздутие живота.
При менингите у новорожденных наблюдают:
- отведение головы кзади (опистотонус);
- напряжённые или выбухающие роднички.
В неонатальном отделении или послеродовой палате имеется высокий риск инфицирования нозокомиальными инфекциями. Весь персонал должен строго придерживаться правил по эффективной обработке рук для предотвращения перекрёстного инфицирования. При интенсивной терапии другими основными источниками инфицирования являются установленные катетеры для парентерального питания или забора проб крови для анализа газового состава, трахеальные трубки, инвазивные процедуры, нарушающие защитный кожный барьер.
В данной ситуации коагулазонегативный стафилококк (Staph, epidermidis) является наиболее часто встречающимся патогеном, однако спектр микроорганизмов широкий и включает Staph, aureus, Escherichia coli, Pseudomonas species, грибы, например Candida. Цель первоначальной терапии (например, флуклоксациллином или гентамицином) — ирадикация большинства стафилококков и грамотрицательных бактерий. Если микроорганизмы устойчивы к этим антибиотикам или состояние младенца не улучшается, необходимы более мощные антибиотики (например, ванкомицин). Серийные исследования белков острой фазы (СРВ) позволяют проводить мониторинг ответа на терапию.
Менингит в неонатальном периоде встречается редко, однако уровень смертности при нём составляет 20-50%, а у трети выживших младенцев остаются серьёзные последствия. Клинические признаки аналогичны таковым при других формах неонатального сепсиса. Выбухание родничка и гиперэкстензия шеи и спины (опистотонус) являются поздними признаками.
Если подозревается менингит, назначают ампициллин или пенициллин и цефалоспорин III поколения (например, цефотаксим, проникающий в СМЖ).
Осложнения включают абсцесс мозга, вентрикулит, гидроцефалию, нарушения слуха и развития нервной системы.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Читайте также:

