Количество лимфоцитов при сифилисе
Обновлено: 18.04.2024
О том, что такое лимфоциты и какую роль они выполняют в организме человека, рассказывает врач-иммунолог Гордиенко Наталия Николаевна. Так же речь пойдет о количестве лимфоцитов в разные периоды жизни: у детей у взрослых, во время беременности.
Виды лимфоцитов
Когда костный мозг выбрасывает в кровеносное русло молодой лимфоцит, он ещё не готов к выполнению своих тончайших функций. Часть из молодых клеток, лимфоцитов, уходит в тимус, или вилочковую железу, и там они должны пройти дозревание или "обучение". Что значит "обучение"? Молодой лимфоцит должен познакомиться с теми антигенами, с которыми наш организм встречался на протяжении всей жизни, начиная с внутриутробного развития. После дозревания тимусозависимые лимфоциты (Т-лимфоциты) начнут распознавать антигены, понимать, что это генетические чужаки и будут готовы к выполнению своих задач.
Т-лимфоциты.
Всего Т-лимфоцитов выделяют несколько видов.
Первый вид – это Т-киллеры. Киллеры – это убийцы. Именно они заточены на то, чтобы распознать генетического чужака и попытаться сразу его убить.
Второй вид – это Т-хелперы, или клетки-помощники. Именно Т-хелперы будут включать следующие клетки, которые будут вырабатывать для нас антитела или защитные белковые структуры.
Третий тип — Т-супрессоры – те клетки, которые будут останавливать иммунный ответ.
И так, если в организм человека попадает генетический чужак, первыми распознавать его будут киллеры, и попытаются сразу убить. Что может выступать в роли генетического чужака? Это вирусы, бактерии, паразиты, грибы, онкоклетки, которые могут появляться ежесекундно. Клетки организма в которых произошёл сбой на генетическом уровне. Если у человека есть непереносимость продуктов питания, то они, к сожалению, тоже могут превратиться в генетических чужаков и тоже истощать лимфоцитарное звено иммунной системы.
В-лимфоциты
Это тоже лимфоциты, которые, выйдя молодыми из костного мозга в кровеносное русло, устремляются в лимфатические узлы, в селезёнку, или в печень, где тоже будет происходить их дозревание. Основная функция В-клеток – это вырабатывать для нас представителей гуморального иммунитета, или кровяного иммунитета. Это именно В-клетки будут вырабатывают антитела, которые будут бороться с вирусами, бактериями – с другими генетическими чужаками.
NK-клетки или натуральные киллеры.
Это группа клеток, которое в первую очередь будет заточено на охрану нас от онкозаболеваний. В первую очередь, натуральные киллеры будут работать в противоопухолевой защите, в противопаразитарной защите. NK-клетки — это основные виды лимфоцитов.
Норма лимфоцитов в крови
К сожалению, бывают часто ситуации, когда лимфоциты в крови могут отклоняться от нормы — повышать или понижаться. Это может быть при различных ситуациях. Прежде, чем говорить о том, когда количество лимфоцитов меняется в крови, нужно поговорить о том, сколько же их нормальная составляющая.
Если говорить о клонах клеток, то:
Т-клетки составляют от общего количества лимфоцитов 75%;
В-клетки где-то 15%;
Естественные киллеры где-то 10%.
И говоря о нормах лимфоцитов, нужно сказать, что в разные периоды жизни человека нормы отличаются.
Лимфоциты начинают вырабатываться костным мозгом уже внутриутробно, и продолжается этот процесс всю жизнь. Продолжительность жизни этих клеток тоже бывает различной – от нескольких месяцев, до шестидесяти лет. И это всё будут лимфоциты.
Норма лимфоцитов у детей и взрослых
- До 1 года содержание лимфоцитов в крови от общего количества всех клеток — 45-70%.
- От 1-2 лет концентрация лимфоцитов должна снижаться — где-то 39-60%.
- От 2-4 то где-то от 33-50% всех белых клеток.
- От 4-10 лет, уже 30-50%.
- От 10-18 лет, то это уже 30-44%.
- У взрослого человека лимфоцитов в крови должно быть от 19-37%.
Количество лимфоцитов в крови при беременности
Соответственно бывают периоды жизни, особенно в женском организме, когда концентрация лимфоцитов тоже будет снижаться. В первую очередь я имею в виду беременность. Для того, чтобы не случилось иммунологического отторжения, всё-таки у плода 50% чужеродных клеток, организм так устраивает всё, что снижается выработка своих собственных лимфоцитов. Именно поэтому мы говорим о физиологическом, иммунодепрессивном состоянии у женщин в период беременности. Идёт снижение иммунитета, чтобы женщина могла спокойно доносить плод.

В рамках консультации вы сможете озвучить свою проблему, врач уточнит ситуацию, расшифрует анализы, ответит на ваши вопросы и даст необходимые рекомендации.
Повышение и понижение лимфоцитов в анализе крови
И так, мы с вами уже поняли, что лимфоциты – это главные клетки нашей иммунной системы. И в зависимости от того, как изменяется их количество в крови, и будут называться изменения формулы крови.
Что заставляет нашу иммунную систему и костный мозг выбрасывать в кровь повышенное количество лимфоцитов? Поскольку это основные клетки, которые стоят на генетической защите нас, значит нужно понимать, что "в государстве не все в порядке".
Ещё хочу обратить ваше внимание — лимфоцитоз, и лимфопения – не заболевания. Это состояния организма человека, при которых в иммунной системе протекает, или не протекает бурная реакция. И любое изменение количества лимфоцитов всегда будет говорить о том, что нужно проверить, какие причины привели к тому или иному изменению.
В последние годы большое внимание уделяется изучению врожденного и адаптивного иммунитета в развитии сифилиса. Показано, что изменения иммунного статуса могут привести к диссеминации бледной трепонемы с формированием вторичных форм и серорезистентности. Цель исследования: анализ показателей иммунофенотипирования клеток крови и сывороточных иммуноглобулинов у пациентов с серорезистентным, ранним и поздним скрытым сифилисом. Обследовано 100 человек с сифилитической инфекцией: 41 пациент с серорезистентным сифилисом, 35 – с ранним скрытым сифилисом, 24 – с поздним скрытым сифилисом. Установлено, что у пациентов с серорезистентным, ранним и поздним скрытым сифилисом отмечается перераспределение состава иммунокомпетентных клеток с увеличением количества цитотоксических/эффекторов. Признаки дефицита Т-клеточного звена иммунитета определяются преимущественно у пациентов с серорезистентным сифилисом в виде уменьшения количества Т-хелперов, NK-клеток.

2. Чеботарев В.В., Чеботарева Н.В., Асхаков М.С. Сифилис: была ли предсказуема ситуация? / В.В. Чеботарев, Н.В. Чеботарева, М.С. Асхаков // Medicus. – 2015. – № 1. – С.12-14.
3. Современные представления о серологической резистентности при сифилисе (обзор литературы) / Г.М. Бондаренко [и др.] // Дерматологiя та венерологiя. – 2015. – № 4. – С.5-16.
4. Кытманова Л.Ю., Москвичева М.Г., Радзиховская М.В. Сравнительный анализ динамики эпидемического процесса при сифилисе, ВИЧ-инфекции и гепатитах В и С / Л.Ю. Кытманова, М.Г. Москвичева, М.В. Радзиховская // Южно-Уральский медицинский журнал. – 2014. – № 3. – С.7-11.
5. Современные представления об иммунных изменениях при сифилисе / В.И. Прохоренков [и др.] // Сибирское медицинское обозрение. – 2014. – № 4. – С.20-27.
6. Qin J., Yang T., Wang H., Feng T., Liu X. Potential Predictors for Serofast State after Treatment among HIV-Negative Persons with Syphilis in China: A Systematic Review and Meta-Analysis // Iran J. Public Health. 2015. Vol. 44, № 2. P. 155-169.
7. Salazar J.C., Cruz A.R., Pope C.D., Valderrama L., Trujillo R., Saravia N.G., Radolf J.D. Treponema pallidum Elicits Innate and Adaptive Cellular Immune Responses in Skin and Blood during Secondary Syphilis: A Flow-Cytometric Analysis // J. Infect Dis. 2007. Vol. 195. № 6. P. 879-887.
8. Li J., Zheng He-Yi. Characteristics of Patients with Primary and Late Latent Syphilis Patients Who Were Initially Non-Reactive to the Rapid Plasma Reagin Test // Jpn. J. Infect. Dis. 2013. Vol. 66. P. 36-40.
10. Новгородова Т.И. Особенности цитокинового профиля и функционального состояния эндотелия у больных нейросифилисом: автореф. дис. … канд. мед. наук. – Екатеринбург, 2013. – 24 с.
11. Bao T.Y., Yu N.S., Zeng K., Li L., Fang L. Cellular immunity in patients with seroresistance of syphilis // Practical Preventive Medicine(China). 2006. Vol. 13. № 2. P. 254–256.
12. Zhang C.Y. Clinical analysis of serofast patients among syphilitic patients // Lab. Med.Clin.(China). 2013. Vol. 10. № 7. P. 887– 888.
13. Charmie B.T., Godornes C., Van Voorhis W.C., Ukehart S.A., CD4+Lymphocytes and Gamma Interferon Predominate in Local Immune Responses in Early Experimental Syphilis. Infect. Immun. 2007. Vol. 75, № 6. P. 3021-3026.
14. Спиридонов В.Е., Майстренок А.М. Особенности эпидемиологической ситуации по сифилису в Витебской области / В.Е. Спиридонов, А.М. Майстренок // Достижения фундаментальной, клинической медицины и фармации:материалы 72-ой научной сессии сотрудников университета. – Витебск: Изд-во Витебского гос. мед. ун-та, 2017. – С.77-78.
Сифилис – одно из самых распространенных венерических заболеваний на планете. По данным Всемирной Организации Здравоохранения ежегодно в мире регистрируется не менее 12–15 миллионов новых случаев сифилитической инфекции [1]. В последние десятилетия отмечается структурное перераспределение клинических форм заболевания с распространением эпидемиологически неблагоприятных ранних скрытых форм сифилиса, а также поздних скрытых форм с развитием висцерального и нейросифилиса [2, 3]. Несмотря на успехи современной венерологии, у 2–20 % больных после лечения наблюдается развитие серорезистентности [2, 3, 4].
Цель исследования: анализ показателей иммунофенотипирования клеток крови и сывороточных иммуноглобулинов у пациентов с серорезистентным, ранним и поздним скрытым сифилисом.
Материал и методы исследования. В работе представлены данные, полученные при иммунологическом обследовании 100 больных сифилитической инфекцией, находившихся под наблюдением в Краевом клиническом кожно-венерологическом диспансере. В группу I вошли 35 пациентов с ранним скрытым сифилисом, в группу II – 24 пациента с поздним скрытым сифилисом, в группу III – 41 пациент с серорезистентным сифилисом. Контрольную группу составили 50 здоровых респондентов, сопоставимых по возрасту и полу.
Для обеспечения репрезентативности полученных результатов из исследования были исключены ВИЧ-инфицированные пациенты, больные сахарным диабетом, аутоиммунными, аллергическими и онкологическими заболеваниями.
Общее количество лейкоцитов, относительное и абсолютное содержание субпопуляций лимфоцитов определяли с использованием одноплатформенной технологии с помощью гетерогенного гейтирования по панлейкоцитарному маркеру CD45+ и показателям светорассеяния с применением калибровочных частиц Flow-Count Fluorоspheres фирмы Beckman Coulter, США.
Определение иммуноглобулинов A, G, M в сыворотке крови выполняли методом количественной иммунотурбодиметрии с помощью биохимического анализатора AU 680 500 фирмы Beckman Coulter, США. Для анализа использовали реактивы фирмы Beckman Coulter, США. Оценку внутриклеточного кислородзависимого метаболизма нейтрофилов крови проводили с помощью НСТ-теста в модификации А.Н. Маянского и М.Е. Виксмана (1979). Фагоцитарную активность нейтрофилов и моноцитов крови исследовали на модели поглощения частиц латекса (Фрейдлин И.С., 1986).
Для оценки межгрупповых различий применяли однофакторный дисперсионный анализ, критерии Ньюмена – Кейлса, Данна. Достоверными считали различия при p
Результаты исследования и их обсуждение. Показатели фагоцитоза и оксидазной активности нейтрофильных гранулоцитов у пациентов с сифилисом не отличались от здоровых респондентов (таблица).
Показатели иммунного статуса у пациентов с сифилисом
Показатель
Ранний скрытый сифилис (I) (n=35)
Поздний скрытый сифилис (II)
(n=24)
Серо-
резистентный сифилис (III)
(n=41)
Контрольная
группа
(IV)
(n=50)
P
У больных всех клинических групп отмечалось снижение относительного содержания лимфоцитов, что согласуется с данными, представленными в литературе.
Содержание Т-лимфоцитов и Т-хелперов при раннем и позднем скрытом сифилисе не отличалось от аналогичных показателей у здоровых доноров (таблица).
У пациентов всех групп установлено увеличение средних показателей HLADR+ Т-лимфоцитов (таблица, рис.1a, 1б).
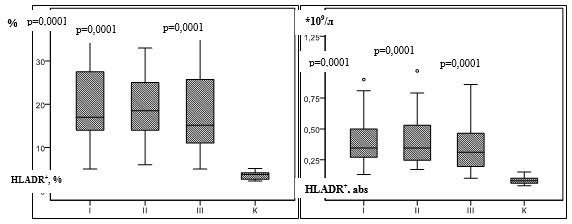
Рис. 1. Содержание HLADR + -лимфоцитов у пациентов с сифилисом
Примечание: p – достоверные отличия по сравнению с контрольной группой; К – контрольная группа, I – ранний скрытый сифилис II – поздний скрытый сифилис, III – серорезистентный сифилис (критерий Ньюмена – Кейлса, критерий Данна).
В группе с серорезистентным сифилисом определялось снижение абсолютного содержания CD3+- и CD4+-клеток по сравнению со здоровыми людьми. Установлены достоверные различия абсолютных показателей CD4+-лимфоцитов при серорезистентном сифилисе по сравнению с ранним и поздним скрытым сифилисом (таблица, рис. 2б).
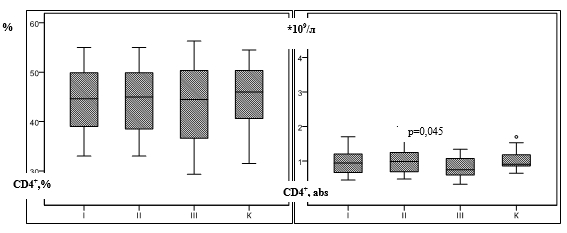
Рис. 2. Содержание CD4 + -лимфоцитов у пациентов с сифилисом
Примечание: p – достоверные отличия по сравнению с контрольной группой; К – контрольная группа, I – ранний скрытый сифилис II – поздний скрытый сифилис, III – серорезистентный сифилис (критерий Ньюмена-Кейлса, критерий Данна).
Примечание: p – достоверные отличия по сравнению с контрольной группой; К – контрольная группа, I – ранний скрытый сифилис II – поздний скрытый сифилис, III – серорезистентный сифилис (критерий Ньюмена-Кейлса, критерий Данна).
Развитие серорезистентности при сифилисе нередко связано с изменением баланса CD4 + /CD8 + -лимфоцитов [6]. Низкие показатели CD3 + - и CD4 + -лимфоцитов у пациентов с серорезистентностью подтверждаются ранее проведенными исследованиями [7, 10]. Содержание и функциональная активность Т-хелперов (CD4 + ) имеет ключевое значение в развитии реакций гиперчувствительности замедленного типа (ГЗТ) и может рассматриваться в качестве одного из факторов, способствующих формированию серорезистентности [6]. Известно, что отсутствие негативации комплекса серологических реакций с высокой частотой отмечается у ВИЧ-инфицированных и иммунокомпрометированных больных сифилисом, что сопровождается ухудшением течения заболевания и отрицательно влияет на результаты лечения [8]. Вероятно, снижение количества CD4 + -лимфоцитов у пациентов с серорезистентным сифилисом может быть связано с недостаточным синтезом IL2 и IL12 мононуклеарами периферической крови [6].
Существует мнение, что дефицит Th1 при вторичном сифилисе обусловлен высоким уровнем апоптоза периферических лимфоцитов посредством активации Fas-опосредованного пути, что затрудняет санацию организма и создает предпосылки для хронизации инфекции [7]. Кроме того, установлено снижение функциональных показателей Th1 по сравнению со здоровыми респондентами [6].
При оценке субпопуляций Т-лимфоцитов нами выявлено увеличение относительного содержания CD8 + -лимфоцитов у пациентов всех групп (таблица, рис.3а).
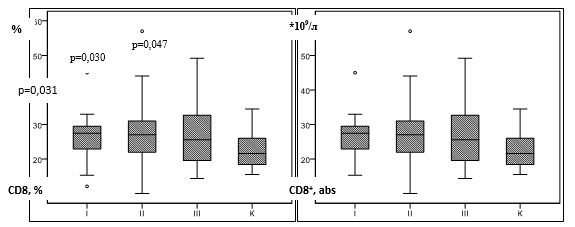
Рис. 3. Содержание CD8 + -лимфоцитов у пациентов с сифилисом
Примечание: p – достоверные отличия по сравнению с контрольной группой (критерий Ньюмена – Кейлса, критерий Данна); К – контрольная группа, I – ранний скрытый сифилис, II – поздний скрытый сифилис, III – серорезистентный сифилис.
Примечание: p – достоверные отличия по сравнению с контрольной группой (критерий Ньюмена – Кейлса, критерий Данна); К – контрольная группа, I – ранний скрытый сифилис, II – поздний скрытый сифилис, III – серорезистентный сифилис.
Роль Т-цитотоксических/эффекторов в клиренсе бледных трепонем до конца не определена. По мнению ряда авторов их увеличение может отражать динамику иммунного ответа, направленного на элиминацию внутриклеточного патогена и имеет компенсаторный характер [6, 11, 12].
В случае экспериментальной инфекции ранее было показано, что появление CD8 + - клеток в месте внедрения T. Pallidum регистрируется уже на 11–18 день после заражения, при этом их преобладание над CD4 + -клетками отмечается в период разрешения процесса между 25 и 39 днем [13]. Установлено, что сифилитические инфильтраты при твердом шанкре у пациентов с сифилисом содержат преимущественно Т-хелперы, в то время как Т-цитотоксические/эффекторы преобладают при вторичных сифилитических поражениях [13]. Вероятно, активированные CD8 + -лимфоциты могут вносить свой вклад в увеличение IFɤ, необходимого для активации макрофагов и реализации ГЗТ или лизировать эпителиальные клетки, инфицированные T. Pallidum, что подтверждается присутствием матричной РНК перфорина и гранзима [9].
Вместе с тем существует мнение, что активация CD8 + -лимфоцитов при сифилисе подавляет реакцию ГЗТ и синтез опсонизирующих антител [9], имеющих определяющее значение в клиренсе T. Pallidum.
При иммунофенотипировании клеток крови у пациентов с серорезистентным сифилисом нами выявлено статистически достоверное уменьшение количества NK-клеток (таблица).
Известно, что NK-клетки играют основную роль в иммунном ответе на внутриклеточные патогены, способствуя синтезу IFNɤ, поляризации Т-лимфоцитов и созреванию дендритных клеток. Натуральные киллеры являются основным источником IFNɤ при стимуляции мононуклеаров периферической крови липопротеинами T. Pallidum [11], что согласуется с существующими в литературе сведениями об уменьшении активности NK-клеток при развитии сифилиса [9, 12].
В исследованиях последних лет у пациентов с вторичной сифилитической инфекцией выявлено появление нетипичной популяции циркулирующих NK (CD56 - CD16 + ) с низким потенциалом секреции IFɤ и других интерлейкинов [9].
Таким образом, при иммунофенотипировании клеток крови у пациентов с серорезистентным, ранним и поздним скрытым сифилисом отмечается перераспределение состава иммунокомпетентных клеток с увеличением количества Т-цитотоксических/эффекторов. Увеличение количества активированных лимфоцитов свидетельствует об активации иммунного ответа в условиях персистенции T. Pallidum.
Признаки дефицита Т-клеточного звена иммунитета определяются преимущественно у пациентов с серорезистентным сифилисом в виде уменьшения количества Т-хелперов, NK-клеток. Полученные данные целесообразно использовать при интерпретации результатов серологических исследований у пациентов с сифилисом и для прогнозирования различных форм заболевания.
Реакции иммунной системы организма при заражении сифилисом

Сифилис - это инфекционное заболевание, вызываемое бледной трепонемой (бактерией Treponema pallidum). Организм человека, заболевшего сифилисом, защищается от возбудителя заболевания с помощью механизмов иммунитета. Проникновение, длительное сохранение в организме (персистенция) и размножение возбудителя заболевания в организме хозяина приводят к выраженным изменениям со стороны иммунной системы.
После попадания бледных трепонем в организм и при их дальнейшем размножении, в организме больного человека происходят иммунные сдвиги. Механизм иммунного ответа при сифилисе исследован не полностью, однако имеются достаточно убедительные данные о том, что в этом процессе участвуют все звенья иммунной системы.
Активируются механизмы как врожденного неспецифического иммунитета, свойственного человеку как биологическуому виду, так и адаптивного, антиген-опосредованного иммунного ответа, вызванного контактом с антигеном. В иммунном ответе организма принимают участие как клеточные (макрофаги, Т-лимфоциты), так и гуморальные механизмы (синтез специфических иммуноглобулинов — антител).
Иммунную реакцию вызывают белки, входящие в состав структур бледной трепонемы; они являются чужеродными веществами для организма человека и относятся к антигенам. Все антигены трепонемы способны стимулировать организм больного вырабатывать антитела соответствующих классов. Вследствие этого, в сыворотке крови больных сифилисом отмечается множественность антител: протеиновых, комплементсвязывающих, полисахаридных реагинов, иммобилизинов, агглютининов.
Классы вырабатываемых антител меняются на разных этапах течения сифилиса — в различных стадиях болезни преобладают то одни, то другие антитела, относящиеся к разным классам иммуноглобулинов. Сила иммунного ответа и спектр антител, выявляемых на разных стадиях развития инфекции, зависит от особенностей организма у данного человека.
Во многих случаях иммунологический ответ не предотвращает поэтапного развития инфекции. Организм хозяина неспособен уничтожить сифилитическую инфекцию, что приводит к дальнейшей эволюции патологического процесса. Болезнь, начавшись с местного процесса, распространяется на весь организм и продолжается много лет.
Клеточный и гуморальный иммунный ответ на внедрение бледной трепонемы в организм
В иммунном ответе организма на заражение принимают участие клеточные и гуморальные механизмы иммунитета.
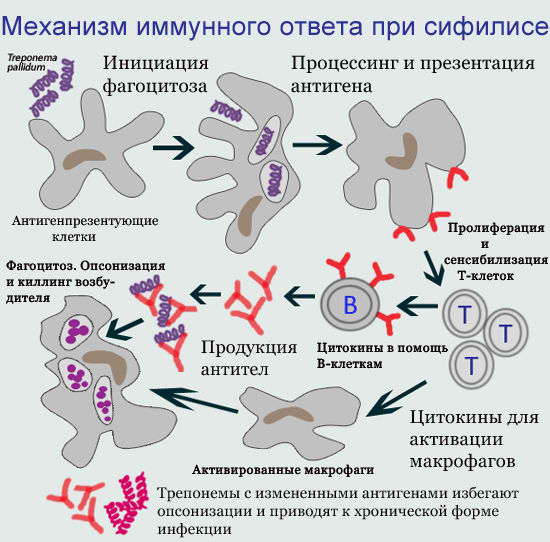
1. Клеточный иммунитет при заражении сифилисом
На клеточном уровне бледной трепонеме противодействуют высокоспециализированные клетки иммунной системы — макрофаги, T-лимфоциты, B-лимфоциты. Происходит изоляция и частичное уничтожение трепонем фагоцитами, в основном макрофагами. Фагоцитоз носит преимущественно незавершенный характер — при поглощении фагоцитом возбудитель не погибает, а остается в клетке, сохраняя свою структуру и способность к размножению. Более того, фагоцит оберегает от антител и воздействия антибиотиков бледную трепонему, которая становится недоступной для защитных сил организма.
Ранний сифилис характеризуется частичным угнетением клеточного иммунитета и развитием состояния иммуносупрессии, постепенно нарастающей активизацией гуморального иммунитета. Клеточное звено страдает в первую очередь, так как Т-лимфоциты более чувствительны к воздействию бактерий T. pallidum.
У больных вторичным, латентным и третичным сифилисом формируется клеточный иммунитет, признаки которого выявляются в реакциях in vivo (кожные пробы) и in vitro (стимуляция Т-лимфоцитов трепонемными антигенами).
2. Гуморальный иммунитет при заражении сифилисе
Гуморальный иммунный ответ заключается в продукции широкого спектра противосифилитических антител. В структуре бледной трепонемы выявлено большое количество соединений, имеющих выраженные антигенные свойства для иммунной системы человека. На начальных этапах развития сифилиса происходит более выраженный синтез антител к антигенам, имеющим высокое содержание в клетке T. pallidum и локализующимся в структуре мембран наружной клеточной стенки или протоплазматического комплекса.
3. Уклонение бледных трепонем от иммунного ответа
Клеточное и гуморальное звенья иммунитета не в состоянии обеспечить полное уничтожение и элиминацию бледных трепонем. Благодаря своему необычному молекулярному строению, T. pallidum обладает замечательной способностью уклоняться от защитной реакции макроорганизма.
Электронно-микроскопические исследования показали, что при сифилисе преобладает незавершенный фагоцитоз трепонем (захват и поглощение трепонем лейкоцитами, макрофагами и другими клетками). При этом трепонемы не погибают, а получают защиту от антибиотиков и антител, и могут даже размножаться в фагоцитирующей клетке. В течение всего инкубационного периода, а также в конце первичного и в начале вторичного периодов сифилиса, возбудители активно размножаются и распространяются по всему организму.
Гуморальный иммунный ответ. Противосифилитические антитела.
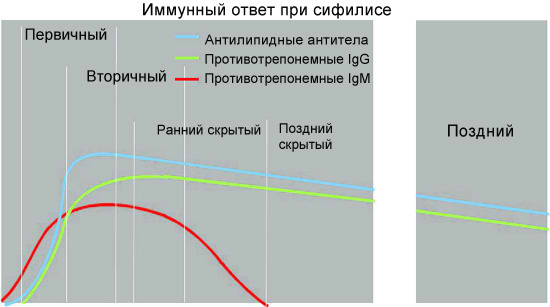
1. Неспецифические антитела при сифилисе
Реагиновые антитела у больного сифилисом — это иммуноглобулины класса IgG и IgM. Они являются комплексным ответом на высвобождение липоидных молекулярных фрагментов из поврежденных клеток хозяина, а также на появление липопротеиноподобных структур, сходных с кардиолипином, входящих в состав бактериальной клетки бледной трепонемы.
Липидные антигены cоставляют значительную часть бактериальной клетки T. pallidum. Помимо других антигенов, в клеточной стенке бледной трепонемы содержится фосфолипид кардиолипин; на его долю приходится около 30% сухого вещества клетки спирохеты. В организме человека, больного сифилисом, могут присутствовать липиды, имеющие сходное строение с липоидными структурами клеточной стенки бледной трепонемы. Это аутоантигены, образующиеся в результате разрушения органов и тканей, в основном липиды митохондриальных мембран.
Аутоантигены - это компоненты клеток и тканей собственного организма, которые распознаются при определённых условиях как частично чужеродные. Аутоантитела к кардиолипину – это антитела, направленные организмом против собственного кардиолипина.
Клетки человека, больного сифилисом выделяют в большом количестве липоидный и липопротеиноподобный материал, сходный с кардиолипином. Бледная трепонема приводит к поражению внутренних органов, в частности, к повреждению печени и сердца, освобождая некоторые фрагменты тканей. При интенсивном размножении спирохет в организме больного происходит распад тканей, в результате чего из поврежденных клеток высвобождаются липоидные молекулярные фрагменты.
Иммунная система пациента реагирует, вырабатывая реагиновые антитела на эти фрагменты. Продукты распада клеток — липоидные белки — поступают в кровяное русло. Эти белки являются чужеродными для организма человека, поэтому реакция организма проявляется в виде выработки неспецифических антител (иммуноглобулинов) класса IgM и IgG к липоидному и липопротеиноподобному материалу. Именно эти антитела исторически называются реагинами.
Следует иметь в виду, что реагины с помощью кардиолипиновых тестов могут обнаруживаться в организме людей, никогда не болевших сифилисом, т.к. их количество повышается при различных физиологических и патологических состояниях, не связанных с сифилисом, например у пациентов с аутоиммунными, воспалительными и гематологическими заболеваниями. Эти реагины могут быть причиной так называемых биологических ложноположительных серологических реакций на сифилис.
Антилипидные (неспецифические) антитела появляются в организме человека со стадии первичного сифилиса —примерно через 7-14 дней после образования твердого шанкра, через 4-5 недель после заражения.
Антитела против кардиолипина выявляют посредством нетрепонемных серологических тестов. При нетрепонемных методах анализа на сифилис не различают тип антител (IgG, IgM или др.), а определяют суммарный ответ.
2. Специфические антитела при сифилисе
Специфические антитрепонемные антитела направлены против бледной трепонемы. Плазматические клетки организма вырабатывают специфические антитела, направленные против соответствующих антигенов возбудителя заболевания.
На ранних этапах развития сифилиса, как бактериальной инфекции, у заболевшего человека осуществляется выработка специфических антител, относящихся преимущественно к иммуноглобулинам класса M (первичный иммунный ответ). Трепонемоспецифические Ig класса M у больных сифилисом могут регистрироваться даже в период инкубации. Позднее происходит переключение на синтез IgG (вторичный иммунный ответ).
Параметры иммунного ответа могут изменяться в результате проводимого лечения. Адекватное лечение раннего сифилиса приводит к быстрому снижению титров неспецифических антител и специфических IgM.
По мере развития патологического процесса постепенно включаются механизмы образования антител классов G и А. Ведущая роль в гуморальном ответе переходит к специфическим антителам IgG и IgА. При этом специфические IgG обычно сохраняются в сыворотке крови в течение длительного периода времени,а иногда и всю жизнь
Динамика образования специфических антител у больного при сифилисе
По данным современных исследований, гуморальный ответ при сифилисе происходит в соответствии с общими закономерностями для бактериальных инфекций. Вначале вырабатываются иммуноглобулины класса M против наиболее иммуногенных и специфичных антигенов возбудителя. Специфические антитела класса M способны выявляться в крови пациентов, инфицированных T. pallidum, на самых ранних этапах развития инфекции, уже через 1,5-2 недели после заражения, что клинически соответствует скрытому инкубационному периоду заболевания. При первичном и вторичном сифилисе содержание указанных антител в крови больных быстро нарастает и сохраняется на высоком уровне; максимальное их содержание у больных сифилисом приходится на 6—9-ю неделю заболевания.
После успешного лечения антибактериальными препаратами специфические IgM у больных относительно быстро элиминируют из кровотока (через 3—12 месяцев). При лечении раннего сифилиса IgM исчезают через 3-6 месяцев, позднего – через 1 год. Большое диагностическое значение приобретает выявление антитрепонемных антител IgM в крови новорожденных. Так как IgM не проходит через плаценту, выявление антитрепонемных IgM-антител у новорожденного указывает на врожденный сифилис. Точно так же IgM-антитела не проникают через гематоэнцефалический барьер, и их появление в спиномозговой жидкости говорит о нейросифилисе.
Многие лабораторные методики диагностики сифилиса основаны именно на выявлении трепонемоспецифических IgM. Например, иммуноферментный анализ (ИФА) на твердой фазе и линейный иммуноблоттинг (ИБ) на микропористых стрипах с использованием антивидовых конъюгатов на основе моноклональных антител к тяжелой мю-цепи в структуре IgМ человека, а также реакция непрямой иммунофлюоресценции (РИФ) с исследованием 19S-фракции сыворотки крови, содержащей тяжелые IgМ.
Раннее определение специфических IgM также может быть применено для своевременного выявления случаев раннего врождённого сифилиса (определение специфических IgM в крови новорожденных) или случаев реинфекции у пациентов, ранее перенесших сифилис.
Без лечения, по мере развития болезни и разрешения клинических проявлений вторичного периода, уровень специфических IgМ в крови больных сифилисом постепенно понижается и начинает преобладать синтез IgG. Развитие иммунного ответа на антигенную стимуляцию в организме больного сифилисом сопровождается постепенным переключением с синтеза антител класса M на продукцию более мелких молекул иммуноглобулинов класса G.
Специфические иммуноглобулины класса G в кровотоке больных сифилисом появляются более поздно, в конце 3-й или на 4-й неделе после заражения и, как правило, достигают более высоких титров, чем IgM. Уже на 6 неделе после инфицирования уровень IgG преобладает над уровнем IgM и может сохраняться в таком состоянии годы.
Содержание специфических IgG, постепенно увеличиваясь, достигает максимальной выраженности через 1—1,5 года, после чего несколько снижается, подвергаясь волнообразным колебаниям в зависимости от активности инфекционного процесса. Количество специфических IgG в циркулирующей крови после адекватно проведенного лечения снижается медленно. Антитела этого класса могут сохраняться даже после клинического излечения пациента в течение десятков лет или пожизненно.
Кроме перечисленных видов антител, в гуморальном иммунитете при сифилисе принимают участие иммуноглобулины класса А. Антитела IgA вырабатываются в сравнительно небольших количествах. Вопрос о синтезе IgE и IgD в настоящее время изучен недостаточно.

В статье дается подробный список причин повышения лимфоцитов в крови при инфекции, онкологии и неблагоприятных факторах. Врач-иммунолог рассказывает почему иммунная система человека реагирует на раздражители и зачем выявлять причину лимфоцитоза.
Лимфоциты — это главные клетки иммунной системы, которые отвечают за всю нашу внутреннюю защиту. Лимфоциты — это представители клеток белой крови, которые являются главными клетками иммунной системы. Их задача — стоять на нашей внутренней генетической чистоте.

В рамках консультации вы сможете озвучить свою проблему, врач уточнит ситуацию, расшифрует анализы, ответит на ваши вопросы и даст необходимые рекомендации.
Повышение лимфоцитов при инфекции
Повышение концентрации лимфоцитов называется лимфоцитоз. При этих заболеваниях мы будем видеть повышение количества лимфоцитов в крови:
- грипп. При гриппе всегда будет лимфоцитоз, независимо от того, какой он тяжести;
- в начальной стадии ВИЧ инфекции;
- инфекционный мононуклеоз – это заболевание, которое вызывается, как правило, вирусом герпеса четвёртого типа, и при нём тоже всегда будет лимфоцитоз;
- герпетическая инфекция, любого типа;
- при ветрянке, (герпес третьего типа) тоже всегда будет лимфоцитоз;
- любые вирусные гепатиты тоже будут изменять формулу крови, повышая уровень лимфоцитов;
- краснуха;
- коклюш;
- эпидемический паротит или в народе называется свинка;
- сифилис;
- туберкулёз;
Это основной перечень инфекционных заболеваний, при которых будет происходить повышение лимфоцитов в крови.
Мы сейчас с вами поговорили о лимфоцитозе, который возникает преимущественно при инфекционных заболеваниях. Но есть ряд заболеваний, которые могут вызвать лимфоцитоз и неинфекционной природы.
Лимфоцитоз при онкологии
Такое грозное заболевание, как лимфобластный лейкоз. Оно может быть острым, может быть хроническим. Естественно при этом грозном заболевании будет катастрофически в десятки, в сотни раз повышено количество лимфоцитов.
- Лимфогранулематоз – онкологическое заболевание с преимущественным поражением лимфоузлов всегда вызывает лимфоцитоз.
- Заболевание крови из серии онкологических, таких как лимфомы, всегда вызывают лимфоцитоз.
- Лимфосаркомы (опухоль из злокачественных клеток лимфоидных элементов)
- Миеломная болезнь (злокачественная опухоль)
Вот это те заболевания, при которых тоже мы можем видеть повышение количества лимфоцитов в периферической крови.
Прочие причины повышения лимфоцитов в анализе крови
Есть ещё и другие состояния, которые не связанны с онкологическими, инфекционными, паразитарными заболеваниями, но так же могут резко изменять работу иммунной системы и стимулировать её на повышение количества лимфоцитов.
- Как правило, на фоне алкоголизма идёт хроническое истощение иммунной системы, но на первом этапе — бурный рост количества лимфоцитов.
- Частое курение тоже может вызвать излишнюю выработку лимфоцитов.
- Приём некротических веществ, лекарств. Некоторые анальгетики, антибиотики – могут вызывать повышение уровня лимфоцитов.
- В женском организме состояние перед менструацией может повышать количество лимфоцитов в крови.
- Длительное голодание, диеты.
- Употребление пищи богатой углеводами. Хотя тут несколько иной механизм, чаще это связано с не прямым воздействием углеводов на концентрацию лимфоцитов, а опосредованно, через разрастание бродильной и грибковой флоры в кишечнике, и уже микробиота кишечника будет стимулировать лимфоцитарное изменение.
- Поражение щитовидной железы, в частности гипотиреоз, тоже будет постоянно стимулировать повышенную концентрацию лимфоцитов.
- Некоторые аллергические состояния могут спровоцировать лимфоцитоз.
- Отравление токсическими веществами, такими как: свинец, мышьяк, дисульфид углерода, любое нарушение иммунитета, тоже может вызывать лимфоцитоз.
- Эндокринные нарушения, в первую очередь нарушение работы щитовидной железы, нарушение работы надпочечников, нарушение работы яичников, яичек, ранние стадии некоторых онкологических заболеваний, при которых идёт активация лимфоцитарного узла.
- Неврастения, стрессы.
- Недостаток витамина В12.
- Травмы, ранения, ожоги.
- Удаление селезёнки. Бывают ситуации, когда есть необходимость удалить селезёнку – это может стимулировать повышение концентрации лимфоцитов.
- Применение некоторых вакцин. При вакцинации мы всегда подразумеваем, что будет период повышения лимфоцитов. Это нормально, потому что мы вводиться вакцина, которая является либо частичкой, либо ослабленным возбудителем инфекционных заболеваний, и иммунная система будет вести себя как с обычным возбудителем.
- Интенсивное занятие спортом. Ибо чрезмерные физические нагрузки тоже могут привести к состоянию лимфоцитоза.
- Аутоиммунные заболевания, которые тоже могут привести к повышению уровня лимфоцитов в крови. В первую очередь это болезнь крона (тяжёлое хроническое иммуноопосредованное воспалительное заболевание желудочно-кишечного тракта).
- Ревматоидные артриты.
- Красная волчанка.
Заключение специалиста
Я не случайно остановилась так подробно на тех заболеваниях и состояниях, при которых мы будем видеть повышенную концентрацию лимфоцитов в крови. Сам по себе лимфоцитоз – не диагноз, это состояние, которое может отражать тот огромный перечень диагнозов о котором мы говорили. Поэтому если вы сдав общий анализ крови с подсчётом лейкоцитарной формулы, увидели, что концентрация лимфоцитов вышла за референсное значение, в зависимости от вашего возраста, то это должно быть для вас важным сигналом, для того, чтобы обратиться к врачу и разобраться, за из-за чего ваша иммунная система бурно работает, какое у вас заболевание есть, или какое состояние испытывает организм.
Всего вам хорошего и будьте здоровы. И пусть ваши клетки иммунной системы всегда стоят на страже и пребывают в коридоре нормы.

Гематологические анализы — лабораторные тесты, которые предоставляют информацию о количественном и качественном составе крови. Они позволяют выявить многие негативные изменения в организме, сузить диагностический поиск, подобрать оптимальную схему лечения.
Виды гематологических исследований
Основным гематологическим исследованием является общий (клинический) анализ крови, результаты которого отражают общее состояние организма, обеспечивают врача информацией о характере гемопоэза (кроветворения). Анализ служит для диагностики воспалительных процессов, анемий, лейкемий и многих других патологических состояний.
Исследование назначается всем пациентам, обратившимся за специализированной медицинской помощью. Также оно проводится во время беременности, профилактических осмотров, при диспансеризации.
Биологическим материалом для исследования может служить капиллярная или венозная кровь. Клинический анализ крови состоит из множества тестов (от 8 до 30). Некоторые из них могут быть самостоятельными гематологическими исследованиями.
Подготовка к общему анализу крови
- За две недели до сдачи анализа важно отказаться от приема лекарственных средств. Если препараты жизненно необходимы, то условия коррекции лечения обсуждаются с врачом.
- За сутки до исследования нужно исключить из меню жирные и жареные продукты, отказаться от алкоголя, избегать физических и эмоциональных нагрузок.
- Накануне исследования ужин должен быть не позднее 22.00.
- Анализ сдается утром натощак. Перед исследованием нельзя курить, пить кофе, чай. Разрешается употреблять воду в объеме не более 0,5 л.

Врач терапевт Ханова Ирина Ивановна расшифрует ваши анализы в режиме онлайн звонка в приложении Zoom или WhatsApp.
- подробное пояснение врача терапевта.
- альтернативное мнение компетентного специалиста по расшифровке анализов.
- возможность задать вопросы врачу, касающиеся результатов анализов.
Основные параметры общего анализа крови, их референтные значения и возможные причины отклонения от нормы
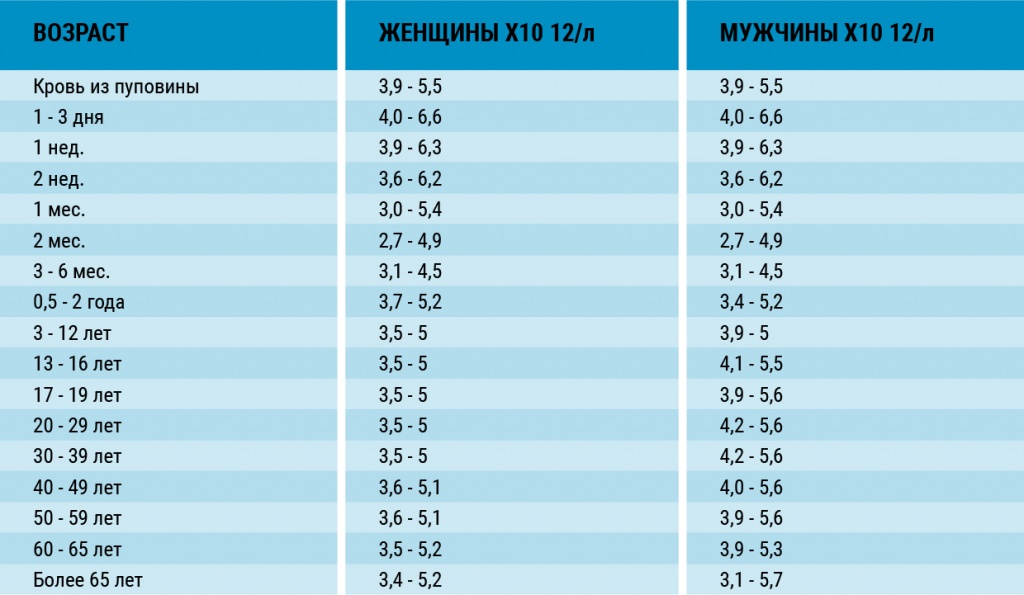
Эритроциты
Самые многочисленные форменные элементы, в состав которых входит гемоглобин. Имеют дисковидную форму, сплющенную в центре. Благодаря такой конфигурации значительно увеличивается площадь клеток, что позволяет эритроцитам успешно выполнять свою первостепенную задачу — газообмен. Помимо этого, они участвуют в защите организма от токсинов, процессах свертывания крови и регуляции водно-солевого обмена. Непрерывное пополнение запасов этих форменных элементов критически важно для здоровья, так как без них организм начинает испытывать гипоксию — нехватку кислорода. На бланке с результатами анализа эритроциты обозначаются английской аббревиатурой RBC.
Низкий уровень эритроцитов наблюдается при анемиях (железодефицитная, В12-дефицитная), при повышенном разрушении эритроцитов в случае некоторых наследственных заболеваний (микросфероцитарные, овалоцитарные анемии), гемоглобинопатиях (патологии, при которых нарушается синтез гемоглобина), гипергидратации (избыточное содержании воды в организме), беременности, кровотечениях, пищевом дефиците.
Высокий показатель может быть следствием обезвоживания организма, эритремии (онкологическое заболевание кровеносной системы), патологий почек.
С референтными значениями содержания эритроцитов в крови вы можете ознакомиться в таблице.
Гемоглобин
Белок, содержащий железо. Способен обратимо соединяться с кислородом и доставлять его к тканям. Гемоглобин входит в состав эритроцитов, поэтому его уровень напрямую зависит от количества красных кровяных телец. Причины отклонения гемоглобина от референтных значений такие же, как и у эритроцитов. На бланке с результатами исследования гемоглобин обозначаются аббревиатурой HGB.
Нормальные значения гемоглобина у детей представлены в таблице (единицы измерения — г/л).
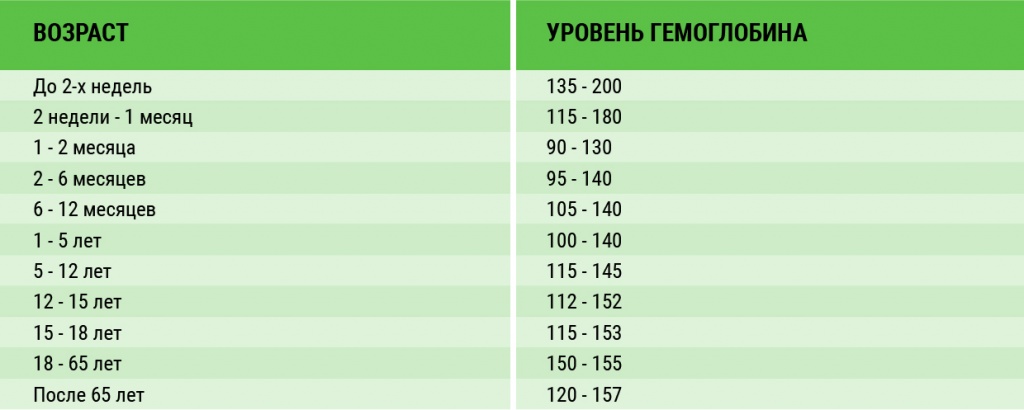
У взрослых нормы таковы:
- Мужчины — 130-160 г /л.
- Женщины — 120-140 г /л.
Цветовой показатель, эритроцитарные индексы
Цветовой показатель (ЦП) показывает относительную концентрацию гемоглобина в одном эритроците. Используется для выявления анемий и прочих патологий, связанных с нарушениями функционирования костного мозга. Как правило, в качестве нормы принимается диапазон 0,80-1,05 единицы.
ЦП определяется в рамках клинического анализа крови, проводимого без участия гематологических анализаторов. В настоящее время, когда практически все лаборатории оснащены современным оборудованием, ЦП постепенно теряет практическое значение. Вместо него определяются эритроцитарные индексы, которые обозначаются английскими аббревиатурами:
- MCV — средний объем эритроцитов. Высокие значения данного индекса — признак В12-дефицитной и фолиеводефицитной анемий, гипотиреоза, патологий печени. Низкие значения наблюдаются при железодефицитной анемии, сахарном диабете, патологиях почек, гемоглобинопатиях — наследственных заболеваниях крови, обусловленных нарушением структуры гемоглобина.
- RDW — распределение эритроцитов по величине. Отклонение этого параметра от нормы указывает на наличие эритроцитов в крови разных размеров. Высокое значение RDW мы можем наблюдать при некоторых анемиях, после переливания крови.
- MCH — среднее количество гемоглобина в эритроците. Норма MCH у взрослых находится в пределах 27-34 пикограмм. Высокие значения наблюдаются при В12-дефицитной анемии, анемии аутоиммунного характера, патологиях печени, гипотиреозе, алкогольной зависимости. Низкий показатель — признак железодефицитной анемии, анемии воспалительного ответа. У детей показатели нестабильны и могут меняться в большую или меньшую сторону за считанные дни, часы.
- MCHC — средняя концентрация гемоглобина в эритроците. Высокие значения наблюдаются при нехватке железа, анемии воспалительного ответа, гемоглобинопатиях.
Лейкоциты и лейкоцитарная формула
Количество лейкоцитов (аббревиатура — WBC) служит индикатором многих патологических процессов. Высокий уровень лейкоцитов чаще указывает на заболевания крови (лейкозы), вирусные и бактериальные инфекции, воспалительные процессы, интоксикации, аллергические реакции. Низкое содержание лейкоцитов наблюдается при ослабленном иммунитете, анемии, приеме антибактериальных, нестероидных противовоспалительных средств, при химио- и лучевой терапии.

Врач терапевт Ханова Ирина Ивановна расшифрует ваши анализы в режиме онлайн звонка в приложении Zoom или WhatsApp.
- подробное пояснение врача терапевта.
- альтернативное мнение компетентного специалиста по расшифровке анализов.
- возможность задать вопросы врачу, касающиеся результатов анализов.
Первостепенная функция лейкоцитов — иммунная. Однако они не смогли бы полноценно ее выполнять, если бы внутри своей группы не были бы разделены на несколько видов, у каждого из которых есть своя, особая задача.
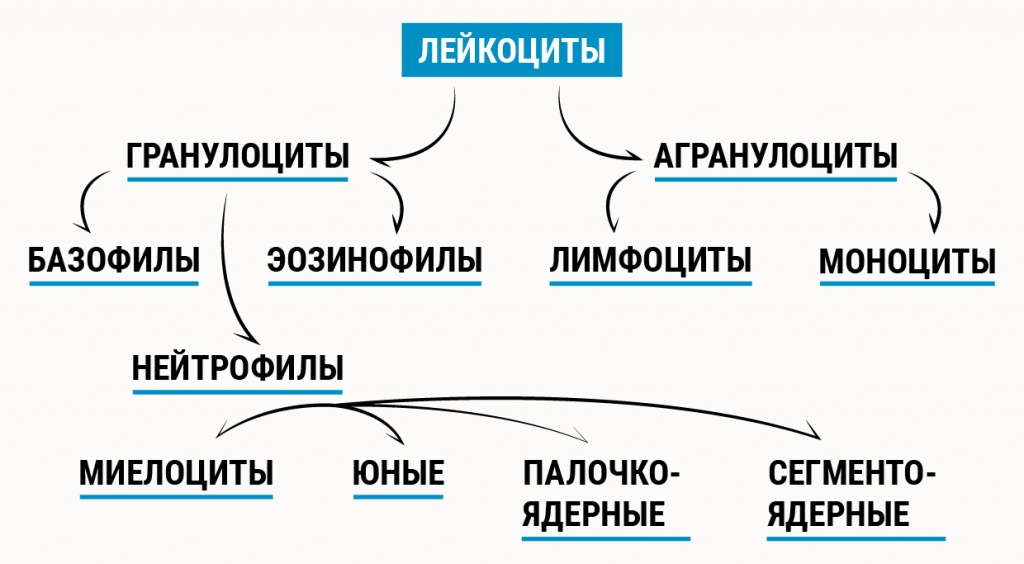
Подсчет всех видов лейкоцитов называется лейкоцитарной формулой. Количество клеток каждого вида может быть приведено в процентах (относительное количество) или в единицах измерения (абсолютное количество). Данные лейкоцитарной формулы необходимы для дифференциальной диагностики некоторых заболеваний, определения стадии болезни, оценки эффективности лечения, прогноза исхода патологического процесса.
С референтными значениями нормального содержания лейкоцитов в крови и параметров лейкоцитарной формулы вы можете ознакомиться в таблице.
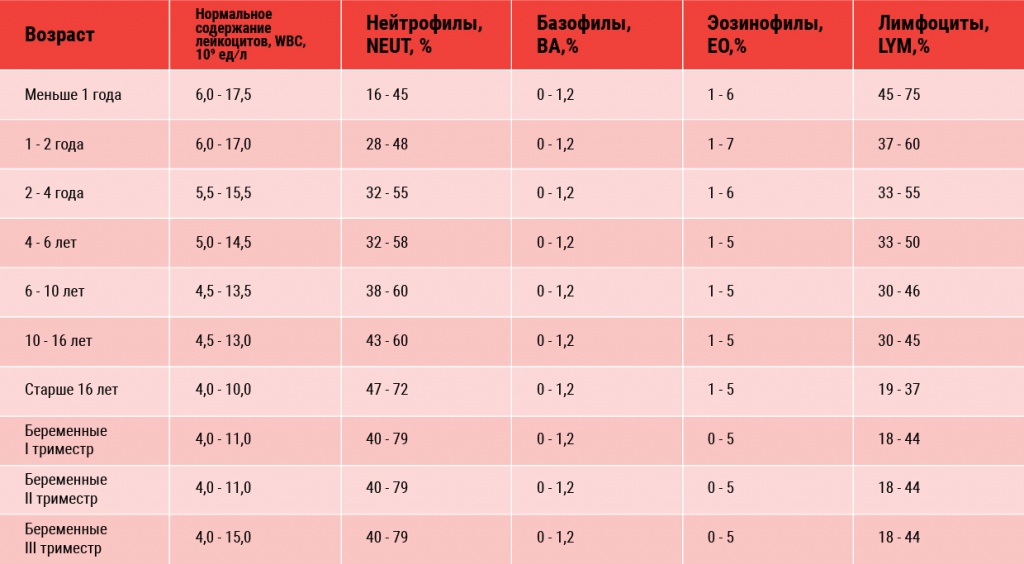
Рассмотрим основные причины отклонения параметров лейкоцитарной формулы от референтных значений:
- нейтрофилы. Обладают бактерицидной и дезинтоксикационной функциями. В норме у взрослых преобладают именно эти клетки среди всех лейкоцитов. Подразделяются на 6 видов, в периферической крови больше всего содержится сегментоядерных нейтрофилов. Высокое содержание нейтрофилов наблюдается при большинстве бактериальных инфекций, воспалениях, некротических процессах, эндотоксикозе, интенсивных физических нагрузках, стрессах. Низкий уровень — при некоторых бактериальных и вирусных заболеваниях (брюшной тиф, туберкулез, вирус гриппа, кори). Кроме этого уровень нейтрофилов снижается при терапии антибактериальными, антигистаминными препаратами;
- базофилы. Это вид лейкоцитов, которые присутствуют в крови здоровых людей в исключительно малых количествах. Основная роль базофилов — поддержание аллергической реакции, запускаемой тучными клетками. Их количество повышается при аллергических состояниях (в том числе на лекарственные средства), онкологии, некоторых инфекционных болезнях (грипп, ветряная оспа), отравлениях тяжелыми металлами;
- эозинофилы. Основные функции этих клеток — борьба с паразитами и контроль аллергических реакций. Количество эозинофилов повышается в крови при аллергических состояниях (особенно при болезнях дыхательных путей — бронхиальная астма, аллергический ринит), кожных патологиях (атопический дерматит), паразитарных инвазиях, острых инфекциях, злокачественных процессах, ревматоидном артрите, дерматомиозите, при приеме лекарственных средств (глюкокортикоиды, антигистаминные препараты). Низкий уровень эозинофилов наблюдается при начальной стадии воспалений, гнойных инфекциях, интоксикации тяжелыми металлами;
- лимфоциты. Лимфоциты относят к группе иммунокомпетентных клеток, т.е. это клетки, которые непосредственно обеспечивают выполнение функций иммунной системы. Одна из основных функций этих клеток — распознавание различных антигенов. Количество лимфоцитов повышено при большинстве вирусных инфекций, болезнях системы крови, отравлении сероуглеродом, мышьяком. Низкое значениелимфоцитов — признак ослабленного иммунитета, почечной недостаточности, некоторых системных воспалительных заболеваний;
- моноциты — крупные клетки, способные распознавать, захватывать и уничтожать бактерии, грибы. Рост количества моноцитов наблюдается при острых и вялотекущих воспалительных процессах, аутоиммунных патологиях, в период восстановления после инфекций. Низкое содержание моноцитов в крови — признак гнойных инфекций, апластической анемии, гемобластозов.
Тромбоциты
Тромбоциты (аббревиатура — PLT) представляют собой безъядерные кровяные тельца, образующиеся в костном мозге. Выполняют важные для организма функции:
- создают тромбоцитарную пробку при травме кровеносного сосуда, которая закрывает место повреждения;
- ускоряют ключевые реакции плазменного свертывания;
- вырабатывают в поврежденные ткани специфические пептиды, которые активизируют процессы регенерации.
Тромбоцитопения (низкое содержание тромбоцитов) бывает при некоторых аутоиммунных заболеваниях (идиопатическая тромбоцитопеническая пурпура, системная красная волчанка, аутоиммунный тиреоидит и др.), наблюдается при гепатитах, циррозе печени, гипотиреозе, некоторых видах лейкозов, лимфомах, мегалобластной и апластической анемиях, алкогольной интоксикации, химио- и лучевой терапии.
Нормальные значения содержания тромбоцитов в крови представлены в таблице.

Гематокрит
Данный показатель определяет процентную долю содержания все форменных элементов (преимущественно эритроцитов) от общего объема биологической жидкости.На бланке с результатами общего анализа крови обозначается аббревиатурой HTC.
Высокое значение HTC наблюдается при обезвоживании, симптомах интоксикации (рвоте, диарее), сердечной и дыхательной недостаточности, перитоните, поликистозе почек. Низкое значение — признак анемий, избыточного содержания воды в организме.
Референтные значения гематокрита представлены в таблице.
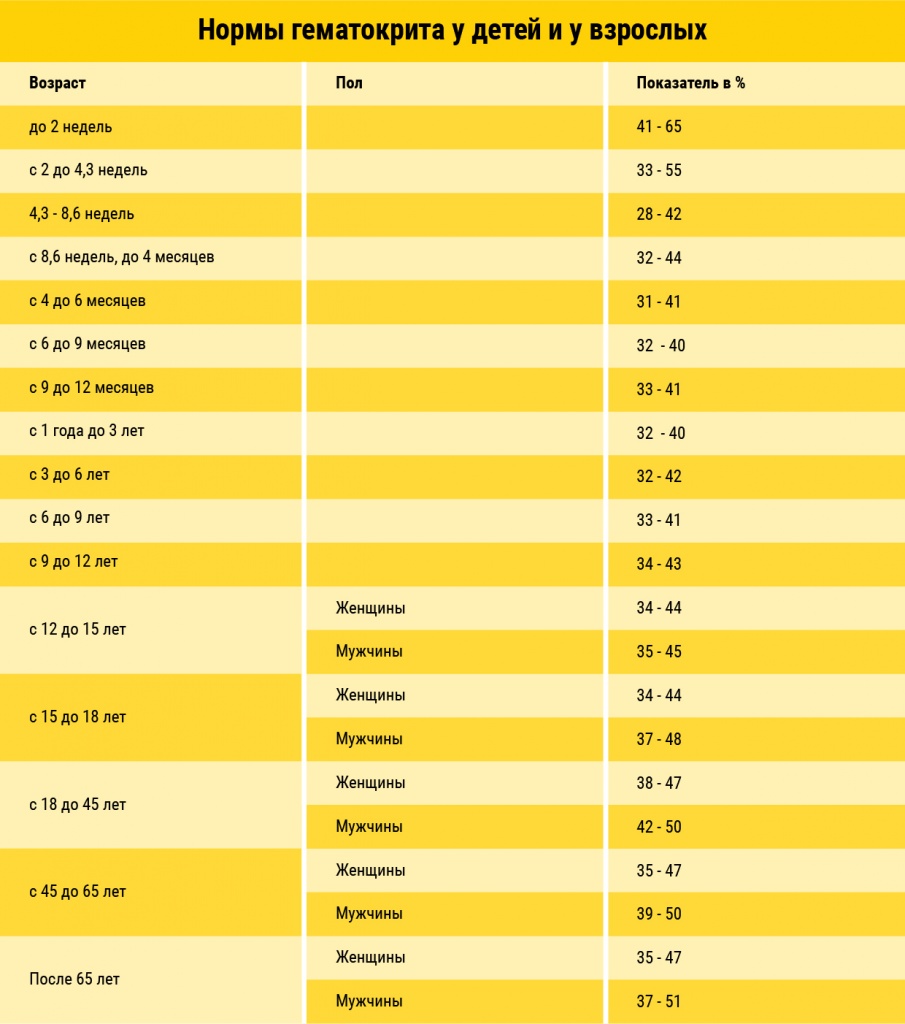
Количество ретикулоцитов
Ретикулоциты (аббревиатура — RET) — молодые, незрелые формы эритроцитов, которые формируются в красном костном мозге. Время жизни ретикулоцитов 3-5 дней, половину этого времени они живут в костном мозге, а половину — в периферической крови. Их трансформация в эритроциты регулируется эритропоэтином (одним из гормонов почек). Показатель RET отражает активность эритропоэза — физиологического процесса формирования и дифференцировки красных кровяных клеток.
Определение RET необходимо в следующих ситуациях:
- если требуется оценка состояния процессов кроветворения;
- при обследовании пациентов, перенесших пересадку костного мозга, химиотерапию;
- для оценки эффективности терапии железосодержащими препаратами, фолиевой кислотой, витамином В12, эритропоэтином.
Повышенное значение RET наблюдается при:
- гемолитических анемиях (талассемия, микросфероцитарная анемия и др.). Ретикулоциты могут достигать 60 % и выше, сильно увеличиваясь при гемолитических кризах;
- острой кровопотере. Показатель может превышать норму в 3-6 раз (на 3-5 день после кровопотери наблюдается ретикулоцитарный криз);
- полицитемии — доброкачественном опухолевом процессе, поражающем систему крови;
- метастазах опухолей в костный мозг;
- гипоксии — низком уровне кислорода в организме;
- малярии — остром инфекционном заболевании, при котором происходит повышенный гемолиз эритроцитов;
- наличии в организме гемолитических ядов — веществ, разрушающих эритроциты. К подобным веществам относятся мышьяк, соединения свинца, нитриты, яды насекомых, змей.
Пониженные значения RET могут указывать на следующие нарушения:
Читайте также:

