Комплексное лечение эндогенной интоксикации
Обновлено: 24.04.2024
Эндотоксины представляют собой естественные продукты, которые образуются в результате жизнедеятельности организма. В норме одни обезвреживаются при помощи различных реакций и выводятся из организма естественным путем. Кроме того, эндотоксины могут вырабатывать некоторые грамположительные и грамотрицательные бактерий. При нарушении естественных защитных механизмов, либо при возникновении определенных заболеваний, уровень эндотоксинов повышается, что неблагоприятно сказывается на работе всего организма. Современное оборудование и методики позволяют произвести удаление вредных продуктов и устранить, тем самым, негативные последствия.
Классификация эндотоксинов
Привести к развитию синдрома эндогенной интоксикации могут несколько групп веществ. К ним относятся:
- Бактериальные эндотоксины.
- Продукты нормального обмена веществ в высокой концентрации.
- Активированные ферменты, которые способны повреждать ткани.
- Медиаторы воспаления.
- Продукты перекисного окисления.
- Среднемолекулярные вещества различной природы.
- Ингредиенты нежизнеспособных тканей.
Таким образом, выделяют ряд состояний, при которых возможно поражение организма эндотоксинами. К ним относятся: все виды шока, ожоговая болезнь, тиреотоксикоз, перитонит и др.
Симптомы синдрома эндогенной интоксикации
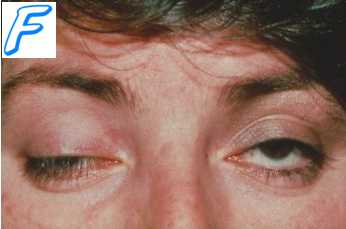
Одним из главных проявлений эндогенной интоксикации является угнетение сознания разной степени выраженности. Вместе с этим, могут наблюдаться и другие симптомы:
- Слабость.
- Головная боль.
- Миалгия.
- Сухость слизистых.
- Тошнота и рвота.
- Тахикардия.
- Гипо- или гипертермия.
- Тахи- или брадипоноэ.
Помимо этого, при повышенной концентрации токсических веществ появляются нарушения микроциркуляции, изменяются реологические свойства крови, снижается сосудистый тонус. Действие данных факторов может привести к развитию кардиодепрессии, респираторного дистресс-синдрома, гипоксии тканей и, как следствие, органной (сердечной, почечной) или полиорганной недостаточности.
Диагностика синдрома эндогенной интоксикации
Помимо анализа клинической картины, для диагностики данного синдрома врач обязательно назначает лабораторное обследование. К признакам эндогенной интоксикации относятся:
- Лейкоцитоз.
- Повышенные значения лейкоцитарного и ядерного индексов интоксикации (выше 1,5 и 0,3 соответственно).
- Пониженное содержание в крови общего белка.
- Высокий уровень билирубина, мочевины, креатинина сыворотки.
- Энзиомпатия (повышение АЛАТ, АСАТ, ЛДГ, кислой фосфатазы).
- Увеличение концентрации среднемолекулярных пептидов.
- Значение коэффициента нейтрофилы/лимфоциты выше 2.
В зависимости от величины данных показателей, выделяют 3 степени эндогенной интоксикации. Состояние пациента, которое соответствует третьей степени, является крайне тяжелым и имеет неблагоприятный прогноз.

Способы удаления эндотоксинов
Лечение происходит с применением методов, которые способствуют максимальному удалению токсических веществ из организма. Выделяются следующие механизмы детоксикации:
- Трансформация в печени. Осуществляется с помощью оксигенации крови, гемоперфузии через ксеноорганы и клеточные взвеси, фотомодификации крови.
- Сорбционный метод, в рамках которого используют множество методик: плазмо- и гемосорбция, лимфосорбция и др. Перспективной является современная технология селективной сорбции эндотоксина на картриджах для экстракорпоральной гемоперфузии.
- Элиминация эндотоксинов. Производится при проведении плазмафереза, форсированного диуреза, гемофильтрации, гемодиализа, обменного переливания крови и др.
Лечение эндогенной интоксикации. Интенсивная терапия эндогеннной интоксикации.
Существенным моментом интенсивной терапии у больных, находящихся в реактивно-токсической стадии эндогенной интоксикации, является предупреждение развития стадии токсемии. Для этого выполняется управляемая гемодилюция.
На фоне проведения управляемой гемодилюции происходит улучшение реологии крови, нормализуется соотношение вязкость/гемато-крит, в результате роста ударного объема увеличивается минутный объем кровообращения. Одновременно с этим гемодилюция улучшает газообмен путем увеличения диффузии кислорода в результате снижения капиллярного сопротивления, повышает устойчивость сурфактанта и предупреждает агрегацию форменных элементов крови в микрососудах легких. Кроме того, снижение концентрации продуктов нарушенного метаболизма, вазоакпшных веществ, ферментов в крови способствует увеличению порога пропускания токсинов почками, увеличивает диурез, способствует более быстрому удалению шлаков из организма.
Для выполнения управляемой гемодилюции используются следующие комбинации растворов:
1. 10% раствор альбумина (3 мл/кг), гемодез (6-8 мл/кг), раствор Рингера.
2. Раствор протеина (5-6 мл/кг), гемодез (6-8 мл/кг), раствор Рингера.
3. Желатаноль (6-8 мл/кг), реополиглюкин (6-8 мл/кг), раствор Рингера.

При острой хирургической патологии, когда снижено онкотическое и повышено осмотическое давление, гемодилюцию необходимо начинать с введения растворов, удерживающих жидкость в сосудистом русле (альбумин, протеин, желатаноль), а затем использовать низкомолекулярные растворы (реополиглюкин, гемодез) и кристаллоиды.
Гемодилюция выполняется под контролем ЦВД, артериального давления, темпа диуреза, уровней гематокрита (0,3-0,035) и гемоглобина (не ниже 95 г/л). Скорость инфузии составляет 15-25 мл в минуту, общий объем растворов - 25-40 мл/кг массы тела.
При выполнении гемодилюции одновременно вводят препараты, улучшающие микроциркуляцию за счет уменьшения общего периферического сопротивления (гепарин, курантил, трентат). С целью профилактики избыточного накопления эндогенных биологически активных веществ следует проводить защиту симпато-адреналовой системы от стрессорного воздействия операционных факторов, которая достигается путем введения альфа-адреноблокаторов (дроперидол 0,15 мг/кг массы .тела или аминазин 0,3-0,5 мг/кг массы тела).
Благодаря управляемой гемодилюции уровень гематокрита поддерживают около 0,30, что создает оптимальные условия для доставки к тканям кислорода.
В стадии выраженной токсемии особое место занимает кратковременная подготовка больного к операции, включающая в себя обязательную коррекцию водно-электролитного баланса и восстановление внутрисосудистого объема жидкости. Известно, что в условиях токсикоза депонирование крови на периферии и фильтрация ее через блокированную капиллярную сеть являются защитной мерой организма, направленной на снижение поступления токсических метаболитов в центральный кровоток, поэтому попытки улучшить периферическую микроциркуляцию не всегда дают желаемый клинический эффект, так-как приводят к поступлению в кровь дополнительного объема эндотоксинов. В связи с этим в предоперационном периоде при проведении инфузионной терапии следует использовать средства, обладающие способностью связывать эндотоксин (альбумин, гемодез).
Достаточно часто встречающимся патологическим состоянием, сопровождающим деструктивные процессы в брюшной полости, является парез кишечника. Для борьбы с парезом в послеоперационном периоде нередко используют эпидуральную блокаду местными анестетиками. В условиях гиповолемии и тяжелой интоксикации эта процедура, с одной стороны часто приводит к значительному снижению артериального давления, с другой - к интенсификации кровотока в кишечной стенке, способствует улучшению лимфатического дренажа и, кроме того, развитию феномена реперфузии, что ведет к значительному возрастанию поступления эндотоксина в кровь. Поэтому в борьбе с парезом кишечника при использовании эпидуральной анестезии следует увеличить темп инфузионной терапии, дополняя ее введением реополиглюкина и гемодеза.
При выборе метода анестезиологического пособия предпочтение следует отдавать многокомпонентному эндотрахеальному наркозу с миорелаксантами и ИВЛ. Для вводного наркоза при стабильных показателях гемодинамики следует использовать барбитураты, а при неустойчивом артериальном давлении - кетамин в сочетании с диазепамом. На этапе основного наркоза целесообразно использовать НЛА в сочетании с оксибутиратом натрия или газонаркотргческой смесью закиси азота с кислородом в соотношении 1:1, причем FiO2 должно быть не менее 0,4.
В стадии мультиорганной дисфункции оперативное вмешательство ограничивается дренированием, некрэктомией и носит паллиативный характер. В этой стадии требуется особо тщательное анестезиологическое обеспечение с использованием детоксикационной и метаболической терапии, направленной на коррекцию функциональных расстройств сердечно-сосудистой, дыхательной и выделительной систем.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Синдром эндогенной интоксикации. Клиника синдрома эндогенной интоксикации.
В настоящее время одной из наиболее сложных проблем интенсивной терапии является синдром эндогенной интоксикации (СЭИ), сопровождающий значительное количество патологических состояний (шок, перитонит, панкреатит и др.), которые по мере своего развития могут приводить к летальному исходу.
Прогрессирование эндотоксикоза обусловлено накоплением в крови различных по происхождению, химической структуре и биологическому воздействию веществ, именуемых эндотоксинами. Эндотоксины способствуют развитию острой почечно-печеночной недостаточности, сердечно-сосудистой недостаточности, острого респираторного дистресс-синдрома, приводя в конечном итоге к появлению крайне тяжелого состояния - синдрома мультиорганной дисфункции.
Эндогенная интоксикация - клинический синдром, возникающий при различных по этиологии патологических состояниях, обусловленных накоплением в тканях и биологических жидкостях организма продуктов нарушенного обмена веществ, метаболитов, деструктивных клеточных и тканевых структур, разрушенных белковых молекул, pi сопровождающийся функциональными и морфологическими поражениями органов и систем организма.
Выделяют три основных звена, которые определяют тяжесть состояния больных и выраженность клинической симптоматики: токсемия, нарушение микроциркуляции, угнетение функций собственных детоксицирующих и защитных систем организма.
Основным звеном патогенеза синдрома эндогенной интоксикации является токсемия. К сожалению, четкая дифференциация токсических веществ эндогенного происхождения практически невозможна. Однако в каждом конкретном случае можно выделить "первичные" и "вторичные" эндотоксины. Так, при ожогах, синдроме длительного раздавливания, облитерирующих сосудистых заболеваниях "первичными" являются продукты белковой деградации, "вторичными" - продукты естественного метаболизма, накопление которых в организме является следствием угнетения функций естественной детоксикации и экскреции.
Эндотоксемия, нарушая тонус периферических сосудов, реологию крови, кинетические и механические свойства форменных элементов крови, приводит к тканевой гипоксии, которая является одним из важных звеньев патогенеза СЭИ, течение которого усугубляется снижением функции органов естественной детоксикации и экскреции. Токсины блокируют места связывания молекул альбумина, что ведет к снижению эффективности проводимого медикаментозного лечения, поскольку этот белок является транспортным агентом для многих фармакологических препаратов.
Клиника синдрома эндогенной интоксикации.
Сопоставление экспериментальных и клинических исследований позволило выявить следующие стадии развития синдрома эндогенной интоксикации.
I стадия синдрома эндогенной интоксикации. Реактивно-токсическая возникает в ответ на формирование первичного деструктивного очага или травматического повреждения. Лабораторными признаками этой стадии являются повышение в крови уровней молекул средней массы (МСМ), продуктов перекисного окисления липидов (ДК и МДА), возрастание ЛИИ.
II стадия синдрома эндогенной интоксикации - стадия выраженной токсемии развивается после прорыва гастогематического барьера, когда в циркулирующую кровь попадают эндотоксины, образовавшиеся в первичном очаге интоксикации, с последующим распространением и накоплением в организме. В зависимости от состояния организма, его резистентности и исходного уровня детоксицирующих и иммунных систем выделяют компенсированную и декомпенсированную стадии выраженной токсемии.
III стадия синдрома эндогенной интоксикации - мультиорганной дисфункции (СМОД) наблюдается при дальнейшем прогрессировашш патологического процесса как следствие тяжелого повреждения эндотоксинами различных органов и систем с развитием их функциональной декомпенсацш!. Клинически эта стадия Проявляется нарушением сознания, гипоксией, выраженной сердечной Недостаточностью, олигурией, паралитической непроходимостью кишечника. В крови определяется высокая концентрация креатинина, мочевины, билирубина.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Хирургическое лечение эндогенной интоксикации при перитоните. Консервативное лечение эндогенной интоксикации при перитоните.
Хирургическое лечение. При активном вмешательстве на ранних стадиях ЭИ достаточно ликвидировать причину, чтобы прервать дальнейшее развитие эндотоксикоза. При запущенных формах продукты промежуточного обмена накапливаются в сосудистом русле и паренхиматозных органах, вызывая полиорганную недостаточность, поэтому хирургическое устранение очага воспаления и его санация способствуют ликвидации лишь отдельных компонентов ЭИ.
Консервативное лечение больных с ЭИ должно строиться с учетом степени эндотоксикоза (В. К. Гостищев и соавт., 1994). К общим методам воздействия на ЭИ относятся инфузионная терапия, различные способы экстракорпоральной детоксикации (см. выше), гипербарическая оксигенация.
Больному необходимо обеспечить полноценное парентеральное питание. Суточный каллораж должен быть не менее 3000 ккал/ сутки, 2/3 этой потребности рекомендуется обеспечивать за счет концентрированных растворов глюкозы, а 1/3 — за счет жировых эмульсий (20% раствор интралипида, липофундина).
Общий объем вводимой жидкости в период острой интоксикации — 4—5 л/сутки. Из этого количества 2,5—3 литра должно приходиться на кристаллоидные растворы, остальное — коллоиды и белковые препараты крови (плазма, альбумин, протеин). Выбор инфузионно-трансфузионных сред, их комбинация определяются характером волемических нарушений, дефицитом белкового и электролитного состава крови. Коррекцию водно-электролитного состава осуществляют с помощью солевых растворов типа Рингер-Локка. Коррекцию диспротеинемий проводят с помощью белковых гидролизатов, плазмы и протеинов.
Простым и широко используемым методом лечения эндогенной интоксикаци является форсированный диурез, основанный на использовании естественного процесса удаления токсических веществ из организма. Предварительно проводят умеренную гемодилюцию, для чего используют растворы кристаллоидов, низкомолекулярных декстранов, а при гиповолемии — белковые кровезаменители. Один из вариантов водной нагрузки: в/в вводится 1000 мл физиологического раствора, 200 мл 4% раствора бикарбоната натрия и 400 мл реополиг-люкина, затем маннитол из расчета 1 — 1,5 г/кг или 40—80 мг лазик-са; мосле этого продолжают вливание 5% раствора глюкозы, белковых препаратов (плазма крови, раствор альбумина, белковый гид-ролизат) в объеме 1000—1500 мл. Кроме того, в состав трансфузи-онных сред включают растворы хлорида калия (40—60 мл 10% раствора или 100—120 мл 4% раствора дробно), хлорида натрия (50 мл 10% раствора), хлорида кальция (30 мл 10% раствора) для коррекции неизбежной при проведении методики форсированного диуреза потери электролитов. Лечение осуществляется под контролем за почасовым диурезом и ЦВД, электролитным и белковым балансом организма, КЩС, остаточным азотом.

Антибактериальная терапия проводится препаратами широкого спектра действия в сочетании трех препаратов разных групп. При этом учитывается вид микроорганизма и его чувствительность к препарату.
В качестве иммунокоррегируюшей терапии используют иммуномодуляторы: Тактивин (синоним: Т-активин) по 1 мл 0,01% раствора п/к (ежедневно, курс 10—12 инъекций), тималин, взрослым по 5—20 мг ежедневно (30—100 мг на курс), левамизол (обычно 50 мг 3 раза в день в течение 4—5 дней, через 7 дней курс повторяют; или по 150 мг 1 раз/день, курс 5—7 дней), диуцифон по 0,1 г 3—4 раза в день или вводят в/м по 4 мл 5% р-ра (0,2 г) 1 раз в сутки.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Самоотравление организма или синдром постоянной интоксикации, известный в медицинской практике как эндотоксикоз долгое время не выделялся в отдельную группу заболеваний. Причина: проявляется эндотоксикоз на фоне других патологий, как условие, усугубляющее состояние человека и мешающее лечению.

Лечение эндотоксикоза без привязки к болезни-провокатору невозможно, что тоже затрудняет выделение его в самостоятельный отдел болезней. Тем не менее не рассматривать отравление организма эндогенными факторами, как патологию, требующую лечения, тоже нельзя.
Суть эндотоксикоза заключается в том, что на фоне общего ослабленного состояния у больного:
- резко снижается активность естественного механизма вывода продуктов метаболизма (эндотоксины);
- нарушается саморегуляция (равновесие реакций);
- начинается накопление эндогенных токсинов с повышенной биоактивностью.
Симптоматика при токсикозе и методы оценки эндогенных факторов
Эндотоксикоз чаще развивается у больных диабетом, людей с наследственными патологиями сосудистой структуры, замедленной работой лимфатической системы. В зависимости от сопутствующего заболевания, на фоне отсутствующего лечения которого наблюдается эндотоксикоз, проявляться отравление может через:
- сильную непреходящую тошноту (долговременную рвоту);
- повышенную температуру, дрожи в конечностях, слабость;
- очень часто эндотоксикоз сопровождается высокой потливостью;
- боли в животе, печени, спине, горле, голове – все это при определенном фоне может быть симптомами эндотоксикоза.
Исследование эндотоксинов

Диагностика эндогенного отравления построена на анализе содержания крови и плазмы.
Наиболее информативными для лечения эндотоксикоза сегодня являются:
- анализ на уровень лейкоцитов (плазма, лимфа, кровь);
- парамецийный тест (определяется период жизни парамеций в потенциально отравленной среде лимфы);
- в качестве маркера активности токсинов (для лечения эндотоксикоза) анализируют пул средних молекул (их концентрация в плазме).
Последний метод диагностики относится к инструментальным и проводится с помощью скринингового оборудования или спектрофотометра. Обязательным при исследовании условий развития эндотоксикоза и возможностей его лечения является лабораторно инструментальный анализ органа-мишени.
Процедурная, инструментальная, медикаментозная терапия
Лечение эндотоксикоза проводится на трех уровнях.
Для устранения фактора, который снижает эффективность лечения основного заболевания, применяются методы токсикодинамической коррекции (купирование симптомов отравления).
К последним (способы эфферентного лечения эндотоксикоза) относят три наиболее широко применяемые процедуры. Во-первых, это диализ или очистка крови на молекулярном уровне. В передовых клиниках его часто заменяют комбинированным лечением на основе гомеосорбции и плазмафереза.
- Гомеосорбция – пропускание отравленной крови через фильтр.
- Плазмаферез – центрифугирование крови с разделением ее на красные тельца и плазму. Поскольку токсины оседают в последней, лечение плазмаферезом заключается в удалении зараженной плазмы с возвратом красных телец в тело пациента с последующим восстановлением жидкостного баланса.
Применение антидотного лечения в практике снижения симптоматики эндотоксикоза сегодня считается слабоэффективным. Хотя в ряде случаев антидот может ускорить эффективность прочих методов лечения.
Читайте также:

