Кровепаразитарные инфекции у собак
Обновлено: 19.04.2024
Кровепаразитарные болезни - это заболевания, которые вызываются паразитами, обитающими в крови организма-хозяина. К таким паразитам относятся разнородные по систематическому положению организмы царства животных и прокариот.
Выделяют несколько групп кровепаразитов, в зависимости от места где они паразитируют:
1. Кровепаразиты живущие и размножающиеся внутри клеток крови - эритроцитов. Эти паразиты относятся к классу простейших и вызывают такие заболевания как пироплазмоз, гемобартонеллез и др.. Также сюда входят паразиты из класса риккетсий - возбудителей анаплазмоза.
2. Кровепаразиты паразитирующие на поверхности эритроцитов - это микоплазмоподобные микроорганизмы, которые могут вызывать следующие заболевания: тейлериоз, эперитрозооноз, малярия, трипаносомоз и др.
3. Кровепаразиты относящиеся к гельминтам, а конкретнее к классу трематод и нематод. Вызывают например такое заболевание, как дирофилляриоз.
Большинство кровепаразитарных болезней передаются с помощью переносчиков - насекомых, клещей, пиявок, в организме которых они проходят определенные стадии развития. Все они имеют схожие клинические признаки, обусловленные нахождением паразитов в крови. Это анемия, угнетенное состояние, слабость, повышенная температура, при некоторых появление крови в моче, гемолиз и др.
Для профилактики этих заболеваний у животных необходимо проводить регулярные обработки средствами против кровососущих насекомых и клещей, которые чаще всего и являются источниками заражения.

Постоянно пополняемая, энциклопедия животных поможет вам узнать много нового о мире вокруг вас и взглянуть на него другими глазами.

Когда вы берете домой щенка или котенка важно точно знать, как и чем их кормить. То, что нужно домашнему животному во многом зависит от возраста любимца, его породы и размера, поэтому, как правило, большинству владельцев требуется некоторое руководство по кормлению. Кошки и собаки быстро развиваются, и обеспечение их правильными питательными.

Причина парагриппа носит вирусный характер (одноцепочечный РНК-вирус семейства парамиксовирусов) и может передаваться другим собакам воздушно-капельным.
Микроскопия мазка крови является одним из методов диагностики векторных (трансмиссивных заболеваний), зачастую на приеме в клинике. Наиболее распространенные из них: анаплазмоз, эрлихиоз, бабезиоз, гепатозооноз, цитозооноз кошек, дирофиляриоз, гематропные микоплазмозы. Реже чума собак, токсоплазмоз, лейшманиоз.
Возможные находки при окраске мазка – вирусные и бактериальные включения, тельца Жолли, и др.
Анаплазмозы ‒ это трансмиссивные заболевания, которые вызываются Anaplasma phagocytophilum и Anaplasma platys ‒ грамотрицательными внутриклеточными паразитическими протобактериями, принадлежащими семейству Anaplasmataceae.
Основными переносчиками A. phagocytophilum являются клещи комплекса Ixodes ricinus-persulcatus. В Европе основным переносчиком являются клещи Ixodes ricinus, а в России и Азии ‒ Ixodes persulcatus и Dermacentor silvarum.
A. phagocytophilum передается между разными стадиями клеща (от личинки нимфе и далее имаго), но не трансовариально (от имаго ‒ яйцам). Заражение собак и кошек происходит при питании на них инфицированных нимф или имаго клещей, которые, в свою очередь, заражаются при питании на диких животных-резервуарах. Инфицирование возможно, если клещ находится на животном в прикрепленном состоянии в течение 36-48 часов. После попадания A.phagocytophilum в кровяное русло микроорганизм прикрепляется к поверхности нейтрофилов, а затем проникает в клетки путем эндоцитоза. A. phagocytophilum вызывает нарушение функции нейтрофилов, что определяет возможность выживания микроорганизма внутри данных клеток. A. phagocytophilum может поражать клетки костного мозга и мегакариоциты, однако их роль в патогенезе инфекции остается неясной.
Эрлихиозы ‒ это группа трансмиссивных заболеваний, которые вызываются внутриклеточными, грамотрицательными бактериями Ehrlichia canis, Ehrlichia ewingii и Ehrlichia chaffeensis и переносятся клещами. Бактерии образуют морулы в фагосомах циркулирующих лейкоцитов. Ehrlichia canis поражает моноциты и вызывает моноцитарный эрлихиоз собак (МЭС), который является одной из наиболее значимых инфекций домашних собак по всему миру. Ehrlichia ewingii поражает гранулоциты и вызывает гранулоцитарный эрлихиоз собак. Ehrlichia chaffeensis поражает мононуклеарные лейкоциты, вызывая моноцитарный эрлихиоз человека; собаки являются резервуарными хозяевами. Географическое распространение того или иного патогена обычно ограничено ареалом переносчиков и резервуарных хозяев.
Тяжесть клинических симптомов при эрлихиозе зависит от таких факторов, как размер инокулума, функционального состояния иммунной системы хозяина, вида и штамма микроорганизма и наличия сопутствующих инфекций. Клиническая картина может осложняться тем, что у разных микроорганизмов могут быть одни и те же переносчики, поэтому часто встречаются коинфекции такими патогенами, как Babesia spp. и Bartonella spp.
E. canis переносится преимущественно коричневым собачьим клещом (Rhipicephalussanguineus), инфекция встречается у собак в Азии, Африке, Америке, Европе. Существует несколько штаммов E. canis, которые отличаются вирулентностью. Личинки клещей заражаются при питании на инфицированных собаках. Возможна трансстадиальная передача инфекции E. canis (от личинки нимфе и имаго).
Очевидной возрастной или половой предрасположенности к МЭС у собак не наблюдается, однако данные, что немецкие овчарки более восприимчивы к заболеванию. Прогноз на исход заболевания у собак этой породы обычно менее благоприятный. У собак смешанных пород заболевание встречается реже. Была описана спонтанная инфекция E. canis у кошек в Северной и Южной Америке, однако клинический эрлихиоз у данного вида встречается редко.
Микроорганизм размножается в мононуклеарных фагоцитах путем бинарного деления; при разрушении инфицированных клеток происходит заражение здоровых клеток.
Микроорганизмы Ehrlichia и Anaplasma можно непосредственно наблюдать при окрашивании по Романовскому мазков периферической крови. Они выглядят как базофильные короткие палочки или плейоморфные коккобациллы размером от 0,2 до 1,0 мкм, обнаруживаемые поодиночке или в скоплениях внутри ограниченных мембраной клетки-хозяина цитоплазматических вакуолях, так называемых морулах. Различные микроорганизмы инфицируют преимущественно различные клетки крови, в том числе нейтрофилы и эозинофилы, лимфоциты и моноциты, а также тромбоциты (A.platys). Количество свободно циркулирующих микроорганизмов часто ниже предела выявления с помощью световой микроскопии. Вероятность выявления возбудителей возрастает при исследовании мазков лейкоцитарной пленки.
Бабезиоз (пироплазмоз) – это широко распространенное трансмиссивное заболевание, вызываемое кровепаразитами рода Babesia, переносчиками которого являются клещи. В зависимости от географического месторасположения, переносчиками бабезиоза могут быть Rhipicephalus sanguineus, Dermatocentor reticulatus, Haemaphysalis eliptica. Передача Babesia spp. происходит при укусе клеща-переносчика. Возможна прямая передача малой бабезии Babesia gibsoni при укусах с глубоким повреждением кожи (у бойцовых собак). На сегодняшний день классификация бабезиоза собак включает деление на большую и малую формы. B. сanis является наиболее распространенной большой бабезией и имеет три отдельных подтипа: B. сanis vogeli (распространена в Африке, Азии, Европе, Америке), B. canis canis (в Европе), B. canis rossi (в Африке). К малым бабезиям собак относят: B. gibsoni (встречается в Африке, Азии, Австралии, Европе, Америке), B. conradae (в Калифорнии), B. microti-like (в Северно-Западной Испании).
Бабезиоз кошек не изучался столь подробно, как бабезиоз собак. У кошек были обнаружены несколько видов малых бабезий, включая Babesia felis, B. cati и B. leo. Инфекция обычно встречается у животных в возрасте до трех лет, породной или половой предрасположенности не наблюдается. Виды больших бабезий также могут вызывать болезни у кошек.
Патогенность бабезий определяется, главным образом, видом и штаммом микроорганизма. В патогенезе заболевания играют роль возраст инвазированного животного и характер иммунного ответа. Цикл развития бабезий протекает в эритроцитах собак или кошек. После деления дочерние формы бабезий выходят из эритроцитов, разрушая их, и проникают в еще не зараженные красные клетки крови. Цикл размножения повторяется. Две основные формы Babesia, большие и мелкие формы, могут быть идентифицированы микроскопически.
Паразиты могут выглядеть в мазке крови как светло-голубые микроорганизмы парной каплевидной формы внутри эритроцита, имеющие темно-фиолетовое ядро (Babesia canis) или как тонкие кольца с эксцентрично расположенным фиолетовым ядром (в виде кольца-перстня), например B.gibsoni.
Нутталлиоз лошадей (nuttalliosis) - это пироплазмидоз, характеризующийся повышением температуры, угнетенностью общего состояния, анемией, желтушностью слизистых оболочек, нарушением сердечно-сосудистой и пищеварительной систем. Нутталлиоз лошадей имеет более широкое распространение на юге страны, вызывается кровопаразитом Nuttallia equi из сем. Piroplasmatidae.
H. canis способен вызывать воспалительные скелетные поражения: поражения надкостницы и периостит. Кроме того, высокая пораженность животных проявляется лихорадкой, летаргией, анемией и истощением. Часто может протекать бессимптомно. Особенно тяжело протекает такая форма при коинфицировании эрлихиями, бабезиями и другими возбудителями трансмиссивных инфекций. Как правило, при заражении.
С использованием микроскопических методов гематоциты Hepatozoon довольно часто диагностируются в нейтрофилах.
В условиях клиники диагностика может быть осуществлена путем обнаружения гамонтов в крови (окрашенный мазок). Однако, чувствительность такого метода крайне низка. Повысить чувствительность исследования можно путем получения концентрата белых клеток крови с помощью седиментации в гематокритном капилляре с последующей окраской выделенного слоя лейкоцитов.
Цитозооноз – трансмиссивное инфекционное заболевание с широким диапазоном географического распространения. Возбудитель - гемопротозойный паразит Cytauxzoon felis, который передается векторным путем ( иксодовые клещи Dermacentor variabilis и Amblyomma americanum, Amblyomma cajennense и др. ) . Относится к отряду Piroplasmida, семейству Theileriidae.
Хотя C. felis является видом, наиболее распространенным среди домашних кошек в США, это только один из нескольких видов из рода Cytauxzoon.
Заражение C. felis или близкородственными простейшими , встречается у широкого круга диких видов кошачьих. Предполагаемый резервуар-хозяин, который обитает в Соединенных Штатах рысь (Lynx rufus rufus), а также крупные и дикие крупные кошки.
Больные и здоровые кошки могут жить вместе без передачи возбудителя при отсутствии вектора. Паразит может присутствовать в организме в двух формах – неэритроцитарной (стадия шизонта) и эритроцитарной (пироплазмы).
Заболевание наблюдается у кошек разного возраста и пола. Породной предрасположенности нет.
В жизненном цикле C. felis половая фаза размножения происходит в кишечнике клеща . Оокинеты выходят из кишечника, попадают в полости организма и мигрируют в слюнные железы, где они размножаются как инфекционные спорозоиты. После того, как они попадают в организм хозяина во время проглатывания клеща , они проникают и развиваются, прежде всего, внутри фагоцитов. Они сначала визуализируются как нечеткие везикулярные структуры в цитоплазме инфицированных клеток и позже, как большие, отчетливые, ядерные шизонты, которые активно подвергаются делению по шизогонии и бинарному делению. Созревшие шизонты отпочковываются (мерозоиты) и в конечном счете, заполняют всю клетку хозяина. Фагоциты заполняют просветы сосудов практически в каждом органе , вплоть до образования тромбов.
Клетка-хозяин, разрушаясь , высвобождает мерозоиты в кровь или тканевую жидкость. Мерозоиты появляются в макрофагах, а через 1-3 дня после этого они наблюдаются в эритроцитах. Затем они внедряются в незараженные эритроциты и вызывают паразитемию поздней стадии, которую можно обнаружить при микроскопии мазков крови , обычно от 1 до 3 дней до клинической болезни.
В мазке крови Cytauxzoon felis похож на Babesia gibsoni, мелкие одиночные включения в виде кольца (перстня) с небольшим темным ядром внутри эритроцита.
Dirofilaria immitis и Dirofilaria repens – паразитические нематоды, принадлежащие надсемейству Filarioidea. Окончательными хозяевами паразитов являются собаки, в редких случаях – кошки. Кроме собак, заражению повержены лисы, волки, койоты, дикие кошки, хорьки, ондатры, носухи, морские львы, а также люди. Промежуточными хозяевами являются комары родов Aedes, Anopheles и Culex.
После инокуляции 2-3 месяца личинки находятся в подкожной клетчатке и мышцах, за это время они два раза линяют.
Dirofilaria repens вызывает кожную форму дирофиляриоза. Взрослые черви, достигающие длины 15 см, локализуются в подкожной клетчатке. Жизненный цикл сходен с таковым D. immitis. Продолжительность препатентного периода составляет 6-8 месяцев. Инвазия обычно протекает в субклинической форме, в некоторых случаях может развиваться дерматит, сопровождающийся локальной алопецией, зудом, эритемой и образованием корочек.
У лошадей возможно обнаружить в мазке крови микрофилярий круглых гельминтов Setaria equina семейства Filariidac подотряда Filariata, которые вызывают заболевание сетариоз лошадей. Половозрелые сетарии паразитируют в брюшной и грудной полостях, печени, перикарде и других органах, личинки — в крови. Преимагинальные стадии развития могут проникать в переднюю камеру глаза. Сетарии — биогельминты. Промежуточными хозяевами являются кровососущие комары родов Aedes и Culex. Известно, что личинки паразита циркулируют в крови лошадей и мулов. Максимальное их количество в периферической крови наблюдается вечером, когда происходит активизация комаров и нападение их на животных для кровососания. В организме насекомых личинки развиваются в грудных мышцах, а потом мигрируют к хоботку. За 12 — 16 суток они становятся инвазионными. Заражение непарнокопытных животных происходит во время нападения на них для кровососания инвазированных промежуточных хозяев. Паразиты достигают половой зрелости в организме лошадей в течение 8 — 10 мес.
При микроскопии окрашенного мазка микрофилярии трудно идентифицировать до вида или рода.
Гемотропные микоплазмозы - гемоплазмы – это мелкие (0,3-0,8 мкм) некультивируемые микроорганизмы, которые локализуются на поверхности эритроцитов и вызывают гемолитическую анемию различной степени тяжести у инфицированных животных. Гемоплазмы поражают широкий круг млекопитающих, включая человека, распространены повсеместно.
Минимум три вида гемоплазм вызывают инфекции у домашних и диких кошек: Mycoplasma haemofelis, Candidatus Mycoplasma haemominutum и Candidatus Mycoplasma turicensis. M. haemofelis (ранее называемая штаммом из Огайо, или крупной формой Haemobartonella felis) является наиболее патогенным организмом, вызывающим гемолитическую анемию от умеренной до выраженной у иммунокомпетентных кошек. Данное заболевание называется инфекционной анемией кошек. При цитологическом исследовании мазков крови M. haemofelis имеют форму кокков, иногда образующих цепи по три-шесть микроорганизмов.
Ca. M. haemominutum (ранее называемая калифорнийским штаммом, или малой формой H. felis) обычно меньше, чем M. haemofelis. Связи между инфицированием данным организмом и заболеванием у иммунокомпетентных кошек установлено не было. При цитологическом исследовании мазков крови Ca. M. haemominutum обнаруживаются как кокки малого размера, от 0,3 до 0,6 мкм в диаметре. Однако достоверно отличить M. haemofelis от Ca. M. haemominutum с помощью данного метода невозможно. Ca. M. haemominutum встречается у кошек по всему миру, инфекции наблюдаются у 20% кошек, поступающих на прием в ветеринарные госпитали. Инфекция Ca. M. haemominutum у кошек вызывает незначительное снижение гематокрита. У кошек с коинфекцией FeLV и Ca. M. haemominutum отмечается более выраженная анемия, чем при моноинфекции Ca. M. haemominutum, а прогрессирование миелопролиферативного заболевания, вызванного FeLV, происходит быстрее.
Несколько видов гемоплазм могут поражать собак. У собак, которым была проведена спленэктомия, и в редких случаях при наличии иммуносупрессивных патологий или коинфекций, наблюдается гемолитическая анемия при инфекции Mycoplasma haemocanis (ранее называемой Haemobartonella canis). M. haemocanis представляет собой микроорганизм округлой формы, зачастую формирующий длинные цепи. Распространенность данной инфекции особенно высока у собак, выращенных в питомниках, у которых часто отмечается субклиническая форма болезни.
У собак было обнаружено еще три вида гемоплазм. Candidatus Mycoplasma haematoparvum представляет собой микроорганизм небольшого размера (0,3 мкм) округлой формы, имеющий морфологическое и генетическое сходство с C.. Mycoplasma haemominutum.
Пути передачи инфекции гемоплазм остаются неясными.Очевидно, блохи и другие членистоногие могут играть роль в передаче инфекции гемоплазм у кошек, однако данные экспериментальных исследований по данному вопросу недостаточно убедительны.
M. haemofelis и C. M. haemominutum - оба эти гемопаразита прикрепляются к поверхности эритроцита, при этом C. M. haemominutum является меньшим из двух микроорганизмов, и обычно выглядит в форме темного стержня на поверхности эритроцита.
M. haemofelis большего размера и может образовывать отчетливые тела в виде кольца , которые можно увидеть на эритроцитах в мазке крови. Часто, только один из этих простейших обнаруживают в мазке крови. Некоторые кошки могут быть заражены обоими видами.
Чума плотоядных- острая контагиозная вирусная болезнь домашних собак и диких животных (многих видов отряда хищных), имеющая большое ветеринарное значение. Заболевание вызывается вирусом чумы плотоядных (Canine Distemper Virus, CDV), который является оболочечным, плеоморфным РНК-содержащим вирусом, принадлежащим роду Morbillivirus (семейство Paramyxoviridae). CDV родственен вирусу кори и вирусу чумы крупного рогатого скота и использовался в качестве модели при изучении патогенеза кори. Вирусная оболочка состоит из трех белков: гемагглютинина (Н), белка слияния (F) и матриксного белка (М). Именно Н-белок играет определяющую роль в присоединении вируса к клеткам и проникновении в них. Инфекция у собак может протекать в форме тяжелого заболевания, поражающего различные системы организма ‒ пищеварительную, респираторную и нервную.
Хорьки восприимчивы к заболеванию, в то время как у кошек оно не встречается. Вирус, выделяемый дикими животными (например, енотами), может поражать домашних собак, а вирус, выделяемый домашними собаками, представляет значительную опасность для диких животных, вызывая вспышки заболевания с высоким уровнем смертности. Вирус чумы плотоядных также является одним из патогенов, вызывающих комплекс респираторных инфекций собак (КРИС).
На ранних стадиях заболевания цитоплазматические тельца-включения, содержащие вирус, можно обнаружить в небольшом количестве циркулирующих лимфоцитов и в единичных моноцитах, нейтрофилах и эритроцитах. Включения крупные (до 3 мкм), округлой или овальной формы, различные по цвету – от синевато-серого до пурпурного. Выявление клеток с включениями более вероятно, при исследовании препаратов лейкоцитарной пленки.
Сроки исполнения: 1 день ( плюс 1-2 дня для регионов).
Исследуемый аналит: цельная кровь.
Метод исследования: микроскопия мазка.
Подготовка пациента, показания и противопоказания: Специальной подготовки животного не требуется.
- Лихорадка;
- анемия (обычно регенеративная);
- тромбоцитопения;
- гиперглобулинемия;
- спленомегалия;
- желтуха и пигментурия;
- скрининг при выборе донора крови или при подборе животных для разведения;
- лимфаденопатия.
Противопоказания: не известны.
Метод отбора биоматериала: венепункция периферической вены.
Преаналитика: взятие крови — пробирка с розовой крышкой (с ЭДТА)0,5 мл; для крупных собак можно использовать пробирку с сиреневой крышкой (с ЭДТА) 2 мл. Заполнить пробирку кровью СТРОГО до отметки на этикетке. Осторожно перевернуть пробирку 7-10 раз для перемешивания крови с антикоагулянтом.
Стабильность пробы: 3 дня при +2°С…+8° С.
Интерпретация результата: в норме кровепаразиты не обнаруживают. Отсутствие кровепаразитов в мазке крови не исключает наличия инфекции.
Результаты исследования содержат информацию исключительно для врачей. Диагноз ставится на основании комплексной диагностики , в т.ч. ПЦР, ИФА или ELISA .
Кровепаразитарные болезни собак и кошек - это болезни, вызванные микроорганизмами, которые попадают в кровеносное русло животного и паразитируют чаще всего в эритроцитах, а также в лейкоцитах. Большинство кровепаразитарных заболеваний передается через укусы инфицированных клещей и насекомых, а при некоторых заболеваниях через укусы во время драки между животными.
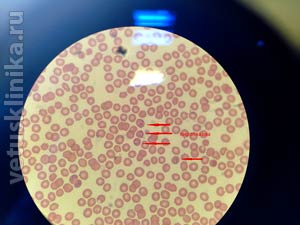
Кровепаразиты делятся на несколько групп:
- Паразитирующие внутри эритроцитов (бабезиоз, гемобартонеллез).
- Паразитирующие на поверхности клеток крови (трипаносомоз, малярия).
- Паразитирующие в клетках белой крови и тромбоцитах (анаплазмоз,эрлихиоз).
Общие симптомы для кровепаразитарных болезней следующие:
- потеря аппетита, вялость
- анемичность слизистых оболочек или желтушность
- повышение температуры тела
- гематурию (кровь в моче)
Одними из распространенных заболеваний у собак являются пироплазмоз и гемобартонеллез. Кошки же чаще заражаются гемобартонеллезом.
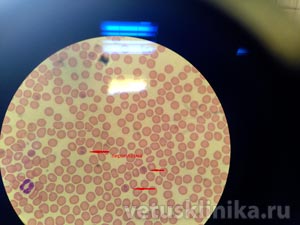
Пироплазмоз собак - сезонное заболевание, вызываемое простейшими кровепаразитами Babesia canis (Piroplasma canis). Заражение пироплазмозом происходит при укусе иксодового клеща. К заболеванию восприимчивы собаки всех возрастов и пород. Тяжелее всего переносят заболевания молодые щенки до 4-х месяцев и пожилые животные. Частые осложнения после переболевания пироплазмозом у особей старше семи лет - анемия, почечная и печеночная недостаточность. После попадания в организм животного пироплазмы начинают размножаться в эритроцитах, разрушая их, и вызывают вышеперечисленные симптомы. Для постановки диагноза "пироплазмоз" используют лабораторные методы исследования, самый эффективный – окрашивание мазка периферической крови. Забор крови производится из вены на лапе, или на стекло берется капля крови из уха. После окраски пироплазмы видны под микроскопом. Без лечения летальность у заболевших пироплазмозом составляет 98%, поэтому, если вы заметили клеща на животном, или было проявление одного из вышеперечисленных симптомов – необходимо как можно быстрее обратиться к специалистам для назначения специфического терапевтического лечения.
Гемобартонеллез собак - болезнь, вызываемая гемотрофической микоплазмой Haemocanis. Микоплазмы заражают собак при укусах клещей и мух, питавшихся кровью зараженных животных. Также заражение происходит при драках, сопровождающихся ранениями, и реже - при переливании крови, когда кровь инфицированного животного переливается здоровому. У собак заболевание чаще всего протекает бессимптомно или проявляется тяжелой анемией. Если у собаки была удалена селезенка, то гемобартонеллез протекает тяжело со всеми перечисленными выше симптомами. Для определения микоплазмы в крови животного используют световую микроскопию, исследуют мазок крови, а также полимеразную цепную реакцию (ПЦР-диагностика), так как микоплазма достаточно мала.
У кошек из кровепаразитарных заболеваний в нашем регионе в основном встречается гемобартонеллез .Кошки больше воспримчевы к гемобартонеллезу, чем собаки, и болезнь протекает с ярко выраженными симптомами. У кошек данное заболевание вызывает микоплазма Haemofelis. Заболеванию подвержены кошки всех возрастов, но молодые животные заболевают чаще. Кошки заражаются через укусы кровососущих насекомых, и чаще всего это блохи, а также во время драк с инфицированными животными через глубокие царапины и укусы. После внедрения микоплазмы в кровеносное русло кошки, они активно размножаются на эритроцитах и клетках ретикулоэндотелиальной системы: печени, селезенки, лимфоузлов, костного мозга. Вызывают разрушение эритроцитов, что приводит к анемии, лихорадке, слабости, потере массы тела и желтушности слизистых. Диагностику гемобартонеллеза у кошек так же проводят, окрашивая мазок крови по Рамановскому-Гимзе и проводят ПЦР диагностику.
Для профилактики от кровепаразитарных заболеваний используют инсекто-акарицидные средства для предотвращения укусов насекомых - переносчиков клещей, блох и других кровососущих.
Гемобартонеллез – довольно распространенное кровепаразитарное заболевание кошек, вызываемое Haemobartonella felis. Его нельзя отнести полностью ни к микоплазмам, ни к риккетсиям, так как он занимает промежуточное положение между ними, по последним данным его больше относят к микоплазмам.
Паразит проникает в цитоплазматическую мембрану эритроцита, повреждает ее сокращая его жизнь. В дальнейшем такой поврежденный эритроцит лизируется в клетках селезенки и печени. Локализация гемобартонеллез происходит и на поверхности тромбоцитов, лейкоцитов, а также в плазме. Размножение паразита происходит в органах ретикулоэндотелиальной системы - печени, селезенки, лимфатических узлах и костном мозге. Организм, вырабатывая антитела и аутоантитела на собственные эритроциты может формировать и их аутоиммунный ответ против и незараженных эритроцитов. Таким образом, происходит иммуноопосредованный внутрисосудистый гемолиз с последующим разрушением эритроцитов системой комплемента.
В результате, когда гибель эритроцитов преобладает над работой системы гепомоэза, развивается анемия, в результате недостаточного питания и кислородоснабжения функции органов нарушаются, происходит дистрофия клеток паренхиматозных органов, нарушается обмен веществ и кислотно-основное равновесие, развивается ацидоз. Особенно тяжело заболевание протекает у животных со сниженным иммунным статусом или у животных прошедших спленэктомию. Так в последнем случае, гемобартонеллез может встречаться у собак, а среди кошек он чаще встречается при наличии вирусного лейкоза или иммунодефицита. Гемобартонеллез может длительно протекать латентно, активация гемопаразита происходит, как правило, при наличии при этом при наличии системных патологий, влияющих на гемопоэз и иммунную систему, такие как хронические болезни почек, системные воспалительные реакции, вирусные инфекции и т.д. Кроме того, гемопаразит активизируется при стрессе, оперативных вмешательствах, родах, лактации и даже вакцинации. Гемобартонеллез часто выявляется и у клинически здоровых животных, причем степень анемии и паразитемии не коррелируют друг с другом.
Данный кровепаразит не может существовать вне организма, поэтому заражение может происходить только при контакте с зараженным животным, в том числе при укусе во время драки или посредством укуса блох или клещей и даже комаров. Соответственно пик заболеваемости приходится на осенне-летний период. Конечно, заражение происходит и при переливании донорской крови у непроверенного животного, в возможно также заражение при оперативных вмешательствах при использовании плохо промытых хирургических инструментов. Может быть передача гемобартонелл от матери к котятам, но на какой именно стадии (трансплацентарно, при родах или лактации) не известно. В целом, животные носители, т.е. не имеющие клинической симптоматики способны заражать других кошек, по крайне мере, в течение не менее 6 месяцев.
При выявлении анемии необходимо исключать все причины, приводящие к ней. Например, отравления крысиным ядом, антисептиками (как метиленовым синим), гликозидами (Сапонинами), Фенотиазном, нафталином, тяжелыми металлами (например, свинцом). К анемии может приводить и окислительное повреждение эритроцитов, как например, при приеме Парацетамола или регулярном потреблении лука или капусты. Анемия может развиваться и при нарушении метаболизма (например, порфинурия у кошек и жировой липидоз печени), а также при наличии гельминтоза и других кишечных паразитов и при иммуно-опосредованной анемии.
Инкубационный период может длиться от 8 до 17 и даже 20 дней. Более предрасположены к данному заболеванию молодые коты, особенно, в возрасте от одного до трех лет, к которых заболевание протекает в острой и довольно тяжелой форме. В целом, можно выделить следующие стадии развития данного заболевания: инкубационный, острая стадия, стадия выздоровления и носительства.
После выздоровления они, однако, часто остаются носителями. У кошек же чаще хроническая форма, протекающая менее выраженно и в течение длительного времени, так стадия бессимптомного носительства может быть несколько лет или даже в течение всей жизни. Ее обострение может произойти при любым условиях, снижающих резистентность организма, как например, инфекционное или онкологическое заболевание, хирургическое вмешательство, неполноценное питание и содержание, стресс и т.п. Заболевание может иметь бессимптомную форму. Однако, при этой форме паразит активизируется в период беременности, что приводит к абортам. Собаки также могут заражаться данным паразитом, однако, он не вызывает у них клинической симптоматики заболевания. Клинические проявления гемобартонеллеза встречаются не столь часто, по статистике только у 25% носителей. Их проявление будет зависеть от множества факторов, в т. ч. от патогенности штамма возбудителя и состояния иммунной системы животного.
Так как заболевание вызывает анемию, то у животного будут наблюдаться соответствующие симптомы: бледность внешних слизистых оболочек, вялость, апатия, малоподвижность, сонливость, тахикардия, тахипноэ, снижение аппетита, парарексия, истощение, увеличение внешних лимфатических узлов, хрипота голоса, гипотрихоз, воспаление, алопеции, шелушение, в виду сухости кожи, вплоть до дерматитов и диатезных геморрагий. При уже тяжелой форме течения и развития полиорганной недостаточности повышенный распад эритроцитов ведет к накоплению гемоглобина в печени, что вызывает ее воспаление, что дает соответствующий симптом - иктеричность кожи и внешних слизистых оболочек и микроглобинурию. Иногда при остром течение возможна и лихорадка, что говорит о сильнейшей интоксикации, вследствие острой формы, подсоединения вторичной инфекции или развития воспаления, например, при орхите. При острой форме симптомы более выраженные и тяжелые, при хронической, напротив, малозаметные, медленно прогрессирующие во времени.
Для постановки диагноза необходимы специфические тесты. Гемобартонеллу иногда можно выявить и в ходе световой микроскопии, посредством окрашивания мазка периферической крови по Романовскому-Гимзе или с помощью акридин оранжевого или Грюнвальд-Гимза или Райта и Райта-Гимза. При этом данный гемопаразит можно обнаружить не только на поверхности мембран эритроцитов, но также лейкоцитов, тромбоцитов и даже в плазме крови. Однако, этот последний метод не всегда надежен, в виду быстрого оседания раствора и краткости жизни паразита. Так только где-то у 25% зараженных животных будет выявлен данный паразит. Кроме того, гемобартонелла не на всех стадиях своего развития присутствует в эритроцитах, поэтому данную диагностику необходимо повторять заново через несколько дней. Кроме того, к примеру, в первый день заболевания данный паразит чаще не может быть обнаружен в крови. В целом, есть много факторов, в виду которых данный метод диагностики может давать как ложноположительные (например, в случае возникновения артефакта при неправильной сушке или фиксации мазка, а также гемобартонеллез можно спутать с седиментом краски) так и ложноотрицательные результаты (в связи с отсутствием паразита в крови в течение первых часов болезни или в связи с циклической паразитемии, кроме того высокая концентрация стабилизатора ЭДТА может приводить к отщеплению гемопаразита от поверхности эритроцита).
По количеству пораженных эритроцитов можно иногда судить о степени тяжести заболевания. Так клинически значимым является поражение более 10% эритроцитов. Данный метод необходимо подтверждать ПЦР диагностикой. Это самый чувствительный специфический метод, в настоящий момент – метод выбора, обнаруживающий фрагменты ДНК возбудителя, позволяющий выявлять гемобартонеллез еще на стадии носительства или уже спустя 8 дней после заражения, однако, важно его применение еще до начала антибиотикотерапии. Считается, что ПЦР диагностика гемобартонеллеза на 37% более эффективна, чем микроскопия мазка крови. Однако, данные по ПЦР диагностики следует интерпретировать и с учетом клинической симптоматики. При отрицательном результате по ПЦР, с большей вероятностью считается, что данное заболевание отсутствует у животного. ПЦР диагностику при положительном результате желательно проводить потом еще раз повторно где-то через полгода после окончания курса лечения, чтобы убедиться в выздоровлении животного.
Возможно также использование метода меченных антител - иммунофлюоресценции антител к возбудителю (метод РИФ), данный метод более надежен, чем микроскопия.
Гемобартенеллез часто сопровождает хронические вирусные инфекции кошек, поэтому при его выявлении необходимо проводить также исследования и на другие причины анемии – вирусный лейкоз кошек и вирусный иммунодефицит кошек.
Обязательным в ходе диагностики является общеклинический анализ крови. Примечательным показателем гемобартонеллеза является регенеративная анемия (повышенное количество ретикулоцитов), если она не осложнена, к примеру, хронической вирусной инфекцией или выраженной почечной недостаточностью. Анемия макроцитарная, полихроматофильная, гипохромная или нормохромная, часто наблюдаются анизоцитоз, микроцитоз, полихромазия, эритроциты с базофильной зернистостью и тельцами Жолли или Гейнца, а также нормобласты.
Соответственно, наблюдается гемоглобинемия и, как правило, тромбоцитопения, лейкоцитоз, но возможна и лейкопения, повышение СОЭ и нормобластов. В плазме крови может развиваться билирубинемия. При сильном гемолизе эритроцитов в моче развивается гемоглобинурия, цвет мочи темнеет.
В результате нарушения функции печени может развиваться, как правило, незначительная гемоглобинурия, что можно увидеть в анализах мочи наличием уробилиногена и гемоглобина, что визуально дает темный цвет мочи.
При ультразвуковой диагностике гемобартонеллеза, как правило, выявляется гепатомегалия и спленомегалия, селезенка при этом заболевании испытывает сильнейшие нагрузки в виду гибели большого количества эритроцитов, которые данный орган должен вывести.
Гемобартенеллез лечится специфическими антибиотиками тетрациклинового ряда. Это прежде всего антибиотики тетрациклинового ряда (Доксициклин, Окситетрациклин). Так Доксициклин применяют в дозе 10 мг/кг/сут. (от 5 мг/кг/сут.) на протяжении 2 и даже 4 недель, однако, даже при таком длительном курсе может не быть полной элиминации возбудителя.
При непереносимости Доксициклина альтернативой лечения являются фторхинолоны. Это прежде всего Энрофлоксацин в дозе 5 мг\кг в сутки курсом около 10 дней. Однако, часто Энрофлоксацин даже в дозе 10 мг/кг в течении 2 недель может не дать достаточного эффекта, а у данного препарата больше побочных действий. Более высокие дозы могут привести к потере зрения. Его нельзя назначать беременным и до годовалого возраста. У щенков и котят может быть его непереносимость в виде рвоты, а также на месте его инъекции может развиваться некроз кожи. Однако, Доксициклин также не рекомендуется котятам и щенкам по причине его накопления в костной ткани, что в дальнейшем нарушает формирование костной системы и зубов. Из других побочных эффектов Доксициклин обладает гепатотоксичностью, а при длительном применении – местно-раздражающим действием при инъекционной форме применения. Поэтому котят и щенков пробуют лечить антипротозойными препаратами, как Имидокарб, при этом достаточно одной инъекции. Однако, эти препараты помогают только при медленном течении болезни. Если дней через 5 наблюдается положительная динамики в общеклиническом анализе крови, то эффект от препарата считается достигнутым. Возможно также применение противопротозойного препарата Азидина в дозе 3,5 мг/кг. В дозе 5 мг/кг/сут. 2-4 недели он элиминирует всех возбудителей.
Азитромицин, применяемый при лечении микоплазмоза у людей, не эффективен при лечении гемобартенеллеза.
Возможно также применение антибиотиков левомецитинового ряда в дозе 25-50 мг в 2-3 приема на протяжении около 2-3 недель, однако, он также не вызывает полной элиминации возбудителя.
Для лечения истощенных и ослабленных кошек можно использовать Тиметосул (в составе которого Сульфадиазин и Триметоприм) в парентеральной форме. Он используется всего лишь трехкратно в дозе 16 и 32 мг/кг.
Необходимо также и симптоматическое лечение. Назначаются препараты железа и витамины группы В. Для поддержки печени необходимы гепатопротекторы (как, например, Гептрал). В случае выраженной анемии (при гематокрите от 20) необходимо уже переливание цельной крови или эритроцитарной массы. При отсутствии хронический вирусных инфекций хороший эффект дают стимуляторы эритропоэза (как Эпокрин, Дарбопоэтин и т.д.). При наличии же вирусного лейкоза кошек прогноз становится, особенно, неблагоприятным. При выраженной тромбоцитопении, в целях предотвращения аутоиммунного разрушения эритроцитов, т.е. для подавления эритрофагоцитоза и снижения вторичной иммуноопосредованной гемолитической анемии (т.е. когда наблюдается прогрессирующая анемия) необходимы кортикостероиды в иммуносупрессивной дозе, т.е. от 2 мг/кг/сут. с последующим ее плавном снижении. При сниженном аппетите необходимо принудительное кормление или даже зондовое с помощью эзофагостомы. Диета в стадию восстановления должна быть высокобелковой, богатой витаминами и минералами. При выраженном обезвоживании проводится гидратация для восстановления водно-электролитного баланса. Без лечения смертность обычно достигает около 30%. После лечения кошки, как правило, остаются носителями гемобартонелл, но рецидивы встречаются крайне редко.
Для профилактики заражения кошек гемобартонеллезом необходимо исключать их контакт с бездомными животными и использовать репелленты и акарициды в виде ошейников и препаратов топикального применения. Важна и периодическая дезинсекция мест обитания бездомных кошек. Необходимо следить за полноценным кормлением и содержанием животного. Вакцина от гемобартонеллеза пока еще не разработана.
Читайте также:

