Круглые черви у енотов
Обновлено: 13.05.2024
В чем заключаются трудности диагностики гельминтозов? Какова терапия гельминтозов? На фоне глобальных экологических изменений, широкого применения иммунных, антибактериальных и прочих лекарственных препаратов, частых нарушений адаптационных процессов
В чем заключаются трудности диагностики гельминтозов?
Какова терапия гельминтозов?
На фоне глобальных экологических изменений, широкого применения иммунных, антибактериальных и прочих лекарственных препаратов, частых нарушений адаптационных процессов (болезни адаптации), постоянного стресса, повышения уровня образованности и культуры населения многие давно известные заболевания человека изменили свою клиническую картину. Некоторые симптомы практически перестали встречаться, другие, наоборот, стали выходить на первый план. Это относится и к заболеваниям, вызываемым гельминтами, в частности, круглыми паразитическими червями (нематодами). В умеренном поясе наиболее широко распространенные нематоды — аскарида и острицы.
Гельминты могут вызывать нарушения функции желудочно-кишечного тракта (ЖКТ), быть причиной аллергических (или псевдоаллергических) реакций или усугублять их, вызывать интоксикацию, а также быть фактором, ослабляющим иммунитет [2]. В настоящее время редко встречаются случаи массивной инвазии, когда диагностика не вызывает затруднений, а клубки гельминтов вызывают обтурации кишечника, — значительно чаще гельминты стали являться причиной развития аллергических проблем. При этом гельминтозы относятся к тем заболеваниям, которые трудно диагностировать в связи с объективными и субъективными трудностями (длительные периоды отсутствия яйцекладки, возможность отсутствия среди паразитирующих особей самок, вероятность технических ошибок). Поэтому важно знать клиническую картину данных заболеваний, чтобы иметь возможность назначать углубленное обследование или эффективную терапию по совокупности косвенных признаков, даже не имея прямых доказательств наличия гельминтоза.
С целью оценить клиническую картину при нематодозах проанализированы жалобы, анамнез и результаты осмотра 150 детей, у которых были обнаружены аскариды (116 детей), острицы (27 детей), аскариды и острицы (7 детей). Гельминты выявлены стандартными методами: обнаружение яиц аскарид в фекалиях методом мазка или яиц остриц в соскобе на энтеробиоз, а также визуальное обнаружение аскарид или остриц в фекалиях, рвотных массах или при оперативном или эндоскопическом вмешательстве в брюшной полости или в области прямой кишки [3].
Среди детей было 67 мальчиков, 83 девочки. Распределение по возрасту представлено в табл. 1. Преобладали дети младшего дошкольного возраста (от одного до трех лет), их количество составило 63%. Именно в этом возрасте — наибольшие эпидемиологические предпосылки появления нематодозов.
У 150 детей с доказанными инвазиями аскаридами и/или острицами отмечались следующие клинические проявления.
У 107 детей (71,3%) были аллергические проблемы: кожные высыпания, диатез, атопический дерматит, нейродермит — у 99 (66%), из них у 18 эти проблемы носили периодический характер, у двух детей, кроме кожных высыпаний, отмечались конъюнктивиты; у десяти (6,7%) отмечалась доказанная пищевая аллергия на какие-то продукты с высоким уровнем специфических IgE в сыворотке крови; у шести детей (4%) отмечался астматический компонент или был установлен диагноз бронхиальная астма.
Бруксизм (скрежетание зубами) — симптом, который часто связывается с глистными инвазиями, но фактически является неспецифическим признаком интоксикации центральной нервной системы и может сопровождать любые хронические интоксикации — отмечался у 25 детей (16,7%).
Нарушения ночного сна отмечались у 81 ребенка (54%): беспокойство к вечеру, затруднения засыпания — у 15 детей (10%); беспокойный ночной сон (вскрикивания, постанывания, метания во сне, пробуждения, плач, бессонница, кошмарные сновидения) — у 76 (50,7%). Некоторые родители старших детей затруднялись охарактеризовать ночной сон ребенка, т. к. ребенок спит в другой комнате. Проблемы с засыпанием и ночным сном — важный симптом глистных инвазий, т. к. известно, что кишечные нематоды (в том числе аскариды и острицы) часто активизируются именно ночью.
У 54 детей (36%) отмечались зуд и/или покраснения в области заднего прохода (анальная эскориация) — у 43 детей (28,7%); зуд — у 38 (25,3%); оба симптома — у 27 (18%). Анальная эскориация и зуд считаются симптомами энтеробиоза (острицы), но при этом из 54 детей, у которых отмечались данные симптомы, энтеробиоз был доказан у 17 детей (31,5% от числа детей с этими симптомами). У других 37 детей (68,5% от числа детей с данными симптомами) было доказано наличие аскаридоза, но ни визуально, ни в анализах не были обнаружены острицы. Это может свидетельствовать либо о том, что в данных случаях присутствовали острицы, которые не были диагностированы, т. е. гельминтоз был смешанным, либо о том, что анальная эскориация и зуд — симптомы, характерные не только для энтеробиоза, но и аскаридоза.
У 29 детей (19,3%) отмечались признаки общего ослабления иммунитета: часто или длительно болеющие дети (по общепринятой классификации Monto J. et al., 87) — 18 детей (12%); рецидивирующие стоматиты, гингивиты отмечались у 13 детей (8,7%); кариес зубов — у шести (4%); рецидивирующие гнойные заболевания кожи или слизистых — у трех (2%).
У 15 детей (10%) имелись результаты исследования иммунного статуса по крови: у 13 детей было снижено количество Т-клеток; у всех 15 детей было снижено количество Т-хелперов, причем у шести из них — существенно; у 12 детей было снижено хелперно-супрессорное соотношение; у семи детей отмечалось снижение уровня IgA (секреторный иммуноглобулин), в том числе у трех — существенное, у остальных же восьми детей уровень IgA в сыворотке крови был либо нормальным, либо повышенным; у шести детей отмечалось снижение количества лимфоцитов, в том числе у одного ребенка была выраженная лимфо- и нейтропения. Эти результаты подтверждают известные данные о том, что аскариды и острицы угнетающе влияют на функции иммунитета, а также что у людей с ослабленным иммунитетом большая вероятность появления гельминтоза [1].
У большинства детей отмечалось более одного симптома. Обобщенные данные по клинической картине представлены в табл. 2.
Терапия во всех случаях состояла из двух этапов: сначала — антигельминтная терапия, причем назначались два разных препарата (декарис и вермокс) с интервалом три — пять дней между ними, чтобы максимально охватить различные стадии жизни гельминтов; через некоторое время после антигельминтной терапии — препараты для микробиологической и функциональной коррекции. Соответственно оценивались результаты противоглистной терапии, результаты всего лечения, а также катамнез в течение шести месяцев после терапии. В большинстве случаев улучшение наступало быстро в процессе лечения. У 36 детей только после антигельминтной терапии существенно уменьшились или полностью исчезли аллергические проявления, у 39 детей после первого этапа терапии нормализовалась работа ЖКТ, у 41 ребенка сразу прекратились боли в животе, по остальным симптомам также наступало улучшение после противоглистных препаратов. Это подтверждает то, что симптомы были вызваны наличием гельминтов.
У 92 детей после всего лечения не было никаких жалоб; о 37 нет данных об изменениях состояния в процессе и после лечения; у 16 детей эффект был неполным, т. е. какие-то симптомы сохранялись и после окончания лечения; у четырех детей эффект от терапии оказался нестойким, поскольку возникли рецидивы после окончания лечения; у трех детей эффекта от терапии не было.
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут бы
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут быть также личинки других аскарид — кошки (T. mystax), коровы, буйвола, (T. vitulorum). Однако роль этих возбудителей в патологии человека практически не изучена
Половозрелые формы T. canis — крупные раздельнополые черви длиной 4 — 18 см локализуются в желудке и тонком кишечнике животных (собак). Интенсивность инвазии у собак может быть очень высокой, особенно у молодых животных. Средняя продолжительность жизни половозрелых особей составляет 4 месяца, максимальная — 6 месяцев. Самка паразита за сутки откладывает более 200 тыс. яиц. В 1 г фекалий может содержаться 10 000—15 000 яиц, так что в почву попадают миллионы яиц, обусловливая тем самым высокий риск заражения токсокарозом.
 |
Яйца токсокар округлой формы, крупнее яиц аскариды (65—75 мкм). Наружная оболочка яйца толстая, плотная, мелкобугристая. Внутри яйца располагается темный бластомер.
Цикл развития возбудителя следующий. Выделившиеся яйца токсокар попадают в почву, где, в зависимости от влажности и температуры почвы, созревают за 5—36 суток, становясь инвазионными. Инвазионность яиц сохраняется в почве длительное время, в компосте — несколько лет.
Жизненный цикл токсокары сложный. Выделяют основной цикл и два варианта вспомогательных. Основной цикл происходит по схеме: окончательный хозяин (псовые) — почва — окончательный хозяин (псовые). Передача инвазии осуществляется геооральным путем. Вспомогательный цикл (вариант 1) идет трансплацентарно, в этом случае паразит в личиночной стадии переходит от беременной самки к плоду, в организме которого совершает полную миграцию, достигая в кишечнике щенка половозрелой стадии. Инвазированный щенок становится функционально полноценным окончательным хозяином, источником инвазии.
Вспомогательный цикл (вариант 2) осуществляется по цепи: окончательный хозяин (псовые) — почва — паратенический хозяин. Паратеническим (резервуарным) хозяином могут быть грызуны, свиньи, овцы, птицы, земляные черви. Человек также выступает в роли паратенического хозяина, но не включается в цикл передачи инвазии, являясь для паразита биологическим тупиком. Дальнейшее развитие возбудителя происходит при условии, что паратенический хозяин будет съеден собакой или другим окончательным хозяином. Механизм передачи инвазии при этом варианте — геооральный — ксенотрофный.
В зависимости от возраста хозяина реализуются разные пути миграции личинок токсокар. У молодых животных (щенков до 5 недель) почти все личинки совершают полную миграцию с достижением половозрелых форм в кишечнике и выделением яиц во внешнюю среду. В организме взрослых животных большая часть личинок мигрирует в соматические ткани, где сохраняет жизнеспособность несколько лет. В период беременности и лактации у беременных сук возобновляется миграция личинок. Мигрирующие личинки через плаценту попадают в организм плода. Личинки остаются в печени пренатально инвазированных щенков до рождения, а после рождения личинки из печени мигрируют в легкие, трахею, глотку, пищевод и попадают в желудочно-кишечный тракт, где через 3—4 недели достигают половозрелой стадии и начинают выделять во внешнюю среду яйца. Кормящие суки могут передавать щенкам инвазию также через молоко.
У человека цикл развития возбудителя, его миграция осуществляется следующим образом. Из яиц токсокар, попавших в рот, затем в желудок и тонкий кишечник выходят личинки, которые через слизистую оболочку проникают в кровеносные сосуды и через систему воротной вены мигрируют в печень, где часть из них оседает, инцистируется или окружается воспалительными инфильтратами, образуя гранулемы. Часть личинок по системе печеночных вен проходит фильтр печени, попадает в правое сердце и через легочную артерию — в капиллярную сеть легких. В легких часть личинок также задерживается, а часть, пройдя фильтр легких, по большому кругу кровообращения заносится в различные органы, оседая в них. Личинки токсокар могут локализоваться в различных органах и тканях — почках, мышцах, щитовидной железе, головном мозге и др. В тканях личинки сохраняют жизнеспособность многие годы и периодически, под влиянием различных факторов, возобновляют миграцию, обусловливая рецидивы заболевания.
- Географическое распространение и эпидемиология
Токсокароз — широко распространенная инвазия, она регистрируется во многих странах. Показатели пораженности плотоядных являются высокими во всех странах мира. Средняя пораженность собак кишечным токсокарозом, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах у части животных достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз. Распространенность инвазии в различных регионах точно неизвестна, поскольку токсокароз не подлежит обязательной регистрации. Совершенно очевидно, что токсокароз имеет широкую геграфию распространения, и число больных значительно выше официально регистрируемых.
| Токсокароз широко распространен и регистрируется во многих странах. Средняя пораженность кишечным токсокарозом собак, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз |
- Патогенез и патологическая анатомия
Патогенез токсокароза сложный и определяется комплексом механизмов в системе паразит — хозяин. В период миграции личинки травмируют кровеносные сосуды и ткани, вызывая геморрагии, некроз, воспалительные изменения. Ведущая роль принадлежит иммунологическим реакциям организма в ответ на инвазию. Экскреторно-секреторные антигены личинок оказывают сенсибилизирующее действие с развитием реакций немедленного и замедленного типов. При разрушении личинок в организм человека попадают соматические антигены личинок. Аллергические реакции проявляются отеками, кожной эритемой, увеличением резистентности дыхательных путей к вдыхаемому воздуху, что клинически выражается развитием приступов удушья. В аллергических реакциях принимают участие тучные клетки, базофилы, нейтрофилы, но основную роль играют эозинофилы. Пролиферация эозинофилов регулируется Т-лимфоцитами при участии медиаторов воспалительных реакций, выделяемых сенсибилизированными лимфоцитами, нейтрофилами, базофилами. Образующиеся иммунные комплексы привлекают в очаг поражения эозинофилы. Вокруг личинок токсокар кумулируются сенсибилизированные Т-лимфоциты, привлекаются макрофаги и другие клетки — формируется паразитарная гранулома.
Патоморфологическим субстратом токсокароза является выраженное в различной степени гранулематозное поражение тканей. При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими. При токсокарозе находят многочисленные гранулемы в печени, легких, поджелудочной железе, миокарде, лимфатических узлах, головном мозге и других органах.
Наиболее характерным лабораторным показателем является повышенное содержание эозинофилов в периферической крови. Относительный уровень эозинофилии может колебаться в широких пределах, достигая в ряде случаев 70 — 80% и более. Повышается содержание лейкоцитов (от 20х109 до 30х109 на 1 л). При исследовании пунктата костного мозга выявляется гиперплазия зрелых эозинофилов. У детей нередко отмечается умеренная анемия. Некоторые исследователи отмечают прямую корреляцию между тяжестью клинических проявлений инвазии и уровнем эозинофилии и гиперлейкоцитоза периферической крови. Характерным лабораторным признаком является также ускорение СОЭ, гипергаммаглобулинемия. В случаях поражения печени наблюдается повышение билирубина, гиперферментемия.
В хронической стадии болезни острые клинические и лабораторные признаки затухают. Наиболее стабильным лабораторным показателем остается гиперэозинофилия периферической крови.
Выделяют субклиническое, легкое, среднетяжелое и тяжелое течение токсокароза. Возможна так называемая бессимптомная эозинофилия крови, когда явные клинические проявления инвазии отсутствуют, но наряду с гиперэозинофилией выявляются антитела к антигенам T.canis.
Одной из наиболее серьезных проблем, связанных с токсокарозом, является его взаимосвязь с бронхиальной астмой. При сероэпидемиологических исследованиях установлено, что у больных бронхиальной астмой нередко обнаруживаются антитела к антигенам T.canis классов Ig G и Ig E. В зависимости от остроты паразитарного процесса, его длительности и длительности клинических проявлений бронхиальной астмы преобладает тот или другой класс иммуноглобулинов. Имеются клинические наблюдения, свидетельствующие об улучшении течения бронхиальной астмы или выздоровлении после ликвидации токсокарозной инвазии.
Паразитологический диагноз устанавливается редко и только по наличию в тканях характерных гранулем и личинок и их идентификации при исследовании биопсийного и секционного материала. Это возможно при пункционной биопсии печени, легких, оперативном вмешательстве. Обычно диагноз токсокароза устанавливается на основании данных эпидемиологического анамнеза, клинической симптоматики и гематологических проявлений. Используют также иммунологические реакции, позволяющие выявлять антитела к антигенам токсокар. Обычно применяют ИФА с секреторно-экскреторным антигеном личинок токсокар второго возраста. В настоящее время в России выпускается коммерческий диагностикум. Диагностическим титром считают титр антител 1:400 и выше (в ИФА). Титр антител 1:400 свидетельствует об инвазированности, но не болезни. Титр антител 1:800 и выше свидетельствует о заболевании токсокарозом. Практика показывает, что прямая корреляция между уровнем антител и тяжестью клинических проявлений токсокароза существует не всегда. Не всегда имеется и корреляция между уровнем антител и гиперэозинофилии крови.
При постановке диагноза и определении показаний к специфической терапии следует учитывать, что токсокароз протекает циклически с рецидивами и ремиссиями, в связи с чем возможны значительные колебания клинических, гематологических и иммунологических показателей у одного и того же больного.
М. И. Алексеева и соавт. (1984) разработали алгоритм диагностики токсокароза, основанный на оценках в баллах значимости клинических симптомов и сопоставлении клинико-эпидемиологических и лабораторных показателей. Этот метод может быть перспективен при проведении массовых обследований населения.
Дифференциальный диагноз проводят с миграционной стадией других гельминтозов (аскаридоз, описторхоз), стронгилоидозом, эозинофильной гранулемой, лимфогранулематозом, эозинофильным васкулитом, метастазирующей аденомой поджелудочной железы, гипернефромой и другими заболеваниями, сопровождающимися повышенным содержанием эозинофилов в периферической крови. Следует иметь в виду, что у больных с системными лимфопролиферативными заболеваниями и серьезными нарушениями в системе иммунитета иммунологические реакции могут быть ложно положительными. В этих случаях необходим тщательный анализ клинической картины заболевания.
| При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими |
Глазной токсокароз. Патогенез этой формы токсокароза до конца не ясен. Существует гипотеза об избирательном поражении глаз у лиц с инвазией низкой интенсивности, при которой не развивается достаточно выраженная иммунная реакция организма из-за слабого антигенного воздействия небольшого числа поступивших в организм личинок токсокар.
Эта форма токсокароза чаще наблюдается у детей и подростков, хотя описаны случаи заболевания и у взрослых.
Для токсокароза характерно одностороннее поражение глаз. Патологический процесс развивается в сетчатке, поражается хрусталик, иногда параорбитальная клетчатка. В тканях глаза формируется воспалительная реакция гранулематозного характера. Патологический процесс часто принимают за ретинобластому, проводят энуклеацию глаза. При морфологическом исследовании обнаруживают эозинофильные гранулемы, иногда — личинки токсокар.
Клинически поражение глаз протекает как хронический эндофтальмит, хориоретинит, иридоциклит, кератит, папиллит. Глазной токсокароз — одна из частых причин потери зрения.
Диагностика глазного токсокароза сложна. Количество эозинофилов обычно нормальное или незначительно повышено. Специфические антитела не выявляются или выявляются в низких титрах.
Разработано недостаточно. Применяют противонематодозные препараты — тиабендазол (минтезол), мебендазол (вермокс), медамин, диэтилкарбамазин. Эти препараты эффективны в отношении мигрирующих личинок и недостаточно эффективны в отношении тканевых форм, находящихся в гранулемах внутренних органов.
Минтезол (тиабендазол) назначают в дозах 25—50 мг/кг массы тела в сутки в три приема в течение 5—10 дней. Побочные явления возникают часто и проявляются тошнотой, головной болью, болями в животе, чувством отвращения к препарату (в настоящее время препарат в аптечную сеть России не поступает).
Вермокс (мебендазол) назначают по 200 —300 мг в сутки в течение 1—4 недель. Побочные реакции обычно не наблюдаются.
 |
Медамин применяют в дозе 10 мг/кг массы тела в сутки повторными циклами по 10 — 14 дней.
Диэтилкарбамазин назначают в дозах 2 — 6 мг/кг массы тела в сутки в течение 2 — 4 недель. (В настоящее время препарат в России не производится, не закупается за рубежом. — Прим. ред.)
Альбендазол назначают в дозе 10 мг/кг массы тела в сутки в два приема (утро — вечер) в течение 7 — 14 дней. В процессе лечения необходим контроль анализа крови (возможность развития агранулоцитоза) и уровня аминотрансфераз (гепатотоксическое действие препарата). Небольшое повышение уровня аминотрансфераз не является показанием к отмене препарата. В случае нарастающей гиперферментемии и угрозы развития токсического гепатита требуется отмена препарата.
Критерии эффективности лечения: улучшение общего состояния, постепенная регрессия клинических симптомов, снижение уровня эозинофилии и титров специфических антител. Следует отметить, что клинический эффект лечения опережает положительную динамику гематологических и иммунологических изменений. При рецидивах клинической симптоматики, стойкой эозинофилии и положительных иммунологических реакциях проводят повторные курсы лечения.
Прогноз для жизни благоприятный, однако при массивной инвазии и тяжелых полиорганных поражениях, особенно у лиц с нарушениями иммунитета, возможен летальный исход.
Включает соблюдение личной гигиены, обучение детей санитарным навыкам.
Важным профилактическим мероприятием является своевременное обследование и дегельминтизация собак. Наиболее эффективно преимагинальное лечение щенков в возрасте 4 — 5 недель, а также беременных сук. Для лечения собак используют противонематодозные препараты. Необходимо ограничение численности безнадзорных собак, оборудование специальных площадок для выгула собак.
Следует улучшить санитарно-просветительскую работу среди населения, давать информацию о возможных источниках инвазии и путях ее передачи. Особого внимания требуют лица, по роду деятельности имеющие контакты с источниками инвазии (ветеринарные работники, собаководы, землекопы и другие).
Класс нематоды (от греч. nema - нитка, и eidos - сходство), также по-другому называемый - собственно круглые черви. Класс нематоды представлен не только паразитическими формами, но и свободноживущими особями, обитающими в морских и пресных водоемах, почве, где их концентрация может превысить 1 млн на 1м 3 . Медицинское значение имеют многие паразитические формы данного класса.
Заболевания, которые вызывают круглые черви, носят название - нематодозы. Разными паразитами поражаются печень, почки, легкие, желудочно-кишечный тракт, мышцы. На современном этапе развития общества успешно разработана терапия большинства нематодозов и они легко поддаются лечению.
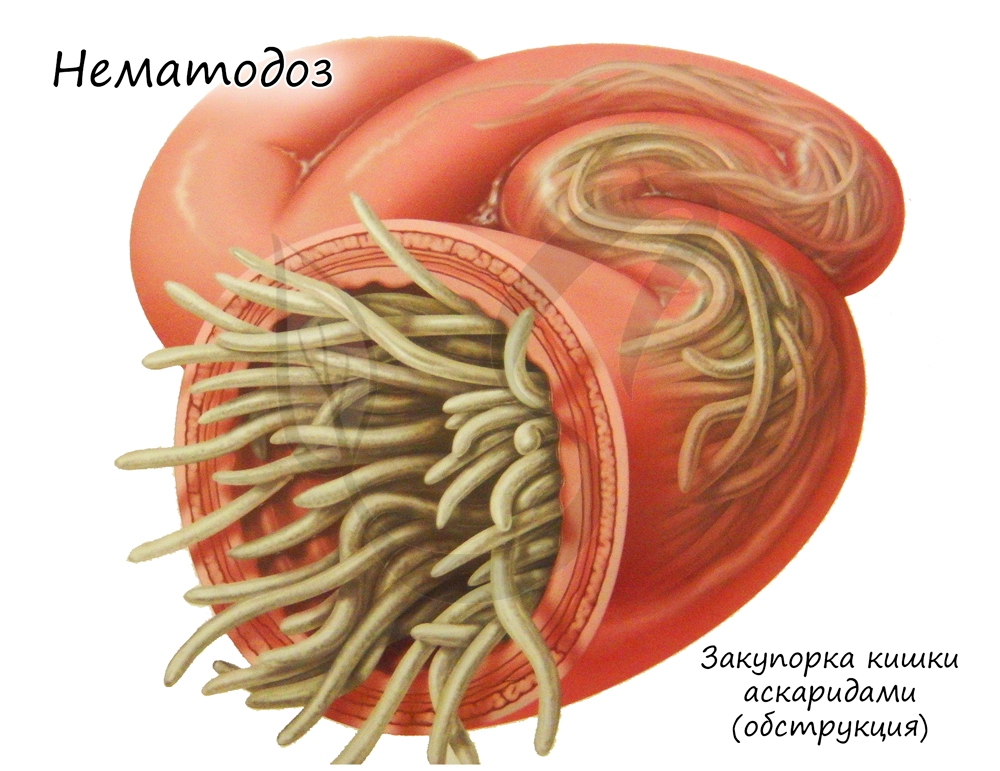
Аскарида
Тело аскариды не сегментировано, заострено с обоих концов, покрыто плотной блестящей кутикулой, которая выполняет функцию наружного скелета и служит защитой от механических воздействий, ядов и пищеварительных ферментов. Характерно наличие только одного слоя продольной мускулатуры.
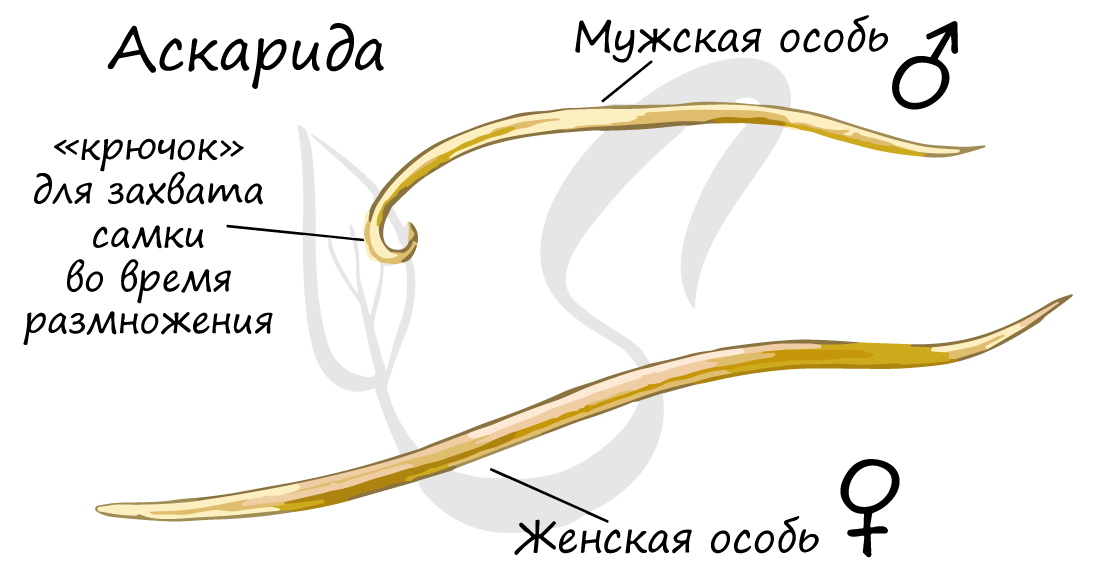
Самки (до 30 см в длину) крупнее самцов (до 20 см). У самцов задний конец тела загнут, на нем расположены кутикулярные иглы - спикулы, которые служат для удержания самки во время копуляции (лат. copulatio - соединение) - соединении двух особей во время полового акта. За один день самка аскариды способна отложить в кишечнике человека до 240 тысяч яиц.
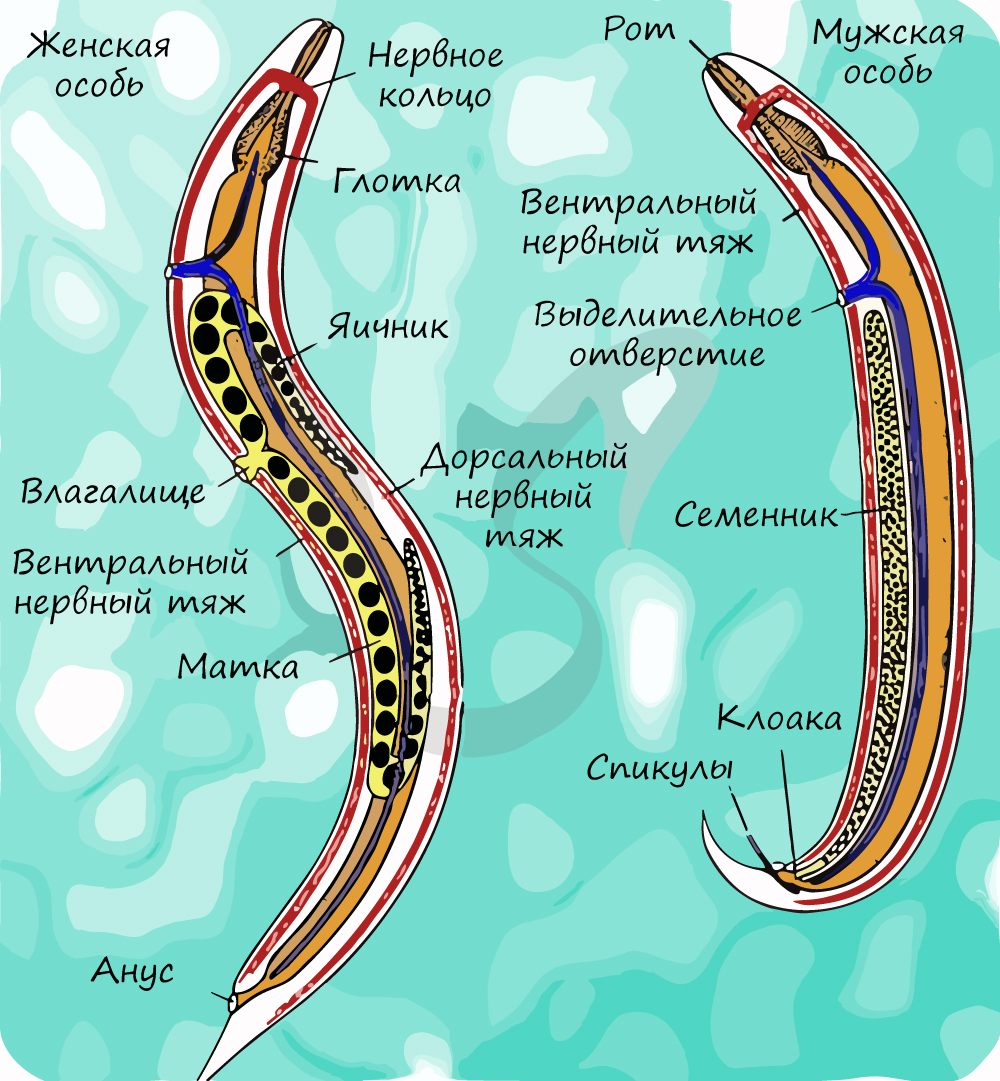
Аскарида, как и многие другие паразиты из класса нематоды, является геогельминтом - ей не нужен промежуточный хозяин, яйца созревают прямо в почве, попав в благоприятные условия.
Взрослые особи живут в кишечнике человека, ежедневно выделяя до 240 тысяч яиц. Вместе с фекалиями яйца попадают во внешнюю среду. В этот момент, они никого не могут заразить. Чтобы яйцо стало инвазионным - способным к заражению, должно пройти 2-3 недели при температуре 20-25°C и достаточной влажности воздуха.
Если все условия соблюдены - яйцо становится инвазионным и может заразить человека. Попав в кишечник, из яйца выходит личинка, которая совершает миграцию. Она пробуравливает стенку кишки, попадает в кровеносное русло и через печень, правое предсердие и правый желудочек достигает легких. Здесь личинка проникает в полость альвеолы (легочный пузырек), а затем ползет вверх, проходя бронхи, трахею, глотку.
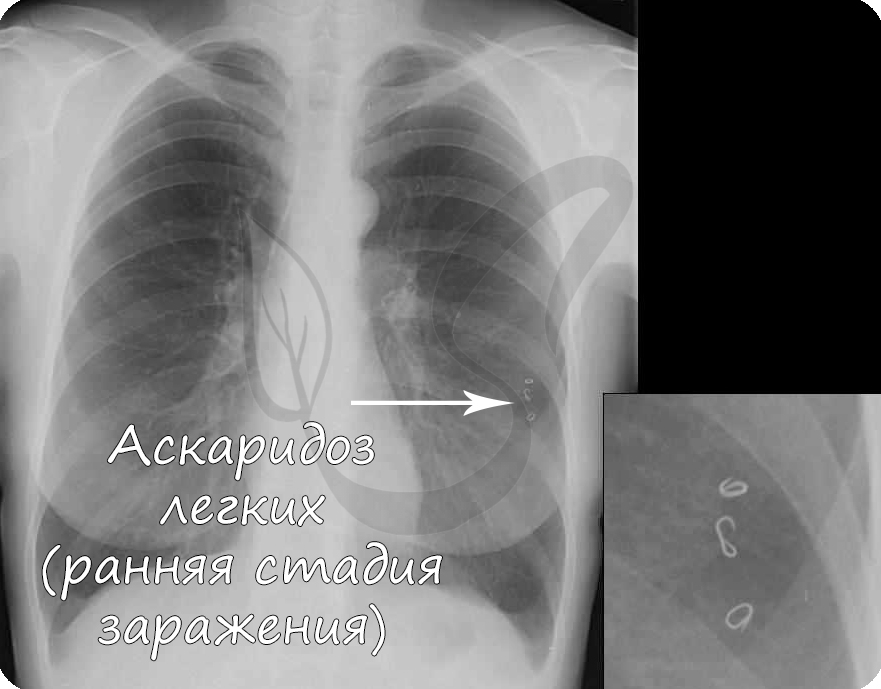
Во время таких массовых миграций личинок возможно воспаление легких. Достигнув глотки, личинка вторично заглатывается человеком и только после этого, попадая в кишечник, превращается в половозрелую особь. Цикл замыкается.
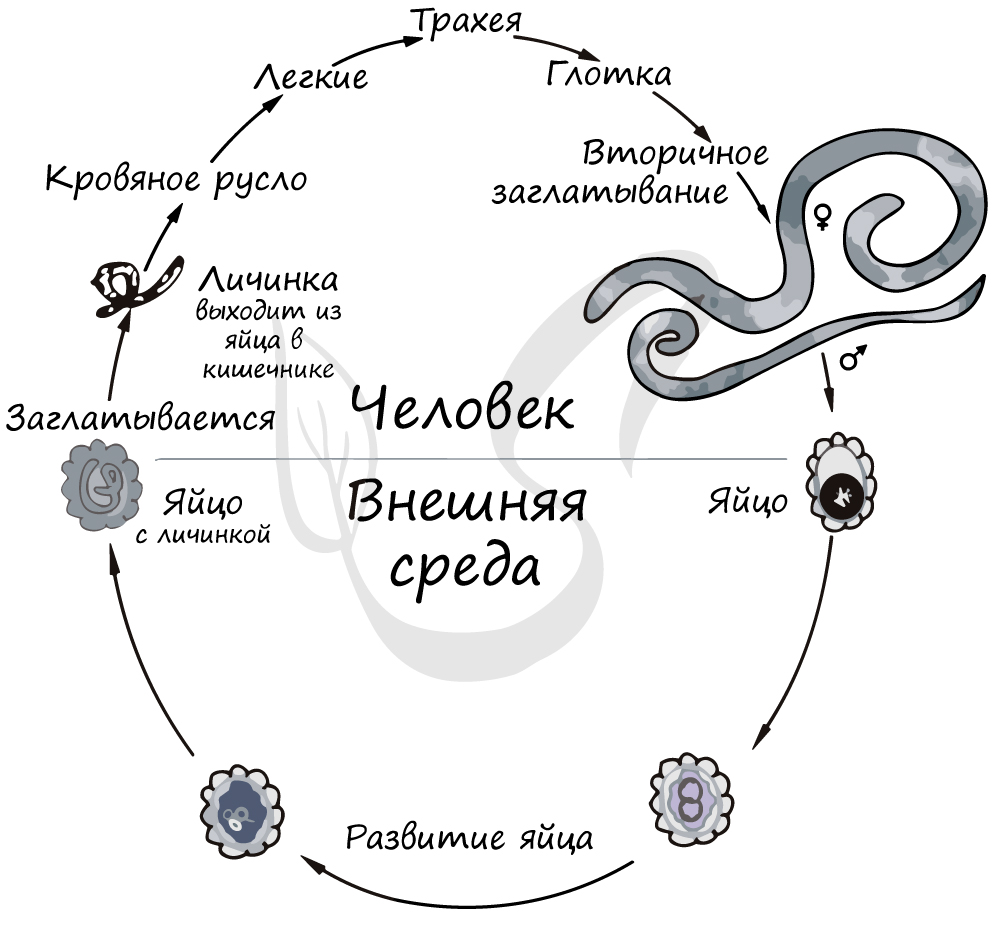
Человек заражается, употребив в пищу инвазионное яйцо аскариды (фекально-оральным путем) с немытыми фруктами, овощами. Аскаридоз - болезнь грязных рук, им часто болеют дети. Профилактика состоит в санитарно-просветительской работе с населением, благоустройстве прилегающих к водоемам населенных пунктов, соблюдении правил личной гигиены (мытье рук, фруктов, овощей).
Острица
Геогельминт, обитающий в кишечнике человека. Вызывает заболевание - энтеробиоз. Самка в длину до 12 мм, самец - 5 мм. Вспышки заболевания острицей случаются в детских коллективах - этот паразит, благодаря своему жизненному циклу, отлично размножается среди детей, давайте разберемся - в чем хитрость острицы?
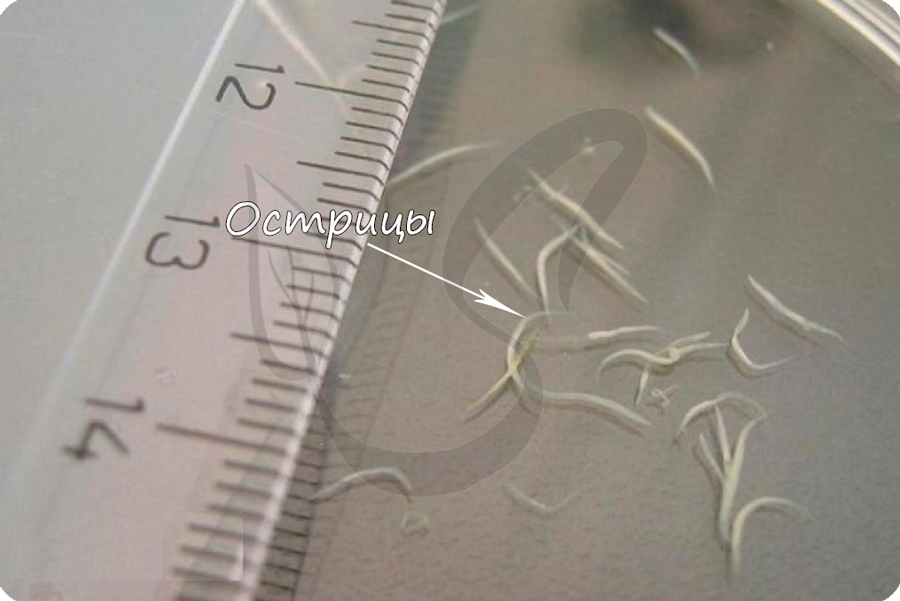
В кишечнике человека взрослые особи размножаются половым путем. После размножения самец погибает, а самка опускается в прямую кишку. Ночью самка выползает из анального отверстия и распространяет яйца в перианальной области. Вскоре после такой вылазки погибает и самка.
При доступе кислорода уже через 4-6 часов яйца становятся инвазионными. У ребенка развивается зуд в перианальной области и, конечно, ребенок начинает чесаться - яйца попадают на руки. При несоблюдении правил гигиены ребенок часто заражает сам себя (аутоинвазия). Яйца попадают в кишечник, где из них развиваются взрослые особи.
Можете представить себе детский сад и (достаточно одного) заболевшего ребенка, который "этими" руками берет игрушки. Энтеробиозом за один день могут заболеть все дети, детский сад закрывается на карантин и проводится тщательная дезинфекция - к сожалению, уверяю вас, это очень правдивый сценарий.
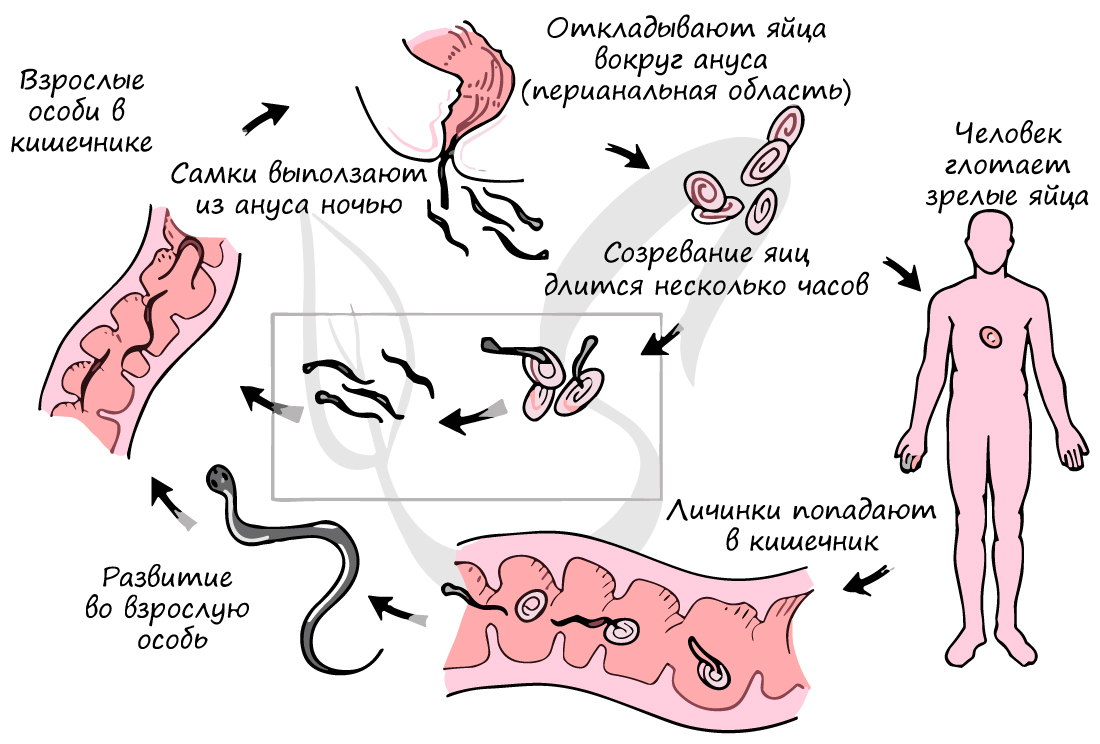
Человек заражается фекально-оральным путем: чаще всего инвазионное яйцо попадает в желудочно-кишечный тракт с немытыми руками. Профилактика состоит в санитарно-просветительской работе, регулярных профилактических мероприятиях в детских коллективах, строгом соблюдении правил гигиены - мытье рук, уход за ногтями.
Ришта
Ришта (тадж., буквально - нить) - паразитический круглый червь, обитающий в подкожно-жировой клетчатке человека и животных. Самка имеет длину до 120 см, самец - до 30 см. Спикулы и сосочки располагаются на заднем конце тела. Окончательным хозяином для ришты является человек, собака, обезьяна. Промежуточный хозяин - пресноводный рачок циклоп. Вызывает заболевание дракункулез.

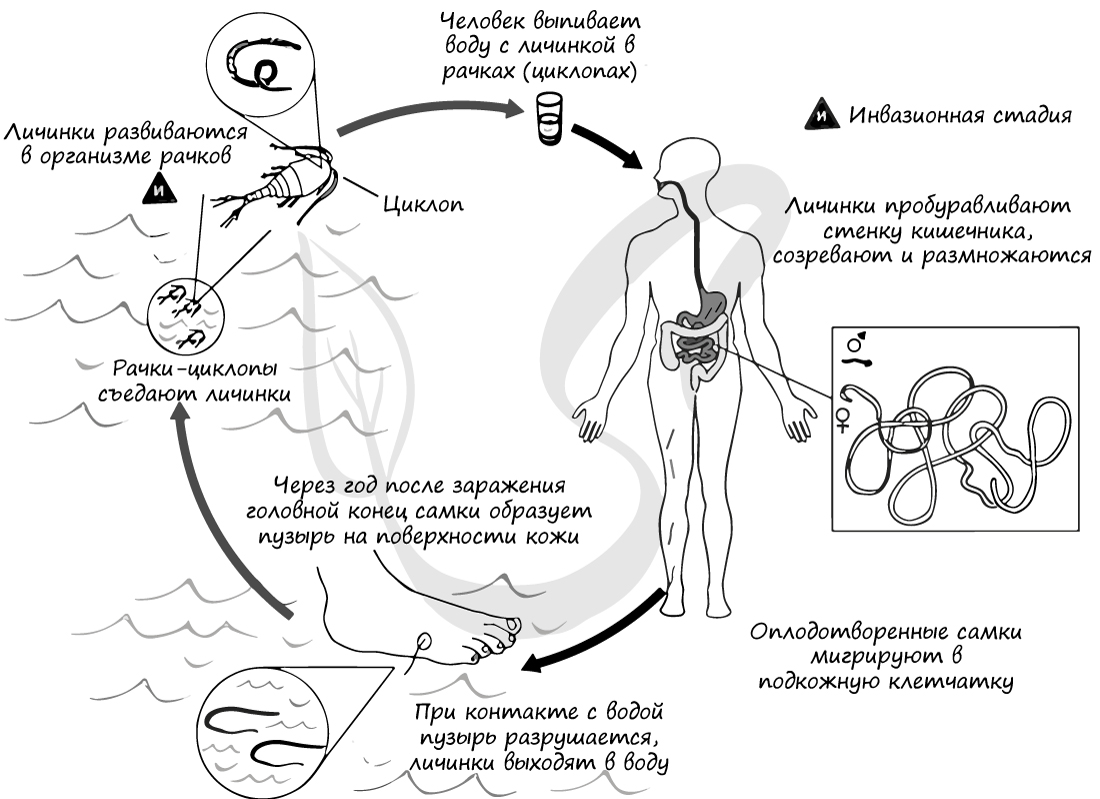
Попав в водоем, личинки ришты внедряются в организм пресноводного рачка циклопа - промежуточного хозяина. По истечению 14 дней личинка становится инвазионной, и может быть вместе с водой из водоема проглочена окончательным хозяином. В кишечнике личинки мигрируют через кишечную стенку в ткани, где достигают половой зрелости, после чего спариваются.
После спаривания самец погибает, а самка мигрирует к подкожной клетчатке хозяина. Примерно через год на теле зараженного человека головной конец самки образует пузырь, который сильно жжет, крайне болезненный. Инстинктивно хочется охладить его водой - этого только и ждет ришта.
При соприкосновении с водой в водоеме пузырь разрывается и тысячи личинок ришты выходят в воду, заражая рачков циклопов. Цикл замыкается. Глядя на картинку ниже, попробуйте своими словами пересказать цикл ришты.
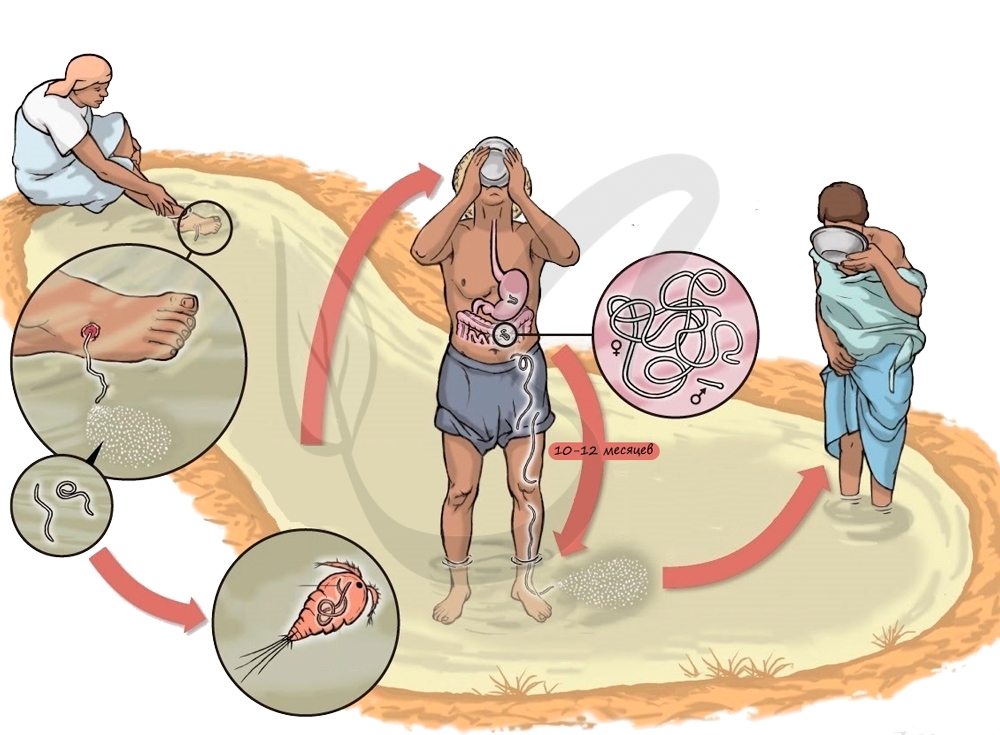
Заражается человек, выпив с водой рачка циклопа, в организме которого находятся жизнеспособные личинки. Профилактика состоит в санитарно-просветительской работе среди населения, охране питьевой воды от загрязнений, уничтожении пресноводных рачков - циклопов, недопустимости питья сырой воды, обязательном ее кипячении.
Трихинелла
Длина самки до 3-4 мм, самца - 1,4-1,6 мм. В роли хозяев трихинеллы чаще всего выступают плотоядные животные. Примечательно, что один и тот же вид служит сначала окончательным, а затем - промежуточным хозяином трихинеллы. Таким образом трихинелла смогла достичь уникального жизненного цикла - вообще без выхода личинок во внешнюю среду. Вызывает заболевание трихинеллез.
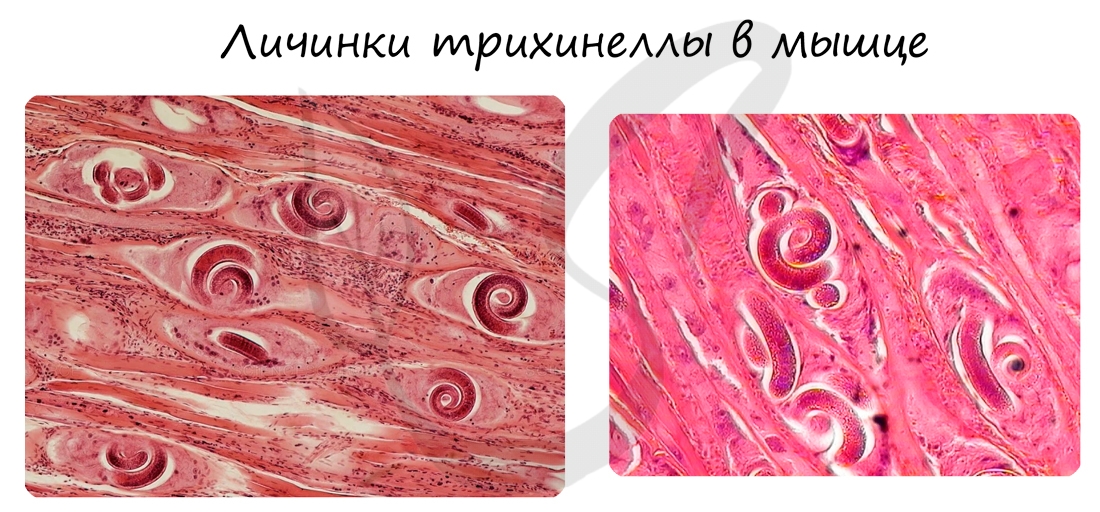
Проглоченные с мясом личинки трихинеллы в кишечнике человека становятся половозрелыми. В результате полового размножения самки рождают личинок, которые пробуравливают стенку кишечника и попадают в кровь, распространяясь по всему организму. В органах и тканях формируются инкапсулированные личинки.
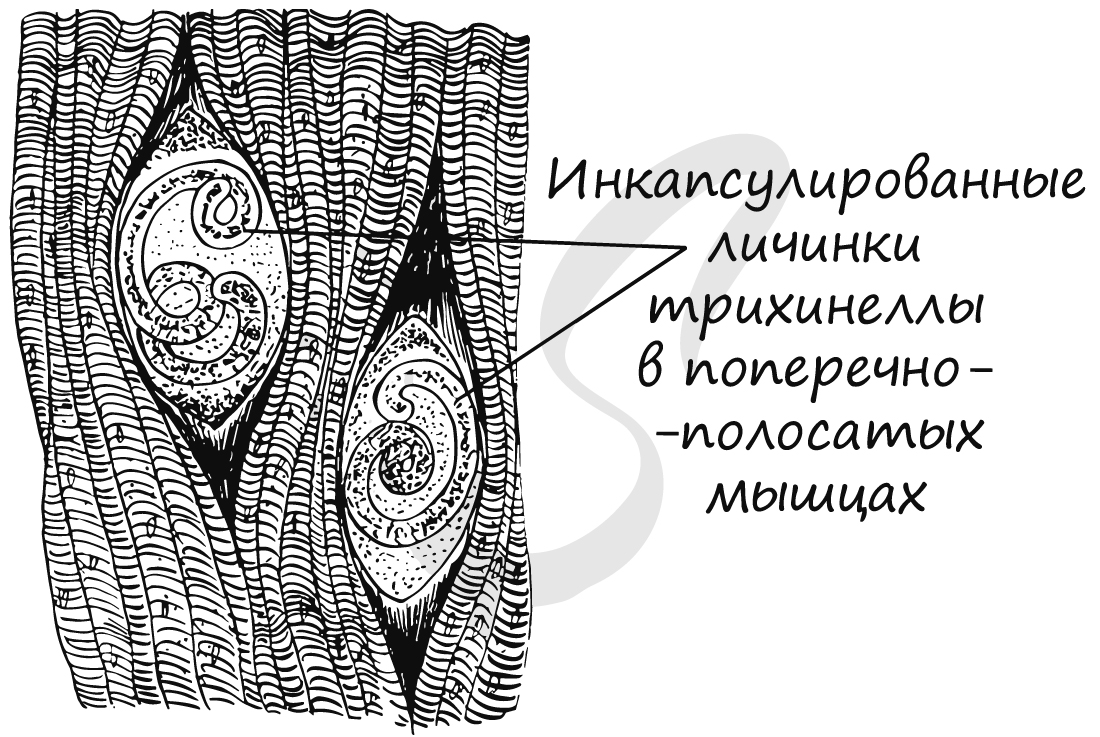
Вдумайтесь - мельчайшие личинки, которые видны только под микроскопом, оседают в мышцах по всему организму! Человеку становится больно двигаться, жевать (поражаются жевательные мышцы) и даже - дышать из-за поражения диафрагмы, дыхательной мышцы. Пять личинок в мышцах на 1 кг тела - смертельная концентрация, приводящая к летальному исходу.
В животном мире паразит передается по пищевой цепочке - хищник поедает жертву, в мышцах которой имеются трихинеллы, и заражается сам: из личинок в кишечнике развиваются взрослые особи. Цикл замыкается. В этом смысле, для трихинеллы человек является тупиковым хозяином, так как его никто не ест.
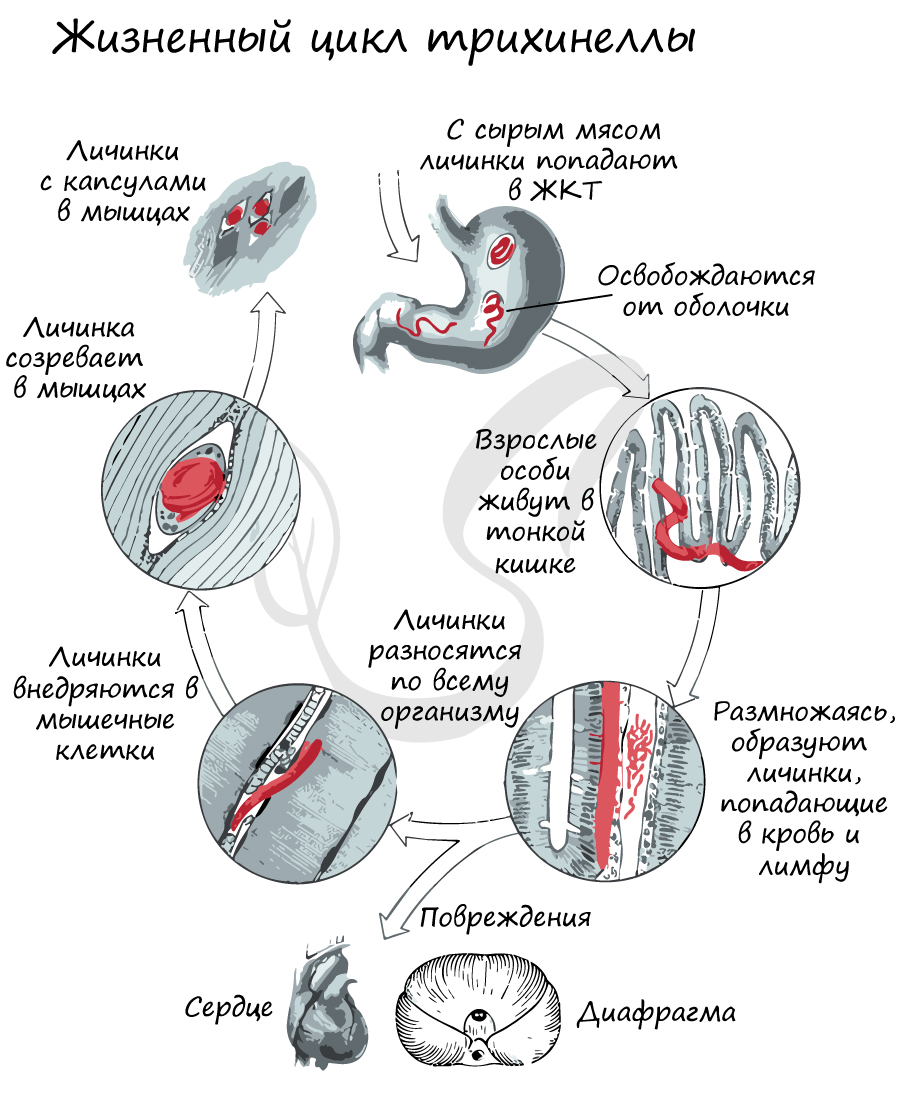
Чаще всего человек заражается трихинеллезом, употребив в пищу мясо свиньи с инкапсулированными личинками (в т.ч. в виде сала), которое не прошло санитарный контроль. Профилактика заключается в санитарно-просветительской работе среди населения, санитарный контроль сала и мяса свиньи, недопустимости употребления мяса, не прошедшего контроль.
Отдельно отмечу, что личинки трихинеллы крайне устойчивы и могут оставаться жизнеспособными даже при длительной варке мяса.
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Тип круглые черви эволюционно происходит от плоских червей - круглые черви также трехслойные, обладают несегментированным телом, билатеральной (двусторонней) симметрией, кожно-мускульным мешком. Возникновение круглых червей сопровождается рядом крупных ароморфозов, которые мы непременно с вами обсудим.
Представители типа: аскарида, острица, ришта, трихинелла.

Ароморфозы круглых червей
У круглых червей впервые возникает полость тела! Отсюда важное наименование, применимое к типу круглые черви - первичнополостные.
Только представьте - у плоских червей пространства внутри тела не было, все заполняла клеточная масса - паренхима (мезенхима). У круглых червей появилось пространство между органами, заполненное межклеточной жидкостью.
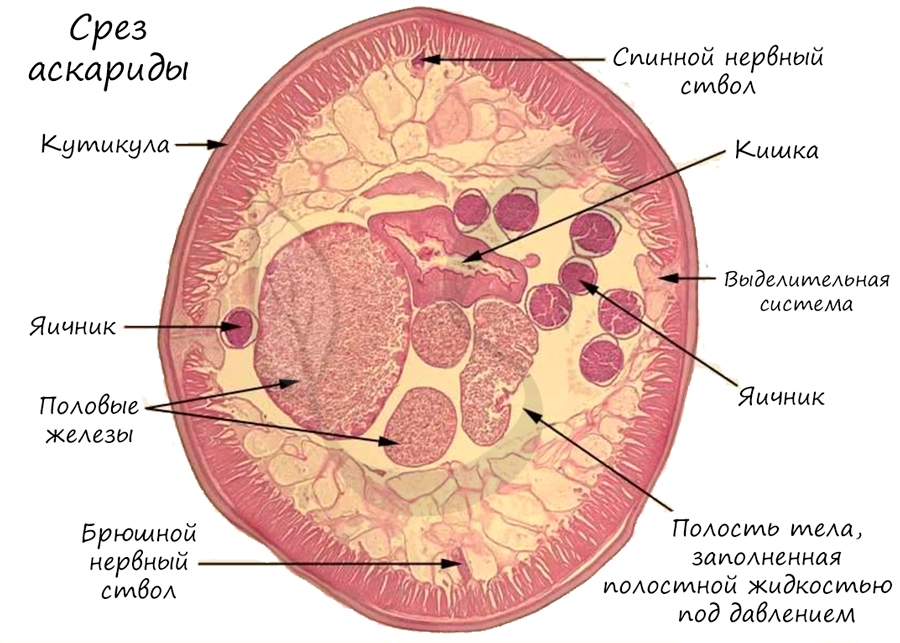
Первичная полость тела, которая характерна для этого типа, по-другому называется - протоцеле, схизоцель, псевдоцель. Эта полость, как мы уже с вами убедились, заполнена межклеточной жидкостью - именно поэтому тело круглых червей на поперечно срезе всегда округлое (в отличие от тела плоских червей, которое "плоское").
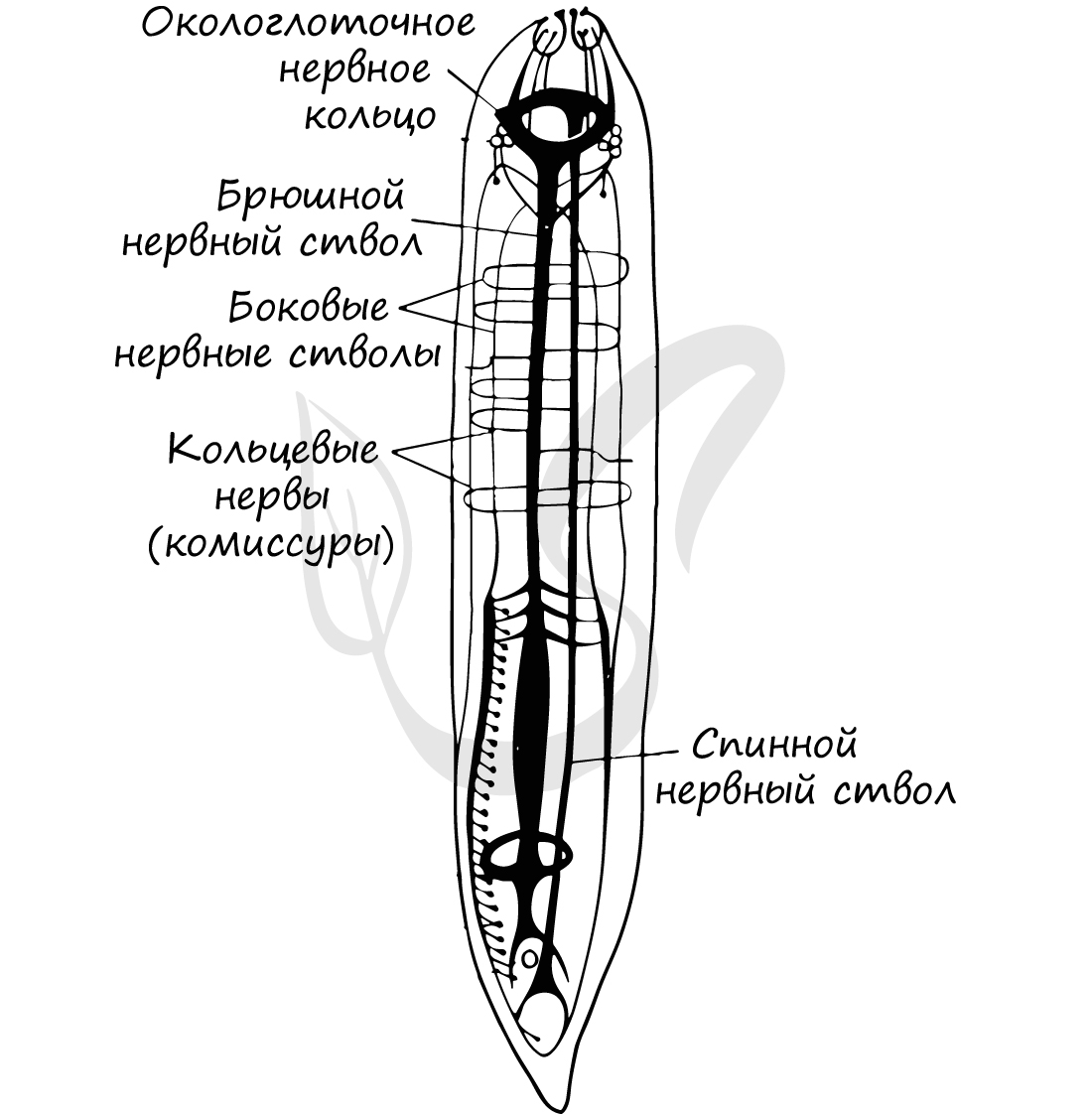
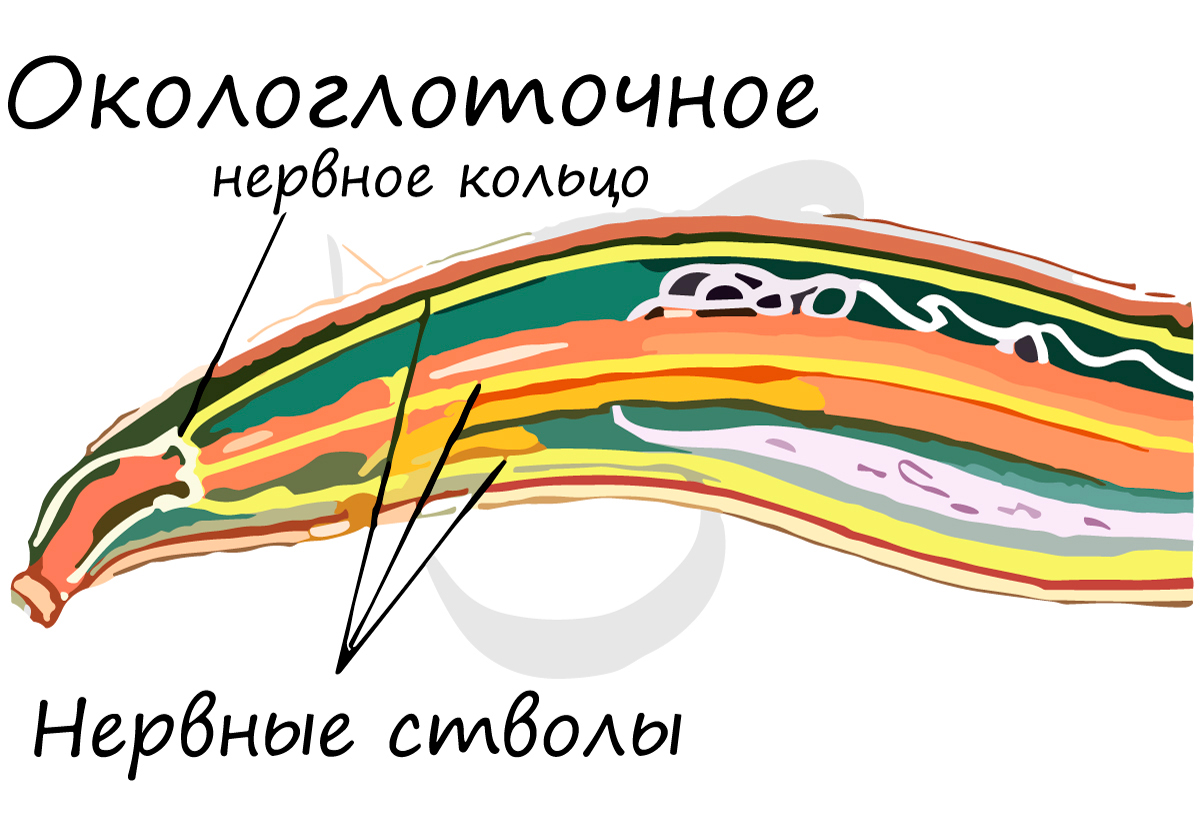
У круглых червей нервная система более развита по сравнению с предшествующими, изученными нами типами. Головные нервные узлы (ганглии) соединены друг с другом множеством перемычек, образуя окологлоточное нервное кольцо. От него отходят спинной и брюшной нервные стволы, соединенные поперечными перемычками - комиссурами.
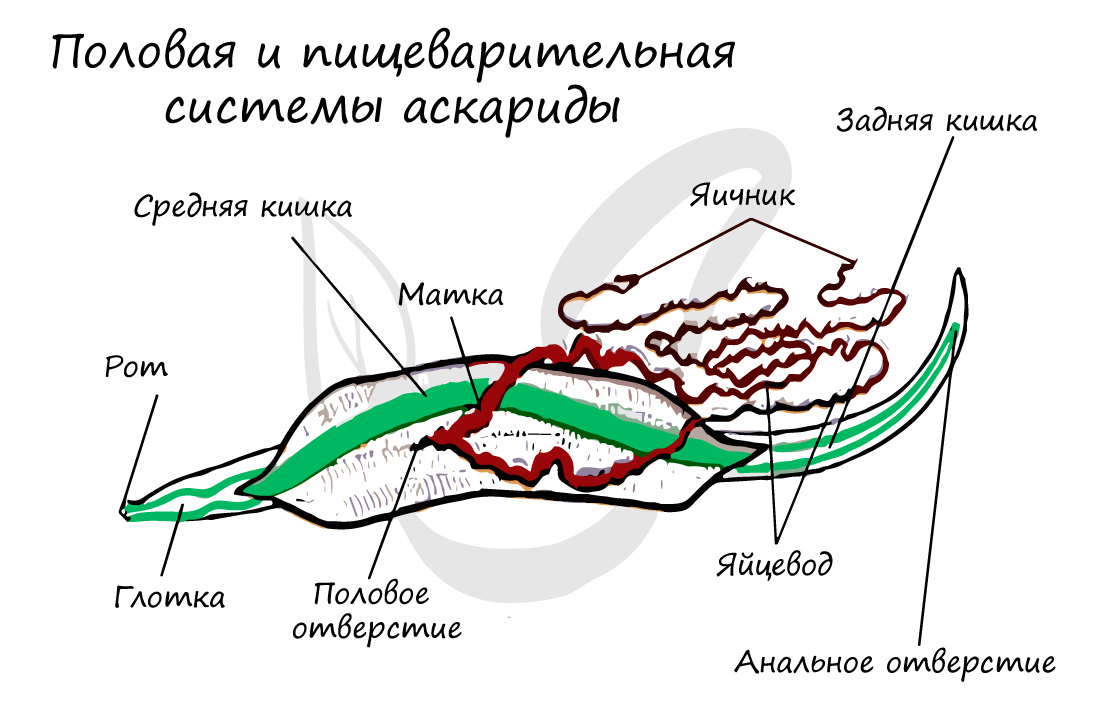
Пищеварительная система претерпевает резкие изменения: появляется задний отдел кишечника и впервые - анальное отверстие. Как вы помните, кишечнополостные и плоские черви из-за его отсутствия были вынуждены выделять непереваренные остатки пищи через рот - это эволюционно осталось позади. Теперь у пищеварительной системы появляется возможность функционировать непрерывно.
Продольная мускулатура дифференцируется (делится) на четыре мышечных тяжа: брюшной, спинной и два боковых. Благодаря такому строению становится возможным змеевидное движение.
Мужские половые органы находятся у мужских организмов, а женские - у женских. Это создает основу для комбинативного разнообразия потомства.
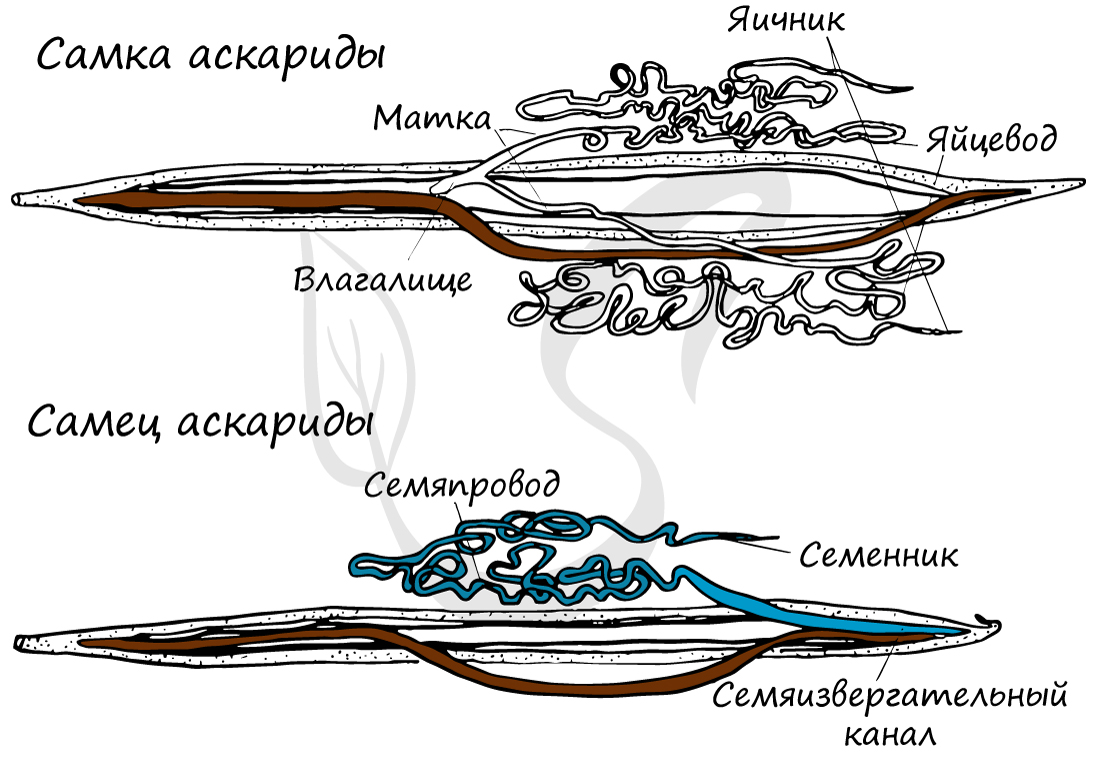
Обратите внимание (картинка ниже) - как хорошо у аскариды выражен половой диморфизм - это свойство имеется и у многих других представителей круглых червей. Половой диморфизм (от греч. di - две и morphe - формы) - внешние признаки различия между мужской и женской особью.
Общая характеристика
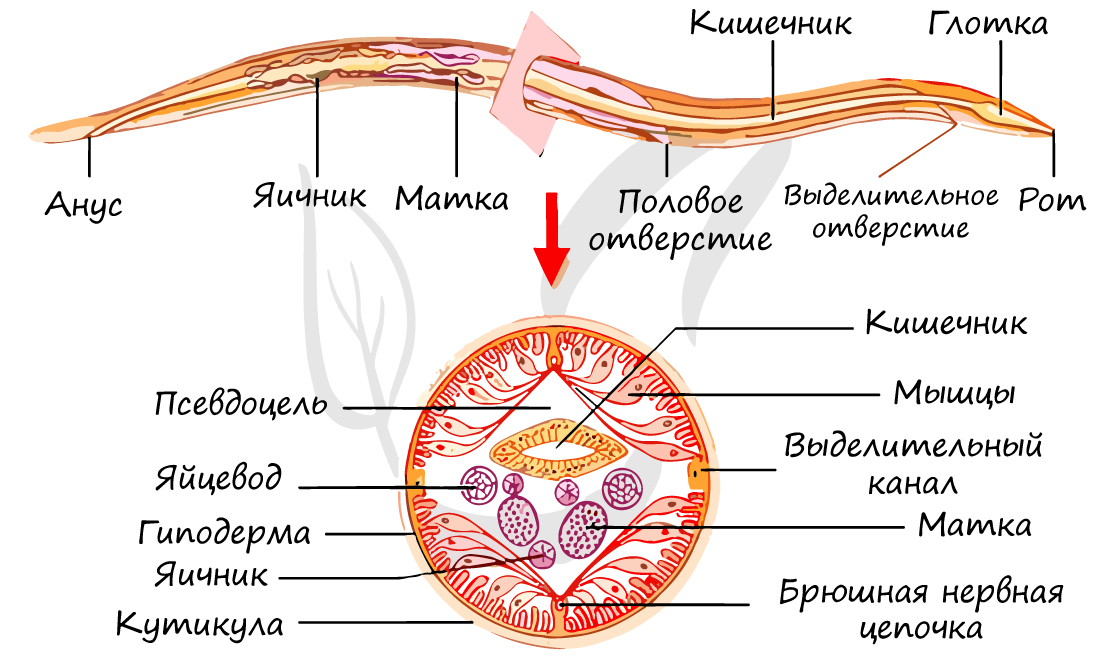
Покровные ткани кожно-мускульного мешка круглых червей представлены многослойной кутикулой и гиподермой. Кутикула (от лат. cuticula - кожица) - производное клеток однослойного покровного эпителия гиподермы. Представляет собой своеобразный "каркас" для мускулатуры. Важнейшая функция кутикулы - защита червя от переваривания ферментами кишечника, что дает возможность паразиту жить долгие годы в организме-хозяине.
Под кутикулой расположена гиподерма. Гиподерма имеет 4 протяженных утолщения, тянущихся вдоль всего тела - 4 гиподермальных валика: спинной, два боковых и брюшной. Под гиподермой располагаются тяжи продольных мышц.
Внутри кожно-мускульного мешка расположена первичная полость тела (псевдоцель), где помещаются все внутренние органы. Протоцель заполнена жидкостью под давлением и выполняет роль гидроскелета - опорную функцию, участвует в движении (жидкость несжимаема). Первичная полость тела выполняет также функцию транспортную (распределительную) - переносит вещества от кишечника к рабочим органам, в том числе - мышцам.
Начинается ротовой полостью, далее продолжается в пищевод, затем в переднюю, среднюю и заднюю кишку с анальным отверстием, открывающимся с брюшной стороны на заднем конце тела. Сквозная пищеварительная система обеспечивает возможность непрерывного питания.
Дыхание осуществляется всей поверхностью тела, у паразитов - анаэробное (бескислородное) дыхание.
Жидкие продукты обмена веществ удаляются через органы выделения - видоизмененные протонефридии (без мерцательного "пламени", которое было у плоских червей). По бокам тела имеются экскреторные боковые каналы, которые в передней части тела соединяются в общий выводной проток. Этот проток заканчивается порой на головном конце тела с брюшной стороны.
Помимо этого в коже имеется много мелких эпидермальных желез, связанных с экскреторными боковыми каналами. Функцией выделения обладают также особые клетки - фагоцитарные. Они накапливают в себе продукты обмена веществ и инородные тела, попавшие в полость тела. Фактически они не выделяют, а накапливают эти вещества, таким образом, удаляют их из организма.
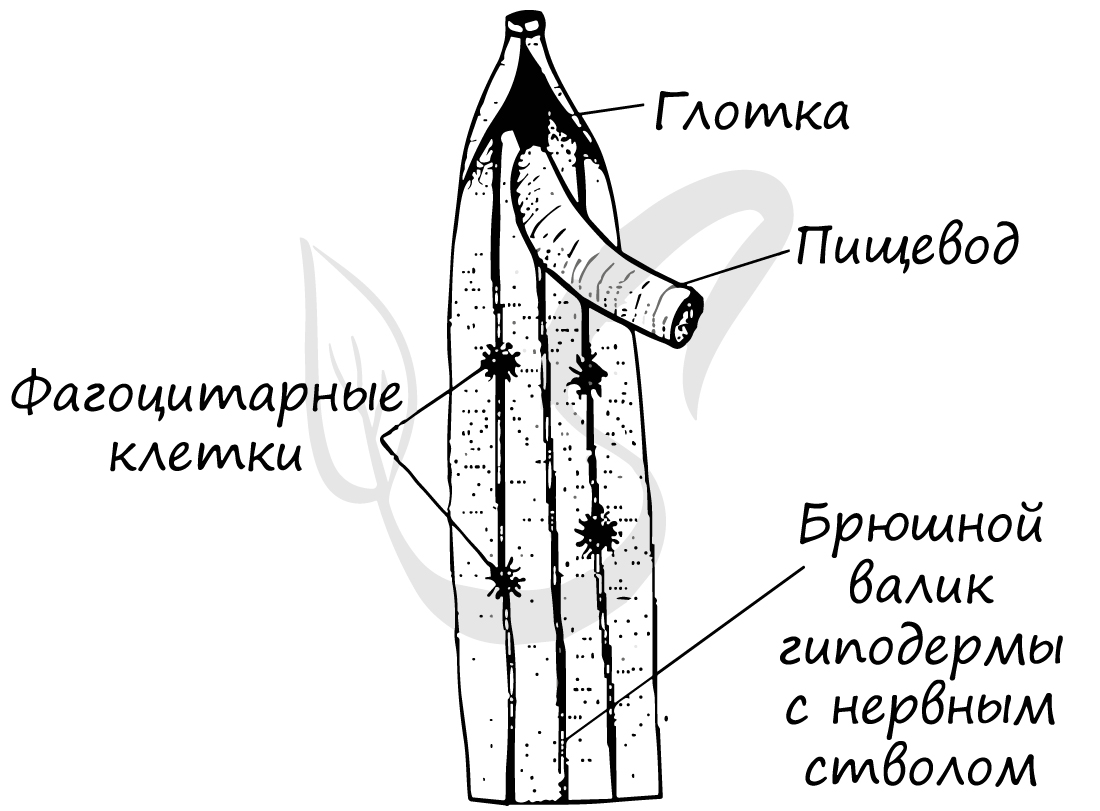
Нервная система круглых червей стволового (лестничного) типа, также называемая - ортогон. Состоит из окологлоточного нервного кольца, от которого отходят нервные стволы, из которых наиболее выделяются брюшной и спинной. Стволы соединены друг с другом поперечными тяжами - комиссурами.
Строение окологлоточного нервного кольца отражает единство всей его структуры - по сути это один большой круговой ганглий (нервный узел).
Круглые черви раздельнополы. Развитие прямое, у части паразитических форм присутствует стадия инвазионной личинки.
Женские половые органы представлены влагалищем, яичником, яйцеводом и маткой. Возможен парный набор женских половых органов, но влагалище всегда одно.
Мужская половая система состоит из семенников с семяпроводами, и единственного семяизвергательного канала. Спермии круглых червей (спермий отличается от сперматозоида отсутствием жгутика) имеют разнообразное строение и отличаются амебоидной подвижностью.
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Читайте также:

