Кто является возбудителем холеры кокки стафилококки бациллы или вибрионы
Обновлено: 18.04.2024
Биохимические свойства холеры. Биовары холеры. Антигены холеры. Антигенная структура холеры. Схемы Хайберга. Серогруппы холеры.
Холерные вибрионы сбраживают с образованием кислоты многие углеводы (глюкозу, сахарозу, мальтозу, маннит, лактозу, гликоген, крахмал и др.). Ферментация маннозы, сахарозы и арабинозы (так называемая триада Хёйберга) имеет диагностическое значение.
По способности разлагать эти три углевода все вибрионы холеры разделяют на 6 групп. Холерные вибрионы разлагают только маннозу и сахарозу и принадлежат к 1-й группе Хейберга.
Бактерии холеры этой группы обладают плазмокоагулирующим (свёртывают плазму кролика) и фибринолитическим (разжижают свёрнутую сыворотку по Леффлеру) свойствами.
Холерные вибрионы свёртывают молоко и разлагают другие белки и их дериваты до аммиака и индола; H2S не образуют, восстанавливают нитраты и образуют индол (эту способность учитывают в нитрозоиндоловой реакции, также известной как холера-рот реакция).
Бактерии серовара Бенгал устойчивы к полимиксину и не проявляют гемолитической активности.
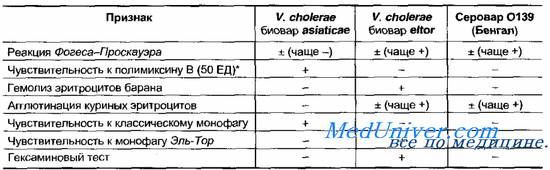
Таблица 18—4. Дифференциальные признаки возбудителей холеры
Антигены холеры. Антигенная структура холеры. Схемы Хайберга. Серогруппы холеры.
У холерных вибрионов выделяют термостабильные О- и термолабильные Н-Аг.
О-антигены. По структуре О-антигены выделяют 139 серогрупп; возбудители холеры относят к 01 группе. Принадлежность к ней отличает их от ходероподобных и парахолерных вибрионов.
Поэтому, несмотря на возможные биохимические различия, при исследовании на холеру обязательно проводят типирование 01-антисывороткой. О-Аг 01 группы холерных вибрионов неоднороден и включает А, В и С компоненты, разные сочетания которых присущи сероварам Огава (АВ). Инаба (АС) и Хикоджима (ABC).
Эти свойства используют в качестве эпидемиологического маркёра для дифференцирования очагов по возбудителям холеры, хотя иногда от одного больного можно выделить бактерии разных сероваров. R-формы, а также слизистые М-формы (с изменённой структурой О-Аг) не агглютинируются О-антисыворотками, для идентификации OR- и R-диссоциатов используют OR-антисыворотки.
Бактерии серовара холеры 0139 не агглютинируются видоспеиифической О1 и типоспецифическими Огава-, Инаба- и RO-сыворотками.
Поскольку холероподобные вибрионы также не агглютинируются 01-антисывороткой, их обозначают как неагглютинирующиесн (НАГ) вибрионы.
Н-антигены — общие антигены для большой группы бактерий, поэтому их разделяют на А и В группы. В группу А входят холерные вибрионы; в группу В — вибрионы, биохимически отличные от холерных. Вибрионы группы В имеют неоднородную структуру О-Аг, их разделяют на 6 серологических подгрупп, состав которых совпадает с разделением на 6 биохимических групп схемы Хайберга.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Холера (cholera) — острая кишечная антропонозная инфекция с фекально-оральным механизмом передачи возбудителя, для которой характерно развитие острого гастроэнтерита с нарушением водно-электролитного баланса с быстрым развитием обезвоживания. Относится к
Холера (cholera) — острая кишечная антропонозная инфекция с фекально-оральным механизмом передачи возбудителя, для которой характерно развитие острого гастроэнтерита с нарушением водно-электролитного баланса с быстрым развитием обезвоживания. Относится к особо опасным конвенционным болезням.
В России отмечается стабилизация эпидемического процесса с 1988 г. и заболевания холерой носят в основном завозной и спорадический характер. За последние 20 лет выявлено более 100 случаев завоза в семь регионов страны. Тяжелой была эпидемия холеры в Дагестане в 1994 г., когда в результате заноса заболевания паломниками, которые совершали хадж в Саудовскую Аравию, заболело 2359 человек.
Этиология. Возбудитель холеры Vibrio cholerae — относится к роду Vibrio, семейства Vibrionaceae, серогруппа 01 биоваров cholerae (классический и eltor). В последние годы до 80% всех случаев холеры были вызваны вибрионом Эль-Тор. По антигенной структуре вибрионы холеры подразделяются на три серовара: Инаба, Огава и Гикошима. Холерный вибрион имеет форму запятой, благодаря наличию жгутика обладает хорошей подвижностью, аэроб, спор не образует, грамотрицателен, способен к очень быстрому размножению, оптимальная температура роста 37 °C. Хорошо растет на питательных средах, имеющих слабощелочную реакцию, разжижает желатин, разлагает крахмал, образует индол, восстанавливает нитраты в нитриты, лизируется специфическими фагами. Из факторов патогенности наибольшее значение имеет экзотоксин — холероген. Возбудитель содержит также эндотоксин, имеющий ведущую роль в развитии постинфекционного иммунитета. Вибрион погибает при кипячении, хорошо переносит низкие температуры и замораживание. Под влиянием света, воздуха и при высушивании холерные вибрионы гибнут в течение нескольких дней. Холерный вибрион чувствителен к хлорсодержащим дезинфицирующим средствам. В воде поверхностных водоемов, иле и в opганизме некоторых гидробионтов возбудитель не только длительно сохраняется, но и размножается. Штаммы, которые циркулируют во внешней среде, слабо вирулентны. На пищевых продуктах вибрионы сохраняются в течение 2–5 дней, на помидорах и арбузах под действием солнечного света вибрионы погибают через 8 ч. Заражение возможно при употреблении рыбы, раков, креветок, устриц, выловленных в загрязненных водоемах и не подвергшихся термической обработке. Вибрионы длительно сохраняются в открытых водоемах, в которые стекают канализационные воды и когда вода прогревается более 17 °С.
В последние годы регистрируются вспышки диарейных заболеваний, которые вызываются холерными вибрионами не О1, а О139 серогруппы. Течение заболевания по своим клинико-эпидемиологическим особенностям не отличается от холеры. Эксперты ВОЗ полагают, что распространение заболеваний, вызванных холерным вибрионом О139, становится реальной угрозой, идентичной той, что произошла с вибрионом Эль-Тор в 1961 г. Вибрионы по отношению к холерным фагам подразделяются на пять основных фаготипов. Отмечаются вибрионы, которые не агглютинируются поливалентной холерной сывороткой О, так называемые НАГ-вибрионы, которые по морфологическим и культуральным признакам, а также по ферментативной активности не отличаются от холерных вибрионов, имеют одинаковый с ними Н-антиген, но относящийся к другим О-группам. В настоящее время установлено свыше 60 серологических О-групп НАГ-вибрионов. Эти вибрионы могут вызывать холероподобные заболевания.
Эпидемиология. Источником инфекции являются больные типичной или стертой формой холеры, вибриононосители (реконвалесцентные, острые, хронические). Возбудитель выделяется в окружающую среду с испражнениями, особенно лицами с типичной формой болезни в первые 4–5 суток. Больные стертыми, атипичными формами болезни опасны благодаря активному образу жизни и контактам с окружающими. В этом же состоит и эпидемическая опасность вибриононосителей, однако хроническое носительство формируется крайне редко.
Механизм передачи — фекально-оральный, основной путь передачи — водный, реже пищевой и контактно-бытовой. Имеет значение не только употребление контаминированной возбудителем воды, но и использование ее для мытья посуды, овощей, фруктов, купание в загрязненных водоемах. Холера имеет склонность к эпидемическому распространению. Вспышки чаще возникают в теплое время года.
Восприимчивость человека к холере высокая. Чаще подвержены заболеванию лица с пониженной кислотностью желудочного сока, некоторыми формами анемии, глистными инвазиями и алкоголизмом. После перенесенного заболевания формируется типоспецифический антимикробный и антитоксический иммунитет, который сохраняется в течение одного года.
Патогенез и патоморфология. Возбудитель проникает в организм человека с инфицированной пищей или водой, преодолевает кислотный барьер, чему способствуют заболевания желудка, которые сопровождаются пониженной кислотностью. Наиболее тяжело протекает холера у лиц, злоупотребляющих алкоголем или перенесших резекцию желудка. В слабощелочной среде тонкой кишки вибрион адгезируется на кайме эпителиоцитов и размножается. Адгезируясь на энтероцитах, холерные вибрионы используют ферментные звенья последних для генерирования энергии синтеза собственных структур. До сих пор остается спорным вопрос, приводит ли сама по себе адгезия к кишечной секреции. Исследования с рекомбинантными, аттенуированными штаммами холерного вибриона, разработанными с целью получения оральных вакцин, показали, что эти штаммы хорошо адгезируются, но не вызывают диареи. Холерные вибрионы размножаются и выделяют холерный токсин. Различают три токсические субстанции: 1) эндотоксин (липополисахарид); 2) экзотоксин (холероген); 3) фактор проницаемости. Описаны также другие токсины холерного вибриона: zot, оказывающий влияние на плотные соединения клеток и регулирующих их проницаемость, а также добавочный токсин ace, вызывающий увеличение тока короткого замыкания в камере Юссинга. Вероятно, это токсин-блокатор натриевого насоса, о котором сообщал Филлипс еще в 60-х годах. Выявлено расположение генов этих токсинов на фрагменте хромосомы. В основе клинических проявлений холеры лежит синдром электролитной диареи. Развитие диареи заключается в гиперсекреторных процессах, которые обусловлены активацией фермента аденилатциклазы в эпителиальных клетках тонкой кишки под действием холерогена и накоплением цАМФ, приводящего к повышенной секреции воды и электролитов в просвет кишки. В исследованиях (D. Powelletal., 1994; CSeurs. G. Kaper., 1996) подробно описаны биохимические свойства и биологическое действие холерного токсина. Через систему циклических нуклеотидов он стимулирует секрецию хлора, тормозит абсорбцию эпителиоцитами электронейтрального хлористого натрия и модулирует их цитоскелет (микротрубочки), вызывает накопление внутриклеточного кальция. Это, в свою очередь, определяет повышение секреторного ответа, так как кальций стимулирует образование циклических нуклеотидов. Кальций и белок кальмодулин активируют фосфолипазу, которая вызывает фосфорилирование протеинов с увеличением проницаемости апикальных мембран энтероцитов крипт, что приводит к гиперсекреции воды и электролитов. На увеличение синтеза циклических нуклеотидов влияют брадикинин, каллидин, вазоактивный интестинальный пептид. Доказано, что диарея возникает также за счет высвобождения серотонина, который в свою очередь стимулирует образование простагландина Е2. Роль серотонина в качестве важнейшего медиатора гиперсекреции в тонкой кишке при действии холерного токсина доказывается успешным применением антогонистов серотониновых рецепторов. При холере имеет место изотоническое обезвоживание. По современным представлениям, холерная диарея обусловлена усилением секреции кишечного сока (ионов натрия, бикарбоната, калия хлора воды), ускорением физиологической десквамации энтероцитов, повышением проницаемости мембран, а также замедлением обратного всасывания ионов натрия, хлора и воды. У больных отмечаются: тяжелый метаболический ацидоз, сгущение крови, повышение ее удельного веса, ухудшение реологических свойств крови, гипокалиемия, повышение содержания белка и др. Потери жидкости с испражнениями и рвотными массами за короткий срок могут достигать объемов, которые не встречаются при диареях другой этиологии. Как следствие дегидратации развиваются значительная гемоконцентрация, гиповолемия, гипоксия, тромбогеморрагический синдром и острая почечная недостаточность. Включаются дополнительные механизмы защиты от обезвоживания и потери электролитов:
а) снижение температуры тела — это приводит к уменьшению естественной перспирации (в сутки теряется около 1,5 литров пота вместе с натрием, калием и другими электролитами);
б) появляется сухость слизистых оболочек рта, глаз, мочеполовых органов (снижена секреция всех желез);
в) развивается олигурия вплоть до анурии.
Однако эти механизмы защиты не спасают, так как коварство холерного вибриона в том, что его токсин (холероген), соединившись с рецепторами эпителиоцитов, вызывает продолжительную гиперсекрецию жидкости и электролитов из крипт тонкого кишечника в течение 18–24 часов. За этот период организм без лечения (регидратации) погибает.
Методом оптической и электронной микроскопии выявлены функциональные изменения в структурах сердца, почек, надпочечников, гипоталамических ядер и гипофиза. Однако все эти изменения являются вторичными, регуляторными, защитными и направлены на восстановление водно-солевого гомеостаза. Эти нарушения при холере никак не связаны с прямым токсическим влиянием на структуры внутренних органов, а обусловлены дегидратацией.
Именно такой подход к пониманию патогенеза холеры — признание первичности дегидратации и дисбаланса электролитов — позволил разработать патогенетическую регидратационную терапию, которая направлена на устранение основной причины патологии.
У 80% людей холера протекает в легкой или умеренной форме. У 10–20% людей развивается тяжелая водянистая диарея с признаками дегидратации. В соответствии с классификацией холеры В. И. Покровского различают четыре степени обезвоживания: I степень предполагает потерю жидкости до 3% от массы тела, II степень — 4–6%, III степень — 7–9%, IV степень (декомпенсированное обезвоживание) — 10% и более.
Обезвоживание I степени выявляется наиболее часто, при этом многие симптомы болезни не выражены и заболевание носит абортивный характер. У некоторых больных отмечается продромальный период продолжительностью около суток, для которого характерны головокружение, недомогание, слабость, тошнота. Первым симптомом болезни является нарушение стула, который у 2/3 больных бывает водянистым и у 1/3 — кашицеобразным. У 5% больных стул может быть оформленным. Частота диареи от 5 до 10 раз в сутки. Длительность заболевания не более 3 суток. Испражнения не обильные. Рвота может быть примерно у половины заболевших. Кожа влажная, тургор сохранен. У 2/3 больных выявляется сухость слизистой оболочки рта. Нарушений гемодинамики нет.
Обезвоживание II степени регистрируется примерно у 20% больных. В большинстве случаев заболевания продромальный период либо не выражен, либо кратковременный. Заболевание характеризуется появлением жидкого стула, который быстро становится водянистым и у половины больных напоминает рисовый отвар. Рвота присоединяется в первые часы болезни, частота ее достигает до 10 раз в сутки. Общая потеря жидкости при II степени дегидратации в среднем составляет 5–6 л. Симптомы обезвоживания развиваются быстро. Характерны слабость, головокружение, обмороки, сухость во рту, жажда, осиплость голоса, снижение тургора кожи. У четверти больных отмечаются цианоз и акроцианоз. Температура тела нормальная либо субнормальная. Повышение температуры тела выявляется редко. Язык сухой. У половины больных отмечается тахикардия, у четверти — артериальная гипотония, в отдельных случаях олигурия. У некоторых больных появляются судороги икроножных мышц, кистей и стоп. При исследовании крови признаки гемоконцентрации минимальные (Ht = 0,46–0,50) вследствие компенсаторного разжижения крови. Электролитные изменения носят компенсированный характер. Чаще всего отмечаются компенсированный или субкомпенсированный метаболический ацидоз (рН 7,36–7,40; BE = -2,0–5,0 ммоль/л), гипокалиемия, гипохлоремия.
Голос изменен, осипший и ослаблен, характерна речь шепотом. Тоны сердца глухие, отмечаются тахикардия и артериальная гипотония. В 3/4 случаев имеет место олигурия, в 1/4 — анурия. Умеренно выражена гемоконцентрация (Ht = 0,50–0,55), отмечаются декомпенсированный метаболический ацидоз (рН 7,30–7,36; BE = -0,5–10,0 ммоль/л), гипокалиемия, гипохлоремия. Состояние больных при отсутствии интенсивной терапии ухудшается и может привести к летальному исходу.
Иногда возможно еще более быстрое развитие дегидратации. В этих случаях дегидратационный шок развивается в течение нескольких часов (одних суток), и такую форму заболевания называют молниеносной.
Сухая холера протекает без диареи и рвоты, но с признаками быстрого развития гиповолемического шока — резким падением артериального давления, развитием тахипноэ, одышки, судорог, афонии, анурии.
Наиболее тяжелое течение холеры наблюдается у детей до 3 лет. Дети хуже переносят обезвоживание, и у них возникает вторичное поражение центральной нервной системы (заторможенность, клонические судороги, конвульсии, нарушение сознания вплоть до развития комы). У детей трудно определить первоначальную степень дегидратации. Нельзя ориентироваться на относительную плотность плазмы вследствие относительно большого внеклеточного объема жидкости. Поэтому целесообразно при поступлении взвешивать детей для наиболее достоверного определения у них степени обезвоживания. Течение холеры у детей имеет некоторые особенности: частое повышение температуры тела, более выраженные апатия, адинамия, склонность к эпилептиформным припадкам, так как быстро развивается гипокалиемия. Заболевание длится от 3 до 10 дней, последующие проявления его зависят от адекватности регидратационной терапии. При возмещении потерь жидкости и электролитов нормализация физиологических функций происходит достаточно быстро и летальные исходы встречаются редко. Основные причины смерти при неадекватном лечении больных — это дегидратационный шок, метаболический ацидоз и уремия в результате острого некроза канальцев.
Наряду с тяжелым течением заболевания возможны стертые и субклинические формы болезни, которые выявляются при детальном обследовании носителей. В анамнезе у таких больных кратковременная диарея, стул 1–2 раза в сутки. Больных с субклинической формой заболевания выявляют в очагах холеры при обнаружении возбудителя в испражнениях, клинических симптомов заболевания у них нет, но при исследовании крови выявляется нарастание титра вибриоидных антител.
Осложнения. Среди осложнений, обусловленных нарушениями кровообращения регионарного характера: инфаркт миокарда, тромбоз мезентериальных сосудов, острое нарушение мозгового кровообращения. Частым осложнением является пневмония, очаговая или сегментарная, у лиц старческого возраста — гипостатическая. К осложнениям надо отнести острую почечную недостаточность с преобладанием преренальной формы. Эксикоз способствует развитию абсцессов, флегмон и рожи. Флебиты и тромбофлебиты обусловлены длительной внутривенной регидратационной терапией.
Основным методом лабораторной диагностики холеры является бактериологическое исследование испражнений и рвотных масс с целью выделения возбудителя. Если невозможно доставить материал в лабораторию в первые 3 ч после взятия, то используют среды-консерванты (щелочная 1% пептонная вода и др.). Материал собирают в индивидуальные отмытые от дезинфицирующих растворов судна, на дно которых помещают меньший по размерам, обеззараженный кипячением, сосуд или листы пергаментной бумаги. Выделения (10–20 мл) с помощью металлических ложек собирают в стерильные стеклянные банки или пробирки, закрывающиеся плотной пробкой. У больных гастроэнтеритом можно брать материал из прямой кишки при помощи резинового катетера. Для активного взятия материала используют ректальные ватные тампоны, трубки.
При обследовании реконвалесцентов и здоровых лиц, контактировавших с источниками инфекции, предварительно дают солевое слабительное (20–30 г магния сульфата). Все пробы для исследования доставляют в стерильной герметизированной посуде с сопровождающим. Каждый образец сопровождается направлением, в котором указывают имя и фамилию больного, название образца, место и время взятия, предполагаемый диагноз и фамилию забравшего материал. Ориентировочным тестом является микроскопия фиксированных окрашенных мазков испражнений и рвотных масс. Скопления вибрионов имеют вид стаек рыб. Ускоренными методами исследования являются иммунофлуоресцентная микроскопия, метод раздавленной капли. Материалом исследования служат испражнения, рвотные массы, порции В и С желчи, секционный материал, вода, пища и другие объекты внешней среды. Для выделения и идентификации чистой культуры используют среды обогащения, элективные и дифференциально-диагностические среды. Результаты экспресс-исследования получают через 2–6 ч (ориентировочный ответ), ускоренного анализа через 8–22 ч (предварительный ответ), полного анализа через 36 ч (окончательный ответ). Используются в качестве ускоренных методов диагностики иммобилизация и микроагглютинация вибрионов холерной сывороткой, ответ получают через несколько минут. Все эти исследования проводятся комплексно. Применяются серологические исследования крови (реакция нейтрализации, иммуноферментный анализ) у больных с типичной клинической картиной холеры, если холерный вибрион из кала и рвотных масс не выделяется. Определяют титры агглютининов, вибриоцидных антител и антитоксинов. При наличии титров антител (агглютининов 1:40, вибриоцидных антител 10–4, антиэнтеротоксинов — 30 антитоксических ед., антимембранотоксинов — 50 антитоксических ед.) следует заподозрить холеру. Положительным является результат при нарастании титров антител в парных сыворотках в 4 раза. Серологические методы исследования являются второстепенными и используются для ретроспективной диагностики.
Наличие Vibrio cholerae в кале подтверждается с помощью проведения лабораторных исследований. Применение нового диагностического экспресс-теста (ДЭТ) позволяет быстро тестировать пациентов. ДЭТ в настоящее время находится в процессе утверждения ВОЗ с целью его включения в перечень предварительно квалифицированных продуктов. В то же время, в случае положительных результатов ДЭТ, ВОЗ предлагает проводить повторное тестирование всех образцов, используя классические лабораторные методы исследования для подтверждения. Если вспышка болезни подтверждена, то достаточно проводить клиническое диагностирование на основе стандартного определения случая заболевания ВОЗ с дополнительным проведением тестирования в отдельных случаях заболевания с регулярными интервалами.
Г. К. Аликеева, кандидат медицинских наук
Н. Д. Ющук, доктор медицинских наук, профессор, академик РАМН
Н. Х. Сафиуллина, кандидат медицинских наук
А. В. Сундуков, доктор медицинских наук, профессор
Г. М. Кожевникова, доктор медицинских наук, профессор
МГМСУ, Москва
Что понимают под дисбактериозом? Какие методы диагностики являются современными и достоверными? Какие лекарственные препараты применяются при дисбактериозе? Вкишечнике человека находится свыше 500 различных видов микробов, общее количество которых
Что понимают под дисбактериозом?
Какие методы диагностики являются современными и достоверными?
Какие лекарственные препараты применяются при дисбактериозе?
Вкишечнике человека находится свыше 500 различных видов микробов, общее количество которых достигает 10 14 , что на порядок выше общей численности клеточного состава человеческого организма. Количество микроорганизмов увеличивается в дистальном направлении, и в толстой кишке в 1 г кала содержится 10 11 бактерий, что составляет 30% сухого остатка кишечного содержимого.
Нормальная микробная флора кишечника
В тощей кишке здоровых людей находится до 10 5 бактерий в 1 мл кишечного содержимого. Основную массу этих бактерий составляют стрептококки, стафилококки, молочнокислые палочки, другие грамположительные аэробные бактерии и грибы. В дистальном отделе подвздошной кишки количество микробов увеличивается до 10 7 –10 8 , в первую очередь за счет энтерококков, кишечной палочки, бактероидов и анаэробных бактерий. Недавно нами было установлено, что концентрация пристеночной микрофлоры тощей кишки на 6 порядков выше, чем в ее полости, и составляет 10 11 кл/мл. Около 50% биомассы пристеночной микрофлоры составляют актиномицеты, примерно 25% — аэробные кокки (стафилококки, стрептококки, энтерококки и коринеформные бактерии), от 20 до 30% приходится на бифидобактерии и лактобациллы.
Количество анаэробов (пептострептококки, бактероиды, клостридии, пропионобактерии) составляет около 10% в тонкой и до 20% в толстой кишке. На долю энтеробактерий приходится 1% от суммарной микрофлоры слизистой оболочки.
До 90-95% микробов в толстой кишке составляют анаэробы (бифидобактерии и бактероиды), и только 5-10% всех бактерий приходится на строгую аэробную и факультативную флору (молочнокислые и кишечные палочки, энтерококки, стафилококки, грибы, протей).
Кишечные палочки, энтерококки, бифидобактерии и ацидофильные палочки обладают выраженными антагонистическими свойствами. В условиях нормально функционирующего кишечника они способны подавлять рост несвойственных нормальной микрофлоре микроорганизмов.
Площадь внутренней поверхности кишечника составляет около 200 м 2 . Она надежно защищена от проникновения пищевых антигенов, микробов и вирусов. Важную роль в организации этой защиты играет иммунная система организма. Около 85% лимфатической ткани человека сосредоточено в стенке кишечника, где продуцируется секреторный IgA. Кишечная микрофлора стимулирует иммунную защиту. Кишечные антигены и токсины кишечных микробов значительно увеличивают секрецию IgA в просвет кишки.
Расщепление непереваренных пищевых веществ в толстой кишке осуществляется ферментами бактерий, при этом образуются разнообразные амины, фенолы, органические кислоты и другие соединения. Токсические продукты микробного метаболизма (кадаверин, гистамин и другие амины) выводятся с мочой и в норме не оказывают влияния на организм. При утилизации микробами неперевариваемых углеводов (клетчатки) образуются короткоцепочечные жирные кислоты. Они обеспечивают клетки кишки энергоносителями и, следовательно, улучшают трофику слизистой оболочки. При дефиците клетчатки может нарушаться проницаемость кишечного барьера вследствие дефицита короткоцепочечных жирных кислот. В результате кишечные микробы могут проникать в кровь.
Под влиянием микробных ферментов в дистальных отделах подвздошной кишки происходит деконъюгация желчных кислот и преобразование первичных желчных кислот во вторичные. В физиологических условиях от 80 до 95% желчных кислот реабсорбируется, остальные выделяются с фекалиями в виде бактериальных метаболитов. Последние способствуют нормальному формированию каловых масс: тормозят всасывание воды и тем самым препятствуют излишней дегидратации кала.
Дисбактериоз
В понятие дисбактериоза кишечника входит избыточное микробное обсеменение тонкой кишки и изменение микробного состава толстой кишки. Нарушение микробиоценоза происходит в той или иной степени у большинства больных с патологией кишечника и других органов пищеварения. Следовательно, дисбактериоз является бактериологическим понятием. Он может рассматриваться как одно из проявлений или осложнение заболевания, но не самостоятельная нозологическая форма.
Крайней степенью дисбактериоза кишечника является появление бактерий желудочно-кишечного тракта в крови (бактериемия) или даже развитие сепсиса.
Состав микрофлоры кишечника нарушается при болезнях кишечника и других органов пищеварения, лечении антибиотиками и иммунодепрессантами, воздействиях вредных факторов внешней среды.
Клинические проявления дисбактериоза зависят от локализации дисбиотических изменений.
Дисбактериоз тонкой кишки
При дисбактериозе тонкой кишки численность одних микробов в слизистой оболочке тонкой кишки увеличена, а других уменьшена. Отмечается увеличение Eubacterium (в 30 раз), α-стрептококков (в 25 раз), энтерококков (в 10 раз), кандид (в 15 раз), появление бактерий рода Acinetobacter и вирусов герпеса. Уменьшается от 2 до 30 раз количество большинства анаэробов, актиномицетов, клебсиелл и других микроорганизмов, являющихся естественными обитателями кишечника.
Причиной дисбактериоза могут быть: а) избыточное поступление микроорганизмов в тонкую кишку при ахилии и нарушении функции илеоцекального клапана; б) благоприятные условия для развития патологических микроорганизмов в случаях нарушения кишечного пищеварения и всасывания, развития иммунодефицита и нарушений проходимости кишечника.
Повышенная пролиферация микробов в тонкой кишке приводит к преждевременной деконъюгации желчных кислот и потере их с калом. Избыток желчных кислот усиливает моторику толстой кишки и вызывает диарею и стеаторею, а дефицит желчных кислот приводит к нарушению всасывания жирорастворимых витаминов и развитию желчнокаменной болезни.
Бактериальные токсины и метаболиты, например фенолы и биогенные амины, могут связывать витамин В12.
Некоторые микроорганизмы обладают цитотоксическим действием и повреждают эпителий тонкой кишки. Это ведет к уменьшению высоты ворсинок и углублению крипт. При электронной микроскопии выявляется дегенерация микроворсинок, митохондрий и эндоплазматической сети.
Дисбактериоз толстой кишки
Состав микрофлоры толстой кишки может меняться под влиянием различных факторов и неблагоприятных воздействий, ослабляющих защитные механизмы организма (экстремальные климатогеографические условия, загрязнение биосферы промышленными отходами и различными химическими веществами, инфекционные заболевания, болезни органов пищеварения, неполноценное питание, ионизирующая радиация).
В развитии дисбактериоза толстой кишки большую роль играют ятрогенные факторы: применение антибиотиков и сульфаниламидов, иммунодепрессантов, стероидных гормонов, рентгенотерапия, хирургические вмешательства. Антибактериальные препараты значительно подавляют не только патогенную микробную флору, но и рост нормальной микрофлоры в толстой кишке. В результате размножаются микробы, попавшие извне, или эндогенные виды, устойчивые к лекарственным препаратам (стафилококки, протей, дрожжевые грибы, энтерококки, синегнойная палочка).
Клинические особенности дисбактериоза
Клинические проявления чрезмерного роста микроорганизмов в тонкой кишке могут полностью отсутствовать, выступать в качестве одного из патогенетических факторов хронической рецидивирующей диареи, а при некоторых болезнях, например, дивертикулезе тонкой кишки, частичной кишечной непроходимости или после хирургических операций на желудке и кишечнике, приводить к тяжелой диарее, стеаторее и В 12 -дефицитной анемии.
Особенностей клинического течения заболевания у больных с различными вариантами дисбактериоза толстой кишки, по данным бактериологических анализов кала, в большинстве случаев установить не удается. Можно отметить, что больные хроническими заболеваниями кишечника чаще инфицируются острыми кишечными инфекциями по сравнению со здоровыми. Вероятно, это связано со снижением у них антагонистических свойств нормальной микрофлоры кишечника и, прежде всего, частым отсутствием бифидобактерий.
Особенно большую опасность представляет псевдомембранозный колит, развивающийся у некоторых больных, длительно лечившихся антибиотиками широкого спектра действия. Этот тяжелый вариант дисбактериоза вызывается токсинами, выделяемыми синегнойной палочкой Clostridium difficile, которая размножается в кишечнике при угнетении нормальной микробной флоры.
Очень редко наблюдается молниеносное течение псевдомембранозного колита, напоминающее холеру. Обезвоживание развивается в течение нескольких часов и заканчивается летальным исходом.
Таким образом, оценка клинической значимости дисбиотических изменений должна основываться прежде всего на клинических проявлениях, а не только на результатах исследования микрофлоры кала.
Методы диагностики
Диагностика дисбактериоза представляет собой сложную и трудоемкую задачу. Для диагностики дисбактериоза тонкой кишки применяют посев сока тонкой кишки, полученного с помощью стерильного зонда. Дисбактериоз толстой кишки выявляют с помощью бактериологических исследований кала.
Микробная флора образует большое количество газов, в том числе водорода. Это явление используют для диагностики дисбактериоза. Концентрация водорода в выдыхаемом воздухе натощак находится в прямой зависимости от выраженности бактериального обсеменения тонкой кишки. У больных с заболеваниями кишечника, протекающими с хронической рецидивирующей диареей и бактериальным обсеменением тонкой кишки, концентрация водорода в выдыхаемом воздухе значительно превышает 15 ppm.
Для диагностики дисбактериоза применяют также нагрузку лактулозой. В норме лактулоза не расщепляется в тонкой кишке и метаболизируется микробной флорой толстой кишки. В результате количество водорода в выдыхаемом воздухе повышается (рис. 1).
Наиболее частыми бактериологическими признаками дисбактериоза толстой кишки являются отсутствие основных бактериальных симбионтов — бифидобактерий и уменьшение количества молочнокислых палочек. Увеличивается количество кишечных палочек, энтерококков, клостридий, стафилококков, дрожжеподобных грибов и протея. У отдельных бактериальных симбионтов появляются патологические формы. К ним относятся гемолизирующая флора, кишечные палочки со слабо выраженными ферментативными свойствами, энтеропатогенные кишечные палочки и т. д.
Углубленное изучение микробиоценоза показало, что традиционные методы не позволяют получить истинную информацию о состоянии микрофлоры кишечника. Из 500 известных видов микробов в целях диагностики обычно изучаются лишь 10-20 микроорганизмов. Важно, в каком отделе — в тощей, подвздошной или толстой кишках — исследуется микробный состав. Поэтому перспективы разработки клинических проблем дисбактериоза в настоящее время связывают с применением химических методов дифференциации микроорганизмов, позволяющих получить универсальную информацию о состоянии микробиоценоза. Наиболее широко для этих целей используются газовая хроматография (ГХ) и газовая хроматография в сочетании с масс-спектрометрией (ГХ-МС). Этот метод позволяет получить уникальную информацию о составе мономерных химических компонентов микробной клетки и метаболитов. Маркеры такого рода могут быть определены и использованы для детектирования микроорганизмов. Главным преимуществом и принципиальным отличием этого метода от бактериологических является возможность количественного определения более 170 таксонов клинически значимых микроорганизмов в различных средах организма. При этом результаты исследования могут быть получены в течение нескольких часов.
Проведенные нами исследования микробиоценоза в крови и биоптатов слизистой оболочки тонкой и толстой кишок у больных с синдромом раздраженного кишечника позволили обнаружить отклонения от нормы до 30-кратного увеличения или уменьшения многих компонентов. Существует возможность оценки изменений микрофлоры кишечника на основании данных анализа крови методом ГХ-МС-микробных маркеров.
Лечение
Лечение дисбактериоза должно быть комплексным (схема) и включать в себя следующие мероприятия:
- устранение избыточного бактериального обсеменения тонкой кишки;
- восстановление нормальной микробной флоры толстой кишки;
- улучшение кишечного пищеварения и всасывания;
- восстановление нарушенной моторики кишечника;
- стимулирование реактивности организма.
Антибактериальные препараты
Антибактериальные препараты необходимы в первую очередь для подавления избыточного роста микробной флоры в тонкой кишке. Наиболее широко применяются антибиотики из группы тетрациклинов, пенициллинов, цефалоспорины, хинолоны (таривид, нитроксолин) и метронидазол.
Однако антибиотики широкого спектра действия в значительной степени нарушают эубиоз в толстой кишке. Поэтому они должны применяться только при заболеваниях, сопровождающихся нарушениями всасывания и моторики кишечника, при которых, как правило, отмечается выраженный рост микробной флоры в просвете тонкой кишки.
Антибиотики назначают внутрь в обычных дозах в течение 7–10 дней.
При заболеваниях, сопровождающихся дисбактериозом толстой кишки, лечение лучше проводить препаратами, которые оказывают минимальное влияние на симбионтную микробную флору и подавляют рост протея, стафилококков, дрожжевых грибов и других агрессивных штаммов микробов. К ним относятся антисептики: интетрикс, эрсефурил, нитроксолин, фуразолидон и др.
При тяжелых формах стафилококкового дисбактериоза применяют антибиотики: таривид, палин, метронидазол (трихопол), а также бисептол-480, невиграмон.
Антибактериальные препараты назначают в течение 10–14 дней. В случае появления в кале или кишечном соке грибов показано применение нистатина или леворина.
У всех больных с диареей, ассоциированной с антибиотиками, протекающей с интоксикацией и лейкоцитозом, возникновение острой диареи следует связывать с Cl. difficile.
В этом случае срочно делают посев кала на Cl. difficile и назначают ванкомицин по 125 мг внутрь 4 раза в сутки; при необходимости доза может быть увеличена до 500 мг 4 раза в день. Лечение продолжают в течение 7-10 суток. Эффективен также метронидазол в дозе 500 мг внутрь 2 раза в сутки, бацитрацин по 25 000 МЕ внутрь 4 раза в сутки. Бацитрацин почти не всасывается, в связи с чем в толстой кишке можно создать более высокую концентрацию препарата. При обезвоживании применяют адекватную инфузионную терапию для коррекции водно-электролитного баланса. Для связывания токсина Cl. difficile используют холестирамин (квестран).
Бактериальные препараты
Живые культуры нормальной микробной флоры выживают в кишечнике человека от 1 до 10% от общей дозы и способны в какой-то мере выполнять физиологическую функцию нормальной микробной флоры. Бактериальные препараты можно назначать без предварительной антибактериальной терапии или после нее. Применяют бифидумбактерин, бификол, лактобактерин, бактисубтил, линекс, энтерол и др. Курс лечения длится 1-2 месяца.
Возможен еще один способ устранения дисбактериоза — воздействие на патогенную микробную флору продуктами метаболизма нормальных микроорганизмов. К таким препаратам относится хилак форте. Он создан 50 лет назад и до настоящего времени применяется для лечения больных с патологией кишечника. Хилак форте представляет собой стерильный концентрат продуктов обмена веществ нормальной микрофлоры кишечника: молочной кислоты, лактозы, аминокислот и жирных кислот. Эти вещества способствуют восстановлению в кишечнике биологической среды, необходимой для существования нормальной микрофлоры, и подавляют рост патогенных бактерий. Возможно, продукты метаболизма улучшают трофику и функцию эпителиоцитов и колоноцитов. 1 мл препарата соответствует биосинтетическим активным веществам 100 млрд. нормальных микроорганизмов. Хилак форте назначают по 40–60 капель 3 раза в день на срок до 4 недель в сочетании с препаратами антибактериального действия или после их применения.
Регуляторы пищеварения и моторики кишечника
У больных с нарушением полостного пищеварения применяют креон, панцитрат и другие панкреатические ферменты. С целью улучшения функции всасывания назначают эссенциале, легалон или карсил, т. к. они стабилизируют мембраны кишечного эпителия. Пропульсивную функцию кишечника улучшают имодиум (лоперамид) и тримебутин (дебридат).
Стимуляторы реактивности организма
Для повышения реактивности организма ослабленным больным целесообразно применять тактивин, тималин, тимоген, иммунал, иммунофан и другие иммуностимулирующие средства. Курс лечения должен составлять в среднем 4 недели. Одновременно назначаются витамины.
Профилактика дисбактериоза
Первичная профилактика дисбактериоза представляет очень сложную задачу. Ее решение связано с общими профилактическими проблемами: улучшением экологии, рациональным питанием, улучшением благосостояния и прочими многочисленными факторами внешней и внутренней среды.
Вторичная профилактика предполагает рациональное применение антибиотиков и других медикаментов, нарушающих эубиоз, своевременное и оптимальное лечение болезней органов пищеварения, сопровождающихся нарушением микробиоценоза.
Холера – это особо опасное инфекционное заболевание, которое вызывает сильную диарею и обезвоживание вплоть до гиповолемического шока и смерти. Чаще всего заражение происходит через загрязненную воду. При отсутствии лечения эта патология может привести к летальным осложнениям в течение нескольких часов даже у ранее здоровых людей. Современные методы очистки воды практически устранили холеру в промышленно развитых странах. Но эта болезнь все еще встречается в Африке и Юго-Восточной Азии. Риск эпидемии холеры наиболее высок, когда бедность, войны или стихийные бедствия вынуждают людей жить в тесноте без надлежащих санитарных условий.
Согласно статистическим данным, ежегодно в мире фиксируется около 5 млн случаев холеры, из которых около 130 тыс. заканчивается летально.
В каких странах можно заразиться холерой?
Повышенный риск инфицирования холерным вибрионом есть у людей, проживающих или пребывающих в длительной командировке в следующих странах:
- Йемен.
- Ирак.
- Иран.
- Индия.
- Нигерия.
- Уганда.
- Мексика.
- Танзания.
- Бразилия.
Симптомы холеры
Большинство людей, инфицированных холерным вибрионом, не заболевают и даже не знают, что были заражены. Но при этом они выделяют бактерии со стулом в течение 7-14 дней, из-за чего все еще могут заразить других через загрязненную воду.
Как правило, клинические проявления холеры представлены умеренной или выраженной диареей, которая мало чем отличается от расстройства стула другого происхождения. Реже развиваются более серьезные симптомы. Как правило, это происходит внезапно, спустя 1-3 дня после заражения.
Симптомами холерной инфекции могут быть:
Сухость слизистых оболочек рта
Умеренный налет на языке белого цвета
Кожа бледная и сухая, ее упругость и эластичность снижены
Резкая общая слабость
Охриплость голоса, снижение его громкости
Судороги в икроножных мышцах
Повышенная частота сердцебиения и падение артериального давления
Синюшный окрас кожи и слизистых оболочек
Человек может говорить только шепотом
Судороги мышц по всему телу
Мочеиспускание частично или полностью прекращается
Ранее упомянутые симптомы развиваются очень быстро
Систолическое артериальное давление опускается ниже 60 мм рт. ст.
Вместо рвоты возникает икота
Снижается температура тела
Темные круги вокруг глаз
Общие тонические судороги
Развивается гиповолемический шок
Когда обратиться к врачу?
Риск вспышки холеры в промышленно-развитых странах невелик. Даже в тех регионах, где он существует, вероятность инфицирования при условии соблюдения рекомендаций по безопасности пищевых продуктов минимален. Тем не менее случаи холеры отмечаются во всем мире.
Таким образом, если после посещения региона с недавно зафиксированными случаями холеры у человека появляется тяжелая диарея, это повод немедленно обратиться к врачу².
Особенности холеры у детей
В возрасте до 3 лет характерное для холеры обезвоживание переносится значительно тяжелее. Из-за этого у детей быстрее развиваются признаки нарушения работы нервной системы в виде резкой общей заторможенности, судорог и даже утраты сознания. При этом, в отличие от взрослых, температура тела у детей при холере часто повышается до 37,5-38,0°С.
Лечение холеры
Лечение больных с холерой проводится в стационарах инфекционного отделения, в изолированном боксе. В большинстве случаев пациенты нуждаются в постельном режиме. Основу лечения составляет коррекция водно-солевого баланса и антибактериальная терапия. Длительность лечения зависит от тяжести протекания холеры и составляет 3-5 дней.
Восстановление водно-солевого баланса
Важную роль в лечении занимает восстановление водно-солевого баланса, которое необходимо начать с первых часов развития заболевания. Необходимо компенсировать потерю жидкости в организме: объем поступающей жидкости должен в 1,5 раза превышать ее потери (рвотные массы, стул).

Регидратацию и коррекцию водно-солевого баланса важно начать как можно раньше. Фото: belchonock / Depositphotos
При 1-2 степени обезвоживания используются водно-солевые растворы, которые принимаются перорально. При 3-4 степенях дегидратации больные теряют возможность пить самостоятельно, из-за чего солевые растворы вводятся внутривенно струйно на протяжении первых нескольких часов, после чего их введение продолжают внутривенно капельно.

В некоторых случаях нет возможности приобрести готовый раствор для пероральной регидратации. В качестве временной меры можно использовать приготовленный в домашних условиях аналог. Для этого нужно смешать:
- 1 литр бутилированной или кипяченой воды.
- 6 чайных ложек без горки (около 30 граммов) столового сахара.
- 1/2 чайной ложки без горки (около 2,5 граммов) поваренной соли.
Антибактериальная терапия
Для борьбы непосредственно с возбудителем заболевания назначаются антибиотики. При холере эффективными средствами считаются:
- тетрациклины: тетрациклин, доксициклин;
- фторхинолоны: ципрофлоксацин;
- макролиды: эритромицин;
- при непереносимости антибиотиков назначаются препараты из группы нитрофуранов (фуразолидон).
Историческая справка
В XIX веке холера начала распространяться по миру из своего первоначального резервуара – дельты реки Ганг в Индии. Шесть последующих пандемий забрали жизни многих миллионов людей на всех континентах планеты. Последняя (седьмая) пандемия началась в Южной Азии в 1961 году, в 1971 году достигла Африки, а в 1991 году – Америки. Сейчас холера является эндемическим заболеванием во многих странах¹.
Факторы риска
К холере восприимчивы все, за исключением младенцев, получивших иммунитет от кормящих матерей, ранее переболевших холерой. Тем не менее, определенные факторы могут сделать человека более уязвимыми для болезни или обусловить более тяжелое течение инфекции. К таковым относятся:
- Плохие санитарные условия. Антисанитария в местах проживания характерна для лагерей беженцев, бедных стран и районов, пострадавших от голода, войны или стихийных бедствий.
- Снижение или отсутствие кислоты в желудке. Бактерии холеры не могут выжить в кислой среде, а обычная желудочная кислота часто служит защитой от инфекции. Но люди с низким уровнем желудочного сока (например, дети, пожилые и люди, принимающие препараты для снижения секреции желудочного сока) лишены этой защиты.
- I (0) группа крови. Причины до конца еще не изучены, но вероятность развития холеры у людей с первой группой крови в два раза выше, чем у остальных².
Диагностика
Постановка диагноза проводится на основе сочетания данных истории болезни, клинических проявлений и результатов лабораторных исследований. При сборе анамнеза выясняются возможные пути инфицирования холерой (употребление в пищу потенциально зараженной воды или морепродуктов) и факторы риска – например, командировка в неблагополучные страны, области, районы за несколько дней до появления симптомов.
При лабораторной диагностике холеры используются следующие анализы:
- Общий анализ крови (ОАК). В нем отмечается умеренное повышение уровня эритроцитов и лейкоцитов, в том числе нейтрофилов. Также повышается насыщение эритроцитов гемоглобином, скорость оседания эритроцитов (СОЭ). При этом может падать уровень моноцитов.
- Общий анализ мочи (ОАМ). Помимо общего уменьшения объема выделяемой мочи по мере нарастания обезвоживания в ней может отмечаться повышение уровня патологических цилиндров и белка.
- Бактериологический посев. При подозрении на холеру с целью выявления возбудителя образец рвотных масс или испражнений сеется на питательную среду. Спустя 1-2 дня получают рост колоний. При подозрении на холеру исследование повторяется еще дважды.
- Экспресс-тесты с моноклональными антителами. Позволяют в течение 5 минут подтвердить факт инфицирования человека холерными вибрионами.
- Реакция непрямой гемагглютинации крови (РНГА). Дает возможность выявить наличие специфических антител в крови. Положительным результатом считается их диагностический титр 1:160. Тест информативен только с 5-го дня заболевания.
- Полимеразная цепная реакция (ПЦР). Позволяет выявить генетический материал (в данном случае – ДНК) возбудителя. Помимо выделений больного для исследования также может использоваться вода или продукты питания, которые являются потенциальным источником заражения.
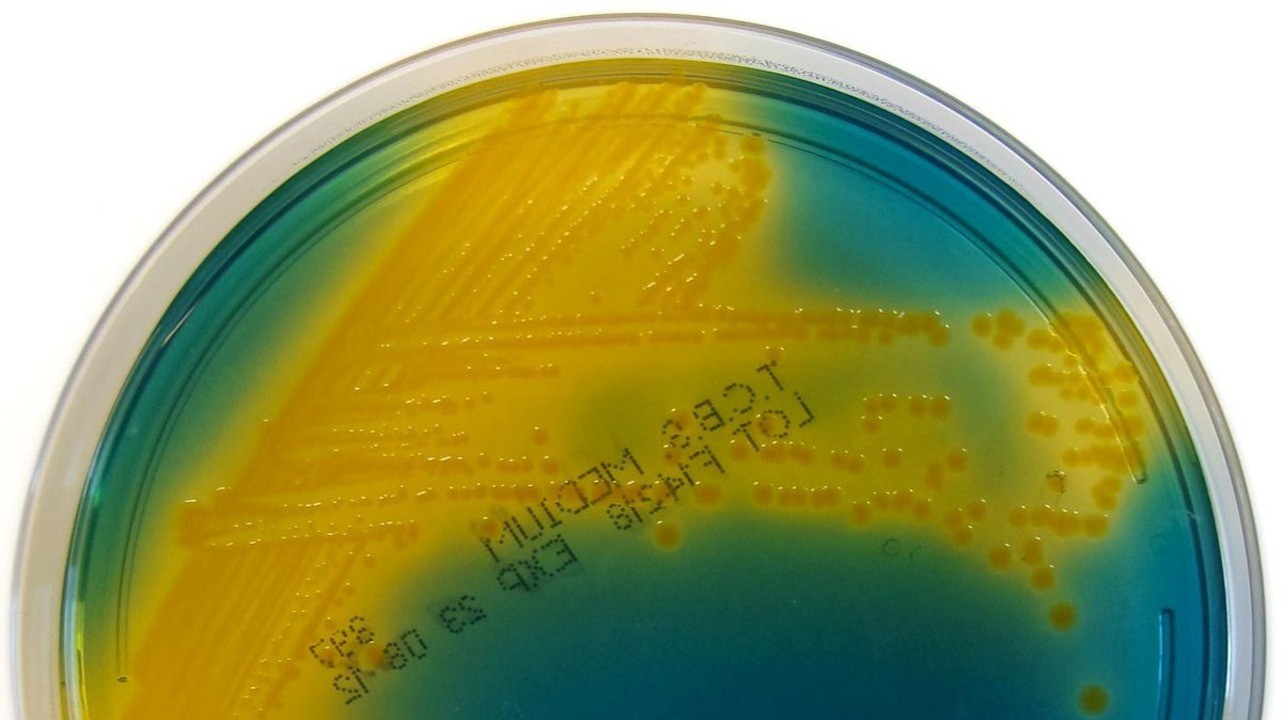
Бакпосев при холере – один из методов диагностики. Фото: Nathan Reading / Flickr (CC BY-NC-ND 2.0)
Дифференциальная диагностика холеры проводится с другими заболеваниями, которые на ранних этапах могут сопровождаться похожими симптомами. К ним относятся:
- Острые кишечные инфекции: сальмонеллез, брюшной тиф, эшерихиоз (дизентерия), ротовирусная инфекция. Они также сопровождаются диареей, рвотой. Однако в отличие от холеры при них повышается температура тела, возникают боли в животе, а обезвоживание зачастую умеренное или вовсе отсутствует.
- Отравления. Симптомы интоксикации химическими веществами напрямую зависят от конкретного реагента. Однако в большинстве случаев они также проявляются рвотой, диареей и признаками нарушения работы ЦНС. При этом дегидратация, как правило, не возникает.
- Ботулизм. Острая инфекция, которая также приводит к нарушению работы ЦНС. При этом помимо судорог скелетных мышц страдает зрение и дыхание. В отличие от холеры часто возникает запор. Причиной инфицирования чаще всего становится употребление в пищу испорченных консервов или копченостей.
Возбудитель и пути инфицирования
Возбудитель холеры – холерный вибрион (Vibrio cholerae), а именно две его серогруппы O1 и O139. Из них основными биотипами, которые вызывают вспышки заболевания, являются: О1 classica – классический биотип. О1 El Tor – преобладает в настоящее время. О139 Bengal – известен с 1992 года, причина крупной эпидемии в Бангладеш, Индии и рядом расположенных странах.
Источником инфекции является больной человек или носитель бактерии. Люди наиболее заразны в первые 7 дней с момента развития холеры – в это время они активно выделяют холерные вибрионы в окружающую среду. Насекомые и животные не являются переносчиками этой болезни.
Передача инфекции чаще всего происходит фекально-оральным способом. Инфицирование может происходить следующими путями:
- Поверхностная или колодезная вода. Загрязненные общественные колодцы – частая причина крупномасштабных вспышек холеры. Особому риску подвержены люди, живущие в тесноте в плохих санитарных условиях.
- Морепродукты. Употребление в пищу сырых или недоваренных морепродуктов, особенно моллюсков, может привести к развитию холеры.
- Сырые фрукты и овощи. Сырые неочищенные фрукты и овощи – частый источник инфекции в эндемичных регионах. Неразложившиеся удобрения или оросительная вода, содержащая неочищенные сточные воды, могут загрязнять продукты на поле.
- Зерна. В регионах, где широко распространена холера, рис и просо, загрязненные после приготовления и хранящиеся при комнатной температуре в течение нескольких часов, могут стать средой для роста бактерий холеры.

Риск развития эпидемии холеры наиболее высок в антисанитарных условиях. Фото: Olgatribe / Depositphotos
Классификация
В клинической практике используется несколько классификаций холеры. Это обусловлено различиями в симптомах заболевания и подходах к лечению в различных случаях. Также некоторые формы болезни могут иметь нехарактерное для классической холеры течение.
В зависимости от развивающихся симптомов холера делится на такие формы:
- Типичная или желудочно-кишечная. Классическая форма холеры, сопровождающаяся расстройствами ЖКТ.
- Атипичная. Включает в себя несколько подвидов, которые существенно отличаются от типичного варианта заболевания. К атипичным формам холеры относятся:
- Молниеносная. Отличается чрезвычайно быстрым развитием с ярко выраженной рвотой и диареей, из-за чего быстро формируется сильное обезвоживание, а в течение 3-4 часов возникает дегидратационный шок.
- Сухая. Характеризуется резким ухудшением общего состояния человека. Еще до появления диареи может развиться коматозное состояние.
- Стертая. Отличается сравнительно легкими симптомами: частота дефекации в сутки составляет от 1 до 3 раз, а стул не видоизменен. Общее состояние при этом зачастую удовлетворительно, диагноз устанавливается только на этапе лабораторных тестов.
- Бессимптомная. Вариант инфицирования, который протекает без каких-либо клинических проявлений. Выявляется только после лабораторной диагностики.
Отдельно принято выделять вибрионосительство. Это состояние, при котором инфицированный человек выделяет в окружающую среду холерные вибрионы, но при этом признаков заболевания у него нет. У него могут быть следующие варианты:
- Реконвалесцентное. Отмечается у людей, которые восстанавливаются после перенесенной холеры.
- Транзиторное. Характерно для людей, которые пребывают в очаге вспышки холеры. Они заражаются, но их организм успешно справляется с инфекцией. Как правило, сохраняется не более 3 месяцев.
- Хроническое. Состояние, при котором холерные вибрионы сохраняют свою активность в организме и человек продолжает выделять их в окружающую среду более 3 месяцев.
В зависимости от состояния больного, выраженности поражения желудочно-кишечного тракта и степени дегидратации выделяют следующие степени тяжести холеры³:
Осложнения
Без должного лечения холера может быстро привести к летальному исходу. В самых тяжелых случаях потеря большого количества жидкости и электролитов может стать причиной смерти в течение нескольких часов. В других случаях люди, не получающие необходимой помощи, могут умереть от обезвоживания и дегидратационного шока через 1-2 дня после появления первых симптомов холеры².
Хотя сильное обезвоживание считается наиболее опасным осложнением холеры, при этой патологии могут возникнуть и другие проблемы:
- Низкий уровень сахара в крови (гипогликемия). Низкий уровень сахара (глюкозы) в крови – основного источника энергии для организма – характерен для тяжелых форм холеры. Гипогликемия может сопровождаться судорогами, потерей сознания и приводить к смерти. Дети наиболее подвержены снижению уровня глюкозы при холере.
- Низкий уровень калия (гипокалиемия). Больные холерой на фоне диареи теряют большое количество электролитов, в том числе калия, в результате чего нарушается работа сердца и нервной системы, что создает угрозу для жизни пациента.
- Почечная недостаточность. Когда почки теряют свою фильтрующую способность, в организме накапливается избыточное количество жидкости, некоторых электролитов и продуктов метаболизма, что также опасно для жизни.
- Вторичная инфекция. На фоне холеры организм становится более восприимчивым к другим бактериям. Это может привести к таким осложнениям, как воспаление легких, абсцессы, сепсис.
Вакцинация против холеры
Специфическая профилактика холеры представлена вакциной, которая принимается внутрь. На данный момент разработано и одобрено для использования три препарата⁴:
Полная программа вакцинации зависит от препарата и возраста человека и может включать 2-3 дозы, которые вводятся с интервалом в 1-2 недели. Полный курс вакцинации обеспечивают защиту от холеры в течение трех лет, тогда как одна доза дает кратковременную защиту.

Ни одна вакцина против холеры не обеспечивает 100% защиты, а вакцинация не заменяет стандартные меры профилактики и контроля, включая меры предосторожности в отношении продуктов питания и воды⁴.
Прогноз и профилактика
При легкой и среднетяжелой форме заболевания прогноз относительно благоприятный. Однако даже в таких случаях без своевременного оказания помощи могут развиться осложнения, приводящие к смерти. После перенесенного заболевания у человека остается стойкий иммунитет.
Несмотря на то что холера редко встречается в странах Европы, риск заражения все еще сохраняется. Также дополнительные меры предосторожности стоит соблюдать при посещении стран с активными вспышками холеры среди населения. Для этого используется специфическая и неспецифическая профилактика.
К основным мерам неспецифической профилактики холеры относятся:
- Соблюдение правил личной гигиены. Необходимо часто мыть руки водой с мылом, особенно после посещения туалета и перед работой с пищевыми продуктами. Если мыло и вода недоступны, нужно использовать дезинфицирующее средство для рук на спиртовой основе.
- Употребление только качественной воды. Важно пить только безопасную воду, в том числе бутилированную, кипяченую или продезинфицированную. Ее нужно использовать даже для чистки зубов. Горячие напитки, напитки в банках или бутылках в целом безопасны, но перед тем, как открывать их, нужно обеззаразить внешнюю поверхность упаковки. Также не стоит добавлять лед в напитки, если нет уверенности в том, что он изготовлен из чистой воды.
- Питание только проверенной пищей. Нужно отдавать предпочтение самостоятельно приготовленной и горячей пище, по возможности избегать еды от уличных торговцев. Рекомендуется отказаться от суши, а также от любой сырой или неправильно приготовленной рыбы и морепродуктов. Важно употреблять в пищу фрукты и овощи, которые можно очистить самостоятельно, например, бананы, апельсины и авокадо.
Заключение
Холера – это редко встречающееся в развитых странах заболевание. Однако это не значит, что риска заражения вовсе нет. Не стоит пренебрегать средствами профилактики в отношении этой инфекции, в особенности при планировании командировки или туристического посещения стран, в которых часто регистрируются случаи холеры.
Читайте также:

