Лечение цитомегаловируса при увеите
Обновлено: 18.04.2024
Для цитирования: Максимов В.Ю., Дмитриева О.Г., Евсеев С.Ю., Александрова Н.М. Диагностика и лечение увеитов герпесвирусной и хламидийной этиологии. РМЖ. Клиническая офтальмология. 2003;4(4):168.
Diagnostics and treatment of herpetic and chlamidial uveitis
V.Yu. Maximov, O.T. Dmitrieva,
S.Yu. Evseev, N.M. Alexandrova
Saratov regionary hospital.
The quantity of patients with virus and chlamidial etiology is growing steadily.The main directions of diagnostics and treatment of uveitis are developing during last years. Usage of accessible, informative enough methods of examination, such as method of fluorescent antibodies, immune–enzyme assay, NST–test allows to define the type of pathogene, immune homeostasis and, relying on this, prescribe specific and immunomodulating treatment.
Воспалительные заболевания глаз являются самой распространенной глазной патологией. По данным А.М. Южакова, 80% временной нетрудоспособности и более 10% слепоты связано с воспалением глаз. В инфекционной патологии органа зрения заболевания, вызываемые вирусами простого герпеса, цитомегаловирусами, хламидиями, по частоте возникновения, тяжести течения и трудностям лечения занимают одно из ведущих мест [1,2,З]. Неуклонно растет количество больных с увеитами вирусной и хламидийной этиологии.
Концепции патогенеза, основные направления терапии увеитов активно развиваются в последние годы, и уже достигнуты значительные успехи в разработке новых методов диагностики с определением вида возбудителя, иммунного гомеостаза больного и на этом основании специфического патогенетического и иммунокорригирующего лечения [4, 5, 6].
Цель работы
1. Провести ретроспективный анализ эффективности лечения увеитов.
2. Определить роль герпесвирусной и хламидийной инфекций в этиологической структуре воспалительных заболеваний глаз.
Материалы и методы
Первым этапом нашей работы был анализ 204 историй болезни пациентов с увеитами, прошедших лечение в Областной офтальмологической больнице в период с 1988 по 1997 г. 14 пациентам (6,9%) был поставлен диагноз туберкулезного увеита. Эти больные получали лечение у фтизиоокулиста. Анализ эффективности их лечения мы не проводили. 52 больным (25,5%) был поставлен диагноз увеита герпетической этиологии, из них 39 – кератоувеита. У 138 пациентов (67,6%) диагностировали увеит неясной этиологии. Основными критериями для постановки диагноза увеита герпесвирусной этиологии были данные клинической картины и результаты метода иммунофлюоресцирующих антител (выявляли антигены вируса простого герпеса в мазках с конъюнктивы и в мазках крови).
Для лечения использовали гормональные препараты (дексаметазон (с/к, в/в), кеналог п/б), нестероидные противовоспалительные препараты (индометацин в таб., диклофенак в таб., в/м), биогенные стимуляторы (алоэ, фибс в/м), в качестве иммуномодуляторов – пирогенал (по стандартной схеме, начиная с 25 МПД № 10), продигиозан (25 мг в/м через 3 дня № 3–6). При лечении герпетического кератоувеита использовали человеческий лейкоцитарный интерферон (в каплях), глазную мазь бонафтон, флореналь.
Второй этап нашей работы – это наблюдение за 52 пациентами с увеитами, проходившими лечение в ООБ с 1999 по 2001 год. Средний возраст больных был 30–40 лет, женщин – 20, мужчин – 32.
Всем больным проводилось комплексное офтальмологическое обследование. Лабораторная диагностика включала общеклинические (OAK, ОАМ, кровь на RW, ВИЧ) и биохимические анализы. Для определения этиологического фактора воспаления использовали метод иммунофлюоресцирующих антител (МФА) – выявляли в мазках крови антиген вируса простого герпеса (АГ ВПГ), иммуноферментный анализ (ИФА) –определяли антитела класса IgM (IgA) и IgG к вирусу простого герпеса (ВПГ), цитомегаловирусу (ЦМВ), хламидиям (Chlamydia trachomatis) в сыворотке крови, полимеразную цепную реакцию (ПЦР) – для выявления ДНК хламидий, ВПГ, ЦМВ при сомнительных результатах ИФА и МФА.
Иммунологическую резистентность больных оценивали по показателям нейтрофильного фагоцитоза: НСТ–тест (фагоцитарный индекс (ФИ), фагоцитарное число (ФЧ), количество активных фагоцитов (КАФ), абсолютное число нейтрофилов (АЧН)). 14 пациентам была выполнена иммунограмма.
Для лечения больных использовали поэтапный подход. При поступлении пациента в стационар назначали препараты патогенетической терапии – глюкокортикоиды (дексаметазон с/к, в/в), нестероидные противовоспалительные препараты (диклофенак, индометацин), дезинтоксикационные (гемодез в/в, энтеродез per os), десенсибилизирующие (фенкарол, тавегил) средства. После установления этиологического фактора воспаления к лечению присоединяли специфические противовирусные и (или) противохламидийные препараты. Этиотропная терапия при лечении пациентов с увеитами герпесвирусной этиологии включала виролекс 250 мг 2 раза в день в/в капельно 5–10 дней, затем ацикловир 200–400 мг 5 раз в день 5–14 дней; при лечении пациентов с цитомегаловирусными увеитами использовали ганцикловир 1,0 г 3 раза в день или 5 мг/кг в/в капельно каждые 12 часов 14 дней; у пациентов с хламидийными увеитами использовали спирамицин (ровамицин) 3 млн. 3 раза в день 10 дней, доксициклин 0,2 г, затем 0,1 г 2 раза в день 10 дней.
После купирования острых воспалительных реакций назначали системные энзимы – вобэнзим 5–7 табл. 3 раза в день 2 недели, рассасывающие препараты – коллализин, химотрипсин (с/к). В качестве иммуномодуляторов использовали реаферон 1 млн 1 раз в день 10 дней, циклоферон 2,0 в/м по схеме 5–10 инъекций (табл.1). Пациентам с увеитами неустановленной этиологии провели курс патогенетической терапии в сочетании с циклофероном.
Результаты
Среди пациентов (190 человек), прошедших лечение в ООБ с 1988 по 1997 год, выраженный терапевтический эффект наблюдали у 45 больных (23,7%), т.е. удавалось добиться полного исчезновения клинических признаков воспаления, значительного рассасывания помутнения в стекловидном теле, повышения остроты зрения до визуса, предшествующего заболеванию. Повторных обращений для стационарного лечения среди этих пациентов не было. У 92 больных (48,4%) эффект был частичным, удавалось добиться значительного, но не полного уменьшения воспалительных явлений, повышения остроты зрения, но не более чем на 70% от исходного визуса. 64 из них повторно лечились в ООБ. У 53 пациентов (27,9%) увеит носил характер хронического рецидивирующего процесса с периодами обострения 2–3 раза в год (у 18 из них исходом повторных обострении явились фиброз стекловидного тела и отслойка сетчатки, у 23 сформировалась осложненная катаракта).
Среди пациентов, прошедших лечение в ООБ в период с 1999 по 2001 год: диагноз герпетического увеита поставлен 14 пациентам (26,9%), увеит хламидийной этиологии – 15 (28,8%), цитомегаловирусной – 3 (5,8%). Смешанная инфекция выявлена у 10 больных (19,2%), из них у 4 (7,6%) – герпесвирусная и цитомегаловирусная инфекция, у 6 (11,6%) – герпесвирусная и хламидийная инфекция. 10 пациентам (19,2%) поставлен диагноз увеита неясной этиологии.
Показатели фагоцитарной активности нейтрофилов в разгар заболевания были изменены у 48 (92,3%) больных – у 30 (57,6%) пациентов ФИ и ФЧ, КАФ снижены, у 18 (34,6%) – отмечалось повышение этих показателей; АЧН было повышено у 36 (69,2%) человек, снижено у 12 (23%). Достоверно значимых изменений в показателях иммунограммы выявлено не было.
После проведенного лечения выраженный терапевтический эффект отмечен у 40 (77%), частичный – у 12 больных (23%) (табл. 2).
Эффективность терапии оценивали и по динамике данных лабораторного исследования. Через месяц после начала лечения у больных с увеитами герпесвирусной этиологии АГ ВПГ в мазках крови не обнаружены. IgM (Ig) к ВПГ и хламидиям не выявлялись ни у одного больного, а к ЦМВ только у одного. Титр IgG к ВПГ, хламидиям и ЦМВ снизился в среднем в 2 раза. Показатели нейтрофильного фагоцитоза нормализовались у 36 больных (69,2%).
Пациентам с цитомегаловирусной инфекцией, микст–инфекцией, в случае частичного терапевтического эффекта, а также при появлении признаков активации инфекции по данным лабораторной диагностики (контрольное обследование через 2, 4 месяца после первого курса) проводили повторные курсы лечения. За весь период наблюдения дважды в стационар обратились 3 пациента (5,7%), один из них проходил лечение в клинике гематологии с диагнозом лимфолейкоз.
Выводы
1. Вирус простого герпеса, цитомегаловирус, хламидии являются наиболее распространенными возбудителями, вызывающими воспалительные заболевания глаз.
2. Лабораторная диагностика с использованием доступных, достаточно информативных методов исследования, таких как метод флюоресцирующих антител, иммуноферментный анализ, НСТ–тест, позволяет определить вид возбудителя, иммунный гомеостаз больного и на этом основании назначить специфическое и иммуномоделирующее лечение.
3. Сочетанное использование противовирусных и (или) противохламидийных и иммуномодулирующих препаратов способствует получению синергидного терапевтического эффекта, уменьшению клинической тяжести заболевания, нормализации лабораторных показателей.
Литература
1. Балашевич Л.И., Вахова Е.С. и соавт. Офтальмохламидиоз. СПб., 1998 г. 2–Гранитов В.М. Герпесвирусная инфекция. М., 2001 г.
3. Кацнельсон Л.А., Танковский В.Э. Увеиты. ( Клиника, лечение). 1998г. стр.155–163.
4.Кетлинский С.А., Калинина Н.М. Иммунология для врача. СПб., 1998 г.
5.Рахманова А.Г., Кирпичникова Г.И. и соавт. Стратегия и тактика диагностики и лечения герпетических инфекций. СПб., 2000 г
6.Нарушение иммунитета и лечение увеитов. Методические рекомендации. М., 1991 г.
Лечение цитомегаловирусной инфекции - препараты
Подход к лечению ЦМВ-инфекции существенно отличается у реципиентов после аллогенной трансплантации костного мозга (ТКМ) и у больных, подвергающихся химиотерапии (в том числе высокодозной после трансплантации аутологичных стволовых клеток). Больным первой группы необходимо упреждающее лечение, поскольку, несмотря на наличие препаратов, эффективно ингибирующих репликацию вируса, лечение уже развившихся висцеральных поражений эффективно не более чем в половине случаев.
Больным, получающим стандартную химиотерапию, специфическое лечение проводят только при установленном или высоковероятном висцеральном поражении.
Методы контроля ЦМВ-инфекции у реципиентов аллогенного костного мозга зависят от ЦМВ-статуса пары донор — реципиент. При серонегативности как донора, так и реципиента самым надежным способом профилактики ЦМВ-инфекции является использование для трансфузий препаратов крови от серонегативных доноров или лейкодеплеция с помощью фильтров последнего поколения, предназначенных для фильтрации в банках крови. При любом другом сочетании ЦМВ-статусов главные инструменты контроля — еженедельный мониторинг ЦМВ-виремии (методом ПЦР или выявлением антигенемии рр65) и упреждающее лечение ганцикловиром при позитивном результате.
Для начала терапии больных высокого риска (реципиенты неродственной или неполностью совместимой трансплантации, лечение РТПХ антитимоцитарным глобулином) достаточно однократного позитивного анализа. В то же время у больных низкого риска при невысокой вирусной нагрузке назначение специфической терапии можно отложить до повторного позитивного анализа, выполненного с интервалом 3— 5 дней. Этот подход проверен многими исследователями, в том числе нами. Доказано, что такой подход эффективнее и дешевле, чем профилактическое использование высоких доз иммуноглобулина и ацикловира, которое было популярно в конце 80-х — начале 90-х годов.

Ганцикловир (1,3-дигидрокси-пропоксиметил-гуанин) сам по себе не является активным противовирусным агентом, необходимо его фосфорилирование вирусной тимидинкиназой. В форме трифосфата ганцикловир ингибирует вирусную ДНК-полимеразу. Сродство ганцикловира к тимидинкиназам человека значительно меньше, поэтому его токсичность для человеческих клеток относительно невелика.
Доза ганцикловира для курса индукции составляет 10 мг/кг в сутки на два введения. Курс индукции продолжается 2—3 нед, после чего назначают поддерживающую дозу — 5 мг/кг в сутки на одно введение ежедневно или 5—6 раз в неделю. Длительность курса поддерживающей терапии определяют индивидуально. При упреждающем лечении реактивации ЦМВ после аллогенной ТКМ при достижении негативной реакции на антигене-мию или виремию поддерживающее лечение можно не проводить, в то время как при органном поражении (пневмония, ЦМВ-колит) лечение должно быть продолжено до купирования симптомов и негативизации результатов вирусологических исследований, а при ЦМВ-ретините терапия может быть пожизненной.
При длительном профилактическом или упреждающем применении ганцикловира в раннем посттрансплантационном периоде высока частота поздних ЦМВ-пневмоний. Таким пациентам необходимо продолжать мониторинг ЦМВ-виремии или антигенемии и после 100-го дня после трансплантации [11]. Примерно у 20 % больных, леченных ганцикловиром в указанной дозе, развивается гранулоцитопения менее 1000 в 1 м\ во всех случаях обратимая (быстрее под влиянием G-CSF), с медианой длительности 12 дней. Резистентность ЦМВ к ганцикловиру является редкостью.
Отличным от ганцикловира по механизму действия (прямое ингибирование ДНК-полимеразы) является натрия фосфоноформат (фоскарнет, фоскавир), который может быть эффективен при резистентности данного штамма вируса к ганцикловиру. Индукционная доза натрия фосфоноформата 90 мг/кг каждые 12 ч. Продолжительность курса лечения составляет 14 дней, затем проводят поддерживающую терапию в половинной дозе. Побочными реакциями являются нарушение функции почек, гипомагнезиемия, гипокальциемия и изъязвление слизистых оболочек наружных половых органов.
Необходимо отметить коммерчески доступный специфический антицитомегаловирусный иммуноглобулин. Убедительных доказательств его эффективности в лечении вызванных ЦМВ болезней нет. С учетом его дороговизны, а также наличия препаратов, оказывающих специфическое противовирусное действие, дальнейшее применение этого препарата вряд ли оправдано.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Инфекции вызванные цитомегаловирусом: диагностика, лечение, профилактика
Вирусы герпеса — большие, покрытые оболочкой, двунитевые ДНК-вирусы (120—200 нм). Геном содержит 120—240 тыс. пар нуклеотидов, кодирующих более 35 белков. Оболочка состоит из гликопротеинов и Fc-рецепторов. Инфекция персистирует у человека на протяжении всей жизни, переходя в латентную форму после острой стадии и периодически рецидивируя (особенно при снижении иммунитета у человека).
Классификация герпес-вирусов
Все вирусы герпеса разделяют на:
• а-герпес-вирусы — быстрорастущие цитолитические вирусы, вызывающие латентную инфекцию и поражающие нейроны (вирусы простого и опоясывающего герпеса);
• бета-герпес-вирусы — медленно растущие вирусы, вызывающие латентные инфекции секреторных желёз и почек (цитомегаловирус);
• у-герпес-вирусы — вирусы, вызывающие латентный инфекционный процесс в лимфоидной ткани (вирус Эпштейна—Барр).
Недавно обнаруженные вирусы герпеса человека типа 6 и 7 (ВГЧ-6 и ВГЧ-7) относят к у-герпес-вирусам, так как они вызывают латентные инфекции лимфатических узлов и имеют генетические сходства именно с этой группой вирусов герпеса. ВГЧ-8, ассоциированный с саркомой Капоши, сходен с вирусом Эпштейна—Барр. Все вирусы герпеса, за исключением вируса простого герпеса типа 1 и 2, различны по антигенной структуре.
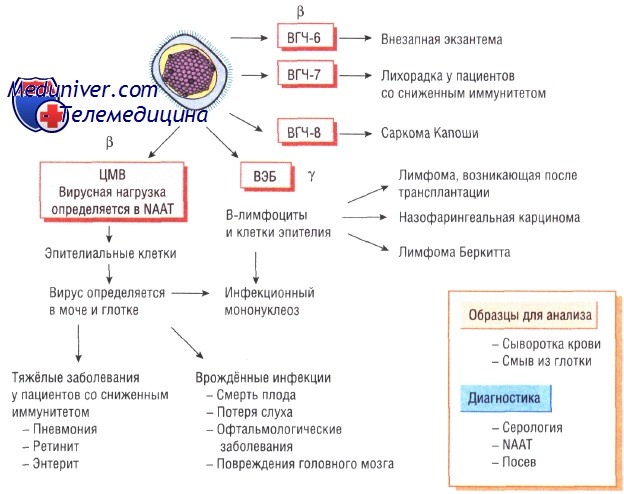
Инфекции вызванные цитомегаловирусом
По своей структуре цитомегаловирус похож на все остальные вирусы герпеса. Обычно он персистирует в организме на протяжении всей жизни. Его обнаруживают в моче и слюне человека. Примерно 50% населения Великобритании инфицированы ВГЧ-5.
Эпидемиология и патогенез цитомегаловирусной инфекции. Механизм передачи инфекции — вертикальный или контактный (от человека к человеку). Чем ниже социально-экономические условия, тем раньше происходит инфицирование. Возможен вертикальный механизм передачи инфекции. Кроме того, заражение может произойти при переливании крови или пересадке органов; в этом случае инфекции свойственно очень тяжёлое течение.
Клинические признаки инфекции вызванной цитомегаловирусом. Врождённая инфекция обычно протекает в тяжёлой форме. В начальном периоде выраженные симптомы заболевания отсутствуют. В дальнейшем возникает прогрессирующая глухота, задержка развития. При заражении после рождения заболевание протекает в лёгкой форме. У пациентов со сниженным иммунитетом (ВИЧ-инфекция, состояние после трансплантации органов) может развиться тяжёлая пневмония, ретинит, поражение кишечника, причём вирусная инфекция может быть приобретённой (от пересаженного органа) или собственной (латентная форма).
Диагностика инфекции вызванной цитомегаловирусом. Врождённую инфекцию диагностируют при проведении анализа мочи через 3 нед после рождения. У взрослых цитомегаловирус может быть культивирован либо определён молекулярно-генетическим методом в образцах мочи и крови. Исследование вирусной нагрузки имеет большое значение для диагностики тяжёлого течения инфекции и назначения своевременного лечения.
Лечение и профилактика инфекции вызванной цитомегаловирусом. При тяжёлой инфекции, угрожающей жизни пациента, а также при риске потери зрения лечение проводят ганцикловиром в комплексе с иммуноглобулином (при развитии пневмонии). Эфир ганцикловира, валганцикловир принимают внутрь, назначают в начале лечения и в качестве поддерживающей терапии. Ещё более токсичные альтернативные препараты (фоскарнет и цидофовир) ингибируют цепочечную ДНК-полимеразу. Важная мера профилактики заболевания — тщательный подбор донорских органов для пересадки и крови для переливания.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
ВИЧ-ассоциированные оппортунистические заболевания, возникающие при развитии синдрома приобретенного иммунодефицита, можно разделить на две группы: вызванные различными инфекционными агентами и новообразования. Это одинаково применимо к любому органу человека, и к глазу, в частности. К офтальмопатологии, связанной с ВИЧ, относятся: заболевания глаз, вызванные герпесгруппой, токсоплазмоз, туберкулез, грибковые поражения, саркома Капоши и другие. Цитомегаловирусный увеит является одним из основных ВИЧ-ассоциированных заболеваний органа зрения инфекционной природы [1, 2, 7-9]. Он может возникать изолированно или же в структуре генерализованной ЦМВ-инфекции (ЦМВИ). Развитие ЦМВИ часто является причиной смерти ВИЧ-инфицированных пациентов со СПИД [6].
Цитомегаловирусный (ЦМВ) увеит при ВИЧ-инфекции – одно из наиболее опасных вторичных заболеваний органа зрения, в отсутствии лечения приводящее к слепоте. Оно возникает у пациента при выраженном иммунодефиците, который характеризуется уменьшением уровня CD4-лимфоцитов до 100 кл/мкл и более, потерей массы тела более 10 кг, кандидозным поражением слизистых оболочек и возможным развитием других ВИЧ-ассоциированных инфекционных и онкологических патологий. Состояние больного в данном случае относится к стадиям 4б, 4в, 5 ВИЧ-инфекции по классификации В.И. Покровского, 2001, синдрому приобретенного иммунодефицита (СПИД).
Клинически данное заболевание проявляется как увеит (передний, средний или задний). Однако из-за отсутствия патогномоничных признаков изолированный иридоциклит, вызванный ЦМВ, не верифицируется, а также является, по-видимому, достаточно редким. Медленный кровоток в сосудах хориоидеи, плотное прилегание сетчатки предопределяет более частое развитие хориоретинита. В острой стадии на глазном дне выявляются ватообразные очаги или обширные площади белесоватой сетчатки, гистологически – некротически измененной, геморрагии. Если этиологическое лечение не было проведено, процесс распространяется на остальные отделы сосудистого тракта, возникает панувеит.
Офтальмологические осложнения при данном заболевании нередки. К ним можно отнести осложненную катаракту, кистозный макулярный отек, атрофию зрительного нерва, отслойку сетчатки [4]. Проведенное своевременно этиотропное лечение устраняет риск потери остроты зрения в связи с инфекцией, но возникшая отслойка сетчатки может послужить причиной его утраты. Лечение таких пациентов сопряжено с рядом трудностей: тяжелое соматическое состояние больного, невозможность пребывания в стационаре общего профиля (туберкулез легких), ятрогенная полипрагмазия и связанный с этим токсический гепатит, позднее обращение к офтальмологу и другие. Тактика лечения таких пациентов, в том числе хирургического, не определена, описана в литературе в рамках единичных клинических случаев [3] и требует изучения и уточнения.
Охарактеризовать клинические особенности течения отслоек сетчатки при ВИЧ-инфекции.
Материалы и методы
Работа проводилась в Санкт-Петербургском Центре по профилактике и борьбе со СПИД и инфекционными заболеваниями (далее – Центр), городской многопрофильной больнице №2 и кафедре офтальмологии СЗГМУ им. И.И. Мечникова.
В процессе работы были выявлены 80 пациентов с диагнозом ЦМВ-увеит, обращавшихся в рамках диспансерного наблюдения к офтальмологу Центра. Критериями включения являлись: ВИЧ-инфекция, подтвержденная реакцией иммунного блоттинга, выявленный клинически ЦМВ-увеит, осложненный отслойкой сетчатки, положительная полимеразноцепная реакция (ПЦР) в режиме реального времени к ДНК ЦМВ в плазме крови. Критериями исключения являлась другая сопутствующая патология глазного дна. Согласно критериям 8 пациентов были исключены из анализа в связи с отсутствием в амбулаторной карте положительной ПЦР ЦМВ в плазме крови. Из оставшихся была сформирована группа для исследования из 29 пациентов, 34 глаза (9 мужчин и 20 женщин).
Все пациенты подвергались стандартному рутинному офтальмологическому обследованию (визометрия, периметрия, биомикроскопия, офтальмоскопия, тонометрия). Для уточнения диагноза также проводились ультразвуковое исследование глаз в режиме В-сканирования и оптическая когерентная томография. Исследовались лабораторные показатели в периферической крови: содержание CD4-лимфоцитов при выявлении заболевания, а также при окончании этиотропного лечения, уровень репликации РНК ВИЧ (вирусная нагрузка) и ДНК ЦМВ.
У всех пациентов диагностирована 4в стадия ВИЧ-инфекции по классификации В.И. Покровского, 2001. Путь передачи ВИЧ-инфекции был преимущественно половой гетеросексуальный (при гомосексуальных контактах – в 3 случаях, при инъекционном введении психоактивных веществ – у 4 больных). Во всех случаях начата антиретровирусная терапия и проведено этиотропное лечение (внутривенное введение ганцикловира или таблетированный валганцикловир перорально). У двух человек также применялся ганцикловир интравитреально.
Для статистического анализа применялись методы параметрической и непараметрической статистики, программа R (R Development Core Team (2009). R: A language and environment for statistical computing. R Foundation for Statistical Computing, Vienna, Austria). Рассчитывались: среднее, стандартное отклонение среднего, медиана, межквартильный размах (25%-75% квартили), 95% доверительный интервал для долей при помощи углового отклонения Фишера и для медианы методом бутстрепа. Для сравнения групп использовались непараметрические методы: t-бутстреп и вложенный t-бутстреп для связанных переменных.
Результаты и обсуждение
Отслойка сетчатки была выявлена у 29 пациентов (34 глаза) из 72 (94 глаза) и составила 40,3% (95%ДИ=29,3-51,79%).
Средний возраст пациентов на момент развития увеита составил 39 л (стандартное отклонение 6,9 л, n=29). У 16 пациентов отмечался двусторонний ЦМВ-увеит. При этом у 5 человек была выявлена двусторонняя отслойка сетчатки.
Иммунологические показатели в группе наблюдения имели ненормальное распределение (табл. 1). Медиана содержания CD4-лимфоцитов составила 37 кл/мкл, являясь меньшим в сравнении с полученными ранее данными [5]. Вероятно, более выраженный уровень иммунодепрессии предопределяет площадь поражения ретинальной ткани, выраженность экссудативной реакции и скорость развития процесса.
Как видно из таблицы 1, вирусная нагрузка характеризовалась значительным разбросом показателей: от неопределяемой до 4,5 млн копий. Необходимо отметить, что развитие ЦМВ-увеита при подавленном размножении ВИЧ в крови на фоне АРВТ позволяет говорить о развитии поражения органа зрения в рамках синдрома иммунной реконституции.
Содержание ДНК ЦМВ в крови определялось количественным методом и равнялось 2,39 lg копий на 105 клеток. ЦМВ-увеит выявлялся даже при малых значениях уровня ЦМВ в плазме крови, а также не определялся у некоторых пациентов, не включенных в анализ. К сожалению, данный показатель не в полной мере отражает происходящие в глазу процессы.
Отслойка сетчатки является угрожающем зрению состоянием, и в отсутствии хирургической помощи приводит к полной его потере, развитию дистрофических процессов в глазу и субатрофии. Медиана остроты зрения в начале заболевания составила – 0,125 и значимо снизилась к моменту последнего осмотра (0 (ноль), p=0,0044, вложенный t-бутстреп). При проведении статистического анализа и математической оценки светоощущение было приравнено к остроте зрения равной 0 (нулю), так как фактически пациенты из группы исследования с таким зрением теряли способность к самообслуживанию в случае двустороннего увеита.
Полная слепота развилась на 18 глазах, у двух человек отмечалась двусторонняя полная потеря зрения. Также у двоих пациентов острота зрения лучше видящего глаза соответствовала неправильной светопроекции, определяемой локально в эксцентричных положениях в соответствии с расположением участков сетчатки, наименее затронутой воспалительным процессом.
Такие зрительные результаты после лечения объясняются малым количеством пациентов, получившим хирургическую помощь. Препятствием к этому послужило множество причин: позднее обращение за медицинской и/или офтальмологической помощью, тяжелый коморбидный фон, выраженная тромбоцитопения в результате угнетения кровяного ростка в целом как одного из симптомов СПИДа, открытые формы туберкулеза легких, стигматизация пациента медицинскими работниками и другие.
Хирургическое лечение было проведено только на 13 глазах. В структуре проводимых вмешательств преобладала витрэктомия (n=9), в ряде случаев дополненная эписклеральным пломбированием (n=3). При всех вмешательствах также была выполнена лазерная коагуляция сетчатки. Острота зрения в группе пациентов с оперированной отслойкой сетчатки стала достоверно ниже при сравнении в начале заболевания и после проведения комплексного лечения (антретровирусного, этиотропного, консервативного и хирургического): Mean1 (Vis)=0,49; Mean2 (Vis)=0,17; p=0,0009. Следует обратить внимание, что только у 4 пациентов операция была произведена в период этиотропного лечения ЦМВ-увеита, а у всех остальных хирургическое лечение потребовалось в отдаленные сроки, значительно позднее стихания острого воспалительного процесса. Только 2 пациента были прооперированы в первые 1,5 месяца от выявления глазного заболевания. Косвенно это свидетельствует о хроническом вялотекущем прогрессирующем течении ЦМВ-увеита, несмотря на все проводимые лечебные мероприятия.
По механизму отслойки сетчатки были выделены следующие формы: острый некроз сетчатки, регматогенная и тракционная отслойки. Обращает на себя внимание тот факт, что в 50% случаев заболевание протекало как острый некроз сетчатки ЦМВ-этиологии (17 больных), что не находит отражения в литературе по данной тематике. В 41,2% случаев первопричиной являлся разрыв ретинальной ткани, и отслойка не имела такого молниеносного течения. В 11,7% случаев имела тракционный характер и предположительно была связана с недостаточно эффективной высокоактивной антиретровирусной или этиотропной терапией.
Персистирование отслоенной ретины приводило к поддержанию вялотекущего воспалительного процесса в глазу. 10 из 29 человек (12 глаз) при диспансерном наблюдении предъявляли жалобы на эпизоды покраснения глазного яблока, дискомфорт в них, боли. При проведении осмотра были выявлены два или более симптомов: гиперемия, преципитаты на эндотелии роговицы, появление/увеличение задних синехий радужки по площади, снижение прозрачности хрусталика, цилиарная болезненность, усиление витреита в динамике. Кроме того, у 5 больных были данные признаки, несмотря на отсутствие жалоб при активном расспросе.
1. ЦМВ-увеит имеет хроническое вялотекущее течение, несмотря на мультикомпонентное лечение.
2. Отслойка сетчатки выявляется у 40% ВИЧ-инфицированных пациентов с ЦМВ-увеитом и в половине случаев имеет характер острого некроза сетчатки.
3. При отсроченном развитии отслойка сетчатки чаще является регматогенной.
4. Пациенты с ЦМВ-увеитом редко получают необходимое хирургическое лечение в сроки, предусмотренные экстренной помощью.
Читайте также:

