Лечение остроконечных кондилом и инфекции впч
Обновлено: 19.04.2024
Распространенность папилломавирусной инфекции в РФ составляет от 29,1 до 44,8%. Результаты различных исследований показывают, что важнейшим фактором канцерогенеза шейки матки является инфицирование женщин вирусом папилломы человека (ВПЧ). Некоторые исследования доказывают связь цервикальной интраэпителиальной неоплазии (ЦИН) и рака шейки матки (РШМ) с определенными вариантами генов HLA I и II класса. Полиморфизм генов НLA I и II класса определяет генетическую предрасположенность к папилломавирусной инфекции и развитию ЦИН и РШМ. Различные типы ВПЧ были выявлены в 99,7% биоптатов при РШМ. По данным последних исследований, ВПЧ является причиной РШМ в 100% случаев, рака прямой кишки — в 90% случаев, рака вульвы и влагалища — в 40%, рака ротоглотки — примерно в 12%, рака ротовой полости — в 3%.
В статье обсуждаются актуальные вопросы эпидемиологии папилломавирусной инфекции, подходы к диагностике и лечению больных с аногенитальными бородавками, приведен клинический случай. Использование инозина пранобекса (Изопринозин) в качестве иммуномодулятора способствует эрадикации вируса папилломы человека, минимизирует частоту рецидивов аногенитальных бородавок и препятствует персистенции вируса с последующей вероятностью эпителиальных трансформаций у мужчин и женщин.
Ключевые слова: вирус папилломы человека, эпидемиология, пути передачи, аногенитальные бородавки, инозин пранобекс, Изопринозин.
Pointed warts: current treatment modalities and treatment compliance
А.А. Khryanin 1 , G.Yu. Knorring 2
1 Novosibirsk State Medical University, Novosibirsk, Russian Federation
2 A.I. Evdokimov Moscow State Medical and Dental University, Moscow, Russian Federation
The prevalence of papillomavirus infection in Russia ranges from 29.1% to 44.8%. Various studies demonstrate that infection with human papillomavirus (HPV) is the major risk factor for cervical cancer (CC). Some studies establish the association between cervical intraepithelial neoplasia (CIN) and CC and certain variants of HLA class I and II genes. Polymorphism of HLA class I and II genes determines genetic predisposition to papillomavirus infection and the development of CIN and CC. Various subtypes of HPV were identified in 99.7% of biopsy specimens in CC patients. Recent findings suggest that HPV accounts for CC in 100%, rectal cancer in 90%, vulvar and vaginal cancer in 40%, oropharyngeal cancer in 12%, and oral cancer in 3%.
The paper discusses important issues of papillomavirus infection epidemiology, diagnostic and treatment approaches to anogenital warts. Clinical case is described. Immunomodulating agent inosine pranobex (Isoprinosine ® ) provides HPV eradication, minimizes recurrence rate of anogenital warts, and prevents virus persistence with further chances of epithelial transformations both in men and women. Clinical trials on this agent has finished in 20th century, therefore, bibliography includes old references.
Keywords: human papillomavirus, epidemiology, routes of transmission, anogenital warts, inosine pranobex, Isoprinosine ® .
For citation: Khryanin А.А., Knorring G.Yu. Pointed warts: current treatment modalities and treatment compliance. Russian Journal of Woman and Child Health. 2019;2(2):–101.
В статье обсуждаются актуальные вопросы эпидемиологии папилломавирусной инфекции, подходы к диагностике и лечению больных с аногенитальными бородавками, приведен клинический случай.
Введение
Проблема папилломавирусной инфекции (ПВИ), вызываемой вирусами папилломы человека (ВПЧ), представляющими собой большую гетерогенную группу вирусов, очень актуальна. Данная группа вирусов обладает онкогенными свойствами и вызывает развитие доброкачественных или злокачественных новообразований. Определенные типы папилломавирусов играют этиологическую роль в патогенезе рака шейки матки (РШМ) [1]. Около 40 генитальных типов ВПЧ обладают тропностью к слизистым оболочкам аногенитальной области. Инкубационный период ПВИ в среднем составляет 3 мес. (от 3–4 нед. до 8 мес.). ПВИ поражает от 29,1 до 44,8% населения в РФ. Многочисленные эпидемиологические, клинические и молекулярно-биологические исследования показывают ведущую роль инфицирования женщин ВПЧ в канцерогенезе шейки матки [1, 2]. Женщины с определенными вариантами генов HLA I и II класса более подвержены цервикальной интраэпителиальной неоплазии (ЦИН) и РШМ. Для элиминации вирус-инфицированных клеток из организма необходимо распознавание ВПЧ-антигенов продуктами генов основного комплекса гистосовместимости HLA I и II класса. Полиморфизм генов НLA I и II класса определяет иммунологическую чувствительность к инфицированию ВПЧ, поэтому генетическая предрасположенность может быть важна для развития ЦИН и РШМ [1–5].
В 99,7% биоптатов при РШМ (как при плоскоэпителиальных карциномах, так и при аденокарциномах) выявляли различные типы ВПЧ [3]. По данным последних эпидемиологических и вирусологических исследований, ВПЧ является причиной РШМ в 100% случаев, рака прямой кишки — в 90% случаев, рака вульвы и влагалища — в 40%, рака ротоглотки — примерно в 12%, рака ротовой полости — в 3% [3].
Возникновение остроконечных кондилом у партнера; заражение обоих партнеров одним типом вируса; крайне редкая заболеваемость у женщин, никогда не практиковавших вагинальные контакты; подтвержденная многими исследованиями прямая связь между количеством половых партнеров в течение жизни (и у мужчин, и у женщин в равной степени) и риском заражения; высокий риск заражения от нового полового партнера, страдающего данной инфекцией, — все это свидетельствует в пользу прямого пути передачи ВПЧ при половом контакте. Существуют и другие пути передачи, кроме полового, но они не имеют существенного значения [4].
В настоящее время известно, что использование презервативов не гарантирует 100% защиты, а только снижает риск передачи ВПЧ [4, 5], особенно это относится к презервативам 1-го поколения. Очевидно, что столь популярный индивидуальный метод профилактики инфекций, передающихся половым путем (ИППП), не обеспечивает выраженной защиты от вирусных инфекций (вируса простого герпеса и ВПЧ) даже при правильном и постоянном их использовании.
Среди факторов риска заражения ВПЧ на первом месте стоит ранний сексуальный дебют. Раннее начало половой жизни может быть маркером рискованного сексуального поведения и соответственно большого числа половых партнеров в течение жизни или конкурентного партнерства. Кроме того, не исключена роль биологических механизмов: инфицированию могут способствовать незрелость шейки матки, неадекватная продукция протективной цервикальной слизи и шеечная эктопия [7, 8].
В организме человека ВПЧ инфицирует базальный слой эпителия, причем наиболее сильно поражается зона трансформации многослойного плоского эпителия в цилиндрический эпителий. В инфицированной клетке ВПЧ паразитирует в доброкачественной эписомальной (вне хромосом клетки) и злокачественной интегрированной (встроенной в геном клетки) формах. По способности трансформировать эпителий слизистой шейки матки вирусы условно разделяют на низкоканцерогенные, высококанцерогенные и вирусы неустановленного канцерогенного риска [9]. К первой группе традиционно относят 6, 11, 42, 43, 44 типы, которые чаще оказывают продуктивное воздействие, результатом которого являются аногенитальные бородавки. Инфекция, вызванная ВПЧ низкого онкогенного риска, обычно протекает доброкачественно. Ко второй группе относят 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68 типы ВПЧ, они могут трансформировать эпителий слизистой оболочки шейки матки, вызывая ЦИН, которые могут прогрессировать в плоскоклеточную карциному и аденокарциному. Типы 30, 34, 40, 53, 54, 55, 57, 61, 62, 64, 67, 69, 70, 72, 73, 80, 82 и другие, недавно открытые, считаются вирусами невыясненного канцерогенного риска [10, 11].
Стадии ПВИ
Персистенция ВПЧ в организме (или латентное течение) — вирус существует в эписомальной форме, не вызывая патологических изменений в клетках; клинических проявлений нет; определить наличие вируса можно только с помощью молекулярно-биологических методов.
Лабораторная диагностика ПВИ
Выявление нуклеиновых кислот (ДНК/РНК) ВПЧ высокого онкогенного риска методами гибридизации нуклеиновых кислот (МГНК) и/или амплификации нуклеиновых кислот (МАНК) лежит в основе молекулярно-биологического исследования. МАНК имеют большую чувствительность и позволяют обнаружить вирус в концентрациях намного меньших, чем предел обнаружения ВПЧ другими лабораторными методами, включая МГНК. Большое диагностическое значение имеют МАНК на основе полимеразной цепной реакции (ПЦР), которые позволяют не только выявлять и дифференцировать группы ВПЧ высокого и низкого канцерогенного риска, но также идентифицировать отдельные филогенетические группы и типы ВПЧ. Тест на ВПЧ обладает гораздо более высокой чувствительностью для выявления ЦИН, чем цитологическое исследование. Однако в качестве диагностического критерия неопластических процессов шейки матки этот метод непригоден. Примерно в 80% случаев инфицирование имеет кратковременный характер и заканчивается спонтанным выздоровлением и элиминацией ПВИ. Положительный результат лабораторного исследования на ДНК ВПЧ в большинстве случаев не позволяет прогнозировать развитие цервикального рака. Однако если на фоне ВПЧ-инфекции уже имеется картина дисплазии эпителия шейки матки, то этот метод можно использовать для прогнозирования неопластических процессов. Генотипирование вируса позволяет дифференцировать персистирующую инфекцию от реинфекции [12].
Одним из критериев клинически значимой инфекции, способной развиться в заболевание, является высокая вирусная нагрузка. Показатель спонтанной элиминации вируса ниже, а риск прогрессии выше в случаях ПВИ с более высокой вирусной нагрузкой. Определение вирусной нагрузки позволяет прогнозировать элиминацию ВПЧ либо прогрессирование инфекции до дисплазии. При вирусной нагрузке менее 3 логарифмов на 10 5 клеток риск развития дисплазии минимален, наблюдается почти 100% спонтанная регрессия. Вирусная нагрузка более 5 логарифмов на 10 5 клеток свидетельствует о наличии дисплазии или высоком риске ее развития, снижение вирусной нагрузки более чем на 1 логарифм за 6 мес. является динамическим маркером транзиторной инфекции [12, 13].
В настоящее время использование вирусной нагрузки как маркера риска неопластической прогрессии в клинической практике по ряду причин затруднительно. Во-первых, данный подход требует стандартного забора материала с достаточным количеством эпителиальных клеток. Во-вторых, необходимо использовать тесты, позволяющие определять истинную концентрацию вирусной ДНК и концентрацию клеток в образце. Точную количественную оценку ДНК ВПЧ можно провести только с применением метода ПЦР в реальном времени [12].
Исследования клинического материала с помощью МАНК должны проводиться с использованием коммерческих тест-систем (наборов реагентов), предназначенных для скрининга и диагностики ПВИ, апробированных в скрининговых исследованиях, прошедших процедуру государственных испытаний согласно действующему законодательству РФ и имеющих регистрационные удостоверения [12].
Клинические проявления ПВИ
Методы терапии ПВИ
Клиническое наблюдение

К врачу обратился 23-летний мужчина с множественными опухолевидными разрастаниями на половом члене, появившимися в течение 2–3 мес. (рис. 1 А). В анамнезе — ВИЧ-инфекция (менее 1 года) после незащищенного сексуального контакта с малознакомой женщиной. После обсуждения вариантов лечения было выбрано комбинированное лечение
Изопринозином и хирургическое иссечение опухолевидных разрастаний. По результатам гистологического исследования была диагностирована гигантская кондилома Бушке — Левенштейна (разновидность остроконечной кондиломы, отличающаяся прогрессирующим ростом и большими размерами). Перед началом терапии пациент был обследован на ИППП. Методом ПЦР выявлена хламидийная инфекция и рекомендована этиотропная терапия (доксициклина моногидрат). На повторном визите отмечена положительная динамика в разрешении процесса (рис. 1 В).
Заключение
Таким образом, использование инозина пранобекса (Изопринозин) способствует в большинстве случаев полной эрадикации ПВИ, минимизирует частоту рецидивов, а также препятствует персистенции вируса с последующей вероятностью эпителиальных трансформаций, которые имеют тяжелые онкологические последствия.
Что такое кондиломы остроконечные? Причины возникновения, диагностику и методы лечения разберем в статье доктора Богданова Дениса Валерьевича, проктолога со стажем в 21 год.
Над статьей доктора Богданова Дениса Валерьевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Остроконечные кондиломы — образования на коже, вызванные наличием в тканях вируса папилломы человека (ВПЧ). Активизация вирусов приводит к появлению разрастаний на поверхности кожи в области заднего прохода, наружных половых органов и анальном канале.
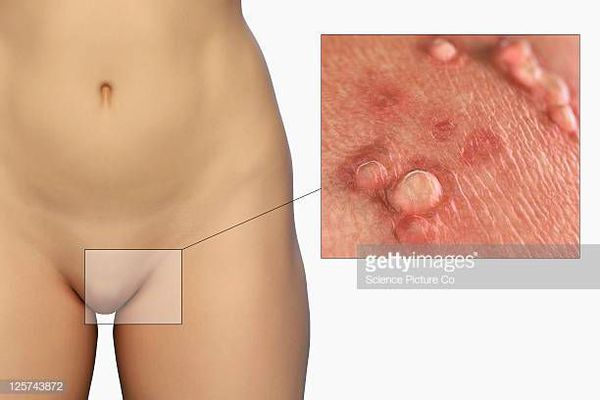
Аногенитальные бородавки представляют собой выступающие над поверхностью кожи объёмные мягкие выросты бледно-розового цвета с неоднородной поверхностью. Размеры и количество бородавок варьируются от единичных кондилом 1-2 мм в диаметре до множественных, часто сливных образований размером до 9-10 см и даже более.
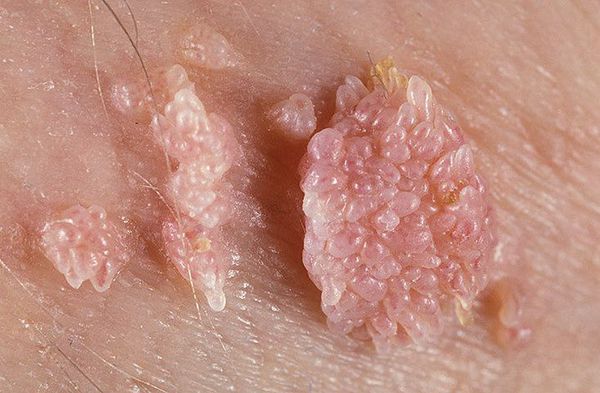
Кондиломы могут появляться и вырастать до значительных размеров буквально за несколько дней.
Причиной появления кондилом является присутствие вируса папилломы человека в крови. В организм вирус попадает при половом контакте через дефекты в слизистой или коже. Возможен перинатальный путь передачи — ребёнок заражается во время родов от больной матери при прохождении по родовым путям. Также имеет место контактно-бытовой путь передачи, но данные об этом варианте передачи немногочисленны.
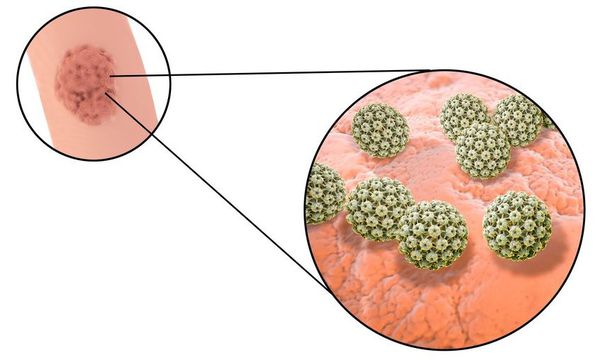
Длительное время после заражения человек может не подозревать о своём носительстве ВПЧ. Период инкубации зависит от особенностей иммунитета индивида и может длиться от двух месяцев до трёх лет. В дальнейшем, при снижении активности иммунных механизмов, в характерных локациях появляются бородавки (кондиломы). [7] [8] [16]
ВПЧ относится к одной из наиболее частых инфекций, передающихся половым путём (ИППП) — до 55-65% от общего числа заболеваний. [1] [4] [6] Опасность его состоит также в том, что носитель может не подозревать о своём заболевании и не иметь внешних признаков инфекции (выростов, бородавок).
Известно до 600 видов ВПЧ (HPV), некоторые из которых проявляются бородавками кожи на груди, лице, подмышечных впадинах. Другие выбирают своей локализацией слизистые оболочки рта, половых органов или анального канала. При аногенитальных кондиломах чаще выявляют 6 и 11 типы HPV (папилломавируса). [4]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы остроконечных кондилом
Вне обострения наличие ВПЧ в крови никак не проявляется. При активации вирусной инфекции симптомы болезни могут появиться буквально за несколько часов:
- образование остроконечных кондилом (чаще в местах наибольшей травматизации, трения при половом контакте):
– на коже вокруг ануса, в промежности, на уздечке, головке полового члена, губках наружного отверстия мочеиспускательного канала у мужчин;
– на слизистой половых губ у женщин, в уретре у мужчин;
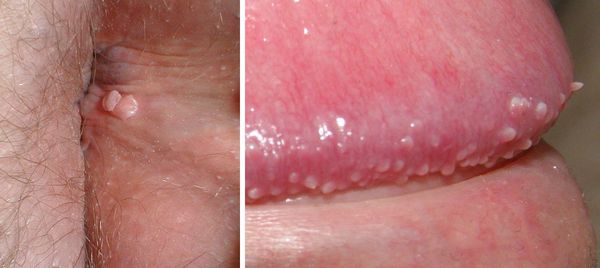
- зуд, жжение, дискомфорт в месте появления бородавок — такие неприятные ощущения часто бывают очень интенсивными и значительно влияют на самочувствие пациента;
- ощущение инородного предмета в анальном канале (при образовании кондилом внутри заднепроходного отверстия);
- выделение небольшого количества крови в виде алых полосок при дефекации (если кондиломы расположены внутри анального канала и травмируются при прохождении каловых масс);
- дизурия, болезненность при мочеиспускании, если бородавки находятся в уретре;
- болезненность во время полового акта (диспареуния).
Другим вариантом проявления ВПЧ может стать наличие в области промежности папул с бархатистой поверхностью или пятен серовато-бурого, розового или красновато-коричневого цвета. [2] Такие морфологические формы встречаются намного реже и часто вызывают затруднение при постановке первичного диагноза.
Патогенез остроконечных кондилом
Ключевым моментом в патогенезе заболевания становится проникновение HPV в организм хозяина. При однократном половом контакте вероятность заражения составляет 80%, затем при хорошем состоянии иммунной системы инфекционные агенты подвергаются элиминации (уничтожаются).
Вирусы различных типов адаптированы к определённому хозяину. Существуют сотни типов вирусов, многие из них не опасны для человека, так как тропны к тканям млекопитающих, рептилий и птиц и вызывают у них доброкачественные опухоли (образование папиллом). [3]
При изучении ВПЧ выделили три рода вирусов — альфа, бета, гамма. Из них аногенитальные поражения вызывают папилломавирусы первой группы (α). Инфекционные агенты, относящиеся к родам Бета и Гамма, чаще встречаются при папилломах ороговевающего эпителия [3] — появляются подошвенные, ладонные бородавки.
В родах при классификации вирусов выделили типы (генотипы). Они обозначаются арабскими цифрами. Из сотни генотипов вирионов выделяют частицы с высоким канцерогенным риском – это α 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59. Их выявляют в 90-95% случаев при злокачественных процессах шейки матки, влагалища и вульвы. Особенно значимы 16 и 18 типы. Такие онкогенные типы ВПЧ, содержащие в своём ДНК белки Е6 и Е7, способны подавлять активность белков-супрессоров опухолей р53 и рRb, приводя к быстрому злокачественному перерождению папиллом в карциномы.
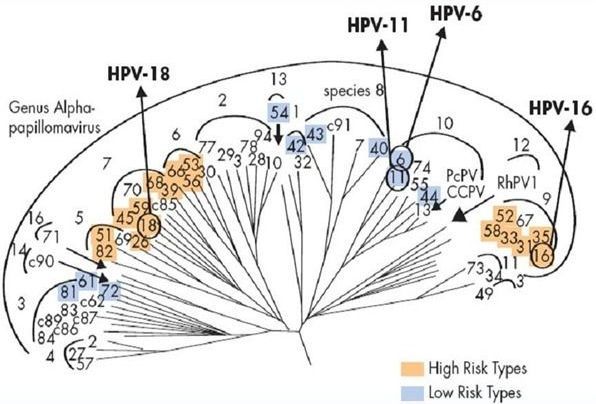
Порядка 90% случаев аногенитальных кондилом вызываются ВПЧ α 6 и 11. Это возбудители низкого канцерогенного риска. [5] К этой же группе низкого риска относят ВПЧ 40, 42, 43, 44, 54, 61, 72, 81.
Проникновение
Вирионы через микроскопические повреждения проникают в базальный слой эпителия, затем прикрепляются к белкам мембраны клетки. Далее они задействуют механизм рецепторного эндоцитоза (при участии интегрина и белка L1 из вирусного капсида) и попадают в цитоплазму. Белок L2 из капсида вируса способствует высвобождению ДНК вируса и попаданию его в ядро. [5]
Размножение
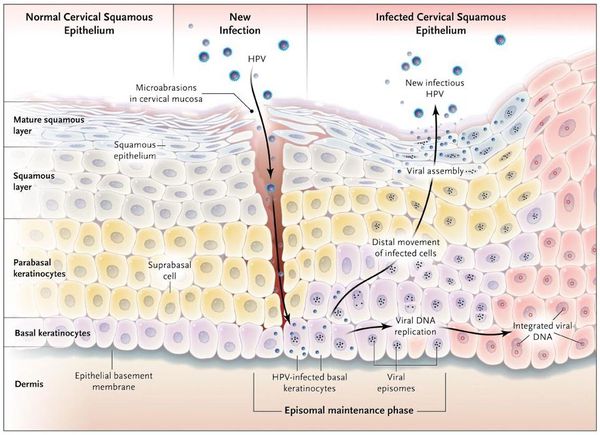
Проявления
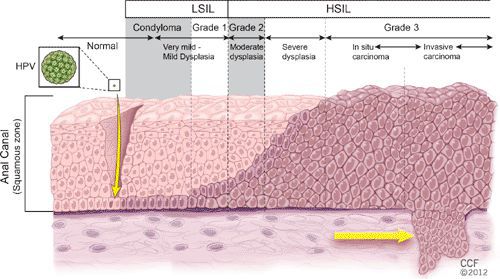
Появляются аномальные эндофитные или экзофитные выросты эпителия — папилломы, пятна или кондиломы. Рыхлая слизистая или атипичный эпителий выростов склонен к быстрой травматизации и мацерации (размягчению). На таком фоне быстрее присоединяется вторичная инфекция, появляются болезненность, дискомфорт, обильное отделяемое, воспаление, отёк, неприятный запах, изъязвление кондилом. [2] [3]
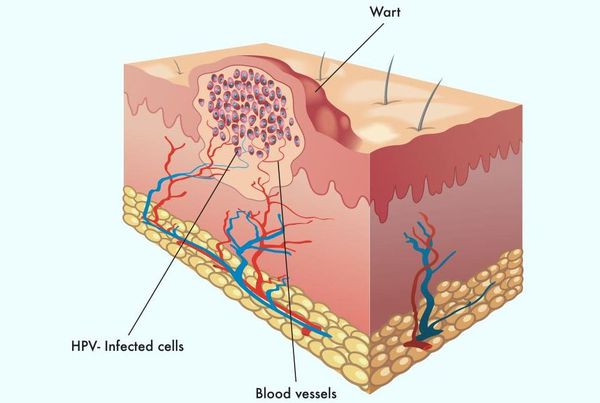
В клетках базального слоя происходит активная репликация вируса, по мере дифференцировки клеток кондилом их кровоснабжение резко обедняется, редуцируют центральные сосуды. Но, оставаясь в верхних слоях эпителия в неактивной форме, именно здесь вирус опасен в плане контактного инфицирования.
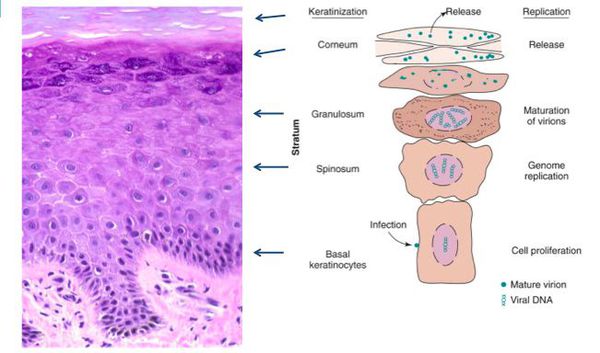
При гистоанализе биопсийных материалов эпителий утолщён, выявляются участки акантоза, папилломатоза. Обнаруживаются койлоциты (изменённые в размерах клетки со светлой цитоплазмой, множеством вакуолей, перинуклеарным светлым ободком). Их ядра гиперхроматичны. Часто встречаются клетки с двумя ядрами и более. [8]
Из вышеперечисленного можно сделать вывод: вирусы, вызывающие образование аногенитальных бородавок, в 90% случаев относятся к типам α 6 и 11 HPV. [6] [7] Они с низкой степенью вероятности могут вызвать малигнизацию (раковое перерождение). Однако часты случаи совместной персистенции (пребывания) вирусов различных типов у одного носителя. Это обязывает пациента и доктора особенно внимательно относится к профилактическим осмотрам, их качеству и регулярности для предотвращения аноректального рака.
Классификация и стадии развития остроконечных кондилом
Остроконечные кондилломы являются наиболее частыми, классическими проявлениями папилломавирусной инфекции кожи и слизистых в аногенитальной области — до 65% от числа заболеваний, передающихся половым путёv. [1]
Другими диагностическими находками могут быть:
- бородавки в виде папул;
- инфильтрация слизистой в виде пятен розовато-серого или коричневого цвета;
- внутриэпителиальная неоплазия;
- бовеноидный папулёз, болезнь Боуэна — отдельный вид папул, они появляются как пятна на слизистых красновато-бурого, оранжево-бурого цвета, на коже цвет образований серовато-розовый;
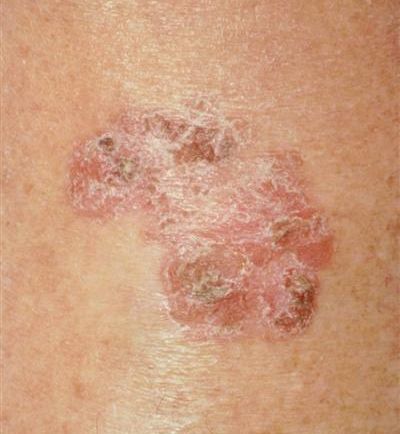
- гигантская папиллома (Бушке — Левенштейна). Её рост начинается с остроконечных кондилом, которые довольно быстро увеличиваются в размерах и количестве, сливаются и превращаются в крупную опухоль с неровной поверхностью, покрытой вегетациями и ворсинчатоподобными выступами.
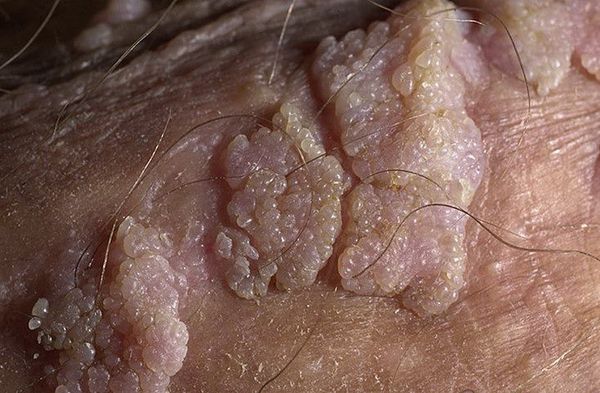
Хотя болезнь (гигантская папиллома) ассоциируется с типами вирусов 6 и 11, с низким риском канцерогенеза, именно в случаях гигантских папиллом происходит подавление белка-супрессора опухолей р53, и образование трансформируется в плоскоклеточный рак. Причиной такой частой малигнизации (озлокачествления) может быть наличие иммунодефицитных состояний, ассоциированных инфекций, хронических дистрофических состояний кожи (склероатрофический лихен, красный плоский лишай). Даже после радикального хирургического лечения [9] папиллома Бушке — Левенштейна склонна к частому рецидивированию. [10]
Осложнения остроконечных кондилом
Эстетические проблемы. Быстро разрастающаяся ткань кондилом, помимо физического дискомфорта, приносит массу неудобств пациенту. Выросты в области наружных половых органов, заднего прохода значительно снижают самооценку и мешают полноценной половой жизни и правильной гигиене.
Нагноение, воспаление. Аногенитальные бородавки имеют свойство быстро травмироваться при незначительных механических воздействиях или трении. Эти микротравмы, ранки становятся воротами для вторичного инфицирования. Появляются эрозии, перифокальное воспаление. Раны начинают мацерироваться (мокнуть), нагнаиваться. При развитии осложнения присоединяются неприятный запах и боль. Проводить тщательную гигиеническую обработку перианальной области из-за разрастаний становится невозможным, что ещё больше усугубляет воспалительный процесс.
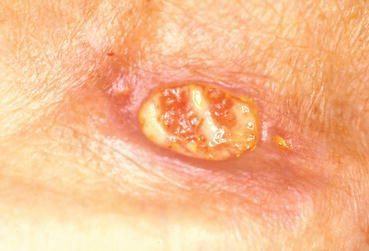
Малигнизация. Типы вирусов с высокой канцерогенной активностью, персистируя (долго находясь) в коже и слизистых, приводят к трансформации клеток и их перерождению в атипичные (раковые) клетки. Как уже упоминалось, аногенитальные бородавки обычно не так опасны в плане раковой трансформации, как вирусное поражение шейки матки (ВПЧ 16, 18 типов и т. д). Но проблема может появиться, если у пациента присутствует два и более типов вируса с различными индексами канцерогенности и имеется иммунодефицитное состояние.
Важно изменение образа жизни в целом для постоянного поддержания здоровья и предупреждения активизации дремлющих вирионов.
Диагностика остроконечных кондилом
При выявлении остроконечных кондилом в перианальной зоне целью дополнительных диагностических исследований является уточнение генотипа ВПЧ, а также исключение внешне схожих с ними образований:
- интрадермальный невус;
- контагиозный моллюск;
- сифилитический шанкр;
- себорейный кератоз.
Быстрым способом установления ВПЧ в образованиях (кондилломах) во время приёма является проба с 5% раствором уксусной кислоты. Под воздействием этого вещества папилломы, вызванные HPV, бледнеют, приобретая сероватый, бледный оттенок, в них визуализируется характерный капиллярный рисунок. Исследование носит предварительных характер.
Минимальные лабораторные исследования:
- серологическая реакция на возбудителей сифилиса;
- обнаружение антител к ВИЧ, гепатитам В,С;
- ПЦР для типирования вируса;
- цитология мазка из шейки матки у женщин;
- цитология мазков-отпечатков;
- исследование биоптатов и удалённых образований — аногенитальных бородавок.
При частых рецидивах болезни, крупных размерах опухолей, быстром их росте или сомнительном диагнозе прибегают к дополнительным методам исследования.
При частых обострениях проводится исследование имунного статуса.
При подозрении на злокачественное перерождение кондилом, папилломах на широком основании, нетипичных выделениях из влагалища или прямой кишки проводят:
- УЗИ вагинальным и ректальным датчиком;
- колоноскопию;
- УЗИ органов брюшной полости;
- рентгенографию органов грудной клетки;
- кольпоскопию;
- исследования на ИППП . [1][12][13]
Часто пациенты направляются на консультацию к гинекологу, урологу, онкологу и дерматовенерологу.
Лечение остроконечных кондилом
В случае с остроконечными кондиломами наиболее результативен комплексный подход к лечению. Следует обязательно информировать пациента о необходимости лечения половых партнёров, их возможном носительстве ВПЧ.
Даются общие рекомендации о необходимости модификации образа жизни для поддержания адекватного состояния иммунитета, предупреждения дополнительного инфицирования другими ИППП:
- упорядочение половой жизни;
- применение барьерных методов контрацепции;
- коррекция веса;
- достаточные физические нагрузки;
- правильное питание и т. д.
Консервативное лечение
Применяются препараты, стимулирующие местный и гуморальный иммунный ответ. Это необходимо, так как у всех больных с папилломатозным поражением выявлялись нарушения интерферонового статуса (системы врождённого иммунитета). [1] Противопоказаниями к терапии иммуномодуляторами являются папилломы на широком основании.
Редуцирование симптомов возможно в трёх из четырёх случаев (до 84%) при единичных кондиломах небольших размеров. [1] [17]
При упорном, рецидивирующем течении болезни, а также если больного беспокоят эстетические моменты, для профилактики раковой трансформации прибегают к хирургическим методам.
Хирургическое лечение
В зависимости от размеров, формы, расположения кондиломы и предпочтений хирурга возможно применение химических, физических, цитотоксических методов удаления.
Физические методы применяются при любых размерах и расположении аногенитальных бородавок. По выбору используется скальпель, лазерная вапоризация, криодеструкция (разрушение ткани бородавки экстремально низкими температурами под воздействием жидкого азота) или радиоволновой способ (radioSURG).
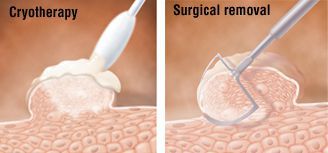
Ткани иссекаются включительно с собственной пластиной дермы. Если удаляется кондилома анального канала, дно раны образует внутренний сфинктер. В перианальной зоне дно раны должна составлять подкожная клетчатка.
Удаление образований не проводится без консультации онколога, если есть малейшие подозрения на малигнизацию (изъязвление, некроз, инфильтративный рост).
Обычно при иссечении кондиломы достаточно местной или спинальной анальгезии (снижения чувствительности к боли). Госпитализация может проводиться в случаях некоторых сопутствующих заболеваний (патология свертывания и другие), а также при невозможности амбулаторного лечения.
Прогноз. Профилактика
Прогноз при своевременном и адекватном лечении остроконечных кондилом благоприятный. Обязательно проведение гистологического исследования удалённых образований для исключения диагноза злокачественной опухоли. В сомнительных случаях необходимы дополнительные консультации гинеколога, дерматовенеролога, онколога, радиолога, лабораторные и инструментальные исследования.
При комплексном лечении обычно все симптомы исчезают. Однако не исключены рецидивы, частота которых колеблется от 10 до 50% и более. На увеличение риска рецидивов влияет общее состояние здоровья пациента, наличие у него сопутствующих заболеваний и иммунодефицитных состояний.
Профилактика включает в себя:
- своевременное, профилактическое обследование у гинеколога, уролога и проктолога;
- коррекцию образа жизни, питания;
- упорядочение половых отношений.
До начала половой жизни можно по схеме пройти вакцинацию поливалентной вакциной от ВПЧ 6, 11, 16, 18 типов (самые частые причины остроконечных кондилом — HPV 6 и 11) и рака шейки матки (HPV 16 и 18). Рекомендуемый возраст для введения вакцины — 9-17 лет (к примеру, в календаре США от 2015 года рекомендуемы возраст вакцинации — 9-11 лет). В ряде стран (США, Австрия, Германия, Франция и др.) вакцинация включена в календарь обязательных прививок. В России в настоящее время это добровольная процедура. [18]
Остроконечные кондиломы (синонимы: condylomata acuminate, вирусные кондиломы, остроконечные бородавки, генитальные бородавки) относятся к заболеваниям, вызываемым вирусом папилломы человека (ВПЧ). Заболевания, обусловленные ВПЧ, являются одними из на

Остроконечные кондиломы (синонимы: condylomata acuminate, вирусные кондиломы, остроконечные бородавки, генитальные бородавки) относятся к заболеваниям, вызываемым вирусом папилломы человека (ВПЧ). Заболевания, обусловленные ВПЧ, являются одними из наиболее распространенных заразных вирусных инфекций человека. ВПЧ представляет собой небольшой округлый двухспиральный ДНК-вирус диаметром от 50 до 55 нм. На сегодняшний день описано более 80 типов ВПЧ (табл. 1). Инфекции, вызываемые ВПЧ, высокоспецифичны для эпидермиса, так как ВПЧ обладает тропизмом к эпителиальным клеткам кожи и слизистых оболочек.
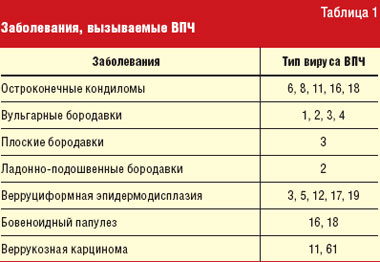
За последние 20 лет отмечается рост заболеваемости остроконечными кондиломами. В США остроконечные кондиломы (или генитальные бородавки) относятся к наиболее часто встречающимся заболеваниям, передающимся преимущественно половым путем. Заболеваемость остроконечными кондиломами превышает 106,5 случая на 100 тыс. населения США, что составляет около 0,1% всей популяции [1]. Пристальное внимание к этому заболеванию объясняется тем, что некоторые из типов ВПЧ, которые вызывают остроконечные кондиломы, могут приводить к малигнизации процесса. Наиболее потенциально опасными являются типы 16 и 18. Неслучайно важно своевременно диагностировать и лечить остроконечные кондиломы. Рецидив остроконечных кондилом не всегда связан с повторным заражением, а может быть вызван реактивацией вируса.
Клиническая картина. Инкубационный период продолжается от 3 нед до 6 мес и в среднем составляет около 2,8 мес. Мужчины и женщины одинаково подвержены этому заболеванию. Средний возраст заболевших колеблется от 22 до 25 лет.
Обычно остроконечные кондиломы локализуются на половых органах и в перианальной области. У ВИЧ-инфицированных пациентов остроконечные кондиломы могут локализоваться в необычных местах, например на лице, веках и ушных раковинах. У мужчин наиболее частая локализация — пенис, уретра, мошонка, перианальная, анальная и ректальная области [2]. Элементы сыпи имеют телесный цвет, могут быть представлены гладкими папулами размером с булавочную головку и на начальных этапах развития не всегда заметны на половом члене. Для их выявления проводят пробу с 5% уксусной кислотой. После обработки кожи окраска папул становится белесоватой. В дальнейшем папулы разрастаются и приобретают бородавчатую или нитевидную форму, напоминая цветную капусту или петушиный гребень. Как правило, остроконечные кондиломы множественные и располагаются группами.
У женщин клиническая картина остроконечных кондилом может быть разнообразной. Классические экзофитные поражения на наружных половых органах носят распространенный характер и легко выявляются при осмотре, однако могут быть и случайными находками при проведении кольпоскопии или ректороманоскопии. На малых половых губах и в преддверии влагалища кондиломы представляют собой влажные, бархатистые или множественные пальцеобразные разрастания и занимают значительную площадь. Кондиломы в цервикальном канале обнаруживаются у 20% женщин, инфицированных ВПЧ и с локализацией остроконечных кондилом на наружных половых органах. Локализация остроконечных кондилом на шейке матки или в цервикальном канале считается неблагоприятным фактором, так как может способствовать развитию рака шейки матки [3].
Даже при своевременном и рациональном лечении остроконечные кондиломы часто рецидивируют. Это связано с тем, что вирус длительное время может сохраняться в инактивированном состоянии во внешне здоровых участках кожи и слизистых оболочках.
Дифференциальный диагноз остроконечных кондилом проводится со вторичным сифилисом (широкие кондиломы), контагиозным моллюском, бовеноидным папулезом, блестящим лишаем, красным плоским лишаем, ангиокератомами, ангиофибромами на венечной борозде головки полового члена, фолликулитами, мягкой фибромой, волосяной кистой (табл. 2).
Диагностика остроконечных кондилом, как правило, клинически не представляет трудности. Дополнительно в некоторых случаях проводят пробу с 5% уксусной кислотой. Для этого смоченную раствором медицинскую салфетку располагают в зоне предполагаемой локализации остроконечных кондилом на 5–10 мин, после чего высыпания приобретают белесоватый оттенок [4].
При установлении диагноза остроконечных кондилом необходимо проводить обследование на сифилис и ВИЧ-инфекцию.
Проведение биопсии показано тем больным, у которых возникает подозрение на предраковые заболевания или плоскоклеточный рак. Удаление остроконечных кондилом не снижает риск развития рака шейки матки. Поэтому всем женщинам, у которых в анамнезе имелись сведения об остроконечных кондиломах, необходимо ежегодно проводить цитологическое исследование мазков с шейки матки с целью своевременного выявления онкологического процесса.
Лечение и профилактика
Использование презервативов снижает риск заражения половых партнеров. Полностью удалить ВПЧ невозможно — можно лишь удалить остроконечные кондиломы, облегчив состояние больного и снизив риск заражения полового партнера. Существует несколько методов лечения остроконечных кондилом. Все они имеют определенные недостатки.
Криодеструкция — один из наиболее часто применяемых методов лечения. Пораженную поверхность обрабатывают жидким азотом с помощью ватного тампона или распылителя. Обработку повторяют каждые 1–2 нед до полного удаления всех кондилом. Метод редко приводит к рубцеванию, отличается невысокой стоимостью. Криодеструкция может вызывать сильную боль. Не всегда можно одномоментно обработать всю пораженную поверхность. В некоторых случаях после криодеструкции может развиваться гиперпигментация или гипопигментация.
Диатермокоагуляция является болезненным методом лечения и оставляет после себя стойкие рубцы, поэтому применяется только для удаления одиночных кондилом.
Удаление лазером осуществляется с помощью углекислотного и неодимового ИАГ-лазеров (лазеров на иттрий-алюминиевом гранате). После удаления могут оставаться рубцы.
Медикаментозные методы лечения. Кондилин (подофиллотоксин) — 0,5% раствор во флаконах по 3,5 мл с аппликатором. Компонент Кондилина подофиллотоксин — наиболее активный в составе растительного экстракта подофиллина, при местном применении он приводит к некрозу и деструкции остроконечных кондилом. Преимущество данного метода лечения состоит в том, что больной может самостоятельно обрабатывать пораженные участки кожи в доступных местах. С помощью пластикового аппликатора препарат наносится на кондилому; постепенно смачиваются все кондиломы, но не более 50 штук за 1 раз (по площади не более 10 см2). Препарат нужно наносить с осторожностью, избегая здоровых участков кожи. Первый раз обработку проводит врач или медсестра, обучая пациента правильно наносить препарат. После обработки препарат должен высохнуть, чтобы не возникло раздражения окружающей кожи или ее изъязвления. Кондилин наносят 2 раза в день в течение 3 дней, а затем делают 4-дневный перерыв. Продолжительность лечения не должна превышать 5 нед. Противопоказанием для применения препарата являются беременность, лактация, детский возраст, применение других препаратов, содержащих подофиллин.
Солкодерм представляет собой смесь кислот: 65% азотной, 98% уксусной, а также молочной и щавелевой кислоты и нитрата меди; выпускается в виде раствора (ампулы по 0,2 мл). После его нанесения на поверхность кожи она окрашивается в желтый цвет, после чего происходит мумификация обработанных тканей. Обработку должен осуществлять медицинский персонал. Препарат наносится на поверхность с помощью стеклянного капилляра или аппликатора, после чего препарат должен высохнуть. Одномоментно допускается обработка площади не более 4–5 см2. При необходимости обработку можно повторить через 4 нед. Нанесение препарата может сопровождаться сильным жжением и болью, в некоторых случаях может возникнуть гиперпигментация и образование рубцов.
Препараты интерферона вводят непосредственно в остроконечные кондиломы. Процедура болезненна и требует проведения повторной обработки.
Трихлоруксусная кислота в концентрации 80–90% наносится непосредственно на кондиломы. Остатки ее удаляют с помощью талька или бикарбоната натрия. При необходимости лечение повторяют с интервалом в 1 нед. Если после 6-кратной обработки остаются остроконечные кондиломы, то необходимо сменить метод лечения.
Литература
Л. П. Котрехова, кандидат медицинских наук, доцент
К. И. Разнатовский, доктор медицинских наук, профессор
СПбМАПО, Москва
Для цитирования: Роговская С.И., Прилепская В.Н., Межевитинова Е.А. КОНДИЛОМЫ ГЕНИТАЛИЙ, ОБУСЛОВЛЕННЫЕ ПАПИЛЛОМАВИРУСНОЙ ИНФЕКЦИЕЙ. РМЖ. 1998;5:6.
В статье изложены современные подходы к диагностике и лечению заболеваний, обусловленных вирусом папилломы человека, подчеркнута актуальность проблемы в связи с широким распространением инфекции и онкогенным потенциалом по отношению к шейке матки.
The paper outlines current approaches to diagnosis and treatment of diseases caused by human papillomavirus, shows the problem to be topical due to the wide spread of the infections and to its oncogenic potential for the cervix. The most common therapies for genital condylomas used in recent years are described .
С.И. Роговская - к.м.н., ст. научн. сотр.
В.Н. Прилепская - проф., д.м.н., руководитель поликлинического отдела
Е.А. Межевитинова - к.м.н., ст. научн. сотр.
Научный центр акушерства, гинекологии и перинатологии (директор - академик РАМН проф. В.И. Кулаков), РАМН, Москва
S.I. Rogovskaya, Candidate of Medical Sciences, Senior Researcher
Prof. V.N. Prilepskaya, Dr. Sci, Head, Outpatient Department,
Ye.A.Mezhevitinova, Candidate of Medical Sciences, Senior Researcher, Research Center of Obstetrics, Gynecology and Perinatology (Director Prof. V.I. Kulakov, Academician of the Russian Academy of Medical Sciences), Russian Academy of Medical Sciences
К ондиломы половых органов, вызываемые вирусом папилломы человека (ВПЧ), являются одним из самых распространенных в мире заболеваний, передающихся половым путем. Проблема их диагностики и лечения привлекает внимание исследователей различных специальностей многих стран ввиду высокой контагиозности и отмеченной тенденции к росту частоты данного заболевания, а также способности ВПЧ инициировать злокачественные процессы нижних отделов половых путей женщины. Доказано, что при раке шейки матки более чем в 70% случаев выявляют наиболее онкогенные типы ВПЧ (типы 16 и 18).
Имеются даные о том, что число людей, инфицированных ВПЧ, за последнее десятилетие в мире увеличилось более чем в 10 раз. Наиболее типичные проявления папилломавирусной инфекции (ПВИ) – остроконечные кондиломы (ОК) аногенитальной области, частота которых, по данным Минздрава РФ, в 1994 г. составила 20,3 на 100 000 населения, что по сравнению с аналогичными данными 1993 г. увеличилось на 25%. 46 – 67% больных передают ВПЧ сексуальному партнеру, у гомосексуалистов передача инфекции отмечается в 5 – 10 раз чаще, чем у гетеросексуалов.
Попадая в организм женщины, ВПЧ не всегда приводит к развитию заболевания. Это происходит лишь при наличии предрасполагающих факторов, к которым относятся высокая сексуальная активность (раннее начало половой жизни, большое количество партнеров, частые половые контакты); наличие партнеров, имевших контакты с женщиной, болеющей раком шейки матки или аногенитальными кондиломами; другие заболевания, передаваемые половым путем; молодой возраст; курение; алкоголь; беременность; эндометриоз; авитаминоз и др.
Полагают, что развитие вирусной инфекции происходит на фоне изменений в иммунной системе организма, что обусловливает необходимость иммунокоррекции при ВПЧ-инфекции.
Клинические признаки и диагностика
Принципы лечения заболеваний, обусловленных ПВИ
Больных ОК и ПК следует предупреждать о том, что они являются контагиозными для половых партнеров и на период лечения им должен быть рекомендован барьерный метод контрацепции. Необходимо также обязательное обследование и при выявлении инфекции лечение всех партнеров, с которым пациентки контактировали за последние 6 мес.
Лечение кондилом проводится в соответствии с локализацией, характером процесса (наличие или отсутствие ЦВН) и учетом сопутствующих заболеваний (другие инфекции, нарушение микробиоценоза влагалища).
Все виды локального лечения направлены на удаление кондилом и атипически измененного эпителия в зависимости от их локализации. Используются различные виды химических коагулянтов, цитостатических препаратов и физиохирургических методов (крио-, электро-, лазертерапия, хирургическое иссечение). Для лечения шейки матки предпочтительны последние.
Однако высокая частота рецидивирования диктует необходимость поиска средств терапии, воздействующих на возбудителя и на макроорганизм. Имеются данные о хороших результатах применения различных методов системной неспецифической противовирусной терапии.
Широко используются в последние годы интерфероны (ИФ) и их индукторы. ИФ являются эндогенными цитокинами, которые обладают противовирусными, антипролиферативными и иммуномодулирующими свойствами. Используют местное, внутриочаговое и системное введение ИФ. Наиболее перспективной считается комбинированная терапия, сочетающая местное и системное лечение. Локальное удаление очагов ПВИ целесообразно производить не ранее чем через 2 – 3 нед после начала системной противовирусной терапии, поскольку клинический опыт свидетельствует о возможности полного исчезновения кондилом или их значительного уменьшения в количестве и размерах только на фоне правильно подобранной системной терапии.
Локальных методов лечения предложено множество. Приводим самые известные и доступные их них.
• Подофиллин (ПД) - смола, полученная из растений, и оказывающая цитотоксическое действие. Обычно применяются 10 – 25% раствор в амбулаторных условиях 1 – 2 раза в неделю на протяжении максимум 5 нед.
• Подофиллотоксин (ПДТ) – наиболее активное вещество в составе ПД. Является действующим веществом препарата кондилин (0, 5% раствор ПДТ в 96% спирте). Применяют также 20% мазь.
• Ферезол представляет собой смесь фенола (60%) и трикрезола (40%). Обработку кондилом производят с перерывом в 1 нед.
– Солкодерм - смесь органических и неорганических кислот. Препарат наносят на патологический участок с помощью специального аппликатора (капилляра) после обработки спиртом или эфиром. Перерыв между сеансами 1 – 2 нед.
• Трихлоруксусная кислота в концентрации 80 – 70% является слабым деструктивным химическим препаратом, который вызывает образование локального коагуляционного некроза. Рекомендуется при слабовыраженном процессе и беременности.
• Местное введение ИФ производят в виде аппликаций (человеческий ИФ), свечей или внутрикондиломно – 3 раза в неделю по 5 млн МЕ в течение 3 нед. Аппликации можно производить до и после лазертерапии.
Среди физиохирургических методов в последние годы предпочтение отдают лазертерапии, которая позволяет разрушать практически любые образования локально и щадяще под контролем кольпоскопа, ее целесообразно производить на 5 – 7-й день цикла. Метод характеризуется меньшим числом рецидивов и менее выраженным рубцеванием, однако в ряде работ доказан высокий риск заражения ВПЧ врача, производящего лазервапоризацию, через дым, возникающий при испарении тканей. Рекомендуется работать в маске и использовать вакуумную эвакуацию дыма.
Каждый из перечисленных методов локального лечения имеет достоинства и недостатки, поэтому только врач способен правильно подобрать способ лечения индивидуально для каждой больной.
Системное лечение ПВИ
Специфических анти- ВПЧ- препаратов для системной терапии не существует. Имеются единичные данные литературы о том, что ацикловир и другие противогерпетические средства могут применяться для лечения ВПЧ-инфекции, однако большинство исследований не подтверждают их эффективность. Вакцин против ВПЧ для широкой практики нет. Обычно проводят неспецифическую противовирусную терапию (витамины В6, С, Е ), назначают десенсибилизирующие средства, транквилизаторы, ИФ и его индукторы, озонотерапию, адаптогены (настойка элеутерококка, китайского лимонника), синтетические иммуномодуляторы (декарис, пентоксил, метилурацил, ликопид ) и др.
Таким образом, к диагностике и лечению заболеваний, обусловленных ПВЧ, следует подходить комплексно. Обязательными являются обследование и лечение обоих партнеров, цитологический и кольпоскопический скрининг и использование барьерных методов контрацепции как минимум в течение 6 мес после окончания терапии.
1. Адаскевич В.П. Заболевания, передаваемые половым путем. Витебск. 1996.
2. Василевская Л.П., Винокур М. Л., Никитина Н. И. // Предраковые заболевания и начальные формы рака шейки матки. М.: Медицина, 1987.
3. Дубенский В. В. и соавт. Интерфероны в комплексном лечении остроконечных кондилом. // ЗППП. – 1996. – №10. – С. 28.
4. Ершов Ф.И. Система интерферона в норме и при патологии. – М., 1996.
5. Исакова Л.М. Цитологическая и морфологическая характеристика ПВИ человека при патологии шейки матки. // Арх. пат. – 1991. – №1.
6. Козаченко В.П., Бычков В.И., Киселева Е.В. Фоновые и предраковые заболевания шейки матки. – М.: Медицина, 1994.
7. Манухин И.Б., Минкина Г.Н., Сапрыкина 0.А., Багирова М.О. Иммунные и микробиологические аспекты заболеваний шейки матки. // Актуальные вопросы клинической медицины. – М., ЮН. – 1993.
8. Новикова Е.Г. Эволюция методов леченния больных начальными формами рака шейки матки. // Вопр. онкол. – 1991. – Т. 37. – №2.
9. Баррассо Р. Кольпоскопическая диагностика патологии шейки матки. ЗППП. – 1995. – №5.
10. Бургхардт. Атлас по патологии шейки матки и кольпоскопии. Лондон-Нью-Йорк, 1991.
11. Anderson MC, et al. Intergrated Colposcopy. Chapman & Hall Medical, 1996, ed.II.
12. Singer A, Monaghan JM. Lower Genital Tract Precancer . Colposcopy, Pathology, Treatment, Blackwell Science. Inc., 1994.
13. Сб. тезисов 16-й интернациональной конференции по папилломавирусной инфекции, Сиена, 1997.
Читайте также:

