Лечение туберкулеза легких и астмы
Обновлено: 18.04.2024
В чем особенность течения туберкулеза на современном этапе? Почему в схеме комплексной терапии туберкулеза необходимо использовать иммуномодуляторы? Tуберкулез — это специфическое инфекционное заболевание, развивающееся в ответ на попадание в орган
В чем особенность течения туберкулеза на современном этапе?
Почему в схеме комплексной терапии туберкулеза необходимо использовать иммуномодуляторы?
Tуберкулез — это специфическое инфекционное заболевание, развивающееся в ответ на попадание в организм микобактерий туберкулеза (МБТ). Туберкулез может поражать все органы и системы организма человека, но наиболее часто — органы дыхания. В настоящее время туберкулез признан ВОЗ глобальной проблемой, наносящей колоссальный экономический и биологический ущерб. В России эпидемиологическая ситуация по туберкулезу характеризуется наличием у большинства больных обширных, запущенных форм туберкулеза, с деструкцией и бацилловыделением, эффективность лечения при этом снижена. В сложившихся неблагоприятных условиях основными противотуберкулезными мероприятиями следует считать выявление и лечение больных туберкулезом.
Различные авторы указывают на многообразие факторов, имеющих существенное значение в развитии туберкулезного воспаления. Среди них большая роль принадлежит иммунологическим процессам, в связи с чем туберкулез может быть признан классическим примером иммунного воспаления. Состояние иммунной системы организма является также одной из причин замедленной регрессии специфических изменений и сохранения морфологической активности туберкулезного процесса [9, 16]. Необходимо признать, что традиционная химиотерапия, даже проводимая правильно, вызывает в основном бактериостатический эффект и не в состоянии полностью устранить многообразие морфологических и функциональных изменений туберкулезного характера. Химиотерапия не стимулирует защитные силы организма и не может во всех случаях обусловить полное выздоровление. У большинства больных туберкулезом легких в процессе эффективного лечения достигается нормализация основных показателей иммунитета, но у части больных развивается вторичное иммунодефицитное состояние [10]. Клинически туберкулез у лиц с иммунодефицитом плохо поддается лечению.
Нарушение иммунорегуляции может корректироваться с помощью иммунотерапии. В связи с этим особое значение в современной комплексной терапии туберкулеза имеет использование иммунотропных препаратов с целью стимуляции защитных сил организма и нормализации измененного иммунологического статуса больных туберкулезом [7, 18]. Клинический опыт свидетельствует о благоприятном влиянии на лечение туберкулеза таких препаратов, как спленин, левамизол, диуцифон, препараты тимуса, туберкулин, вакцина БЦЖ. Включение в комплексную терапию больных туберкулезом иммуномодуляторов способствует ускорению нормализации показателей иммунитета и более быстрой регрессии туберкулезного процесса [1, 16]. Актуальной задачей является поиск новых отечественных иммунокорригирующих препаратов и изучение механизмов их действия [2, 4, 5, 6]. В работах Р. В. Петрова, Р. М. Хаитова и соавторов обоснован новый подход к поиску иммунокорректоров с избирательным воздействием на конкретное звено иммунитета, в основе которого заложен принцип создания иммуногенов путем структурного объединения антигена (АГ) и полимера-иммуностимулятора [17]. В качестве иммуностимуляторов предложено использовать водорастворимые полиэлектролиты. Экспериментально доказано, что иммунный ответ на комплексы АГ, конъюгированных с водорастворимыми полиэлектролитами, гораздо выше ответа на сами АГ. В Институте иммунологии МЗ РФ А. В. Некрасовым впервые в нашей стране создан принципиально новый синтетический высокомолекулярный иммуностимулятор — полиоксидоний (ПО; рег. № 96/302/9, патент РФ № 2073031) [14, 15].
ПО, обладающий в большом диапазоне доз широким спектром фармакологического действия и высокой иммуностимулирующей активностью, оказывает выраженное иммуностимулирующее действие на гуморальный иммунный ответ, усиливает кооперацию Т- и В-лимфоцитов. Установлено его преимущественное влияние на фагоцитарное звено иммунитета. ПО активирует функцию макрофагов и лимфоцитов. При этом препарат обладает неспецифическим защитным действием от широкого спектра патогенов, основанным не на прямом угнетении микроорганизмов, а на стимуляции иммунитета. Кроме того, в экспериментах была показана стимулирующая способность клеток ретикулоэндотелиальной системы захватывать и удалять из циркулирующей крови чужеродные микрочастицы [14, 15]. Известно, что ПО, стимулируя иммунные реакции, не нарушает естественных механизмов их торможения, не истощает резервных возможностей кроветворной системы [14, 15]. Показано, что введение ПО приводит к значительному повышению интенсивности антителообразования в ответ на чужеродные АГ различной природы [14, 17].
Установлено также, что токсичность ряда лекарственных препаратов снижается при совместном их введении в организм с ПО.
Отсутствие побочных эффектов и токсичности, четко показанное в эксперименте, указывает на возможность применения ПО в качестве лечебного и профилактического средства при различных заболеваниях, в том числе при хронических заболеваниях легких. ПО может применяться как иммуностимулятор широкого спектра действия, детоксикант, иммуностимулирующий и пролонгирующий носитель для АГ в структуре конъюгированных вакцин нового поколения. В настоящее время на основе ПО созданы гриппозная, бруцеллезная, брюшнотифозная вакцины и ряд аллерговакцин, разрабатываются и другие вакцины, в том числе форсифицированные.
Препарат обладает пролонгированным эффектом. Однократно введенный, он действует в течение одной-двух недель. Клинические испытания препарата на здоровых добровольцах показали хорошую переносимость ПО, отсутствие каких-либо побочных явлений или аллергических реакций [6].
В клинике ПО применялся у хирургических больных с послеоперационными инфекционными осложнениями, с трофическими нарушениями нижних конечностей при сахарном диабете, с острыми и хроническими инфекционно-воспалительными урогенитальными заболеваниями, с аллергией и бронхиальной астмой, с онкологическими заболеваниями [8, 11, 12, 13]. Проведено исследование клинической эффективности и переносимости ПО при лечении пациентов с хроническим бронхитом и хроническим рецидивирующим фурункулезом — заболеваниями, представляющими собой вторичные иммунодефициты с поражением различных звеньев иммунной системы [6].
В литературе имеются лишь единичные сведения об исследованиях эффективности использования ПО в клинике фтизиатрии [3].
Целью настоящей работы явилось исследование клинической эффективности ПО в комплесной иммунохимиотерапии больных туберкулезом органов дыхания.
Курс иммунотерапии ПО проводился по схеме: 6 мг в сутки внутримышечно два раза в неделю; 27 пациентам было сделано 10 инъекций, двум больным — 4 и 6 инъекций ПО соответственно.
Больным проводилось комплексное клинико-лабораторное, рентгенологическое, инструментальное и иммунологическое обследование. Эффективность ПО у больных туберкулезом легких оценивали в процессе комплексной иммунохимиотерапии, сразу после проведения курса лечения ПО и через месяц после его окончания. Пациенты контрольной группы обследовались в те же сроки. Схемы специфической химиотерапии у пациентов основной и контрольной группы были идентичными.
Анализ влияния иммунотерапии ПО на ликвидацию симптомов интоксикации у больных туберкулезом легких представлен на рис. 2. Необходимо отметить, что улучшение общего самочувствия, уменьшение или исчезновение жалоб со стороны органов дыхания отмечалось больными после первых инъекций ПО.
Наряду с оценкой дезинтоксикационного эффекта ПО поводилось изучение влияния препарата на состояние специфического процесса в легочной ткани у больных туберкулезом. Динамика рассасывания инфильтративных изменений в легочной ткани у больных основной и контрольной групп представлена на рис. 3. Анализ данных, представленных на рис. 3, позволяет сделать вывод о выраженном положительном влиянии ПО на процесс рассасывания специфического воспаления в легочной ткани у больных туберкулезом.
Важными являются результаты исследования прекращения бактериовыделения у пациентов через месяц после окончания курса иммунотерапии ПО. Анализ этих данных представлен на рис. 4.
Результаты изучения другого важного критерия эффективности лечения больных туберкулезом — инволюции полостей распада под влиянием иммунотерапии ПО — представлены на рис. 5. Проанализировав эти данные, можно сделать вывод о положительном влиянии ПО на процесс заживления деструкции легочной ткани у больных туберкулезом.
Ниже мы приводим клиническое наблюдение, подтверждающее сделанные нами выводы.
Больному начали проводить курс противотуберкулезной химиотерапии четырьмя препаратами (изониазид + рифампицин + стрептомицин + пиразинамид). Учитывая данные клинико-лабораторного исследования, свидетельствующие о наличии у больного резко выраженного интоксикационного синдрома, было решено начать лечение ПО. Курс иммунотерапии составил 10 инъекций ПО два раза в неделю по 0,006 г в течение 5 недель. На фоне проводимого лечения у больного уже в первые две недели отмечалось улучшение самочувствия, значительное уменьшение симптомов интоксикации. При рентгенологическом исследовании в динамике отмечалось значительное рассасывание инфильтративных изменений и уменьшение размеров деструкции в верхней доле правого легкого. Через месяц после окончания курса иммунотерапии ПО полость распада четко не определялась.
Заключение: у больного с впервые выявленным инфильтративным туберкулезом верхней доли правого легкого в фазе распада и обсеменения МБТ(+) назначение иммунотерапии ПО позволило добиться полной ликвидации симптомов интоксикации, нормализации гемограммы, прекращения бактериовыделения, значительного рассасывания воспалительной инфильтрации и закрытия деструкции легочной ткани к третьему месяцу химиотерапии.
Поскольку иммунотерапия ПО проводилась в разные сроки от начала антибактериального лечения, представлялось целесообразным оценить ее эффективность при раннем (в течение первых одного-двух месяцев) назначении ПО совместно с антибактериальными препаратами (I подгруппа) и в более поздние сроки (II подгруппа). Первая подгруппа в основном была сформирована из больных инфильтративной формой туберкулеза легких (73,1%), тогда как во II подгруппе преобладали больные фиброзно-кавернозной формой туберкулеза легких (47,4%).
Мы изучали дезинтоксикационный эффект ПО у больных туберкулезом легких в различные сроки от начала антибактериального лечения, а также динамику рассасывания инфильтрата, прекращения бактериовыделения и инволюции деструктивных изменений в легочной ткани. Анализ полученных данных показал эффективность использования ПО с дезинтоксикационной целью на различных этапах антибактериального лечения больных туберкулезом легких. Симптомы интоксикации через месяц после окончания курса ПО ликвидированы у больных I и II подгрупп в 78,6 и 72,7% случаев соответственно. Значительное рассасывание специфических воспалительных изменений в легких у больных после курса ПО чаще отмечалось в I (68,7%), чем во II (30,8%) подгруппе. Абациллирование достигнуто через месяц после окончания курса ПО в I подгруппе у всех больных, а во II подгруппе — у 54,5% больных. Закрытие деструкции легочной ткани через месяц после курса иммунотерапии ПО у больных чаще происходило в I, чем во II подгруппе (46,7 и 18,2% соответственно).
Таким образом, анализ клинической эффективности ПО у больных туберкулезом легких показал преимущества комплексной иммунохимиотерапии, проводимой пациентам с наличием интоксикации, бактериовыделения, инфильтративными изменениями и деструкцией легочной ткани в первые один-два месяца от начала антибактериальной терапии.
Туберкулез легких – это инфекционная патология, вызываемая бациллой Коха, характеризующаяся различными в клинико-морфологическом отношении вариантами поражения легочной ткани. Многообразие форм туберкулеза легких обусловливает вариабельность симптоматики. Наиболее типичны для туберкулеза легких респираторные нарушения (кашель, кровохарканье, одышка) и симптомы интоксикации (длительный субфебрилитет, потливость, слабость). Для подтверждения диагноза используются лучевые, лабораторные исследования, туберкулинодиагностика. Химиотерапия туберкулеза легких проводится специальными туберкулостатическими препаратами; при деструктивных формах показано хирургическое лечение.
МКБ-10

Общие сведения
На сегодняшний день туберкулез легких представляет не только медико-биологическую, но и серьезную социально-экономическую проблему. По данным ВОЗ, туберкулезом инфицирован каждый третий житель планеты, смертность от инфекции превышает 3 млн. человек в год. Легочный туберкулез является самой частой формой туберкулезной инфекции. Удельный вес туберкулеза других локализаций (суставов, костей и позвоночника, гениталий, кишечника, серозных оболочек, ЦНС, глаз, кожи) в структуре заболеваемости значительно ниже.

Причины
Характеристика возбудителя
Отличительной чертой МБТ является их высокая устойчивость к внешним воздействиям (высоким и низким температурам, влажности, воздействию кислот, щелочей, дезинфектантов). Наименьшую стойкость возбудители туберкулеза легких демонстрируют к солнечному свету. Для человека опасность представляют туберкулезные бактерии человеческого и бычьего типа; случаи инфицирования птичьим типом микобактерий крайне редки.
Пути заражения
Основной путь заражения при первичном туберкулезе легких – аэрогенный: от больного открытой формой человека микобактерии распространяются с частичками слизи, выделяемыми в окружающую среду при разговоре, чихании, кашле; могут высыхать и разноситься с пылью на значительные расстояния. В дыхательные пути здорового человека инфекция чаще попадает воздушно-капельным или пылевым путем.
Меньшую роль в инфицировании играют алиментарный (при употреблении зараженных продуктов), контактный (при использовании общих предметов гигиены и посуды) и трансплацентарный (внутриутробный) пути. Причиной вторичного туберкулеза легких выступает повторная активация ранее перенесенной инфекции либо повторное заражение.
Факторы риска
Однако попадание МБТ в организм не всегда приводит к заболеванию. Факторами, на фоне которых туберкулез легких развивается особенно часто, считаются:
- неблагоприятные социально-бытовые условия
- курение и другие химические зависимости
- недостаточное питание
- иммуносупрессия (ВИЧ-инфекция, прием глюкокортикоидов, состояние после трансплантации органов)
- онкологические заболевания и др.
В группе риска по развитию туберкулеза легких находятся мигранты, заключенные, лица, страдающие наркотической и алкогольной зависимостью. Также имеет значение вирулентность инфекции и длительность контакта с больным человеком.
Патогенез
При снижении местных и общих факторов защиты микобактерии беспрепятственно проникают в бронхиолы, а затем в альвеолы, вызывая специфическое воспаление в виде отдельных или множественных туберкулезных бугорков или очагов творожистого некроза. В этот период появляется положительная реакция на туберкулин - вираж туберкулиновой пробы. Клинические проявления туберкулеза легких на этой стадии часто остаются нераспознанными. Небольшие очажки могут самостоятельно рассасываться, рубцеваться или обызвествляться, однако МБТ в них длительно сохраняются.
Классификация
Первичный туберкулез легких - это впервые развившаяся инфильтрация легочной ткани у лиц, не имеющих специфического иммунитета. Диагностируется преимущественно в детском и подростковом возрасте; реже возникает у лиц старшего и пожилого возраста, которые в прошлом перенесли первичную инфекцию, закончившуюся полным излечением. Первичный туберкулез легких может принимать форму:
- первичного туберкулезного комплекса (ПТК)
- туберкулеза внутригрудных лимфоузлов (ВГЛУ)
- хронически текущего туберкулеза.
Вторичный туберкулез легких развивается при повторном контакте с МБТ или в результате реактивации инфекции в первичном очаге. Основные вторичные клинические формы представлены:
Отдельно различают кониотуберкулез (туберкулез, развивающийся на фоне пневмокониозов), туберкулез верхних дыхательных путей, трахеи, бронхов; туберкулезный плеврит. При выделении больным МБТ в окружающую среду с мокротой говорят об открытой форме (ВК+) туберкулеза легких; при отсутствии бацилловыделения – о закрытой форме (ВК–). Также возможно периодическое бацилловыделение (ВК±).
Течение туберкулеза легких характеризуется последовательной сменной фаз развития:
- 1) инфильтративной
- 2) распада и обсеменения
- 3) рассасывания очага
- 4) уплотнения и обызвествления.
Симптомы туберкулеза легких
Первичный туберкулезный комплекс
Первичный туберкулезный комплекс сочетает в себе признаки специфического воспаления в легком и регионарный бронхоаденит. Может протекать бессимптомно или под маской простудных заболеваний, поэтому выявлению первичного туберкулеза легких способствуют массовые скрининги детей (проба Манту) и взрослых (профилактическая флюорография).
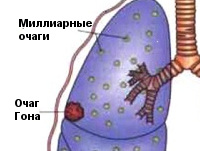
Чаще возникает подостро: больного беспокоит сухой кашель, субфебрилитет, утомляемость, потливость. При острой манифестации клиника напоминает неспецифическую пневмонию (высокая лихорадка, кашель, боль в груди, одышка). В результате лечения происходит рассасывание или обызвествление ПТК (очаг Гона). В неблагоприятных случаях может осложняться казеозной пневмонией, образованием каверн, туберкулезным плевритом, милиарным туберкулезом, диссеминацией микобактерий с поражением почек, костей, мозговых оболочек.
Туберкулез внутригрудных лимфоузлов
Признаки туберкулезной интоксикации включают отсутствие аппетита, снижение массы тела, утомляемость, бледность кожи, темные круги под глазами. На венозный застой в грудной полости может указывать расширение венозной сети на коже грудной клетки. Данная форма нередко осложняется туберкулезом бронхов, сегментарными или долевыми ателектазами легких, хронической пневмонией, экссудативным плевритом. При прорыве казеозных масс из лимфоузлов через стенку бронхов могут формироваться легочные очаги туберкулеза.
Очаговый туберкулез легких
Клиническая картина очагового туберкулеза малосимптомна. Кашель отсутствует или возникает редко, иногда сопровождается выделением скудной мокроты, болями в боку. В редких случаях отмечается кровохарканье. Чаще больные обращают внимание на симптомы интоксикации: непостоянный субфебрилитет, недомогание, апатию, пониженную работоспособность. В зависимости от давности туберкулезного процесса различают свежий и хронический очаговый туберкулез легких.
Течение очагового туберкулеза легких относительно доброкачественное. У больных с нарушенной иммунной реактивностью заболевание может прогрессировать в деструктивные формы туберкулеза легких.
Инфильтративный туберкулез легких
Клиническая картина инфильтративного туберкулеза легких зависит от величины инфильтрата и может варьировать от нерезко выраженных симптомов до острого лихорадочного состояния, напоминающего грипп или пневмонию. В последнем случае отмечается выраженная высокая температура тела, ознобы, ночная потливость, общая слабость. Со стороны органов дыхания беспокоит кашель с мокротой и прожилками крови.
В воспалительный процесс при инфильтративной форме туберкулеза легких часто вовлекается плевра, что обусловливает появление болей в боку, плеврального выпота, отставание пораженной половины грудной клетки при дыхании. Осложнениями инфильтративного туберкулеза легких могут стать казеозная пневмония, ателектаз легкого, легочное кровотечение и др.
Диссеминированный туберкулез легких
Может манифестировать в острой (милиарной), подострой и хронической форме. Тифоидная форма милиарного туберкулеза легких отличается преобладанием интоксикационного синдрома над бронхолегочной симптоматикой. Начинается остро, с нарастания температуры до 39-40 °С, головной боли, диспепсических расстройств, резкой слабости, тахикардии. При усилении токсикоза может возникать нарушение сознания, бред.
При легочной форме милиарного туберкулеза легких с самого начала более выражены дыхательные нарушения, включающие сухой кашель, одышку, цианоз. В тяжелых случаях развивается острая сердечно-легочная недостаточность. Менингеальной форме соответствуют симптомы поражения мозговых оболочек.
Подострое течение диссеминированного туберкулеза легких сопровождается умеренной слабостью, понижением работоспособности, ухудшением аппетита, похуданием. Эпизодически возникают подъемы температуры. Кашель продуктивный, не сильно беспокоит больного. Иногда первым признаком заболевания становится легочное кровотечение.
Хронический диссеминированный туберкулез легких при отсутствии обострения бессимптомен. Во время вспышки процесса клиническая картина близка к подострой форме. Диссеминированный туберкулеза легких опасен развитием внелегочного туберкулеза, спонтанного пневмоторакса, тяжелых легочных кровотечений, амилоидоза внутренних органов.
Кавернозный и фиброзно-кавернозный туберкулез легких
Характер течения кавернозного туберкулезного процесса волнообразный. В фазу распада нарастают интоксикационные симптомы, гипертермия, усиливается кашель и увеличивается количество мокроты, возникает кровохарканье. Часто присоединяется туберкулез бронхов и неспецифический бронхит.
Фиброзно-кавернозный туберкулез легких отличается формированием каверн с выраженным фиброзным слоем и фиброзными изменениями легочной ткани вокруг каверны. Протекает длительно, с периодическими обострениями общеинфекционной симптоматики. При частых вспышках развивается дыхательная недостаточность II-III степени.
Осложнениями, связанными с деструкцией легочной ткани, являются профузное легочное кровотечение, бронхоплевральный свищ, гнойный плеврит. Прогрессирование кавернозного туберкулеза легких сопровождается эндокринными расстройствами, кахексией, амилоидозом почек, туберкулезным менингитом, сердечно-легочной недостаточностью – в этом случае прогноз становится неблагоприятным.
Цирротический туберкулез легких
Является исходом различных форм туберкулеза легких при неполной инволюции специфического процесса и развитии на его месте фиброзно-склеротических изменений. При пневмоциррозе бронхи деформированы, легкое резко уменьшено в размерах, плевра утолщена и нередко обызвествлена.
Изменения, происходящие при цирротическом туберкулезе легких, обусловливают ведущие симптомы: выраженную одышку, тянущую боль в груди, кашель с гнойной мокротой, кровохарканье. При обострении присоединятся признаки туберкулезной интоксикации и бацилловыделение. Характерным внешним признаком пневмоцирроза служит уплощение грудной клетки на стороне поражения, сужение и втянутость межреберных промежутков. При прогрессирующем течении постепенно развивается легочное сердце. Цирротические изменения в легких необратимы.
Туберкулома легкого
Представляет собой инкапсулированный казеозный очаг, сформировавшийся в исходе инфильтративного, очагового или диссеминированного процесса. При стабильном течении симптомы не возникают, образование выявляется при рентгенографии легких случайно. В случае прогрессирующей туберкуломы легкого нарастает интоксикация, появляется субфебрилитет, боль в груди, кашель с отделением мокроты, возможно кровохарканье. При распаде очага туберкулома может трансформироваться в кавернозный или фиброзно-кавернозный туберкулез легких. Реже отмечается регрессирующее течение туберкуломы.
Диагностика
Диагноз той или иной формы туберкулеза легких выставляется врачом-фтизиатром на основании совокупности клинических, лучевых, лабораторных и иммунологических данных. Для распознавания вторичного туберкулеза большое значение имеет подробный сбор анамнеза. Для подтверждения диагноза проводится:
- Лучевая диагностика.Рентгенография легких является обязательным диагностической процедурой, позволяющей выявить характер изменений в легочной ткани (инфильтративный, очаговый, кавернозный, диссеминированный и т. д.), определить локализацию и распространенность патологического процесса. Выявление кальцинированных очагов указывает на ранее перенесенный туберкулезный процесс и требует уточнения данных с помощью КТ или МРТ легких.
- Анализы. Обнаружение МБТ достигается неоднократным исследованием мокроты (в т. ч. с помощью ПЦР), промывных вод бронхов, плеврального экссудата. Но сам по себе факт отсутствия бацилловыделения не является основанием для исключения туберкулеза легких. Современные иммунологические тесты позволяют выявить туберкулезную инфекцию почти со 100%-ной вероятностью. К ним относятся QuantiFERON и Т-спот. ТБ.
- Туберкулинодиагностика. К методам туберкулинодиагностики относятся диаскин-тест, пробы Пирке и Манту, однако сами по себе данные методы могут давать ложные результаты. Иногда для подтверждения туберкулеза легких приходится прибегать к пробному лечению противотуберкулезными препаратами с оценкой динамики рентгенологической картины.
По результатам проведенной диагностики туберкулез легких дифференцируют с пневмонией, саркоидозом легких, периферическим раком легкого, доброкачественными и метастатическими опухолями, пневмомикозами, кистами легких, абсцессом, силикозом, аномалиями развития легких и сосудов. Дополнительные методы диагностического поиска могут включать бронхоскопию, плевральную пункцию, биопсию легкого.

Лечение туберкулеза легких
Во фтизиатрической практике сформировался комплексный подход к лечению туберкулеза легких, включающий медикаментозную терапию, при необходимости - хирургическое вмешательство и реабилитационные мероприятия. Лечение проводится поэтапно: сначала в тубстационаре, затем в санаториях и, наконец, амбулаторно. Режимные моменты требуют организации лечебного питания, физического и эмоционального покоя.
- Противотуберкулезная терапия. Ведущая роль отводится специфической химиотерапии с помощью препаратов с противотуберкулезной активностью. Для терапии различных форм туберкулеза легких разработаны и применяются 3-х, 4-х и 5-тикомпонентные схемы (в зависимости от количества используемых препаратов). К туберкулостатикам первой линии (обязательным) относятся изониазид и его производные, пиразинамид, стрептомицин, рифампицин, этамбутол; средствами второго ряда (дополнительными) служат аминогликозиды, фторхинолоны, циклосерин, этионамид и др. Способы введения препаратов различны: перорально, внутримышечно, внутривенно, эндобронхиально, внутриплеврально, ингаляторно. Курсы противотуберкулезной терапии проводят длительно (в среднем 1 год и дольше).
- Патогенетическая терапия. При туберкулезе легких включает прием противовоспалительных средств, витаминов, гепатопротекторов, инфузионную терапию и пр. В случае лекарственной резистентности, непереносимости противотуберкулезных средств, при легочных кровотечениях используется коллапсотерапия.
- Хирургическое лечение. При соответствующих показаниях (деструктивных формах туберкулеза легких, эмпиеме, циррозе и ряде др.) применяются различные оперативные вмешательства: кавернотомию, торакопластику, плеврэктомию, резекцию легких.
Профилактика
Профилактика туберкулеза легких является важнейшей социальной проблемой и приоритетной государственной задачей. Первым шагом на этом пути является обязательная вакцинация новорожденных, детей и подростков. При массовых обследованиях в дошкольных и школьных учреждениях используется постановка внутрикожных туберкулиновых проб Манту. Скрининг взрослого населения осуществляется путем проведения профилактической флюорографии.
В статье представлены данные по распространенности и особенностям течения патологического процесса при сочетании туберкулеза и хронической обструктивной болезни легких.
The article presents data on the prevalence and characteristics of the pathological process in combination tuberculosis and chronic obstructive pulmonary disease.
Хроническая обструктивная болезнь легких (ХОБЛ) характеризуется хроническим воспалением дыхательных путей с прогрессивным ухудшением функции легких и закономерно считается одной из основных причин заболеваемости, инвалидности и смертности населения — четвертой по значимости причиной смерти. Хроническим бронхитом страдает 6,4% населения, эмфиземой — 1,8% и бронхиальной обструкцией — 9,2%.
Способствуют развитию ХОБЛ, в первую очередь, курение, загрязнение атмосферного воздуха, воздействие некоторых газов, инфекции, наличие в анамнезе туберкулеза легких, бронхиальной астмы, тяжелое социально-экономическое положение и генетические факторы. Распространенность ХОБЛ среди некурящих составляет 6,6%, но около 25–45% больных ХОБЛ никогда не курили. В Южной Африке общенациональный опрос показал, что в эндемичных по туберкулезу районах именно туберкулез легких является серьезным фактором риска развития ХОБЛ [1, 5].
Туберкулез представляет собой глобальную угрозу здоровью населения и остается ведущей причиной смерти среди инфекционных заболеваний, особенно в слаборазвитых и развивающихся странах. Хотя туберкулез может возникнуть в любом органе или ткани, поражение органов дыхания является наиболее часто встречающимся. Без лечения при туберкулезе прогрессирует специфическое хроническое воспаление, и 5-летний рубеж переживает только 50%. Хотя стандартное лечение является весьма эффективным, способствует быстрому разрешению клинической симптоматики с низким риском рецидивов, несвоевременное начало его остается большим препятствием на пути к быстрому выздоровлению. После завершения лечения туберкулеза легких примерно две трети больных имеют нарушение легочной функции [2, 3].
Важным требованием к препарату, назначаемому больным при обострении ХОБЛ, является минимальный уровень резистентности к нему основных этиологически значимых микроорганизмов. Особое значение микробная резистентность приобретает у больных с факторами риска (наличие тяжелой сопутствующей патологии, пожилой возраст, предшествующая терапия антибиотиками, наличие тяжелой сопутствующей патологии). Наиболее реальна прoблема резистентности S. рneumoniae к пенициллинам и макролидам (перекрестная резистентность), а также рост частоты штаммов H. influenzae и M. catarrhalis, продуцирующих β-лактамазу. Если разрушительное действие β-лактамаз может быть преодолено благодаря назначению защищенных пенициллинов (амоксициллин + клавулановая кислота), то резистентные штаммы S. pneumoniae оказываются нечувствительными к защищенным пенициллинам. Однако имеются данные, что амоксициллин + клавулановая кислота оказываются эффективны в отношении S. pneumoniae c низкой чувствительностью к пенициллину. Такая активность обусловлена оптимальными фармакокинетическими и фармакодинамическими параметрами препарата, позволяющими создавать высокую минимальную подавляющую концентрацию для резистентных штаммов S. pneumoniae. Особенно отчетливо данный эффект выражен при использовании амоксициллин + клавулановая кислота в дозе 875/125 мг.
В принципе, несвоевременное назначение терапии и несоблюдение протоколов может увеличить продолжительность и выраженность воспалительных изменений дыхательных путей и, соответственно, деструкцию легких, что может привести к развитию ХОБЛ. Тем не менее, до сих пор не изучалась связь между своевременностью противотуберкулезной терапии и развитием ХОБЛ [4].
Как ХОБЛ, так и туберкулез легких являются важными причинами бронхолегочной заболеваемости и смертности. Они имеют сходные факторы риска, такие как курение, низкий социально-экономический статус и нарушение иммунной защиты организма. Туберкулез и ХОБЛ могут взаимоотягощать течение каждого заболевания в отдельности. Туберкулез может являться фактором риска развития, обострения и прогрессирования ХОБЛ, а ХОБЛ, являясь сопутствующим заболеванием, изменять типичное течение туберкулеза, что затрудняет его диагностику и лечение [5, 6].
Целью данной работы было изучение клинико-эпидемиологических особенностей течения туберкулеза у больных с ХОБЛ.
Материалы и методы исследования
В исследование включены пациенты с впервые выявленным туберкулезом. Исследование ретроспективное. Обследовано 230 больных, поступивших в противотуберкулезный диспансер с впервые выявленным туберкулезом (142 мужчины (57,5) и 88 женщин (42,5%), средний возраст 42,3 ± 1,1 года). Всем больным проводили сбор анамнеза, клинические, лабораторные и инструментальные исследования, фиксировали результаты исследований, осуществляемых ранее. Проводилось исследование функции внешнего дыхания. Оценивались форсированная жизненная емкость легких (ФЖЕЛ), объем форсированного выдоха за первую секунду (ОФВ1 в литрах и в процентах от должных величин), тест Тиффно (ОФВ1/ФЖЕЛ). Из 230 обследованных 74 выставлен диагноз ХОБЛ, 156 — без ХОБЛ, 170 человек имели анамнез курения. Согласно существующим рекомендациям, основным методом верификации обструкции и степени тяжести ХОБЛ является спирометрия. В качестве ключевых параметров были приняты ОФВ1 и индекс Тиффно. Обследование пациентов проводилось исходно при поступлении в стационар. Диагноз туберкулеза устанавливался на основании клинических, лабораторных и рентгенологических методов исследования с определением формы, наличия или отсутствия бактериовыделения и распада.
Статистическая обработка данных была проведена с использованием программ Statistica 6.0 и Windows XP.
Результаты и обсуждение
В исследование включались все пациенты с впервые выявленным туберкулезом в результате самообращения или при проведении профилактического флюорографического обследования, которые за определенный период поступали в стационар на лечение, группа исследования составила 230 человек, из них 170 (73,9%) имели больший или меньший стаж курения. Пациенты после дополнительного обследования (сбор жалоб, анамнеза, проведение спирометрии) были распределены на 2 группы: I группа — имеющие ХОБЛ, II группа — без ХОБЛ. В I группу вошло 74 (32,2% от общего числа обследованных) человека, II группа — 156 (73,8%) человек. Можно предположить, что распространенность ХОБЛ на 1000 больных туберкулезом составит 321,7. Столь частая встречаемость данной патологии среди больных туберкулезом, возможно, приведет к изменению течения заболевания или может стать одним из факторов риска его развития.
Курение является основным фактором риска ХОБЛ. В I группе курящих было 66 человек (89,2%), стаж курения составил 23,1 ± 2,3 года, количество выкуриваемых сигарет 14,7, индекс курения составил 17,6. А в группе без ХОБЛ курящие составили 67,7% (111 человек), интенсивность и продолжительность их курения были ниже, что к моменту исследования не привело к развитию ХОБЛ. Стаж курения — 15,4, количество выкуриваемых сигарет в сутки 10,1, индекс курения — 12,8.
Для подтверждения диагноза ХОБЛ всем пациентам, независимо от наличия анамнеза курения, проводилось исследование функции внешнего дыхания. При изучении показателей спирометрии в I группе среднее значение ОФВ1 — 57,2 ± 2,1, ФЖЕЛ — 81,1 ± 2,7, ОФВ1/ФЖЕЛ — 57,9 ± 1,4, что подтверждает диагноз ХОБЛ, кроме того, чаще встречались пациенты с тяжелой и среднетяжелой степенью тяжести заболевания. Во II группе ОФВ1 — 73,9 ± 2,0, ФЖЕЛ — 76,4 ± 2,2, ОФВ1/ФЖЕЛ — 82,5 ± 0,8.
При анализе форм туберкулеза самой частой формой в обеих группах был инфильтративный туберкулез (86,5% и 65,2% соответственно). Но у пациентов с ХОБЛ чаще встречались распространенные процессы с деструкцией (83,2% против 67,4%; р = 0,01) и бактериовыделением (92,7% против 73,8; р = 0,02). В группе пациентов с ХОБЛ чаще имела место лекарственная устойчивость, что требовало назначения более агрессивной медикаментозной терапии (схема IIБ — 43,2%, схема IV — 10,8%).
Заключение
Полученные в результате проведенного исследования данные свидетельствуют о высокой распространенности как курения, так и ХОБЛ больных туберкулезом. ХОБЛ, как системное воспалительное заболевание, может являться провоцирующим фактором в развитии туберкулезной инфекции. Установлено, что у пациентов с ХОБЛ чаще встречаются распространенные формы с деструкцией и бактериовыделением, при низкой эффективности противотуберкулезной терапии.
Среди пациентов с ХОБЛ чаще встречались среднетяжелые и тяжелые формы заболевания, которые изначально требуют медикаментозной коррекции, которая не проводилась в противотуберкулезных учреждениях, возможно, оптимизация подходов к лечению ХОБЛ позволит повысить эффективность лечения туберкулеза и снизить эпидемиологическую опасность у данной категории пациентов.
Выводы
Таким образом, ХОБЛ имела место у 32,2% больных с впервые выявленным туберкулезом, что составило 321,7 на 1000 больных туберкулезом. Большая частота встречаемости деструктивных форм и бактериовыделения, худшие результаты лечения дают право предположить, что ХОБЛ может служить как фоном для присоединения и активного развития туберкулезной инфекции, так и предиктором неблагоприятного течения и исхода заболевания. Внедрение стандартизованной терапии ХОБЛ в схемы лечения пациентов с сочетанной патологией, возможно, будет способствовать повышению эффективности лечения.
Литература
- Глобальная стратегия диагностики, лечения и профилактики хронической обструктивной болезни легких. Пересмотр 2011 г. М.: Атмосфера, 2012. 85 с.
- Великая О. В., Руснак А. С. Скрининговое исследование функции внешнего дыхания у больных туберкулезом легких // Системный анализ и управление в биомедицинских системах. 2012. № 2, т. 11. С. 455–458.
- Завражнов С. П., Долматов В. В., Собкин А. Л., Батурова Г. А. Терапия обострений ХОБЛ у больных туберкулезом легких // Туберкулез и болезни легких. 2011. № 4, т. 88. С. 147.
- Респираторная медицина: Руководство для врачей / Под. ред. А. Г. Чучалина. В 2 т.: Т. 1. М.: ГЭОТАР-Медиа, 2007. 797 с.
- Чучалин А. Г. Хронические обструктивные болезни легких. М.: БИНОМ. 2000. 512 с.
- De Mello K. G., Mello F. C., Borga L., Rolla V., Duarte R. S., Sampaio E. P., Holland S. M., Prevots D. R., Dalcolmo M. P. Clinical and therapeutic features of pulmonary nontuberculous mycobacterial disease, Brazil, 1993–2011 // Emerg Infect Dis. 2013. № 19 (3). P. 393–399.
- Hsing S. C., Weng S. F., Cheng K. C., Shieh J. M., Chen C. H., Chiang S. R., Wang J. J. Increased risk of pulmonary tuberculosis in patients with previous non-tuberculous mycobacterial disease // I nt J Tuberc Lung Dis. 2013. № 17 (7). P. 928–933.
А. В. Мордык*, доктор медицинских наук, профессор
О. Г. Иванова*, кандидат медицинских наук
Д. А. Сулим**
Н. В. Багишева* , 1 , кандидат медицинских наук
Рисунок 1. Зачастую у больных астмой снижены виды на будущее, хотя некоторые склонны недооценивать тяжесть симптомов своего заболевания Какова дифференциальная диагностика между бронхиальной астмой и ХОЗЛ? С чем связаны возможны
 |
| Рисунок 1. Зачастую у больных астмой снижены виды на будущее, хотя некоторые склонны недооценивать тяжесть симптомов своего заболевания |
Какова дифференциальная диагностика между бронхиальной астмой и ХОЗЛ?
С чем связаны возможные ошибки в диагностике?
Какова основная роль b-агонистов в терапии бронхиальной астмы?
Как назначаются кортикостероиды?
Несмотря на возросшую компетентность врачей и доступность эффективных методов лечения, смертность от бронхиальной астмы остается высокой. Предотвратить многие смертельные исходы и даже избежать большинства случаев госпитализации можно было бы при проведении правильного лечения.
Необходимо помнить, что ведение больных астмой — процесс сложный и длительный.
Недооценка степени несостоятельности дыхания. Тяжесть состояния пациента и степень несостоятельности его дыхательной системы можно не распознать, если пренебречь тщательным выяснением всех проявлений болезни и построением диаграммы измерений максимальной скорости потока (МСП) выдыхаемого воздуха.
Зачастую у больных астмой снижены виды на будущее, хотя некоторые и склонны недооценивать серьезность симптомов своего заболевания. Чтобы выявить такую недооценку, нужно подробно расспросить пациента, бывает ли у него кашель или хриплое дыхание ночью или при физической нагрузке.
Если пациентам не удается достичь наилучшей возможной функции легких, то для коррекции этого состояния необходимо для начала вычислить нормальную МСП выдыхаемого воздуха для данного пациента, пользуясь диаграммой, прилагаемой к пикфлуометру.
Если измеренная МСП более чем на 20% меньше вычисленной, стоит провести исследование обратимости этого состояния, что делается путем сопоставления МСП или жизненной емкости легких (ЖЕЛ) до и после лечения.
Необходимая терапия может состоять всего лишь в однократном приеме бронходилятатора, но если это не увеличивает МСП на 20%, то есть до вычисленного уровня, могут понадобиться более серьезные меры, например трехнедельный курс системных кортикостероидов (30 мг преднизолона в день для взрослых). Таким образом выясняется наилучший достижимый уровень МСП, на который ориентируются в последующем лечении.
Иногда пациенты сообщают об уменьшении одышки, но при этом значения МСП не изменяются. В таких случаях необходимо провести измерение ЖЕЛ с помощью спирометра, которое может подтвердить улучшение, не определяемое по МСП (рис. 2). Спирометрами в настоящее время укомплектованы все врачебные приемные.
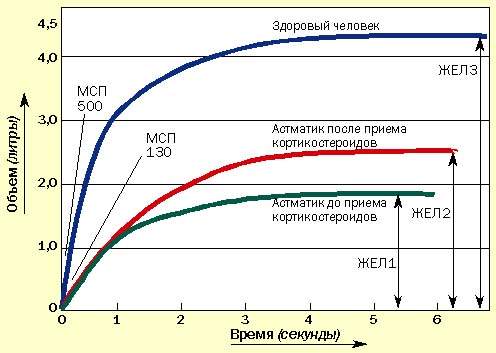 |
| Рисунок 2. Изменение ЖЕЛ под влиянием курса кортикостероидов. МСП может не измениться, но увеличение ЖЕЛ свидетельствует об улучшении состояния |
Бронхиальная астма, замаскированная под хроническое обструктивное заболевание легких (ХОЗЛ). Страдающие одышкой пациенты, которым поставлен диагноз ХОЗЛ или эмфизема, могут иметь скрытый бронхоспастический элемент, обусловленный бронхиальной астмой.
Таким пациентам необходимо провести исследование обратимости процесса, как описано выше. Любое улучшение функции легких можно поддержать, проводя адекватное лечение бронхиальной астмы. При отсутствии улучшения легочной функции назначение кортикостероидов ничем не оправдано, а только приводит к нежелательным побочным эффектам, таким как остеопороз.
Что должен помнить врач, наблюдающий больных с бронхиальной астмой
- Сказал ли я, что нужно применять спейсер при ингалировании кортикостероидов?
- Проверил ли я навыки ингаляции?
- Осмотрел ли я всех пациентов, недавно перенесших тяжелые приступы или госпитализацию?
- Все ли пациенты с повторными назначениями регулярно приходят на прием?
- Все ли я сделал, чтобы исключить астму у пациентов с ХОЗЛ?
- Проводятся ли регулярные проверки для достижения единообразного подхода к ведению астматиков?
Постоянный прием b-агонистов короткого действия. Показано, что лечение астмы постоянным приемом b-агонистов увеличивает гиперреактивность легких и утяжеляет бронхиальную астму [1]. Если пациент использует b-агонисты скорее регулярно, чем случайно, их применение должно сопровождаться назначением ингаляционных кортикостероидов или, если кортикостероиды уже применяются, увеличением их дозы до достаточной, чтобы контролировать астму. Таким образом, b-агонисты оставляют на случаи одышки и хрипов.
Последние методические указания по лечению бронхиальной астмы в Британии рекомендуют начинать с высокой дозы ингаляционных или системных кортикостероидов для достижения быстрого контроля, затем постепенно снижать дозу до минимальной, обеспечивающей нормальное самочувствие пациента и оптимальные значения МСП или ЖЕЛ на фоне минимального применения бронходилятатора (рис. 3). Быстрое облегчение состояния, достигаемое при применении кортикостероидов, улучшает настроение пациента и увеличивает его доверие к лечению.
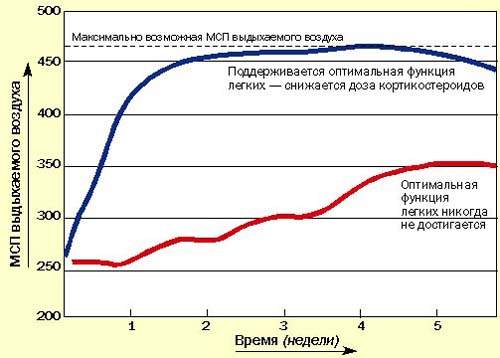 |
| Рисунок 3. Рекомендуется начинать с высоких доз кортикостероидов, а затем постепенно снижать дозу до минимальной (оптимальные значения МСП или ЖЕЛ) |
Последние данные свидетельствуют о том, что назначать кортикостероиды нужно как можно раньше всем астматикам, и не только для контролирования симптомов, но и для предотвращения прогрессирующих структурных повреждений легких, обусловленных хроническим воспалением [2,3]. Это означает, что кортикостероиды следует предпочесть b-агонистам, как только диагноз подтверждается МСП-диаграммой. b-агонисты остаются препаратами резерва на крайний случай.
Возможность альтернативного лечения. Хотя ингалируемые кортикостероиды должны быть краеугольным камнем в лечении астмы, в случаях, трудно поддающихся лечению, можно использовать и некоторые другие препараты. Доказано, что противовоспалительным эффектом обладают теофиллины в достаточно небольших дозах, но надо учитывать в каждом индивидуальном случае их возможное взаимодействие с другими препаратами.
Пожилым пациентам целесообразно назначать ипратропиум. Иногда оказываются эффективными недокромил и кромогликат.
Бронходилятаторы длительного действия, такие как сальметерол, могут облегчать состояние, особенно ночью, блокируя бронхоконстрикторные механизмы. Однако необходимо, чтобы все вышеперечисленные препараты сопровождались применением адекватных доз кортикостероидов.
Техника ингаляции. Нужно добиться, чтобы у пациентов выработались правильные навыки обращения с ингалятором. Врач должен помочь подобрать тот тип ингалятора, который наиболее удобен пациенту, и проверить его работоспособность. Для этого в кабинете врача должен быть полный набор ингаляторов.
Спейсеры. Применяемые вместе с аэрозольными ингаляторами, спейсеры облегчают проникновение препарата в легкие и снижают как накопление его в глотке, так и системное всасывание за счет проглатывания.
Спейсеры помогают координировать выброс препарата со вдохом. Это особенно важно при ингалировании кортикостероидов. Так как кортикостероиды применяются только дважды в день, громоздкий спейсер можно хранить дома.
Спейсеры обеспечивают лучшее накопление препарата в легких, чем распылители. Необходимо правильно их применять: встряхнуть ингалятор, чтобы лекарство смешалось с носителем, и однократно впрыснуть смесь с последующим скорейшим вдохом [4].
Триггерные факторы. Нераспознанные триггерные факторы могут быть и дома, и на работе, и на отдыхе, то есть практически в любом месте. Выявить источник поможет анамнез. Например, при профессиональной бронхиальной астме состояние улучшается во время отпуска и в выходные дни. Отсутствие раздражителя уменьшает или устраняет проявления болезни и снижает необходимость в лекарствах.
Проблемой, которую часто не принимают во внимание, может быть пассивное курение. Такие препараты, как b-блокаторы и нестероидные противовоспалительные средства (НПВС), также могут вызывать астму.
Использование распылителей (небулайзеров) без фоновой кортикостероидной терапии. При лечении острого астматического приступа без назначения пероральных кортикостероидов все еще используют распылители, которые обеспечивают проникновение более высокой дозы b-агонистов. Это действительно снимает бронхоспазм, но поскольку высокая доза b-агонистов не воздействует на сопутствующий воспалительный процесс, необходимо сразу же дать больному кортикостероиды внутрь, чтобы предотвратить нарастание приступа; эффект бронходилятаторов снижается по мере увеличения отека слизистой.
Если тяжесть приступа такова, что требуется небулайзер, необходимо назначить системные кортикостероиды. Даже при умеренном приступе бронходилятаторы сами по себе приносят лишь временное облегчение и есть опасность повторения приступа — возможно, глубокой ночью!
Несвоевременное назначение оральных кортикостероидов. Если не проводить противовоспалительной терапии, у больных нарастает отек слизистой, что приводит к повторению приступов. Такие пациенты часто нуждаются в госпитализации и назначении высоких доз кортикостероидов в течение нескольких дней, прежде чем у них наступит стабилизация состояния.
Пациенты, подверженные быстроразвивающимся приступам, нуждаются в как можно более раннем назначении кортикостероидов и бронходилятаторов. Они должны уметь распознавать ухудшение состояния, всегда иметь под рукой кортикостероиды и знать, как их использовать. Не следует заставлять этих пациентов дожидаться прихода к ним врача (рис. 4).
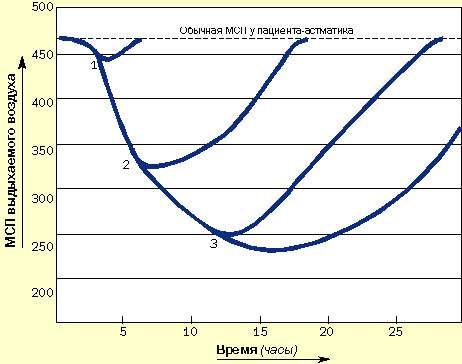 |
| Рисунок 4. Зависимость развития острых приступов от времени назначения кортикостероидов и как результат применения длительных курсов системной кортикостероидной терапии. (1) Кортикостероиды назначены сразу после возникновения приступа: выздоровление наступает быстро. (2) Кортикостероиды назначены через 6 часов: выздоровление замедлено. (3) Кортикостероиды назначены позже чем через 12 часов: приступ тяжелый и длительный, выздоровление наступает медленно |
Пациенты с постепенным развитием приступов могут подождать и посмотреть, помогает ли увеличенная доза ингаляционных кортикостероидов в сочетании с бронходилятаторами.
Неадекватный курс системных кортикостероидов. Иногда назначенные кортикостероиды отменяют до полного купирования приступа, что ведет к сохранению гиперреактивности бронхов и очередному приступу.
Подобная цепь событий может привести пациента к ложному заключению, что у него бронхиальная астма, трудно поддающаяся лечению.
Прекращение наблюдения за пациентом после острого приступа или госпитализации. Трудности возникают при отмене системного кортикостероида и назначении ингаляционного. В этот переходный период необходимо тщательное наблюдение; по достижении стабилизации состояния дозу ингалируемого кортикостероида постепенно снижают до минимально необходимой, чтобы заболевание никак себя не проявляло и функция легких была оптимальной.
Целью последующего лечения становится поддержание наивысшей МСП, достигнутой в больнице после курса системных кортикостероидов.
Консультация, проведенная через некоторое время после выписки, дает хорошую возможность проверить план ведения пациента, выяснить, что не так, и внести соответствующие поправки.
Кашель и хрипы с гнойной мокротой иногда принимают за легочную инфекцию. Однако мокрота больных астмой содержит гораздо больше эозинофилов, чем полиморфных клеток и бактерий. В пожилом возрасте левожелудочковая недостаточность и сердечная астма должны наводить на мысль о предшествующей бронхиальной астме. Будьте осторожны с b-блокаторами!
Внезапная одышка может быть обусловлена пневмотораксом или легочной эмболией. Хрипы встречаются при туберкулезе легких, бронхиальной карциноме или инородном теле и могут быть четко локализованы. Следовательно, у любого пациента с астмой, развившейся во взрослом возрасте, необходимо провести рентгенологическое исследование органов грудной клетки.
После установления диагноза основная цель врача — освободить пациента от проявлений болезни и оптимизировать функцию легких, а также установить контроль за болезнью. Для этого специально обученный медперсонал должен обучать больных и проверять правильность выполнения ими всех назначений.
Конечно, в некоторых случаях это может оказаться затруднительным, однако план предписанных действий способно усвоить абсолютное большинство больных.
Все пациенты должны:
- уметь распознать начало приступа
- знать, как применять высокие дозы b-агонистов;
- самостоятельно начать прием преднизолона внутрь;
- знать, когда звонить врачу или отправляться в больницу;
- все страдающие от приступов, должны быть обеспечены кортикостероидами.
Литература
1. Sears M. R., Taylor D. R. et al. Regular inhaled b-agonist treatment in bronchial asthma. Lancet 1990;336:1491–1396.
2. Tari Haahtela et al. Comparinson of terbutaline with budesonide in newly detected asthma. N Engl J Med 1991;325:388–392.
3. Redingon A. K., Howarth P. H. Airway remodelling in asthma. Thorax 1997;52:310–312.
4. O'Callaghan C., Barry P. Spacer devices in the treatment of asthma. BMJ 1997;314:1061–1062.
Спирометрия при хронической бронхиальной астме
Бочкообразная грудная клетка при хронической бронхиальной астме возникает из-за задержки воздуха в периферических отделах легких, что приводит к постоянному поддержанию грудной клетки в состоянии вдоха. Задержанный воздух не выдыхается и бесполезно занимает большую часть легких (остаточный объем). Это снижает объем воздуха (жизненную емкость легких), входящего в легкое.
Воздух задерживается из-за хронического воспаления, вызывающего отек слизистой периферических бронхиол. При лечении кортикостероидами отек спадает и воздух высвобождается. Это доказывается увеличением ЖЕЛ, определенной спирометрически. МСП может не изменяться (см. рис. 2.)
Читайте также:

