Лечение вич у молодых
Обновлено: 19.04.2024
Испытания лекарств от ВИЧ часто включает в себя аналитическое прерывание лечения, когда пациенты с ВИЧ прекращают прием антиретровирусной терапии (АРТ), чтобы ученые могли понаблюдать, как неконтролируемый вирус реагирует на исследуемые препараты.
Участие в такого рода клинических испытаниях может вызвать страх у человека с ВИЧ, который привык поддерживать неопределяемую вирусную нагрузку. Кроме того, предыдущее исследование, проведенное доктором Лау, показало, что многие люди с ВИЧ не были уверены в том, как работают эти испытания, и многие из них не были готовы к длительным периодам определяемой вирусной нагрузки.
Ученые работают над различными стратегиями излечения ВИЧ-инфекции. Некоторые методы нацелены на сокращение латентных резервуаров ВИЧ — инфицированных иммунных клеток, которые не производят новые вирионы в течение многих месяцев или лет. Другие виды терапии пытаются повысить способность иммунной системы контролировать вирус.
Существуют два типа исследований, основанных на прерывании лечения, которые используются для оценки потенциальной терапии: изучение времени до восстановления вирусной активности (TVR) и изучение контрольных точек. В исследованиях TVR после того, как участники прекращают АРТ, ученые измеряют время, необходимое, чтобы вирусная нагрузка сначала достигла обнаруживаемого уровня (50 копий/мл), а затем время, необходимое для достижения более высокого порога (часто 10 000 копий/мл), после чего участники возобновляют прием АРТ. Если тем, кто получает лечение, требуется больше времени для достижения этих пороговых значений по сравнению с контрольной группой, это указывает на то, что терапия замедляет восстановление вирусной активности. Исследования TVR часто используются для оценки методов терапии, нацеленной на резервуары, обычно они длятся всего несколько недель.
Исследования контрольных точек демонстрируют, насколько эффективно иммунная система участников контролирует ВИЧ самостоятельно. В этих гораздо более длительных исследованиях (до нескольких месяцев) исследователи позволяют вирусным нагрузкам участников достигать высоких уровней, имитируя острую фазу ВИЧ, чтобы проследить, сможет ли их иммунная система в дальнейшем снизить эту нагрузку. Порог для возобновления АРТ обычно устанавливается на высоком уровне (часто 100 000 копий/мл). Когда участники, получающие лечение, способны контролировать ВИЧ при более низких уровнях вирусной нагрузки и в течение более длительного времени, чем участники контрольной группы, это говорит о том, что терапия повышает их иммунитет против вируса.
Несмотря на то, что нет конкретных рекомендаций, определяющих, как планировать исследования с прерыванием лечения, группа ученых, занимающихся исследованием ВИЧ, встретилась в 2018 году, чтобы обсудить этические стороны и выработать методы для снижения риска. Прекращение АРТ во время этих исследований не просто подвергает участников риску длительных периодов определяемой, а в некоторых случаях и высокой вирусной нагрузки. Более высокие вирусные нагрузки также могут подвергать опасности и ВИЧ-отрицательных половых партнеров участников.
До сих пор в большинстве исследований риск снижался за счет небольшого числа участников и отсутствия контрольной группы, которая вместо лечения принимала неактивное плацебо. Включение контрольной группы важно, потому что это позволяет ученым сравнивать тех, кто принимает лекарства, с теми, кто находится на плацебо. Тем не менее научное сообщество обсуждало этичность использования контрольных групп в подобных испытаниях лекарств, потому что они подвергаются длительным периодам повышенной вирусной нагрузки в отсутствие каких-либо препаратов, даже экспериментальных.
Исследование
Доктор Лау и ее коллеги использовали данные предыдущих клинических испытаний для создания математических моделей, позволяющих оценить, как различные их параметры влияют на статистическую мощность испытания.
Статистическая мощность аналогична чувствительности. Например, тест на ВИЧ с чувствительностью 80% успешно идентифицирует вирус у 80% людей, которые на самом деле ВИЧ-положительны, но не выявит у остальных 20% ВИЧ-положительных людей. Когда клиническое испытание, оценивающее лечебную терапию, должно достигнуть статистической мощности в 80% (при условии, что терапия имеет реальную пользу для тех, кто ее принимает), в испытании будет 80-процентная вероятность обнаружить пользу и 20-процентная вероятность ее упустить.
Проще говоря, чем больше данных задействовано в испытании, тем большей статистической мощностью оно будет обладать. Такие факторы, как количество участников, число контрольных параметров, продолжительность испытания и частота анализов крови, влияют на статистическую мощность испытания.
Результаты пробного моделирования TVR
В отношении недавнего исследования TVR с участием 13 человек такая модель показала, что при мощности 80% исследование выявило бы только лечение со значительным снижением реактивации (от 70 до 80%). Чтобы исследование TVR выявило снижение реактивации на 30%, потребуется уже по 120 участников в группе терапии и в контрольной группе. Поскольку в большинстве исследований TVR задействовано малое число участников, они, вероятно, не устанавливают умеренных результатов терапии.
Может показаться нелогичным планирование исследования для выявления меньшего эффекта от лечения, когда конечной целью является поиск максимальной пользы (т. е. терапия, приводящая к 100% снижению реактивации). Тем не менее на начальных этапах поиска лекарства необходимо фиксировать даже умеренные результаты, чтобы решить, требует ли этот метод дальнейшего изучения.
Помимо рекомендации увеличить количество участников, команда предлагает использовать ретроспективные контрольные данные в дополнение к контрольным группам. Данные из предыдущих испытаний, в которых люди прерывали АРТ, могли бы повысить потенциал выявления умеренной пользы от лечения. Они смоделировали гипотетическое исследование TVR, в которое вошли 50 участников и 50 человек из контрольной группы. При мощности 80% эта конструкция может обнаруживать снижение реактивации до 43%. Добавление ретроспективных данных еще 150 участников позволило бы в том же испытании выявить снижение до 36%.
Такое моделирование также не показало практически никакого улучшения способности обнаруживать снижение реактивации при увеличении продолжительности испытаний TVR свыше пяти недель. После этого срока модель предсказала улучшение обнаружения не более чем на 1%. Точно так же они не обнаружили практически никакой пользы от проведения лабораторного мониторинга чаще, чем раз в неделю. Наблюдение за людьми два раза в неделю почти не помогло обнаружить снижение реактивации.
Ученые провели отдельный анализ для оценки максимального риска передачи ВИЧ во время исследований TVR на основе предыдущих данных. Они оценили максимальный риск передачи, предполагая, что участники занимались незащищенным сексом и что доконтактная или другие методы профилактики не использовались. Кроме того, если во время еженедельного мониторинга не сообщать пациенту показатель вирусной нагрузки сразу же, то участник, которому необходимо возобновить АРТ (если его вирусная нагрузка превысила 1000), скорее всего, отложит это до следующего еженедельного визита.
Было подсчитано, что в этом случае во время пятинедельного исследования TVR с порогом вирусной нагрузки 1000 для повторного начала АРТ максимальный риск передачи ВИЧ составил 3,6 на 1000 участников, занимающихся вагинальным сексом. При анальном сексе для вводящих партнеров максимальный риск составлял около 7 на 1000, а для принимающих партнеров — около 70 из 1000. Изменение схемы исследования, включающее экспресс-тестирование на вирусную нагрузку и возобновление АРТ в тот же день, снижает предполагаемый максимальный риск до 0,9, 1,8 и 18 на 1000 соответственно.
Результаты моделирования исследования по контрольным величинам
Исследования контрольных точек должны иметь достаточную статистическую мощность, чтобы отделять преимущества предлагаемой лечебной терапии от контроля после лечения. Используя результаты исследования CHAMP, ученые предположили, что исходный уровень контроллеров после лечения ниже 4%. Если целью исследования было определить увеличение количества контролеров до 20% (это означает, что терапия помогла людям, которые не являются естественными контроллерами, подавить вирус), их модель показала, что 24-недельное исследование со статистической мощностью 80% потребует участия 60 пациентов.
Из-за чрезвычайно высоких вирусных нагрузок в типичных исследованиях контрольных величин (до 100 000) авторы сравнили, как использование более консервативного порогового значения (1000) для возобновления АРТ повлияет на способность этих исследований обнаруживать увеличение числа контроллеров после лечения. CHAMP показало, что у 55% контроллеров после лечения первоначальные всплески вирусной нагрузки не превышали 1000 копий/мл, и в дальнейшем они сохраняли вирусную нагрузку ниже этого порога.
Используя эти данные, Лау и Кромер предположили, что использование порога в 1000 копий маскирует 45% естественных контроллеров после лечения, что может помешать обнаружить, когда терапия усиливает иммунный контроль участников над ВИЧ. Чтобы восстановить статистическую мощность, потребуется больше участников. Как и в приведенном выше примере, при мощности 80% и цели выявления 20-процентного повышение числа контроллеров после лечения свыше базового уровня 4%, более низкий порог вирусной нагрузки потребует увеличить количество участников с 60 до 120 как в лечебных, так и контрольных группах.
Как и в случае исследований TVR, ученые также оценили максимальный риск передачи ВИЧ во время определения контрольных величин, используя те же предположения, что и описанные выше (отсутствие стратегий профилактики и экспресс-тестирования на вирусную нагрузку, незащищенный секс, недельная задержка перед возобновлением АРТ). Из-за гораздо большей продолжительности испытаний и высоких пороговых значений вирусной нагрузки (для этого они сослались на исследование контрольных величин, в котором использовали данные 50 000 человек) они оценили максимальный риск передачи ВИЧ как 13 случаев на 1000 при вагинальных половых контактах, около 25 на 1000 — для вводящего партнера при анальном сексе, 214 на 1000 — крайне высокий — для принимающего партнера при анальном сексе.
Предлагаемая гибридная схема испытаний
Основываясь на собственном моделировании и оценках максимального риска передачи, ученые предлагают использовать гибридную модель для анализа прерывания лечения. В озвученной ими схеме прерывания будут начинаться с пятинедельного исследования TVR. Хотя оно, как правило, применяется, когда терапия нацелена на резервуары ВИЧ, у людей, отвечающих на терапию, направленную на усиление иммунитета, также будет наблюдаться более медленное восстановление вируса (если лечение было эффективным).
Начало испытания для оценки потенциального лечения с помощью исследования TVR подвергнет участников гораздо более коротким перерывам в лечении, что позволит исследователям определить, имела ли эта терапия достаточную эффективность, чтобы перейти к более длительному изучению заданных значений. Если медики согласятся с необходимостью дальнейшего исследования, а пациенты с вирусной нагрузкой ниже 1000 согласятся перейти к следующей фазе, они продолжат тщательное наблюдение в течение 24 недель или до тех пор, пока вирусная нагрузка участников не превысит 1000 копий/мл, после чего они возобновят АРТ.
Ученые рекомендуют провести экспресс-тестирование на вирусную нагрузку и возобновить АРТ в тот же день, чтобы свести к минимуму риск передачи инфекции. По их оценке, ограничение контрольной точки теми, кто уже демонстрирует контроль за вирусом, до вирусной нагрузки ниже 1000, снижение порога вирусной нагрузки для возобновления АРТ до 1000, ограничение продолжительности до 24 недель, а также включение тестирования по месту оказания медицинской помощи и возобновление АРТ в тот же день снижают максимальный риск передачи до 0,2 на 1000 при вагинальном сексе, до 0,35 на 1000 — для вводящего партнера при анальном сексе и до 3,1 на 1000 — для принимающего партнера при анальном сексе. И это значительное улучшение показателей по сравнению с оценкой, полученной в ходе традиционных исследований контрольных величин.
Если первоначальное исследование TVR показывает, что лечение не требует дальнейшего изучения (например, если не обнаружено позитивного эффекта), то ученые смогут избежать затрат на проведение длительного исследования контрольных величин.
Выводы
Ученые пришли к выводу, что в испытаниях лекарств недостаточно участников для обеспечения знаковой статистической мощности при умеренных результатах лечения. Поскольку чаще всего при испытаниях терапии также не используются контрольные группы, количественная оценка пользы лечения чрезвычайно сложна. Специалисты рекомендуют сотрудничать всем заинтересованным структурам для создания ретроспективной контрольной базы данных, которая позволила бы разработать схему испытаний, не полностью полагающуюся на контрольные группы плацебо. Тем не менее они отмечают, что задействование ретроспективных контрольных данных означает включение людей, которые с большей вероятностью начали АРТ во время хронической ВИЧ-инфекции, и тех, кто использует более старые схемы АРТ, которые могут действовать как искажающие факторы.
Тем не менее сокращение числа участников, получающих плацебо, снижение пороговых значений вирусной нагрузки, продолжительности испытаний и рисков передачи ВИЧ могут побудить большее число людей с ВИЧ участвовать в исследованиях с прерыванием лечения.




Клиника является первым частным медицинским учреждением России и единственным в Москве и области, успешно прошедшим процедуру сертификации Росздравнадзора (Сертификат №0023/01КБМД от 10.10.2019 г.).
ВИЧ и СПИД – отличия, длительность развития, прогнозы
СПИД – это конечная стадия ВИЧ, которая характеризуется сильно сниженным иммунитетом. Важно не путать два этих понятия. С момента инфицирования ВИЧ болезнь до стадии СПИДа без лечения может развиваться в течение 9-11 лет (в среднем). При постановке диагноза СПИД без лечения продолжительность жизни короткая – в среднем до 19 месяцев.
Если вовремя начать лечение, то на стадии ВИЧ можно прожить очень долгую жизнь – продолжительность жизни таких пациентов благодаря современному лечению составляет 20-50 лет. И хоть при стадии СПИД ситуация гораздо сложнее, но многие пациенты при должном лечении и крепком организме могут прожить более 10 лет.
Очевидно, что прием терапии – важнейший фактор для лечения ВИЧ и полноценной долгой жизни. Более того, именно лечение позволяет значительно снизить вирусную нагрузку и сделать зараженного человека неопасным для партнера, а также членов семьи.
Пути передачи ВИЧ
Основные пути заражения ВИЧ:
- незащищенный секс с зараженным человеком (самый распространенный путь передачи ВИЧ). Заразиться можно как после однократного контакта, так и после нескольких;
- использование иглы для введения наркотиков после зараженного человека. Либо другие варианты ситуаций, при которых происходит контакт крови здорового человека с кровью зараженного;
- передача от матери к плоду во время родов или от матери ребенку во время вскармливания. Важная ремарка: если женщина лечится и находится под контролем врачей, у нее есть все шансы родить здорового малыша;
- переливание инфицированной крови. В современных клиниках и больницах это уже исключено, поскольку все материалы проходят очень серьезную проверку.
Также выделяют так называемые группы риска – это люди, которые больше других подвержены заражению ВИЧ:
- люди, ведущие беспорядочную половую жизнь;
- гомосексуалисты;
- наркоманы, которые колют инъекции;
- люди с партнером, зараженным вирусом.
Такие люди должны постоянно сдавать анализ. В ряде случаев им рекомендованы профилактические препараты (только по рекомендации врача).
Говоря о том, как можно заразиться ВИЧ, следует уточнить, в каких случаях это невозможно:
- во время бытовых контактов;
- при использовании посуды инфицированного;
- при укусе насекомого;
- при поцелуе.
Контакт с ВИЧ-зараженным на бытовом уровне (в семье, на работе, в другом формате общения) абсолютно безопасен и не несет никакой угрозы для окружающих.
Основные стадии заболевания

Стадии ВИЧ делятся на следующие:
- инкубационная. Это стадия, на которой происходит заражение и последующее размножение вируса в крови. Она длится до шести недель, иногда меньше. Даже будучи зараженным, на этом этапе человек не увидит явных признаков, а анализ крови не покажет, что в крови есть антитела;
- первичная. Здесь уже могут появиться первые признаки инфекции. Длится вторая стадия в течение 3 недель – в это время появляются антитела, вирус определяется лабораторно;
- субклиническая. Появляется первый признак болезни – увеличенные лимфоузлы. Ппациент чувствует себя полностью здоровым, на самочувствие не жалуется;
- появление вторичных заболеваний. Иммунитет начинает давать сбои, из-за чего проявляются самые разные болезни: от частых простуд и кандидоза до пневмоний, туберкулеза;
- терминальная. Стадия предполагает истощение (довольно быстрое и прогрессирующее), а также последующую смерть больного.
Стадии не имеют единственно верных временных рамок – они могут отличаться у разных людей. Например, часто ВИЧ-инфицированные годами чувствуют себя хорошо или не обращают внимание на небольшие признаки. Болезнь обнаруживается только на стадии сильного ухудшениям самочувствия или благодаря случайным анализам.
Симптомы ВИЧ
Выяснив, как передается ВИЧ, нужно разобраться с симптомами. Проблема в том, что эти симптомы проявляются на ранней стадии, затем пропадают и долгое время больше не беспокоят человека – буквально годами. А еще они очень похожи на проявления других болезней, что может вводить в заблуждение.
Так, на первом этапе, когда вирус себя проявил, человек может чувствовать:
- боль в горле, повышение температуры;
- болезненность кожи, суставов, костей4
- озноб, лихорадку.
Одновременно с этим увеличиваются шейные лимфоузлы, могут проявиться разные высыпания. Все это часто принимается за признаки ОРВИ или других подобных болезней.
Новые симптомы ВИЧ возвращаются через несколько лет спокойной и здоровой жизни. К ним относятся:
- сильная усталость, быстрая утомляемость;
- увеличение лимфоузлов – не только шейных, а уже нескольких групп;
- снижение веса. Обычно оно выглядит беспричинным, человек не понимает, в чем дело;
- лихорадка, озноб, потливость (преимущественно ночная);
- проблемы с ЖКТ – обычно проявляются жидким стулом без видимых на то причин.
На этом этапе, как правило, и обнаруживается заболевание – потому что пациент обращается к врачу, а специалист назначает дополнительное обследование.
Как диагностируют ВИЧ в Москве
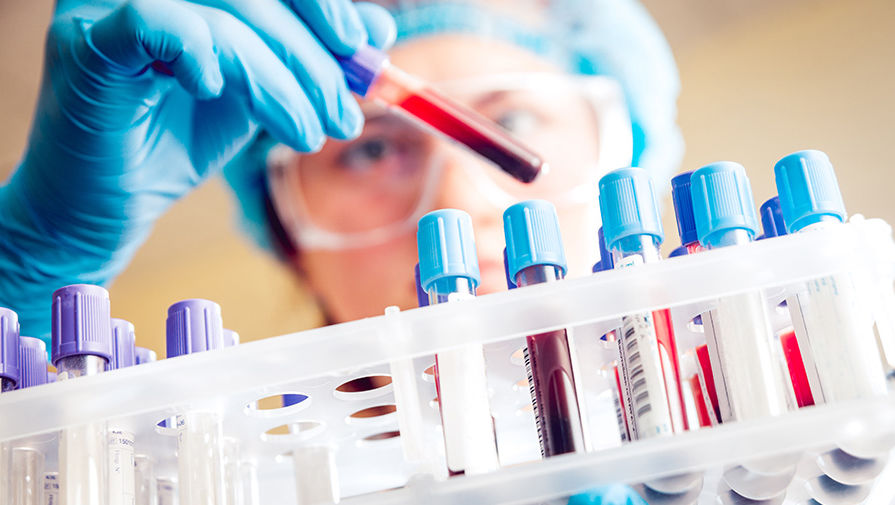
Для диагностики вируса есть два теста: предварительный ИФА и максимально точный иммуноблот. Точность ИФА составляет около 90%. Его рекомендуют проводить через 3-6 месяцев после контакта с вирусом, тогда он дает максимальную точность. Обычный тест ИФА основан на анализе крови, есть также экспресс-тесты, которые помогают получить информацию на основе мочи или слюны. Такие тексты покупают исключительно в аптеке (ни в коем случае не в интернете!), поскольку необходимо использовать официально утвержденные изделия.
Важно: тест не показывает, как передается ВИЧ в конкретной ситуации – то есть определить путь заражения можно только путем анализа собственных действий.
Лечение ВИЧ
Лечение сводится к назначению антиретровирусной терапии. Пациенту составляют схему приема препаратов – и ее нужно соблюдать максимально точно, не отклоняясь от программы. В противном случае вирус может выработать устойчивость к лечению и не поддаваться дальнейшему подавлению.
Показателями качественного лечения являются снижение вирусной нагрузки, а также увеличение в крови клеток CD4+, которое говорит об активности иммунитета.
Лекарства для лечения выдаются в медицинских учреждениях, пациенты ставятся на учет и получают препараты бесплатно, в установленном порядке. Информация о заболевании является конфиденциальной – она не направляется на работу, место учебы или в другие места. Пациент имеет право оставить ее втайне (если это не предусмотрено отдельными рабочими договорами).
При соблюдении правил приема терапии вирус в крови постепенно снижается, со временем пациент становится полностью безопасным для своего полового партнера и не способен никого заразить.
Профилактика ВИЧ-инфекции
Первое и главное правило – регулярно проверяться на ВИЧ даже в том случае, если вы не имели подозрительных контактов. Рекомендуется обследоваться раз в полгода – тем более для этого есть удобные экспресс-тесты.
Внимательно нужно относиться и к выбору партнеров. Не стоит верить на слово человеку, который говорит, что он точно не болеет – лучше попросить результаты исследования и самостоятельно убедиться, что ему можно доверять. Но помните, что в течение полугода даже зараженная кровь может не давать положительных результатов.
Профилактика ВИЧ заключается в следующих моментах:
- защищенный секс с непостоянными половыми партнерами, а также постоянными, если нет уверенности в том, что партнер не болен или хранит верность;
- исключение из жизни наркотиков, беспорядочных половых связей;
- соблюдение общей гигиены. Не стоит делиться бритвой, зубной щеткой, кусачками для ногтей и другими предметами, которые могут контактировать с маленькими ранками.
Главная профилактика заключается в том, чтобы знать об инфекции и всегда помнить об опасности заражения.
Популярные вопросы-ответы про ВИЧ
Как проявляется ВИЧ у мужчин и женщин?
Симптомы ВИЧ у женщин ровно такие же, как и симптомы ВИЧ у мужчин. Проявления могут отличаться только на уровне заболеваний мочеполовой сферы, когда организм уже сильно ослаблен – например, у женщин чаще проявляется молочница. В остальном специфических признаков по полу не наблюдается.
Лечится ли ВИЧ?
Технически можно сказать, что ВИЧ не лечится – пациентам постоянно показана специальная терапия. Но те результаты, которых она позволяет добиться, делают из пациента здорового человека, который может спокойно прожить десятки лет без особых проблем – нужно только постоянно принимать препараты и следить за здоровьем.
ВИЧ давно не является смертельным заболеванием!
ВИЧ – это болезнь наркоманов и людей с беспорядочным образом жизни?
Кто такие ВИЧ-диссиденты?
Это люди, которые вопреки научным данным и здравому смыслу отрицают существование вируса. Они отказываются от лечения, что неминуемо ведет к ранней смерти. Такие люди опасны и тем, что из-за отсутствия лечения распространяют вирус среди своих половых партнеров, не предупреждая их о возможной опасности (поскольку не считают, что она есть).
Успех лечения ВИЧ и долгой жизни заключается в том, чтобы как можно раньше обратиться за помощью и начать терапию. В этом случае человека ждет долгая жизнь без страхов и сложностей.




Клиника является первым частным медицинским учреждением России и единственным в Москве и области, успешно прошедшим процедуру сертификации Росздравнадзора (Сертификат №0023/01КБМД от 10.10.2019 г.).
В сфере здравоохранения ВИЧ-инфекция остается самой глобальной проблемой. По предварительным данным на начало 2020 года в РФ зафиксировано 1452942 человек с лабораторно выявленным диагнозом. По сравнению с прошлым годом показатель снизился на 6,1%. В среднем болеет 740 человек на 100 тыс. населения. Согласно статистике, в 60% случаев диагноз имеют мужчины. СПИД (синдром приобретенного иммунодефицита) – последняя стадия ВИЧ-инфекции. Смертельно опасное заболевание поражает защитную систему организма. Оно уничтожает клетки, которые отвечают за разрушение инфекционных возбудителей, – CD4-лимфоциты.
Все об иммунодефицитном заболевании у мужчин и женщин
Болезнь СПИД распространяется с большой скоростью. Ежегодно диагностируется около 2 млн. новых случаев заражения. Это означает, что именно такое количество людей теряет способность защищать себя естественным путем от инфекций и опухолей. Полностью вылечиться невозможно и вакцины не существует – факт, с которым приходится жить. Только профилактика СПИДа способна предотвратить заболевание. От момента заражения до развития последней стадии иммунодефицита может пройти около 10 лет. Возбудитель СПИДа – это вирус иммунодефицита человека (ВИЧ). Международное обозначение – HIV (human immunodeficiency virus).
Симптоматика заболевания
В зависимости от стадии заболевания симптомы СПИДа проявляются в разном сочетании и с разной интенсивностью. Стоит помнить, что при любых недомоганиях нужно обращаться за медицинской помощью. Это поможет на ранних стадиях правильно поставить диагноз и не потерять время, в течение которого вирус активно атакует иммунные клетки. Признаки СПИДа бывают следующие:
- гриппоподобное состояние (лихорадка, боли в горле, головная боль, кашель);
- тошнота и рвота без видимых причин;
- ночное потение и частая гипертермия;
- дерматит, кандидоз, онихомикоз;
- воспаление лимфатических узлов;
- потеря веса;
- длительная диарея;
- пневмония, герпес и туберкулез в анамнезе.
Признаки СПИДа у мужчин совпадают с женскими симптомами – различий нет. Опасность заболевания состоит в его коварности. На ранних стадиях привычные всем лихорадочные состояния и недомогания воспринимаются на уровне простуды с самостоятельным назначением лекарств. Признаки СПИДа у женщин могут проявляться интенсивнее только в плане молочницы.
Как происходит передача заболевания
Как передается СПИД – это первое, что необходимо знать о ВИЧ-инфекции. Источником может быть, как бессимптомный вирусоноситель, так и человек со СПИДом. Передача заболевания может произойти следующими путями:
- незащищенные половые акты;
- переливание зараженной крови и ее производных;
- использование общих шприцов и игл (наркомания);
- от матери при беременности и грудном вскармливании.
Стоит помнить о правилах контактирования с инфицированными людьми. Пути передачи СПИДа ограничены, поэтому не бойтесь пожать руку человеку с таким диагнозом. Инфекция не передается при кашле человека или чихании, пользовании одной посудой в доме, при посещении бассейна, туалета. Укусы насекомых тоже не представляют опасность. Это не пути заражения СПИДом.
Какие стадии развития болезни в организме
От момента попадания инфекции в организм до диагноза СПИД может пройти 10-12 лет. За этот период вирус способен полностью вывести из строя иммунную систему. Выделяют стадии СПИДа:
Диагностика и лечение людей с диагнозом СПИД
Как передается СПИД необходимо знать каждому человеку. Вирус нельзя полностью вылечить. И в этом его главная опасность. В самом начале, когда идет инкубационный период, нет проявлений инфекции.
Симптомы СПИДа впервые проявляются в острой фазе, когда ошибочно ставят диагнозы гриппа, мононуклеоза. Без должного внимания к диагностике переход к латентному состоянию происходит быстро. Не стоит путать ВИЧ и СПИД. В первом случае речь идет об инфекции, а во втором о тяжелом заболевании. По этой причине важно своевременно диагностировать мужчин и женщин с целью предотвращения развития тяжелой стадии недуга. При ранней постановке диагноза длительность жизни составляет 20-50 лет. Если СПИД уже на последней стадии и лечение отсутствует, длительность жизни составляет не более 6-9 месяцев.
Как проводят диагностику
Диагностика СПИДа проводится на основе исследования крови – ИФА (иммуноферментный анализ) и иммунный блоттинг. С помощью первого анализа определяют количественное содержание вируса в сыворотке. Иммунный блоттинг имеет большую чувствительность и специфичность до 99,7%. Из лабораторных исследований нужно отметить еще один вид тестирования – оценка иммунного статуса. Инкубационный период СПИДа составляет 3 месяца. Если тест показал отрицательный результат, но факт инфицирования есть или предполагается, рекомендуется повторить анализы через 6 месяцев. Для постановки диагноза СПИД расшифровка должна показать CD4-лимфоциты в крови в количестве не более 200.
Методика проведения лечения
Полностью вылечить ВИЧ невозможно. Вакцина от СПИДа также еще не создана, поиски и разработки продолжаются. Основным способом приостановить развитие болезни можно с помощью медикаментозной терапии. Применяют препараты для лечения СПИДа, которые способны подавлять репликацию вируса в организме и поддерживают иммунную систему для борьбы с ВИЧ. В медикаментозном списке находятся также лекарства для лечения оппортунистических болезней и для предупреждения развития вторичных инфекций и заболеваний у пациентов с ВИЧ. Терапия назначается до конца жизни.
Профилактика заражения
Меры профилактики СПИДа предполагают исключение частой смены половых партнеров, незащищенные половые акты. Нельзя пользоваться уже использованными инъекционными иглами и шприцами. В стоматологических клиниках при оперативных вмешательствах должны использоваться стерильные инструменты. Нельзя пользоваться чужими зубными щетками, бритвами.
В середине 1980-х ученые идентифицировали вирус иммунодефицита человека и сразу же стали искать лекарство. История антиретровирусной терапии началась в 1987 году, когда для лечения ВИЧ-инфекции стали использовать препарат зидовудин. Но его эффективность была невысокой, а побочные эффекты слишком сильными. Первая высокоэффективная терапия появилась только через десять лет — в 1996 году. Эта комбинация из нескольких лекарств блокирует размножение попавшего в организм вируса сразу на нескольких этапах его цикла. С тех пор ВИЧ-инфекция — не смертельное, а хроническое заболевание, которое можно контролировать при должном лечении.
Антиретровирусные препараты (АРВ) подавляют размножение ВИЧ, но неспособны полностью удалить вирус из организма, именно поэтому их нужно принимать постоянно в течение всей жизни. Как только концентрация препарата в крови падает ниже порогового значения, вирус снова начинает размножаться. Это особенно опасно, ведь если вирус размножается в присутствии небольшого количества лекарства, то он вырабатывает устойчивость к этому препарату.
Пить таблетки на протяжении всей жизни с точностью до минут — не самая простая задача. Этому мешают и банальная забывчивость, и разные случайные обстоятельства. А чем чаще человек нарушает время приема терапии, тем выше риск развития у вируса устойчивости. Именно поэтому врачи стараются назначать схемы с приемом лекарств один раз в день и с минимальным числом таблеток — чем реже и меньше нужно принимать лекарств, тем проще соблюдать режим. Правильное соблюдение режима приема терапии называют высокой приверженностью лечению.
Сейчас лучшими схемами считаются те, при которых пациенту нужно принимать одну таблетку один раз в день, да еще и независимо от приема пищи. Но настоящим прорывом в АРВТ станет разработка схем, при которых лекарство достаточно будет принимать всего один или несколько раз в месяц, — пролонгированных схем терапии. Хотя в настоящее время неизвестно, как поведут себя пролонгированные режимы в рутинной практике. Будет ли к ним сохраняться высокая приверженность — как это показывают исследования?
по теме

Общество
Грудное молоко VS смеси при ВИЧ: что говорят эксперты в 2020 году?
Основной недостаток таких таблеток — срок их действия ограничено временем нахождения таблетки в кишечнике и не превышает 12—24 часов. В случае же диареи таблетка может покинуть организм гораздо быстрее, а значит, уменьшится концентрация лекарства в крови, что может быть опасно. Для антиретровирусных препаратов создание таблеток или капсул с замедленным высвобождением лекарственного вещества не очень перспективно — современные схемы уже позволяют принимать терапию один раз в день. То есть удобство применения терапии такие таблетки не повысят.
Если нужно добиться продления эффекта препарата на дни и недели, а лекарство всасываться через кожу упорно не хочет, приходится прибегать к парентеральным пролонгированным формам. Можно зашить под кожу специальную стерильную таблетку, которая будет медленно растворяться и выделять лекарственное вещество: на коже делается небольшой разрез, в него вводят таблетку и зашивают рану.
Помимо таблеток, под кожу можно вводить специальные полимерные импланты, содержащие нужное лекарство. Преимущество имплантов — они могут выделять лекарственное вещество очень долго, до нескольких лет. Чаще всего такие импланты используют для гормональной контрацепции. Так как гормоны действуют в очень маленьких дозах, даже в небольшой по размерам имплант можно сразу поместить запас препарата на несколько лет. Например, противозачаточный препарат Имплантон, который вводится под кожу, продолжает действовать три года. Если действие препарата нужно прекратить — достаточно просто извлечь имплант.
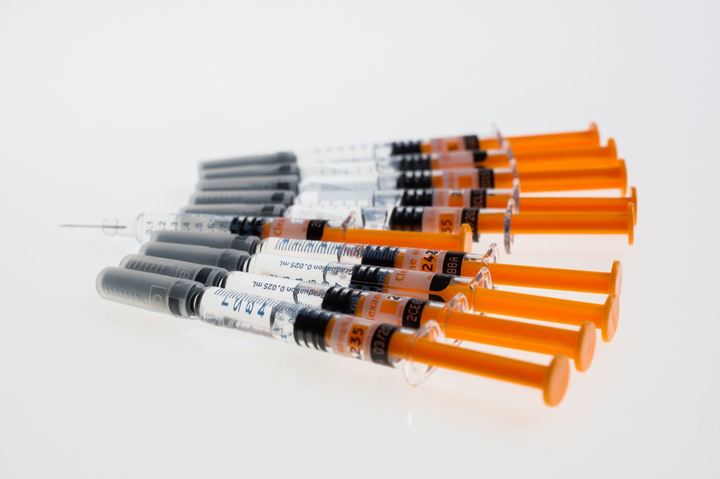
Более простой вариант — ввести в мышцу взвесь маленьких крупинок лекарства в подходящем растворителе. Выглядит это как обычный укол, при этом крупинки лекарства задерживаются в мышце, медленно растворяются и попадают в кровь. Такие способы введения лекарства особенно удобны в случаях, когда пациент может часто пропускать прием препарата, или забывать, принял ли он лекарство. Например, в случае лечения психических заболеваний. Но есть и недостатки: вводить такой препарат должен медицинский работник, а в случае непереносимости или выраженных побочных эффектов лекарство очень трудно быстро удалить из организма.
Что уже доступно на рынке?
Многие фармацевтические компании проводят исследования пролонгированных АРВ-препаратов, но разработка одного такого препарата сама по себе очень большой пользы не принесет — ведь для лечения ВИЧ-инфекции необходимо сочетание нескольких препаратов, то есть нужна комбинированная пролонгированная схема.
Такую схему, разработанную ViiV Healthcare совместно с Janssen, одобрили в марте 2020 года в Канаде — первый пролонгированный комбинированный АРВ-препарат Cabenuva. Схема показала высокую эффективность и безопасность в клинических исследованиях LATTE-2, FLAIR, ATLAS с участием более тысячи пациентов. В состав Cabenuva входят каботегравир и рилпивирин, то есть это двухкомпонентная схема. Препарат вводят один раз в месяц внутримышечно.
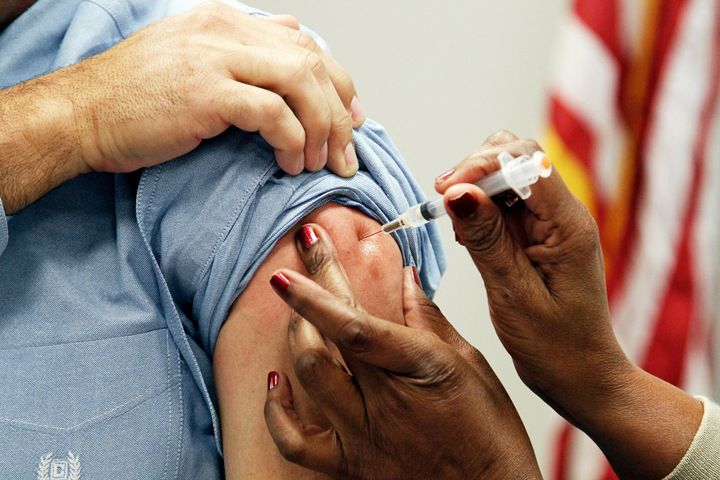
Перед началом применения Cabenuva пациент не менее месяца принимает каботегравир в таблетках (называется Vocabria) в комбинации с Эдюрантом — таблетками рилпивирина. Это необходимо, чтобы проверить переносимость такой схемы у конкретного пациента и оценить побочные эффекты. Если схема переносится хорошо, пациенту вводят первую нагрузочную дозу Cabenuva — 3 миллилитра суспензии, содержащей 600 миллиграммов каботегравира, и 3 миллилитра суспензии, содержащей 900 миллиграммов рилпивирина. Суспензии вводятся в разные участки ягодичной мышцы, то есть делают два укола. После этого поддерживающие дозы вводят ежемесячно: 2 мл (400 мг) каботегравира и 2 мл (600 мг) рилпивирина. Если по каким-то причинам введение очередной ежемесячной поддерживающей дозы невозможно, пациент до момента следующей инъекции может принимать пероральную схему (Vocabria + Эдюрант). Пролонгированная форма каботегравира также имеет большие перспективы для использования в качестве доконтактной профилактики ВИЧ-инфекции.
Еще один препарат, который уже применяется в клинической практике, — ибализумаб (Трогарзо) — можно назвать пролонгированным с несколькими оговорками. По химической природе ибализумаб — моноклональное антитело, то есть близок к человеческим иммуноглобулинам. Ибализумаб связывается с некоторыми белками на поверхности вируса и мешает проникновению ВИЧ в клетки. Препарат вводят внутривенно один раз в две недели и часто сочетают с другими АРВ-препаратами. Такая схема — не самый удобный вариант, поэтому сейчас ибализумаб используется только для лечения ВИЧ с множественной лекарственной устойчивостью, когда другие схемы оказываются неэффективными. Поэтому ибализумаб правильнее будет отнести к нишевым препаратам.
К сожалению, на этом и заканчивается не очень длинный перечень пролонгированных АРВ-препаратов, которые уже применяются на практике. Дальше пойдет речь о препаратах, находящихся на разных стадиях исследований.
Что сейчас находится в разработке?
PRO 140
С точки зрения места в клинической практике на ибализумаб похоже еще одно моноклональное антитело, находящееся в стадии клинических исследований, — PRO 140. Этот препарат также можно будет использовать для лечения ВИЧ-инфекции, если у пациента не работают другие схемы. А по механизму действия PRO 140 похож на уже существующий на рынке препарат маравирок (Целзентри). Он связывается с CCR-5 рецепторами на поверхности клеток-мишеней и мешает проникновению вируса в клетку. Строение активного центра молекулы PRO 140 отличается от маравирока, поэтому он активен даже в тех случаях, когда вирус выработал устойчивость к маравироку. Как и маравирок, PRO 140 активен только против CCR-5-тропных подтипов ВИЧ, то есть подойдет не всем пациентам. Препарат вводят внутривенно, один раз в неделю.
Нейтрализующие антитела
На разных стадиях клинических исследований находятся несколько перспективных антител, которые связываются с вирусным белком gp120 и нейтрализуют вирус: VRC01, 3BNC117 и 10-1074. Предполагается, что эти препараты достаточно будет вводить раз в месяц или даже реже и их можно будет применять совместно с другими пролонгированными АРВ-препаратами.
Албувиртид
Аналог уже применяющегося на практике энфувиртида (Фузеон). Этот препарат связывается с вирусным белком gp-41 и мешает проникновению вируса в клетку. Основное отличие в том, что Фузеон вводят подкожно два раза в сутки, что очень неудобно, а албувиртид — только один раз в 2—4 недели. Препарат должен применяться совместно с другими АРВ-лекарствами.
Исцеление – не то слово, которое часто используется в связи с термином "ВИЧ-инфекция". 35 лет прошло с момента обнаружения вируса и большую часть времени врачи рассматривали полное выздоровление скорее как фантазию, а не возможную перспективу. Всю потому, что ВИЧ не похож ни на один другой вирус. Он уничтожает те самые иммунные клетки, которые предназначены для того, чтобы с ним бороться. Он разрушает иммунную защиту месяцами, а иногда – годами.
На сегодняшний день с заболеванием живут 37 млн человек по всему миру. Однако сегодня ученые больше понимают о том, как вирус "скрывается" в клетках организма и почему наша бдительная иммунная система "не замечает" его.
Национальные институты здравоохранения (NIH) США финансируют усилия по лечению ВИЧ, а фонды – например AmfAR – ищут ресурсы, которые позволят полностью искоренить эпидемию.
"Абсолютно точно, что ВИЧ можно излечить, – говорит Ровена Джонстон, вице-президент и директор по исследованиям AmfAR. – Вопрос на миллиард долларов: "Как это сделать?".
Профессор медицины из Медшколы при Университете Джона Хопкинса Роберт Силичано одним из первых идентифицировал резервуары ВИЧ.
"Проблема в том, что такая форма ВИЧ не видна иммунной системе и на нее не влияют лекарственные препараты", – говорит Силичано. По словам доктора, вирус покидает свою укреплённую башню и идёт на штурм лишь тогда, когда человек перестаёт принимать лекарства.
В одном из докладов, которые представили на конференции по ретровирусам и оппортунистическим инфекциям 2018 года в Бостоне, исследователи обнаружили убедительные доказательства того, что резервуары могут быть активированы и устранены, по крайней мере – у животных. Дэн Барух и его коллеги из Медицинского центра Beth Israel Deaconess и Гарвардской медицинской школы показали, что препарат, который стимулирует иммунную систему и активирует резервуары, в сочетании с мощным антителом может нейтрализовать ВИЧ у инфицированных обезьян на полгода.
"Я думаю, что наши данные повышают вероятность получить препарат для полного вызоровления. Это возможно", – заявил Барух.
Такой метод в научной среде называют shock and kill: он основан на "выталкивании" спящего вируса из резеруаров и последующем уничтожении. Это шаг к избавлению людей от пожизненной зависимости от АРВ-препаратов.
Этот метод еще не был протестирован на людях и вопрос полного выздоровления еще в процессе изучения. Исследователи напоминают, что на сегодняшний день единственным полностью излечившимся от ВИЧ человеком является "берлинский" пациент, которому пересадили костный мозг от донора с особой мутацией, которая не позволяет вирусу иммунодефицита "прикрепляться" к клеткам. Браун прекратил прием АРВ-препаратов после пересадки. Прошло уже больше 10 лет и его тест на ВИЧ остаётся отрицательным.
[Подробнее об излечении Тимоти Рэя Брауна – в материале СПИД.ЦЕНТРа]
Случай Брауна доказывает, что полное выздоровление возможно, но врачи дожны добраться до "каждого закутка" организма, где может прятаться вирус, говорит доктор Стивен Дикс, профессор медицины Калифорнийского университета в Сан-Франциско.
Сейчас некоторые исследователи даже полагают, что возможно полностью реконструировать иммунную систему человека, чтобы она была способна успешно устранить любой вирус. Этим уже пользуются онкологи в борьбе с опухолями: иммунную систему программируют таким образом, что та сама атаковала злокачественные клетки.
"Я настроен оптимистично, поскольку параллели в терапии ВИЧ-инфекции и онкологии настолько тесны, что мы сможем применять товые технологии и в терапии ВИЧ", – говорит Дикс.
Никто из специалистов не ожидает, что ВИЧ будет побежден в следующем году или ближайшие пару лет. Но они более чем уверены, что в будущем мы победим эпидемию.
Читайте также:

