Лейкопения может наблюдаться при следующих профессиональных интоксикациях
Обновлено: 24.04.2024
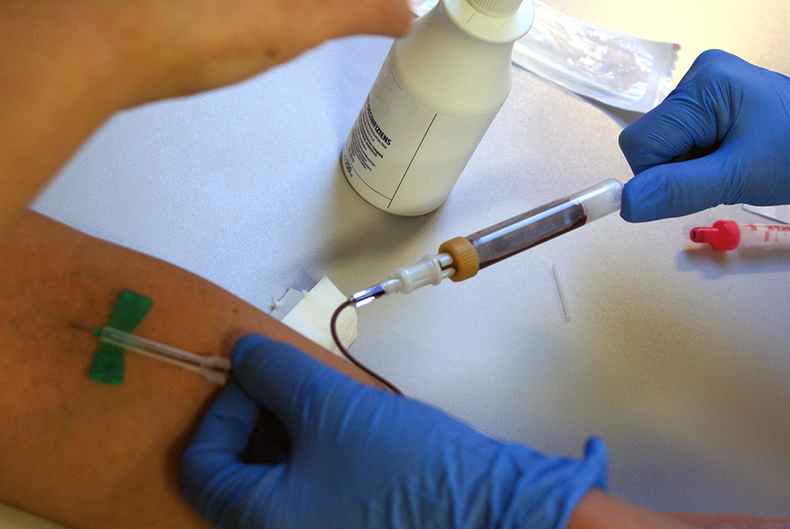
Лейкопения – это снижение уровня лейкоцитов в периферической крови ниже 4000 в 1 мкл. Причиной данного состояния могут быть инфекционные, воспалительные аутоиммунные заболевания, генетические дефекты иммунной системы и пр. Клинически лейкопения проявляется повышенной восприимчивостью организма к различным инфекциям, однако может протекать абсолютно бессимптомно. Уровень лейкоцитов измеряется при заборе венозной либо капиллярной крови утром натощак. Для коррекции данного лабораторного отклонения проводится лечение основного заболевания.
Классификация
Низкий уровень белых кровяных телец может встречаться у абсолютно здоровых лиц – конституциональная безвредная лейкопения отмечается примерно у 2-5% людей. По происхождению патологические лейкопении разделяют на:
- Наследственные (первичные). Низкое содержание лейкоцитов обусловлено генетически детерминированными нарушениями образования и созревания клеток в красном костном мозге. К ним относятся нейтропения Костмана, наследственная нейтропения аутосомно-доминантного типа и т.д.
- Приобретенные (вторичные). Более распространенный вариант. Лейкопения развивается вследствие действия ионизирующего излучения, неблагоприятного эффекта лекарственных препаратов, биологических агентов (бактерий, вирусов) или факторов иммунной аутоагрессии.
По патогенезу (механизму развития) различают лейкопении, возникшие вследствие:
- Нарушения поступления лейкоцитов в кровь из костного мозга. Развитие лейкопении обусловлено повреждением кроветворных клеток либо неэффективным лейкопоэзом из-за дефектов митоза, созревания лейкоцитов. Наблюдается при длительном приеме цитостатических лекарственных препаратов, действии ионизируюшей радиации, генетических заболеваниях, выраженном дефиците витамина В12, фолиевой кислоты.
- Перераспределения лейкоцитов. Происходит изменение соотношения между циркулирующим и пристеночным пулом белых клеток крови в результате их скопления в расширенных капиллярах органов-депо. Встречается при шоковых состояниях.
- Сокращения времени пребывания в крови. Время присутствия в крови лейкоцитов может уменьшаться из-за их деструкции антителами (при аутоиммунных патологиях), токсическими факторами (при тяжелых инфекциях), чрезмерно активированными макрофагами (при гиперспленизме). Усиленное выведение белых клеток крови может наблюдаться при гнойных процессах – холангите, эндометрите.
В зависимости от типа клеток лейкоцитарного ряда выделяют следующие разновидности лейкопении:
- Нейтропении. Снижение содержания нейтрофилов меньше 47% от общего числа лейкоцитов. Наиболее частый вариант лейкопении. Встречается при вирусных, бактериальных инфекциях, токсическом действии медикаментов. Также возможны наследственные формы нейтропении.
- Лимфопении. Уменьшение уровня лимфоцитов ниже 19%. Характерно для вирусных инфекций, коллагенозов, гранулематозных процессов.
- Эозинопении. Содержание эозинофилов меньше 1%. Наблюдается при избыточной продукции гормонов коры надпочечников (болезнь/синдром Иценко-Кушинга). Эозинопения является индикатором неблагоприятного прогноза при септических процессах.
- Моноцитопения. Показатели моноцитов в лейкоцитарной формуле опускаются ниже 2%. Встречается при острых инфекциях, длительном приеме глюкокортикоидов.
- Агранулоцитоз. Редкое тяжелое жизнеугрожающее состояние, характеризующееся полным или почти полным исчезновением нейтрофилов в крови (ниже 0,75х10^9/л). Наблюдается при приеме миелотоксичных лекарств (цитостатиков, тиреостатиков, некоторых НПВС), действии радиации.

Причины лейкопении
Инфекции
Одна из наиболее распространенных причин лейкопении – вирусные и генерализованные бактериальные инфекции. Патогенез снижения уровня лейкоцитов может быть различным – непосредственное повреждение клеток лимфотропными вирусами (ВИЧ, Варицелла-Зостер, корь), подавление образования в костном мозге, усиленная их потеря с экссудацией.
- Вирусные инфекции. Лейкопения развивается преимущественно за счет снижения содержания лимфоцитов (лимфопения). При инфекционном мононуклеозе, гриппе, вирусных гепатитах лейкоциты снижаются незначительно и быстро возвращаются к норме после выздоровления. При ВИЧ-инфекции уровень лимфоцитов нередко достигает нуля на стадии СПИДа. Даже после лечения значения лейкоцитов могут сохраняться низкими, так как препараты для терапии ВИЧ сами по себе способны вызвать лейкопению.
- Бактериальные инфекции. Лейкопения встречается только при тяжелых генерализованных инфекциях (менингококцемия, риккетсиозы, перитонит). Падение числа лейкоцитов является одним из критериев для диагностирования септического состояния и синдрома системного воспалительного ответа. Наблюдается в основном нейтропения, ее степень коррелирует с тяжестью заболевания. Регресс наступает практически сразу после проведения антибактериальной терапии.
Прием лекарственных препаратов
К развитию лейкопении способен привести широкий спектр лекарственных средств. Известно два основных механизма лекарственно-индуцированной лейкопении: токсическое повреждение костного мозга, ведущее за собой нарушение кроветворения, и образование иммунных комплексов, в результате чего вырабатываются антитела, атакующие собственные лейкоциты макроорганизма.
Лейкопения возникает в среднем на 15 сутки от начала приема лекарства. Степень тяжести может быть самой различной – от незначительного снижения количества белых кровяных клеток до агранулоцитоза. В связи с поражением всех 3-х ростков гемопоэза часто встречается сочетание с анемией и тромбоцитопенией (панцитопения). В большинстве случаев достаточно отмены лекарственного препарата. При развитии агранулоцитоза может потребоваться применение колониестимулирующих факторов. Медикаменты, наиболее часто вызывающие лейкопению:
- Цитостатики: циклофосфамид, хлопамбуцил, метотрексат.
- Тиреостатики: пропилтиоурацил, мерказолил.
- Нестероидные противовоспалительные средства: анальгин, амидопирин.
- Антибактериальные средства: левомицетин, сульфаниламиды.
- Противовоспалительные ЛС: D-Пеницилламин, сульфасалазин.
- Антипсихотические ЛС (нейролептики): аминазин, хлорпромазин.
- Противосудорожные ЛС: карбамазепин, диазепам.
Аутоиммунные воспалительные заболевания
Причиной лейкопении могут быть аутоиммунные заболевания. В этих случаях преимущественно снижаются лимфоциты и нейтрофилы. Существует два основных патогенетических механизма аутоиммунной лейкопении – образование антилейкоцитарных антител и снижение экспрессии на мембранах иммунных клеток специальных белков (CD55, CD59), которые защищают клетки от цитолиза. Лейкопения обычно умеренная, регрессирует во время ремиссии или под влиянием патогенетического лечения. Лейкопенический синдром характерен для следующих патологий:
- Заболевания суставов: ревматоидный артрит, синдром Фелти.
- Диффузные болезни соединительной ткани (коллагенозы): системная красная волчанка, синдром Шегрена.
- Демиелинизирующие заболевания: рассеянный склероз.
- Системные васкулиты: гранулематоз с полиангиитом, неспецифический аортоартериит Такаясу.
- Воспалительные заболевания кишечника (ВЗК): неспецифический язвенный колит, болезнь Крона.
Болезни крови
Механизмов лейкопении при гематологических патологиях несколько – замещение кроветворной ткани злокачественными клетками, фиброзной или жировой тканью, синтез антилейкоцитарных антител, дефицит некоторых химических элементов для гранулоцитопоэза (железа, цианкобаламина, фолиевой кислоты):
- Онкогематологические заболевания. Лейкопенией, вплоть до агранулоцитоза, могут дебютировать острые лейкозы (алейкемическая форма) – такое начало заболевания встречается примерно в 20% случаев. Почти всегда в анализе крови дополнительно выявляются тромбоцитопения и анемия. Лейкопения характерна для лимфогранулематоза (лимфомы Ходжкина). Уровень лейкоцитов нередко остается на низком уровне и после лечения.
- Гемолитические анемии. При аутоиммунных гемолитических анемиях, гемоглобинопатиях, наследственном микросфероцитозе возможна умеренная нейтропения. Примечательно, что падение уровня лейкоцитов происходит вне криза. Период гемолитического криза, напротив, сопровождается небольшим лейкоцитозом.
- Дизэритропоэтические анемии. При апластической анемии, а также длительно протекающей недостаточности витамина В12 и фолиевой кислоты из-за угнетения функционирования всех ростков кроветворения наблюдается панцитопения. Лейкопения при железодефицитной анемии развивается только при крайне выраженном дефиците железа и носит умеренный характер.
Лучевая болезнь
Действие ионизирующей радиации неблагоприятно сказывается на всем организме человека. В первую очередь и сильнее всего страдают органы с высокой скоростью клеточного обновления, к которым относится костный мозг. Под влиянием гамма-лучей, имеющих высокую проникающую способность, гемопоэтические стволовые клетки утрачивают митотическую активность.
Наследственные формы лейкопений
К первичным лейкопениям относятся генетические заболевания, обусловленные мутациями генов, регулирующих созревание или дифференцировку лейкоцитов. Некоторые мутации приводят к изменению структуры лейкоцитарных антигенов, из-за чего они подвергаются аутоиммунному разрушению. В подавляющем большинстве случаев встречаются первичные нейтропении.
Другие наследственные лейкопении часто сопровождаются инфекционными осложнениями, которые зачастую становятся фатальными уже в детском возрасте: болезнь Костмана (генетически детерминированный агранулоцитоз), первичные иммунодефициты (синдром Ди Джорджи, Вискотта-Олдрича), синдром Чедиака-Хегаси. При этих болезнях для восстановления нормальных значений лейкоцитов требуется специфическое лечение.
Другие причины
- Белковое голодание.
- Переливание крови или лейкоцитарной массы.
- Эндокринные расстройства: гипотиреоз, акромегалия, гиперкортицизм.
- Заболевания, протекающие с гиперспленизмом: цирроз печени, малярия, висцеральный лейшманиоз.
- Болезни накопления: болезнь Гоше, болезнь Ниманна-Пика.
Диагностика
Лейкопения выявляется при клиническом исследовании крови. Ввиду многообразия этиологических факторов данного отклонения при его обнаружении следует обратиться к врачу-терапевту для тщательного сбора анамнеза, физикального осмотра, назначения дополнительного обследования:
- Анализы крови. Выполняется подсчет лейкоцитарной формулы, определяется концентрация маркеров воспаления – СОЭ, СРБ, прокальцитонина. Изучается наличие аутоантител (антител к ДНК, цитоплазме нейтрофилов, аЦЦП).
- Выявление инфекционного возбудителя. Методом иммуноферментного анализа идентифицируются антитела к возбудителям (вирусам, бактериям). Для подтверждения ВИЧ-инфекции назначается иммуноблоттинг. Проводится бактериальный посев крови, мокроты, мочи.
- Биопсия. При подозрении на лейкоз выполняется морфологическое исследование костного мозга, при котором обнаруживается гиперплазия гранулоцитарного ростка, большое количество бластных клеток. Для диагностики лимфом проводится аспирационная биопсия увеличенного лимфатического узла, в биоптате выявляется лимфоцитарная гиперклеточность, разрастание коллагена.
- Генетические исследования. Для подтверждения наследственных форм лейкопений необходимо обнаружение мутаций методом полимеразной цепной реакции и цитогенетическими исследованиями.

Коррекция
Конституциональная лейкопения не требует никакого вмешательства. Если причиной развития данного отклонения стал лекарственный препарат, необходима срочная его отмена. При выраженном снижении лейкоцитов или агранулоцитозе прибегают к введению гранулоцитарного колониестимулирующего фактора (Г-КСФ) или инфузии донорских гранулоцитов. Главное условие успешности терапии – лечение основной патологии:
- Элиминация возбудителя. Для лечения гриппа применяется осельтамивир, для борьбы с ВИЧ-инфекцией – антиретровирусные препараты (зидовудин, саквинавир). При бактериальной инфекции назначаются антибиотики.
- Противовоспалительная терапия. Чтобы достигнуть ремиссии аутоиммунных заболеваний, используются глюкокортикостероиды, иммуносупрессанты, производные 5-аминосалициловой кислоты.
- Химиотерапия. При подтверждении онкогематологической патологии назначаются комбинации химиотерапевтических средств – хлорамбуцил, винкристин, этопозид.
- Пересадка костного мозга. В случае неэффективности химиотерапии гемобластозов, а также при тяжелых первичных нейтропениях выполняется трансплантация гемопоэтических стволовых клеток.
Прогноз
Некоторые формы первичных лейкопений характеризуются высоким уровнем смертности (50-90%) среди детей от инфекционных осложнений. При вторичных лейкопениях прогноз в большей степени зависит от основного заболевания. Поэтому при любом уровне снижения лейкоцитов в крови показано тщательное обследование, направленное на выяснение причины и своевременное начало лечения.
1. Патофизиология системы крови. Часть II. Нарушения в системе лейкоцитов/ Николаева О.В., Кучерявченко М.А., Шутова Н.А. и др. – 2016.
4. Синдромная диагностика и базисная фармакология заболеваний внутренних органов. Том 2/ под ред. Г.Б. Федосеева, Ю.Д. Игнатова. – 2004.

Лейкопения – состояние, при котором уровень лейкоцитов в крови ниже 4000 в 1 мкл. Спровоцировать его развитие могут различные факторы: патогенные агенты, воспалительные процессы, аутоиммунные заболевания, генетические нарушения и многое другое. Проявляется лейкопения в виде повышенной восприимчивости организма к инфекциям. При соблюдении мер безопасности и рекомендаций врача обычно протекает бессимптомно. Выявить лейкопению удастся по анализу капиллярной или венозной крови.
Разновидности лейкопений
Даже у абсолютно здоровых людей может быть лейкопения. Статистика ВОЗ называет, что около 3% населения имеют пониженный уровень лейкоцитов в крови. По происхождению это заболевание бывает 2 видов:
- Первичное. В таком случае болезнь носит наследственный характер. Она развивается из-за генетических детерминированных нарушений, из-за которых в костном мозге не созревает достаточное количество лейкоцитов;
- Вторичное. Это приобретенная лейкопения. Она возникает из-за влияния патологических факторов, таких как облучение или длительный прием лекарственных препаратов.
Также лейкопению принято различать по механизму развития. Болезнь развивается из-за:
- Нарушения поступления лейкоцитов из костного мозга;
- Неправильного перераспределения лейкоцитов;
- Сокращения времени пребывания лейкоцитов в крови.
Лейкоциты состоят из нескольких типов клеток. При диагностике болезни нужно определять, какого именно фрагмента в крови недостаточно. В зависимости от типа недостающих клеток, существуют следующие формы лейкопений:
- Нейтропения – снижение уровня нейтрофилов;
- Лимфопения – недостаток уровня лимфоцитов;
- Эозинопения – концентрация эозинофилов не достигает 1%;
- Моноцитопения – показатель моноцитов ниже 2%;
- Агранулоцитоз – полное или почти полное отсутствие нейтрофилов в крови.


Основные симптомы лейкопении
При незначительном снижении уровня лейкоцитов выявить лейкопению удастся только при помощи клинического анализа крови. Болезнь не будет проявлять себя явными признаками. Если же отклонение от нормы значительное, пациенты могут жаловаться на следующие симптомы:
- Повышение температуры тела до 37,5-38 градусов;
- Постоянное ощущение усталости, общую слабость;
- Головную боль, головокружение;
- Ощущение нехватки воздуха;
- Боли в животе, расстройство пищеварения;
- Ломоту в костях, суставах.
Пациенты с лейкопенией склонны к различным инфекционным процессам. Это происходит из-за снижения иммунных способностей организма. Первыми поражаются слизистые оболочки ротовой полости, так как в них изначально присутствует мощная бактериальная флора. У пациента развивается язвенно-некротический стоматит.
Затем поражается мочеполовая система. Больные жалуются на учащенное болезненное мочеиспускание, ощущение неполного опорожнения мочевого пузыря. У женщин наблюдаются проблемы с менструацией: она становится нерегулярной, удлиненной. Наибольшую опасность представляет некротическая энтеропатия – тяжелое поражение кишечника.
Самым грозным осложнением лейкопении является сепсис. Это – генерализованное воспаление на фоне локальной инфекции. В таком случае вероятность смертельного исхода высока.
Лейкопения – это рак?
Особую опасность представляет ситуация, когда снижение лейкоцитов сопровождается появлением синяков по всему телу, повышением температуры тела, быстрой утомляемостью, многочисленными кожными высыпаниями. В таком случае нужно пройти комплексную диагностику и обратиться к врачу.
Лейкопения является одним из симптомов рака крови. Это опасное заболевание, главная коварность которого – отсутствие опухоли, которую нужно удалять. Именно поэтому лейкопения требует обязательного диагностического обследования, ведь онкология, выявленная на начальных стадиях, хорошо поддается лечению.
Причины возникновения лейкопений
Спровоцировать развитие лейкопении способно множество факторов. Очень важно определить точную причину этого нарушения, ведь от нее будет зависеть и тактика лечения. Причиной снижения лейкоцитов в крови человека могут стать следующие факторы:
- Патологии клеток крови и костного мозга: апластическая анемия, миелофиброз, миелодиспластические синдромы, гиперспленизм, миелопролиферативный синдром;
- Наследственные заболевания: миелокатексис, синдром Костмана;
- Инфекции: туберкулез, ВИЧ, СПИД, различные вирусные заражения;
- Аутоиммунные патологии: системная красная волчанка, полиневрит, ревматоидный артрит;
- Авитаминоз: недостаток витаминов группы В, меди, цинка, других минералов. Обычно происходит из-за несбалансированного питания;
- Прием некоторых лекарственных препаратов: Интерферона, Клозапина, Миноциклина, Циклоспорина, некоторых антибактериальных средств;
- Саркоидоз: заболевание, при котором наблюдается слишком бурная реакция иммунитета;
- Онкология: при раке происходит снижение концентрации белых кровяных клеток из-за повреждения костного мозга. Подобный клинический признак наблюдается и у пациентов после лучевой либо химиотерапии, пересадки костного мозга.
Диагностика лейкопении
Определить лейкопению можно при помощи общего анализа крови. Именно он показывает концентрацию лейкоцитов в крови. Дополнительно проводят исследование крови с дифференциацией лейкоцитов: исследование помогает определить, каких именно белых кровяных клеток недостаточно. Этот анализ позволяет обозначить круг возможных причин лейкопении. Также диагностика лейкопений включает:
- Гемограмму – определяет абсолютное количество эритроцитов, лейкоцитов, тромбоцитов, показывает процентное соотношение различных видов белых клеток;
- Иммунологический анализ крови – выявляет антигранулоцитарные и антинуклеарные иммуноглобулины;
- Биохимический анализ крови – отражает количество фолатов, витамина В12, печеночных трансаминаз, билирубина в крови;
- Цитологическое исследование – направлено на определение конкретного типа лейкопений, устанавливает механизм ее развития;
- Анализ крови на гепатиты, ревматоидный фактор.
Может потребоваться проведение и других исследований. Они нужны для определения причины лейкопении. Через некоторое время после первого обследования назначаются повторные анализы – это необходимо для получения достоверного результата.
Методы лечения
При первых признаках инфекции пациентам с лейкопенией назначают антибактериальные препараты. Первоначально применяются антибиотики широкого спектра действия. Когда будут готовы результаты о чувствительности микроорганизмов, подбирается подходящая терапия. Если состояние пациента улучшается в течение 72 часов, то схема лечения подобрана эффективно. Препараты продолжают принимать в течение недели или до полного исчезновения симптомов в той же дозировке.
Отсутствие эффекта от лечения говорит об антибиотикорезистентности, когда микроорганизмы устойчивы к действующим веществам препарата, или наличии двух и более инфекций. Если у пациента нет признаков заражения, но уровень лейкоцитов значительно снижен, проводится профилактическая терапия антибиотиками. При грибковых инфекциях показаны противогрибковые препараты.
Для лечения лейкопении также назначают колониестимулирующие факторы – факторы роста. Они заставляют красный костный мозг активнее продуцировать новые кровяные клетки. Используются препараты 2 видов:
- G-CSF – гранулоцитарные колониестимулирующие факторы. Способствуют быстрому росту нейтрофилов;
- GM-CSF – гранулоцитарно-макрофагальные колониестимулирующие факторы. Вызывают ускоренную выработку гранулоцитов и макрофагов.
В качестве поддерживающей терапии назначаются глюкокортикостероиды, анаболические стероиды, витаминные комплексы. Они не помогают вырабатывать лейкоциты, но препятствуют их стремительному разрушению.
При развитии тяжелого инфекционного процесса (сепсиса, пневмонии, некротической энтеропатии) и при отсутствии эффекта от антибиотиков проводится переливание лейкоцитарной массы. Если лейкопения возникла на фоне лучевой либо химиотерапии, необходимо пересмотреть используемую схему терапии или заменить отдельные препараты.
Трансплантация костного мозга при лейкопении
В редких случаях лейкопения обусловлена низким уровнем агранулоцитов в крови. В таком случае медикаментозная терапия неэффективна. Химиотерапия, которая необходима для лечения онкологии, разрушает собственный костный мозг. Для терапии лейкопении такого типа проводится трансплантация костного мозга – пересадка части стволовых клеток. Именно они и будут вырабатывать новые лейкоциты.
При низком уровне лейкоцитов также проводится переливание лейкоцитарной массы. Обычно процедура назначается пациентам с системной вирусной инфекцией при отсутствии эффекта от антибиотиков. Однако при локальном бактериологическом воспалении или же инфицировании вирусом переливание лейкоцитарной массы не дает никакого результата.
Прогноз и профилактика
Смертность от лейкопении на фоне лучевой или химиотерапии составляет 4-6%. Если болезнь не вызвана лечением онкологии, то показатель колеблется на уровне 5-10%. Еще 20 лет назад это значение достигало 20%. Снижения данного параметра удалось добиться за счет разработки адекватной антибактериальной терапии, грамотного ухода за больным, применения КСФ.
Высокая смертность наблюдается у пожилых пациентов, у людей с почечной и печеночной недостаточностями, если лейкопения осложнилась септическим шоком либо бактериемией. Специфической профилактики лейкопении не существует. Врачи дают следующие обязательные к выполнению рекомендации:
- Каждую неделю сдавайте анализ крови;
- Пропивайте витаминные комплексы;
- Минимизируйте стрессы и переживания;
- Носите защитную маску в общественных местах;
- Соблюдайте правила личной гигиены, ежедневно принимайте душ;
- Не контактируйте с домашними животными, их фекалиями;
- Откажитесь от бритья, маникюра (всего, из-за чего можно пораниться);
- Откажитесь от работ с почвой;
- Правильно и полноценно питайтесь;
- Откажитесь от вредных привычек;
- Строго соблюдайте протокол химиотерапии.
Лейкопения – опасное состояние. Оно требует обязательного соблюдения всех рекомендаций врача. Игнорирование этих правил часто приводит к смертельным осложнениям. Если вы проходите химиотерапию, нужно быть максимально внимательным к своему здоровью. Контролировать течение лейкопении и подобрать эффективное лечение вам помогут в медицинском центре Медскан. Опытные врачи смогут разработать индивидуальную схему терапии, которая снизит риск развития каких-либо осложнений.
Нейтропения – состояние, при котором снижено количество нейтрофилов в крови. Из-за этого бактериальные и грибковые заболевания протекают гораздо сложнее. Симптомы патологического процесса могут быть невыраженными, однако у пациента стремительно развивается лихорадка. В таком случае нужны антибиотики широкого спектра действия. При диагностике нейтропении важно не только определять число нейтрофилов, но и причину снижения их концентрации. Часто такое состояние развивается у раковых больных после химиотерапии.
Почему нейтропения возникает после лучевой и химиотерапии?
Нейтропения – снижение количества нейтрофилов к крови. Это белые кровяные клетки, которые отвечают за обнаружение инфекции и ее уничтожение. Это значит, что нейтрофилы нужны человеку для защиты всего организма.
Из-за повреждения быстроделящихся клеток костного мозга нейтропения часто развивается у пациентов, которые прошли лучевую или химиотерапию. Это приводит к снижению количества нейтрофилов в крови. Это частая практика, когда костный мозг пытается восполнить дефицит, однако концентрация нейтрофилов все равно не может обеспечить полноценную защиту. Степень нейтропении зависит от режима лучевой или химиотерапии, возраста и других особенностей самого пациента.
Уже через неделю после первой процедуры химиотерапии в организме начинает стремительно снижаться количество нейтрофилов. Минимальное значение наблюдается в течение 1-2 недель после процедуры. Это время является наиболее опасным, так как пациент максимально подвержен любым инфекционным процессам. Постепенно костный мозг начнет восстанавливаться и вырабатывать необходимое количество нейтрофилов. Но для восстановления нужно время.
Пациентам, страдающим нейтропенией, нужно помнить о следующих фактах:
- Нейтропения угрожает жизни. Статистика утверждает, что каждый 14 пациент умирает от осложнений, вызванных этим состоянием;
- 7-12 день после химиотерапии – период наибольшего риска. Именно тогда уровень нейтрофилов максимально низок;
- Химиотерапия всегда вызывает нейтропению. Такое воздействие на организм убивает не только раковые, но и здоровые нужные клетки. Из-за этого иммунитет ослабляется;
- Любые инфекции при нейтропении прогрессируют очень быстро. У пациентов после химиотерапии может стремительно расти температура тела. Если ее значение поднялось выше 38 градусов, нужно сообщить об этом врачу.

Возможные причины нейтропении
Спровоцировать развитие нейтропении может огромное количество факторов. Они могут быть естественными и патологическими. Чаще всего патологию вызывают:
- Онкологические заболевания. Лучевая и химическая терапии при лечении рака повреждают костный мозг. Также процедуры убивают не только раковые, но и полезные клетки крови. Из-за этого костный мозг некоторое время не может вырабатывать достаточное количество нейтрофилов;
- Длительный прием лекарственных препаратов. Способствовать нейтропении способны средства для лечения гиперфункции щитовидки, некоторые антибиотики, противовирусные, противовоспалительные, антипсихотические препараты, комплексы для лечения аритмий;
- Инфекционные процессы. Нейтропению вызывают ВИЧ, СПИД, ветряная оспа, сальмонеллез, корь, вирус Эпштейна-Барр, гепатиты;
- Аутоиммунные заболевания. Это ревматоидный артрит, системная красная волчанка, гранулематоз, полиангиит;
- Патологии костного мозга. Такие как апластическая анемия, миелофиброз, миелодиспластический синдром;
- Авитаминоз. Способствовать развитию нейтропении может дефицит витаминов группы В, D.
Нейтропения – опасное состояние. Оно представляет серьезную угрозу здоровью и жизни пациента. Любая инфекция, протекающая на ее фоне, значительно ослабляет организма.
Основные симптомы нейтропении
Скорость появления нейтропении зависит от тяжести инфекционного процесса, а также степени снижения уровня этих кровяных клеток. Обычно у пациентов в первую очередь образуются стоматиты, появляется тонзиллит, фарингит. Из-за отсутствия движения лейкоцитов воспаление имеет фиброзно-некротический характер.
На слизистых формируется серый налет, который указывает на развитие бактериального процесса. Инфекционные агенты попадают в общий кровоток и стремительно распространяются по организму. У пациента появляется головная боль, апатия, тошнота, температура тела может достигать 40 градусов. Также к характерным симптомам нейтропении относят:
- Стремительное формирование язв. Первоначально они распространяются по слизистым оболочкам щек. В будущем это может привести к гангрене тканей лица. Затем поражается желудочно-кишечный тракт: возникает некроз слизистой желудка, кишечника, пищевода;
- Из-за поражения ЖКТ появляется сильная боль и вздутие живота. Глубокие нарушения проявляются кровоизлияниями. Возрастает риск развития желтухи;
- Воспаление легких. При нейтропении оно протекает атипично, при отсутствии лечения переходит на соседние органы. На легких формируются надрывы и гангрены. Определить воспаление можно по сильному кашлю, одышке, боли в груди при дыхании;
- Поражение мочеполовой системы. Инфекция затрагивает мочевой пузырь, уретру либо матку. В таком случае у пациента возникает боль внизу живота, острые рези при мочеиспускании. Для женщин характерно появление белесых выделений из влагалища;
- Нарушения в работе сердца. Из-за общей интоксикации организма развивается венозная и артериальная гипотония. При прослушивании сердца – присутствуют функциональные шумы;
- Поражение почек. На фоне активности инфекционных агентов организм выводит белок. Также в моче обнаруживается кровь, эпителиальные клетки почечных канальцев;
- Развитие септических осложнений. Патогенные агенты стремительно распространяются по организму и вызывают многочисленные нарушения. Из-за сапрофитной флоры может произойти заражение крови. В таком случае болезнь протекает очень тяжело, температура тела возрастает до 41-42 градусов. По всему телу появляются очаги черной сыпи.
Нейтропения – тяжелая болезнь, которая при несоблюдении мер безопасности приводит к серьезным осложнениям и даже смерти. При соблюдении всех рекомендаций врача пациент сможет защитить себя от таких последствий. Легкую степень нейтропении определяют только по результатам общего анализа крови. Назначаются поддерживающие препараты, которые не допустят нарастания более серьезных симптомов.
Каждый пациент с этой патологией должен быть максимально внимательным к своему здоровью. Особенно, если он находится в группе повышенного риска. Нужно обязательно обратиться к врачу, если появились подобные симптомы:
- Температура тела повысилась до 38 градусов;
- Озноб либо обильное потоотделение;
- Покраснение, боль, отечность при небольшом повреждении кожи;
- Одышка, кашель;
- Зуд, выделения из половых органов;
- Болезненное и учащенное мочеиспускание;
- Нарастающая боль в животе;
- Боль в горле, полости рта.
Методы диагностики
Нейтропения часто развивается у пациентов, которые подвержены инфекциям. В группе повышенного риска находятся люди, прошедшие лучевую либо химическую терапию. Выявить нейтропению можно по общему анализу крови. По результатам врач сможет определить инфекционный процесс в организме. Дополнительно диагностика включает проведение следующих исследований:
- Бактериального посева крови – выявляет патологических агентов;
- Общего анализа мочи – определяет функцию почек;
- Миелограммы – исследования состава костного мозга;
- Рентгенографии легких – диагностирует воспаление легких.
Лечение
Определенной схемы лечения при нейтропении не существует: болезнь отличается разнообразным течением, причинами возникновения. Интенсивность терапии будет зависеть от самого пациента: его состояния, возраста, степени поражения и распространения воспалительного процесса. Легкие формы нейтропении не требуют какого-либо лечения. Обострения инфекций лечатся так же, как и у всех больных.
Пациентам с тяжелой нейтропенией нужно находиться под постоянным врачебным контролем – их кладут в стационар. Назначаются противовирусные, антибактериальные, противогрибковые препаратами с повышенными дозами. При выборе лекарства необходимо провести анализ чувствительности микрофлоры к действующим веществам. До получения результатов пациенту внутривенно вводят антибиотики широкого спектра действия. Если его состояние не улучшилось после 3 дней медикаментозной терапии, увеличивают дозу антибиотика или меняют препарат.
Больным нейтропенией, у которых болезнь развилась на фоне химиотерапии или лучевого облучения, показан прием антибиотиков до тех пор, пока количество нейтрофилов не достигнет 500 мг/мкл крови. Если к инфекционному процессу присоединяется грибковый, необходим прием фунгицидов. Чтобы минимизировать риск бактериального заражения, пациенту назначают триметоприма сульфаметоксазола. Все чаще для лечения нейтропении используются колониестимулирующие факторы. Для поддержания иммунитета необходимо принимать глюкокортикостероиды, витаминные комплексы.
Если на фоне нейтропении произошло разрушение селезенки, показано ее хирургическое удаление. Однако операция категорически противопоказана при септических осложнениях и тяжелых формах патологии. В наиболее запущенных случаях может потребоваться пересадка костного мозга.
Прогноз и профилактика
Прогноз при нейтропении зависит от того, насколько оперативно и полноценно была начата терапия. При первых признаках лихорадки необходимо незамедлительно обращаться к врачу и подбирать комплексное лечение. Чтобы минимизировать вероятность инфекций, пациентам с нейтропенией нужно помнить о следующих правилах:
- Ежедневно принимайте душ с мочалкой и мылом;
- Используйте антибактериальное мыло для рук;
- Пользуйтесь спиртосодержащим антисептиком для рук вне дома;
- После каждого приема пищи чистите зубы;
- Постарайтесь свести к минимуму любые контакты. Полностью ограничьте контакты с людьми, которые недавно болели или имеют признаки инфекций;
- При посещении общественных мест надевайте маску;
- Не посещайте стоматолога без острой необходимости;
- Не употребляйте в пищу сырые продукты, соблюдайте низкомикробную диету;
- Выделите себе отдельные столовые приборы, предметы гигиены;
- Не делайте никакие процедуры красоты;
- Не пользуйтесь бритвой – возможны порезы;
- После каждого контакта с животными мойте руки;
- Откажитесь от работ в саду, не контактируйте с почвой;
- Не трогайте лотки животных, продукты их жизнедеятельности.
Нейтропения – опасное состояние, которое представляет огромную угрозу для жизни. Оно требует соблюдения особых мер безопасности, а также назначения грамотного лечения. Если у вас присутствует риск развития нейтропении или же это заболевание уже есть, вам необходимо находиться под постоянным врачебным контролем. Вы можете обратиться в медицинский центр Медскан, где вам проведут комплексную диагностику и разработают индивидуальную схему лечения.

Раковая интоксикация (эндотоксикоз) – это патологический процесс, который развивается в организме онкологического больного в результате распада злокачественной опухоли. Состояние характерно для поздних стадий рака. Вызвать опухолевую интоксикацию может и активная противораковая терапия.
К характерным признакам эндотоксемии (отравления организма продуктами опухолевого распада) относятся тошнота, рвота, утомляемость, слабость, снижение веса, сухость слизистых, боли в суставах, психические нарушения и др. Опухолевая интоксикация, клинические проявления которой имеют интенсивную симптоматику, приводит к системным нарушениям в виде почечной и печеночной недостаточности. Возникает риск развития инфекционных осложнений и сепсиса.
Если проигнорировать симптомы интоксикации и не принять меры по их устранению, пациент быстро теряет силы и вес, развивается кахексия. Далее человек впадает в состояние комы, из которого его вывести практически невозможно. Принимать лечебные меры нужно незамедлительно при появлении первых подозрений на раковую интоксикацию.

Причины опухолевой интоксикации
Отличительной особенностью раковых заболеваний является быстрый и неконтролируемый рост злокачественного образования, клетки которого продуцируют токсины. Сосуды, обеспечивающие кровоснабжение опухоли, растут медленнее, чем сама опухоль.
Способность раковых клеток выживать в условиях гипоксии, несколько затягивает процесс. Но гибель клеток все же происходит. Их огромное количество распадается и попадает в кровоток. Большая концентрация в крови погибших клеток вызывает интоксикацию. Зараженная кровь продолжает циркулировать по всему организму, затрагивая все органы. Это приводит к необратимому процессу и системным нарушениям.
В патогенезе раковой интоксикации:
- повышение уровня мочевой кислоты;
- увеличение числа ионов калия;
- рост процентного соотношения фосфатов;
- снижение концентрации кальция.
Рассмотренные вещества образуются при отмирании тканей злокачественного образования и проникают в кровоток. Этот процесс приводит к осложнениям из-за нарастающего обезвоживания организма. Отмечается перевозбуждение организма вследствие снижения уровня ионов кальция на фоне излишней концентрации фосфатов. Из-за повышенного содержания кальция происходит негативное воздействие на функционирование миокарда, что проявляется аритмией.
Синдром опухолевой интоксикации характерен для более обширных новообразований. Гибель большого количества раковых клеток – основная причина распада опухоли и отравления организма. На степень развития интоксикационного процесса влияет природная специфика атипичных клеток и их общее количество.
Яркие признаки отравления организма при распаде раковых клеток часто наблюдаются в результате проведения интенсивного химиотерапевтического лечения. При проведении химио- или лучевой терапии речь идет о массовой гибели раковых клеток. В дальнейшем продукты распада попадают в кровь и вызывают интоксикационное воздействие на организм больного. Вещества, которые находятся в составе препаратов, используемых при химиотерапии, плохо выводятся из организма и имеют свойство накапливаться. Опухолевая интоксикация проявляется яркой выраженностью уже в первые дни химиотерапевтических процедур.
Существует ряд факторов, которые усложняют и усугубляют течение интоксикационного процесса:
- возраст и общее состояние пациента;
- наличие сопутствующих заболеваний;
- интенсивность процесса распада;
- кровопотери в результате оперативного вмешательства.
Прогноз жизни при раковой интоксикации на последних стадиях является неблагоприятным. Летальный исход возможен при внутреннем кровотечении, истощении и тромбозе. Огромный риск смерти при раковой интоксикации возникает при почечной недостаточности, нарушении сердечной деятельности, а также при поражении органов метастазами.
Симптомы раковой интоксикации
Симптомы опухолевой интоксикации характеризуются постепенным проявлением. Исключением является развитие синдрома лизиса опухоли после проведения химиотерапии. Быстрый рост симптоматики требует моментального реагирования, имеется риск развития острой стадии почечной недостаточности.
Типичные симптомы раковой интоксикации:
- Слабость и усталость. Появляются даже при незначительных физических нагрузках. Пациент большую часть времени проводит в постели.
- Повышение субфебрильной температуры. Образование некротической полости и распад большей части опухолевого конгломерата (может сопровождаться повышением температуры до 400C).
- Изменение цвета кожи. Сначала становится бледной, затем появляется землистый оттенок. Бледность может быть причиной развития анемии, в результате нарушения работы почек и эндокринной системы.
- Нарушение сердечной деятельности. Меняется ритм сердечных сокращений, учащается дыхание.
- Повреждение нервной системы. Ночной сон нарушается, появляется дневная сонливость с признаками депрессии. Характерны периодические приступы мигрени и головокружения.
- Нарушение функции почек. Продукты метаболизма блокируют почечные канальцы, в результате снижается мочевыделительная функция. Большая концентрация мочевины в крови проявляется зудом и образованием на теле пятен, похожих на синяки.
Опухолевая интоксикация проявляется повышенной потливостью и отечностью. Постоянное ощущение тошноты, не проходит даже после рвоты. Нарушается функция печени, что приводит к уменьшению сопротивляемости токсинам и изменению вязкости крови.
Диагностика и лечение опухолевой интоксикации
На первом этапе диагностических мероприятий проводится осмотр больного и оценка симптомов раковой интоксикации и прогноза для жизни. Далее назначаются анализы крови на биохимию и дополнительные инструментальные исследования. Важную роль здесь играет определение основной причины, повлекшей развитие симптоматики. Если наблюдается характерная для опухолевой интоксикации картина клинических проявлений, назначается комплексное исследование.
Основные диагностические мероприятия при раковой интоксикации:
- общий анализ мочи и крови;
- анализ крови на биохимию;
- кровь на онкомаркеры;
- сцинтиграфия костного аппарата;
- осмотр гинеколога (для женщин);
- рентген грудной клетки;
- УЗИ брюшной полости и органов малого таза.
План проводимых исследований имеет индивидуальный подход. Для определения степени тяжести опухолевой интоксикации при диагностированном раке используется перечень стандартных анализов.
Однозначное определение эндогенной или раковой интоксикации дать сложно. Это связано с тем, что интоксикация при почечной недостаточности имеет определенную схожесть с эндотоксикозом. Многие промежуточные метаболиты, которые оказывают токсическое действие, до сих пор не идентифицированы. В качестве неспецифического маркера используется высокий уровень олигопептидов. Без тщательного исследования и коррекции раковой интоксикации адекватное лечение не может быть проведено, поэтому и полного излечения быть не может.
Лечение раковой интоксикации
При интенсивном росте опухолевого очага признаки интоксикации могут наблюдаться на более ранних стадиях. Поэтому онкологи заранее назначают пациенту мероприятия для предупреждения или облегчения интоксикационного синдрома. Все известные процедуры (гемодиализ, экстракорпоральная гемосорбция и др.) имеют недостаточный уровень эффективности и кратковременный результат.
Для улучшения показателей проводимого лечения при раковой интоксикации используется комплексный подход:
- углеродные волокнистые и гранулированные энтеросорбенты;
- экстракорпоральная гемосорбция (при химиотерапии).
Полученный результат является кратковременным, но мощным. Энтеросорбция гранулированными или волокнистыми сорбентами позволяет добиться медленного, но существенного снижения уровня эндотоксемии. При проведении многочисленных исследований удалось установить, что энтеросорбенты при пероральном приеме дают длительный и выраженный детоксицирующий эффект. Это именно то, что нужно при хронической раковой интоксикации.
Терапевтические мероприятия направлены на устранение симптоматики и восстановление функций поврежденных органов и систем. Тяжелая опухолевая интоксикация предусматривает применение плазмафереза или гемодиализа.
Основные направления лечения больных с опухолевой интоксикацией:
- Рвотная симптоматика устраняется противорвотными средствами (метоклопрамид, домперидон).
- При запорах назначаются слабительные препараты (бисакодил, макрогол).
- Широко используются сорбенты, зарекомендовавшие себя, как средство для детоксикации. Они обладают свойством связывать токсины, и с каловыми массами выводят их из организма.
- Проводится дезинтоксицирование организма введением большого количества жидкости, с последующим ускоренным ее выведением.
- Пациентам с низким уровнем гемоглобина назначаются железосодержащие препараты, в виде капельниц или инъекций (эритропоэтин).
- При наличии психических расстройств пациентам назначаются седативные средства, при депрессивных состояниях – антидепрессанты и транквилизаторы.
В соответствии с показателями долголетней практики, у большей части пациентов с эндотоксикозом происходит развитие сердечной или почечной недостаточности. Эти патологии в большинстве случаях являются причиной скоропостижной смерти больного. При принятии неотложной онкологической помощи такой исход удается предотвратить. Лечебная программа, направленная на устранение выраженной симптоматики, позволяет улучшить состояние больного, повысить качество и продолжительность жизни. Основным путем улучшения прогноза жизни при раковой интоксикации является усиление ранней диагностики злокачественного процесса с помощью проведения профилактических программ в практику здравоохранения (поезд здоровья, онкопатруль и др.).
Режим питания при раковой интоксикации предусматривает употребление еды небольшими порциями. При этом между приемами пищи интервалы должны быть небольшими. В рацион следует ввести самые необходимые для жизнеобеспечения минералы и микроэлементы. Ни в коем случае нельзя допустить обезвоживания. Известно, что жидкость выводит токсины. При невозможности приема пищи, ее вводят парентерально. Ежедневный рацион должен включать продукты, насыщенные витаминами и минералами. Обязательное составляющее – белок, углеводы и жиры. Рекомендована умеренная физическая активность. Для лежачих больных необходим массаж.
Лейкопения — состояние, при котором в крови снижается количество белых кровяных телец — лейкоцитов. Её причины бывают очень разными. Лейкопения может возникать как в норме (физиологическая), так и при различных заболеваниях (патологическая).


Классификация
Прежде чем говорить о причинах лейкопении, рассмотрим основные её типы. В первую очередь нужно понимать, что белые кровяные тельца бывают разных видов, и они выполняют различные функции. В зависимости от того, каких клеток не хватает, различают нейтропению (нейтрофилы), эозинопению (эозинофилы), моноцитопению (моноциты) и лимфопению (лимфоциты). Если количество клеток уменьшено по сравнению с нормой, это абсолютная лейкопения, а если уменьшен только процент относительно других видов лейкоцитов — относительная лейкопения.
Физиологическая лейкопения встречается у 2–12% людей. Они не испытывают симптомов, у них не нарушено кроветворение и не снижен иммунитет. Это их индивидуальная норма. Лейкопения, возникшая в результате тех или иных заболеваний, называется патологической.
Некоторые люди страдают наследственными лейкопениями. Существует также много видов приобретенных лейкопений.
Иногда в анализе обнаруживают сниженное количество белых кровяных телец, потому что значительная часть лейкоцитов переместилась в определенные сосуды. В таких случаях говорят о перераспределительных лейкопениях. Если же число лейкоцитов снизилось во всем кровяном русле — это истинная лейкопения.

Среди всех видов лейкопений чаще всего встречаются нейтропении. Нейтрофилы составляют большую часть всех лейкоцитов крови. Они играют важную роль в защите организма: выполняют функцию фагоцитов (поглощают и разрушают чужеродные частицы, в первую очередь бактерии и грибки), выделяют вещества, которые участвуют в развитии воспаления.
Нейтропения бывает трех степеней тяжести:
- Легкая: от 1000 до 1500 нейтрофилов в 1 мкл крови.
- Средней степени тяжести: от 500 до 1000 в 1 мкл.
- Тяжелая: менее 500 мкл в 1 мл.
Симптомы острой нейтропении возникают в течение нескольких часов или дней. Хроническая нейтропения продолжается от нескольких месяцев до нескольких лет.
Наши врачи вам помогут
Причины развития заболевания
Существует очень много разных причин возникновения лейкопении. Перечислим некоторые из них:

Лейкопения в онкологии
Снижение уровня лейкоцитов в крови нередко встречается у людей, страдающих злокачественными опухолями. Здесь причины тоже бывают очень разными, важно в них правильно разобраться, чтобы понять, как помочь пациенту.
Нередко лейкопения возникает после химиотерапии, лучевой терапии и трансплантации красного костного мозга как побочный эффект этих видов лечения. Это происходит того, что химиопрепараты и ионизирующие излучения уничтожают не только опухолевые, но и здоровые быстро размножающиеся клетки, в том числе в красном костном мозге. Лучевая терапия несет особенно высокие риски лейкопении, когда облучают несколько частей тела.
Тяжесть лейкопении во время курса химиотерапии зависит от видов и дозировок препаратов. Обычно уровень белых кровяных телец начинает снижаться через неделю с момента начала очередного цикла. Через 7–14 дней он достигает минимума. В это время наиболее высок риск заболеть инфекцией. Затем уровень лейкоцитов начинает постепенно подниматься. Обычно он возвращается к норме через 3–4 недели. После этого пациент готов к новому циклу химиотерапии.
К снижению уровня лейкоцитов может привести рак с метастазами. Это типичный симптом злокачественных опухолей кроветворной и лимфоидной ткани: лимфом, лейкозов, множественной миеломы.
Многие люди, страдающие злокачественными опухолями на поздних стадиях, находятся в ослабленном, истощенном состоянии, не могут полноценно питаться. У больных в отделении реанимации повышены риски тяжелых инфекций — сепсиса, пневмонии.
Наиболее высок риск лейкопении у онкологических больных старше 70 лет, у людей с изначально сниженной иммунной защитой: при ВИЧ/СПИД, приеме иммунодепрессантов после трансплантации органов, других сопутствующих заболеваниях, которые мы перечислили выше.
Позаботьтесь о себе, запишитесь на консультацию сейчас
Какими симптомами проявляется снижение уровня лейкоцитов?
Нередко больной не испытывает симптомов, а снижение уровня лейкоцитов у него выявляют по результатам общего анализа крови. Некоторые лишь отмечают, что чаще стали чувствовать усталость.
Главная проблема пациентов с лейкопенией — снижение защитных сил организма. У них даже легкая инфекция может быстро перейти в тяжелую форму.
Все основные симптомы лейкопении связаны с инфекционными осложнениями:
- Температура 38 градусов и выше.
- Потливость, озноб.
- Язвы во рту, зубная боль, боль в горле.
- Зуд, язвы в области ануса.
- Боли в животе.
- Жидкий стул.
- Частые мочеиспускания, сопровождающиеся болью, жжением.
- Одышка, кашель.
- Отек, покраснение, боль на коже, особенно в области ран, порезов, венозных катетеров.
- Зуд в области половых органов у женщин, выделения из влагалища необычного характера.

Методы диагностики
У многих больных лейкопению диагностируют случайно по результатам общего анализа крови. В других случаях причиной для обследования становятся частые, тяжелые инфекции. Онкологическим больным во время курса лечения регулярно назначают анализы.
В общем анализе крови важно не просто подсчитать количество лейкоцитов, но и их отдельных видов, оценить лейкоцитарную формулу. Это даст полную картину.
Врач тщательно осматривает пациента, пытаясь выявить признаки инфекций. Затем, для подтверждения инфекционного заболевания, проводят культуральные посевы.
Биопсия красного костного мозга — процедура, во время которой получают ткань с помощью иглы или специального инструмента и отправляют в лабораторию для цитологического, гистологического исследования. Этот метод помогает разобраться, вызвано ли снижение уровня лейкоцитов нарушением их производства в красном костном мозге, диагностировать некоторые причины лейкопении, такие, как лейкозы, апластическая анемия, миелофиброз. В некоторых случаях прибегают к дополнительным исследованиям клеток красного костного мозга: проточной цитометрии, цитогенетическому анализу и др.
Некоторые методы визуализации помогают обнаружить места локализации инфекции:
- Рентгенография грудной клетки — её назначают всем пациентам с лейкопенией.
- Компьютерная томография грудной клетки — по показаниям, при ослабленном иммунитете.
- Компьютерная томография придаточных пазух носа — если есть симптомы синусита.
- Компьютерная томография живота — если беспокоят боли в животе, была перенесена операция на брюшной полости.
- УЗИ брюшной полости может подтвердить увеличение селезенки (спленомегалию).
Чтобы разобраться в причинах лейкопении, могут потребоваться другие анализы и исследования, в каждом конкретном случае они будут разными.
Терпеть боль опасно для жизни!
Современные методы лечения
Если у пациента имеются признаки инфекции и снижено количество лейкоцитов в крови, обычно лечение начинают с антибиотиков. Сначала назначают антибактериальные препараты широкого спектра действия, затем, когда из лаборатории приходят данные о чувствительности микроорганизмов, подбирают подходящую терапию, исходя из этой информации.
Если лечение антибиотиками помогает, и состояние пациента улучшается в течение 72 часов, препараты продолжают применять в течение недели или до тех пор, пока не появятся признаки прогрессирования инфекции.
Если лечение не помогает, нужно разбираться в причинах. Чаще всего это происходит антибиотикорезистентности (устойчивости) микроорганизмов, инфекции двумя и более разными возбудителями, локализованного инфекционного процесса (абсцесс).
Если признаков инфекции нет, но уровень лейкоцитов сильно снижен, пациенту может быть показана профилактическая антибактериальная терапия.
При грибковых инфекциях применяют противогрибковые препараты.
Нередко для лечения лейкопении назначают колониестимулирующие факторы (факторы роста). Эти препараты заставляют красный костный мозг более активно производить новые клетки крови. Выделяют две основные группы факторов роста:
- Гранулоцитарные колониестимулирующие факторы () стимулируют производство гранулоцитов, в первую очередь нейтрофилов.
- колониестимулирующие факторы () стимулируют производство гранулоцитов и макрофагов.
Некоторым пациентам назначают витамины, анаболические стероиды, глюкокортикостероиды. Эти препараты не стимулируют производство лейкоцитов, но могут замедлить их разрушение.
При тяжелых инфекциях (пневмония, сепсис, некротическая энтеропатия), когда не помогают антибиотики, и уровень лейкоцитов падает ниже 0,75×10 9 /л, рассматривают возможность переливания лейкоцитарной массы.
Если лейкопения возникла как побочный эффект химиопрепаратов, может встать вопрос об изменении схемы терапии, коррекции дозировок, отмене определенных препаратов.
Читайте также:

