Лекарства вьетнама от туберкулеза
Обновлено: 19.04.2024
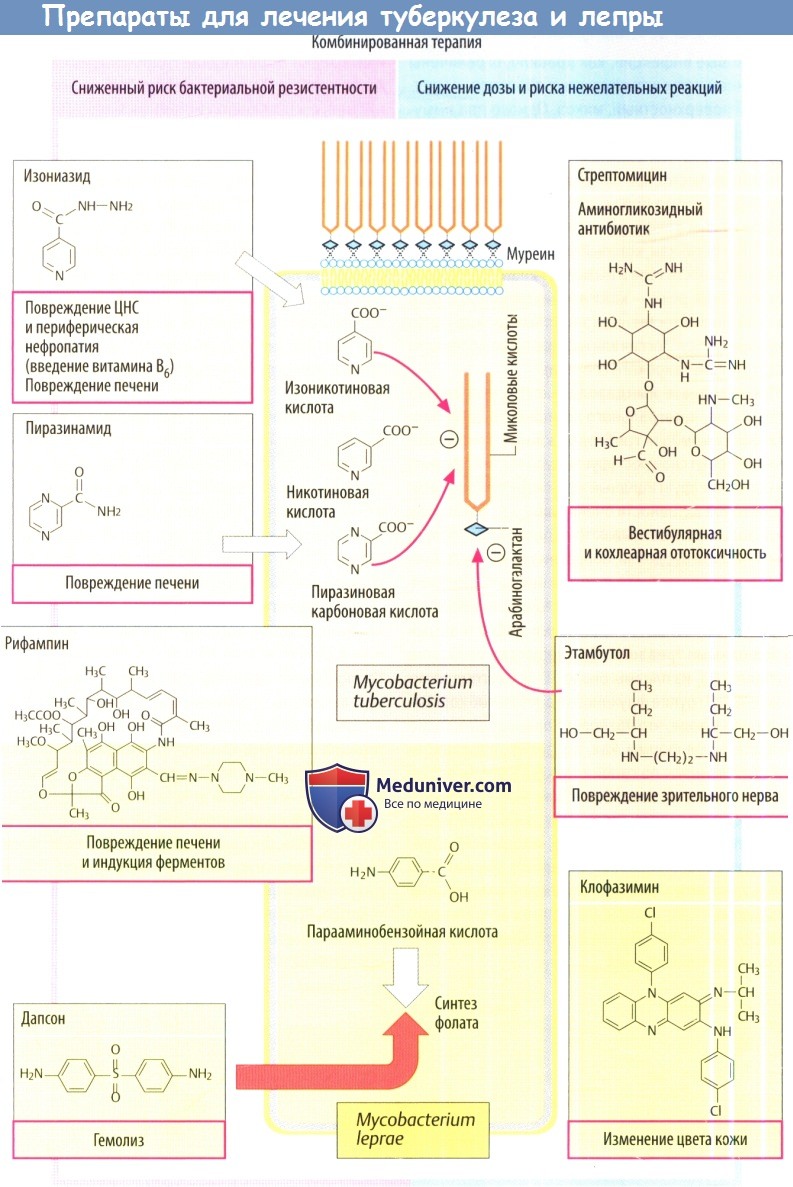
Лекарства для лечения туберкулеза и лепры
За последние 100 лет благодаря достижениям в гигиене значительно снизилась заболеваемость туберкулезом в развитых странах. Инфекцию, вызванную Mycobacterium tuberculosis, в большинстве случаев можно устранить с помощью системной длительной терапии (6-12 мес.) эффективными химиопрепаратами.
Тем не менее во всем мире туберкулез остается одним из самых опасных заболеваний. В развивающихся странах долговременная комбинированная терапия врядли осуществима.
Успеху лечения препятствует слабая медицинская инфраструктура, отсутствие финансирования и низкая приверженность пациентов к лечению. В результате миллионы человек умирают ежегодно из-за туберкулезной инфекции. Недостаточное лечение влечет за собой дополнительное отрицательное последствие: у все большего числа штаммов микобактерий развивается резистентность, возрастающая до нескольких препаратов одновременно (туберкулез с чрезвычайной лекарственной резистентностью), в силу чего невозможно провести адекватное лечение. У пациентов с иммунодефицитом заболевание, вызванное инфекцией М. tuberculosis, протекает тяжелее.
Противотуберкулезные препараты
Препаратами выбора являются изониазид, рифампицин и этамбутол, вместе со стрептомицином и пиразинамидом. Сочетания двух или трех препаратов используются в первые месяцы лечения.
а) Изониазид обладает бактерицидным свойством в отношении М. tuberculosis. Внутри бактерии он превращается каталазой/пероксидазой в изоникотиновую кислоту, накапливающуюся в клетке, где она ингибирует синтез миколовых кислот. Обычно эти кислоты образуют слой, охраняющий микроб от защитных иммунных механизмов хозяина. Миколовые кислоты связаны полисахаридом арабиногалактаном, который связывается с муреином клеточной стенки.
Изониазид быстро всасывается после введения внутрь. В печени он активируется путем ацетилирования. К значимым побочным эффектам относятся периферическая нейропатия, неврит зрительного нерва, который можно предупредить введением витамина В6 (пиридоксин), и повреждение печени.
б) Рифампин. Источник заболевания, антибактериальная активность и пути введения описаны в отдельной статье на сайте. Несмотря нехорошую в основном переносимость, данный препарат может вызывать ряд побочных эффектов, в т. ч. повреждение печени, гиперчувствительность с гриппоподобными симптомами, неприятное, но безобидное изменение цвета жидкостей организма на красный/оранжевый и индукцию ферментов (которая проявляется, например, неэффективностью пероральных контрацептивов и т. п.).
О рифабутине полдробно расписано в отдельной статье на сайте.
в) Пиразинамид тоже ингибирует синтез миколовой кислоты через активный метаболит. Он вводится внутрь. Препарат нарушает функцию печени и вызывает гиперурикемию за счет подавления выведения уратов почками.
г) Стрептомицин должен вводится в/в, как и другие аминогликозидные антибиотики. Он повреждает внутреннее ухо и лабиринт. У него сравнительно низкая нефротоксичность.
д) Этамбутол ингибирует синтез арабиногалактана. Этамбутол вводится внутрь. Обычно хорошо переносится, но может вызывать дозозависимые необратимые нарушения зрения (красно-зеленая цветовая слепота, дефекты полей зрения).
Противолепрозные препараты
Рифампицин часто применяется в сочетании с одним или двумя препаратами, указанными ниже.
а) Дапсон является сульфоном, который как и сульфаниламиды, ингибирует синтез ДГФ. Он обладает бактерицидным свойством против чувствительных к нему штаммов М. leprae. Дапсон вводится внутрь. Наиболее частой нежелательной реакцией является метгемоглобинемия с ускоренным разрушением эритроцитов (гемолиз).
б) Клофазимин — краситель с бактерицидной активностью в отношении M. leprae и противовоспалительными свойствами. Он вводится внутрь, но всасывается не полностью. Из-за высокой липофильности препарат накапливается в жировой и других тканях и достаточно медленно покидает организм (t1/2 70 дней). Красно-коричневая пигментация кожи является нежелательной реакцией, особенно у пациентов со светлой кожей.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Это РНК-содержащий вирус животного происхождения, относящийся к группе коронавирусов. Согласно данным ВОЗ, он передается от заболевшего человека через мелкие капли, которые выделяются при чихании и кашле из носа и рта. С момента заражения до появления первых симптомов проходит от 1 до 14 дней (в среднем – 7). Носитель вируса еще не знает о своей болезни, но в плане заражения уже представляет опасность для окружающих. По информации коронавирусной эпидемиологии, COVID-19 в 2-3 раза заразнее гриппа, но в 2-3 раза менее заразен, чем корь.
При легком течении болезни ее симптомы сходны с ОРВИ и заканчиваются выздоровлением через 14 дней без каких-либо дальнейших последствий. В тяжелых случаях COVID продолжается до 8 недель. Даже при отсутствии выраженных признаков заболевания у переболевших формируется иммунитет. Но учитывая, пусть и нечастые случаи повторного заражения, сохраняется он не слишком долго. Гораздо большим эффектом обладает вакцина.

Как действует вакцина?
Сегодня в мире используется несколько иммунопрепаратов, разработанных специалистами разных стран и прошедших необходимые клинические испытания. Все они предназначены для формирования иммунитета к возбудителю. После их введения иммунная система:
У человека, прошедшего вакцинацию, формируется стойкий иммунитет к COVID.

Опасна ли вакцинация?
Каждый человек реагирует на иммунопрепарат индивидуально. Поэтому даже самая качественная вакцина может вызвать побочные эффекты. Их появление на непродолжительное время – единственная опасность.
Чем опасна вакцинация от коронавируса:
- незначительным повышением температуры;
- головной болью, головокружением;
- сбоем сердечного ритма;
- кожными высыпаниями;
- слабостью.
Эти неприятные симптомы исчезают в течение нескольких дней.

Тяжелые состояния после введения иммунопрепарата могут развиваться у людей, имеющих противопоказания. Нельзя проводить вакцинацию, если наблюдаются:
- хронические патологии почек, сердечно-сосудистой системы (ССС), эндокринной системы;
- болезни кроветворной системы;
- аутоиммунные нарушения;
- выраженные патологии центральной нервной системы (ЦНС);
- аллергические реакции на ранее вводимые вакцины.
При этих патологиях прививка может спровоцировать обострение.
Также противопоказанием является возраст (младше 18), для данного населения в данный момент разрабатывается отдельная вакцина, а также недавно перенесенная тяжелая форма коронавирусной инфекции, таким пациентам нужно вакцинироваться по окончанию 6-месячного периода. Однако, вакцинация рекомендуется, так как для работы иммунитета нужен высокий титр антител, а его достичь можно только вакцинацией.
При беременности лучше вакцинироваться на стадии планирования, но, если такой возможности не было, привиться нужно после 22-ой недели срока, так как в этот момент плод уже почти сформирован.
Как уменьшить негативные проявления?
Снизить развитие побочных явлений поможет соблюдение всех рекомендаций врача. Чтобы уменьшить риск развития негативных симптомов после вакцинации, нужно:
- внимательно следить за своим самочувствием;
- как минимум за неделю до предполагаемой вакцинации избегать контактов с заболевшими;
- за 2 дня до прививки пройти обследование и сдать кровь на антитела;
- отказаться от иммуномодуляторов и иммуностимуляторов за 10 дней до введения вакцины;
- предупредить перед постановкой вакцины о приёме препаратов, которые стимулируют иммунитет.
При отсутствии противопоказаний и соблюдении всех требований, риск побочных эффектов сводится к минимуму.
После прививки от коронавируса врачи советуют соблюдать щадящий режим и выпивать не менее 1,5 литров жидкости в день. При повышении температуры рекомендуется принять жаропонижающее средство. Если слабость не проходит в течение нескольких дней, появились аллергические реакции, нужно немедленно обратиться к доктору.

Когда будет массовая вакцинация?
Массовая вакцинация в США, Канаде и европейских странах началась еще в декабре прошлого года. В это же время стартовала она и в России. Но на начальном этапе мероприятие проводилось только для определенной категории лиц – молодых людей и тех, кто по роду своей профессиональной деятельности не может ограничить число контактов. Сегодня привиться от ковида можно в любом регионе страны.
Решение о вакцинации каждый человек принимает самостоятельно. Но те, кто отказывается от прививки, должны знать, что даже легкая форма COVID – это серьезный удар по организму. Также не стоит забывать о потере трудоспособности не менее, чем на 2 недели, и вероятности заражения членов семьи. После вакцинации эти риски значительно понижаются. Но даже вакцинированным людям необходимо носить маску и перчатки, чтобы на 100% уберечь себя от заражения COVID-19.
Печень самая большая биохимическая лаборатория в нашем организме. Она участвует более чем в 500 реакциях. Поэтому любые изменения в её состоянии могут отразиться на самочувствии. Все знают ее важную роль и наслышаны о таком грозном диагнозе, как цирроз, многие хотят её почистить, попить специальные лекарства. Кто-то ищет народные средства, другие больше доверяют разработкам фармацевтической промышленности. Остается вопрос, что будет эффективно на самом деле?
А что же печень?
Можно подумать, что печень только и ждет, когда же мы ей поможем. Это не так. Компенсаторные и регенераторные возможности печени огромны. При сохранении 25% здорового органа она может сама восстановиться. Как работает здоровая печень, мы никогда не почувствуем. В ней нет нервных окончаний, поэтому она никогда не болит. Клетки печени — гепатоциты. Если гибнет клетка, её нагрузку перераспределяют между собой оставшиеся. Так, при разрушении значительной части печени, может не быть никаких симптомов и даже изменений в анализах.
С одной стороны, это хорошо, печень не беспокоит нас по пустякам как желудок, который может скрутить после плохой пищи, а через 3 дня мы уже и забыли об этом. Но если симптомы появились, это может свидетельствовать уже о серьезных проблемах, просто так от которых не избавиться. При проблемах с печенью могут страдать следующие функции:
- фильтрация и переработка токсичных продуктов, поступающих из желудочно-кишечного тракта;
- производство молекул белка, их накопление, преобразование аминокислот, образование мочевины и синтез креатина;
- образование и хранение гликогена;
- хранение и трансформация многих витаминов (A, PP, B, D, K), ионов металлов железа, меди, цинка, марганца, молибдена и др.;
- производство ферментов, участвующих в обменных процессах;
- поддержание баланса между свертывающей и антисвертывающей системами крови, образование гепарина;
- депонирование плазмы крови и форменных элементов, регуляция системы крови.
Ошибочно за проблемы с печенью принимают проблемы с желчным пузырем, поджелудочной железой, позвоночником и многие другие. Боль в печени может появиться, когда она увеличена и растягивает собственную капсулу, но обычно это уже запущенные проблемы.

Часто за проблемы с печенью принимают проблемы с желчным пузырем, поджелудочной или позвоночником.
Препараты
Проблемы с печенью могут развиваться более 10 лет и никак не беспокоить. Средняя продолжительность жизни с диагнозом цирроз — 9 лет. Поэтому даже имея проблемы с печенью, можно с ними бороться. Одних наименований средств, применяемых в гепатологии около 1000. При терапии не только лечат само заболевание, но и поддерживают печень, чтобы создать ей максимально благоприятные условия для восстановления. Одной из таких групп препаратов являются гепатопротекторы. Гепатопротекторы помогают восстановлению обменных процессов в печени, повышают устойчивость органа к действию разрушающих факторов, нормализуют функциональную активность и стимулируют регенеративные процессы в печени.
Требования к гепатопротекторам
Так как печень является тем органом, через который происходит обмен многих веществ, препараты должны быть не только мощными, но и отвечать определенным требованиям безопасности, а также:
Несмотря на то, что требования известны, идеального препарата еще не создано. Более половины представленных средств растительного происхождения, оставшуюся часть делят между собой фосфолипиды, синтетические производные, органопрепараты и аминокислоты.

Несмотря на то, что требования к препаратам для печени известны, идеального еще не создано.
Список лекарств
Группы гепатопротекторов разделяются в зависимости от состава.
Группа I: флавоноиды расторопши могут входить как натуральная вытяжка из растений, так и произведенные синтетическим способом:
Эти продукты содержат в себе вещество из расторопши пятнистой – силимарин (силибинин). Он защищает и стабилизирует мембраны клеток. Расторопша пятнистая обладает мощным антитоксическим действием, способна помочь при отравлениях бледной поганкой. Правда, в этом случае используют модификацию с внутривенным введением. Также имеется антиоксидантный и метаболический эффекты, ускоряет регенерацию гепатоцитов. Замедляется образование рубцовой ткани в органе.
Холестаз, то есть затрудненный отток желчи может быть противопоказанием к приему. Если это игнорировать, застой от приема препаратов может усилиться.
Обычно курс приема составляет около 4 недель, затем делают перерыв.
Группа II: остальные флавоноиды, кроме расторопши:
Лив 52 помогает усилить защиту печени от токсинов, имеет в составе компоненты широко используемые в индийской медицине. Но применение препарата в острой воспалительной фазе небезопасно и может усилить воспаление. Поэтому рекомендуется применять препарат, когда активна фаза регенерации и печень нуждается в поддержке.
Группа III: гепатопротекторы из органов животных:
Гепатносан – высушенные гепатоциты животных. В кишечнике он абсорбирует токсины. Перевариваясь, питательные компоненты клеток всасываются и доставляются в печень. Они работают как защитные факторы на уровне клеток печени, восстанавливают активность гепатоцитов. Препарат способствует ускорению репаративных процессов.
Сирепар — гидролизат экстракта печени крупного рогатого скота. Содержит в 1 мл 10 мг цианокобаламина. Способствует регенерации печени, оказывает очищающее действие. Не следует использовать в активную фазу болезни, так как может усилиться воспалительный процесс. Принимается при хронических гепатитах и циррозах, отравлениях токсинами и лекарствами.

Некоторые препараты не следует использовать в активную фазу болезни, так как может усилиться воспалительный процесс.
Группа IV: лекарства, имеющие в своем составе эссенциальные фосфолипиды:
Фосфолипиды, в том числе фосфатидилхолин, важнейший компонент, из которого как из кирпичиков состоит большая часть мембран самих клеток печени. Фосфолипиды выделены и изучаются почти 50 лет, проведены различные опыты и эксперименты. Восстанавливая мембраны клеток, печень нормализует свою функцию. Применяются при очень широком спектре заболеваний. Курс приема обычно длится около 3 месяцев при отсутствии противопоказаний и нежелательных эффектов.
Средства из других групп, не вошедшие в первые четыре:
-
; ;
- Нестероидные анаболики (метилурацил, натрия нуклеинат); ; .
Из этой группы разберем подробно Урсофальк, как препарат, имеющий широкое назначение среди врачей. Действующее вещество (урсодезоксихолевая кислота) помогает защитить орган и обладает желчегонным действием. Используется для растворения желчных камней. Снижает токсические эффекты на эпителий желчных протоков в печени и мембраны гепатоцитов. Облегчает выведение желчи из протоков, вследствие чего облегчает выведение токсинов.
Имеет противопоказания в виде неработающего желчного пузыря, воспалительных болезней кишечника, желчных протоков, желчные камни с высоким содержанием кальция (видны на рентгене), в общем любые состояния, которые будут препятствовать усиленному оттоку желчи из печени. Также цирроз в стадии декомпенсации.
Вывод
Гепатопротекторов множество, они отличаются составом, механизмом действия. У врачей отношение к ним неоднозначное, многие из них применяются и выпускаются только для территории постсоветских стран. Иногда можно встретить, отзывы, что человек после выхода из алкогольного запоя пропил некий препарат в течение 3 месяцев и его анализы улучшились. Это могло случиться и не из-за препарата, а от того, что токсины перестали действовать на печень, и она смогла в определенной мере восстановиться.

При прекращении воздействия токсинов, печень может сама в определенной мере восстановиться.
Главное в лечении печени не прием лекарств для компенсации вреда, который мы наносим сами, а прекращение воздействия токсинов и других разрушающих факторов. То есть нужно отказаться от алкоголя, курения и лишних килограммов (риск неалкогольного жирового гепатоза). Так как чередуя курсы препаратов с неправильным образом жизни мы создаем иллюзию благополучия. Если есть подозрения, что с печенью что-то не так, — обязательно обратитесь к врачу. Неправильное самолечение при проблемах с печенью может только навредить.
По оценкам ВОЗ, ежегодно в мире появляется около 500 000 новых случаев мультирезистентного туберкулеза, из них около 200 000 пациентв погибают. В 2018 году только 1 из 3 пациентов получал эффективное лечение, и только половина из них была вылечена
Новый терапевтический режим для мультирезистентного туберкулеза показал эффективность у 85% пациентов (в том числе с тяжелым коморбидным состоянием) в международном когортном исследовании.
Данные, полученные из 17 стран, подчеркивают важность распространения недавно разработанных противотуберкулезных препаратов – бедаквилина и деламанида. На настоящий момент стандарт лечения мультирезистентного туберкулеза, повсеместно используемый по всему миру, имеет эффективность только 60%.
Работа опубликована в журнале American Journal of Respiratory and Critical Care Medicine. Выборка включает более 1000 пациентов с мультирезистентным туберкулезом. Ранние исходы оценивались через 6 мес после начала лечения, которое длилось не менее 15 мес.
По оценкам ВОЗ, ежегодно в мире появляется около 500 000 новых случаев мультирезистентного туберкулеза, из них около 200 000 пациентв погибают. В 2018 году только 1 из 3 пациентов получал эффективное лечение, и только половина из них была вылечена.
В начале 2010-ых годов впервые за 50 лет были одобрены новые противотуберкулезные препараты – бедаквилин и деламинид, дав новую надежду на эффективное лечение мультирезистентного туберкулеза с меньшим количеством побочных эффектов. При этом известно, что пациенты с тяжелым коморбидным статусом часто имеют более плохие исходы, что зачастую не позволяет им участвовать в клинических испытаниях.
Исследование endTB показало, что новые терапевтические страгии демонстрируют хороший ранний ответ на лечение пациентов с тяжелой коморбидностью, схожий с таковым для другой группы пациентов с меньшим количеством сопутствующих заболеваний. Например, среди пациентов с ВИЧ хороший ответ на лечение наблюдался у 73% в сравнении с 84% случаев без ВИЧ.
Заболеваемость туберкулезом находится на практически нулевом уровне у обеспеченных слоев населения, в то время как для менее обеспеченных социальных групп это остается одной из самых критических проблем. Важнейшая особенность подбора терапии против мультирезистентного туберкулеза заключается в том, что она должна работать в условиях низкой обеспеченности ресурсами и в сложной популяции с высоким уровнем разнообразия, включая людей с постоянным недоеданием или тяжелыми сопутствующими заболеваниями.
Какие возможны варианты туберкулеза легких по отношению к лекарственному лечению? Какова роль фторхинолонов в лечении туберкулеза легких?
Какие возможны варианты туберкулеза легких по отношению к лекарственному лечению?
Какова роль фторхинолонов в лечении туберкулеза легких?
Таблица. Стандартные концентрации ПТП, используемые для выявления лекарственной устойчивости МБТ
Первый этап характеризуется проведением интенсивной насыщенной химиотерапии четырьмя-пятью ПТП в течение 2-3 месяцев, что ведет к подавлению размножающейся микобактериальной популяции, уменьшению ее количества и предотвращению развития лекарственной резистентности. На первом этапе используется комбинация препаратов, состоящая из изониазида, рифампицина, пиразинамида, стрептомицина и/или этамбутола.
Второй этап — менее интенсивной химиотерапии — проводится, как правило, двумя-тремя ПТП. Цель второго этапа — воздействие на оставшуюся бактериальную популяцию, в большинстве своем находящуюся внутриклеточно в виде персистирующих форм микобактерий. Здесь главной задачей является предупреждение размножения оставшихся микобактерий, а также стимуляция репаративных процессов в легких с помощью различных патогенетических средств и методов лечения.
Такой методический подход к лечению ЛЧТЛ позволяет к концу первого этапа комбинированной химиотерапии под непосредственным медицинским наблюдением абациллировать 100%, а к завершению всего курса лечения — закрыть каверны в легких у более чем 80% больных с впервые выявленным и рецидивным туберкулезом легких [5].
Намного сложнее вопрос о проведении этиотропного лечения второго варианта, к которому мы относим ЛУТЛ, вызванный лекарственно резистентными (ЛР) МБТ к одному и более ПТП и/или их сочетанию. Особенно тяжело протекает ЛУТЛ у больных с множественной ЛР МБТ к изониазиду и рифампицину, то есть к основным и самым эффективным ПТП. Поэтому поиск новых концептуальных путей повышения эффективности лечения ЛУТЛ и разработка современной методологии специфического воздействия на ЛР МБТ является одним из важнейших и приоритетных направлений современной фтизиатрии.
Развитие ЛР у МБТ к ПТП — одна из главных причин недостаточно эффективной этиотропной химиотерапии. Больные туберкулезом, выделяющие ЛР-штаммы МБТ, длительное время остаются бактериовыделителями и могут заражать окружающих ЛР-возбудителем. Чем больше число больных, выделяющих ЛР МБТ, тем выше риск распространения инфекции среди здоровых лиц и появления новых случаев заболевания туберкулезом с первичной резистентностью не только к основным, но и к резервным ПТП.
Феномен ЛР МБТ имеет важное клиническое значение. Существует тесная взаимосвязь количественных изменений микобактериальной популяции и изменения ряда биологических свойств МБТ, одним из которых является ЛР. В активно размножающейся бактериальной популяции всегда имеется небольшое количество ЛР-мутантов, которые практического значения не имеют, но по мере уменьшения бактериальной популяции под влиянием химиотерапии изменяется соотношение между количеством ЛР и устойчивых МБТ [5]. В этих условиях происходит размножение главным образом устойчивых МБТ, эта часть бактериальной популяции увеличивается. Следовательно, в клинической практике необходимо исследовать ЛР МБТ и результаты этого исследования сопоставлять с динамикой туберкулезного процесса в легких [5].
По определению экспертов ВОЗ [3], ЛУТЛ — это случай туберкулеза легких с выделением МБТ, резистентных к одному и более ПТП. По данным Центрального НИИ туберкулеза РАМН, у каждого второго впервые выявленного и ранее не леченного противотуберкулезными препаратами больного в мокроте выявлялись ЛР к ПТП МБТ, при этом у 27,7% из них наблюдалась устойчивость к двум основным противотуберкулезным препаратам — изониазиду и рифампицину. При хроническом фиброзно-кавернозном туберкулезе частота вторичной ЛР МБТ возрастает до 95,5%.
По нашему мнению, и это составляет основу нашей концепции, для повышения эффективности лечения туберкулеза, вызванного ЛР МБТ, необходимо в первую очередь использовать ускоренные методы выявления ЛР МБТ, что позволяет своевременно изменять режим химиотерапии.
Исследование лекарственной устойчивости МБТ в настоящее время возможно по прямому и непрямому методам.
Непрямой метод определения лекарственной чувствительности МБТ требует от 30 до 60, а иногда до 90 суток, ввиду того что вначале производится посев мокроты на твердые питательные среды и только после получения культуры МБТ производят ее пересев уже на среды с добавлением ПТП. При этом коррекция химиотерапии носит отсроченный характер, как правило, уже на конечном этапе интенсивной фазы химиотерапии.
В последнее время для ускоренного определения лекарственной устойчивости нами применялся радиометрический метод с использованием автоматической системы ВАСТЕС-460 ТВ (Becton Dickinson Diagnostic Systems, Sparks, MD), которая позволяет выявлять лекарственную резистентность МБТ на жидкой среде Middlebrook 7H10 через 6-8 дней.
Не менее важно правильное лечение впервые выявленных больных туберкулезом легких и применение современных режимов химиотерапии с использованием в начале лечения комбинации из четырех-пяти основных противотуберкулезных препаратов до получения результатов лекарственной устойчивости МБТ [2]. В этих случаях существенно повышается вероятность того, что даже при наличии первичной ЛР МБТ бактериостатическое действие окажут два или три химиопрепарата, к которым чувствительность сохранена. Именно несоблюдение фтизиатрами научно обоснованных комбинированных режимов химиотерапии при лечении впервые выявленных и рецидивных больных и назначение ими только трех ПТП является грубой врачебной ошибкой, что в конечном счете ведет к формированию наиболее трудно поддающейся лечению вторичной ЛР МБТ.
Наличие у больного туберкулезом легких ЛР МБТ существенно снижает эффективность лечения, приводит к появлению хронических и неизлечимых форм, а в ряде случаев и летальных исходов. Особенно тяжело протекают специфические поражения легких у больных с полирезистентными МБТ, которые обладают множественной ЛР, как минимум к изониазиду и рифампицину, т. е. к основным и самым активным противотуберкулезным препаратам. ЛР МБТ имеет не только чисто клиническое и эпидемиологическое, но и экономическое значение, так как лечение таких больных резервными ПТП обходится намного дороже, чем больных с чувствительными МБТ к основным химиопрепаратам.
В этих условиях расширение списка резервных ПТП, воздействующих на ЛР МБТ, является актуальным и крайне важным для повышения эффективности лечения больных с ЛУТЛ. Кроме того, присоединение к ЛУТЛ неспецифической бронхолегочной инфекции существенным образом утяжеляет течение специфического процесса в легких, требуя назначения дополнительных антибиотиков широкого спектра. В этом плане применение антибиотиков, воздействующих как на МБТ, так и на неспецифическую патогенную бронхолегочную микрофлору, является научнообоснованным и целесообразным.
В этом плане хорошо себя зарекомендовал в России такой препарат из группы фторхинолонов, как офлоксацин (таривид) [3]. Мы же свой выбор остановили на ломефлоксацине, как препарате, который еще не столь широко применяется при лечении туберкулеза и у которого, судя по имеющимся данным, практически не выявляются побочные эффекты и крайне редко формируется ЛР возбудителей инфекционных заболеваний [2].
Ломефлоксацин (максаквин) — антибактериальный препарат из группы фторхинолонов. Как и все представители производных оксихинолонкарбоновой кислоты, максаквин обладает высокой активностью против грамположительных (включая метициллин-устойчивые штаммы Staphylococcus aureus и Staphylococcus epidermidis) и грамотрицательных (включая Pseudomonas) микроорганизмов, в том числе по отношению к различным типам Micobacterium tuberculosis).
Механизм действия максаквина заключается в ингибировании хромосомной и плазмидной ДНК-гиразы, фермента, ответственного за стабильность пространственной структуры микробной ДНК. Вызывая деспирилизацию ДНК микробной клетки, максаквин ведет к гибели последней.
Максаквин обладает иным механизмом действия, нежели другие антибактериальные средства, поэтому к нему не существует перекрестной устойчивости с другими антибиотиками и химиотерапевтическими препаратами [2].
Основной целью настоящего исследования явилось изучение клинической и микробиологической эффективности максаквина при комплексном лечении больных деструктивным ЛУТЛ, выделяющих ЛР МБТ к изониазиду, рифампицину и другим ПТП, а также при сочетании туберкулеза с неспецифической бронхолегочной инфекцией.
Под наблюдением находилось 50 больных деструктивным ЛУТЛ, выделяющих с мокротой ЛР МБТ к изониазиду, рифампицину и ряду других ПТП. Эти люди в возрасте от 20 до 60 лет составили основную группу.
В контрольную группу вошли также 50 больных деструктивным ЛУТЛ легких в той же возрастной группе, выделяющие ЛР МБТ к изониазиду, рифампицину и другим ПТП. Эти пациенты лечились только протионамидом, амикацином, пиразинамидом и этамбутолом.
У 47 больных основной группы и 49 контрольной в мокроте микробиологическими методами были выявлены различные возбудители неспецифической бронхолегочной инфекции.
Среди больных основной группы диссеминированный туберкулез был установлен у 5 человек, инфильтративный — у 12, казеозная пневмония — у 7, кавернозный — у 7 и фиброзно-кавернозный туберкулез — у 17 человек. Большинство больных (45 пациентов) имели распространенный туберкулез легких с поражением более двух долей, у 34 больных был двусторонний процесс. У всех больных основной группы в мокроте были обнаружены МБТ, как методом микроскопии по Цилю — Нильсену, так и методом посева на питательные среды. При этом у них МБТ были устойчивы как минимум к изониазиду и рифампицину. Необходимо отметить, что все пациенты уже ранее неоднократно и неэффективно лечились основными ПТП, и специфический процесс у них приобрел рецидивирующий и хронический характер.
В клинической картине преобладали симптомы интоксикации с высокой температурой тела, потливостью, адинамией, изменениями в крови воспалительного характера, лимфопенией, увеличенной СОЭ до 40-50 мм в час. Следует отметить наличие грудных проявлений болезни — кашель с выделением мокроты, подчас значительного количества, слизисто-гнойной, а у половины больных — гнойной, с неприятным запахом. В легких выслушивались обильные катаральные явления по типу мелко-, средне-, а подчас и крупнопузырчатых влажных хрипов.
У большинства больных преобладали клинические проявления, которые скорее укладывались в картину неспецифического бронхолегочного поражения (бронхита, острой пневмонии, абсцедирования) с частыми и практически не стихающими обострениями.
Основным возбудителем неспецифической инфекции был Streptococcus hemoliticus — у 15,3% и Staphilococcus aureus — у 15% больных. Среди грамотрицательной микрофлоры преобладал Enterobacter cloacae в 7,6% случаев. Следует отметить высокую частоту ассоциации возбудителей неспецифической бронхолегочной инфекции.
МБТ были обнаружены у всех 50 больных. У 42 человек определялось обильное бактериовыделение. У всех пациентов выделенные штаммы МБТ были устойчивы к изониазиду и рифампицину. При этом у 31 больного лекарственная устойчивость МБТ к изониазиду и рифампицину сочеталась с другими ПТП.
Определение минимальной ингибирующей концентрации (МИК) максаквина проводили на лабораторных штаммах H37Rv и Academia, а также клинических штаммах (изолятах), выделенных от 30 больных, из которых 12 изолятов были чувствительны ко всем основным химиопрепаратам и 8 обладали резистентностью к изониазиду, рифампицину и стрептомицину. В опытах in vitro подавление роста лабораторных штаммов МБТ наблюдалось в зоне 57,6±0,04 до 61,8±0,02 мкн/мл, что почти в семь раз больше, чем показатели, характерные для остальных ПТП .
Таким образом, в ходе микробиологических исследований было установлено выраженное бактериологическое действие максаквина на МБТ, при этом более выраженный эффект наблюдался при его воздействии на лекарственно чувствительные штаммы и изоляты. Однако при повышенных концентрациях максаквина эффект также заметен при воздействии на полирезистентные МБТ, устойчивые к основным ППТ.
Лечение максаквином проводилось у всех 50 больных основной группы в разработанной нами комбинации с другими резервными препаратами: протионамидом, амикацином, пиразинамидом и этамбутолом.
Максаквин назначали в дозе 800 мг в сутки перорально однократно в утренние часы сразу вместе с другими противотуберкулезными препаратами для создания максимальной суммарной бактериостатической концентрации в крови и очагах поражения. Доза максаквина выбрана с учетом микробиологических исследований и соответствовала МИК, при которой отмечалось существенное подавление роста МБТ. Терапевтический эффект определяли через месяц — для оценки воздействия его на неспецифическую патогенную бронхолегочную микрофлору и через два месяца — для оценки воздействия на полирезистентные МБТ. Длительность курса лечения резервными химиопрепаратами в сочетании с максаквином составляла два месяца.
Через месяц комплексного лечения было отмечено значительное улучшение состояния больных основной группы, что проявлялось в уменьшении количества мокроты, кашля и катаральных явлений в легких, снижении температуры тела, при этом более чем у двух третей больных — до нормальных цифр.
У всех больных к этому сроку в мокроте перестал определяться рост вторичной патогенной бронхолегочной микрофлоры. К тому же у 34 больных значительно уменьшилась массивность выделения микобактерий туберкулеза. Практически у всех больных нормализовались анализы крови.
Следует отметить, что у 28 пациентов рентгенологически через месяц лечения максаквином в сочетании с протионамидом, амикацином, пиразинамидом и этамбутолом отмечалось частичное рассасывание специфических инфильтративных изменений в легких, а также существенное уменьшение перикавитарной воспалительной реакции. Это позволило применить на данном этапе искусственный пневмоторакс, который является обязательным методом в лечении ЛУТЛ и составляет вторую и не менее важную часть нашей концепции повышения эффективности лечения больных деструктивным туберкулезом легких, выделяющих полилекарственнорезистентные МБТ.
При анализе эффективности специфического действия комбинации резервных противотуберкулезных препаратов в сочетании с максаквином на полирезистентные МБТ при лечении 50 больных основной группы мы делали основной акцент на показатель прекращения бактериовыделения, как по микроскопии мокроты по Цилю — Нильсену, так и по посеву на питательные среды через два месяца после химиотерапии.
Анализ частоты прекращения бактериовыделения у больных основной и контрольной группы через два месяца лечения показал, что у пациентов, получавших максаквин в сочетании с протионамидом, амикацином, пиразинамидом и этамбутолом, прекращение бактериовыделения было достигнуто в 56% случаях. В контрольной группе больных, не получавших максаквина, — только в 30% случаев.
Следует отметить, что у остальных больных основной группы за этот период времени существенно уменьшилась массивность выделения МБТ.
Инволюция локальных изменений в легких у 50 больных контрольной группы также шла более замедленными темпами, и только у 25 больных к концу второго месяца удалось достичь частичного рассасывания перикавитарной инфильтрации и применить к ним искусственный пневмоторакс. К 39 из 50 пациентов основной группы был применен искусственный пневмоторакс в течение 1,5-2 месяцев, и 17 из них удалось достигнуть закрытия каверн в легких. 11 оставшихся больных, имеющих противопоказания к проведению искусственного пневмоторакса, в этот период были подготовлены к плановому оперативному вмешательству.
При определении лекарственной устойчивости МБТ к максаквину через два месяца лечения у больных основной группы только в 4% случаев была получена вторичная лекарственная устойчивость, сформировавшаяся в процессе двухмесячной химиотерапии, что в конечном итоге потребовало его отмены и замены на другой химиопрепарат, к которому МБТ сохранили свою чувствительность.
К концу второго месяца у 4% больных отмечались явления непереносимости максаквина — в виде диспепсических явлений и диареи, связанной с дисбактериозом, аллергических кожных проявлений и эозинофилии до 32%, что привело к полной отмене препарата. Во всех остальных случаях при двухмесячном ежедневном применении максаквина в суточной дозе 800 мг побочных явлений не отмечалось.
Проведенная после окончания курса лечения максаквином комбинированная химиотерапия резервными препаратами и динамическое наблюдение за этими же больными показали, что достигнутый ко второму месяцу положительный результат в абациллировании мокроты оказал положительное влияние и на конечный результат излечения больных с ЛУТЛ.
Таким образом, применение максаквина в дозе 800 мг в сутки в сочетании с протионамидом, амикацином, пиразинамидом и этамбутолом у больных деструктивным ЛУТЛ с сопутствующей неспецифической бронхолегочной инфекцией показало его достаточную эффективность как антибиотика широкого спектра, воздействующего на грамотрицательную и грамположительную микрофлору, и препарата, действующего на туберкулезное воспаление.
Максаквин с полной уверенностью может быть отнесен к группе резервных ПТП. Он эффективно действует не только на МБТ, чувствительные ко всем ПТП, но и на ЛУ МБТ к изониазиду и рифампицину, что и обусловливает целесообразность его назначения таким больным. Тем не менее максаквин не следует рассматривать как основной препарат в схемах лечения больных с впервые выявленным туберкулезом легких, он должен оставаться в резерве и применяться только при ЛУТЛ и сопутствующей неспецифической бронхолегочной инфекции.
Для изониазида это составляет 1 мкг/мл, для рифампицина — 40 мкг/мл, стрептомицина — 10 мкг/мл, этамбутола — 2 мкг/мл, канамицина — 30 мкг/мл, амикацина — 8 мкг/мл, протионамида (этионамида) — 30 мкг/мл, офлоксацина (таривида) — 5 мкг/мл, циклосерина — 30 мкг/мл и для пиразинамида — 100 мкг/мл.
Литература
1. Лечение туберкулеза. Рекомендации для национальных программ. ВОЗ. 1998. 77 с.
2. Мишин. В. Ю., Степанян И. Э. Фторхинолоны в лечении туберкулеза органов дыхания // Русский медицинский журнал. 1999. № 5. С. 234-236.
3. Рекомендации по лечению резистентных форм туберкулеза. ВОЗ. 1998. 47 с.
4. Хоменко А. Г., Мишин В. Ю., Чуканов В. И. и др. Эффективность применения офлоксацина в комплексном лечении больных туберкулезом легких, осложненным неспецифической бронхолегочной инфекцией // Новые лекарственные препараты. 1995. Вып. 11. С. 13-20.
5. Хоменко А. Г. Современная химиотерапия туберкулеза // Клиническая фармакология и терапия. 1998. № 4. С. 16-20.
Читайте также:

